co有可燃性,燃烧时放大量的热,常用作
 465053072022-10-04 11:39:543条回答
465053072022-10-04 11:39:543条回答co有还原性,常用于
co与co2化学性质有差异的原因是

已提交,审核后显示!提交回复
共3条回复
 tohn 共回答了16个问题
tohn 共回答了16个问题 |采纳率87.5%- co有可燃性,燃烧时放大量的热,常用作燃料
co有还原性,常用于还原金属
co与co2化学性质有差异的原因是 分子的构成不同 - 1年前
 一毛一 共回答了3个问题
一毛一 共回答了3个问题 |采纳率- 还原金属,C价态不同
- 1年前
 俞泡泡 共回答了12个问题
俞泡泡 共回答了12个问题 |采纳率- 还原剂
CO有可燃性
CO2没有可燃性
CO中 C+2价O-2价
CO2中C+4价0-2价
CO不稳定 CO2 较稳定 - 1年前
相关推荐
- KCLO3具有可燃性么KCLO3受热分解成氧气 可助燃 但KCLO3属于可燃物么 给个定义 通俗易懂的
 阿枚1年前1
阿枚1年前1 -
 大兵炮手 共回答了14个问题
大兵炮手 共回答了14个问题 |采纳率85.7%KCLO3当然不是可燃物
很简单的问题是,它如果是可燃物,那么它的燃烧温度是多少?它一遇热就分解了,怎么燃烧呢?
这个道理也没那么复杂,换个说法,
就像你问我 SO2能否在水溶液中导电一样,
SO2 一进入水,就不是SO2了,
还需讨论SO2在水中的导电性吗?1年前查看全部
- 氧气可以支持燃烧,为什么不能说明氧气具有可燃性?
 独具魅力1年前1
独具魅力1年前1 -
 叙述43 共回答了12个问题
叙述43 共回答了12个问题 |采纳率100%支持燃烧不代表可以燃,燃烧的条件之一是有氧气,而如果具有可燃性的话,氧气就是可燃物,那么谁支持氧气燃烧?1年前查看全部
- 可燃性油气着火可立即用泡沫灭火器灭火,为啥错
 erbing21年前1
erbing21年前1 -
 gcy1232 共回答了25个问题
gcy1232 共回答了25个问题 |采纳率100%应该用干粉或二氧化碳灭火器1年前查看全部
- 可燃性气体点燃时为什么要检验纯度
可燃性气体点燃时为什么要检验纯度
不纯为什么会爆炸,比如甲烷验纯? 宝宝v花花1年前1
宝宝v花花1年前1 -
 xiangli 共回答了21个问题
xiangli 共回答了21个问题 |采纳率71.4%主要是检测氧气含量,如果混合物超过爆炸极限,点燃就会发生爆炸.除了氧气,还可能检测二氧化氮、氯气等,也都是这个原因.
爆炸极限:
可燃物质(可燃气体、蒸气和粉尘)与空气(或氧气)必须在一定的浓度范围内均匀混合,形成预混气,遇着火源才会发生爆炸,这个浓度范围称为爆炸极限,或爆炸浓度极限.
爆炸:
短时间内一定空间内的剧烈的化学或物理反应,并且产生大量的热加热空间内的气体,使其膨胀,剧烈的将化学能或其他形式的能量转化为热和机械能.1年前查看全部
- 点燃或加热可燃性气体之前,必须检验气体的____是否达到______
 橄榄树197405071年前1
橄榄树197405071年前1 -
 mitsuo11 共回答了22个问题
mitsuo11 共回答了22个问题 |采纳率95.5%点燃或加热可燃性气体之前,必须检验气体的纯度是否达到爆炸极限1年前查看全部
- 金红石,碳粉混合在高温条件下,通入氯气制得TiCl4和一种可燃性气体,此反应的化学式的方程式是什么?
 ghd877777777771年前1
ghd877777777771年前1 -
 林子8610 共回答了18个问题
林子8610 共回答了18个问题 |采纳率94.4%TiO2+2C+2Cl2==TiCl4+2CO
条件是高温1年前查看全部
- 下列有关氧气说法不正确的是( ) A具有可燃性 B能使带火星的木条复燃 C能提供
下列有关氧气说法不正确的是( ) A具有可燃性 B能使带火星的木条复燃 C能提供
下列有关氧气说法不正确的是( ) A具有可燃性 B能使带火星的木条复燃 C能提供呼吸 D能与许多物质发生氧化反应 蚂蚁76021年前7
蚂蚁76021年前7 -
 不知道你好吗 共回答了17个问题
不知道你好吗 共回答了17个问题 |采纳率100%选A
A氧气具有助燃性,所以A错误;
氧气能使带火星的木条复燃,所以B正确;
氧气能供呼吸,所以C正确;、
氧气能与许多物质发生氧化反应,同时放出大量的热,所以D正确;
希望我的回答能对你的学习有帮助!1年前查看全部
- 氢气可燃性氧气助燃性用分子观点解释其化学性质不同的原因是什么
 ybbgdjtg1年前2
ybbgdjtg1年前2 -
 vv85 共回答了17个问题
vv85 共回答了17个问题 |采纳率82.4%楼上是文盲,谁都知道氢不容易失去电子的.是氢气粒子具有可燃性.而氧气没有氢气分子一样的可燃介质.只可以通过其它物质助其燃烧1年前查看全部
- 氧气 甲烷 二氧化碳 氨气 氦气 它们的可燃性(或助燃性
氧气 甲烷 二氧化碳 氨气 氦气 它们的可燃性(或助燃性
氧气 甲烷 二氧化碳 氨气 氦气
这五种气体是否具备可燃性(或助燃性)
那么氨气据不具备可燃性呢? 神呐_救救我吧1年前1
神呐_救救我吧1年前1 -
 泥巴6677 共回答了13个问题
泥巴6677 共回答了13个问题 |采纳率76.9%氧气有助燃性
甲烷 有可燃性
二氧化碳 氦气能灭火用
氨气不能燃烧,有刺激性!1年前查看全部
- 具有可燃性,具有助燃性,CO具有可燃性,那它助燃吗?氧气呢?
 jesy561年前4
jesy561年前4 -
 eric_huangyy 共回答了15个问题
eric_huangyy 共回答了15个问题 |采纳率80%当然不一样,可燃是自己燃烧,助燃是让其他物质燃烧,CO是可燃,O2是助燃1年前查看全部
- 可燃性,助燃性,氧化性,挥发性哪个属于物理性质?
 google8081年前3
google8081年前3 -
 forkme 共回答了20个问题
forkme 共回答了20个问题 |采纳率100%挥发性1年前查看全部
- 为什么氧气在燃烧反应中一般表现为氧化性而非可燃性?
为什么氧气在燃烧反应中一般表现为氧化性而非可燃性?
对张合果的回答也表示感谢! ohb8881年前2
ohb8881年前2 -
 嘛古 共回答了18个问题
嘛古 共回答了18个问题 |采纳率88.9%O2助燃并不是可燃!
O2一般做氧化剂是因为具有较强的非金属性即较强的氧化性1年前查看全部
- 我认为将火柴吹灭或吹灭蜡烛不应该是降低温度到着火点以下,应该是将其生成的可燃性气体吹离,使燃烧停止
我认为将火柴吹灭或吹灭蜡烛不应该是降低温度到着火点以下,应该是将其生成的可燃性气体吹离,使燃烧停止
那我是对的?书上说错了? 星恒1年前1
星恒1年前1 -
 失落蚂蚁 共回答了17个问题
失落蚂蚁 共回答了17个问题 |采纳率82.4%是降低到着火点下.
燃烧是什么?是物质发生剧烈的氧化反应,空气中一般都是指和氧气发生氧化反应.燃烧的条件是①可燃物②充足的氧气(燃烧表面附近氧气要充足)③达到燃点.
你吹气的时候,单从氧气角度实际上是带来了充足的氧气(这也是为什么生炉子要煽火).
你所说的可燃性气体……实际上是有的,一些气化点比较低的物质也许会在可燃物表面附近生成气态分子.就算你把这些分子吹开了,他们还是和空气接触的(吹气时火焰形状改变).他们会很快反应完.
你吹气之后,会带来低温的空气(低能量的分子),和高温的可燃物或氧气(高能量分子)碰撞,而交换能量.持续,大量的吹气,带来大量低能量分子,使得燃烧面附近的分子能量降低,也就是温度降低了,直到降低到燃点以下,燃烧停止.1年前查看全部
- 蜡烛蒸气燃烧蜡烛燃烧用短导管插入焰心,另一端也会燃烧.导管理一定有可燃性气体,气体成分可能会是什么呢猜想:贝贝认为:是蜡
蜡烛蒸气燃烧
蜡烛燃烧用短导管插入焰心,另一端也会燃烧.
导管理一定有可燃性气体,气体成分可能会是什么呢
猜想:贝贝认为:是蜡烛不完全燃烧产生CO,
芳芳认为:是蜡烛受热产生石蜡蒸气,
丽丽认为:两种都有.
方案:找一根较长导管,然后在另一端做点火实验.
如果观察到——————,则贝贝的猜想正确.如果观察到——————,则芳芳的猜想正确.如果观察到——————,则丽丽猜想正确. 张畔溪1年前1
张畔溪1年前1 -
 ggoodd1985 共回答了19个问题
ggoodd1985 共回答了19个问题 |采纳率84.2%玻璃棒内无白色固体,导管的另一端的气体可以燃烧
玻璃棒内有白色固体,导管的另一端的气体不可以燃烧
玻璃棒内有白色固体,导管的另一端的气体可以燃烧1年前查看全部
- 可燃性和助燃性是不是氧化性?和氧化性有什么关系?
 小伙你贵姓1年前1
小伙你贵姓1年前1 -
 star_shine 共回答了19个问题
star_shine 共回答了19个问题 |采纳率94.7%助燃性是能够支持燃烧的性质,可燃性是能够燃烧的性质.
助燃性和可燃性二者不能兼得,有助燃性的没有可燃性,有可燃性的没有助燃性,而它们又是相互依存的,要想燃烧就必须要有具有助燃性和可燃性的两种物质.1年前查看全部
- 怎样验证氢气和一氧化碳等可燃性气体已收满
 天见0221年前1
天见0221年前1 -
 偷着qq 共回答了20个问题
偷着qq 共回答了20个问题 |采纳率95%收集一小试管气体 用大拇指堵住试管口 倒立试管使试管靠近酒精灯 松开拇指
若只听见轻微爆鸣声则已收集满 若听见巨大爆鸣声则为收集满1年前查看全部
- 下列实验结论正确的是 ①既可说明甲烷具有可燃性,又说明了甲烷是由氢元素和碳元素组成 ②既可说明二氧化碳的密度比空气大,又
下列实验结论正确的是
①既可说明甲烷具有可燃性,又说明了甲烷是由氢元素和碳元素组成
②既可说明二氧化碳的密度比空气大,又说明了二氧化碳不能燃烧也不支持燃烧
③既可说明水是由氢元素、氧元素组成, 又可推导出水分子中氢原子和氧原子个数之比为2:1
④既可说明二氧化碳能溶于水,又说明了二氧化碳能与水反应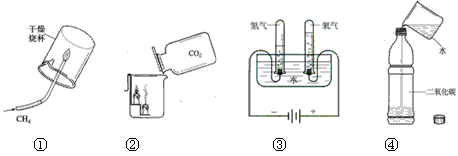 [ ]
[ ]A.①②③
B.②③
C.②③④
D.①②③④ putiansun1年前1
putiansun1年前1 -
 coffeea 共回答了16个问题
coffeea 共回答了16个问题 |采纳率93.8%B1年前查看全部
- 一氧化碳能和氯气反应?我觉得CO具有可燃性,Cl2具有助燃性,那么我说CO在氯气中点燃会不会生成光气?那为什么我听说CO
一氧化碳能和氯气反应?
我觉得CO具有可燃性,Cl2具有助燃性,那么我说CO在氯气中点燃会不会生成光气?那为什么我听说CO和Cl2反映还需要催化剂啊? ctc921年前3
ctc921年前3 -
 宝玉快跑 共回答了20个问题
宝玉快跑 共回答了20个问题 |采纳率90%首先要知道燃烧必须条件:1.有可燃物,2.可燃物达到着火点,3.与氧气接触(空气),因此CO和Cl2的反应不是燃烧
CO具有可燃性是指:一氧化碳能够在空气中或氧气中燃烧,生成二氧化碳:2CO+O2=2CO2
CO+Cl2→COCl2此时CO可视作不饱和物(它应有4个价健只利用了2个),它与氯气的反应可看作加成反应
根据化学反应动力学
CO+Cl2→COCl2的反应机理为:
① Cl2→2Cl(快) ; K1
② Cl+CO→COCl(快);k2
③ COCl+Cl2→COCl2+Cl(慢) k3
k31年前查看全部
- 如何用实验证明某可燃性气体只含氢元素而不含氧元素
 doriszy1年前2
doriszy1年前2 -
 小小的穷人 共回答了15个问题
小小的穷人 共回答了15个问题 |采纳率86.7%火焰呈淡蓝色,罩一冷烧杯,杯璧有水珠,倒入澄清石灰水,石灰水不变浑浊.1年前查看全部
- 某纯净的可燃性气体仅含碳、氢两种元素,取一定质量的该气体在足量氧气中充分燃烧.若将燃烧产物通入足量的澄清石灰水中,得到白
某纯净的可燃性气体仅含碳、氢两种元素,取一定质量的该气体在足量氧气中充分燃烧.若将燃烧产物通入足量的澄清石灰水中,得到白色沉淀30克.若用足量的固体氢氧化钠将燃烧产物全部吸收,增重24克
(1)请计算燃烧产物中二氧化碳的质量
(2)请计算燃烧产物中水的质量 卡佛1年前0
卡佛1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 考试化学题,急!A.B.D.E是前20号元素,原子序数依次增大,EA2与水反应产生可燃性有机物气体和白色浆状物,向该浆状
考试化学题,急!
A.B.D.E是前20号元素,原子序数依次增大,EA2与水反应产生可燃性有机物气体和白色浆状物,向该浆状物通AB2气体,可获得另一白色不容物,B.D同主族,D的阴离子与E的阳离子有相同核外电子排布 回答 (1)写出A与B的元素符号 (2) 已知AD2与AB2结构相似写出AD2结构式 (3)D单质放入浓HNO3中加热,生成红棕色气体和强酸,写出该反应式
 滨儿1年前1
滨儿1年前1 -
 ychwjw 共回答了28个问题
ychwjw 共回答了28个问题 |采纳率96.4%1. A:C; B: O; D: S; E: Ca
2. S=C=S
3. S (s)+ 6HNO3 = H2SO4 + 6NO2 (g) + 2H2O (l)1年前查看全部
- H2,CO2,CH4,N2,He、五中气体中具有可燃性的气体是那个?
 neodawn1年前1
neodawn1年前1 -
 SHUIBO_LIANG 共回答了21个问题
SHUIBO_LIANG 共回答了21个问题 |采纳率95.2%H2,CH41年前查看全部
- 具有可燃性,还原性并可用作火箭燃料的是什么?
具有可燃性,还原性并可用作火箭燃料的是什么?
提示:这个化合物中含有H,O,C,Ca这四种其中两.三种元素 LIHU1231年前5
LIHU1231年前5 -
 画工谁写银屏面 共回答了20个问题
画工谁写银屏面 共回答了20个问题 |采纳率95%汗,根据高中课本,该是乙醇或者甲烷,氢气也提过,不过只含一种元素.但2楼的很有道理啊...1年前查看全部
- 标准状况下,1.68升某无色可燃性气体在足量的氧气中完全燃烧,若将产物通入澄清的石灰水中得到白色沉淀为15克,如果用足量
标准状况下,1.68升某无色可燃性气体在足量的氧气中完全燃烧,若将产物通入澄清的石灰水中得到白色沉淀为15克,如果用足量的碱石灰吸收燃烧产物碱石灰增重9.3克.问若原气体为两种等物质的量的气体混合物,只有一种是烃,写出它的分子式.
 sfhadosidho1年前2
sfhadosidho1年前2 -
 水-灵-光 共回答了17个问题
水-灵-光 共回答了17个问题 |采纳率88.2%答案:该烃的分子式可能为C3H8或C4H6
气体的物质的量为1.68L/(22.4L/mol)=0.075mol;白色沉淀为CaCO3,其物质的量为15g/(100g/mol)=0.15mol,则生成的CO2也为0.15mol;碱石灰增重9.3g是因为吸收了气体燃烧产物CO2和H2O的结果,所以燃烧生成的H2O质量为:9.3g-0.15mol*44g/mol=2.7g,其物质的量为2.7g/(18g/mol)=0.15mol.
所以:0.075mol该气体混合物完全燃烧生成0.15molCO2和0.15molH2O,则该混合气体每摩气体中含C元素0.15/0.075=2mol、含H元素0.15*2/0.075=4mol.
根据高中所学化学知识及题中要求只有一种烃可知,二种气体可能是CO和烃或H2和烃.
若为等物质的量的CO和烃(CxHy)混合的,则有:
(1+x)/2=2,x=3;y/2=4,y=8.即烃为C3H8
若为等物质的量的H2和烃(CxHy)混合的,则有:
x/2=2,x=4;(2+y)/2=4,y=6.即烃为C4H61年前查看全部
- 将某可燃性气体在氧气中燃烧,把燃烧后生成的气体依次通过装置A、B,发现A质量增加,B中出现浑浊
将某可燃性气体在氧气中燃烧,把燃烧后生成的气体依次通过装置A、B,发现A质量增加,B中出现浑浊
(1)该可燃性气体是——
(2)该可燃性气体在氧气中燃烧的化学方程式为—— pfgawq1年前1
pfgawq1年前1 -
 styumi 共回答了15个问题
styumi 共回答了15个问题 |采纳率86.7%若A:H2SO4 B:Ca(OH)2
气体为CH4
化学方程式为CH4+2O2=CO2+2H2O1年前查看全部
- 可燃性气体点燃前一定要
 骐骐是骐骐1年前2
骐骐是骐骐1年前2 -
 边走边喊 共回答了20个问题
边走边喊 共回答了20个问题 |采纳率85%如果是氢气的话.在点燃前一定要验纯.1年前查看全部
- 下列各组物质相互反应时,能产生可燃性气体的是( )
下列各组物质相互反应时,能产生可燃性气体的是( )
①炭块投入热的浓硝酸中②铁丝投入稀硫酸中③过氧化钠投入水中④电石投入食盐水中.
A.①③
B.②③④
C.①④
D.②④ 赋笃笃1年前1
赋笃笃1年前1 -
 joobuy 共回答了17个问题
joobuy 共回答了17个问题 |采纳率82.4%解题思路:①碳和热的浓硝酸反应生成二氧化碳和二氧化氮,不是可燃气体;
②铁和稀硫酸反应生成氢气,氢气是可燃性气体;
③过氧化钠和水反应生成氢氧化钠和氧气,氧气是助燃气体,不是可燃气体;
④电石和水反应生成乙炔是可燃气体;所给各组物质发生的化学反应为:①C+4HNO3(浓)
△
.
CO2↑+4NO2↑+2H2O; ②Fe+H2SO4=FeSO4+H2↑;③2Na2O2+2H2O=4NaOH+O2↑;
④CaC2+2H2O=Ca(OH)2+C2H2↑;显然只有H2、C2H2可燃性气体.
故选D.点评:
本题考点: 硝酸的化学性质;钠的重要化合物;乙炔炔烃.
考点点评: 本题考查物质性质的应用,气体性质的分析,可燃性气体判断是关键,题目难度中等.1年前查看全部
- 下列说法正确的是( )A.氧气有可燃性和氧化性B.催化剂不都加快化学反应速率C.空气中只含氮气和氧气两种气体D.金属锈
下列说法正确的是( )
A.氧气有可燃性和氧化性
B.催化剂不都加快化学反应速率
C.空气中只含氮气和氧气两种气体
D.金属锈蚀属于剧烈氧化 漠然天下1年前1
漠然天下1年前1 -
 嘟嘟della 共回答了20个问题
嘟嘟della 共回答了20个问题 |采纳率90%解题思路:A、掌握氧气的性质;
B、掌握催化剂的特点和性质;
C、了解空气的成分;
D、了解缓慢氧化;A、氧气有可燃性和氧化性,说法错误,因为氧气无可燃性;
B、催化剂不都加快化学反应速率,说法正确,因为催化剂也可以减慢化学反应速率;
C、空气中只含氮气和氧气两种气体,说法错误,因为还含有二氧化碳、稀有气体等;
D、金属锈蚀属于剧烈氧化,说法错误,金属锈蚀属于缓慢氧化.
故选:B.点评:
本题考点: 氧气的化学性质;空气的成分及各成分的体积分数;催化剂的特点与催化作用;燃烧、爆炸、缓慢氧化与自燃.
考点点评: 本题难度不大,但考查知识点较多,掌握催化剂的特点和性质、氧气和空气的有关知识即可解答.1年前查看全部
- 向某种物质的无色水溶液中加入铁片后会有无色可燃性气体产生,向其中加入氢氧化钠溶液,溶液颜色是?
向某种物质的无色水溶液中加入铁片后会有无色可燃性气体产生,向其中加入氢氧化钠溶液,溶液颜色是?
原因是什么? 流浪者之鼠1年前1
流浪者之鼠1年前1 -
 thomas1979 共回答了15个问题
thomas1979 共回答了15个问题 |采纳率73.3%“向某种物质的无色水溶液中加入铁片后会有无色可燃性气体产生.”从这句话可以知道无色水溶液是强酸,产生的是氢气.剩下的溶液是含二价或三价铁离子的溶液.由于题目没说清,所以酸可能过量.
“向其中加入氢氧化钠溶液”,如果酸过量,氢氧化钠溶液加的不够多,则溶液还是无色.如果氢氧化钠溶液加过量,则呈现出氢氧化铁的颜色(红褐色).(氢氧化亚铁在氧气作用下,很快转化成氢氧化铁).1年前查看全部
- 氢气和一氧化碳都有可燃性和还原性吗
 风雅百代1年前3
风雅百代1年前3 -
 andyazou2006cfa 共回答了17个问题
andyazou2006cfa 共回答了17个问题 |采纳率88.2%H2和CO 都有可燃性,原因在于他们(H、C)的最外层电子没达到2或者8的稳定结构 燃烧过程中生成水和二氧化碳后稳定.
还原性的典型实验是能使黑色的CuO在加热条件下生成红色的Cu,同样是把电子给出后生成稳定的+1的H(水) 和+4的C(二氧化碳)1年前查看全部
- 电石的主要成分是碳化钙(CaC2),可以与水反应生成一种可燃性气体及白色固体.某化学兴趣小组对它的化学性质产生了浓厚的兴
电石的主要成分是碳化钙(CaC2),可以与水反应生成一种可燃性气体及白色固体.某化学兴趣小组对它的化学性质产生了浓厚的兴趣并进行下列探究.
【查阅资料】乙炔(C2H2)燃烧时伴有大量黑烟.CaO+H2O→Ca(OH)2.Ca(OH)2溶液能使酚酞变红.
【猜想与假设】
电石与水反应生成的可燃性气体是:O2、H2或乙炔(C2H2);电石与水反应生成的白色固体是:氧化钙、氢氧化钙或碳酸钙.
大家讨论后一致认为该气体不可能是O2,原因是______,白色固体不可能是氧化钙,原因是______.
【实验探究】
【反思交流】载有电石的货车可以在雨中整整燃烧一天而不熄灭,说明电石与水的反应是______(填“吸热”或“放热”)反应.实验步骤 实验现象 实验结论 (1)取适量电石加水反应,收集生成的气体,验纯后点燃. 气体燃烧,产生黄色火焰并伴有浓烈黑烟. 电石与水反应产生的气体是______. (2)取适量反应后生成的固体于试管中,滴加过量稀盐酸. 固体溶解,______. 电石与水反应产生的固体不是碳酸钙 (3)取适量反应后生成的固体于试管中加水,向上层清液中滴加2~3滴______. 溶液变红 电石与水反应产生的固体是氢氧化钙  ww龙1年前1
ww龙1年前1 -
 颠僧 共回答了24个问题
颠僧 共回答了24个问题 |采纳率95.8%解题思路:【猜想假设】根据氧气不具有可燃性及氧化钙遇到水会产生氢氧化钙分析;
【实验探究】根据信息结合实验的现象分析产物的成分;根据碳酸钙和氢氧化钙的性质分析实验;
【反思交流】根据现象分析能量的变化.【猜想假设】由于电石与水反应生成的是可燃性气体,而氧气不具有可燃性,故不可能是氧气;因为氧化钙遇到水会产生氢氧化钙,所以白色固体不可能是氧化钙;
【实验探究】(1)资料中乙炔(C2H2)燃烧时伴有大量黑烟,而氢气燃烧不会产生黑烟,因此电石与水反应产生的气体是乙炔;
(2)因为结论电石与水反应产生的固体不是碳酸钙,因此加盐酸不会产生气泡;
(3)因为结论电石与水反应产生的固体是氢氧化钙,氢氧化钙的溶液呈现碱性,能够使酚酞试液变成红色;
【反思交流】根据满载电石的货车遇大雨着火的原因是电石主要成分碳化钙(CaC2)能与水反应生成可燃性气体,且该反应放热;
故答案为:【猜想假设】氧气不具有可燃性;氧化钙会和水反应产生氢氧化钙(或CaO+H2O═Ca(OH)2);
【实验探究】乙炔(C2 H2 );没有气泡产生;酚酞;
【反思交流】放热.点评:
本题考点: 实验探究物质的性质或变化规律;常见气体的检验与除杂方法;生石灰的性质与用途;酸的化学性质.
考点点评: 本题属于信息题的考查,可以依据题目提供的信息结合碳酸钙、氢氧化钙的化学性质等相关的知识进行分析得出结论,难度不大.1年前查看全部
- 下列有关氧气性质的叙述 ①通常氧气是无色、无嗅的气体 ②氧气有可燃性 ③有氧气参加的反应一定属于氧化反应 ④氧
下列有关氧气性质的叙述 ①通常氧气是无色、无嗅的气体 ②氧气有可燃性 ③有氧气参加的反应一定属于氧化反应 ④氧气能与许多物质发生反应 ⑤氧气能支持燃烧
其中正确的是( )
A. ①②③④
B. ①③④⑤
C. ②③④⑤
D. 以上叙述都正确 大雨雨1年前2
大雨雨1年前2 -
 海鹰2000 共回答了8个问题
海鹰2000 共回答了8个问题 |采纳率100%解题思路:根据氧气的物理性质和化学性质进行分析判断即可.①通常氧气是无色、无味的气体,故说法正确;
②氧气能够支持燃烧,但不能燃烧,氧气不具有可燃性;故说法错误;
③物质与氧气发生的反应都属于氧化反应,故说法正确;
④氧气的化学性质活泼,具有较强的氧化性,能与许多物质发生反应;故说法正确;
⑤由氧气的化学性质可知,氧气能支持燃烧;故说法正确.
故①③④⑤说法正确.
故选B.点评:
本题考点: 氧气的化学性质;氧气的物理性质.
考点点评: 本题难度不大,掌握氧气的物理性质和化学性质是正确解题的关键.1年前查看全部
- 下列叙述中,两句话均正确且有因果关系的是( )A.水通电可以产生氢气和氧气,水是由这两种气体组成B.氢气具有可燃性,氮气
下列叙述中,两句话均正确且有因果关系的是( )A.水通电可以产生氢气和氧气,水是由这两种气体组成B.氢气具有可燃性,氮气一般不可燃也不助燃C.冰山总是漂浮在海面上,冰的密度总是小于水的密度D.有些在空气中不能燃烧的物质可以在氧气中燃烧,氧气的助燃性大于空气请解答后逐条说明对或不对的原因,
 scl_scl1年前1
scl_scl1年前1 -
 bkf0810 共回答了20个问题
bkf0810 共回答了20个问题 |采纳率90%选C.A中应该说水是由水分子构成的,或由氢氧元素组成的.B中两句话虽都正确,但没有因果关系;顺便说,镁条可以在氮气中燃烧,氮气是助燃气体,但由于氮气很稳定,所以氮气一般不可燃也不助燃.C很正确.D中的原因是氧气中的氧的浓度大于空气,所以有些在空气中不能燃烧的物质可以在氧气中燃烧,而不能说氧气的助燃性大于空气1年前查看全部
- 为了确定三种可燃性气体:CH 4 、H 2 和CO(简称试验气),分别将它们在O 2 中燃烧,再将燃烧后的产物分别依次通
为了确定三种可燃性气体:CH 4 、H 2 和CO(简称试验气),分别将它们在O 2 中燃烧,再将燃烧后的产物分别依次通过图中A、B两个洗气瓶.
试回答:
(1)装置A中的液体是______,装置B中的液体是______;
(2)若装置A的质量增加,B的质量不变,则待测试验气是______;
(3)若装置A质量不变,B的质量增加,则试验气是______;
(4)若装置A、B的质量都增加,则试验气是______,若这时装置B的质量增加m g,则装置A的质量增加______.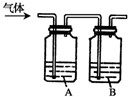
 wang_tzc1年前1
wang_tzc1年前1 -
 不在摇摆 共回答了22个问题
不在摇摆 共回答了22个问题 |采纳率86.4%CH 4 燃烧生成二氧化碳和水,H 2 燃烧生成水,CO燃烧生成二氧化碳;浓硫酸可吸收水分,质量增加,NaOH溶液可以吸收二氧化碳,质量增加,
(1)如果气体先通过氢氧化钠溶液,当气体通过氢氧化钠溶液时会带出部分水蒸气,导致测量不准确,所以应该先通过浓硫酸再通过氢氧化钠溶液,所以A是浓硫酸,B是氢氧化钠溶液,
故答案为:浓H 2 SO 4 ;NaOH溶液;
(2)若装置A的质量增加,B的质量不变,则说明该气体燃烧后只生成水,所以是氢气,故答案为:氢气;
(3)若装置A质量不变,B的质量增加,说明该气体燃烧后只生成二氧化碳,所以是一氧化碳,故答案为:CO;
(4)若装置A、B的质量都增加,说明该气体燃烧后生成二氧化碳和水,所以该气体是甲烷,B质量增加的量是二氧化碳,根据方程式CH 4 +2O 2
点燃
.
C0 2 +2H 2 O知,A质量增加的量=
mg
44 ×(2×18) =
9m
11 g ,
故答案为:CH 4 ;
9
11 mg.1年前查看全部
- 与钙形成离子化合物与水反应生成可燃性气体方程式为
 qpzm20031年前1
qpzm20031年前1 -
 韩寒军师刘建燃 共回答了23个问题
韩寒军师刘建燃 共回答了23个问题 |采纳率95.7%最简单的由离子构成的电石:碳化钙CaC2,与水反应生成氢氧化钙和乙炔气,方程式为CaC2 + 2H2O == Ca(OH)2 + C2H2气体上箭头,1年前查看全部
- 可燃性的物质:助燃性的物质:还原性的物质:氧化性的物质:酸碱性的物质:以上这些物质请大家帮忙想几个
 zl6281年前2
zl6281年前2 -
 xiaobao20 共回答了25个问题
xiaobao20 共回答了25个问题 |采纳率92%可燃性的物质:
H2、CO、C、CH4、S
助燃性的物质:
O2
还原性的物质:
Fe、Na、Al、Mg...金属活动顺序表的金属
C、H2、CO
氧化性的物质:
O2、CL2、浓硫酸,硝酸,Fe3+、H2O2
酸碱性的物质:
酸性:常见的酸有HCl,H2SO4、CH3COOH、HNO3、H2CO3、H3PO4、H2SO3.
还有某些强酸弱碱盐FeCL3、CuSO4...
碱性:常见的碱有NaOH、Ca(OH)2、Ba(OH)2、KOH、NH3·H2O
还有强碱弱酸盐:Na2CO3、NaHCO3、CaHCO3.1年前查看全部
- 一氧化碳支不支持燃烧氧气支持燃烧,氧气不能燃烧,支持燃烧与是否具有可燃性区别
 zqian30001年前3
zqian30001年前3 -
 柏原 共回答了23个问题
柏原 共回答了23个问题 |采纳率82.6%支持燃烧,是指帮助别的物质燃烧,象氧气 具有助燃性,但是本身不可燃烧.
可燃性,是指该物质可以燃烧,象木炭 具有可燃性,但是本身不能帮助别的物质燃烧.1年前查看全部
- 铁丝放在硫酸铜溶液中,表面有红色固体附着,还有可燃性气体产生,为啥啊
铁丝放在硫酸铜溶液中,表面有红色固体附着,还有可燃性气体产生,为啥啊
我知道红色固体产生的原因,为啥有气泡啊,硫酸铜溶液是酸性的,为何有气泡?
可以的话,写一下方程式吧,谢谢 halic171年前1
halic171年前1 -
 怕女人的男人 共回答了12个问题
怕女人的男人 共回答了12个问题 |采纳率83.3%两种原因:
一是生成铜后,铜和铁成了原电池的两个极,此时有电极反应,铁所在的一极(负极)会产生氢气.
二是溶液中含有大量H(+)离子,会与铁反应而被还原成氢气,释出.1年前查看全部
- 下列关于实验操作的叙述中正确的是……( ) A.从试剂瓶中取出的任何药品,若有剩余均不能放回原试剂瓶 B.任何可燃性气
下列关于实验操作的叙述中正确的是……()
A.从试剂瓶中取出的任何药品,若有剩余均不能放回原试剂瓶 B.任何可燃性气体点燃之前都必须检验纯度 C.用胶头滴管向试管中滴加液体,一定要将滴管伸入试管中,以避免液体洒落 D.在中和滴定的实验过程中,目光要密切注视滴定管中的液面,以避免过量滴加  浴火而生1年前1
浴火而生1年前1 -
 男子汉36318 共回答了23个问题
男子汉36318 共回答了23个问题 |采纳率87%B
A、一般药品剩余不能放回原试剂瓶,但像金属钾或金属钠,取出大块切割完后剩余部分必须放回原试剂瓶;
B、正确;
C、用胶头滴管向试管中滴加液体,必须将滴管垂直于试管口的上方,不能伸入试管里面(特殊情况例外,如制取氢氧化亚铁时);
D、滴定时眼睛应注意观察锥形瓶中溶液颜色的变化,同时注意滴加液体的流速。1年前查看全部
- 甲醇[CH3OH]是一种有毒,有酒的气味的可燃性液体.甲醇在氧气中不完全燃烧可发生如下反应:
甲醇[CH3OH]是一种有毒,有酒的气味的可燃性液体.甲醇在氧气中不完全燃烧可发生如下反应:
可发生如下反应:8CH3OH+nO2=mCO2+2CO+16H2O.若反应生成3.6g的水,请计算:[1]M的值是______ [2]参加反应的氧气质量是多少克?[写出规范计算步骤] keaikeai1年前2
keaikeai1年前2 -
 风解羽 共回答了20个问题
风解羽 共回答了20个问题 |采纳率85%[1]M的值是( 8 )——依据是:方程两边,碳原子的个数相等
经配平后的化学方程式为:
8CH3OH+13O2=8CO2+2CO+16H2O
[2]设参加反应的氧气质量是x克
8CH3OH+13O2=8CO2+2CO+16H2O
416 288
x 3.6g
416/x=288/3.6g
x=5.2g
答:参加反应的氧气质量是5.2克1年前查看全部
- 有abcdef六个初中常见的物质B是无色液体,D用于灭火F为可燃性气体他们的化学式
 wello1年前2
wello1年前2 -
 蔑视你的美 共回答了14个问题
蔑视你的美 共回答了14个问题 |采纳率85.7%B H2O F H2 氢气 D CO21年前查看全部
- (2006•南平模拟)我们知道燃烧的条件是:①物质具有可燃性,②可燃物的温度要达到着火点,③可燃物要与氧气接触.一蘸有水
(2006•南平模拟)我们知道燃烧的条件是:①物质具有可燃性,②可燃物的温度要达到着火点,③可燃物要与氧气接触.一蘸有水的棉花球在酒精灯火焰上烧不着,原因是:______.
某网吧因电路老化或超负荷而引起线路着火,在一时来不及切断电源的情况下,不能采用的灭火方法是______.
A、泼水B、拨119火警电话求救
C、用二氧化碳灭火器灭火D、用泡沫灭火器灭火. 阳光中的浮尘1年前1
阳光中的浮尘1年前1 -
 sdfsdlfj09 共回答了14个问题
sdfsdlfj09 共回答了14个问题 |采纳率92.9%解题思路:燃烧的条件是:(1)物质具有可燃性.(2)可燃物与氧气接触.(3)温度达到可燃物的着火点.棉花球上的水汽化时吸收热量,使温度不能达到棉花的着火点,棉花球不能燃烧.故填:温度没有达到棉花的着火点.
因为天然水、泡沫灭火器中的药品中含有易导电的物质,在一时来不及切断电源的情况下,如果用天然水、泡沫灭火器灭火时容易发生触电事故.故填:AD.点评:
本题考点: 燃烧与燃烧的条件;灭火的原理和方法.
考点点评: 本题主要考查燃烧条件方面的知识,解答时要理解燃烧的三个条件必须同时具备,缺一不可.1年前查看全部
- 下列做法中错误的是 [ ] A.点燃可燃性气体之前必须验纯
下列做法中错误的是 [ ]A.点燃可燃性气体之前必须验纯
B.给玻璃仪器加热时都要垫石棉网
C.做实验的废液倒入指定容器内
D.在实验药品贮藏室门口写上“严禁烟火” 春风得意6201年前1
春风得意6201年前1 -
 pujiay 共回答了18个问题
pujiay 共回答了18个问题 |采纳率94.4%B1年前查看全部
- (2012•顺义区二模)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知:N2(g)+2O2(g)=2N
(2012•顺义区二模)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知:N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol
2N2H4(g)+2NO2(g)=3N2(g)+4H2O (g)△H=-1 135.7kJ/mol;下列说法正确的是( )
A.N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-1 068 kJ/mol
B.肼是与氨类似的弱碱,它易溶于水,其电离方程式:N2H4+H2O═N2H5++OH-
C.铂做电极,以KOH溶液为电解质溶液的肼--空气燃料电池,放电时的负极反应式:N2H4-4e-+4OH-=N2+4H2O
D.铂做电极,以KOH溶液为电解质溶液的肼--空气燃料电池,工作一段时间后,KOH溶液的pH将增大 寒竹木青1年前1
寒竹木青1年前1 -
 三秋夜冷 共回答了17个问题
三秋夜冷 共回答了17个问题 |采纳率82.4%解题思路:A、根据盖斯定律,由已知热化学方程式乘以适当的系数进行加减构造目标热化学方程式,反应热也乘以相应的系数,进行相应的加减.
B、肼是与氨类似的弱碱,N2H4不是电解质,N2H4•H2O是弱电解质,N2H4•H2O存在电离平衡电离出N2H5+、OH-.
C、原电池总反应为N2H4+O2=N2+2H2O,原电池正极发生还原反应,氧气在正极放电,碱性条件下,正极电极反应式为O2+2H2O+4e-=4OH-,总反应式减去正极反应式可得负极电极反应式.
D、原电池总反应为N2H4+O2=N2+2H2O,反应生成水,随反应进行KOH溶液浓度降低,溶液PH值减小.A、已知:①N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol
②2N2H4(g)+2NO2(g)=3N2(g)+4H2O (g)△H=-1 135.7kJ/mol;
由盖斯定律,①+②得2N2H4(g)+2O2(g)=2N2(g)+4H2O(g)△H=67.7kJ/mol-1135.7kJ/mol=-1068 kJ/mol.
即N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-534kJ/mol.故A错误;
B、N2H4不是电解质,N2H4•H2O是弱电解质,N2H4•H2O存在电离平衡,电离方程式为N2H4•H2O⇌N2H5++OH-,故B错误;
C、原电池总反应为N2H4+O2=N2+2H2O,原电池正极发生还原反应,氧气在正极放电,碱性条件下,正极电极反应式为O2+2H2O+4e-=4OH-,总反应式减去正极反应式可得负极电极反应式为N2H4-4e-+4OH-=N2+4H2O,故C正确;
D、原电池总反应为N2H4+O2=N2+2H2O,反应生成水,随反应进行KOH溶液浓度降低,碱性减弱,溶液PH值减小,故D错误.
故选:C.点评:
本题考点: 用盖斯定律进行有关反应热的计算;化学电源新型电池.
考点点评: 考查盖斯定律、热化学方程式书写、弱电解质的电离、原电池工作原理与电极反应式书写,难度中等,注意利用正、负电极反应式之和等于总反应式书写电极反应式.1年前查看全部
- A是地壳中含量第二的金属元素,A的单质在B单质中燃烧时火星四射,生成一种黑色固体C,把A单质放在稀硫酸中产生可燃性气体D
A是地壳中含量第二的金属元素,A的单质在B单质中燃烧时火星四射,生成一种黑色固体C,把A单质放在稀硫酸中产生可燃性气体D,A单质与氯化铜溶液反应能生成红色金属E.
(1)写出:A元素的符号 ______;B单质的名称 ______;D单质的化学式 ______.
(2)写出有关化学方程式:
A→C3Fe+2O2
Fe3O4点燃 .3Fe+2O2;
Fe3O4点燃 .
A→D ______;
A→E ______. ni983gnh1年前1
ni983gnh1年前1 -
 yide1 共回答了17个问题
yide1 共回答了17个问题 |采纳率88.2%解题思路:(1)“A是地壳中含量第二的金属元素”,则A为铁;铁在B单质中燃烧时火星四射,生成一种黑色固体C,则知B为氧气;C为四氧化三铁;把铁放在稀硫酸中产生可燃性气体D,则D为氢气;铁与氯化铜溶液反应能生成红色金属E,则红色金属E为铜.
(2)①A→C:铁和氧气生成四氧化三铁;②A→D:铁和硫酸生成氢气;③A→E:铁与氯化铜生成铜.(1)找出突破口,推知A为铁,B为氧气,C为四氧化三铁,D为氢气,E为铜.
(2)根据反应物和生产物,利用质量守恒定律正确书写化学方程式:
①3Fe+2O2
点燃
.
Fe3O4;②Fe+H2SO4=FeSO4+H2↑;③Fe+CuCl2=FeCl2+Cu
故答为:(1)Fe;氧气;H2(2)3Fe+2O2
点燃
.
Fe3O4;Fe+H2SO4=FeSO4+H2↑;Fe+CuCl2=FeCl2+Cu点评:
本题考点: 金属的化学性质;物质的鉴别、推断;化学式的书写及意义;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题主要考查了金属的化学性质及应用;掌握物质的推断、鉴别方法和技巧,掌握化学方程式的书写技巧.1年前查看全部
- 下列有关氧气的说法正确的是( ) A.植物的呼吸作用是氧气的重要来源 B.氧气可以支持燃烧,说明氧气具有可燃性 C.氧
下列有关氧气的说法正确的是( )
A.植物的呼吸作用是氧气的重要来源 B.氧气可以支持燃烧,说明氧气具有可燃性 C.氧气是空气中含量最多的物质 D.硫在氧气中燃烧发出蓝紫色火焰,产生刺激性气味  gmw002261年前1
gmw002261年前1 -
 望穿ee的眼 共回答了23个问题
望穿ee的眼 共回答了23个问题 |采纳率95.7%D
1年前查看全部
- 下列有关实验操作不正确的是 [ ] A.点燃可燃性气体时,先验纯
下列有关实验操作不正确的是 [ ]A.点燃可燃性气体时,先验纯
B.用酒精灯火焰的外焰给物质加热
C.倾倒液体时,标签的一面朝向手心
D.将液体加热至沸腾的试管,立即用冷水冲洗 dasiming1年前1
dasiming1年前1 -
 性情故事 共回答了13个问题
性情故事 共回答了13个问题 |采纳率92.3%D1年前查看全部
- 一氧化碳还原氧化铜可以说明一氧化碳具有可燃性吗
 daner11年前1
daner11年前1 -
 cara4807 共回答了17个问题
cara4807 共回答了17个问题 |采纳率88.2%无法说明,一氧化碳还原氧化铜可以说明一氧化碳具有(还原性).
❤您的问题已经被解答~(>^ω^1年前查看全部
- (2014•天桥区三模)已确定某可燃性气体含有甲烷(CH4)和乙炔(C2H2),为进一步确定其组成,现取5.8g混合气体
(2014•天桥区三模)已确定某可燃性气体含有甲烷(CH4)和乙炔(C2H2),为进一步确定其组成,现取5.8g混合气体充分燃烧,测得生成CO2为17.6g,H2O为9g,则混合气体中CH4和乙炔C2H2的质量比为( )
A. 13:23
B. 16:13
C. 3:8
D. 13:8 笨鱼泡泡1年前1
笨鱼泡泡1年前1 -
 玲雅馨君 共回答了14个问题
玲雅馨君 共回答了14个问题 |采纳率78.6%解题思路:根据质量守恒定律,化学反应前后元素的种类和原子的质量不变,将甲烷的化学式改写成CH•H3进行解答即可.将甲烷的化学式改写成CH•H3,则混合气体中甲烷和乙炔碳元素和氢元素的原子个数比是1:1;
生成二氧化碳的质量是17.6g,则碳元素的质量是17.6g×[12/44]=4.8g,设和碳元素结合的氢元素的质量为x
C--H
12 1
4.8g x
[12/4.8g=
1
x] x=0.4g
故混合气体中CH的质量和是:4.8g+0.4g=5.2g,故甲烷中H3的质量是5.8g-5.2g=0.6g,设甲烷中CH的质量是y
CH--H3
13 3
y 0.6g
[13/y=
3
0.6g] y=2.6g
故甲烷的质量是2.6g+0.6g=3.2g,故乙炔的质量是5.8g-3.2g=2.6g
故甲烷和乙炔的质量比是3.2g:2.6g=16:13,观察选项,故选B.点评:
本题考点: 有关化学式的计算和推断;化合物中某元素的质量计算.
考点点评: 本题考查了混合物成分的推断,完成此题,可以巧妙的将化学式进行转化,然后进行计算即可.1年前查看全部
大家在问
- 1当x____时,√(-9x²+6x+3)有意义?
- 2火车的速度为8m/s ,关闭发动机后经过20s停下,则火车这段时间内的运动的距离为
- 3已知(x)是定义在{x>0}上的增函数,满足f(xy)=f(x)+f(y),f(3)=1,求当f(x)+f(x-8)>2
- 4这双袜子5美元——请用英语重复这一句话
- 5第23题的(2)④.求完整解析,写纸上
- 6AgX为什么不溶解于稀硝酸卤化银 为什么不溶解于稀硝酸呢?硝酸不是全部都溶解么?不溶解于稀硝酸又怎么了呀?注意是两问哦~
- 7为什么同样钢丝绳掉方型体的工件比球体重?
- 8虽然它只是一小口井英文翻译
- 9关于x的方程x²-(k-1)x-1=0的两个实数根满足x1<1<x2求实数k的取值范围
- 10如何练习标准的英语口音?有什么好的方法?【我们老师的发音整个就山东腔英语.跟着他越练越糟
- 11一个鸡蛋质量为25分之1kg 比鹅蛋少25分之3kg 一个驼蛋的质量可达1又2分之1kg
- 12倘若在我们中间(猜一英语单词)
- 13一袋大米重25千克,吃了20%,吃了______千克;还剩______千克.
- 14两个数的和是345,差是54,那这两个数分别是?(列式计算)
- 15other怎么表示剩余的全部
