铁的氧化物中谁是碱性氧化物?
 没好2022-10-04 11:39:541条回答
没好2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 BlueYOUME 共回答了16个问题
BlueYOUME 共回答了16个问题 |采纳率87.5%- 铁有五种氧化物:氧化铁、氧化亚铁、二氧化铁、三氧化铁、四氧化三铁,常见的是氧化铁、氧化亚铁和四氧化三铁.
其中氧化亚铁呈现碱性,溶于酸形成能二价铁盐溶液.
氧化铁具有两性,与酸作用生成Fe(Ⅲ)盐,与强碱作用得[Fe(OH)6]3-,可以视作铁的含氧酸中酸性最弱的.
以氧化铁作为分界,铁在Ⅲ价以上的氧化物,包括二氧化铁和三氧化铁均为酸性氧化物,可以视作铁的对应价态的含氧酸的的酸酐.
四氧化三铁是混合价态铁氧化物,性质较特殊,高中简单做氧化铁和氧化亚铁共处处理,也有不妥的地方,就其反应而言能与酸反应,体现出碱性,但一般不作讨论.
一般氧化物酸碱性的规律中,同一元素多种价态的氧化物氧化数高的酸性强.
例如 MnO MnO2 MnO3 Mn2O7
B AB A A
铁与之类似
FeO Fe2O3 FeO2 FeO3
B AB A A - 1年前
相关推荐
- (2014•南宁)下列有关碳和碳的氧化物的说法中,错误的是( )
(2014•南宁)下列有关碳和碳的氧化物的说法中,错误的是( )
A.一氧化碳和二氧化碳都有毒
B.木炭、活性炭都具有吸附性
C.木炭、一氧化碳在一定条件下都能与氧化铜反应
D.金刚石和石墨物理性质不同,是因为它们的碳原子排列方式不同 郁蓝的花儿1年前1
郁蓝的花儿1年前1 -
 LTequila 共回答了14个问题
LTequila 共回答了14个问题 |采纳率92.9%解题思路:A、根据一氧化碳的毒性、二氧化碳的化学性质进行分析判断.
B、木炭、活性炭具有吸附性,能吸附异味和色素.
C、根据木炭、一氧化碳的化学性质进行分析判断.
D、根据金刚石和石墨性质不同的原因进行分析判断.A、一氧化碳有毒,CO2没有毒性,故选项说法错误.
B、木炭、活性炭具有吸附性,能吸附异味和色素,故选项说法正确.
C、木炭、一氧化碳具有还原性,在一定条件下都可与氧化铜反应,夺取氧化铜中的氧,故选项说法正确.
D、金刚石和石墨的结构中碳原子排列方式不同,故选项说法正确.
故选A.点评:
本题考点: 一氧化碳的毒性;二氧化碳的化学性质;碳单质的物理性质及用途;碳的化学性质.
考点点评: 不同难度不大,掌握碳单质的性质与用途、二氧化碳与一氧化碳的化学性质是正确解答本题的关键.1年前查看全部
- 急求:化学.1.有一种非金属氧化物,既能跟某些酸性氧化物化合,又能跟某些碱性氧化物化合,但反应的生成物都不是盐,此氧化物
急求:化学.
1.有一种非金属氧化物,既能跟某些酸性氧化物化合,又能跟某些碱性氧化物化合,但反应的生成物都不是盐,此氧化物的化学式是_______.
2.既能跟某些酸性氧化物化合,又能跟某些碱性氧化物化合,但反应的生成物都不是盐的氧化物____. fjezh46k1年前1
fjezh46k1年前1 -
 精神不ww 共回答了14个问题
精神不ww 共回答了14个问题 |采纳率100%H2O(水与酸性氧化物,如CO2,化合生成碳酸;与碱性氧化物,如Na2O,化合生成强碱氢氧化钠.)1年前查看全部
- 在标准状况下,112ml气态氮的氧化物质量为0.38g.该氧化物中氧元素的质量分数是63.10%求该氧化物的化学式
在标准状况下,112ml气态氮的氧化物质量为0.38g.该氧化物中氧元素的质量分数是63.10%求该氧化物的化学式
A NO2 B N2O C N2O5 D N2O3【本人化学实在不好,如有学好化学的的一些方法,也请教教我, renata_yu1年前1
renata_yu1年前1 -
 tsui_shine 共回答了19个问题
tsui_shine 共回答了19个问题 |采纳率94.7%该气态氮的氧化物的摩尔质量=m/n=m/(v/Vm)=0.38/(0.112/22.4)=76g/mol
因为氧占其质量分数的63.1%=76*0.631=48所以n=3mol,nN=2mol 所以选D
学好化学的话,做笔记非常重要1年前查看全部
- 下列物质中一定属于氧化物的是A某化合物分解后只生成两种氧化物B某化合物分解后只生成两种单质且其中一种
下列物质中一定属于氧化物的是A某化合物分解后只生成两种氧化物B某化合物分解后只生成两种单质且其中一种
是氧气C某化合物是由氧气与一种氧化物发生化合反应而生成的D某化合物是含有氧元素的化合物 applo12201年前1
applo12201年前1 -
 DBGDBGDBG 共回答了17个问题
DBGDBGDBG 共回答了17个问题 |采纳率94.1%感觉应该是C对
A的话,CaCO3=CaO+CO2,但它不是氧化物
B的话,氧化钠和氧气反应生成过氧化钠,但是过氧化物和氧化物是不同的.
D肯定是错的,比如CaCO3就不是氧化物但含有氧元素1年前查看全部
- 化学物质推断题.A元素氢化物的核外电子总数为10个.A的最高价氧化物B与烧碱反应生成盐C.C受热分解出新盐D和气体E.问
化学物质推断题.
A元素氢化物的核外电子总数为10个.A的最高价氧化物B与烧碱反应生成盐C.C受热分解出新盐D和气体E.问A.B.C.D.E各是什么.并给出所有反应的化学方程式和离子方程式.
我推断出A是碳..但是E跟B物质就是一样的了?是不是有问题..请高手给出推断依据.. yl761年前3
yl761年前3 -
 40009024110 共回答了29个问题
40009024110 共回答了29个问题 |采纳率86.2%A不一定是碳,氮、氧、氟均有可能(NH3、H2O、HF的核外电子总数都是10个,不信你数数),通过第二、三句话,把氧和氟排除掉.当A是氮时,B是N2O5(五氧化二氮,硝酸的酸酐),C是NaNO3,硝酸盐不稳定,受热会分
2NaNO3==2NaNO2(亚硝酸钠)+O2
则D是NaNO2,E是氧气1年前查看全部
- X、Y、Z、甲、乙、丙均为初中化学中常见的物质,其中X、Y、Z为单质,Z为红色固体,甲、乙、丙为氧化物,X、丙为黑色固体
 X、Y、Z、甲、乙、丙均为初中化学中常见的物质,其中X、Y、Z为单质,Z为红色固体,甲、乙、丙为氧化物,X、丙为黑色固体.它们之间在一定条件下存在右图所示的转化关系.
X、Y、Z、甲、乙、丙均为初中化学中常见的物质,其中X、Y、Z为单质,Z为红色固体,甲、乙、丙为氧化物,X、丙为黑色固体.它们之间在一定条件下存在右图所示的转化关系.
(1)Z的化学式是______.Y的化学式是______.
(2)写出有关反应的化学方程式:X+Y-C+O2
CO2点燃 .C+O2;
CO2点燃 .
乙+丙-CO+CuO
Cu+CO2△ .CO+CuO.
Cu+CO2△ . chenyue19861年前1
chenyue19861年前1 -
 喜怒哀乐人 共回答了25个问题
喜怒哀乐人 共回答了25个问题 |采纳率92%解题思路:在做推断题时,首先找到解决这一题的题眼,然后根据题眼推断出其它物质.如这一题的题眼是Z为单质,Z为红色固体,所以Z为铜.因Z为单质,Z为红色固体,所以Z为铜.
又因X、丙为黑色固体,且X为单质,丙为氧化物,且X与丙生成Z,所以X为炭,丙为氧化铜.
乙与丙生成Z,且乙为氧化物,所以乙为一氧化碳.
同时,X与Y生成甲,且甲又与X反应生成乙,所以甲为二氧化碳,Y为氧气.
故答案为:
(1)Cu;O2;
(2)C+O2
点燃
.
CO2;CO+CuO
△
.
Cu+CO2点评:
本题考点: 物质的鉴别、推断;化学式的书写及意义;化学性质与物理性质的差别及应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 在做推断题时,不光要求我们找到解决此题的题眼,还要求我们掌握所学的化学知识.同时也要大胆的猜测,然后用化学知识去验证.1年前查看全部
- A、B、C、D、E是中学常见的5种化合物,A、B是氧化物,元素X、Y的单质是生活中常见的金属,相关物质间的关系如图所示.
A、B、C、D、E是中学常见的5种化合物,A、B是氧化物,元素X、Y的单质是生活中常见的金属,相关物质间的关系如图所示.

(1)X的单质与A反应的化学方程式是2Al+Fe2O3
Al2O3+2Fe高温 .2Al+Fe2O3.
Al2O3+2Fe高温 .
(2)若试剂1是NaOH溶液.X的单质与试剂1反应的离子方程式是______.
(3)若试剂1和试剂2均是稀硫酸.
①将物质C溶于水,其溶液呈______性(填“酸”、“碱”或“中”).
②某高效净水剂是由Y(OH)SO4聚合得到的,工业上以E、稀硫酸和亚硝酸钠(NaNO2)为原料制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式为______. tysouthriver1年前1
tysouthriver1年前1 -
 我要到月球 共回答了17个问题
我要到月球 共回答了17个问题 |采纳率100%解题思路:元素X、Y的单质是生活中常见的金属,分别为Al、Fe中的一种,且X与氧化物A反应得到Y与氧化物B,应是铝热反应,则X为Al,Y为Fe,B为氧化铝,A为Fe的氧化物,Y(Fe)与试剂2(硫酸)反应得到E为硫酸亚铁,A与试剂2(硫酸)反应得到D,且D能与Fe反应得到E,则A为氧化铁,D为硫酸铁.Al、氧化铝都与试剂1(NaOH溶液)反应得到C,则C为偏铝酸钠,据此解答.元素X、Y的单质是生活中常见的金属,分别为Al、Fe中的一种,且X与氧化物A反应得到Y与氧化物B,应是铝热反应,则X为Al,Y为Fe,B为氧化铝,A为Fe的氧化物,Y(Fe)与试剂2(硫酸)反应得到E为硫酸亚铁,A与试剂2(硫酸)反应得到D,且D能与Fe反应得到E,则A为氧化铁,D为硫酸铁.Al、氧化铝都与试剂1(NaOH溶液)反应得到C,则C为偏铝酸钠,
(1)X的单质与A反应的化学方程式是:2Al+Fe2O3
高温
.
Al2O3+2Fe,故答案为:2Al+Fe2O3
高温
.
Al2O3+2Fe;
(2)若试剂1是NaOH溶液.X的单质与试剂1反应的离子方程式是:2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(3)①C为偏铝酸钠,其溶液中偏铝酸根水解,溶液呈碱性,故答案为:碱;
②某高效净水剂是由Fe(OH)SO4聚合得到的,工业上以FeSO4、稀硫酸和亚硝酸钠(NaNO2)为原料制备Fe(OH)SO4,反应中有NO生成,还有硫酸钠生成,该反应的化学方程式为:2FeSO4+2NaNO2+H2SO4=2Fe(OH)SO4+Na2SO4+2NO↑,
故答案为:2FeSO4+2NaNO2+H2SO4=2Fe(OH)SO4+Na2SO4+2NO↑.点评:
本题考点: 无机物的推断.
考点点评: 本题考查无机物的推断,涉及Fe、Al元素单质化合物的性质,注意对铝热反应的掌握,在推断中经常涉及,难度中等.1年前查看全部
- 氧化物、酸、碱、盐相互之间的关系是九年级化学中重要学习内容之一.现有如图所示的转换关系:
氧化物、酸、碱、盐相互之间的关系是九年级化学中重要学习内容之一.现有如图所示的转换关系:

(1)已知人体的胃液中含有A,试写出下列物质的化学式B______,F______G______.
(2)C→E的化学方程式______;D→G的化学方程式______. yanzhimiao1年前1
yanzhimiao1年前1 -
 lijz58 共回答了19个问题
lijz58 共回答了19个问题 |采纳率84.2%解题思路:(1)根据C中加入氢氧化钠蓝色沉淀判断E为氢氧化铜,C为可溶性铜盐,根据C的种类和氧化铜的性质判断A为酸,D溶液中加入氯化钡生成不溶于硝酸的白色沉淀,说明G为硫酸钡,D中含有硫酸根,则B为硫酸;结合推知C,再推导A.
(2)根据氧化铜与盐酸反应的性质以及硫酸铜溶液和氯化钡溶液反应的性质书写方程式.(1)D溶液中加入氯化钡生成不溶于硝酸的白色沉淀,说明G为硫酸钡或氯化银,根据D的来源,D中不可能含有银离子,故必含有硫酸根,为可溶性的硫酸盐;又因是氧化铜与B反应生成的,故D为硫酸铜,B为硫酸;硫酸铜与氯化钡反应生成硫酸钡和氯化铜,故C为氯化铜;氯化铜与氢氧化钠反应能生成蓝色的氢氧化铜沉淀和氯化钠,则E为氢氧化铜,F为氯化钠;氧化铜与A反应生成氯化铜,则A 为盐酸.
(2)A为盐酸,C为氯化铜,氧化铜与盐酸反应生成氯化铜和水,方程式为CuO+2HCl=CuCl2+H2O;D为硫酸铜,与氯化钡反应生成硫酸钡和氯化铜,方程式为CuSO4+BaCl2=CuCl2+BaSO4↓.
故答案为:(1)H2SO4;NaCl;BaSO4;(2)CuO+2HCl=CuCl2+H2O;CuSO4+BaCl2=CuCl2+BaSO4↓.点评:
本题考点: 物质的鉴别、推断;化学式的书写及意义;书写化学方程式、文字表达式、电离方程式.
考点点评: 物质的推断是初中化学的难重点,也是中考的热点之一,了解物质的性质是解题的前提条件,解题时还要注意前后步骤间的联系,充分利用综合归纳法得出完整合理的结论.1年前查看全部
- KMnO4,氨气是含有氧元素的物质,混合物,纯净物,化合物,氧化物还是单质
KMnO4,氨气是含有氧元素的物质,混合物,纯净物,化合物,氧化物还是单质
KMnO4,氨气如果不属于一类物质可以分着答,急用! zzsspp011年前1
zzsspp011年前1 -
 CHUAHYAPWIN 共回答了25个问题
CHUAHYAPWIN 共回答了25个问题 |采纳率88%KMnO4是由多种元素合成的,当然是化合物啦!
NH3氨气是由两种元素合成的,也是化合物!1年前查看全部
- (2012•佛山)A是钠的氧化物,B、C、D、E是初中常见的盐.图1是这些物质的转化关系,部分反应物、生成物及反应条件已
(2012•佛山)A是钠的氧化物,B、C、D、E是初中常见的盐.图1是这些物质的转化关系,部分反应物、生成物及反应条件已省略.

(1)请写出下列物质的化学式:C______,E______.
(2)A→B反应的化学方程式为______.
(3)可用D制烧碱,写出反应的化学方程式______.
(4)要将没有标签的B、C、D、E四种溶液区分开来,某同学设计了如图2所示实验方案.方案中试剂①为______(填化学式,下同),试剂②为______溶液. 刘改之1年前1
刘改之1年前1 -
 mmsaraqi 共回答了14个问题
mmsaraqi 共回答了14个问题 |采纳率92.9%解题思路:(1)根据题意,A是钠的氧化物,应为氧化钠,氧化钠与硫酸反应生成了硫酸钠和水,硫酸钠和硝酸钡反应生成了硫酸钡和硝酸钠,氧化钠与硝酸反应也能生成硝酸钠,所以,可推出C为硝酸钠;由硫酸钠与氯化钡反应生成了硫酸钡沉淀和氯化钠,氧化钠和盐酸反应应为能生成氯化钠,所以可推出E为氯化钠;
(2)根据氧化钠和硫酸的反应写出反应的方程式;
(3)氧化钠和二氧化碳反应生成了碳酸钠,碳酸钠和氢氧化钙反应生成了氢氧化钠,根据反应写出反应的方程式;
(4)根据碳酸钠与酸反应放出气体,可以先鉴别出来,再根据硫酸钠能与可溶性的钡盐反应生成了硫酸钡沉淀,将硫酸钠鉴别出来.由此可推出试剂②.(1)由题意可知,A是钠的氧化物,应为氧化钠,氧化钠与硫酸反应生成了硫酸钠和水,硫酸钠和硝酸钡反应生成了硫酸钡和硝酸钠,氧化钠与硝酸反应也能生成硝酸钠,所以,可推出C为硝酸钠,化学式是NaNO3;由硫酸钠与氯化钡反应生成了硫酸钡沉淀和氯化钠,氧化钠和盐酸反应应为能生成氯化钠,所以可突出E为氯化钠,化学式是:NaCl;
(2)氧化钠和硫酸的反应,生成了硫酸钠和水,反应的方程式是:Na2O+H2SO4=Na2SO4+H2O;
(3)碳酸钠和氢氧化钙反应生成了氢氧化钠和碳酸钙沉淀,常用此反应制取烧碱,反应的方程式是:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
(4)由于碳酸钠与酸反应放出气体,可以先鉴别出来.所以,试剂①是硝酸;再根据硫酸钠能与可溶性的钡盐反应生成了硫酸钡沉淀,将硫酸钠鉴别出来.由此,可推出试剂②是硝酸钡.
故答为:(1)NaNO3NaCl(2)Na2O+H2SO4=Na2SO4+H2O;(3)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;(4)HNO3,Ba(NO3)2.点评:
本题考点: 物质的鉴别、推断.
考点点评: 此题为框图式物质推断题,完成此类题目,关键是找准解题突破口,直接得出结论,然后利用顺向或逆向或两边向中间推,逐一导出其他结论.1年前查看全部
- 用适当溶液吧3.31g某铁矿石溶解,加入过量碱溶液,烧灼生成的沉淀,的2.4gFe2O3,已知铁矿石中铁的氧化物
用适当溶液吧3.31g某铁矿石溶解,加入过量碱溶液,烧灼生成的沉淀,的2.4gFe2O3,已知铁矿石中铁的氧化物
质量分数位70%.计算(1)铁矿石中铁的质量分数(2)铁矿石中铁的氧化物的化学式 henryjx1年前1
henryjx1年前1 -
 篮球杰 共回答了27个问题
篮球杰 共回答了27个问题 |采纳率96.3%(1)Fe2O3有2.4克,铁元素有1.68g,所以其质量分数为1.68/3.31=50.8%
(2)铁氧化物有3.31*70%=2.317g,而铁有1.68g,所以铁约占72.5%,故应是Fe3O41年前查看全部
- 已知:A是相对分子质量最小的氧化物,D是最简单的有机物,也是天然气中最主要的成分.请分析A、B、C、D、E五种物质之间的
已知:A是相对分子质量最小的氧化物,D是最简单的有机物,也是天然气中最主要的成分.请分析A、B、C、D、E五种物质之间的变化关系,回答有关问题.
(1)请写出D、E的化学式:D______ E______
(2)请写出①反应的化学方程式:______;
(3)E溶于水后溶质的化学式为______.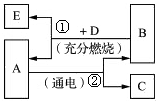
 将青春挥洒向大海1年前1
将青春挥洒向大海1年前1 -
 好ID被狗用了 共回答了16个问题
好ID被狗用了 共回答了16个问题 |采纳率93.8%A是相对分子质量最小的氧化物,则A是水,通电能分解生成氢气和氧气,故B和C为氢气或氧气;D是最简单的有机物,也是天然气中最主要的成分,则D是甲烷;甲烷能与氧气反应生成水和二氧化碳,故B是氧气,C是氢气,生成的E为二氧化碳,带入框图,推断合理;
(1)D是甲烷,E是二氧化碳,故填:CH 4 ,CO 2 ;
(2)甲烷能与氧气反应生成二氧化碳和水,故填:CH 4 +2O 2
点燃
.
CO 2 +2H 2 O;
(3)E是二氧化碳,溶于水与水反应生成碳酸,故溶质是碳酸,故填:H 2 CO 3 ;1年前查看全部
- S.H.O.N四种元素中(选择一种或几种),1最轻的气体_2污染空气的氧化物_3常温常压下以液态形式存在的氧化物
 denver451年前1
denver451年前1 -
 zz_555 共回答了15个问题
zz_555 共回答了15个问题 |采纳率93.3%H2
SO2
H2O1年前查看全部
- 怎样最容易判断是阴离子和阳离子Y和最容易判断化合物,氧化物、单质、纯净物,混合物
 小马过河-01年前3
小马过河-01年前3 -
 allenwxy 共回答了25个问题
allenwxy 共回答了25个问题 |采纳率92%带正电荷的是阳离子,带负电荷的是阴离子.
由多种元素组成的纯净物是化合物
只有氧元素和其他一种元素组成的化合物是氧化物
只由一种元素组成的纯净物是单质
只含有一种物质的是纯净物
含有多种物质的是混合物1年前查看全部
- 下列物质是自来水厂对水净化过程常用的消毒剂,其中属于氧化物的是 ( )
下列物质是自来水厂对水净化过程常用的消毒剂,其中属于氧化物的是( )
A.Cl2
B.O3
C.ClO2
D.Ca(ClO)2 koine1年前1
koine1年前1 -
 hj1019 共回答了19个问题
hj1019 共回答了19个问题 |采纳率94.7%解题思路:氧化物是指由两种元素组成并且其中一种元素是氧元素的化合物.氧化物的特点是由两种元素组成的化合物,其中一种元素是氧元素.A、氯气是由氯元素组成的纯净物,属于单质,不属于氧化物.故不正确;
B、臭氧是由氧元素组成的纯净物,属于单质,不属于氧化物.故不正确;
C、二氧化氯是由氧元素和氯元素组成的化合物,属于氧化物.故正确;
D、次氯酸钙是由钙元素、氯元素和氧元素组成的,不属于氧化物.故不正确.
故选:C.点评:
本题考点: 从组成上识别氧化物.
考点点评: 解答本题要正确的分析物质是由几种元素组成的,如果由氧元素和另外一种元素组成并且属于化合物就属于氧化物.1年前查看全部
- 快考试了,化学不好,求助怎么判断物质加入水中后,得到的溶液时无色透明的?哪些离子能在水溶液中共存?氧化物+水→碱,怎么写
快考试了,化学不好,求助
怎么判断物质加入水中后,得到的溶液时无色透明的?
哪些离子能在水溶液中共存?
氧化物+水→碱,怎么写化学方程式?是复分解反应吗?
 key20031年前1
key20031年前1 -
 fu2046 共回答了19个问题
fu2046 共回答了19个问题 |采纳率94.7%【1】怎么判断物质加入水中后,得到的溶液时无色透明的?
答:记住无色的离子(大部分阳离子、阴离子);也可以牢记有色的离子(少量的阳离子、阴离子;例如:3价铁离子、高锰酸根离子),要记全部的有色离子,除此之外的,就得到无色透明的溶液.
【2】哪些离子能在水溶液中共存?
答:不能发生化学反应的离子,就可以共存.
【3】氧化物+水→碱,怎么写化学方程式?是复分解反应吗?
答: 氧化物+水→碱, 例如 CaO + H2O = Ca(OH)2 不是复分解反应.1年前查看全部
- 已知ABCDEFG七种物质,C是最常见的氧化物,D是蓝色沉淀,G是一种化合物,A是由2种元素组成.
已知ABCDEFG七种物质,C是最常见的氧化物,D是蓝色沉淀,G是一种化合物,A是由2种元素组成.
且有A+B=C+D C+D=E+F B+D=E+G 问:1、C是什么物质?2、请写出B+D=E+G的化学方程式.(这是今年长沙市初中化学竞赛复赛的最后一题.我想了半天都没想出来,总觉得A+B=C+D C+D=E+F有问题.)
如果我的问题题目中有错误的话,请指出改正,并给予回答。 姗姗ID1年前1
姗姗ID1年前1 -
 wengzhj 共回答了31个问题
wengzhj 共回答了31个问题 |采纳率87.1%如果题目没问题的话,只能是这种推断,D是蓝色沉淀,只能是氢氧化铜,C是最常见氧化物,有水和二氧化碳,水不可能,只能是二氧化碳,考虑到A是两种元素组成,那么A只能是水了,那么B要么是碳酸铜要么是碱式碳酸铜,AB反应就是碱...1年前查看全部
- 氢氧化钙与氧化钙反应吗现有钙、氢、氧、硫四种元素现用这些元素组成碱与氧化物写出碱与氧化物反应方程式氢氧化钙与氧化钙反应吗
 玫瑰烤翅1年前1
玫瑰烤翅1年前1 -
 度是0549 共回答了19个问题
度是0549 共回答了19个问题 |采纳率100%氢氧化钙与氧化钙不反应
Ca(OH)2+SO2=CaSO3+H2O
Ca(OH)2+SO3=CaSO4+H2O1年前查看全部
- (2014•徐汇区一模)有一种高效安全的灭菌消毒剂,其化学式为RO2,实验测得该氧化物中R与O的质量比为71:64,则R
(2014•徐汇区一模)有一种高效安全的灭菌消毒剂,其化学式为RO2,实验测得该氧化物中R与O的质量比为71:64,则R02是( )
A.ClO2
B.NO2
C.SO2
D.CaO gl99991年前1
gl99991年前1 -
 yuanye188 共回答了18个问题
yuanye188 共回答了18个问题 |采纳率94.4%解题思路:根据根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,可计算出R的相对原子质量,从而确定R的元素种类,写出其氧化物的化学式即可.设R的相对原子质量是x,则
x:(16×2)=71:64 解得x=35.5
因为氯原子的相对原子质量是35.5,所以RO2的化学式为ClO2.
故选:A.点评:
本题考点: 元素质量比的计算.
考点点评: 本题难度不大,考查同学们灵活运用化学式的有关计算进行推断化学式的能力.1年前查看全部
- (2006•南通模拟)氧化物X(初中化学未学过)是一种安全无毒的物质,常用作长途运输时鱼苗的供氧剂.已知X含有的两种元素
(2006•南通模拟)氧化物X(初中化学未学过)是一种安全无毒的物质,常用作长途运输时鱼苗的供氧剂.已知X含有的两种元素的质量比为5:4.由X出发有下列转化关系,其中⑤是工业中冶炼目前使用最广泛的一种金属I 的反应,B、E、G是常见的气体,E、F是非金属单质,B能使澄清石灰水变浑浊.回答下列问题:

(1)写出反应⑤的化学方程式3CO+Fe2O3
2Fe+3CO23CO+Fe2O3高温 .
2Fe+3CO2;高温 .
(2)如何证明高温下C物质发生了部分分解?答:首先,取少量③反应后的固体加入稀盐酸,如果产生气泡,说明碳酸钙有剩余加入稀盐酸,如果产生气泡,说明碳酸钙有剩余;然后,再取少量③反应后的固体,加入少量的水,搅拌,滴入几滴酚酞试液,如果变红色,说明已有氧化钙生成,碳酸钙发生了分解加入少量的水,搅拌,滴入几滴酚酞试液,如果变红色,说明已有氧化钙生成,碳酸钙发生了分解.
(3)氧化物X是CaO2CaO2.(写化学式) 老三到了1年前1
老三到了1年前1 -
 wxb163 共回答了13个问题
wxb163 共回答了13个问题 |采纳率92.3%I为目前使用最广泛的金属,则I为铁;B能使澄清的石灰水变浑浊,则B为二氧化碳;⑤是工业中冶炼目前使用最广泛的一种金属I 的反应,G为气体,生成物中还有二氧化碳,则G为一氧化碳;H为氧化铁;E和F点燃生成G一...1年前查看全部
- 某兴趣小组同学在一份资料中了解到:铜有CuO和Cu2O(红色)两种常见的氧化物.因为Cu和Cu2O均为红色,故他们猜测,
某兴趣小组同学在一份资料中了解到:铜有CuO和Cu2O(红色)两种常见的氧化物.因为Cu和Cu2O均为红色,故他们猜测,在H2还原CuO所得的红色产物中可能含有Cu2O.
(1)该小组同学准确称取了8.0g黑色CuO粉末放入大试管中,不断通入足量的H2,在加热条件下进行还原,如果产物只有Cu,其质量应为 ___ .
(2)该小组在H2还原CuO时,当发现8.0g黑色CuO粉末全部转变成红色时,停止加热,冷却后称得固体质量为6.8g.此红色固体中氧元素的质量为 ___ ,以此推得Cu2O的质量为 ___ .
(3)将(2)中所得的6.8g固体放入烧杯中,加入48.0g过量稀盐酸(Cu2O与稀盐酸的反应为:Cu2O+2HCl=CuCl2+Cu+H2O),充分搅拌,除有红色固体外,还发现溶液变蓝.试计算此蓝色溶液中CuCl2的质量分数.
 辽东鹤1年前1
辽东鹤1年前1 -
 码婆 共回答了19个问题
码婆 共回答了19个问题 |采纳率100%解题思路:氢气的化学性质有:可燃性和还原性.根据元素守恒,可以用氧化铜的质量求铜的质量.冷却后称得固体质量为6.8g,因此有氧化亚铜,与6.4g的差值就是氧元素的质量,从而得到氧化亚铜的质量.铜与氧化亚铜的混合物,加入过量稀盐酸,只有氧化亚铜反应,铜不反应,因此根据化学方程式可以求氯化亚铜的质量,根据质量守恒定律求溶液的质量,再根据溶质的质量分数求反应后溶液的质量分数.(1)本题中通入足量的H2,在加热条件下进行还原,如果固体产物只有Cu,根据元素守恒,CuO粉末是8.0g,那么铜的质量是:8.0g×[64/80×100%=6.4g,故答案为:6.4g
(2)固体产物只有铜时,质量是6.4g,第二次反应,冷却后称得固体质量为6.8g,是铜与氧化亚铜的混合物,因此增加的质量是氧元素的质量,氧元素的质量是:6.8g-6.4g=0.4g;根据氧元素的质量求氧化亚铜的质量为:0.4g÷
16
144]=3.6g.故答案为:0.4g3.6g
(3)设生成CuCl2的质量为x,生成Cu的质量为y.
Cu2O+2HCl=CuCl2+Cu+H2O
14413564
3.6gx y
[144/3.6g=
135
x],x=3.375g
[144/3.6g=
64
y],y=1.6g
w(CuCl2)=[3.375g/48.0g+3.6g-1.6g]×100%=6.75%
故答案为:6.75%点评:
本题考点: 碳、一氧化碳、氢气还原氧化铜实验;有关溶质质量分数的简单计算;根据化学反应方程式的计算.
考点点评: 本考点既考查了氢气的还原性和质量守恒定律,又考查了根据化学方程式的计算和溶质的质量分数公式的综合应用,通过计算探究物质的组成,是中考的一个重点,也是一个难点.本题考查的知识点比较多,只要认真分析,问题就不难解决.本考点主要出现在填空题和实验题中.1年前查看全部
- A、B、C分别是三种常见单质;D、E、F则是常见的三种氧化物,且有如图所示转化关系,下列说法错误的是( )
 A、B、C分别是三种常见单质;D、E、F则是常见的三种氧化物,且有如图所示转化关系,下列说法错误的是( )
A、B、C分别是三种常见单质;D、E、F则是常见的三种氧化物,且有如图所示转化关系,下列说法错误的是( )
A.B可能是金属
B.A、B、C中肯定有O2
C.D中一定含有A元素
D.D、E组成元素不可能完全相同 花悦1年前1
花悦1年前1 -
 hjabmysys 共回答了23个问题
hjabmysys 共回答了23个问题 |采纳率91.3%解题思路:A.置换反应B+D→A+F可以是氧化性置换,也可以是还原性置换,以此判断金属或非金属;
B.根据反应B+D→A+F和A+C→E判断;
C.根据反应A+D→E和A+C→E以及B+D→A+F判断;
D.常见的氧化物中氧为-2价,则另一种元素显正价,故在D中A元素显正价,被还原剂B可以还原为A中的0价态.A.置换反应B+D→A+F可以是氧化性置换(则B是非金属),也可以是还原性置换(B是非金属或金属单质),故以A正确;
B.B+D→A+F是置换反应,B是单质,其中D、F为氧化物,则A肯定不含O元素,A+C→E是化合反应,A、C为单质,E为氧化物,所以C一定为氧气,故B正确;
C.由转化关系可知:A+D→E和A+C→E都是化合反应,故E中一定含有A元素,而B+D→A+F是置换反应,B是单质,则A元素只能来自化合物D,故C正确;
D.因为常见的氧化物中氧为-2价,则另一种元素显正价,故在D中A元素显正价,被还原剂B(金属)可以还原为A中的0价态,而D被A还原为A元素低价态的化合物E,如若D是CO2;B为Mg;A为C;E为CO,故D错误;
故选D.点评:
本题考点: 无机物的推断.
考点点评: 本题考查无机物的推断,题目难度中等,本题从物质的转化关系和物质的种类的角度分析.1年前查看全部
- 写出氮的气态氢化物与硫的最高价氧化物对应水化物反应的化学方程式
 ccc6543211年前0
ccc6543211年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 液氧是什么颜色?什么类别?是氧化物,酸,碱,盐,金属,还是非金属?两个问题都要回答
 missroad20041年前1
missroad20041年前1 -
 musk2005 共回答了14个问题
musk2005 共回答了14个问题 |采纳率100%淡蓝色,是非金属单质1年前查看全部
- 某元素R的最高价氧化物分子式为RO2,其中R的含量占27.3%,则R的原子量为
某元素R的最高价氧化物分子式为RO2,其中R的含量占27.3%,则R的原子量为
如题 addisonpi1年前1
addisonpi1年前1 -
 ptaclh 共回答了14个问题
ptaclh 共回答了14个问题 |采纳率100%12,CO2,是二氧化碳1年前查看全部
- 由氢氧氮组成的化学式酸 碱 盐 形成酸雨的一种氧化物
 版主的vv1年前5
版主的vv1年前5 -
 鞭策人生 共回答了16个问题
鞭策人生 共回答了16个问题 |采纳率93.8%酸:HNO3
碱:NH4OH
盐:NH4NO3
形成酸雨的一种氧化物:NO21年前查看全部
- R元素的氧化物相对分子质量 142,其中氧原子相对原子质量和 80,R原子核16粒子不带电,儿核电荷数为15 求
R元素的氧化物相对分子质量 142,其中氧原子相对原子质量和 80,R原子核16粒子不带电,儿核电荷数为15 求
2.R元素化合价 babylady111年前3
babylady111年前3 -
 贫血的蚂蚁 共回答了19个问题
贫血的蚂蚁 共回答了19个问题 |采纳率94.7%P2O5
化合价为-3,+5 ,在P2O5中显示+5价1年前查看全部
- 某元素R的一种化合物的化学式为R3PO4,期中P为+5价,则元素R以相同的化合价形成的氧化物的化学式为( )
某元素R的一种化合物的化学式为R3PO4,期中P为+5价,则元素R以相同的化合价形成的氧化物的化学式为( )
A、R2O B、R2O5 C、R2O3 D、RO2 香熏柠檬1年前6
香熏柠檬1年前6 -
 灵动第七感 共回答了15个问题
灵动第七感 共回答了15个问题 |采纳率86.7%R的化合价×3 + 5 + 4 × ( - 2) = 0
所以R的化合价 = +1
A中R是+1价,正确
B中R是+5价,错误.
C中R是+3价,错误
D中R是+4价,错误
选择A1年前查看全部
- 1.下列叙述正确的是( )A.氧化反应一定是化合反应B.碳跟氧化物的反应不一定都是置换反应C.单质和化合物的反应一定都是
1.下列叙述正确的是( )
A.氧化反应一定是化合反应
B.碳跟氧化物的反应不一定都是置换反应
C.单质和化合物的反应一定都是置换反应
D.有沉淀生成的反应一定是复分解反应
2.电离时,一定相等的是( )
A.每个阴,阳离子所带电荷
B.阴,阳离子个数
C.阴阳离子所带电荷总数
D.以上说法都不对
并说说为什么?↓_↓ outdidi3211年前1
outdidi3211年前1 -
 逆鳞乱 共回答了15个问题
逆鳞乱 共回答了15个问题 |采纳率80%1.B
A错 反例:电解水
B对 如C在高温下与CO反应
C错 如铁与浓硫酸
D错 如H2S与SO2反应
2.C,因为电荷守恒1年前查看全部
- 某+2价金属的氧化物中,金属元素与氧元素的质量比为3:2,则此氧化物的相对分子质量为
 coolersummer1年前4
coolersummer1年前4 -
 mw_j99 共回答了24个问题
mw_j99 共回答了24个问题 |采纳率83.3%金属的相对分子量为x
x:16=3:2
新4
金属为镁 相对分子量为40
或5*16/2=401年前查看全部
- 1.有一种氧化物既能跟某些酸性要化物化合,又能跟某些碱性氧化物化合,但反应物都不是盐,此氧化物的化学式是_
1.有一种氧化物既能跟某些酸性要化物化合,又能跟某些碱性氧化物化合,但反应物都不是盐,此氧化物的化学式是_
2.在白色粉末A中加入B后成为蓝色溶液,向其中加入试剂C生成白色沉淀硫酸钡,过滤后向滤液中加入试剂D得到蓝色沉淀E.再次过滤后,滤液为氯化钡溶液.
根据以上现象判断:
A_ B_ C_ D_ E_
3.在硫酸钠溶液中,含有少量杂质碳酸钠,适量加入下列试剂,即可除去杂质碳酸钠有不会引入新杂质的是_.
A.硝酸银 B.硫酸 C.盐酸 D.氯化钡 兰色灵魂1年前5
兰色灵魂1年前5 -
 言留 共回答了19个问题
言留 共回答了19个问题 |采纳率89.5%1 Al2O3
2 A CuSO4
B H2O
C BaCl2
D Ba(OH)2
E Cu(OH)2 解有很多
3 B1年前查看全部
- 已知周期表中,元素Q、W、Y与元素X相邻.R与Y同族.Y的最高化合价氧化物的水化物是强酸.回答下列问题:
已知周期表中,元素Q、W、Y与元素X相邻.R与Y同族.Y的最高化合价氧化物的水化物是强酸.回答下列问题:
(1)W与Q可以形成一种高温结构陶瓷材料.W的氯化物分子呈正四面体结构,W的氧化物的晶体类型是______;
(2)Q的具有相同化合价且可以相互转变的氧化物是______;
(3)R和Y形成的二种化合物中,Y呈现最高化合价的化合物是化学式是______;
(4)这5个元素的氢化物分子中,①立体结构类型相同的氢化物的沸点从高到低排列次序是(填化学式)______,其原因是______
②电子总数相同的氢化物的化学式和立体结构分别是______;
(5)W和Q所形成的结构陶瓷材料的一种合成方法如下:W的氯化物与Q的氢化物加热反应,生成化合物W(QH2)4和HCl气体;W(QH2)4在高温下分解生成Q的氢化物和该陶瓷材料.上述相关反应的化学方程式(各物质用化学式表示)是______. feifei87171年前1
feifei87171年前1 -
 小袄 共回答了20个问题
小袄 共回答了20个问题 |采纳率85%解题思路:(1)根据W与Q可以形成一种高温结构陶瓷材料,及W的氯化物分子呈正四面体结构可知W为硅,然后分析二氧化硅的晶体类型;
(2)根据高温结构陶瓷材料可知Q可能为氮元素,则二氧化氮与四氧化二氮可以相互转变;
(3)根据位置及Y的最高化合价氧化物的水化物是强酸、R和Y形成的二价化合物来推断R;
(4)根据氢键的存在来比较氢化物的沸点,并根据最外层电子数来分析结构;
(5)根据W的氯化物与Q的氢化物加热反应,生成化合物W(QH2)4和HCl气;W(QH2)4在高温下分解生成Q的氢化物和该陶瓷材料,利用反应物与生成物来书写化学反应方程式.(1)W的氯化物为正四面体型,则应为SiCl4或CCl4,又W与Q形成高温陶瓷,故可推断W为Si,W的氧化物为SiO2,原子之间以共价键结合成空间网状结构,则为原子晶体,故答案为:原子晶体;(2)高温陶瓷可联想到Si3N4,Q为...
点评:
本题考点: 位置结构性质的相互关系应用.
考点点评: 本题考查位置、结构、性质的关系及应用,明确物质的性质及元素的位置来推断元素是解答的关键,并注意与元素化合物知识、原子结构与性质相联系来分析解答即可.1年前查看全部
- 为测定某纯净的铁的氧化物的组成,称取14.4g该氧化物,在加热的条件下用CO气体还原该氧化物,并将反应后导出的气体通入过
为测定某纯净的铁的氧化物的组成,称取14.4g该氧化物,在加热的条件下用CO气体还原该氧化物,并将反应后导出的气体通入过量的澄清石灰水中,得到20g沉淀,试确定铁的氧化物的化学式.
 背着氧气的鱼1年前1
背着氧气的鱼1年前1 -
 xufeiya 共回答了18个问题
xufeiya 共回答了18个问题 |采纳率88.9%FexOy --------- yCO------yCO2------yCaCO3
56x+16y---------------------------------------100y
14.4------------------------------------------------20
解得,x:y=1:1
即FeO1年前查看全部
- 某元素X的碳酸氢盐[X(HCO3)]在高温下完全分解的产物都是氧化物,现取3.24g这种碳酸氢盐高温完全分解后得到
某元素X的碳酸氢盐[X(HCO3)]在高温下完全分解的产物都是氧化物,现取3.24g这种碳酸氢盐高温完全分解后得到
1.12g固体,又知X的原子核里有20个中子.
(1)通过计算确定X是什么元素 zouhailiang123451年前3
zouhailiang123451年前3 -
 fsy494944105 共回答了23个问题
fsy494944105 共回答了23个问题 |采纳率95.7%钙元素1年前查看全部
- 有氧化氯吗?属于氯化物还是氧化物?我想多识一点.
有氧化氯吗?属于氯化物还是氧化物?我想多识一点.
好像有个 Cl2O7 flashbinbin1年前3
flashbinbin1年前3 -
 t_dolphin 共回答了15个问题
t_dolphin 共回答了15个问题 |采纳率93.3%基本上就这几种:Cl2O、Cl2O3、ClO2、Cl2O5、Cl2O6、Cl2O7.其中偶数价Cl的化合物ClO2、Cl2O6更不稳定.其它对应是氯的含氧酸HClO、HClO2、HClO3、HClO4的酸酐,也不是很稳定.
氧的非金属性强于氯,因此氯和氧的化合物是氧化物而不是氯化物.
====
[原创回答团]1年前查看全部
- 我需要纯净物的30个混合物的10个化合物氧化物各20个谢谢
我需要纯净物的30个混合物的10个化合物氧化物各20个谢谢
可以加分不能超过20...还有不愿意帮忙的请绕道走谢谢,无聊发言也别来 dd唐龙1年前1
dd唐龙1年前1 -
 beete 共回答了19个问题
beete 共回答了19个问题 |采纳率100%化学方程式不是这么分的(纯净物的30个混合物的10个化合物氧化物各20个)
化合反应:S+O2=SO2,C+O2=CO2,2Mg+O2=2MgO,3Fe+2O2=Fe3O4,4P+5O2=2P2O5,2H2+O2=H2O,2CO+O2=CO2(反应条件全是点燃),C+CO2=2CO(高温),CuSO4+5H2O=CuSO4.5H2O,CaO+H2O=Ca(OH)2,CaCO3+H2O+CO2=Ca(HCO3)2,CO2+H2O=H2CO3
分解反应:2KMnO4=O2气体+MnO2+K2MnO4,2HgO=O2气体+2Hg,Ca(HCO3)=CaCO3沉淀+H2O+CO2气体,CuSO4.5H2O=CuSO4+5H2O,H2CO3=CO2气体+H2O(反应条件全是加热),2KClO3=3O2气体+2KCl(MnO2,加热),2H2O2=2H2O+O2气体(MnO2),CaCO3=CaO+CO2气体(高温),2H2O=2H2气体+O2气体(通电)
置换反应:C+2CuO=2Cu+CO2气体(高温),H2+CuO=Cu+H2O(加热),
复分解反应:CaCO3+HCl=CaCl2+H2O+CO2气体
其他反应:Ca(OH)2+CO2=H2O+CaCO3沉淀,CO+CuO=Cu+CO2(加热)1年前查看全部
- 测定植物体内的氧化物酶同工酶有何意义
 q_gyo5c7ee454e1年前2
q_gyo5c7ee454e1年前2 -
 shaojialin 共回答了12个问题
shaojialin 共回答了12个问题 |采纳率91.7%判断植物的功能1年前查看全部
- 下列能与酸反应生成盐和水的氧化物是( )
下列能与酸反应生成盐和水的氧化物是( )
1.H2O
2.NaOH
3.CO2
4.MgO uu堂1年前3
uu堂1年前3 -
 nnfmx 共回答了20个问题
nnfmx 共回答了20个问题 |采纳率90%4 比如 2HCL+MgO=H2O+MgCl21年前查看全部
- 锆(Zr)的一种氧化物是耐高温的新型陶瓷材料,经测定,锆原子核内有51个中子,核外有40个电子,其氯化物的相对分子质量为
锆(Zr)的一种氧化物是耐高温的新型陶瓷材料,经测定,锆原子核内有51个中子,核外有40个电子,其氯化物的相对分子质量为233,若锆的氯化物和氧化物中锆的化合价相同.则氧化物的化学式为( )
A. Zr2O
B. ZrO
C. Zr2O3
D. ZrO2 溪里鱼1年前1
溪里鱼1年前1 -
 安眠花宝 共回答了20个问题
安眠花宝 共回答了20个问题 |采纳率90%解题思路:就原子来说,质子数=原子序数=核外电子数,质子数+中子数=相对原子质量.首先计算出锆原子的相对原子质量,然后根据氯化物的相对分子质量为233,可以算出锆元素的化合价,最后写出氧化物的化学式.就原子来说,质子数=原子序数=核外电子数,质子数+中子数=相对原子质量.根据题目信息可知,锆原子核内有51个中子,核外有40个电子,所以质子有40个,相对原子质量=51+40=91.
设锆元素的化合价为+X,其氯化物的化学式为:ZrClx,
∵锆的氯化物的相对分子质量为233.
∴91+35.5X=233
得:X=4
∵在锆的氧化物中锆的化合价是+4价,氧元素的化合价是-2价.
∴氧化物的化学式为:ZrO2,故选D.点评:
本题考点: 有关化学式的计算和推断;常见元素与常见原子团的化合价;化合价规律和原则.
考点点评: 掌握相对原子质量和质子、中子之间的关系式,学会根据化合价书写物质的化学式.1年前查看全部
- 3.下列各组物质按单质,氧化物,混合物的顺序排列的是
3.下列各组物质按单质,氧化物,混合物的顺序排列的是
3.下列各组物质按单质、氧化物、混合物的顺序排列的是
A.钢、氧化镁、空气 B.氮气、氧气、牛奶
C.稀有气体、水、果汁 D.金刚石、冰水、矿物质水 xiaoxiaobbmi1年前3
xiaoxiaobbmi1年前3 -
 人似黄花瘦77 共回答了16个问题
人似黄花瘦77 共回答了16个问题 |采纳率93.8%选择D
金刚石化学式是C,是碳的一种,为单质
冰水混合物是H2O,有氧元素存在且前面只有一种元素,是氧化物
矿物质水含有矿物质和水等,是混合物1年前查看全部
- 1.在硫与氧形成的氧化物中,硫与氧的质量比为2:3,则此氧化物中,硫元素的化合价是( )
1.在硫与氧形成的氧化物中,硫与氧的质量比为2:3,则此氧化物中,硫元素的化合价是( )
A.+4 B.+6 C.-2 D.+2
我以经演算到比值了,,
但是不是得到3:1么?
你们怎么算得1: fast37211年前1
fast37211年前1 -
 TIANYONGLE 共回答了11个问题
TIANYONGLE 共回答了11个问题 |采纳率100%B
三氧化硫
你不是写着2:3的1年前查看全部
- 选择“元素”、“单质”、“化合物”、“氧化物”中合适的词填在下列横线上:
选择“元素”、“单质”、“化合物”、“氧化物”中合适的词填在下列横线上:
(1)具有相同质子数的一类原子总称为_______.
(2)氯酸钾是由氧、氯、钾3种不同_____组成的,它是______.
(3)氧气和磷都是由同种______组成的,它们都属于______.两者经化学变化,生成的五氧化二磷属于______物,也属于______物. qdwmail1年前5
qdwmail1年前5 -
 破哦 共回答了7个问题
破哦 共回答了7个问题 |采纳率100%(1)具有相同质子数的一类原子总称为 元素
(2)氯酸钾是由氧、氯、钾3种不同 元素 组成的,它是 化合物
(3)氧气和磷都是由同种 元素 组成的,它们都属于 单质 .两者经化学变化,生成的五氧化二磷属于 化合物 ,也属于 氧化物 .1年前查看全部
- 无机物一般分为氧化物,酸碱盐,请问分类依据是什么?急……
 luoxuxiaojun1年前2
luoxuxiaojun1年前2 -
 迷梦未醒 共回答了18个问题
迷梦未醒 共回答了18个问题 |采纳率83.3%NA2O MGO CAO SO2 NO2 CO2氧化物
HCL HNO3 H2SO4 H2CO3 H2SO3 酸
NAOH LIOH KOH CA(OH)2 BA(OH)2碱
NA2SO3 NANO3 NACL K2CO3 CACO3 MGCO3 盐1年前查看全部
- 引火铁的燃烧方程式在加热条件下用普通铁粉和水蒸气反应,可以得到Fe3O4,该氧化物又可以经过此反应的逆反应,生成颗粒很细
引火铁的燃烧方程式
在加热条件下用普通铁粉和水蒸气反应,可以得到Fe3O4,该氧化物又可以经过此反应的逆反应,生成颗粒很细的铁粉.这种铁粉具有很高的反应活性,在空气中受撞击或受热时会燃烧,所以俗称“引火铁”.
写出引火铁在空气中燃烧的方程式 3326312151年前1
3326312151年前1 -
 vxbzauwg 共回答了23个问题
vxbzauwg 共回答了23个问题 |采纳率95.7%在加热条件下用普通铁粉和水蒸气反应,可以得到Fe3O4
3Fe+4H2O=Fe3O4+4H2
该氧化物又可以经过此反应的逆反应,生成颗粒很细的铁粉
Fe3O4+4H2=3Fe+4H2O
引火铁在空气中燃烧的方程式
3Fe+2O2=Fe3O41年前查看全部
- 铜有两种常见氧化物铜有两种常见的氧化物:CuO和Cu2O.某学习小组取0.98gCu(OH)2固体加热,有铜的氧化物生成
铜有两种常见氧化物
铜有两种常见的氧化物:CuO和Cu2O.某学习小组取0.98gCu(OH)2固体加热,有铜的氧化物生成,其质量随温度变化如图1所示.另外,某同学绘制了三条表示金属氧化物与其所含金属元素的质量的关系曲线,如图2所示.则下列分析正确的是
[ ]


A.图1中产物A、B的化学式分别为Cu2O和CuO
B.图1整个过程中共生成0.26g水
C.图2三条曲线中,表示CuO和其中所含Cu元素质量关系的曲线是C
D.图1中,A到B过程中有0.01mol电子发生了转移
D liulei1237891年前1
liulei1237891年前1 -
 2006开往春天 共回答了16个问题
2006开往春天 共回答了16个问题 |采纳率93.8%0.80和0.72分别对应了CuO和Cu2O的分子量——80和144(一半,因为1摩尔俩铜),A对
加热时H全部以H2O形式离开,起始H共0.2mol,则水有0.1mol即0.18g,B错
CuO中,Cu与CuO质量比为4:5,趋近B线,C错
A至B被还原者仅为Cu,其还原量为0.005mol,每mol转移1mol电子(因为是1价Cu)故转移0.005mol电子,D错
综上选A
希望能帮助你1年前查看全部
- 金属氧化物和非金属氧化物跟水反应,反应物的条件是什么?怎么才能知道反应的氧化物溶不溶于水?
 sheyue1年前3
sheyue1年前3 -
 新妖妖 共回答了12个问题
新妖妖 共回答了12个问题 |采纳率91.7%1.碱性氧化物+水→碱
多数碱性氧化物不能跟水直接化合.判断某种碱性氧化物能否跟水直接化合,一般的方法是看对应碱的溶解性,对应的碱是可溶的或微溶的,则该碱性氧化物能与水直接化合.如:
对应的碱是难溶的,则该碱性氧化物不能跟水直接化合.如CuO、Fe2O3都不能跟水直接化合.
2.酸性氧化物+水→含氧酸
除SiO2外,大多数酸性氧化物能与水直接化合成含氧酸.如:SO21年前查看全部
- 某种氮的气态氧化物的质量是相同状态下同体积氧气质量的1.375倍,求此氧化物的相对分子质量?
 有你youni1年前3
有你youni1年前3 -
 ronaldomhl1 共回答了19个问题
ronaldomhl1 共回答了19个问题 |采纳率94.7%氮的氧化物的相对分子质量为:
1.375*32=44
设氮的氧化物的化学式为N2Ox
14*2+16x=44
x=1
氮的氧化物的化学式为N2O.1年前查看全部
- 若S:O=2:3,氧元素的化学价为-2,求硫的氧化物的化学式与化学价
 相信一见钟情的人1年前5
相信一见钟情的人1年前5 -
 Mr林 共回答了11个问题
Mr林 共回答了11个问题 |采纳率90.9%设SxOy
32x/16y=2/3
所以x/y=1/3
所以是SO3
设硫的化合价为x
x+3*(-2)=0
x=6
所以硫的化合价为+61年前查看全部
- 化学怎么区分纯净物,单质,混合物,氧化物.
化学怎么区分纯净物,单质,混合物,氧化物.
例如河水,冰,高锰酸钾,液氧,氧化铜,没被污染的空气,氯化钾,镁 leixuer1年前4
leixuer1年前4 -
 palla1040 共回答了22个问题
palla1040 共回答了22个问题 |采纳率77.3%纯净物:只含一种物质或一种分子.
混合物:含有两种以上的物质或分子
单质:只含一种元素的纯净物.
氧化物:含两种元素,且一种是氧元素的化合物.
纯净物:冰,高锰酸钾,液氧,氧化铜,氯化钾,镁
混合物:河水,没被污染的空气.
单质:液氧,镁
化合物:高锰酸钾,氧化铜,氯化钾
氧化物:氧化铜
盐:高锰酸钾,氯化钾1年前查看全部
大家在问
- 1我需要关于“挑战”的英语短文用来出黑板报的,字数不要太多哥哥姐姐们自己发挥写一些也可以啊Er...能不能补充下中文,不好
- 2下列词语中,有两个错别字的一组是 A.籍贯筹划家具百废待新 B.翔实瞭望暴燥斐然成章 C.肖像赢弱修葺一愁莫展 D.迁徙
- 3一个"厂"字加一个“人”字读什么
- 4已知两个有理数a,b,如果ab<0,且a+b<0,那么( )
- 5长期记忆的三个原理是什么
- 6资源种类:(1)矿产资源:______、______、铬铁矿、______等储量和产量都居世界前列.(2)植物资源:桃花
- 7一个角的度数越大,它的两条边也就越长
- 8成语玩命猜中有一个人在烫衣服答案是什么成语玩命猜中有一个
- 9如图,角C等于角D等于90度,要证明三角形ABC全等于三角形BAD,还需要一个什么条件?把这些条件写出来(至少四个)并填
- 10英语中打某人某部位用bit+sb+prep.+部位 具体哪些部位用什么介词?
- 11请试着用比喻的修辞手法描写以下事物
- 12一本故事书120页小明第一天读了总页数的4/1多3页,第二天看了总页数的6/1多5页,两天共看了多少页
- 13求幂级数∑(上面∞,下面n)(1-∞)(x∧n)/n+1)的和函数
- 14求中学生作文 美丽的瞬间以“美丽的瞬间”为题,写一篇镜头式的作文,500字以上
- 15说明:若a为整数,则a的立方减a能被6整除.
