乙硫醇与乙酸发生酯化反应的化学方程式
 20050142022-10-04 11:39:542条回答
20050142022-10-04 11:39:542条回答
已提交,审核后显示!提交回复
共2条回复
 3ixw 共回答了17个问题
3ixw 共回答了17个问题 |采纳率70.6%- CH3COOH+HSCH2CH3 = CH3COSCH2CH3+H2O 条件:催化剂 加热、加压 酒化酶
- 1年前
 如盈虚者 共回答了1个问题
如盈虚者 共回答了1个问题 |采纳率- C2H5OH CH3COOH=CH3COOC2H5 H2O
- 1年前
相关推荐
- (2011•丹徒区模拟)在煤气中加入的少量有特殊气味的乙硫醇(C2H5SH)也可以燃烧,其反应的化学方程式为2C2H5S
(2011•丹徒区模拟)在煤气中加入的少量有特殊气味的乙硫醇(C2H5SH)也可以燃烧,其反应的化学方程式为2C2H5SH+9O2
4CO2+2X+6H2O,则x的化学式是( )点燃 .
A.H2SO3
B.SO2
C.SO3
D.H2SO4 arronsilver1年前1
arronsilver1年前1 -
 魏小鹏 共回答了12个问题
魏小鹏 共回答了12个问题 |采纳率100%(1)方法一:根据质量守恒定律:参加反应的元素种类不变;各种原子在化学反应前后,个数不变.根据反应方程式为2C2H5SH+9O2
点燃
.
4CO2+2X+6H2O,故可知:碳原子反应前为4个,反应后也是4个;氢原子反应前12个,反应后12个;硫原子反应前2个,反应后2S应在“2X”中;氧原子反应前18个,反应后6个水分子和4个二氧化碳分子用掉14个;故剩余的4个氧原子在“2X”中,则X为SO2
(2)方法二:此题也可以用代入法,A、B、C、D四项中的化学式分别代入反应方程式,再结合质量守恒定律,可知A、C、D都不对.
故选B.1年前查看全部
- 为了防止煤气逸散使人中毒,常在煤气中加入少量的有特殊气味的乙硫醇(C2H5SH).乙硫醇在煤气燃烧过程中也可充分燃烧,其
为了防止煤气逸散使人中毒,常在煤气中加入少量的有特殊气味的乙硫醇(C2H5SH).乙硫醇在煤气燃烧过程中也可充分燃烧,其化学方程式为:2C2H5SH+9O2
4CO2+2X+6H2O. 则X的化学式为( )点燃 .
A.CO
B.SO2
C.H2SO4
D.SO3 JONNY1年前1
JONNY1年前1 -
 冲浪的鱼 共回答了17个问题
冲浪的鱼 共回答了17个问题 |采纳率94.1%解题思路:在化学反应中遵循质量守恒定律,参加反应的物质的质量等于反应后生成的物质的质量.由2C2H5SH+9O2
点燃
.
4CO2+2X+6H2O可知,每个X中含有1个硫原子和2个氧原子,是二氧化硫,化学式是SO2.
故选:B.点评:
本题考点: 质量守恒定律及其应用.
考点点评: 在化学反应中遵循质量守恒定律,即反应前后元素的种类不变,原子的种类、个数不变,这是书写化学方程式的基础.1年前查看全部
- 乙硫醇在氧气中充分燃烧的化学方程式
 hjk271年前1
hjk271年前1 -
 非常瘦 共回答了20个问题
非常瘦 共回答了20个问题 |采纳率85%2 C2H5SH + 9 O2====6 H2O + 4 CO2 + 2 SO2;条件:点燃1年前查看全部
- 为了能及时发现煤气泄漏,常在煤气中加入少量有特殊气味的乙硫醇(C 2 H 5 SH),乙硫醇燃烧的化学方程式为:2C 2
为了能及时发现煤气泄漏,常在煤气中加入少量有特殊气味的乙硫醇(C 2 H 5 SH),乙硫醇燃烧的化学方程式为:2C 2 H 5 SH+9O 2  4CO 2 +2X+6H 2 O,则X的化学式是 [ ]
4CO 2 +2X+6H 2 O,则X的化学式是 [ ]A.S
B.SO 2
C.SO 3
D.CO MZF玫瑰余香1年前1
MZF玫瑰余香1年前1 -
 潮流华华 共回答了19个问题
潮流华华 共回答了19个问题 |采纳率78.9%B1年前查看全部
- 已知乙硫醇CH3CH2SH结构与乙醇相似,但显弱酸性,
已知乙硫醇CH3CH2SH结构与乙醇相似,但显弱酸性,
能与NaOH溶液反应,生成CH3CH2S-和H2O,且CH3CH2SH在空气中能被氧化成CH3CH2S-SCH2CH3.现有有机物A,可有毛发等天然蛋白质水解得到.其分子式为C3H7NO2S,常温下为无色晶体,能溶于水,不溶于苯.A有两性 ,等量的A消耗H+、OH-的物质的量之比为1:2.A在空气中被氧化成有机物B,B的分子式为C6H12N2O4S2,B能与酸、碱反应,经测定:A中不同环境的氢有5种,而B中只有4种.试回答:
(1)A、B的结构简式:A B
(2)A与强碱反应的离子方程式:
(3)A在空气中被氧化成B的化学方程式: 背黑锅我来1年前1
背黑锅我来1年前1 -
 lc7825 共回答了17个问题
lc7825 共回答了17个问题 |采纳率94.1%http://baike.baidu.com/view/264557.htm
A就是它半胱氨酸,上面有结构式,(自己看吧,百度不让粘);B是把半胱氨酸中两个SH(巯基)对在一起脱去一个H2形成的,画不出来再问我
第二问是A+2NaOH生成A的羧酸盐,且巯基上氢有酸性,被中和,改为SNa
第三问为4A+O2=2B+2H2O1年前查看全部
- 为了防止煤气逸散使人中毒,常在煤气中加入少量的有特殊气味的乙硫醇(C2H5SH).乙硫醇在煤气燃烧过程中也可充分燃烧,其
为了防止煤气逸散使人中毒,常在煤气中加入少量的有特殊气味的乙硫醇(C2H5SH).乙硫醇在煤气燃烧过程中也可充分燃烧,其化学方程式为:2C2H5SH+9O2
4CO2+6H2O+2X.下列说法正确的是( )点燃 .
A.X的化学式为S
B.CO不仅能做燃料还可用于冶炼金属
C.可以在室内放一盆水防止煤气中毒
D.CO、CO2都是污染空气的有毒气体 风之天下1231年前1
风之天下1231年前1 -
 大势 共回答了21个问题
大势 共回答了21个问题 |采纳率90.5%解题思路:A、根据质量守恒定律中原子的种类与数量不便解决.
B、一氧化碳具有还原性与可燃性,所以一氧化碳能够燃烧并能与一些金属氧化物反应.
C、利用一氧化碳的溶解性解决,一氧化碳难溶于书.
D、二氧化碳是无毒物质一氧化碳是剧毒物质.A、根据质量守恒定律中原子的种类与数量可知:方程式的左边有4个碳原子、12个氢原子、2个硫原子和18个氧原子,右边有4个碳原子、12个氢原子、14个氧原子和2个X分子.根据质量守恒定律中元素种类不变、原子个数不变的特点可知:2个X分子含有2个硫原子和4个氧原子,即1个X分子含有1个硫原子和2个氧原子.因此X的化学式为SO2,故此选项错误.
B、一氧化碳具有还原性与可燃性,所以它可以做燃料也可以用来冶炼金属,故此选项正确.
C、一氧化碳难溶于水,所以放盆水不能避免煤气中毒,故此选项错误.
D、二氧化碳是无毒物质,而一氧化碳是有毒物质,故此选项错误.
故选B.点评:
本题考点: 质量守恒定律及其应用;防治空气污染的措施;一氧化碳的毒性.
考点点评: 此题是对质量守恒定律以及一氧化碳与二氧化碳物理性质的考查题,解题的易错点是利用守恒定律求X的化学式,解题时主要是利用原子的种类及数量的不变完成.1年前查看全部
- 燃气安全是家庭生活的头等大事.为了防止燃气泄漏,常在燃气中加入少量有特殊气味的乙硫醇(C2H5SH),一旦泄露即可闻到气
燃气安全是家庭生活的头等大事.为了防止燃气泄漏,常在燃气中加入少量有特殊气味的乙硫醇(C2H5SH),一旦泄露即可闻到气味,从微观的角度分析原因是___________.乙硫醇充分燃烧时产生二氧化碳、二氧化硫和水,燃烧的化学方程式为________________ .
 传说9131年前2
传说9131年前2 -
 terryjojo 共回答了19个问题
terryjojo 共回答了19个问题 |采纳率100%燃气安全是家庭生活的头等大事.为了防止燃气泄漏,常在燃气中加入少量有特殊气味的乙硫醇(C2H5SH),一旦泄露即可闻到气味,从微观的角度分析原因是___分子是在不断运动的________.
乙硫醇充分燃烧时产生二氧化碳、二氧化硫和水,燃烧的化学方程式为_2C2H5SH+9O2=4CO2+2SO2+6H2O__ .1年前查看全部
- (2006•平凉)煤气泄漏会发生危险.为了及时发现煤气泄漏,常在煤气中加有少量特殊气味的乙硫醇,乙硫醇燃烧的化学方程式为
(2006•平凉)煤气泄漏会发生危险.为了及时发现煤气泄漏,常在煤气中加有少量特殊气味的乙硫醇,乙硫醇燃烧的化学方程式为:2X+9O2═4CO2+2SO2+6H2O,则乙硫醇(X)的化学式为( )
A.C2H3SH
B.CH3SH
C.C2H5SH
D.C2H5OH xl_charles1年前1
xl_charles1年前1 -
 haixiao1257 共回答了17个问题
haixiao1257 共回答了17个问题 |采纳率94.1%解题思路:由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断反应物X的化学式.根据反应的化学方程式2X+9O2═4CO2+2SO2+6H2O,反应物中氧原子个数分别为18,反应后的生成物中碳、氧、硫、氢原子个数分别为4、18、2、12,根据反应前后原子种类、数目不变,则2X中含有4个碳原子、12个氢原子、2个硫原子,则每个X分子由2个碳原子、6个氢原子和1个硫原子构成,则物质X的化学式为C2H5SH.
故选:C.点评:
本题考点: 质量守恒定律及其应用.
考点点评: 本题难度不大,利用化学反应前后元素守恒、原子守恒来确定物质的化学式是正确解题的关键.1年前查看全部
- (2013•宝坻区二模)(1)乙硫醇有特殊气味,加入到煤气中可提示煤气是否泄漏.乙硫醇(用X表示),燃烧时发生的反应为
(2013•宝坻区二模)(1)乙硫醇有特殊气味,加入到煤气中可提示煤气是否泄漏.乙硫醇(用X表示),燃烧时发生的反应为
2X+9O2
4CO2+2SO2+6H2O,则X是______.点燃 .
(2)一定条件下,下列物质在密闭容器内充分反应,测得反应前后各物质的质量如下:
则反应后B的质量为______g;该反应中B和D两种物质变化的质量比为______.物质 A B C D 反应前质量/g 3.4g 6.6 0 2.7 反应后质量/g 1.7 待测 7.9 0.9  我爱安佳1年前1
我爱安佳1年前1 -
 qfj0511 共回答了18个问题
qfj0511 共回答了18个问题 |采纳率88.9%解题思路:(1)根据质量守恒定律,化学反应前后各原子的种类和数目不变,反应前各原子的数目之和等于反应后各原子的数目之和,据此可推断X的化学式;
(2)根据表中的数据和质量守恒定律进行分析.反应中,反应物质量会减少,生成物质量会增加,从而判断生成物与反应物,再利用质量关系进行求解.(1)反应后生成物4CO2、2SO2、6H2O中,共有4个碳原子、2个硫原子、18个氧原子、12个氢原子,反应物中除2X外有18个氧原子,根据质量守恒定律,反应前物质中原子的种类和数目不变,2X中应含有4个碳原子、2个硫原子、1...
点评:
本题考点: 质量守恒定律及其应用.
考点点评: 此题是有关质量守恒定律的考查题,解题的关键是利用质量守恒定律对相关量的分析与判断,难度不大.1年前查看全部
- 为了及时知道煤气泄漏,长在天然气中加入少量有特殊气味的乙硫醇作指示气体,乙硫醇可以燃烧,发生的反应为2X+9O2=点燃=
为了及时知道煤气泄漏,长在天然气中加入少量有特殊气味的乙硫醇作指示气体,乙硫醇可以燃烧,发生的反应为2X+9O2=点燃=4CO2+2SO2+6H2O x是
 yylh351701年前1
yylh351701年前1 -
 小aa 共回答了15个问题
小aa 共回答了15个问题 |采纳率93.3%H6C2S1年前查看全部
- 天然气为无色无味的气体,为了能及时发现厨房内天然气是否泄漏,常在天然气中加入少量有特殊气味的乙硫醇(C2H5SH).在燃
天然气为无色无味的气体,为了能及时发现厨房内天然气是否泄漏,常在天然气中加入少量有特殊气味的乙硫醇(C2H5SH).在燃烧过程中乙硫醇可以充分燃烧,其化学方程式为2C2H5SH+9O2═4CO2+2X+6H2O下列说法正确的是( )
A.天然气是化合物
B.X是由硫元素组成的单质
C.X的相对分子质量为64
D.反应中的O2与生成的X的质量比为9:2 雅若之女1年前1
雅若之女1年前1 -
 单饨不是罪 共回答了19个问题
单饨不是罪 共回答了19个问题 |采纳率94.7%解题思路:化学反应前后,元素的种类不变,原子的种类、总个数不变.由2C2H5SH+9O2═4CO2+2X+6H2O可知,
反应前碳原子是4个,反应后是4个;
反应前氢原子是12个,反应后是12个;
反应前硫原子是2个,反应后应该是2个,包含在2X中;
反应前氧原子是18个,反应后应该是18个,其中4个包含在2X中;
由分析可知,每个X中含有1个硫原子和2个氧原子,是二氧化硫,反应的化学方程式为:2C2H5SH+9O2═4CO2+2SO2+6H2O;
A、天然气的主要成分是甲烷,属于混合物,该选项说法不正确;
B、X是由硫元素和氧元素组成的化合物,该选项说法不正确;
C、X的相对分子质量为:32+16×2=64,该选项说法正确;
D、反应中的O2与生成的X的质量比为:32×9:64×2=9:4,该选项说法不正确.
故选:C.点评:
本题考点: 质量守恒定律及其应用;单质和化合物的判别;相对分子质量的概念及其计算.
考点点评: 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.1年前查看全部
- 在120℃,101000Pa时,将乙醇和乙硫醇的混合气体1L和5L氧气混合,充分燃烧后,恢复到原状况,气体密度减小到原气
在120℃,101000Pa时,将乙醇和乙硫醇的混合气体1L和5L氧气混合,充分燃烧后,恢复到原状况,气体密度减小到原气体的10/11,则乙醇和乙硫醇蒸汽的体积比为多少?1:4)写出过程,
 nona5201年前3
nona5201年前3 -
 与激扬同行 共回答了18个问题
与激扬同行 共回答了18个问题 |采纳率77.8%2C2H6S+9O2=4CO2+2SO2+6H2O……①
C2H6O+3O2=2CO2+3H2O……②
反应①中每2体积乙硫醇,体积增大1体积;②中每1体积乙醇,增大1体积
密度减小到原来的10/11,m/V =m/6 *10/11,V=6.6L
设乙醇有xL,乙硫醇有yL
x+y=1(根据总体积)
6+x+y/2=6.6
解得x=0.2 ,y=0.8
所以两者体积比为1:41年前查看全部
- 为及时发现煤气泄漏,常在煤气中加入少量的有特殊气味的乙硫醇(C2H5SH),乙硫醇在煤气燃烧过程中也发生燃烧,其反应如下
为及时发现煤气泄漏,常在煤气中加入少量的有特殊气味的乙硫醇(C2H5SH),乙硫醇在煤气燃烧过程中也发生燃烧,其反应如下:2C2H5SH+9O2
4CO2+6H2O+2X,则生成物中X的化学式为( )点燃 .
A.H2SO4
B.SO3
C.SO2
D.CO 虫虫闯yy1年前1
虫虫闯yy1年前1 -
 我是ee女人 共回答了16个问题
我是ee女人 共回答了16个问题 |采纳率100%解题思路:根据质量守恒定律中元素种类不变、原子个数不变的特点,可以确定X的化学式.由题干中的化学方程式可知:方程式的左边有4个碳原子、12个氢原子、2个硫原子和18个氧原子,右边有4个碳原子、12个氢原子、14个氧原子和2个X分子.根据质量守恒定律中元素种类不变、原子个数不变的特点可知:2个X分子含有2个硫原子和4个氧原子,即1个X分子含有1个硫原子和2个氧原子,因此X的化学式为SO2.
故选:C.点评:
本题考点: 质量守恒定律及其应用.
考点点评: 本题主要考查根据质量守恒定律和化学方程式推断物质的化学式.难度较小.1年前查看全部
- 煤气是无色无味的气体,为了使人警觉,通常在其中加入少量有特殊臭气味的乙硫醇,这是为什么?
 祢祢祢1年前1
祢祢祢1年前1 -
 leon0576 共回答了21个问题
leon0576 共回答了21个问题 |采纳率85.7%一旦煤气泄漏,让人即时闻到气味,采取措施,避免中毒。1年前查看全部
- 为了能及时发现煤气泄漏,常在煤气中加入少量有特殊气味的乙硫醇(C2H5SH),乙硫醇燃烧的化学方程式为:2C2H5SH+
为了能及时发现煤气泄漏,常在煤气中加入少量有特殊气味的乙硫醇(C2H5SH),乙硫醇燃烧的化学方程式为:2C2H5SH+9O2
4X+2SO2+6H2O,则X的化学式为( )点燃 .
A.S
B.CO2
C.SO2
D.CO 八月花香1年前1
八月花香1年前1 -
 cyg25gz 共回答了19个问题
cyg25gz 共回答了19个问题 |采纳率94.7%解题思路:在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变,所以反应前后物质的质量总和相等.乙硫醇燃烧的化学方程式:2C2H5SH+9O2
点燃
.
4X+2SO2+6H2O
反应前C、H、S、O元素的原子个数分别为4、12、2、18;
反应后2SO2和6H2O中H、S、O元素的原子个数分别为12、2、10;
对比反应前后,可发现反应后缺少了:C原子4个、O原子8个,所以在4X中含有这些原子,则每个X中含1个C原子和2个O原子.
故选B点评:
本题考点: 质量守恒定律及其应用;有关化学式的计算和推断.
考点点评: 化学反应的过程,就是参加反应的各物质(反应物)的原子,重新组合而生成其他物质的过程.1年前查看全部
- 为了防止煤气逸散使人中毒,常在煤气中加入少量的有特殊气味的乙硫醇(C2H5SH).乙硫醇在煤气燃烧过程中也可充分燃烧,其
为了防止煤气逸散使人中毒,常在煤气中加入少量的有特殊气味的乙硫醇(C2H5SH).乙硫醇在煤气燃烧过程中也可充分燃烧,其化学方程式为:2C2H5SH+9O2
4CO2+6H2O+2X.下列说法正确的是( )点燃 .
A. X的化学式为S
B. CO不仅能做燃料还可用于冶炼金属
C. 可以在室内放一盆水防止煤气中毒
D. CO、CO2都是污染空气的有毒气体 anyclub31年前1
anyclub31年前1 -
 testuser123 共回答了15个问题
testuser123 共回答了15个问题 |采纳率86.7%解题思路:A、根据质量守恒定律中原子的种类与数量不便解决.
B、一氧化碳具有还原性与可燃性,所以一氧化碳能够燃烧并能与一些金属氧化物反应.
C、利用一氧化碳的溶解性解决,一氧化碳难溶于书.
D、二氧化碳是无毒物质一氧化碳是剧毒物质.A、根据质量守恒定律中原子的种类与数量可知:方程式的左边有4个碳原子、12个氢原子、2个硫原子和18个氧原子,右边有4个碳原子、12个氢原子、14个氧原子和2个X分子.根据质量守恒定律中元素种类不变、原子个数不变的...
点评:
本题考点: 质量守恒定律及其应用;防治空气污染的措施;一氧化碳的毒性.
考点点评: 此题是对质量守恒定律以及一氧化碳与二氧化碳物理性质的考查题,解题的易错点是利用守恒定律求X的化学式,解题时主要是利用原子的种类及数量的不变完成.1年前查看全部
- (2014•奉贤区一模)2mol乙硫醇(C2H5SH)与9molO2完全燃烧生成4molCO2、6molH2O及2mol
(2014•奉贤区一模)2mol乙硫醇(C2H5SH)与9molO2完全燃烧生成4molCO2、6molH2O及2molX,则X的化学式为( )
A.SO2
B.SO3
C.H2S
D.H2SO4 NYSS1年前1
NYSS1年前1 -
 五月双子 共回答了24个问题
五月双子 共回答了24个问题 |采纳率95.8%解题思路:由质量守恒定律:反应前后,原子种类、数目均不变,据此根据题意推断生成物X的化学式.2mol乙硫醇(C2H5SH)与9molO2中含碳、氢、硫、氧四种原子的物质的量为:(2mol×2)、(2mol×6)、(2mol×1)、(9mol×2),即4mol、12mol、2mol、18mol;生成物中4molCO2、6molH2O中含碳、氢、氧三种原子的物质的量为:(4mol×1)、(6mol×2)、(4mol×2+6mol×1),即4mol、12mol、14mol;则根据反应前后原子种类、数目不变,则2molX中含有2mol个硫原子和4mol氧原子,则1molX分子由1mol个硫原子和2mol氧原子构成,则物质X的化学式为SO2.
故选A.点评:
本题考点: 有关化学式的计算和推断.
考点点评: 本题难度不大,利用化学反应前后原子守恒来确定物质的化学式是正确解题的关键.1年前查看全部
- 煤气中加人有特殊气味的乙硫醇可提示煤气是否泄漏.乙硫醇(用X表示)燃烧时发生反应的化学方程式为:2X+9O2
煤气中加人有特殊气味的乙硫醇可提示煤气是否泄漏.乙硫醇(用X表示)燃烧时发生反应的化学方程式为:2X+9O2
4CO2+2SO2+6H2O,则X的化学式为( )点燃 .
A. C4H12S2
B. C2H6S
C. C2H6O2
D. C2H6S2 kimi13141年前5
kimi13141年前5 -
 bj_yc 共回答了15个问题
bj_yc 共回答了15个问题 |采纳率93.3%解题思路:根据质量守恒定律,化学反应前后各原子的种类和数目不变,反应前各原子的数目之和等于反应后各原子的数目之和,据此可推断X的化学式.反应后生成物4CO2、2SO2、6H2O中,共有4个碳原子、2个硫原子、18个氧原子、12个氢原子,反应物中除2X外有18个氧原子,根据质量守恒定律,反应前物质中原子的种类和数目不变,2X中应含有4个碳原子、2个硫原子、12个氢原子,因此一个X分子的组成为2个碳原子、1个硫原子、6个氢原子.
故选B.点评:
本题考点: 质量守恒定律及其应用.
考点点评: 本题考查根据化学方程式推断物质的化学式.此类试题的解题依据是质量守恒定律,只要能深刻理解质量守恒定律的含义,不难解决.1年前查看全部
- 为防止煤气逸散使人中毒,常在煤气中加入少量的有特殊激性气味的乙硫醇(C 2 H 5 SH).乙硫醇在煤气燃烧过程中也可以
为防止煤气逸散使人中毒,常在煤气中加入少量的有特殊激性气味的乙硫醇(C 2 H 5 SH).乙硫醇在煤气燃烧过程中也可以充分燃烧,其化学方程式为:2C 2 H 5 SH+9O 2
4CO 2 +2Ⅹ+6H 2 O,则X的化学式为( )点燃 . A.H 2 SO 4 B.SO 3 C.SO 2 D.CO  p20201年前1
p20201年前1 -
 sophiaooo 共回答了19个问题
sophiaooo 共回答了19个问题 |采纳率94.7%由题干中的化学方程式可知:
方程式的左边有4个碳原子、12个氢原子、2个硫原子和18个氧原子,右边有4个碳原子、12个氢原子、14个氧原子和2个X分子.根据质量守恒定律中元素种类不变、原子个数不变的特点可知:2个X分子含有2个硫原子和4个氧原子,即1个X分子含有1个硫原子和2个氧原子.因此X的化学式为SO 2 .
故选C.1年前查看全部
- 家庭中常用液化石油气作燃料,为防止其泄漏造成危害,常在其中加入少量具有特殊臭味的乙硫醇(化学式为C2H5SH),可以提醒
家庭中常用液化石油气作燃料,为防止其泄漏造成危害,常在其中加入少量具有特殊臭味的乙硫醇(化学式为C2H5SH),可以提醒人们预防泄漏.乙硫醇也可充分燃烧,其反应方程式为2C2H5SH+9O2
4CO2+2X+6H2O.则X的化学式为( )点燃 .
A.SO2
B.SO3
C.CO
D.H2S kelvin_sea1年前1
kelvin_sea1年前1 -
 心似飘渺 共回答了20个问题
心似飘渺 共回答了20个问题 |采纳率100%解题思路:根据质量守恒定律,化学反应前后各原子的种类、数目不变,结合反应方程式分析X的化学式.根据质量守恒定律,化学反应前后原子的种类不变、原子的数目不变,结合化学方程式可知:反应前出现了18个氧原子、2个硫原子、12个氢原子、4个碳原子,而反应后除2X外出现了14个氧原子、12个氢原子、4个碳原子,比较反应前后原子的种类和个数可以知道,在2X中含有2个硫原子、4个氧原子,所以X中含有2个氧原子和1个硫原子,故X化学式为SO2.
故选A.点评:
本题考点: 质量守恒定律及其应用.
考点点评: 本题主要考查有关化学式的计算和推断的方法,掌握质量守恒定律的内容和实质涵义及其应用.1年前查看全部
- 天然气是无色无味的气体,但在使用时常在天然气中加少量又特殊气味的乙硫醇,加入乙硫醇的作用是
 zhh1256901年前1
zhh1256901年前1 -
 yakohama333 共回答了15个问题
yakohama333 共回答了15个问题 |采纳率73.3%使天然气泄漏的时候能够第一时间被人发现,从而尽快做出反应1年前查看全部
- (2006•菏泽)为了能及时以现煤气泄漏,常在煤气中加入少量有特殊气味的乙硫醇(C2H5SH),乙硫醇燃烧 的
(2006•菏泽)为了能及时以现煤气泄漏,常在煤气中加入少量有特殊气味的乙硫醇(C2H5SH),乙硫醇燃烧 的化学方程式为2C2H5SH+9O2
xCO2+2Y+6H2O,已知Y由两种元素组成,则x=______,Y的化学式为______.点燃 . kongq2i1年前1
kongq2i1年前1 -
 长戟兵 共回答了16个问题
长戟兵 共回答了16个问题 |采纳率87.5%解题思路:根据乙硫醇燃烧的化学方程式为2C2H5SH+9O2
xCO2+2Y+6H2O,利用质量守恒定律来分析解答.点燃 .由乙硫醇燃烧的化学方程式为2C2H5SH+9O2
点燃
.
xCO2+2Y+6H2O,
根据质量守恒定律可知,原子在反应前后的个数相等,
已知Y由两种元素组成,则Y中一定含有S元素,且S原子总数为2,
根据C原子守恒,反应前共4个C原子,则二氧化碳的化学计量数为4,即x=4;
根据O原子守恒,反应前共18个O原子,反应后现有O原子为4×2+6=14,
则Y中有O元素,含O原子为18-14=4,
又Y的化学计量数为2,则Y的化学式为SO2.
故答案为:4;SO2.点评:
本题考点: 有关化学式的计算和推断;质量守恒定律及其应用;化学方程式的配平.
考点点评: 本题考查学生利用化学方程式来确定化学计量数和物质的化学式,学生应能利用原子守恒的方法来确定化学计量数,利用元素守恒和原子守恒确定某物质的化学式.1年前查看全部
- 化学就在我们身边,它与生产、生活和科技密切相关.为了及时发现煤气泄漏,常在煤气中加入少量有特殊气味的乙硫醇(化学式为C2
化学就在我们身边,它与生产、生活和科技密切相关.为了及时发现煤气泄漏,常在煤气中加入少量有特殊气味的乙硫醇(化学式为C2H5SH)作指示气体,乙硫醇可以燃烧,该反应的化学方程式为:2C2H5SH+9O2
4CO2+2X+6H2O.请推断X的化学式为______.点燃 . pennyluang1年前1
pennyluang1年前1 -
 风南 共回答了21个问题
风南 共回答了21个问题 |采纳率81%解题思路:根据质量守恒定律中元素种类不变、原子个数不变的特点,可以确定X的化学式.由题干中的化学方程式2C2H5SH+9O2
点燃
.
4CO2+2X+6H2O,可知:化学方程式的左边有4个碳原子、12个氢原子、2个硫原子和18个氧原子,右边有4个碳原子、12个氢原子、14个氧原子和2个X分子.根据质量守恒定律中元素种类不变、原子个数不变的特点可知:2X中含有2个硫原子和4个氧原子,所以在X中含有1个硫原子和2个氧原子,即X的化学式为:SO2.
故答案为:SO2点评:
本题考点: 质量守恒定律及其应用.
考点点评: 熟练掌握质量守恒定律的实质并会应用,反应的化学方程式中各物质化学式前的化学计量数表示参加此反应的该物质的分子个数,在统计反应前后原子个数时,要正确使用化学计量数.1年前查看全部
- 为了能及时发现煤气泄漏,常在煤气中加入少量有特殊气味的乙硫醇(C2H5SH).乙硫醇在煤气燃烧过程中可以充分燃烧,其化学
为了能及时发现煤气泄漏,常在煤气中加入少量有特殊气味的乙硫醇(C2H5SH).乙硫醇在煤气燃烧过程中可以充分燃烧,其化学方程式为2C2H5SH+9O2
4CO2+2X+6H2O由此判断,下列说法正确的是( )点燃 .
A.煤气是化合物
B.X是由硫元素组成的
C.X的相对分子质量为64
D.反应中的O2与生成的X的质量比为9:2 avv11年前1
avv11年前1 -
 deri12 共回答了16个问题
deri12 共回答了16个问题 |采纳率93.8%解题思路:根据题干提供的信息进行分析,煤气的主要成分是一氧化碳,属于混合物;根据质量守恒定律,化学反应前后原子的种类和个数不会改变即可判断X的化学式和计算反应中各物质的质量比.A、煤气的主要成分是一氧化碳,属于混合物,故A错误;
B、由题干中的化学方程式可知:方程式的左边有4个碳原子、12个氢原子、2个硫原子和18个氧原子,右边有4个碳原子、12个氢原子、14个氧原子和2个X分子.根据质量守恒定律中元素种类不变、原子个数不变的特点可知:2个X分子含有2个硫原子和4个氧原子,即1个X分子含有1个硫原子和2个氧原子,因此X的化学式为SO2,因此X是由硫、氧两种元素组成的,故B错误;
C、由B分析可知,X是二氧化硫,其相对分子质量为64,故C正确;
D、反应中的O2与生成的X(二氧化硫)的质量比为9×32:64×2=9:4,故D错误.
故选:C.点评:
本题考点: 质量守恒定律及其应用;单质和化合物的判别;相对分子质量的概念及其计算.
考点点评: 本题考查了常见物质的分类以及质量守恒定律的应用,完成此题,可以依据题干提供的信息结合已有的知识进行.1年前查看全部
- 家庭中常用液化石油气作燃料,为防止其泄漏造成危害,常在其中加入少量具有特殊臭味的乙硫醇(化学式为C 2 H 5 SH),
家庭中常用液化石油气作燃料,为防止其泄漏造成危害,常在其中加入少量具有特殊臭味的乙硫醇(化学式为C 2 H 5 SH),可以提醒人们预防泄漏.乙硫醇也可充分燃烧,其反应方程式为2C 2 H 5 SH+9O 2
4CO 2 +2X+6H 2 O.则X的化学式为( )点燃 . A.SO 2 B.SO 3 C.CO D.H 2 S  lxorb1年前1
lxorb1年前1 -
 八乐蒙干 共回答了16个问题
八乐蒙干 共回答了16个问题 |采纳率87.5%根据质量守恒定律,化学反应前后原子的种类不变、原子的数目不变,结合化学方程式可知:反应前出现了18个氧原子、2个硫原子、12个氢原子、4个碳原子,而反应后除2X外出现了14个氧原子、12个氢原子、4个碳原子,比较反应前后原子的种类和个数可以知道,在2X中含有2个硫原子、4个氧原子,所以X中含有2个氧原子和1个硫原子,故X化学式为SO 2 .
故选A.1年前查看全部
- (2007•广元)为防止煤气逸散使人中毒,常在煤气中加入少量的有特殊激性气味的乙硫醇(C2H5SH).乙硫醇在煤气燃烧过
(2007•广元)为防止煤气逸散使人中毒,常在煤气中加入少量的有特殊激性气味的乙硫醇(C2H5SH).乙硫醇在煤气燃烧过程中也可以充分燃烧,其化学方程式为:2C2H5SH+9O2
4CO2+2Ⅹ+6H2O,则X的化学式为( )点燃 .
A.H2SO4
B.SO3
C.SO2
D.CO 枫之花1年前1
枫之花1年前1 -
 78bc 共回答了16个问题
78bc 共回答了16个问题 |采纳率93.8%解题思路:根据质量守恒定律中元素种类不变、原子个数不变的特点,可以确定X的化学式.由题干中的化学方程式可知:
方程式的左边有4个碳原子、12个氢原子、2个硫原子和18个氧原子,右边有4个碳原子、12个氢原子、14个氧原子和2个X分子.根据质量守恒定律中元素种类不变、原子个数不变的特点可知:2个X分子含有2个硫原子和4个氧原子,即1个X分子含有1个硫原子和2个氧原子.因此X的化学式为SO2.
故选:C.点评:
本题考点: 有关化学式的计算和推断;质量守恒定律及其应用.
考点点评: 本题主要考查根据质量守恒定律和化学方程式推断物质的化学式.难度较小.1年前查看全部
- (2005•长春)为及时发现煤气(主要成分是CO)泄漏,常加入少量有特殊气味的乙硫醇(化学式为C2H5SH).乙硫醇完全
(2005•长春)为及时发现煤气(主要成分是CO)泄漏,常加入少量有特殊气味的乙硫醇(化学式为C2H5SH).乙硫醇完全燃烧的化学方程式为
2C2H5SH+9O2
4CO2+6H2O+2X.下列有关说法中,正确的是( )点燃 .
A.X的化学式为S
B.可以在室内放一盆水防止煤气中毒
C.CO、CO2都是污染空气的有毒气体
D.CO不仅能做燃料还可用于冶炼金属 hanschen1年前1
hanschen1年前1 -
 最近特忙 共回答了12个问题
最近特忙 共回答了12个问题 |采纳率91.7%解题思路:A、根据质量守恒定律的实质结合化学方程式可以判断出X的化学式;
B、一氧化碳是难溶于水的物质,可以据此答题;
C、二氧化碳无毒,一氧化碳有毒,可以据此判断该选项;
D、一氧化碳具有可燃性和还原性,可以据此解答该题.A、根据反应的化学方程式,反应前共有4个碳原子,12个氢原子,18个氧原子,2个硫原子,反应后已有4个碳原子,12个氢原子,14个氧原子,故2X中含有2个硫原子和4个氧原子,X的化学式为SO2,故A错误;
B、一氧化碳是难溶于水的有毒气体,所以放入一盆水并不能防止煤气中毒,故B错误;
C、二氧化碳没有毒,故C错误;
D、物质的性质决定物质的用途,一氧化碳具有可燃性所以可以作为燃料,一氧化碳具有还原性,所以可以用于冶炼金属,故D正确.
故选D.点评:
本题考点: 质量守恒定律及其应用;空气的污染及其危害;一氧化碳的化学性质;常见中毒途径及预防方法.
考点点评: 本题考查了常见物质的性质以及质量守恒定律的应用,完成此题,可以依据题干提供的信息结合已有的知识进行.1年前查看全部
- (2009•贺州)煤气中添加少量有特殊臭味的乙硫醇(C2H5SH),可以提醒人们预防煤气泄露.乙硫醇在煤气燃烧过程中也可
(2009•贺州)煤气中添加少量有特殊臭味的乙硫醇(C2H5SH),可以提醒人们预防煤气泄露.乙硫醇在煤气燃烧过程中也可充分燃烧,其反应方程式为2C2H5SH+9O2
4CO2+2X+6H2O,则X的化学式为( )点燃 .
A.SO3
B.SO2
C.CO
D.H2SO4 penjiayo1年前1
penjiayo1年前1 -
 leoistiger 共回答了15个问题
leoistiger 共回答了15个问题 |采纳率100%解题思路:理解质量守恒定律的实质:原子概念→化学变化的微观实质→化学变化前后物质总质量守恒.此线索的具体内容是:原子是化学变化中的最小粒子,因此,化学变化的过程,实质上是反应物的原子重新构成新物质的分子或直接构成新物质的过程,在这一过程中,原子的种类、数目、质量都没有发生变化,所以参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和.(1)方法一:根据质量守恒定律:参加反应的元素种类不变;各种原子在化学反应前后,个数不变.根据反应方程式为2C2H5SH+9O2
点燃
.
4CO2+2X+6H2O,故可知:碳原子反应前为4个,反应后也是4个;氢原子反应前12个,反应后12个;硫原子反应前2个,反应后2S应在“2X”中;氧原子反应前18个,反应后6个水分子和4个二氧化碳分子用掉14个;故剩余的4个氧原子在“2X”中,则X为SO2
(2)方法二:此题也可以用代入法,A、B、C、D四项中的化学式分别代入反应方程式,再结合质量守恒定律,可知A、C、D都不对.
故选B.点评:
本题考点: 有关化学式的计算和推断;质量守恒定律及其应用.
考点点评: 本题主要考查有关化学式的计算和推断的方法,掌握质量守恒定律的内容和实质涵义及其应用.1年前查看全部
- 为什么乙硫醇的化学方程式不是C2H6S?
 nevergiveup3651年前4
nevergiveup3651年前4 -
 vivw 共回答了21个问题
vivw 共回答了21个问题 |采纳率81%是C2H5SH
相当于乙醇中的氧被硫取代了1年前查看全部
- 已知酸性H2O<H2S,试判断乙醇与乙硫醇分别与金属钠反应的剧烈程度
已知酸性H2O<H2S,试判断乙醇与乙硫醇分别与金属钠反应的剧烈程度
CH3CH2OH__CH3CH2SH(填<、>或=)
要说明原因啊~ 雕龙鑫1年前2
雕龙鑫1年前2 -
 狂风牛牛 共回答了15个问题
狂风牛牛 共回答了15个问题 |采纳率86.7%H2O比H2S的酸性弱.说明,H-S断键释放的能量大于H-O断裂的能量.
所以 <1年前查看全部
- (2007•呼和浩特)为了能及时发现煤气泄漏,常在煤气中加入少量有特殊气味的乙硫醇(C2H5SH),乙硫醇燃烧的化学方程
(2007•呼和浩特)为了能及时发现煤气泄漏,常在煤气中加入少量有特殊气味的乙硫醇(C2H5SH),乙硫醇燃烧的化学方程式为2C2H5SH+9O2═4CO2+2x+6H2O,则X的化学式是( )
A.S
B.H2S
C.SO3
D.SO2 1232005ttl1年前1
1232005ttl1年前1 -
 靓晶 共回答了19个问题
靓晶 共回答了19个问题 |采纳率100%解题思路:化学反应前后,元素的种类不变,原子的种类、总个数不变.由2C2H5SH+9O2═4CO2+2x+6H2O可知,
反应前碳原子是4个,反应后是4个;
反应前氢原子是12个,反应后是12个;
反应前硫原子是2个,反应后应该是2个,包含在2x中;
反应前氧原子是18个,反应后应该是18个,其中的4个包含2x中;
由分析可知,每个x中含有1个硫原子和2个氧原子,是二氧化硫,化学式是SO2.
故选:D.点评:
本题考点: 质量守恒定律及其应用.
考点点评: 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.1年前查看全部
- (2013•镇江二模)乙硫醇俗称煤气的“报警器”,煤气泄漏时它的臭味可使人们警觉,马上采取措施,防止发生爆炸、中毒等事故
(2013•镇江二模)乙硫醇俗称煤气的“报警器”,煤气泄漏时它的臭味可使人们警觉,马上采取措施,防止发生爆炸、中毒等事故.某校兴趣小组对乙硫醇作了探究.
[提出问题]乙硫醇能燃烧吗?假如能,那完全燃烧的产物是什么?
[查阅资料]
(1)乙硫醇(C2H6S),无色液体,有强烈的蒜气味,具有可燃性.
(2)二氧化硫和二氧化碳一样能使澄清石灰水变浑浊.
(3)三氧化硫(SO3)在常温(250C)下是液态,能与水反应生成硫酸.
[提出猜想]甲同学认为:乙硫醇完全燃烧的产物是水、二氧化碳和二氧化硫,你认为他猜想的依据是:______;
[进行实验]甲同学根据自己的猜想设计、进行了下列实验: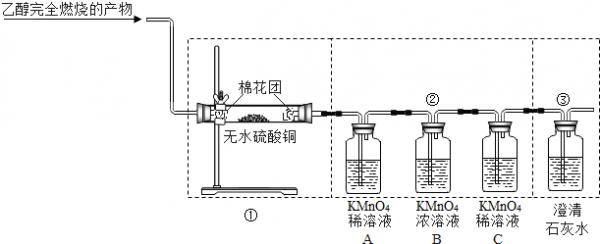
[现象与结论]
①装置中观察到______,证明有H2O;
②组合A装置中观察到______,证明有SO2.
③装置中澄清石灰水变浑浊,同时观察到______,证明有CO2.
[实验反思]
(1)如果装置中①、②、③三部分仪器的连接顺序改为②、①、③,则不能检出的物质是______.
(2)写出乙硫醇完全燃烧的化学方程式为:2C2H5SH+9O2
4CO2+6H2O+2SO2点燃 .2C2H5SH+9O2.
4CO2+6H2O+2SO2点燃 . 没事说2句1年前1
没事说2句1年前1 -
 恐龙大笨蛋 共回答了23个问题
恐龙大笨蛋 共回答了23个问题 |采纳率78.3%解题思路:[提出猜想]
质量守恒定律是判断反应物、生成物的依据之一;
[现象与结论]
无水硫酸铜遇水变蓝色;
二氧化硫能使高锰酸钾溶液褪色;
[实验反思]
气体从溶液中逸出时会带上水蒸气;
根据反应物、生成物及其质量守恒定律可以书写化学方程式.[提出猜想]
甲同学认为:乙硫醇完全燃烧的产物是水、二氧化碳和二氧化硫,他猜想的依据是质量守恒定律.
故填:质量守恒定律.
[现象与结论]
①装置中观察到白色固体变蓝色,证明有H2O;
故填:白色固体变蓝色.
②组合A装置中观察到高锰酸钾溶液褪色,证明有SO2.
故填:高锰酸钾溶液褪色.
③装置中澄清石灰水变浑浊,同时观察到②组合C装置中高锰酸钾溶液不褪色,证明有CO2,因为②组合C装置中高锰酸钾溶液不褪色,说明进入石灰水中的气体中没有二氧化硫.
故填:②组合C装置中高锰酸钾溶液不褪色.点评:
本题考点: 实验探究物质的组成成分以及含量;常见气体的检验与除杂方法;书写化学方程式、文字表达式、电离方程式.
考点点评: 在化学反应中遵循质量守恒定律,即反应前后元素的种类不变,原子的种类、个数不变.1年前查看全部
- (2007•青海)为了能及时发现煤气泄漏,常在煤气中加少量有特殊气味的乙硫醇(C2H5SH).乙硫醇在煤气燃烧过程中可以
(2007•青海)为了能及时发现煤气泄漏,常在煤气中加少量有特殊气味的乙硫醇(C2H5SH).乙硫醇在煤气燃烧过程中可以充分燃烧,其化学方程式为2C2H5SH+9O2
4CO2+2X+6H2O则X的化学式为( )点燃 .
A.S
B.SO3
C.SO2
D.CO hackku1年前1
hackku1年前1 -
 房西故人 共回答了24个问题
房西故人 共回答了24个问题 |采纳率91.7%解题思路:化学反应前后,元素的种类不变,原子的种类、总个数不变.由2C2H5SH+9O2
点燃
.
4CO2+2X+6H2O可知,
反应前碳原子是4个,反应后是4个;
反应前氢原子是12个,反应后是12个;
反应前硫原子2个,反应后应该是2个,包含在2X中;
反应前氧原子是18个,反应后应该是18个,其中4个包含在2X中;
由分析可知,每个X中含有1个硫原子和2个氧原子,是二氧化硫,二氧化硫的化学式是SO2.
故选:C.点评:
本题考点: 质量守恒定律及其应用.
考点点评: 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.1年前查看全部
- 乙硫醇中的碳,氢元素的质量比为氢元素的质量比不是那3种物质的质量比 -_-|||我不认识那些符号。
 刘俊杰1年前1
刘俊杰1年前1 -
 phoenixwang1980 共回答了14个问题
phoenixwang1980 共回答了14个问题 |采纳率85.7%乙硫醇元素质量比:C2H6S C:H:S===24:6:32===12:3:161年前查看全部
- (2010•溧阳市模拟)为了能及时发现煤气泄漏,常在煤气中加入少量有特殊气味的乙硫醇(C2H5SH),乙硫醇燃烧的化学方
(2010•溧阳市模拟)为了能及时发现煤气泄漏,常在煤气中加入少量有特殊气味的乙硫醇(C2H5SH),乙硫醇燃烧的化学方程式为:2C2H5SH+902═4C02+2X+左H20,则X的化学式为( )
A.S
B.S02
C.S03
D.H2S03 tkmtyh1年前1
tkmtyh1年前1 -
 birdegg1981 共回答了18个问题
birdegg1981 共回答了18个问题 |采纳率100%解题思路:根据质量守恒定律中元素种类不变、原子个数不变的特点,可以确定X的化学式.由题干中的化学方程式可知:方程式的左边有49碳原子、129氢原子、29硫原子和189氧原子,你边有49碳原子、129氢原子、149氧原子和29X分子.根据质量守恒定律中元素种类不变、原子9数不变的特点可知:2X中含有29硫原子和49氧原子,所以在X中含有19硫原子和29氧原子,即X的化学式为:SO2.
故选:B.点评:
本题考点: 质量守恒定律及其应用.
考点点评: 熟练掌握质量守恒定律的实质并会应用,反应的化学方程式中各物质化学式前的化学计量数表示参加此反应的该物质的分子个数,在统计反应前后原子个数时,要正确使用化学计量数.1年前查看全部
- (2007•呼和浩特)为了能及时发现煤气泄漏,常在煤气中加入少量有特殊气味的乙硫醇(C2H5SH),乙硫醇燃烧的化学方程
(2007•呼和浩特)为了能及时发现煤气泄漏,常在煤气中加入少量有特殊气味的乙硫醇(C2H5SH),乙硫醇燃烧的化学方程式为2C2H5SH+9O2═4CO2+2x+6H2O,则X的化学式是( )
A. S
B. H2S
C. SO3
D. SO2 olvt1年前2
olvt1年前2 -
 lchycq1234 共回答了15个问题
lchycq1234 共回答了15个问题 |采纳率86.7%解题思路:化学反应前后,元素的种类不变,原子的种类、总个数不变.由2C2H5SH+9O2═4CO2+2x+6H2O可知,
反应前碳原子是4个,反应后是4个;
反应前氢原子是12个,反应后是12个;
反应前硫原子是2个,反应后应该是2个,包含在2x中;
反应前氧原子是18个,反应后应该是18个,其中的4个包含2x中;
由分析可知,每个x中含有1个硫原子和2个氧原子,是二氧化硫,化学式是SO2.
故选:D.点评:
本题考点: 质量守恒定律及其应用.
考点点评: 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.1年前查看全部
- 乙硫醇和乙醇哪个更难电离出H离子
 z3qe1年前1
z3qe1年前1 -
 痞子凡123 共回答了10个问题
痞子凡123 共回答了10个问题 |采纳率90%楼上的错了!
乙醇更难电离出H+,因为H-S键与H-O键中S对电子的吸引力弱与O所以S上面的电子云密度会小于O上的由于H+带正电性电子云密度越高负电荷越密集对H+的吸引力就越强H+就月难以得到电离,这也是H-O-C三N(氧氰酸)的酸性弱于H-S-C三N(硫氰酸),H2O的酸性弱于H2S,HF的酸性弱于HI等等的原因,至于一般多元无氧酸的酸性弱于单元无氧酸的酸性还有其它的原因,以H2S的酸性弱于HCl为例由于S具有双重负电荷而Cl只具有一重负电荷,由于电荷吸引是无饱和性的所以S对H的吸引力大于Cl对H的吸引力,所以使得H2S的酸性小于HCl,而H-S-C三N是强酸.
另外我HS-和HO-都是亲水基不是憎水基.1年前查看全部
- (2013•苏州一模)煤气中加人有特殊气味的乙硫醇可提示煤气是否泄漏.乙硫醇(用X表示)燃烧时发生反应的化学方程式为:2
(2013•苏州一模)煤气中加人有特殊气味的乙硫醇可提示煤气是否泄漏.乙硫醇(用X表示)燃烧时发生反应的化学方程式为:2X+9O2
4CO2+2SO2+6H2O,则X的化学式为( )点燃 .
A.C4H12S2
B.C2H6S
C.C2H6O2
D.C2H6S2 wyn1972101年前1
wyn1972101年前1 -
 kitten2016 共回答了14个问题
kitten2016 共回答了14个问题 |采纳率85.7%解题思路:根据质量守恒定律,化学反应前后各原子的种类和数目不变,反应前各原子的数目之和等于反应后各原子的数目之和,据此可推断X的化学式.反应后生成物4CO2、2SO2、6H2O中,共有4个碳原子、2个硫原子、18个氧原子、12个氢原子,反应物中除2X外有18个氧原子,根据质量守恒定律,反应前物质中原子的种类和数目不变,2X中应含有4个碳原子、2个硫原子、12个氢原子,因此一个X分子的组成为2个碳原子、1个硫原子、6个氢原子.
故选B.点评:
本题考点: 质量守恒定律及其应用.
考点点评: 本题考查根据化学方程式推断物质的化学式.此类试题的解题依据是质量守恒定律,只要能深刻理解质量守恒定律的含义,不难解决.1年前查看全部
- 75%的甲醇 10%的乙硫醇 10%轻质油 5%丙三醇 真空加压后能否产生可燃烧气体 热量值多少
75%的甲醇 10%的乙硫醇 10%轻质油 5%丙三醇 真空加压后能否产生可燃烧气体 热量值多少
主要是哪几种原料产生的气体 sanjianren1年前1
sanjianren1年前1 -
 可怜的小蚂蚁 共回答了17个问题
可怜的小蚂蚁 共回答了17个问题 |采纳率100%可以肯定的是可以燃烧,产物看你燃烧的完全程度,如果完全燃烧的话,产物是是二氧化碳、水和二氧化硫。。。
至于热值,那个轻质油的组份不是特别清楚,不过轻质油和汽油的组份接近,按这个计算的话,1kg混合物,燃烧大概放出:23748kJ的热量,就是5672千卡的热量。1年前查看全部
- 为及时发现煤气(主要成分是CO)泄漏,常加入少量有特殊气味的乙硫醇(化学式为C2H5SH).乙硫醇完全燃烧的化学方程式为
为及时发现煤气(主要成分是CO)泄漏,常加入少量有特殊气味的乙硫醇(化学式为C2H5SH).乙硫醇完全燃烧的化学方程式为2C2H5SH+9O2
4CO2+6H2O+2X.下列说法中正确的是( )点燃 .
A.CO是一种有刺激性气味的气体
B.X的化学式是SO2
C.CO、CO2都是污染空气的有毒气体
D.乙硫醇是由四种元素组成 h97120481年前1
h97120481年前1 -
 a13360402392 共回答了11个问题
a13360402392 共回答了11个问题 |采纳率100%解题思路:根据题干提供的信息进行分析,一氧化碳是无色无味的气体.根据质量守恒定律,化学反应前后原子的种类和个数不会改变即可判断X的化学式.A、一氧化碳是无味的气体,故A错误;
B、根据反应的化学方程式,反应前,共有4C,12H,18O,2S,反应后已有4C,12H,14O,故2X中含有2S和4O,X的化学式为SO2,故B正确;
C、二氧化碳不是空气污染气,故C错误;
D、乙硫醇由碳、氢、硫三种元素组成,故D错误;
故选:B.点评:
本题考点: 一氧化碳的物理性质;空气的污染及其危害;物质的元素组成;质量守恒定律及其应用.
考点点评: 本题考查了常见物质的性质以及质量守恒定律的应用,完成此题,可以依据题干提供的信息结合已有的知识进行.1年前查看全部
- (2004•云南)(1)为防止煤气泄漏使人中毒,常在煤气中加入少量有特殊气味的乙硫醇(C2H5SH).1乙硫醇由____
(2004•云南)(1)为防止煤气泄漏使人中毒,常在煤气中加入少量有特殊气味的乙硫醇(C2H5SH).1乙硫醇由______种元素组成,其相对分子质量是______;2乙硫醇在煤气燃烧过程中也可以充分燃烧,其化学方程式为:2C2H5SH+9O2═4CO2+2x+6H2O,则X的化学式为______
(2)防毒面具是一种保护人的呼吸器官、眼睛和面部的防护器材.过滤式防毒面具中一般装有活性炭,它能抵御多种毒气的进攻.原因是______. deyil1年前1
deyil1年前1 -
 smflove 共回答了20个问题
smflove 共回答了20个问题 |采纳率90%解题思路:(1)根据乙硫醇的化学式为C2H5SH,利用组成来分析元素的种类,利用相对原子质量来计算相对分子质量,再利用2C2H5SH+9O2═4CO2+2x+6H2O和质量守恒定律来推断物质的化学式;
(2)根据过滤式防毒面具中一般装有活性炭,利用活性炭的性质来分析能抵御多种毒气的进攻的原因.(1)由乙硫醇的化学式为C2H5SH,则该物质是由C、H、S三种元素组成的,其相对分子质量为12×2+1×6+32=62,由反应为2C2H5SH+9O2═4CO2+2x+6H2O,根据质量守恒定律可知,在反应前后的元素种类、原子的种类和个数不变,碳、氢原子的个数在反应前后相等,反应前共有2个硫原子、18个氧原子,则反应后应共有2个硫原子、18个氧原子,反应后已经有14个氧原子,则X中应含有2个硫原子、4个氧原子,又X的化学计量数为2,则X的化学式为SO2,
故答案为:三;62;SO2;
(2)根据过滤式防毒面具中一般装有活性炭,因活性炭具有疏松多孔的结构,则具有较强的吸附性,
从而能抵御多种毒气的进攻,故答案为:活性炭具有较强的吸附作用.点评:
本题考点: 相对分子质量的概念及其计算;碳单质的物理性质及用途;物质的元素组成;有关化学式的计算和推断.
考点点评: 本题属于信息题,学生应注意利用信息中物质的化学式和化学反应方程式,结合所学知识来解决新问题,训练了学生分析解决问题的能力.1年前查看全部
- 煤气中常假如少量有特殊气味的乙硫醇(C2H5)乙硫醇燃烧的化学方程式为2C2H5SH+9O
 luotong6021年前1
luotong6021年前1 -
 短信签名 共回答了24个问题
短信签名 共回答了24个问题 |采纳率100%2 C2H5SH + 9 O2====6 H2O + 4 CO2 + 2 SO2;条件:点燃1年前查看全部
- 煤气中加入有特殊臭味的乙硫醇可提示煤气是否泄漏.乙硫醇(用X表示)燃烧时发生的反应为:
煤气中加入有特殊臭味的乙硫醇可提示煤气是否泄漏.乙硫醇(用X表示)燃烧时发生的反应为:
2X+9O2点燃4CO2+2SO2+6H2O,则下列说法中不正确的是( )
A.X的化学式是C2H6S B.该反应属于氧化还原反应
C.乙硫醇是一种有机物 D.煤气泄漏时应立即打开排气扇或油烟机
那个正确.乙硫醇的燃烧是氧化反应,氦是氧化还原反应. jimjyy841年前1
jimjyy841年前1 -
 iambest2046 共回答了31个问题
iambest2046 共回答了31个问题 |采纳率93.5%答案是 D,那样的话会点燃煤气的.
是氧化还原反应.1年前查看全部
- 在120度,1.01x10^5Pa时,将乙醇,乙硫醇的混合蒸汽1L和5LO2混合,充分燃烧后,恢复到原情况,
在120度,1.01x10^5Pa时,将乙醇,乙硫醇的混合蒸汽1L和5LO2混合,充分燃烧后,恢复到原情况,
接上,气体密度减小为燃烧前混合气体的10/11,则乙醇和乙硫醇的体积之比为? ruik85101年前1
ruik85101年前1 -
 士多啤梨_517 共回答了24个问题
士多啤梨_517 共回答了24个问题 |采纳率91.7%乙醇燃烧方程式:C2H5OH+3O2→2CO2+3H20乙硫醇的燃烧方程式:2C2H5SH+9O2→4CO2+2SO2+6H2O设乙醇体积为x乙硫醇的体积为y则x+y=1气体密度减小为燃烧前混合气体的10/11,所以反应前气体体积是反应后气体体积的10/11
C2H5OH+3O2→2CO2+3H20 △v 2C2H5SH+9O2→4CO2+2SO2+6H2O △v
1 增1 2 增1
x x Y y/2
6/(6+x+y/2)=10/11 解得 x =0.2 Y=0.8 所以 乙醇和乙硫醇的体积之比
为1:41年前查看全部
- 乙醇和乙硫醇哪个沸点高?
 娇ai狐狸1年前2
娇ai狐狸1年前2 -
 傲雁蓝馨 共回答了23个问题
傲雁蓝馨 共回答了23个问题 |采纳率87%乙醇的沸点高.
这个类似于比较水和H2S的沸点.
因为乙硫醇分子之间没有氢键,沸点很低,沸点(℃):36.2 .
但是乙醇有氢键,沸点相对很高,78.4 °C .
希望对你有帮助O(∩_∩)O~1年前查看全部
- 乙硫醇在氧气中燃烧化学方程式
 九米1年前1
九米1年前1 -
 xiaobai417 共回答了16个问题
xiaobai417 共回答了16个问题 |采纳率87.5%2 C2H5SH + 9 O2====6 H2O + 4 CO2 + 2 SO2;条件:点燃1年前查看全部
- 乙硫醇的反应乙硫醇与NaOH反应生成什么?与金属钠反应呢?3Q~
 香竹海1年前3
香竹海1年前3 -
 一杯清茗-MM 共回答了19个问题
一杯清茗-MM 共回答了19个问题 |采纳率89.5%C2H5SH+NaOH=C2H5SNa+H2O
2C2H5SH+2Na=H2+2C2H5SNa1年前查看全部
- 乙硫醇燃烧的化学方程式为2C2H5SH+9O2 点燃 . 4CO2+2X+6H2O,则x的
乙硫醇燃烧的化学方程式为2C2H5SH+9O2
4CO2+2X+6H2O,则x的化学式是( )点燃 .
A. S
B. SO2
C. SO3
D. CO yyf12775431年前4
yyf12775431年前4 -
 三载ii 共回答了21个问题
三载ii 共回答了21个问题 |采纳率85.7%解题思路:根据质量守恒定律中元素种类不变、原子个数不变的特点,可以确定X的化学式.由题干中的化学方程式可知:左边有4个碳原子、12个氢原子、2个硫原子和18个氧原子,右边有4个碳原子、12个氢原子、14个氧原子和2个X分子.根据质量守恒定律中元素种类不变、原子个数不变的特点可知:2个X分子含有2个硫原子和4个氧原子,即1个X分子含有1个硫原子和2个氧原子,因此X的化学式为SO2.
故选:B.点评:
本题考点: 质量守恒定律及其应用.
考点点评: 本题主要考查根据质量守恒定律和化学方程式推断物质的化学式,难度较小.1年前查看全部
- (2007•呼和浩特)为了能及时发现煤气泄漏,常在煤气中加入少量有特殊气味的乙硫醇(C2H5SH),乙硫醇燃烧的化学方程
(2007•呼和浩特)为了能及时发现煤气泄漏,常在煤气中加入少量有特殊气味的乙硫醇(C2H5SH),乙硫醇燃烧的化学方程式为2C2H5SH+9O2═4CO2+2x+6H2O,则X的化学式是( )
A. S
B. H2S
C. SO3
D. SO2 心飞翔在月亮之上1年前1
心飞翔在月亮之上1年前1 -
 我心高飞 共回答了14个问题
我心高飞 共回答了14个问题 |采纳率100%解题思路:化学反应前后,元素的种类不变,原子的种类、总个数不变.由2C2H5SH+9O2═4CO2+2x+6H2O可知,
反应前碳原子是4个,反应后是4个;
反应前氢原子是12个,反应后是12个;
反应前硫原子是2个,反应后应该是2个,包含在2x中;
反应前氧原子是18个,反应后应该是18个,其中的4个包含2x中;
由分析可知,每个x中含有1个硫原子和2个氧原子,是二氧化硫,化学式是SO2.
故选:D.点评:
本题考点: 质量守恒定律及其应用.
考点点评: 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.1年前查看全部
大家在问
- 1佛组词,两个读音的,
- 2一件商品的原价是3000元,现在8折促销,活动结束后,再提价百分之几才能恢复原价?(要式子)
- 3用公式法解下列方程要有步骤谢谢(1)x^2-x-1=0(2)2x^2-9x+8=0(3)5x+2=3x^2(4)3y^2
- 4八上英语书 p45页的2b翻译
- 5一个等腰三角形的底是9分米,腰是6分米,它的面积是多少?
- 6英语只要答案1选词填空coat take country keep absent spend luckly weeken
- 7下列命题中,正确的命题有( )
- 80.2度电可使一个标有"220伏,2000瓦"字样的电热水壶连续正常工作___小时
- 9When all the students ________,the professor began his lectu
- 10刚学的物质两量,有点不懂..请问为什么“我们能推知1molO的质量是16g”啊?为什么这么说啊?1molO中包含6.02
- 11Mg2-+Ca(OH)2是复分解反应吗
- 12英语翻译我感到很震惊,有那么多数量的盒子破损吗?你能提供更多的照片关于这500个盒子破损的情况吗?那么,我们可以更好地要
- 13一矩形线圈,绕垂直匀强磁场并位于线圈平面内的固定轴转动,线圈中的感应电动势e随时间t的变化如图二所示,下列说法中正确的是
- 14(2010•阆中市模拟)当氧化铜中混有少量碳粉时,提纯的方法是( )
- 15写出百位十位和个位上的数都是6且近似数是七万的所有五位数
