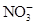氢化亚铜(CuH)是一种难溶物质,用CuSO 4 溶液和“另一种反应物”在40℃~50℃时反应可生成它。CuH不稳定,易
 windview12022-10-04 11:39:541条回答
windview12022-10-04 11:39:541条回答| 氢化亚铜(CuH)是一种难溶物质,用CuSO 4 溶液和“另一种反应物”在40℃~50℃时反应可生成它。CuH不稳定,易分解;CuH在氯气中能燃烧;跟盐酸反应能产生气体,以下有关的推断中错误的是
|

已提交,审核后显示!提交回复
共1条回复
 剑情客 共回答了17个问题
剑情客 共回答了17个问题 |采纳率82.4%- C
- 1年前
相关推荐
- (5分)氢化亚铜(CuH)是一种难溶物质,用CuSO 4 溶液和“另一物质”在40~50 ℃时反应可生成它。CuH具有的
(5分)氢化亚铜(CuH)是一种难溶物质,用CuSO 4 溶液和“另一物质”在40~50 ℃时反应可生成它。CuH具有的性质有:不稳定,易分解;在氯气中能燃烧生成氯化铜和氯化氢;Cu + 在酸性条件下发生的反应是2Cu + ===Cu 2 + +Cu。与稀盐酸反应能生成一种空气中燃烧火焰为淡蓝色的气体;(提示:CuH中H为-1价)
根据以上信息,结合自己所掌握的化学知识,回答下列问题:
(1)用CuSO 4 溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中作________(填“氧化剂”或“还原剂”)。
(2)写出CuH在氯气中燃烧的化学反应方程式: 。
(3)写出CuH溶解在稀盐酸中生成气体的化学方程式:
__________ 。 senda1031年前1
senda1031年前1 -
 gmydawx 共回答了17个问题
gmydawx 共回答了17个问题 |采纳率94.1%)(1)还原剂(1分) (2)2CuH+3Cl 2 2CuCl 2 +2HCl
(3) 2CuH+2HCl==CuCl 2 +Cu+2H 2 ↑
1年前查看全部
- 氢化亚铜(CuH)是一种难溶的物质,用铜或铜的某些化合物和“另一物质A”在一定条件下反应可生成它.CuH 不稳
氢化亚铜(CuH)是一种难溶的物质,用铜或铜的某些化合物和“另一物质A”在一定条件下反应可生成它.CuH 不稳定易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;Cu+在酸性条件下可发生反应2Cu+═Cu2++Cu.根据以上信息,结合自己所掌握的知识,回答下列问题:
(1)在溶液和“另一物质A”制CuH 的反应中,用氧化还原观点分析,这“另一物质A”在反应中所起的作用是______ (填氧化剂或还原剂).若A的化学式为NH5,它所有原子最外层电子都达到稀有气体的稳定结构,它的电子式为______,A溶于水后,溶液显______ (填酸性、碱性、中性).
(2)写出CuH在氯气中燃烧的化学方程式2CuH+3Cl2
2CuCl2+2HCl点燃 .2CuH+3Cl2.
2CuCl2+2HCl点燃 .
(3)CuH溶解在稀HCl中,产生的现象有______.
(4)如果把CuH溶解在足量的稀硝酸中产生的气休只有NO,请写出反应的离子方程式______. Blue_lion1年前0
Blue_lion1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 氢化亚铜(CuH)是一难溶物质,用CuSO4溶液和“另一种反应物”在40℃~50℃时反应可生成它.CuH不稳定,易分解;
氢化亚铜(CuH)是一难溶物质,用CuSO4溶液和“另一种反应物”在40℃~50℃时反应可生成它.CuH不稳定,易分解;CuH在氯气中能燃烧;跟盐酸反应能产生气体,以下有关它的推断中错误的是( )
A. “另一种反应物”一定具有氧化性
B. CuH既可做氧化剂也可做还原剂
C. CuH+Cl2═CuCl+HCl↑(燃烧)
D. CuH+HCl═CuCl+H2↑(常温) 00420501年前3
00420501年前3 -
 熊猫ee 共回答了14个问题
熊猫ee 共回答了14个问题 |采纳率100%解题思路:A.Cu元素的化合价由+2价降低为+1价,在反应中CuSO4作氧化剂;
B.CuH中Cu元素为+1价,既能升高又能降低;
C.CuH在氯气中能燃烧,Cu元素的化合价升高,Cl元素的化合价降低;
D.CuH跟盐酸反应能产生气体,气体为氢气.A.Cu元素的化合价由+2价降低为+1价,在反应中CuSO4作氧化剂,则“另一种反应物”在反应中作还原剂,具有还原性,故A错误;
B.CuH中Cu元素为+1价,既能升高又能降低,所以CuH既可做氧化剂也可做还原剂,故B正确;
C.CuH在氯气中能燃烧,Cu元素的化合价升高,Cl元素的化合价降低,则发生2CuH+3Cl2═2CuCl2+2HCl↑,题中未配平,故C错误;
D.CuH跟盐酸反应能产生气体,气体为氢气,该反应中只有H元素的化合价发生变化,反应为CuH+HCl═CuCl+H2↑,故D正确;
故选AC.点评:
本题考点: 铜金属及其重要化合物的主要性质.
考点点评: 本题主要考查氧化还原反应,注意利用信息及反应中元素的化合价变化来解答,题目难度不大,注重知识的迁移应用来考查学生.1年前查看全部
- (2012•潍坊一模)氢化亚铜(CuH)是一种红棕色的难溶物,能在Cl2中燃烧生成CuCl2和HCl,与盐酸反应生成Cu
(2012•潍坊一模)氢化亚铜(CuH)是一种红棕色的难溶物,能在Cl2中燃烧生成CuCl2和HCl,与盐酸反应生成CuCl和H2.下列关于氢化亚铜的推断正确的是( )
A.与盐酸反应属于置换反应
B.KSP随浓度和温度的变化而变化
C.在Cl2中燃烧时铜元素和氢元素均被氧化
D.与盐酸反应的离子方程式:H-+H+═H2↑ 风子0071年前1
风子0071年前1 -
 ychong1981 共回答了13个问题
ychong1981 共回答了13个问题 |采纳率92.3%解题思路:A.氢化亚铜和盐酸的反应方程式为:CuH+HCl=CuCl+H2↑,一种单质和一种化合物反应生成另外的单质和化合物的反应是置换反应;
B.溶度积常数只与温度有关;
C.失电子化合价升高的元素被氧化;
D.氢化亚铜不溶于水.A.氢化亚铜和盐酸的反应方程式为:CuH+HCl=CuCl+H2↑,该反应属于氧化还原反应但不属于置换反应,故A错误;
B.溶度积常数只与温度有关,与物质的浓度无关,故B错误;
C.氢化亚铜在氯气中燃烧时,铜元素和氢元素都失电子而被氧化,故C正确;
D.氢化亚铜与盐酸反应的离子方程式:CuH+H+═Cu++H2↑,故D错误;
故选C.点评:
本题考点: 氧化还原反应.
考点点评: 本题考查氧化还原反应,明确元素化合价是解本题关键,注意氢化亚铜中氢元素显-1价,为易错点.1年前查看全部
- 氢化亚铜(CuH)是一难溶物质,用CuSO 4 溶 液和另一种“反应物”在40℃~50℃时反应可生成它。CuH不稳定,易
氢化亚铜(CuH)是一难溶物质,用CuSO 4 溶 液和另一种“反应物”在40℃~50℃时反应可生成它。CuH不稳定,易分解;CuH在氯气中能燃烧,跟盐酸反应能产生气体。 下列有关推断中错误的是 [ ]A.这里的“另一种反应物”具有还原性
B.CuH可作氧化剂、还原剂
C.CuH+ Cl 2 ==CuCl+ HCl(点燃)
D.CuH+ HCl==CuCl+H 2 ↑ cz4281年前1
cz4281年前1 -
 277267104 共回答了19个问题
277267104 共回答了19个问题 |采纳率94.7%C1年前查看全部
- 氢化亚铜(CuH)是一种不稳定物质,能在氯气中燃烧,也能与酸反应。用CuSO 4 溶液和“某物质”在40~50℃时反应可
氢化亚铜(CuH)是一种不稳定物质,能在氯气中燃烧,也能与酸反应。用CuSO 4 溶液和“某物质”在40~50℃时反应可产生它。下列有关叙述中错误的是 [ ]A.这“某物质”具有还原性
B.CuH与盐酸反应,可能产生H 2
C.CuH与足量的稀硝酸反应:CuH+3H + +NO 3 - =Cu 2+ +NO↑+2H 2 O
D.CuH在氯气中燃烧:CuH+Cl 2 =CuCl+HCl 转世灵妖1年前1
转世灵妖1年前1 -
 瞬间命运 共回答了24个问题
瞬间命运 共回答了24个问题 |采纳率91.7%D1年前查看全部
- 氢化亚铜(CuH)是一种不稳定物质,能在氯气中燃烧;也能与酸反应,用CuSO 4 溶液和“某物质”在40-50℃时反应可
氢化亚铜(CuH)是一种不稳定物质,能在氯气中燃烧;也能与酸反应,用CuSO 4 溶液和“某物质”在40-50℃时反应可产生它.下列有关叙述中错误的是( ) A.这“某物质”具有还原性 B.CuH与盐酸反应,可能产生H 2 C.CuH与足量的稀硝酸反应:CuH+3H + +NO 3 - =Cu 2+ +NO↑+2H 2 O D.CuH在氯气中燃烧:CuH+Cl 2 =CuCl+HCl  tbzfrmg1年前1
tbzfrmg1年前1 -
 烟花烫1 共回答了17个问题
烟花烫1 共回答了17个问题 |采纳率94.1%A、因在该反应中,铜的化合价降,则“某物质”中元素的化合价必升高,体现了还原性,故A正确;
B、因CuH中-1价的H可以与盐酸中+1价氢发生归中反应:CuH+HCl═CuCl+H 2 ↑,故B正确;
C、因CuH具有还原性,与硝酸发生氧化还原反应:CuH+3HNO 3 =Cu ( NO 3 ) 2 +NO↑+2H 2 O,离子方程式:CuH+3H + +NO 3 - =Cu 2+ +NO↑+2H 2 O,故C正确;
D、因氯气的具有强氧化性,能够将+1价的铜氧化成+2价:2CuH+3Cl 2 =2CuCl 2 +2HCl,故D错误;
故选:D.1年前查看全部
- 氢化亚铜(CuH)是一种难溶物质,用CuSO 4 溶液和“另一物质”在40~50℃时反应可生成它。CuH具有的性质有:不
氢化亚铜(CuH)是一种难溶物质,用CuSO 4 溶液和“另一物质”在40~50℃时反应可生成它。CuH具有的性质有:不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;Cu + 在酸性条件下发生的反应是:2Cu + =Cu 2 + +Cu。
根据以上信息,结合自己所掌握的化学知识,回答下列问题:
(1)用CuSO 4 溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中作______(填“氧化剂”或“还原剂”)。
(2)写出CuH在氯气中燃烧的化学反应方程式:________________________。
(3)CuH溶解在稀盐酸中生成的气体是______(填化学式)。
(4)如果把CuH溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH溶解在足量稀硝酸中反应的离子方程式:_____________________________________。 风飘浪子1年前1
风飘浪子1年前1 -
 dsgz_555 共回答了18个问题
dsgz_555 共回答了18个问题 |采纳率100%1年前查看全部
- 氢化亚铜(CuH)可用CuSO4溶液和另一种反应物在40℃~50℃时反应生成.CuH不稳定,易分解,在氯气中能燃烧,常温
氢化亚铜(CuH)可用CuSO4溶液和另一种反应物在40℃~50℃时反应生成.CuH不稳定,易分解,在氯气中能燃烧,常温下跟盐酸反应能产生气体.以下表述错误的是( )
A.生成CuH的反应中CuSO4被氧化
B.CuH既可作氧化剂也可作为还原剂
C.2CuH+3Cl2
2CuCl2+2HCl点燃 .
D.CuH+HCl=CuCl+H2↑ wd2fly1年前1
wd2fly1年前1 -
 zz 共回答了19个问题
zz 共回答了19个问题 |采纳率63.2%解题思路:CuSO4溶液和“另一种物质”在40°C~50°C时反应来制备CuH,反应中CuSO4的Cu元素化合价降低,CuSO4为氧化剂,在反应中被还原;CuH中Cu元素的化合价为+1价,处于中间价态,既可做氧化剂又可做还原剂,在氯气中燃烧生成CuCl2.A.CuSO4溶液和“另一种物质”在40°C~50°C时反应来制备CuH,反应中CuSO4的Cu元素化合价降低,CuSO4为氧化剂,在反应中被还原,故A错误;
B.CuH中Cu元素的化合价为+1价,处于中间价态,既可做氧化剂又可做还原剂,故B正确;
C.CuH在氯气中燃烧生成CuCl2,方程式为2CuH+3Cl2
点燃
.
2CuCl2+2HCl,故C正确;
D.CuH跟盐酸反应能产生气体,气体为氢气,该反应中只有H元素的化合价发生变化,反应为CuH+HCl═CuCl+H2↑,故D正确;
故选A.点评:
本题考点: 氧化还原反应.
考点点评: 本题考查氧化还原反应,题目难度不大,注意元素化合价的判断,根据化合价的变化分析氧化还原反应.1年前查看全部
- 氢化亚铜(CuH)是一种难溶的物质,可用CuSO4溶液和“另一种物质”在40°C~50°C时反应来制备,CuH不稳定,它
氢化亚铜(CuH)是一种难溶的物质,可用CuSO4溶液和“另一种物质”在40°C~50°C时反应来制备,CuH不稳定,它既能与HCl反应产生气体,又能在氯气中燃烧,以下有关判断不正确的是( )
A.CuH既可做氧化剂又可做还原剂
B.另一种物质一定具有还原性
C.CuH跟HCl反应的化学方程式为:2CuH+2HCl=CuCl2+2H2↑+Cu
D.CuH在Cl2燃烧的化学方程式为:CuH+Cl2
CuCl+HCl点燃 . shirleyweng1年前1
shirleyweng1年前1 -
 心跳不会吧 共回答了14个问题
心跳不会吧 共回答了14个问题 |采纳率85.7%解题思路:CuSO4溶液和“另一种物质”在40°C~50°C时反应来制备CuH,反应中CuSO4的Cu元素化合价降低,CuSO4为氧化剂,则另一种物质为还原剂,CuH中Cu元素的化合价为+1价,处于中间价态,既可做氧化剂又可做还原剂,在氯气中燃烧生成CuCl2.A.CuH中Cu元素的化合价为+1价,处于中间价态,既可做氧化剂又可做还原剂,故A正确;
B.CuSO4溶液和“另一种物质”在40°C~50°C时反应来制备CuH,反应中CuSO4的Cu元素化合价降低,CuSO4为氧化剂,则另一种物质为还原剂,故B正确;
C.CuH跟HCl反应时生成的气体为H2,Cu自身发生氧化还原反应生成CuCl2和Cu,反应的化学方程式为2CuH+2HCl=CuCl2+2H2↑+Cu,故C正确;
D.CuH在氯气中燃烧生成CuCl2,方程式为2CuH+3Cl2
点燃
.
2CuCl2+2HCl,故D错误.
故选D.点评:
本题考点: 氧化还原反应;化学方程式的书写.
考点点评: 本题考查氧化还原反应,题目难度不大,注意元素化合价的判断,根据化合价的变化分析氧化还原反应.1年前查看全部
- 氢化亚铜(CuH)是一种不稳定的物质,能在氯气中燃烧,也能与酸反应。用CuSO 4 溶液和“某物质”在40~50 ℃时反
氢化亚铜(CuH)是一种不稳定的物质,能在氯气中燃烧,也能与酸反应。用CuSO 4 溶液和“某物质”在40~50 ℃时反应可生成CuH。下列叙述中错误的是 ( )。
A.“某物质”具有还原性 B.CuH与盐酸反应可能产生H 2 C.CuH与足量稀硝酸反应:CuH+3H + +NO 3 - =Cu 2 + +NO↑+2H 2 O D.CuH在氯气中燃烧:CuH+Cl 2 =CuCl+HCl  6pha1年前1
6pha1年前1 -
 ammy_chen 共回答了25个问题
ammy_chen 共回答了25个问题 |采纳率80%D
A项,用CuSO 4 溶液和“某物质”在40~50 ℃时反应可生成CuH,Cu元素由+2价变为+1价,则CuSO 4 作氧化剂,“某物质”为还原剂,表现出还原性;B项,CuH与盐酸发生氧化还原反应:2CuH+4HCl=2CuCl 2 +3H 2 ↑;C项,HNO 3 具有强氧化性,与CuH反应时,+1价Cu、-1价H均被氧化成最高价态;D项,Cl 2 具有强氧化性,CuH具有强还原性,二者反应会生成CuCl 2 和HCl。1年前查看全部
- 氢化亚铜(CuH)是一难溶物质,用CuSO 4 溶液和“另一种反应物”在40℃~50℃时反应可生成它。
氢化亚铜(CuH)是一难溶物质,用CuSO 4 溶液和“另一种反应物”在40℃~50℃时反应可生成它。
CuH不稳定,易分解;CuH在氯气中能燃烧;CuH跟盐酸反应能产生气体。以下有关推断中不正确的是[ ]A.“另一种反应物”在反应中表现还原性
B.CuH在化学反应中既可做氧化剂也可做还原剂
C.CuH在氯气中燃烧的化学方程式为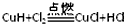
D.CuH与盐酸反应生成的气体是H 2 大胡扯1年前1
大胡扯1年前1 -
 chenguozhu11 共回答了12个问题
chenguozhu11 共回答了12个问题 |采纳率91.7%C1年前查看全部
- 氢化亚铜(CuH)是一种不稳定物质,能在氯气中燃烧;也能与酸反应。用CuSO 4 溶液和“某物质”在40~50℃时反应可
氢化亚铜(CuH)是一种不稳定物质,能在氯气中燃烧;也能与酸反应。用CuSO 4 溶液和“某物质”在40~50℃时反应可产生它。下列有关叙述中错误的是
A.这“某物质”具有还原性 B.CuH与盐酸反应,可能产生H 2 C.CuH与足量的稀硝酸反应:CuH + 3H + + NO 3 — = Cu 2+ + NO↑+ 2H 2 O D.CuH在氯气中燃烧:CuH + Cl 2 =" CuCl" + HCl  10015361年前1
10015361年前1 -
 卡卜卡卜 共回答了19个问题
卡卜卡卜 共回答了19个问题 |采纳率89.5%D
1年前查看全部
- 氢化亚铜和稀硝酸反应方程式.气体只生成一氧化氮.
 晓风寒_有烟相伴1年前0
晓风寒_有烟相伴1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40~50℃时反应可生成它.CuH具有的性质有:不稳定
氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40~50℃时反应可生成它.CuH具有的性质有:不稳定,易分解;在氯气中能燃烧生成氯化铜和氯化氢;Cu+在酸性条件下发生的反应是2Cu+═Cu2++Cu.与稀盐酸反应能生成一种空气中燃烧火焰为淡蓝色的气体;(提示:CuH中H为-1价)
根据以上信息,结合自己所掌握的化学知识,回答下列问题:
(1)用CuSO4溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中作还原剂还原剂(填“氧化剂”或“还原剂”).
(2)写出CuH在氯气中燃烧的化学反应方程式:2CuH+3Cl2
2CuCl2+2HCl2CuH+3Cl2点燃 .
2CuCl2+2HCl.点燃 .
(3)写出CuH溶解在稀盐酸中生成气体的化学方程式:
2CuH+2HCl=CuCl2+Cu+2H2↑2CuH+2HCl=CuCl2+Cu+2H2↑. qqqqMM1年前1
qqqqMM1年前1 -
 水杉落叶了 共回答了16个问题
水杉落叶了 共回答了16个问题 |采纳率75%(1)根据化合价的变化判断,CuSO4做氧化剂、所以另一物质做还原剂,故答案为:还原剂;
(2)CuH在氯气中燃烧,氯气做氧化剂,CuH做还原剂,所以反应方程式为:2CuH+3Cl2
点燃
.
2CuCl2+2HCl;
故答案为:2CuH+3Cl2
点燃
.
2CuCl2+2HCl;
(3)CuH溶解在稀盐酸中,CuH中的H-失电子,盐酸中H+得电子,所以得到的气体是H2,故答案为:2CuH+2HCl=CuCl2+Cu+2H2↑.1年前查看全部
- 氢化亚铜溶于稀盐酸生成什么气体
 nihenfanzdma1年前3
nihenfanzdma1年前3 -
 劫匪2007 共回答了21个问题
劫匪2007 共回答了21个问题 |采纳率90.5%生成氢气.
反应如下:2CuH+2HCl=2H2 ↑+CuCl2+Cu
理解请及时采纳!1年前查看全部
- 氢化亚铜化合价求学长详解
 心是沙1年前1
心是沙1年前1 -
 2005005 共回答了19个问题
2005005 共回答了19个问题 |采纳率84.2%铜有两种常见化合价:+1价、+2价
亚铜为:+1价,
氢化亚铜是铜的二元氢化物,化学式为:CuH
根据化合物中各元素化合价的代数和为零的规律,可计算出
氢化亚铜中氢元素的化合价为:-1价
如帮到了你,
【你的10分满意,我们团队的无限动力】1年前查看全部
- 氢化亚铜(CuH)是一难溶物质,用CuSO4溶液和“另一种反应物”在40℃~50℃时反应可生成它.CuH不稳定,易分解;
氢化亚铜(CuH)是一难溶物质,用CuSO4溶液和“另一种反应物”在40℃~50℃时反应可生成它.CuH不稳定,易分解;CuH在氯气中能燃烧;跟盐酸反应能产生气体,以下有关它的推断中错误的是( )
A.“另一种反应物”一定只具有氧化性
B.CuH既可做氧化剂也可做还原剂
C.2CuH+3Cl2═2CuCl2+2HCl↑(燃烧)
D.CuH+HCl═CuCl+H2↑(常温) xulikun1001年前1
xulikun1001年前1 -
 rightcare 共回答了18个问题
rightcare 共回答了18个问题 |采纳率100%解题思路:A.Cu元素的化合价由+2价降低为+1价,在反应中CuSO4作氧化剂;B.CuH中Cu元素为+1价,既能升高又能降低;C.CuH在氯气中能燃烧,Cu元素的化合价升高,Cl元素的化合价降低;D.CuH跟盐酸反应能产生气体,气体为氢气.A.Cu元素的化合价由+2价降低为+1价,在反应中CuSO4作氧化剂,则“另一种反应物”在反应中作还原剂,具有还原性,故A错误;
B.CuH中Cu元素为+1价,既能升高又能降低,所以CuH既可做氧化剂也可做还原剂,故B正确;
C.CuH在氯气中能燃烧,Cu元素的化合价升高,Cl元素的化合价降低,则发生2CuH+3Cl2═2CuCl2+2HCl↑,故C正确;
D.CuH跟盐酸反应能产生气体,气体为氢气,该反应中只有H元素的化合价发生变化,反应为CuH+HCl═CuCl+H2↑,故D正确;
故选A.点评:
本题考点: 氧化还原反应.
考点点评: 本题考查氧化还原反应,注意利用信息及反应中元素的化合价变化来解答,题目难度不大,注重知识的迁移应用来考查学生.1年前查看全部
- CuH自燃化学方程式22.(8分)氢化亚铜(CuH)是一种难溶物质,不稳定;60℃时可在空气中自燃;与稀盐酸 反应能生成
CuH自燃化学方程式
22.(8分)氢化亚铜(CuH)是一种难溶物质,不稳定;60℃时可在空气中自燃;与稀盐酸
反应能生成气体,Cu+在酸性条件下发生如下反应 2Cu+ = Cu2+ + Cu.
根据以上信息,结合自己所掌握的化学知识,回答下列问题:
(1)在40℃~50℃时,用CuSO4溶液和"另一物质"可制得CuH,用氧化还原观点分析,
这"另一物质"在反应中所起的作用是 (填"氧化剂"或"还原剂");
(2)60℃时CuH在空气中自燃的化学反应方程式为 ;
(3)CuH溶解在稀盐酸中的反应方程式为 ;
(4)如果把CuH溶解在足量的稀硝酸中反应,则CuH中的两种元素在生成物中分别存在于 物质中(填化学式). bingzi1年前5
bingzi1年前5 -
 向ww狂奔 共回答了21个问题
向ww狂奔 共回答了21个问题 |采纳率81%(1)Cu由2价变1价 被还原 所以另一物质是还原剂
(2)4CuH+3O2=4CuO+2H2O
(3)2CuH+2HCl=CuCl2+Cu+2H2
(4)Cu(NO3)2 Cu H21年前查看全部
- 氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40-50℃时反应可生成它.CuH具有的性质有:不稳定
氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40-50℃时反应可生成它.CuH具有的性质有:不稳定,易分解,在氯气中能燃烧;与稀盐酸反应能生成气体:Cu+在酸性条件下发生的反应是:
2Cu+=Cu2++Cu.
根据以上信息,结合自己所掌握的化学知识,回答下列问题:
(1)在CuSO4溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中所起的作用是______(填氧化剂或还原剂).
(2)写出CuH在氯气中燃烧的化学反应方程式______
(3)CuH溶解在稀盐酸中生成的气体是______(填化学式)
(4)如果把CuH溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH溶解在足量稀硝酸中反应的离子方程式______. 生命科学1年前1
生命科学1年前1 -
 mj59 共回答了8个问题
mj59 共回答了8个问题 |采纳率100%解题思路:(1)根据化合价的变化判断氧化剂、还原剂;
(2)CuH在氯气中燃烧,氯气做氧化剂,CuH做还原剂;
(3)CuH溶解在稀盐酸中,CuH中的H-失电子,盐酸中H+得电子;
(4)Cu+在酸性条件下发生的反应是:2Cu+=Cu2++Cu,稀硝酸具有强氧化性,能和铜反应生成一氧化氮气体.(1)根据化合价的变化判断,CuSO4做氧化剂、所以另一物质做还原剂,故答案为:还原剂;
(2)CuH在氯气中燃烧,氯气做氧化剂,CuH做还原剂,所以反应方程式为:2CuH+3Cl2
点燃
.
2CuCl2+2HCl;
故答案为:2CuH+3Cl2
点燃
.
2CuCl2+2HCl;
(3)CuH溶解在稀盐酸中,CuH中的H-失电子,盐酸中H+得电子,所以得到的气体是H2,故答案为:H2;
(4)Cu+在酸性条件下发生的反应是:2Cu+=Cu2++Cu,稀硝酸具有强氧化性,CuH具有还原性,二者反应生成一氧化氮气体、铜离子、H2O,
故答案为:CuH+3H++NO3-=Cu2++2H2O+NO↑.点评:
本题考点: 铜金属及其重要化合物的主要性质;化学方程式的书写;氧化还原反应.
考点点评: 本题是信息给予题,筛选有用信息结合已学知识进行整合处理.1年前查看全部
- 氢化亚铜的离子化合价
 nimingwei1231年前1
nimingwei1231年前1 -
 72948832 共回答了23个问题
72948832 共回答了23个问题 |采纳率91.3%氢和金属的化合物,氢-1价,金属正价
亚铜是+1价
所以氢化亚铜由Cu+和H-构成
Cu+ +1价
H- -1价1年前查看全部
- 氢化亚铜如何制取硫酸铜和什么能制取氢化亚铜?
 硬帮帮二郎1年前1
硬帮帮二郎1年前1 -
 蜀气东渐 共回答了17个问题
蜀气东渐 共回答了17个问题 |采纳率82.4%在65℃下将次磷酸[H2PO(OH)]加到CuSO4溶液反应而制得.1年前查看全部
- 氢化亚铜与稀硝酸反应是氢化亚铜
 懒人-20031年前1
懒人-20031年前1 -
 frq13483810136 共回答了17个问题
frq13483810136 共回答了17个问题 |采纳率94.1%CuH + 3HNO3 = Cu(NO3)2 + NO↑ + 2H2O1年前查看全部
大家在问
- 1To get a better view of the stage,.
- 2一个数的3倍比450多63,求这个数?
- 3sin的平方2 π/12-1/2
- 4我爱这土地仿写第一节假如你是一只鸟,在改革开放的新时代,你会歌唱些什么呢?
- 5色子一般是正方体形状,在它的六个面上分别刻有1~6个小圆点.随便投掷色子,
- 6已知数列{an}的前n项和为Sn,a1=2,an+1=Sn+1,n∈N*,则a6等于( )
- 7请问:l myself drive the car.
- 8小明按一定的规律写数1、-2、3、4、-5、6、7、-8、9.当写完第200个数时,写的数中有几个正数几个负数
- 9One day I_________ him in the street and he said he_________
- 103.87除以4.3乘以(1.2+0.3)要求简算 怎么算?
- 11在下面各题的等号左边添上合适的运算符号和括号,使计算结果正好等于右边的数
- 12仿照例句的表达方法,仿写句子.老桥,你如一位德高望重的老人.
- 13x-1=6x-12,x=多少
- 14一般现在时的谓语分为哪四种情况
- 15我挑战我快乐 作文