减压蒸馏过程中如何加温
 村上春树272022-10-04 11:39:541条回答
村上春树272022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 5ica1i 共回答了18个问题
5ica1i 共回答了18个问题 |采纳率88.9%- 用电热板或电加热套对烧瓶加热加温
- 1年前
相关推荐
- 减压后物质的熔点如何变化有一种物质常压下熔点95℃,减压到-0.1MPa后,熔点会不会变低?
 congdecai1年前3
congdecai1年前3 -
 ItDoesnMatter 共回答了20个问题
ItDoesnMatter 共回答了20个问题 |采纳率65%熔点随压强的变化有两种不同的情况.
对于大多数物质,熔化过程是体积变大的过程,当压强增大时,这些物质的熔点要升高;
对于像水这样的物质,与大多数物质不同,冰熔化成水的过程体积要缩小(金属铋、锑等也是如此),当压强增大时冰的熔点要降低.1年前查看全部
- 如何减压的英语作文
 bonny_ch1年前1
bonny_ch1年前1 -
 白糖素面 共回答了13个问题
白糖素面 共回答了13个问题 |采纳率100%How to reduce pressure
There are some advice about how to reduce our pressure.
First,you should often remind yourself that you are the best one,you can do well what you want to do.second,listen to music when you feel stressful,it can help you become relax.Finely,if you can’t get rid of the pressure by yourself,you can also ask your teache or parent for help,they will solve the problem which you are facing.
你是初中的吧 不知道可不可以帮到你1年前查看全部
- 三相笼型异步电动机采用星形—三角形减压启动时,启动转矩变为额定转矩的()
 cw_19681年前2
cw_19681年前2 -
 endy-lau 共回答了13个问题
endy-lau 共回答了13个问题 |采纳率100%对于一般的鼠笼式电动机.它的启动转矩为额定转矩的1.0——1.8倍.主要因转子回路电阻的不同而不同.
启动转矩与电压的平方成正比.所以星三角启动时的启动转矩为额定的三分之一
5-7倍这个数字是全压正常启动的电流与额定电流之比值1年前查看全部
- 加压,减压,常压蒸馏……何解?如题,它们更有什么效果?压强不同会有什么不同的结果?
 ljleejam1854161年前2
ljleejam1854161年前2 -
 zlp572500 共回答了19个问题
zlp572500 共回答了19个问题 |采纳率78.9%蒸馏是把液体加热到沸腾,再把蒸汽冷凝成液体进行分离提纯的一种操作.
加压,减压,常压蒸馏应用的对象不同.
常压蒸馏应用于大气压下沸点较低,蒸汽压较大的液体;
减压应用于沸点较高或者高温下容易分解、氧化的液体;
加压会使蒸馏变得困难,很少使用.1年前查看全部
- 反应mA(g)+nB(g)===(可逆符号)pC(g)达到平衡后,当升高温度时,B的转化率变大,当减压后混合体系中C的百
反应mA(g)+nB(g)===(可逆符号)pC(g)达到平衡后,当升高温度时,B的转化率变大,当减压后混合体系中C的百分含量减小.
(1).逆反应是?热反应.
(2).加压后,A的浓度是减小、增大还是不变.
(3).若B是有色物质,A、C是无色物质,减小压强,反应混合物的颜色是变深、变浅还是不变.
请写出计算过程和结果并说明理由好吗? 冰箱遥控器1年前3
冰箱遥控器1年前3 -
 ootangqun 共回答了25个问题
ootangqun 共回答了25个问题 |采纳率92%(1)升高温度平衡右移,说明正反应是吸热反应,逆反应则是放热反应.
(2)减压后C百分含量减小,减压反应朝气体增多的方向移动,所以m+n>p
加压反应向气体减少的方向移动,由于m+n>p,平衡右移,A浓度减小.
(3)减小压强,B的量增多,但密度仍是减小的,因此反应混合物颜色变浅.1年前查看全部
- 如何获得大量的乙烯.丙烯丁二烯1.石油的常压分馏2.石油的减压分馏3.石油裂化4.石油裂解
 流泪的开心果1年前1
流泪的开心果1年前1 -
 0oau 共回答了20个问题
0oau 共回答了20个问题 |采纳率95%4石油裂解1年前查看全部
- 将5.6g Fe投入浓硝酸溶液,产生红棕色气体A,把所得溶液减压蒸干,得到20g Fe(NO3)2和
将5.6g Fe投入浓硝酸溶液,产生红棕色气体A,把所得溶液减压蒸干,得到20g Fe(NO3)2和Fe(NO3)3的混合物,将该固体在高温下加热,得到红褐色的Fe2O3和气体B,A、B气体混合通入足量水中,在标准状况下剩余气体的体积为( )
A. 2240mL
B. 4480mL
C. 3360mL
D. 1120mL SunTa0071年前2
SunTa0071年前2 -
 平静的mm 共回答了22个问题
平静的mm 共回答了22个问题 |采纳率77.3%解题思路:根据题意可知,红棕色气体为二氧化氮,即铁与浓硝酸反应时,铁失去电子,氮元素得到电子;在Fe(NO3)2和Fe(NO3)3的混合物,将该固体在高温下加热,得到红褐色的Fe2O3和气体B是亚铁失去电子,氮元素得电子;再A、B气体混合通入足量水中剩余气体一定为NO,则可利用得失电子守恒来计算NO的物质的量.因最后气体为NO,设其物质的量为x,
铁与浓硝酸反应时,铁失去电子,氮元素得到电子,且A为二氧化氮,
在Fe(NO3)2和Fe(NO3)3的混合物,将该固体在高温下加热,得到红褐色的Fe2O3和气体B,是亚铁失去电子,氮元素得电子,且B为氧气,
A、B气体混合通入足量水生成硝酸和NO,
根据守恒思想,计算时抓住反应的始终态即可,反应物可看作Fe、HNO3和水,最终生成物是Fe2O3和剩余气体,A和B混合气体通入水中,剩余气体是NO或O2,根据电子得失守恒可定性判断出剩余气体不可能是O2,则剩余气体只能是NO,设其物质的量为x,则整个过程中由得失电子守恒可知,
[5.6g/56g/mol]×(3-0)=x×(5-2),
解得x=0.1mol,
即标准状况下体积为0.1mol×22.4L/mol=2240mL,
故选A.点评:
本题考点: 有关混合物反应的计算.
考点点评: 本题较难,明确发生的化学反应,注意元素化合价的变化,明确最后的物质,利用电子守恒来快速计算是解答的关键,从而可避免中间过程的繁杂计算.1年前查看全部
- 高压分馏与减压分馏请分别简要解释原理,并列举一些应用
 一生如水1年前2
一生如水1年前2 -
 烟头咖啡 共回答了23个问题
烟头咖啡 共回答了23个问题 |采纳率95.7%液体的沸点跟压力是有关系的,压力越大,沸点就会越高,压力越低,沸点就会越高.
依据这个原则,高压分馏,通过提高压力,从而使馏分的沸点升高,从而得到低沸点馏分,
而减压,则是降低压力,使沸点降低,从而使本应要很高温度才能沸腾的馏分,在较低温度下就可以沸腾,从而得到高沸点馏分.
只要明白沸点与压力的关系,就可以解决这一类的问题了.1年前查看全部
- 关于初三学生面对中考,减压的英语作文
 loli爱8卦1年前1
loli爱8卦1年前1 -
 dustin_xu 共回答了12个问题
dustin_xu 共回答了12个问题 |采纳率91.7%Reasons and plans for reducing pressure
Nowadays, more and more people are easily get into troubles and gain pressure almost at every time. For students, most of them are studying under great pressure. For adults, nearly all of them feel stressed out. People of all ages are facing pressure because the growing competition. There's no exception.
For pressure do cause a lot of trouble for our daily life. It's best for us to make some plans for reducing them. In my point of view, we should first have a right attitude towards failure. We should learn to face our disadvantages and mistakes. No one is perfect.Only if we draw lessons from failure can we improve ourselves. Then, we should take enough exercise to strengthen our body. To be healthy is the most important thing for standing pressure. What's more, we can spend our holiday going sightseeing. Nature could help us forget all the troubles and relax better than ourselves. Then once we get back to our work or study, we can put all our energy into it.
From what has been discussed above, it's really important to reduce pressure to live a more relaxing life. Let's just try our best to achieve a comfortable life.
许多学习生活中的烦恼都会使人产生压力,为了更好地发现及解决同学们中存在的心理压力问题,你们班特意开展了一次以"Less Pressure, Better Life"为主题的英语演讲比赛,请你准备发言稿,谈谈你的一些缓解压力的好办法,与同学分享,内容包括:
(1) 同学们中普遍存在的压力是什么;
(2) 我的压力是什么;
(3) 我是如何成功缓解我的压力的.
注意:文中不得出现真实的姓名和校名.词数80~100.
★ 范文
Less Pressure, Better Life
Hello, boys and girls!
Pressure is a serious problem in today’s world. Students in our class are under too much pressure. Some students can’t get on well with their classmates, while others may worry about their exams.
I’m always under pressure, too. My parents want me to be the top student in class. So they send me to all kinds of after-classes at weekends. Last Monday evening, I had a talk with my mother. I told her I was not lazy. I really felt tired. I needed time to relax. My mother agreed with me at last. So I think a conversation with parents is necessary to solve the problem.
That’s all. Thank you!1年前查看全部
- 给水排水 中小学化学试验室给水减压方法
给水排水 中小学化学试验室给水减压方法
中小学建筑设计规范上要求,当化学实验室绐水水嘴的工作压力大于0.02MPa,急救冲洗水嘴的工作压力大于0.01MPa时,应采取减压措施.
这个该怎么减压?因为最后要求压力非常小,是在总的支管处减压,还是在每个水嘴处减压,如果在总的给水支管处减压一般阀后压力应在多少合适? 1912021年前1
1912021年前1 -
 泡泡ICE 共回答了17个问题
泡泡ICE 共回答了17个问题 |采纳率100%在支管处加装一个减压阀,可调式,根据需要调节到合适的压力1年前查看全部
- 天然气减压后管道应大于减压前吗?关于天然气流量和管径的计算公式吗?减压前压力100千帕,减压后5千帕
天然气减压后管道应大于减压前吗?关于天然气流量和管径的计算公式吗?减压前压力100千帕,减压后5千帕
120个(GR1602)红外线燃烧器
每小时59m3天然气需要多大的管径 yxml1年前1
yxml1年前1 -
 jsnh2008 共回答了19个问题
jsnh2008 共回答了19个问题 |采纳率84.2%这些是一个系统的计算,不是简单条件的计算.假如减压后一个燃烧器具和1000个燃烧器具的管道直径可以一样吗?这些问题需要许多经验数据的使用,没有经验难以计算准确.纯粹的从气态性能效果方面计算就需要试验数据支持.
经验感觉使用内径50毫米的无缝管即可.假如距离调压器大于200米,管径还要加大.1年前查看全部
- 请问哪位高手知道为什么我做出的柠檬酸三丁酯减压脱醇后会变成黄色呢?酯化反应后颜色很白的啊,
 doublesong1年前1
doublesong1年前1 -
 zhidaowangzi 共回答了18个问题
zhidaowangzi 共回答了18个问题 |采纳率94.4%柠檬酸三丁酯合成可用的催化剂较多,不知你用的是固体还是液体,固体好滤去,液体酸就要好好洗洗(水洗、碱洗)才能减压脱醇1年前查看全部
- 减压蒸馏中真空泵会抽走气和水蒸气,如果要回收溶剂不会因此也给真空泵抽走吗
 波恩的nn1年前2
波恩的nn1年前2 -
 zhuchao123 共回答了12个问题
zhuchao123 共回答了12个问题 |采纳率100%真空蒸馏使用中抽走的只是气体,气体的冷凝度数是不一样的,回收方式也不一样.
如果所有的气体都需要回收,可以在排气口增加汽水分离器(假设使用的是水环式真空泵)实现气体与水分离.
如果固定回收一中气体,那就需要增加冷凝回流装置.
问题需要精确到那种气体,回收什么.
一般情况下就是这两种回收方式,具体实施需要请教一下化工系的老师,分析研究不同的气体回收方式.
------------------------------------------------------------------------------------------------------------------
淄博博山群圣真空设备厂 希望可以帮到您1年前查看全部
- 把CO2通入含NaOH 0.8g的碱溶液中,将产物在减压条件下蒸干后,得固体1.37g,则通入CO2的质量是( )
把CO2通入含NaOH 0.8g的碱溶液中,将产物在减压条件下蒸干后,得固体1.37g,则通入CO2的质量是( )
A. 0.44g
B. 0.88g
C. 0.66g
D. 都不是 Aska20051年前2
Aska20051年前2 -
 zhangqianyuok 共回答了20个问题
zhangqianyuok 共回答了20个问题 |采纳率80%解题思路:首先根据NaOH的质量和固体的质量判断反应产物的成分,利用假设法进行,假定0.8g氢氧化钠全部生成碳酸钠,0.8g氢氧化钠全部生成碳酸氢钠,计算碳酸钠与碳酸氢钠的质量,根据实际固体质量判断进行的反应,进而根据反应的方程式计算.设0.8g氢氧化钠全部生成碳酸钠,质量为x,则有
2NaOH+CO2=Na2CO3+H2O
80 106
0.8g x
x=[0.8g×106/80]=1.06g,
设0.8g氢氧化钠全部生成碳酸氢钠,质量为y,则有
NaOH+CO2=NaHCO3
4084
0.8g y
y=[0.8g×84/40]=1.68g,
而题干中给出的物质的质量为1.37g,所以产物为碳酸钠、碳酸氢钠.
设混合物中含有mmolNa2CO3,nmolNaHCO3,根据钠元素守恒有:2m+n=[0.8/40],根据固体质量有:106m+84n=1.37,联立方程解得:m=0.005,n=0.01,所以通入CO2的质量为:(0.005+0.01)mol×44g/mol=0.66g.
故选:C.点评:
本题考点: 化学方程式的有关计算.
考点点评: 本题考查化学方程式的计算,根据反应物的量判断生成物的组成为解答该题的关键,题目难度中等.1年前查看全部
- 怎样减压英语作文80词连翻译
 cclihua19821年前0
cclihua19821年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 过氧化值测定或酸价中“减压挥发”如何做?是用抽中空吗?
过氧化值测定或酸价中“减压挥发”如何做?是用抽中空吗?
称取100g绞匀的试样于500mL具塞三角瓶中,加100mL~200mL石油醚(30℃~60℃沸程)振荡10min后,放置过夜,过滤后减压挥发溶剂,得到油脂. XH幸福1年前1
XH幸福1年前1 -
 流放的zz王 共回答了20个问题
流放的zz王 共回答了20个问题 |采纳率95%恩,抽中空,不能加热蒸发啊怕影响,只好这样了
你在做这个啊?我也是,不过是KI和硫代硫酸钠滴定
同时也测P茴香胺值,一回事1年前查看全部
- 你如何减压? 英语作文 带翻译
 椰根情痴1年前1
椰根情痴1年前1 -
 谎言爱情 共回答了13个问题
谎言爱情 共回答了13个问题 |采纳率92.3%How to reduce pressure
There are some advice about how to reduce our pressure。
First,you should often remind yourself that you are the best one,you can do well what you want to do。second,listen to music when you feel stressful,it can help you become relax。Finely,if you can’t get rid of the pressure by yourself,you can also ask your teache or parent for help,they will solve the problem which you are facing。1年前查看全部
- 关于减压的初中英语作文中考作文 缓解考试压力
 蓝色蓝雨1年前2
蓝色蓝雨1年前2 -
 苏樱爱玲 共回答了21个问题
苏樱爱玲 共回答了21个问题 |采纳率95.2%Reasons and plans for reducing pressure
Nowadays, more and more people are easily get into troubles and gain pressure almost at every time. For students, most of them are studying under great pressure. For adults, nearly all of them feel stressed out. People of all ages are facing pressure because the growing competition. There's no exception.
For pressure do cause a lot of trouble for our daily life. It's best for us to make some plans for reducing them. In my point of view, we should first have a right attitude towards failure. We should learn to face our disadvantages and mistakes. No one is perfect.Only if we draw lessons from failure can we improve ourselves. Then, we should take enough exercise to strengthen our body. To be healthy is the most important thing for standing pressure. What's more, we can spend our holiday going sightseeing. Nature could help us forget all the troubles and relax better than ourselves. Then once we get back to our work or study, we can put all our energy into it.
From what has been discussed above, it's really important to reduce pressure to live a more relaxing life. Let's just try our best to achieve a comfortable life.1年前查看全部
- 当减压蒸馏完所要的化合物后,应如何停止减压蒸馏?为什么?
 诶彼西帝1年前1
诶彼西帝1年前1 -
 无限变有限 共回答了26个问题
无限变有限 共回答了26个问题 |采纳率80.8%先移去热源,然后慢慢旋开夹在毛细管上的橡皮管的螺旋夹放空,待蒸馏瓶稍冷后再慢慢开启安全瓶上的活塞,平衡内外压力,(若开得太快,水银柱很快上升,有冲破测压计的可能),最后才关闭真空水泵
为什么:如果不按上面这样操作可能会导致蒸馏瓶内残留液形成蒸汽状而冲入接收瓶中使整个蒸馏过程失败,测压计可能会被冲破,1年前查看全部
- 将适量的CO2通入含0.8克NaOH的碱溶液中,将产物在减压、低温下蒸干后得到1.37克固体物质.问:产物是什么物质?通
将适量的CO2通入含0.8克NaOH的碱溶液中,将产物在减压、低温下蒸干后得到1.37克固体物质.问:产物是什么物质?通入CO2的质量是多少?
 flyEmirate1年前1
flyEmirate1年前1 -
 cimlch308 共回答了19个问题
cimlch308 共回答了19个问题 |采纳率94.7%解题思路:二氧化碳可以与氢氧化钠反应生成碳酸钠和水,二氧化碳与氢氧化钠能反应生成碳酸氢钠,根据生成固体的质量可以求得通入的二氧化碳的质量.二氧化碳可以与氢氧化钠反应生成碳酸钠和水,二氧化碳与氢氧化钠能反应生成碳酸氢钠,设0.8g氢氧化钠全部生成碳酸钠的质量为x,则有
2NaOH+CO2=Na2CO3+H2O
80 106
0.8g x
[80/0•8g]=[106/x]
x=1.06g
设8g氢氧化钠全部生成碳酸氢钠的质量为y,则有
2NaOH+CO2=2NaHCO3
80 168
0.8g y
[80/0•8g]=[168/y]
y=1.68g
而题干中给出的物质的质量为1.37g,所以有一部分氢氧化钠转化生成了碳酸氢钠,故产物为碳酸钠和碳酸氢钠的混合物,
设生成碳酸钠需要氢氧化钠的质量为a,生成碳酸钠的质量为b,则有
2NaOH+CO2=Na2CO3+H2O
80 106
a b
[80/a]=[106/b] ①
2NaOH+H2O+2CO2=2NaHCO3
80 168
0.8g-a 1.37g-b
[80/0•8g−a]=[168/1•37g−b] ②
联立①②可以解得b=0.53g
所以生成的碳酸氢钠的质量为:1.37g-0.53g=0.84g,
根据碳元素质量守恒,设通入的二氧化碳的质量为Z,则有
[12/44]×Z=[12/106]×0.53g+[12/84]×0.84g
Z=0.66g
答:所得产物为碳酸钠和碳酸氢钠的混合物,通入二氧化碳的质量为0.66g.点评:
本题考点: 碱的化学性质;根据化学反应方程式的计算.
考点点评: 本题考查了氢氧化钠与二氧化碳的反应,完成此题,要根据生成的物质的质量正确判断出反应的生成物,然后再进行有关的计算.1年前查看全部
- 反应ma+nb=pc在某温度下达到平衡 若abc是气体,减压后正反应速率小于逆反应速率则mnp的关
反应ma+nb=pc在某温度下达到平衡 若abc是气体,减压后正反应速率小于逆反应速率则mnp的关
反应ma+nb=pc在某温度下达到平衡
若abc是气体,减压后正反应速率小于逆反应速率则mnp的关系 爱家的女人19831年前1
爱家的女人19831年前1 -
 happyfishme 共回答了25个问题
happyfishme 共回答了25个问题 |采纳率80%反应m A+n B⇌p C在某温度下达到平衡.
①若A、B、C都是气体,减压后正反应速率小于逆反应速率,则m、n、p的关系是
m+n>p
.
②若C为气体,且m+n=p,在加压时化学平衡发生移动,则平衡必定向
逆向
方向移动.
③如果在体系中增加或减少B的量,平衡均不发生移动,则B肯定不能为
气
态.
考点:化学平衡的影响因素;化学平衡状态的判断.
专题:化学平衡专题.
分析:①根据影响化学平衡因素结合速率大小分析判断反应前后的体积变化;
②反应前后系数相同,改变压强平衡移动说明反应物中含有固体或纯液体;
③固体和纯液体对平衡无影响.
①反应mA+nB⇌pC,若A、B、C都是气体,减压后正反应速率小于逆反应速率,证明逆向反应是气体体积增大的反应,得到m+n>p,故答案为:m+n>p;
②若反应mA+nB⇌pC;C为气体,且m+n=p,在加压时化学平衡发生移动,说明AB中至少有一种是固体或纯液体,加压平衡逆向进行,故答案为:逆向;
③若反应mA+nB⇌pC;如果在体系中增加或减少B的量,平衡均不发生移动,证明B一定是固体或纯液体,不是气体,故答案为:气.
点评:本题考查了化学平衡的影响因素判断,主要考查压强对平衡的影响和物质性质的判断,化学平衡的移动规律是解题的关键.1年前查看全部
- 减压蒸馏装置适用于什么体系
 兰若诗的黄小咬1年前1
兰若诗的黄小咬1年前1 -
 不是uu 共回答了16个问题
不是uu 共回答了16个问题 |采纳率87.5%适用于升高温度会产生分解、结焦等等影响或危害到生产安全的变化.利用温度对沸点的影响,使用减压,使液体在较低的温度下就沸腾而蒸馏出来,不至于出现上述险情.1年前查看全部
- 减压蒸馏得到油状物如何重结晶油状物不溶于石油醚易溶于甲醇
 mxsy1年前1
mxsy1年前1 -
 蜗牛snailie 共回答了15个问题
蜗牛snailie 共回答了15个问题 |采纳率100%你的油状物恐怕也不是个纯组分,还要继续萃取精制,最后才进行重结晶一步.
萃取是关键,主要是选择好合适的溶剂,不同溶剂配合使用来达到提纯的目的.
这些过程可以看看《有机化学实验》中提取精制部分.1年前查看全部
- 增大反应物的量,什么时候用视为加压减压来分析,什么时候用增大浓度来分析平衡移动?
增大反应物的量,什么时候用视为加压减压来分析,什么时候用增大浓度来分析平衡移动?
例1:某恒温恒容的容器中,建立如下平衡:2no2(g) n2o4(g),在相同条件下,若分别向容器中通入一定量的no2气体或n2o4气体,重新达到平衡后,容器内n2o4的体积分数比原平衡时增大.
分析:反应达到平衡后,无论向密闭容器中加入还是n2o4气体,可视为加压,平衡都向右移动
问:这种恒容的情况为什么要变为加压来考虑,为什么不能用增大浓度来考虑呢?求分析!加n2o4气体,就是增大n2o4的浓度啊,平衡逆向移动)
如果是容积可变的情况,加入反应物为什么又可以用浓度来判断平衡移动的方向呢?如
某温度下,在一容积可变的容器中,反应2a(g)+b(g) 2c(g)达到平衡时,a、b和c的物质的量分别为4mol、2 mol和4 mol.保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是(2003年***理综) ( )
a.均减半 b.均加倍 c.均增加1 mol d.均减少1 mol
分析c 1mol的a和c只需要0.5mol的b及可平衡,现在加入了1mol.可以这样理解,先加入1mola、0.5molb、1molc,这时平衡,再加入0.5molb,所以向右.
这里再加0.5molb相当于增大反应物的浓度,所以平衡向右移动.为什么这里可以用浓度来分析?
恒温恒容 co(气) + h2o(气) ——co2 (气) + h2(气) 对于这个反应前后气体体积不变的,增加h2o(气) 就相当于增加反应物浓度,然后平衡向右移动了,这个有没有办法用增大压力来解释?378234300的解释:“1中空间和温度都恒定,所以增加了反应物的量,为了更好的存在,总的量就需要向着减少的方向变化,于是反应正向移动.2中空间可变,温度恒定,于是要想平衡正向移动,只需要多加点反应物,平衡就会正向移动了”
别的网友的解释 没有不良反应1年前1
没有不良反应1年前1 -
 断眉小妖精 共回答了10个问题
断眉小妖精 共回答了10个问题 |采纳率100%1中条件是恒温恒容,加入NO2,生成物浓度增加了,反应物浓度也增加了,但是反应物浓度增的比生成物多,所以平衡正向移动.
2中是恒温容积可变,就是压强不变.要使平衡正向移动,就需要增加反应物浓度.
A、B都是和原来一样,平衡不移动,等效平衡.
其实如果分不清状况就不要这样考虑,换种思维,资源的充分利用原理(我自己这么叫的)
1中空间和温度都恒定,所以增加了反应物的量,为了更好的存在,总的量就需要向着减少的方向变化,于是反应正向移动.
2中空间可变,温度恒定,于是要想平衡正向移动,只需要多加点反应物,平衡就会正向移动了1年前查看全部
- 将一定量的二氧化碳通入400ml、0.5mol/L的氢氧化钠溶液中,然后将产物在低温、减压条件下蒸干,得不含结晶水的固体
将一定量的二氧化碳通入400ml、0.5mol/L的氢氧化钠溶液中,然后将产物在低温、减压条件下蒸干,得不含结晶水的固体13.7g,试求通入二氧化碳气体的体积
是3.0688L吗 huadian1年前1
huadian1年前1 -
 天才胖子 共回答了15个问题
天才胖子 共回答了15个问题 |采纳率93.3%是高一的吧 我也是
用不能400ml、0.5mol/L的氢氧化钠那数据 有可能没反应完
用碳酸钠13.7g往前推1年前查看全部
- 关于减压蒸发本人有一液体物质需要蒸发,得其固体物质,但是本人没有冷凝管(一不小心打碎了)现在不考虑液体回收,我想直接用真
关于减压蒸发
本人有一液体物质需要蒸发,得其固体物质,但是本人没有冷凝管(一不小心打碎了)现在不考虑液体回收,我想直接用真空泵接在密封的烧瓶口,一边加温一边抽气,这样做能行吗?主要是液体中的物质,受到高温可能会改变其性质,所以一定要减压 zhaohaixia1年前1
zhaohaixia1年前1 -
 快乐天之使 共回答了22个问题
快乐天之使 共回答了22个问题 |采纳率90.9%这样做理论上可以,只是液体被抽到你的真空泵(如果是油泵的话)里面,可能对泵不好.
最好的情况:你的泵没事儿,但你的液体溶解在泵的泵油中,你得去换泵油.
如果你的泵是无油泵,那应该没事儿.但也不太好.1年前查看全部
- 傻傻的问个减压蒸馏的问题比如说:要蒸干【水,乙醇,丙酮】混合液中的乙醇,要怎么弄,需要减压吗;如果要蒸干X和水溶液中的X
傻傻的问个减压蒸馏的问题
比如说:要蒸干【水,乙醇,丙酮】混合液中的乙醇,要怎么弄,需要减压吗;如果要蒸干X和水溶液中的X【沸点150度】,要怎么调?是看沸点还是其他什么的?我是个文盲来的 cchn61年前2
cchn61年前2 -
 泥上舞 共回答了22个问题
泥上舞 共回答了22个问题 |采纳率95.5%前三个会不会有共沸呢?后面一个要看你是x还是除x了,要x旋蒸把水蒸掉,x留在烧瓶里;除x的话,水肯定被先蒸完了.1年前查看全部
- 将5.6g Fe投入浓硝酸溶液,产生红棕色气体A,把所得溶液减压蒸干,得到20g Fe(NO3)2和
将5.6g Fe投入浓硝酸溶液,产生红棕色气体A,把所得溶液减压蒸干,得到20g Fe(NO3)2和Fe(NO3)3的混合物,将该固体在高温下加热,得到红褐色的Fe2O3和气体B,A、B气体混合通入足量水中,在标准状况下剩余气体的体积为( )
A. 2240mL
B. 4480mL
C. 3360mL
D. 1120mL 小O树1年前1
小O树1年前1 -
 偌文 共回答了21个问题
偌文 共回答了21个问题 |采纳率90.5%解题思路:根据题意可知,红棕色气体为二氧化氮,即铁与浓硝酸反应时,铁失去电子,氮元素得到电子;在Fe(NO3)2和Fe(NO3)3的混合物,将该固体在高温下加热,得到红褐色的Fe2O3和气体B是亚铁失去电子,氮元素得电子;再A、B气体混合通入足量水中剩余气体一定为NO,则可利用得失电子守恒来计算NO的物质的量.因最后气体为NO,设其物质的量为x,
铁与浓硝酸反应时,铁失去电子,氮元素得到电子,且A为二氧化氮,
在Fe(NO3)2和Fe(NO3)3的混合物,将该固体在高温下加热,得到红褐色的Fe2O3和气体B,是亚铁失去电子,氮元素得电子,且B为氧气,
A、B气体混合通入足量水生成硝酸和NO,
根据守恒思想,计算时抓住反应的始终态即可,反应物可看作Fe、HNO3和水,最终生成物是Fe2O3和剩余气体,A和B混合气体通入水中,剩余气体是NO或O2,根据电子得失守恒可定性判断出剩余气体不可能是O2,则剩余气体只能是NO,设其物质的量为x,则整个过程中由得失电子守恒可知,
[5.6g/56g/mol]×(3-0)=x×(5-2),
解得x=0.1mol,
即标准状况下体积为0.1mol×22.4L/mol=2240mL,
故选A.点评:
本题考点: 有关混合物反应的计算.
考点点评: 本题较难,明确发生的化学反应,注意元素化合价的变化,明确最后的物质,利用电子守恒来快速计算是解答的关键,从而可避免中间过程的繁杂计算.1年前查看全部
- 为什么有减压分馏而不是增压分离
 金陵店小二1年前2
金陵店小二1年前2 -
 瑾儿11 共回答了17个问题
瑾儿11 共回答了17个问题 |采纳率88.2%在常压下,有些高沸点的成分需要很高的温度才能被蒸馏出来,但此时由于温度太高使得一部分成分发生炭化.这样就得不到这些成分而得到炭了.减压后这些成分的沸点下降,这样就能在它们发生炭化前而被蒸馏出来1年前查看全部
- 标准状况下2.24LCO2气体通入一定量NaOH溶液中(100mL)减压蒸干后得到9.5g固体则(1)得到的固体是什么
标准状况下2.24LCO2气体通入一定量NaOH溶液中(100mL)减压蒸干后得到9.5g固体则(1)得到的固体是什么
(2)NaOH溶液的物质的量浓度是多少? xx雨夜12341年前2
xx雨夜12341年前2 -
 s小石头 共回答了21个问题
s小石头 共回答了21个问题 |采纳率76.2%CO2~Na2CO3
22.4 106
2.24L 10.6g
CO2~NaHCO3
22.4 84
2.24L 8.4g
现在是9.5g所以是Na2CO3和NaHCO3的混合物
10.6 1.1
9.5
8.4 1.1
∴n(Na2CO3):n(NaHCO3)=1:1,由C元素守恒可知n(Na2CO3)=0.05mol,n(Na2CO3)=0.05mol,总共n(Na+)=0.15mol,所以c(NaOH)=1.5mol/L1年前查看全部
- H2O2溶液在减压蒸馏情况下,水的沸点会降低,H2O2的沸点会不会降低
 fangxiwen1年前3
fangxiwen1年前3 -
 人不学习要落后 共回答了11个问题
人不学习要落后 共回答了11个问题 |采纳率81.8%肯定也要相应降低的,没有任何疑问的,具体降低多少要根据真空度而定,压力和沸点的关系可以去查相关资料1年前查看全部
- 把CO2通入含NaOH0.8g的溶液中,将产物在减压的条件下蒸干后,得固体1.37g,则通入CO2的质量是( ).
把CO2通入含NaOH0.8g的溶液中,将产物在减压的条件下蒸干后,得固体1.37g,则通入CO2的质量是( ).
66g,但我不知道为什么, anhei1681年前2
anhei1681年前2 -
 fghthy45 共回答了15个问题
fghthy45 共回答了15个问题 |采纳率100%极限问题
第一种 全部NAOH 所得固体0.8g
第二种 全部NA2CO3 所得固体1.06g
第三种 全部NAHCO3 所得固体1.68g
可以知道1.37g是有NA2CO3和NAHCO3的混合物,列方程NA2CO3 x mol .NAHCO3 y mol
106x+84y=1.37
2x+y=0.02 x=0.005 mol y=0.01 mol
mC02=44*(0.005+0.01)=6.6g1年前查看全部
- 向300毫升氢氧化钾溶液中缓慢滴入一定量的二氧化碳气体,充分反应后,在减压低温下蒸发溶液,得到白色固体.若通入二氧化碳气
向300毫升氢氧化钾溶液中缓慢滴入一定量的二氧化碳气体,充分反应后,在减压低温下蒸发溶液,得到白色固体.若通入二氧化碳气体为2.24升(标准状况下),得到11.9克的白色固体.请通过计算确定此白色固体是由哪些物质组成的?其质量各为多少?所用的氢氧化钾溶液的物质的量浓度是多少?
 爱你没有永远1年前1
爱你没有永远1年前1 -
 还有吗 共回答了25个问题
还有吗 共回答了25个问题 |采纳率80%2KOH+ CO2 = K2CO3 + H2O
112g 1mol 39g
11.2g 0.1mol 3.9g
3.9g小于11.9g,说明co2不足量,也就是KOH有剩余
那白色粉末就是3.9gKCO3和8gKOH
w=(11.2g+8g)/56/0.3L约=1.14mol/L
11.2g+8g是KOH的质量,除以56(摩尔质量)就是KOH的物质的量,再除以0.3L就是物质的量浓度1年前查看全部
- 1立方1兆帕的空气,减压到0.1兆帕有多少个立方
1立方1兆帕的空气,减压到0.1兆帕有多少个立方
如果是10立方的话,那么1立方1兆帕的空气 减压到0.01兆帕是不是就有100个立方?依据是什么 从什么书上可以找到。谢谢!! skytianya1年前3
skytianya1年前3 -
 东邪老道 共回答了22个问题
东邪老道 共回答了22个问题 |采纳率86.4%这个根据公式得出的
P1V1/T1=P2V2/T2=C
因为等温变化(题目隐含条件),T1=T2所以P1V1=P2V2
代入数据
1兆帕*1立方=0.1兆帕*V2
得出V2=10立方1年前查看全部
- 将5.6克某固体投入HNO3中,产生红棕色气体A,把所得溶液减压蒸干,得到20克硝酸亚铁和硝酸铁的混合物;将该股题在隔绝
将5.6克某固体投入HNO3中,产生红棕色气体A,把所得溶液减压蒸干,得到20克硝酸亚铁和硝酸铁的混合物;将该股题在隔绝空气的条件下高温加热,得到红棕色的三氧化二铁和气体B,A、B气体混合后通入足量水中充分反应后,收集到标况下气体体积为(不考虑气体的溶解)( )
A.2240ml B.4480ml C.3360ml D.1120ml 冷冰霜931年前3
冷冰霜931年前3 -
 boyxinqing 共回答了24个问题
boyxinqing 共回答了24个问题 |采纳率95.8%5.6g 的 Fe 最后全变成三氧化二铁,Fe为+3价,也就是铁提供了0.3mol的电子,给谁?硝酸.最后一步A、B混合通入水中,反应,肯定生成了HNO3溶液,气体是NO.那么生成的气体NO应该是原来的HNO3的还原.N从+5将为+2,得到0.3mol的气体,就是有0.1mol的N被还原,生成NO 0.1mol,标况体积为2.24L,即2240mL.选择A
整个过程就是个元素守恒,不用管反应中具体每步发生了什么反应.N元素的过程就是由HNO3——硝酸亚铁、硝酸铁、红棕色气体A(就是NO2)——分解生成的是N的氧化物——与水反应变为HNO3和NO,也就是N元素开始时硝酸,最后有部分还是硝酸,部分还原成了NO,而被还原的这部分就是所有的Fe被氧化成+3价所提供的电子.就是一个电子守恒,元素守恒1年前查看全部
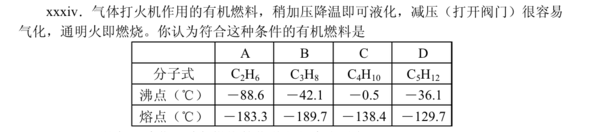
- 加压降温可液化,减压容易气化,通明火燃烧和沸点的关系.(如图)
加压降温可液化,减压容易气化,通明火燃烧和沸点的关系.(如图)
/> 爱的qq商1年前1
爱的qq商1年前1 -
 silmshafy 共回答了20个问题
silmshafy 共回答了20个问题 |采纳率90%丁烷,即为C4H10,它的沸点最高,容易加压液化,且需要的压强并不是很大,还有,它在常温常压下为气态,满足打火机的需要.希望能够帮助到您.1年前查看全部
- 减压可使液体沸点降低 ,why?
 木青哲1年前2
木青哲1年前2 -
 口袋小猪宝宝 共回答了17个问题
口袋小猪宝宝 共回答了17个问题 |采纳率82.4%我们平常说“水的沸点是100℃”,那是指在一个大气压下 (101.5Kpa)水沸腾时的温度.那么水的沸点是不是一成 不变呢?不是的.水的沸点是随大气压强的变化而变化的 :气压增大了,沸点就升高.因为水面上的大气压力,总 是...1年前查看全部
- 星三角,跟自耦减压启动原理图里面,交流接触器 KM1 闭合,三相都连通了,
星三角,跟自耦减压启动原理图里面,交流接触器 KM1 闭合,三相都连通了,


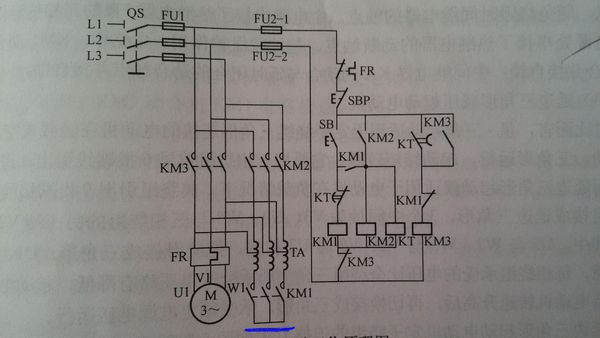
那这个自耦减压启动的KM1下面三相都短接了, GloomySnow1年前1
GloomySnow1年前1 -
 liyanhua6600 共回答了16个问题
liyanhua6600 共回答了16个问题 |采纳率87.5%自耦减压启动时,KM2和KM1接通状态、KM3断开状态,也就是自耦变压器是采用的星形接法,KM1短接的是中性点,理论上电流为零,所以,不存在短路的问题.与电机的星形接法一样的,只不过星形接法的电机是在电机的接线端子上短接的.1年前查看全部
- 一个化学反应生成物是1mol气体,生成了2mol气体,在恒温恒压条件下通入惰性气体,为什麽相当于减压?
 bangduozhen1年前2
bangduozhen1年前2 -
 ranse9999 共回答了18个问题
ranse9999 共回答了18个问题 |采纳率94.4%这是一个分压的概念,可以用浓度来理当总溶液增加了(加水),某溶质的质量分数会减小.加入其它物质气体,总体积增加了,分压就减小了.1年前查看全部
- 减压蒸馏跟恒温蒸馏有什么区别减压蒸馏跟恒温蒸馏的区别,如果物质溶易因温度的升高而蒸发,采用减压蒸馏控制沸点而使物质不易因
减压蒸馏跟恒温蒸馏有什么区别
减压蒸馏跟恒温蒸馏的区别,如果物质溶易因温度的升高而蒸发,采用减压蒸馏控制沸点而使物质不易因温度的问题而导致蒸发.那如果我们不采用减压装置,如真空泵之类,直接把温度控制在沸点之下有什么区别吗?我举个例子,如果物质易挥发,沸点在70.为了确保物质的蒸发,我们不采用减压,而是直接把加热套的温度设在70以下,这样跟减压蒸馏有区别吗 小P孩991年前2
小P孩991年前2 -
 樵夫住瓦屋 共回答了16个问题
樵夫住瓦屋 共回答了16个问题 |采纳率81.3%同意楼上的回答,减压蒸馏的目的是针对温度过高会变质的物质,以及常压下沸点较高的物质,比如DMF溶液,就需要水浴加热,减压蒸馏,因为温度太高,溶液里的东西容易变坏,和你的电热套设置没有什么关系!1年前查看全部
- 固液分离长采用减压过滤.为了防止倒吸,减压过滤完成后应先
 驭将1年前1
驭将1年前1 -
 wzhhluck 共回答了17个问题
wzhhluck 共回答了17个问题 |采纳率82.4%先恢复常压再关闭减压装置1年前查看全部
- 如何才能将过热蒸汽转化为饱和水2.5MPa、290度的过热蒸汽能通过减温减压至220度的饱和水吗?这时的压力有多大?
 忍不住伤心1年前1
忍不住伤心1年前1 -
 唐昕之 共回答了19个问题
唐昕之 共回答了19个问题 |采纳率78.9%根据热学知识点分析:pv=nRT去求得,我们这边前后的n(水的物质量是不变的).
你可以通过以上的知识点去试求一下.
有什么问题,可以接着提问1年前查看全部
- 自行把煤气瓶气阀减压会有什么后果?
 rdgs_wang1年前1
rdgs_wang1年前1 -
 孤独在人海 共回答了17个问题
孤独在人海 共回答了17个问题 |采纳率100%火会变小1年前查看全部
- 将11.2g Fe投入浓硝酸溶液,产生红棕色气体A,把所得溶液减压蒸干,得到40g Fe(NO3)2和Fe(NO3)3的
将11.2g Fe投入浓硝酸溶液,产生红棕色气体A,把所得溶液减压蒸干,得到40g Fe(NO3)2和Fe(NO3)3的混合物,将该固体在高温下加热,得到红褐色的Fe2O3和气体B,A、B气体混合通入足量水中,在标准状况下剩余气体的体积为 A.2240mL B.4480mL C.3360mL D.1120mL
 sdb00331年前1
sdb00331年前1 -
 mapleaflj 共回答了16个问题
mapleaflj 共回答了16个问题 |采纳率81.3%选B,
分析:写出各组反应:
①:Fe+6HNO3(浓)=Fe(NO3)3+3NO2↑+3H2O
②:Fe + 2Fe(NO3)3=3Fe(NO3)2……(因为溶液中有Fe(NO3)3,Fe完全反应)
③:4Fe(NO3)3 =高温= 2Fe2O3+ 12NO2↑ + 3O2↑
④:4Fe(NO3)2 =高温= 2Fe2O3+ 8NO2↑ + O2↑
通入足量的水的反应:
⑤:4NO2+O2+2H2O=4HNO3……(不管是A、B气体,NO2:O2都大于4:1,氧气不足量)
⑥:3NO2+H2O=NO+2HNO3
我们看一下由Fe到NO的过程:
总共有Fe0.2mol,设参加反应①的有amol,则参加反应②的有(0.2-a)mol,写在上面反应式:
①:Fe+6HNO3(浓)=Fe(NO3)3+3NO2↑+3H2O
a a 3a
②:Fe + 2Fe(NO3)3=3Fe(NO3)2
0.2-a 0.4-2a 0.6-3a
③:4Fe(NO3)3 =高温= 2Fe2O3+ 12NO2↑ + 3O2↑
a-( 0.4-2a)=3a-0.4 9a-1.2 9a/4-0.3
④:4Fe(NO3)2 =高温= 2Fe2O3+ 8NO2↑ + O2↑
0.6-3a 1.2-6a 0.15-3a /4
A、B气体共有NO2 :3a+(9a-1.2)+(1.2-6a)=6a,
有氧气(9a/4-0.3)+(0.15-3a /4)=1.5a-0.15
通入足量的水的反应:
⑤:4NO2 + O2 + 2H2O=4HNO3
4 1
x 1.5a-0.15
x=6a-0.6 剩下的NO2 为:6a-(6a-0.6)=0.6
⑥:3NO2+H2O=NO+2HNO3
3 1
0.6 y
y=0.2mol,标准状况选体积为0.2×22.4*1000=4480ml1年前查看全部
- 水在减压0.09Mpa下为热沸点会是多少度?如果加热套调到300度又是多少沸点
 s1767997551年前2
s1767997551年前2 -
 飞越梦想_vv 共回答了23个问题
飞越梦想_vv 共回答了23个问题 |采纳率91.3%加热套调节到300度并不是代表反应瓶内的温度就有300度,而且一般液体的沸点只与它的饱和蒸汽压有关,可以通过公式:PV=nRT(P表示压强、V表示气体体积、n表示物质的量、T表示绝对温度、R表示气体常数)求得.1年前查看全部
- 硝酸,氮氧化物的计算16.将5.6 g Fe投入热的浓硝酸,产生红棕色气体A,把所得溶液减压蒸干,得到20g Fe(NO
硝酸,氮氧化物的计算
16.将5.6 g Fe投入热的浓硝酸,产生红棕色气体A,把所得溶液减压蒸干,得到20g Fe(NO3)2和Fe(NO3)3的混合物,将该固体在高温下加热,得到红棕色的Fe2O3和混合气体B,A、B气体混合通入足量水中,在标准状况下剩余气体的体积为 ( )
A.2240mL B.4480mL C.3360mL D.1120mL
要详解 最好用守恒法 冷凝紫儿1年前2
冷凝紫儿1年前2 -
 mimilala 共回答了10个问题
mimilala 共回答了10个问题 |采纳率100%守恒法
5.6 g Fe =0.1mol----0.1mol +3价的Fe-----转移0.3mol电子
剩余气体不可能是O2 ,只能是 NO
产生1mol转移3mol电子,所以生成的NO为 0.1mol---选A.2240mL
( 5.6 g Fe最终全部变为+3价,HNO3最终转变为NO,然后利用电子守恒)1年前查看全部
- 向300mL KOH溶液中缓慢通入一定量的CO2气体,充分反应后,在减压低温下蒸发溶液,得到白色固体.请回答下
向300mL KOH溶液中缓慢通入一定量的CO2气体,充分反应后,在减压低温下蒸发溶液,得到白色固体.请回答下列问题:
(1)由于CO2通入量不同,所得到的白色固体的组成也不同,试推断有几种可能的组成,并分别列出.
(2)若通入CO2气体为2.24L(标准状况下),得到11.9g的白色团体.请通过计算确定此白色固体是由哪些物质组成的?其质量各为多少?所用的KOH溶液的物质的量浓度为多少. vvwsnb1年前2
vvwsnb1年前2 -
 weiniduzun 共回答了21个问题
weiniduzun 共回答了21个问题 |采纳率85.7%解题思路:(1)KOH过量,溶液中有KOH,也有K2CO3;CO2过量,溶液中可能全都是KHCO3或KHCO3和K2CO3的混合物
(2)首先根据反应物的质量计算反应物的成分,根据化学方程式列方程计算.(1)本题涉及的反应有:CO2+2KOH=K2CO3+H2O,CO2+KOH=KHCO3,
由方程式可知,反应分四个阶段进行:
①CO2通入量较少时主要得到K2CO3并有过量的KOH;
②当KOH恰巧完全反应,只存在生成物K2CO3;
③继续通入CO2时,开始有KHCO3生成;
④通入的CO2使K2CO3全部转化成KHCO3.
所以有四种组合,分别是:①K2CO3+KOH②K2CO3③K2CO3+KHCO3④KHCO3;
答:可能的组成有:①K2CO3+KOH②K2CO3③K2CO3+KHCO3④KHCO3;
(2)由:①CO2+2KOH=K2CO3+H2O②CO2+KOH=KHCO3
2.24L(标态)CO2气体的物质的量为0.100mol,
由碳元素守恒可知:0.1 molCO2既能生成0.1mpl的K2CO3,即13.8g;也可生成0.1mol的KHCO3,即10.0g,
∵13.8g>11.9g>10.0g
∴得到的白色固体是 K2CO3和KHCO3的混合物.
设白色固体中K2CO3 x mol,KHCO3 y mol,即
①CO2+2KOH=K2CO3+H2O
②CO2+KOH=KHCO3
x mol+y mol=[2.24L/22.4L/mol]=0.100 mol,
138g•mol-1×x mol+100 g•mol-1×y mol=11.9g
解此方程组,得
x=0.0500mol(K2CO3)
y=0.0500mol(KHCO3)
∴白色固体中,K2CO3 质量为138g•mol-1 ×0.0500mol=6.90g
KHCO3质量为100 g•mol-1×0.0500mol=5.00g
消耗KOH物质的量为 2xmol+ymol=2×0.0500mol+0.0500mol=0.150mol
∴所用KOH溶液物质的量浓度为 0.150mol/0.300L=0.500 mol•L-1
答:K2CO3 质量为:6.9g,KHCO3质量为:5.0g,KOH溶液物质的量浓度为:0.5mol•L-1点评:
本题考点: 有关范围讨论题的计算.
考点点评: 本题考查混合物的计算,题目难度角度,注意把握物质的性质,判断反应的可能性以及反应的程度,根据方程式列方程计算.1年前查看全部
- 热过滤属于减压过滤还是常压过滤,为什么
 武林大会1年前2
武林大会1年前2 -
 办公室比尔 共回答了14个问题
办公室比尔 共回答了14个问题 |采纳率78.6%属于常压过滤
热过滤就是在普通过滤器外套上一个热滤漏斗,
某些热的浓溶液,过滤时,由于温度降低,晶体很容易在滤纸上析出,这将使滤出的固体杂质与晶体相混,因此该种溶液就需在保温的情况下进行过滤,即热过滤.
1.热过滤装置的准备:
热滤漏斗是铜制的,具有夹层和侧管.夹层内盛水,漏斗上沿有一注水口,侧管处用于加热.
热滤漏斗内的玻璃漏斗其大小应与热滤漏斗相匹配,且应为短颈(比热滤漏斗的底端稍长).
2.过滤操作:
(1)从注水口处向热滤漏斗夹层中注水,水不可盛得过满,以防水沸腾时溢出.
(2)将过滤器准备好后,开始加热漏斗侧管,使漏斗内的水温达到要求.过滤前还应把玻璃漏斗在水浴上用蒸气加热一下.
(3)过滤过程中若有结晶析出,应待过滤结束,将滤纸上的晶体再用溶剂溶解,然后用新滤纸重新过滤.
过滤的注意事项
(1)常压过滤时,如果滤纸和漏斗的隔层和漏斗管里有气泡或者漏斗管口(斜面背后)没有贴紧烧杯壁,就会使过滤受到空气的阻力而减慢.
(2)在热过滤时,要经常向保温漏斗中添加热水.
(3)抽滤的关键在于控制水的流量,开始时如果水的流速过大,会使滤纸穿孔.当固体物质增厚时,如果水的流速过小,将使抽滤速率减小.1年前查看全部
- 0.5Mpa/m3的空气在减压到0.1Mpa时是多少立方米
 angie_babe1年前1
angie_babe1年前1 -
 jinyan090304 共回答了22个问题
jinyan090304 共回答了22个问题 |采纳率68.2%根据等温状态理想气体状态方程,P1*V1=P2*V2,减压后的体积为V2=0.5*1/0.1=5立方米1年前查看全部
大家在问
- 1把四个表面积都是12平方厘米的正方体木块拼成一个长方体,这个长方体的表面积是多少?
- 2在三角形ABC中,AD平分角BAC,E`F分别为AB`AC上的点,且角EDF+角EAF=180°求:DE=DF
- 3ATP的来源是什么能不能说细胞呼吸是ATP的全部来源?为什么?尽可能详细一点,
- 4观察下图,(1)请你找出a.b.d之间的关系,用等式表示它们之间的关系
- 5这里第五小题自然加倍和花药壁培养是什么意思呀?自然加倍难道不是将二倍体自然加倍到四倍体吗?花药壁培养是不是产生的基因一定
- 6不需要化学就表现出来的性质这句话是什么意思?
- 7用括号中动词的适当形式填空.不限词数
- 839.5-(18+36.5)x0.32用简便方法怎样算
- 9高数 向量 空间直角坐标系点M(4,-3,5)到各坐标轴的距离
- 10改变滑片P的位置,使电压表、电流表指针偏离零刻度线的角度恰好相同这句花什么意思
- 11like the game (call)“cats catch mice”very much.那个(call)是填cal
- 12mom,i'd like to lie on the grass and have a rest 单选
- 13一个好朋友应该在学业上有所帮助 翻译成英语
- 14麻烦在线的网友帮个忙,对了给悬赏分5/10
- 15把1时15分,1又15/1,115分按时间长短排短排列.从长到短
