硫离子和亚硫酸根离子能不能共存?
 毛毛10212022-10-04 11:39:541条回答
毛毛10212022-10-04 11:39:541条回答
硫离子和亚硫酸根离子能不能共存?
我知道,这在酸性条件下,一定是不能的了
但是在碱性条件下,还有没有氧化还原反应呢?
我知道,这在酸性条件下,一定是不能的了
但是在碱性条件下,还有没有氧化还原反应呢?

已提交,审核后显示!提交回复
共1条回复
 kathy_wong 共回答了16个问题
kathy_wong 共回答了16个问题 |采纳率93.8%- 碱性可以共存的
S与NAOH反应后产物不就是在碱性条件下共存了 - 1年前
相关推荐
- 氢硫酸溶液中通入氯气的离子方程式,为什么不是硫离子和氯气反应生成单质硫(沉淀)和氯离子?
 flywmf1年前3
flywmf1年前3 -
 mellansky 共回答了23个问题
mellansky 共回答了23个问题 |采纳率95.7%因为氢硫酸是弱电解质,不能完全电离.所以不能写成硫离子.
正确的应是:
H₂S + Cl₂==== 2H+ + Cl- + S↓1年前查看全部
- 碳,氮,氧,钠,铝,硫离子,镉,铜的电子排布式是什么
 乖乖女20061年前1
乖乖女20061年前1 -
 我的雨雪 共回答了19个问题
我的雨雪 共回答了19个问题 |采纳率78.9%碳1s*2,2s*2,2p*2氮1s*2;2s*2;2p*3 氧1s*2;2s*2;2p*4 钠1s*2;2s*2;2p*6;3s*1铝1s*2;2s*2;2p*6;3s*2;3p*1 离1s*2;2s*2,2p*6.3s*13p*31年前查看全部
- 2价铁离子和硫离子的方程式
 教我如何不爱他1年前1
教我如何不爱他1年前1 -
 纯玉米 共回答了19个问题
纯玉米 共回答了19个问题 |采纳率100%Fe(2+)+S(2-)===FeS沉淀1年前查看全部
- 在银离子中依次加入碘离子,二价硫离子,氨水,氰根哪个的氧化性最强?
 小古哥1年前3
小古哥1年前3 -
 StarbuckNO_1 共回答了15个问题
StarbuckNO_1 共回答了15个问题 |采纳率86.7%碘离子,二价硫离子,氨水,氰根在此与银离子反应,不是发生氧化还原反应,不存在氧化性强弱的问题.银离子与碘离子和二价硫离子可生成AgI和Ag2S沉淀,而与氨水、氰根可分别生成[Ag(NH3)2]+及[Ag(CN)2]-络离子,我想出题的本意是问银离子与哪个最容易发生反应吧.
1.先比较碘离子和二价硫离子.AgI的Ksp=8.3*10^-17(10的-17次方),Ag2S的Ksp=6*10^-50,显然Ag2S的溶解度比AgI小得多,因此Ag+优先与S2-反应.
2.再比较氨水和氰根.[Ag(NH3)2]+的K稳=10^7.40(10的7.40次方),[Ag(CN)2]-的K稳=10^21.1(10的21.1次方),很明显[Ag(CN)2]-更易生成,因此Ag+优先与CN-络合.
3.最后比较S2-与CN-.形成Ag2S沉淀的常数K=1/Ksp=1.7*10^49比形成[Ag(CN)2]-的K稳=10^21.1大得多,所以S2-更易与Ag+反应.1年前查看全部
- 硫化钠溶液与氯化铁溶液反应离子方程式是什么?2氯离子+3硫离子=Fe2S3 请问哪里错了?
 最喜欢阳春三月1年前1
最喜欢阳春三月1年前1 -
 zpc533 共回答了19个问题
zpc533 共回答了19个问题 |采纳率89.5%应该说Fe3+可以氧化S2-,先考虑2Fe3+ + S2- =======S(沉淀)+2Fe2+
但是也会有Fe2S3沉淀的存在.
一般说来,Fe3+具有较强的氧化性,而S2-则具有还原性,因此当Fe3+与S2-相遇时,Fe3+能将S2-氧化成S,而自身被还原为Fe2+,即发生反应:
2Fe3++S2-=2Fe2++S↓
Fe3+在酸性条件下,其氧化性要比在碱性条件下强.在FeCl3溶液中加入Na2S,此时Fe3+过量,溶液呈酸性.因此,应发生上述反应.但如果反过来,将FeCl3加入Na2S溶液,Na2S过量,溶液呈碱性,此时Fe3+氧化性减弱.Fe3+和S2-会结合成溶解度极小的Fe2S3沉淀,即:
2Fe3++3S2-=Fe2S3↓
总之哪个过量对反应也是有影响的,因为FeCl3酸性,而Na2S是碱性的1年前查看全部
- 硫离子与硫酸根离为什么可以共存,
 cornerhk1年前7
cornerhk1年前7 -
 mxy821110 共回答了16个问题
mxy821110 共回答了16个问题 |采纳率87.5%你是高中生吧.
硫酸根中固然有六价硫,硫离子中固有负二价硫,他们可以在一定条件下发生归中反应.但是在一般的情况下(比如你说的条件)他们是不会发生归中反应的.(就像碳和二氧化碳常温下不反应,在高温下归中反应生成一氧化碳一样.)
硫酸根在碱性,中性和弱酸性时的氧化性都不强.都不可以氧化硫离子.即不可以与硫离子发生归中反应.在浓硫酸时之所以氧化性变强,是因为此时硫酸分子不完全电离,硫酸分子的氧化性很强的缘故.
回到你的问题.硫离子要与硫酸根共存.必须要保持碱性的状态.
因为在中性或者一般酸性的状态时,硫离子与氢离子生成硫化氢气体跑掉.(所以一楼的反应式是错的.酸性时发生的反应是S2- + 2H+=H2S)
浓硫酸时 会和硫离子发生归中反应生成硫或者二氧化硫.
碱性时(也是硫离子和硫酸根能共存的环境),硫酸根一般不具有氧化性.不会发生归中反应.
鉴于楼主知识还不够.等你学了电化学,甚至有机会学习大学无机化学之后,或许会有一些更加深刻的认识.1年前查看全部
- 为何钠离子 -2价硫离子 氢氧根离子 硫酸根离子不能共存 写出离子方程式
为何钠离子 -2价硫离子 氢氧根离子 硫酸根离子不能共存 写出离子方程式
在足量co2通入的水溶液中 岸芷M1年前5
岸芷M1年前5 -
 神奇乖乖 共回答了27个问题
神奇乖乖 共回答了27个问题 |采纳率88.9%二氧化碳通入水中与氢氧根反应,除去氢氧根,溶液呈酸性.酸性条件下,-2价硫离子会与硫酸根离子发生归中反应产生二氧化硫.CO2(足量) + H2O =H2CO3
H2CO3 + 2OH- = 2HCO3- S2- + 3(SO4) 2- + 8(H+) = 4SO2 + 4H2O1年前查看全部
- 关于化学(离子反应及物质的量)1.钾离子,钠离子,亚硫酸根离子,硫离子在强酸还是强碱中不能共存?(最好再举几个不能与亚硫
关于化学(离子反应及物质的量)
1.钾离子,钠离子,亚硫酸根离子,硫离子在强酸还是强碱中不能共存?
(最好再举几个不能与亚硫酸根离子或硫离子共存的离子)
2.标况下,100毫升氢硫酸溶液中通入二氧化硫气体,PH先增大后减小,当通入112毫升,PH=7,求原来氢硫酸溶液的物质的量浓度是多少?
3(百思不解)“标况下,46克二氧化氮气体中含有1摩尔的物质的量”这个命题为什么错误?
急!
打错了 问题3。“含1摩尔的分子数” 飞雪流痕1年前3
飞雪流痕1年前3 -
 ljzaity 共回答了14个问题
ljzaity 共回答了14个问题 |采纳率100%1、由于反应:2S 2- + SO3 2- + 6H+ = 3S + 3H2O 所以,酸性溶液中不能共存.
2、反应为:2H2S + SO2 = 3S + 2H2O,随着二氧化硫气体的通入,上述反应逐渐完全,所以pH增大,恰好反应时pH=7,继续通入,则变为亚硫酸溶液,所以pH又减小.112mLSO2是0.005mol,则H2S是0.01mol,浓度是0.1mol/L.
3、因为平衡2NO2=可逆符号=N2O4的存在,导致46克“二氧化氮气体”中含1摩尔的分子就错了,小于1mol.1年前查看全部
- 求 S 和 NaOH H2S 和O2 亚硫酸根离子和氢离子 硫离子和氢离子 的 过量与少量反应
 倪若1年前1
倪若1年前1 -
 lgz88 共回答了19个问题
lgz88 共回答了19个问题 |采纳率94.7%3S + 6NaOH -----> 2Na2S + Na2SO3 + 3H2O
2H2S + O2 -----> 2H2O + 2S
2H2S + 3O2 -----> 2H2O + 2SO2
SO32- + H+ -----> HSO3-
SO32- + 2H+ -----> H2SO3
S2- + H+ -----> HS-
S2- + 2H+ -----> H2S1年前查看全部
- 氢离子 硫离子,亚硫酸根离子为什么不能共存...
 why1233211年前3
why1233211年前3 -
 三分贱醉 共回答了16个问题
三分贱醉 共回答了16个问题 |采纳率81.3%氢离子与(弱酸酸式根)是不能共存的 因为两者能结合生成弱酸,即两者发生了化学反应所以不能共存.2H+ +S2- = H2S H+ + SO32-= H2SO31年前查看全部
- 氢硫酸溶液中,c(氢离子)=2c(硫离子).这个说法正确吗
 还是叫蚂蚁1年前1
还是叫蚂蚁1年前1 -
 woxinyongheng1 共回答了18个问题
woxinyongheng1 共回答了18个问题 |采纳率77.8%不正确.氢硫酸是弱酸,不能完全电离、.1年前查看全部
- 为什么在水溶液中氢离子与硫离子、硫酸氢根离子、亚硫酸根离子不能共存?
 紫苏12311年前1
紫苏12311年前1 -
 zzualu 共回答了19个问题
zzualu 共回答了19个问题 |采纳率84.2%因为H离子可以和它们发生复分解反应
H++S2-=H2S 生成气体H2S
H++SO32-=SO2+H2O 生成气体SO21年前查看全部
- 负2价硫离子不能和哪些离子在溶液中共存如果共存的话会生成什么?沉淀还是气体?氢离子呢?
负2价硫离子不能和哪些离子在溶液中共存如果共存的话会生成什么?沉淀还是气体?氢离子呢?
对硫离子和氢离子分别说明. 莉莉的宝宝1年前2
莉莉的宝宝1年前2 -
 liulu8866 共回答了17个问题
liulu8866 共回答了17个问题 |采纳率76.5%硫离子:和大多数金属离子都会硫化物沉淀
和Na,K,NH4+共存
和Al3+发生双水解反应,生成氢氧化铝和硫化氢
和氢离子产生硫化氢气体
和强氧化性的离子发生氧化还原反应,生成硫沉淀,甚至是硫酸根
氢离子:和OH-生成水
和碳酸根生成二氧化碳
和硫离子生成硫化氢气体
和弱酸根都不能共存,太多了
和偏铝酸根产生沉淀,氢离子过量则沉淀再次溶解,这个比较特殊,说一下
和硅酸根产生沉淀1年前查看全部
- 硫离子和氯离子的结构与氩原子是一样的,为什么离子半径还不一样呢?
硫离子和氯离子的结构与氩原子是一样的,为什么离子半径还不一样呢?
有条规律是,结构相同的离子,价越低,半径越大. ywjingxuan1年前2
ywjingxuan1年前2 -
 faky 共回答了18个问题
faky 共回答了18个问题 |采纳率83.3%所谓结构是指外层的电子结构
但是原子核内的核电荷数是不一样的,硫为16个,氯为17个,同周期的元素核电荷数越多,对外层电子的引力越大,半径越小.
所以,结构相同的离子,价越低,核电荷数越小,引力越小,半径自然越大.1年前查看全部
- 硫离子和亚硫酸根为什么在pH=1时才沉淀
 沙漠里的半瓶水1年前2
沙漠里的半瓶水1年前2 -
 四季窝 共回答了13个问题
四季窝 共回答了13个问题 |采纳率92.3%2S2- + SO3^2- + 6H+ = 3S + 3H2O
pH值太高时,H+少,不反应
(1)S2-和SO3^2-在碱性介质中能共存,在酸性价质中不能共存.
因为酸性介质中S2-和SO3^2-分别会发生如下反应:S2-+2H+=H2S,SO32-+2H+=SO2+H2O,生成的H2S和SO2会继续发生反应:2H2S+SO2=3S+2H2O.
所以酸性介质中S2-和SO3^2-会发生总反应式为:2S2- + SO3^2- + 6H+ = 3S + 3H2O.
而在碱性介质中能共存可从另一反应明白:3S + 6NaOH =(加热)2Na2S+Na2SO3+3H2O
(2)久置的H2S与O2发生反应:2H2S+O2=2H2O+2S;
Na2SO3也会被O2氧化:2Na2SO3+O2=2Na2SO41年前查看全部
- 硫化氢与硫离子反应机理为什么硫化氢与硫离子生成硫氢根离子?是因为硫离子破坏了电离平衡吗?
 告诉天蝎1年前1
告诉天蝎1年前1 -
 新打狗棒 共回答了17个问题
新打狗棒 共回答了17个问题 |采纳率88.2%H₂S+S²- ==2HS-
这个可以理解为较强酸制取较弱酸,H₂S与HS-比是较强的酸,所以反应能够发生1年前查看全部
- 下列表达式错误的是( ) A.甲基的电子式: B.碳原子的价电子轨道表示式: C.硫离子的核外电子排布式:1s 2 2
下列表达式错误的是()
A.甲基的电子式: 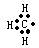
B.碳原子的价电子轨道表示式: 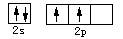
C.硫离子的核外电子排布式:1s 2 2s 2 2p 6 D.碳-14原子:14 6C  jp_yin1年前1
jp_yin1年前1 -
 c7tc 共回答了26个问题
c7tc 共回答了26个问题 |采纳率100%C
1年前查看全部
- 钠离子和硫离子和镁离子的化学式是什么
 永恒10月13号1年前4
永恒10月13号1年前4 -
 344217574 共回答了19个问题
344217574 共回答了19个问题 |采纳率94.7%Na+,S2-,Mg2+1年前查看全部
- 用化学式或化学符号表示:(1)一个氧分子______;(2)一个硫离子______;(3)氮元素______;(4)在水
用化学式或化学符号表示:
(1)一个氧分子______;
(2)一个硫离子______;
(3)氮元素______;
(4)在水分子中氧元素的化合价为-2价H2−2 O H2.−2 O  k4e6mmx1年前1
k4e6mmx1年前1 -
 蝴蝶sun 共回答了14个问题
蝴蝶sun 共回答了14个问题 |采纳率92.9%解题思路:本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目.(1)由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则一个氧分子可表示为:O2.
(2)由离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略;一个硫离子可表示为:S2-.
(3)氮元素可以用氮的元素符号表示,故答案为:N;
(4)元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,所以在水分子中氧元素的化合价为-2价,故可表示为:H2
−2
O;
故答案为:(1)O2(2)S2-(3)N(4)H2
−2
O;点评:
本题考点: 化学符号及其周围数字的意义.
考点点评: 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.1年前查看全部
- 三价铁离子与硫离子在水溶液中是否能大量共存?
三价铁离子与硫离子在水溶液中是否能大量共存?
最好告诉我实验准确结果或者科学的理论根据.问题来自一名化学奥赛考生. 今天是0801011年前1
今天是0801011年前1 -
 恋莹 共回答了20个问题
恋莹 共回答了20个问题 |采纳率80%三价铁离子存在的环境显然是强酸环境,这时电对S/H2S标准电极电势是+0.141V,而电对Fe3+/Fe2+标准电极电势为+0.771V超过前一电对,因而可以将其氧化;更进一步的,反应会造成难溶的硫生成,这会增加体系的熵,也会有利于反应的进行 ^_^
PS:楼主也是做化学竞赛嗒?加油!祝功成名就!了却君王天下事,赢得身前身后名! ^_^1年前查看全部
- 硫代硫酸根与硫离子能否共存RT,原因
 陈飒aa1年前1
陈飒aa1年前1 -
 joey_zeng 共回答了15个问题
joey_zeng 共回答了15个问题 |采纳率73.3%在碱性环境中可以大量共存;但在酸性环境中不能大量共存,方程式为:
S2O32-+2S2-+6H+=3S↓+3H2O
原因:碱性环境中H+浓度太小,不能结合S2O32-中的O.1年前查看全部
- 亚硫酸氢根和硫离子能否共存
 lynn1131年前2
lynn1131年前2 -
 不爱学习的家伙 共回答了23个问题
不爱学习的家伙 共回答了23个问题 |采纳率91.3%不能,亚硫氢酸根离子显氧化性,硫离子显还原性,会发生氧化还原反应,生成单质硫
HSO3- + 2S2- + 5H+ = 3S↓ + 3H2O1年前查看全部
- 硫离子与亚硫酸根共存,而次氯酸根与亚硫酸根不共存
硫离子与亚硫酸根共存,而次氯酸根与亚硫酸根不共存
为什么呢?老师讲说硫离子与亚硫酸根共存是因为两个盐为什么不共存呢?只有在酸性条件下才反应而不共存,那为什么次氯酸根与亚硫酸根又不共存了呢?它不是两个盐吗?如果说他是因为能发生氧化还原反应,那为什么第一个又不行呢? cupit_0_01年前1
cupit_0_01年前1 -
 三千楚地 共回答了23个问题
三千楚地 共回答了23个问题 |采纳率91.3%亚硫酸根离子在碱性环境下氧化性非常弱,不能氧化硫离子,所以二者在碱性环境下可以共存
(相反的,单质硫在碱性环境下加热或长期放置会歧化成硫离子和亚硫酸根离子).
而次氯酸根离子即使在碱性环境下也具有比较强的氧化性,能氧化亚硫酸根离子,所以二者即使在碱性环境下也不能共存.1年前查看全部
- 在碱性溶液中,硫离子与亚硫酸根离子是否可以共存?
在碱性溶液中,硫离子与亚硫酸根离子是否可以共存?
在碱性溶液中,硫离子与亚硫酸根离子可以共存吗?额,在酸性溶液中呢? 卉hui1年前1
卉hui1年前1 -
 mimikitty 共回答了22个问题
mimikitty 共回答了22个问题 |采纳率95.5%不论在什么条件下都不行,会归宗成单质硫1年前查看全部
- 亚铁离子和硫离子反应的化学方程式怎么写?
 宝贝不说话1年前4
宝贝不说话1年前4 -
 l95447 共回答了24个问题
l95447 共回答了24个问题 |采纳率91.7%Fe2+ + S2-=========FeS(沉淀)
硫化亚铁沉淀可溶于强酸1年前查看全部
- 下面哪组离子能共存碳酸根、钠离子、硫离子、硝酸根、氢氧根 另一组:铵根、钡离子、偏铝酸根、硝酸根和三价铁
 婉鸿1年前1
婉鸿1年前1 -
 情迷梦露3 共回答了14个问题
情迷梦露3 共回答了14个问题 |采纳率92.9%第一组可以共存.碱性环境中,硝酸根不能把硫离子氧化.
第二组不能共存.铁离子,铵根离子都应存在于酸性化境(水解),偏铝酸根离子应存在于碱性环境,两者发生双水解不能大量共存.
请参考.1年前查看全部
- 用数字和符号表示 2个氢离子 3个硫离子 3个铵根离子 2个氮分子 +5价氯元素 3个水分子
 13apple1年前4
13apple1年前4 -
 为你走tt 共回答了22个问题
为你走tt 共回答了22个问题 |采纳率86.4%2个氢离子:2H +
3个硫离子:3S 2-
3个铵根离子:3NH4 +
2个氮分子:2N2
+5价氯元素:+5
Cl
3个水分子:3H2O1年前查看全部
- 钡离子,硫离子,氯离子,硫酸根离子能否在强碱溶液中共存?
 jessie1711年前1
jessie1711年前1 -
 唯物xx者FND 共回答了21个问题
唯物xx者FND 共回答了21个问题 |采纳率81%不能 Ba2+与(SO4)2-不能共存
就算没有(SO4)2- 在碱性溶液里 Ba2+也不能存在 因为会生成Ba(OH)2沉淀1年前查看全部
- 请问在酸性条件下硫酸根和硫离子可以共存吗?
请问在酸性条件下硫酸根和硫离子可以共存吗?
是硫酸根不是亚硫酸根,而且是在稀溶液的情况下,它们可以共存吗?请来个肯定一点的回答…… 自己也不清楚的就算了…… cjz20021年前8
cjz20021年前8 -
 020sj 共回答了19个问题
020sj 共回答了19个问题 |采纳率94.7%可以!非常确定!
碱性条件下,共存,没问题
酸性条件不行,S2-与H+反应了,不过没有SO42-什么事.
只有浓硫酸才能氧化S2-得到S或SO21年前查看全部
- 硫化钠和亚硫酸钠为什么要共存?硫离子不是负二价,而亚硫酸钠中硫又是正四价,两者应该发生归中反应,生成硫单质吗?为什么它们
硫化钠和亚硫酸钠为什么要共存?
硫离子不是负二价,而亚硫酸钠中硫又是正四价,两者应该发生归中反应,生成硫单质吗?为什么它们不反应,而要共存呢?
但是为什么必须要在酸性条件下才可以呢?
那么,硫化氢和亚硫酸钠共存吗? nkkn20001年前2
nkkn20001年前2 -
 shi0897 共回答了18个问题
shi0897 共回答了18个问题 |采纳率88.9%四价硫只有在酸性条件下才有氧化性,能斯特方程是大学中学到的,见无机化学,硫化氢和亚硫酸钠能反应生成S沉淀,硫化氢电离出H离子,使溶液成酸性1年前查看全部
- 如何比较硫离子、氯离子、溴离子、碘离子的极化能力(变形能力)大小?
 英文911年前1
英文911年前1 -
 313448801 共回答了20个问题
313448801 共回答了20个问题 |采纳率80%离子极化作用的规律:1.正离子电荷越高,半径越小,离子势φ(Z / r)越大,则极化作用越强;2.在相同离子电荷和半径相近的情况下,不同电子构型的正离子极化作用不同:8电子构型 < 9-17电子构型 < (18,18+2) 电子构...1年前查看全部
- 写离子符号:氢离子 硫酸根离子 碳酸根离子 钠离子 硫离子
 如歌的行板11年前0
如歌的行板11年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 稀硫酸和硫离子反应方程式?
 wumhi1年前2
wumhi1年前2 -
 sucai980333 共回答了23个问题
sucai980333 共回答了23个问题 |采纳率87%2H++S2-====H2S,H2SO4稀的时候没有氧化性1年前查看全部
- 化学,向硫化氢溶液中加入硫酸铜溶液,为什么硫离子的浓度会减少?
 zhouyifei1年前2
zhouyifei1年前2 -
 x80bzr 共回答了28个问题
x80bzr 共回答了28个问题 |采纳率89.3%发生反应H2S + CuSO4 == CuS↓ + H2SO4 ,生成了更难电离的CuS沉淀,故硫离子浓度减小1年前查看全部
- 硫化氢溶液中,在采取错施使pH增大的时候,则j硫离子的溶度的变化情况
 无限期的等待1年前3
无限期的等待1年前3 -
 fsdagou 共回答了20个问题
fsdagou 共回答了20个问题 |采纳率100%在碱性溶液中提高PH值,需要加大OH的量,若加入氨水,则氨的浓度加大,如NH3·H2O=NH4++OH-,根据化学平衡移动规律,增大PH,即增加OH-离子浓度,1年前查看全部
- 硫离子的核外电子数和电子数是多少
 ltchu1年前5
ltchu1年前5 -
 雪碧30 共回答了20个问题
雪碧30 共回答了20个问题 |采纳率95%硫离子核外电子结构式(因为不方便所以省略了弧线):(2,8,8)2- 核外电子数是2+8+8=18,最外层电子数8
硫还有两种离子(2,8,2)4+ 核外电子数12
(2,8) 核外电子数101年前查看全部
- 怎么判断化学式是原子还是离子比如:2S2-前面的2表示的是有2个硫离子后面的2表示的是硫离子带2个负电荷.你怎么判断S会
怎么判断化学式是原子还是离子
比如:2S2-
前面的2表示的是有2个硫离子
后面的2表示的是硫离子带2个负电荷.
你怎么判断S会是离子?
初中马上要学了,先预习一下,多多指教! lili062181年前3
lili062181年前3 -
 漠木清痕 共回答了26个问题
漠木清痕 共回答了26个问题 |采纳率96.2%在化学式的右上角有X-或X 的都是离子.(X是常数)1年前查看全部
- 一个硫离子带的电荷数
 瞌睡鬼1年前3
瞌睡鬼1年前3 -
 oo凤凰 共回答了18个问题
oo凤凰 共回答了18个问题 |采纳率83.3%硫离子就是:S2-(+4、+6价硫不形成简单离子),所以电荷数为-21年前查看全部
- 硫离子和亚硫酸根离子的氧化性比较
 wjq0508021年前3
wjq0508021年前3 -
 晨曦花雨 共回答了14个问题
晨曦花雨 共回答了14个问题 |采纳率85.7%SO32- 大于S2-,S2-离子没有氧化性,已经是最低价了只能做还原剂
酸性溶液中SO32-能把S2-氧化成S1年前查看全部
- (10贵港15)(4分)请用化学符号填空:2个氢原子______;3个二氧化氮分子______;带两个单位负电荷的硫离子
(10贵港15)(4分)请用化学符号填空:2个氢原子______;3个二氧化氮分子______;带两个单位负电荷的硫离子______;镁单质______。
 bnap0011年前1
bnap0011年前1 -
 長大了麼 共回答了12个问题
長大了麼 共回答了12个问题 |采纳率91.7%2H 3NO 2 S 2- Mg
元素或原子用元素符号来表示,氢原子用氢元素符号来表示,即H;
表示粒子个数的数字写在化学符号的前面,因此2个氢原子表示为2H.
表示化学式中原子或原子团个数的数字写在元素符号或原子团符号的右下角,1个二氧化氮分子含有1个氮原子和2个氧原子,因此1个二氧化氮分子表示为NO 2 ;
表示粒子个数的数字写在化学符号的前面,因此3个二氧化氮分子表示为3NO 2 .
表示离子所带电荷数的数字写在元素符号或原子团符号的右上角,且数字在前,正、负号在后.数字是“1”时省略,因此带两个单位负电荷的硫离子表示为S 2- .
金属单质的化学式用元素符号表示,因此镁单质表示为Mg.
故答案为:
2H;3NO 2 ;S 2- ;Mg.1年前查看全部
- 分别把溶液中含有的氯离子,碳酸根,负二价硫离子依次沉淀出来,加入试剂的正确顺序是
分别把溶液中含有的氯离子,碳酸根,负二价硫离子依次沉淀出来,加入试剂的正确顺序是
A.Cu2+,Ag+,Ba2+ B.Ba2+,Ag+,Cu2+
C.Ba2+,Cu2+,Ag+ D.Ag+,Ba2+,Cu2+
原理请说明清楚, xiaoxin38381年前2
xiaoxin38381年前2 -
 shjyjlwc 共回答了15个问题
shjyjlwc 共回答了15个问题 |采纳率80%Ba2+只与碳酸根反应;Cu2+与碳酸根,负二价硫离子都可以反应;Ag+与氯离子,碳酸根,负二价硫离子三个都可以反应产生沉淀.故先加入.Ba2+再到Cu2+最后加入Ag+,故c正确1年前查看全部
- 在饱和的H2S水溶液中硫离子浓度为什么等于ka2?
 曾为县吏民知否1年前1
曾为县吏民知否1年前1 -
 小强特攻队 共回答了21个问题
小强特攻队 共回答了21个问题 |采纳率100%既然是饱和的溶液了,就不存在浓度的变化了,浓度一定了,在外间条件不变的条件下,那么他对应的PH就一定了,电离的平衡就一定了,而且就是Ka2
希望读你能有帮助!1年前查看全部
- ①0.1mol/LH2S溶液 ②0.1mol/LH2S和0.1mol/LNaHS混合液,二者硫离子浓度大小关系怎么分析?
 泰山樵夫1年前1
泰山樵夫1年前1 -
 快乐小猪与墩墩 共回答了13个问题
快乐小猪与墩墩 共回答了13个问题 |采纳率100%②>①
①中的S2-离子来源于H2S的二次电离、HS-的一次电离
②中的S2-离子来源于也是H2S的二次电离、HS-的一次电离
但是HS-的浓度比①中的浓度要大许多,电离出的S2-也大很多
所以,②中S2-更多1年前查看全部
- C D 微粒分别指 硫离子 钠离子 写出他们的元素符号
C D 微粒分别指 硫离子 钠离子 写出他们的元素符号
为什么不是写成 S Na 要写成 S2- Na2- 狮心1年前2
狮心1年前2 -
 三哥不是男人 共回答了18个问题
三哥不是男人 共回答了18个问题 |采纳率94.4%因为离子是带电荷的原子或原子团,必须把它们所带的电荷写在右上角.S2-,Na+1年前查看全部
- 为什么钾离子,钠离子,氯离子,硫离子不能大量共存?
为什么钾离子,钠离子,氯离子,硫离子不能大量共存?
它们是要在无色溶液中大量共存
。 ss661年前2
ss661年前2 -
 shadan2000 共回答了18个问题
shadan2000 共回答了18个问题 |采纳率88.9%钾离子,钠离子,氯离子,硫离子可以大量共存1年前查看全部
- 亚硫酸根和负二价硫离子在酸性条件下不共存生成什么、谢谢…
 wxg5119883561年前1
wxg5119883561年前1 -
 punk1942 共回答了22个问题
punk1942 共回答了22个问题 |采纳率86.4%2S2- + SO32- + 6H+ === 3S+3H2O1年前查看全部
- 氢离子可以和硫离子共存吗为什么氢离子可以和硫离子不能共存,而氢离子为什么可以和氯离子能共存,它们不会生成氯化氢吗
 squallshuai1年前8
squallshuai1年前8 -
 manfreeze 共回答了18个问题
manfreeze 共回答了18个问题 |采纳率94.4%氢离子可以和硫离子共存,只是不能大量共存.
因为H+ 和S2-的离子浓度大就会 形成H2S(硫化氢是弱电解质,在溶液中氢离子和硫离子的浓度不能很大) 会以硫化氢气体形式逸出.
而HCl 是强电解质,极易溶于水,可以存在大浓度的H+和Cl-,所以氢离子可以和氯离子能大量共存,溶液中不存在HCl分子,所以不会结合成氯化氢逸出的,只能以氢离子和氯离子共存于溶液中.1年前查看全部
- 氧化性氯大于硫,还原性氯离子小于硫离子,为什么?
 jb141年前2
jb141年前2 -
 zimo99 共回答了14个问题
zimo99 共回答了14个问题 |采纳率71.4%Cl 得到电子比 S 强,即Cl氧化性强
Cl- 得到电子后比S2- 更加难失去电子,则Cl-不易被氧化,即Cl-还原性小于S2-1年前查看全部
大家在问
- 1亚硫酸氢根和硫离子能否共存
- 2硫离子与亚硫酸根共存,而次氯酸根与亚硫酸根不共存
- 3把数字4、4、10、10用"加、减、乘、除括号"列算式结果为24.
- 4初中化学中哪些离子不能共存?
- 5已知行星轨道参数 (1)a=4cm e=0.5 (2) a=4cm e=0.8 这种情况下 请画出轨道 r(Φ)=a/
- 6三角形的中位线等于第三边的一半怎么证明啊?
- 7500千克花生可以榨油340千克.照这样计算,2吨花生可以榨油多少千克?
- 8我该如何去爱你),怎么翻译,标准?
- 92.3.4.5.余暇:2.阴霾:3.迫不及待:4.孜孜不倦:5.梦寐以求:
- 10平衡力与相互作用力比较:相同点:不同点:
- 111.从甲地寄往乙地的包裹邮资标准是:1kg(不足1kg按1kg计算)77.10元,达到或超过1kg后,每增加1kg(不足
- 12如图,点E,F分别在正方形ABCD的边AB和对角线BD上,且EF⊥BA于E,若点G为DF中点,连接EG,CG.
- 13求怀念家乡或童年的大家文章同题
- 14计算机电路基础填空题 逻辑函数F=A+B,则F=()
- 15滚环扩增所需引物有什么要求吗?怎样设计引物?
