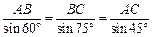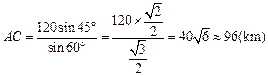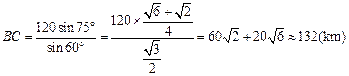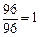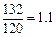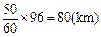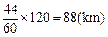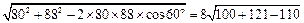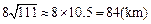直线型需求曲线的斜率不变,因此其价格弹性也不变,该说法是否正确?求解析
 xpez161832022-10-04 11:39:541条回答
xpez161832022-10-04 11:39:541条回答如题.

已提交,审核后显示!提交回复
共1条回复
 帐子 共回答了14个问题
帐子 共回答了14个问题 |采纳率100%- 错的,价格弹性是直线斜率*P/Q,P,Q是变化的,所以价格弹性是变化的
- 1年前
相关推荐
- 由两个周期中的三种元素组成的直线型分子
 bobbyfromcd1年前1
bobbyfromcd1年前1 -
 xrbbxoqe 共回答了21个问题
xrbbxoqe 共回答了21个问题 |采纳率81%氰化氢,化学式HCN.H-C≡N是直线型分子.C和N是一个周期,H是一个周期.1年前查看全部
- 为什么晶界腐蚀后是黑色的,怎么鉴别侵蚀后观察时发现的直线型映像是金属本身磨痕还是划痕
为什么晶界腐蚀后是黑色的,怎么鉴别侵蚀后观察时发现的直线型映像是金属本身磨痕还是划痕
如果答对!我会加十分给你的 推板车的人1年前1
推板车的人1年前1 -
 aenjoy 共回答了20个问题
aenjoy 共回答了20个问题 |采纳率85%因为晶界能量高,容易被腐蚀,形成凹槽,所以是黑色的.
划痕是比较一致的,本身的磨痕比较突出一点,就是与众不同一点1年前查看全部
- C原子作为中心原子形成直线型分子的时候,C原子的基态电子是如何被激发形成等性的sp杂化轨道?或者有其他理论来解释CO2分
C原子作为中心原子形成直线型分子的时候,C原子的基态电子是如何被激发形成等性的sp杂化轨道?或者有其他理论来解释CO2分子的C-O键的形成?
 口袋的烟头1年前1
口袋的烟头1年前1 -
 韶之恋 共回答了17个问题
韶之恋 共回答了17个问题 |采纳率88.2%C原子的基态电子是1s2 2s2 2p2,杂化时,2S上的两个电子中的1个被激发到2P的最后一个空轨道上,此时2s和2p总共4个轨道上各有一个电子,然后2S和一个2P杂化,形成2个sp杂化轨道,其上各有一个电子,以乙炔为例,这两个电子一个和氢原子形成一个"头对头"的sigma共价键,一个和另一个碳的一个sp杂化轨道上的电子形成一个sigma共价键,剩下的两个P轨道上的电子与另一个碳的两个P轨道上的电子形成两个肩并肩的pai键.1年前查看全部
- 为什么三个碳以上的烷烃分子中的碳链不是直线型?怎么判断烷烃的碳链形状呀?
 WSHILWL1年前2
WSHILWL1年前2 -
 rsrteam 共回答了18个问题
rsrteam 共回答了18个问题 |采纳率88.9%烷烃碳原子都采用SP3杂化,每条键的键角都是109°28′,所以不是一条直线1年前查看全部
- 下列分子构型是直线型的是C2H6C2H4C2H2CO2
 ii狂飑1年前1
ii狂飑1年前1 -
 liangyun72 共回答了21个问题
liangyun72 共回答了21个问题 |采纳率90.5%C2H21年前查看全部
- 小学准备在120米长的直线型跑道一边和边长20米的正方形草地四周栽树,没隔10米在一棵,跑道一边的两都栽,
小学准备在120米长的直线型跑道一边和边长20米的正方形草地四周栽树,没隔10米在一棵,跑道一边的两都栽,
正方形草地的四角上都栽.
1、跑道一边需要在多少棵树?
2、草地四周需要在多少棵树?
学准备在120米长的直线型跑道一边和边长20米的正方形草地四周栽树,没隔10米在一棵,跑道一边的两端都栽,正方形草地的四角上都栽。
1、跑道一边需要在多少棵树?
2、草地四周需要在多少棵树? itokumo1年前2
itokumo1年前2 -
 wangke198320 共回答了15个问题
wangke198320 共回答了15个问题 |采纳率80%1、跑道一边需要在多少棵树?
120÷10+1
=12+1
=13(棵)
2、草地四周需要在多少棵树?
(20×4)÷10
=80÷10
=8(棵)1年前查看全部
- hclo 空间构型资料上说是直线型,怎么计算出是sp的?
 守71年前1
守71年前1 -
 鹤云之想 共回答了19个问题
鹤云之想 共回答了19个问题 |采纳率89.5%氯的含氧酸的中心原子已经确定为氧,两个不同的非极性共价键以O为中心组成正负电荷中心不重合的极性分子,即不对称,故空间结构为V型.直线型是错的.1年前查看全部
- C、H两元素组成的分子构型可能是直线型,三角锥形,正四面体,求举例
 huadong18601年前1
huadong18601年前1 -
 dagang129 共回答了17个问题
dagang129 共回答了17个问题 |采纳率88.2%直线:乙炔,三角锥:碳负离子,正四面体:甲烷1年前查看全部
- 亚氯酸根中,Cl与O之间是否为配位键?“凡是直线型的分子中心原子上的孤电子对均为零”为什么错了?PCl3,BF3的VSE
亚氯酸根中,Cl与O之间是否为配位键?
“凡是直线型的分子中心原子上的孤电子对均为零”为什么错了?
PCl3,BF3的VSEPR模型及立体构型,如何得到的?
四原子分子的立体构型除了平面三角形和三角锥形外还能是什么?
“根据价层电子对互斥理论可推断,BeCl2分子立体构型可能为直线型”为什么错了?
如何判断四原子分子采取平面三角形还是三角锥形的立体构型?
立体构型为三角锥形的阳离子的化学式
 z小波1年前2
z小波1年前2 -
 yzxwk 共回答了15个问题
yzxwk 共回答了15个问题 |采纳率93.3%楼主高中生吧,
1 Cl和O是配位键
2 CO2,SO2的结构就是例子,证明是错的
3 这个结构的的得到是通过理论推导和实验验证
4 还有正四面体结构,P4就是例子
5 Be的原子半径太小了,Cl比较大,两个Cl在一条直线上两个相互排斥,不能在一条线上形成平衡,所以不是直线型
6 这个比较难判断
7 这个不一定的,P4就是很好地例子.望采纳1年前查看全部
- B地在A地的正东方向4千米处,C地在B地的北偏东45°的22千米处.有一直线型的马路l过C地且与线段BC垂直,现欲在马路
B地在A地的正东方向4千米处,C地在B地的北偏东45°的2
千米处.有一直线型的马路l过C地且与线段BC垂直,现欲在马路l上造一个车站P.造一公里马路的费用为5万元,则修筑两条马路PA、PB的最低费用为 ___ 万元.2
 王中军爱井宝1年前0
王中军爱井宝1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- CO2的直线型结构与SP2杂化有关么
CO2的直线型结构与SP2杂化有关么
因为有碳氧双键 hallozero1年前1
hallozero1年前1 -
 SHUIBO_LIANG 共回答了21个问题
SHUIBO_LIANG 共回答了21个问题 |采纳率95.2%碳原子是sp杂化的,因此CO2是直线型的1年前查看全部
- 二氧化碳自由度为什么是6?二氧化碳是直线型分子,它的自由度为什么不是5而是6?如何用实验证明?
 d5d2n431年前1
d5d2n431年前1 -
 负罪魔鬼 共回答了17个问题
负罪魔鬼 共回答了17个问题 |采纳率94.1%三个平动自由度
两个专动自由度
一个振动自由度
实验也就是能均分、热平衡了,气体的比热1年前查看全部
- 已知:E为常见金属,C、D、F、I均为常见气体,其中C、D为单质,F、I为化合物,且组成元素相同,D、F有毒,I为直线型
已知:E为常见金属,C、D、F、I均为常见气体,其中C、D为单质,F、I为化合物,且组成元素相同,D、F有毒,I为直线型非极性分子,B的结构为三角双锥(如图所示),图中○代表F分子,●代表E原子,它们有如下框图关系:
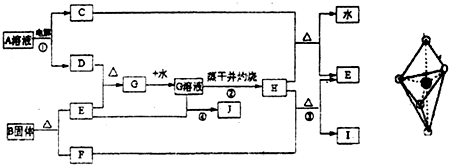
(1)H的颜色是______;B的化学式是______;I的电子式是______.
(2)反应①阳极的电极反应式______.
(3)反应③的化学方程式是Fe2O3+3CO
2Fe+3CO2△ .Fe2O3+3CO,该反应在工业上的用途是______.
2Fe+3CO2△ .
(4)反应④的离子方程式______.
(5)从G溶液制得G的结晶水合物的操作是______.
(6)反应②蒸干并灼烧最终得H而不是无水的G,试用简要文字和方程式解释:因为加热时发生FeCl3+3H2O═Fe(OH)3↓+3HCl↑,这是个完全水解过程,加热蒸干后生成了Fe(OH)3,灼烧时发生了2Fe(OH)3
Fe2O3+3H2O↑,所以把氯化铁溶液蒸干灼烧,最后的得到的固体产物是氧化铁.△ .因为加热时发生FeCl3+3H2O═Fe(OH)3↓+3HCl↑,这是个完全水解过程,加热蒸干后生成了Fe(OH)3,灼烧时发生了2Fe(OH)3.
Fe2O3+3H2O↑,所以把氯化铁溶液蒸干灼烧,最后的得到的固体产物是氧化铁.△ . jh_991年前1
jh_991年前1 -
 eptrk 共回答了20个问题
eptrk 共回答了20个问题 |采纳率90%解题思路:由电解生成D并且有毒,则D应为氯气,I为直线型非极性分子,则应为CO2,F为CO,根据E与氯气反应后能继续与E反应,说明E是一种变价金属,应为Fe,则G为FeCl3,H为Fe2O3,J为FeCl2,C为H2,B分解生成Fe和CO,根据其结构模型可推知为Fe(CO)5;根据物质的性质结合质量守恒定律书写化学方程式和离子方程式;根据物质的性质完成实验操作.(1)由电解生成D并且有毒,则D应为氯气,I为直线型非极性分子,则应为CO2,其电子式为
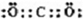 ,F为CO,根据E与氯气反应后能继续与E反应,说明E是一种变价金属,应为Fe,则G为FeCl3,H为Fe2O3,为红棕色固体,J为
,F为CO,根据E与氯气反应后能继续与E反应,说明E是一种变价金属,应为Fe,则G为FeCl3,H为Fe2O3,为红棕色固体,J为
FeCl2,C为H2,B分解生成Fe和CO,根据其结构模型可推知为Fe(CO)5;
故答案为:红棕色;Fe(CO)6;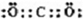 ;
;
(2)根据题意,电解A溶液生成氢气和氯气,电解时阳极发生氧化反应,Cl-放电生成Cl2,故答案为:2Cl--2e-═2Cl2↑;
(3)工业炼铁是用还原性气体和CO在高温条件下发生氧化还原反应生成Fe,根据质量守恒定律可写出化学方程式,故答案为:Fe2O3+3CO
△
.
2Fe+3CO2;工业炼铁;
(4)反应④为Fe3+和Fe发生氧化还原反应生成e2+,故答案为:2Fe3++Fe═3Fe2+;
(5)氯化铁在加热下易发生水解生成Fe(OH)3,为防止FeCl3水解,应在酸性条件下进行加热浓缩,并进行结晶和过滤,最后才能得到氯化铁晶体,故答案为:在加入盐酸后的溶液中蒸发浓缩、冷却结晶、过滤干燥.;
(6)加热条件下,氯化铁水解生成Fe(OH)3,Fe(OH)3不稳定,在灼烧时发生分解生成Fe2O3,故答案为:因为加热时发生FeCl3+3H2O═Fe(OH)3↓+3HCl↑,这是个完全水解过程,加热蒸干后生成了Fe(OH)3,灼烧时发生了2Fe(OH)3
△
.
Fe2O3+3H2O↑,所以把氯化铁溶液蒸干灼烧,最后的得到的固体产物是氧化铁.点评:
本题考点: 常见金属元素的单质及其化合物的综合应用;离子方程式的书写;物质的结构与性质之间的关系;电极反应和电池反应方程式;盐类水解的应用.
考点点评: 本题考查无机物的推断,并考查盐的水解、物质的制备等知识,具有一定的思维力度,做题时注意找出题目的关键点,牢固掌握物质的性质和实验基础知识.1年前查看全部
- 氯化铍是非极性分子么?它是直线型,应该是对称的啊
 luopo03131年前1
luopo03131年前1 -
 Google测试员5555 共回答了16个问题
Google测试员5555 共回答了16个问题 |采纳率81.3%氯化铍是非极性分子.
Be是4号元素,电子排布为1s(2),2s(2).括号里指上标.另外还有3个空的2p轨道.
BeCl2是sp杂化,直线型分子,同时还有2个两两垂直的空p轨道.
由于有空的p轨道,可以接受外来电子,H2O中的O可以提供孤电子对,因此它可以形成水合物.
关于你说的非极性分子可以溶于极性溶剂(水)的问题,我觉得是否可溶应该看两者的亲和力大,从微观上说,氯化铍分子和水分子应该有一定亲和力,我没有去查相关资料,如果它确实可溶于水的话,这个解释应该可以说得过去吧.
我大三了,以前学的知识都忘得差不多了,大概就这样吧.1年前查看全部
- (2013•长宁区一模)如图,某人顺着山坡沿一条直线型的坡道滑雪,当他滑过130米长的路程时,他所在位置的竖直高度下降了
 (2013•长宁区一模)如图,某人顺着山坡沿一条直线型的坡道滑雪,当他滑过130米长的路程时,他所在位置的竖直高度下降了50米,则该坡道的坡比是______.
(2013•长宁区一模)如图,某人顺着山坡沿一条直线型的坡道滑雪,当他滑过130米长的路程时,他所在位置的竖直高度下降了50米,则该坡道的坡比是______.  chl55111年前1
chl55111年前1 -
 淡淡明月 共回答了18个问题
淡淡明月 共回答了18个问题 |采纳率88.9%解题思路:首先根据勾股定理求得滑行的水平距离,然后根据坡比的定义即可求解.滑行的水平距离是:
1302−502=120(米),
故坡道的坡比是:50:120=1:2.4.
故答案是:1:2.4.点评:
本题考点: 解直角三角形的应用-坡度坡角问题.
考点点评: 本题考查了勾股定理,以及坡比的定义,正确求得滑行的水平距离是关键.1年前查看全部
- (本小题满分12分) 如图, A , B , C 是三个汽车站, AC , BE 是直线型公路.已知 AB =120 k
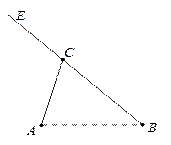
(本小题满分12分) 如图, A , B , C 是三个汽车站, AC , BE 是直线型公路.已知 AB =120 km,∠ BAC =75°,∠ ABC =45°.有一辆车(称甲车)以每小时96(km)的速度往返于车站 A , C 之间,到达车站后停留10分钟;另有一辆车(称乙车)以每小时120(km)的速度从车站 B 开往另一个城市 E ,途经车
 站 C ,并在车站 C 也停留10分钟.已知早上8点时甲车从车站 A 、乙车从车站 B 同时开出.
站 C ,并在车站 C 也停留10分钟.已知早上8点时甲车从车站 A 、乙车从车站 B 同时开出.
(1)计算 A , C 两站距 离,及 B , C 两站距离;(2)若甲、乙两车上各有一名旅客需要交换到对方汽车上,问能否在车站 C 处利用停留时间交换.(3)求10点时甲、乙两车的距离.(可能用到的参考数据:
离,及 B , C 两站距离;(2)若甲、乙两车上各有一名旅客需要交换到对方汽车上,问能否在车站 C 处利用停留时间交换.(3)求10点时甲、乙两车的距离.(可能用到的参考数据: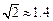 ,
,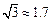 ,
,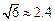 ,
,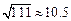 )
)
 zhangqi_0081年前1
zhangqi_0081年前1 -
 傲雁蓝馨 共回答了23个问题
傲雁蓝馨 共回答了23个问题 |采纳率87%1年前查看全部
- 一条直线型需求曲线 为什么还是 每一点的需求弹性系数都不一样
 cwb941910341年前1
cwb941910341年前1 -
 intothewc119 共回答了14个问题
intothewc119 共回答了14个问题 |采纳率85.7%弹性是指自变量变化百分之一所引起因变量变化的百分比
所以对于一条直线而言:斜率=a (常数)
某一点的弹性=a×X/Y (X,Y是这一点的坐标)
某一段的弹性则将上式的X,Y替换成这一段的中点坐标即可
不知道我说的清不清楚,有问题找我1年前查看全部
- 关于偶极矩的问题为什么CO2的μ=0,可以判断它是直线型的;H2S的μ≠0,可判断它是折线型的.
 hnyuandong1年前1
hnyuandong1年前1 -
 盘盘 共回答了18个问题
盘盘 共回答了18个问题 |采纳率77.8%偶极矩是表示分子中电性分布的指数.
μ=0,就是说分子内部电性分布均匀.反之同理.
CO2含有三个原子,只有当直线时,分子才能呈对称状,以使电荷分布均匀.
H2S,μ≠0.一定不是直线,所以只能是折线.1年前查看全部
- 8.管理层次少而管理宽度大的组织结构被称为( ) A.直线型组织结构 B.扁平式结构 C.职能型组织结构
8.管理层次少而管理宽度大的组织结构被称为( ) A.直线型组织结构 B.扁平式结构 C.职能型组织结构
D.事业部制组织结构 baobaole1年前1
baobaole1年前1 -
 菜农 共回答了19个问题
菜农 共回答了19个问题 |采纳率94.7%明显是扁平结构嘛~~~~~1年前查看全部
- 大一无机化学用杂化轨道说明下列分子或离子的几何构型,1:HgCl²(直线型)BCl3(平面三角形)
 frankemail1年前4
frankemail1年前4 -
 十五_zz 共回答了23个问题
十五_zz 共回答了23个问题 |采纳率100%1、HgCl2中心原子有2个价电子,配位原子Cl可以提供1个价电子
可以求出价电子对数目为(2+1*2)/2=2,所以中心原子Hg的外围轨道发生sp杂化
2、BCl3
这是原子最外层的一个s轨道和两个p轨道发生的杂化.杂化后形成三个等价的sp2轨道.B原子最外层的3个电子分别占据1个杂化轨道.在空间以B原子为中心3个sp2轨道伸向平面三角形的三个顶点.所以sp2杂化轨道夹角为120度1年前查看全部
- 双原子分子空间结构都是直线型的吗Co是什么型的?高中阶段直线型分子,v型分子都有哪些?
 chewang60291年前2
chewang60291年前2 -
 spark269 共回答了17个问题
spark269 共回答了17个问题 |采纳率94.1%如果是双原子分子,只有2个原子,空间结构翻不出什么花儿,只能直线型.
CO属直线型,直线型还有CO2、HCN、C2H2等等.
V型有H2O、H2S等.1年前查看全部
- 怎么比较需求的价格点弹性大小两条线性需求曲线D1和D2相交于a点,在交点a,这两条直线型的需求的价格点弹性相等吗?两条曲
怎么比较需求的价格点弹性大小
两条线性需求曲线D1和D2相交于a点,在交点a,这两条直线型的需求的价格点弹性相等吗?
两条曲线型需求曲线D1和D2相交于a点,在交点a,这两条曲线型的需求的价格点弹性相等吗? DNDST1年前1
DNDST1年前1 -
 DJmegi 共回答了16个问题
DJmegi 共回答了16个问题 |采纳率93.8%不相等,你可以用两条极端的需求曲线来证明它:
1、水平的需求曲线,它的价格弹性是无穷大的;
2、垂直的需求曲线,它的价格单性为零;
现在我们可以想想它们相交的那一点,显然是价格点弹性是不等的,一个为无穷大,一个为零.1年前查看全部
- 求一些化学物质的结构,比如什么是直线型,三角锥型啊.
 梁飞1年前1
梁飞1年前1 -
 scorpion5 共回答了16个问题
scorpion5 共回答了16个问题 |采纳率100%甲烷 空间正四边形
氨气 三角锥
水 不是直线型,就是三个原子不公线,和氧的电子对有关
二氧化碳 直线
差不多高中的都包括了
注意类比,C族形成化合物的基本都是非极性分子1年前查看全部
- 为什么甲烷的结构是正四面体,乙烯是平面结构,还有乙炔是直线型,求人告诉我这是为什么啊
 程昀1年前4
程昀1年前4 -
 微不足道的mm 共回答了23个问题
微不足道的mm 共回答了23个问题 |采纳率100%这个到高中化学选修物质结构与性质那里会详细的讲,与sp杂化有关
甲烷分子的轨道是如何形成的呢?
形成甲烷分子时,中心原子的2s和2px,2py,2pz等四条原子轨道发生杂化,形成一组新的轨道,即四条sp3杂化轨道,这些sp3杂化轨道不同于s轨道,也不同于p轨道.
根据参与杂化的s轨道与p轨道的数目,除了有sp3杂化轨道外,还有sp2 杂化和sp杂化,sp2 杂化轨道表示由一个s轨道与两个p轨道杂化形成的,sp杂化轨道表示由一个s轨道与一个p轨道杂化形成的.
三种杂化轨道的轨道形状,SP杂化夹角为180°的直线型杂化轨道,SP2 杂化轨道为120°的平面三角形,SP3杂化轨道为109°28′的正四面体构型.
你简单点想,甲烷一个C四个H,各H是完全相同的,所以是四面体
乙烯两个C四个H,中间是双键,每边一个C连两个H,H也是完全相同的,所以是平面夹角120°
乙炔两个C两个H,中间是叁键,每边一个C连一个H,所以是直线型1年前查看全部
- 化学的H20的立体结构为什么图一中的c H 不在A处呢?不是均匀分吗 那样不就成 直线型了吗
化学的H20的立体结构
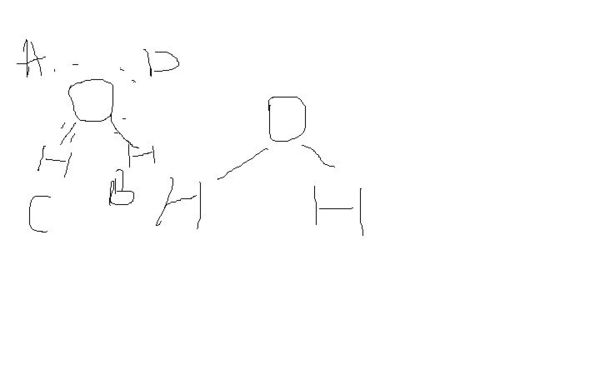
为什么图一中的c H 不在A处呢?不是均匀分吗 那样不就成 直线型了吗 dyii002161年前2
dyii002161年前2 -
 水水走ss 共回答了19个问题
水水走ss 共回答了19个问题 |采纳率89.5%你画的是平面图,实际上这是一个立体的结构,自己拿甲烷出来对比一下就可以了,ACD相对於B来说都是等价的位置,因此H2O是角形分子.注意只有H,O,H在同一平面,两对孤对电子不在平面内.1年前查看全部
- 在无水硫酸介质中,硒酸酐也能与无水N2O4反应,生成两种盐A和B.已知A和B具有相同的阴离子,而阳离子都为直线型.A、B
在无水硫酸介质中,硒酸酐也能与无水N2O4反应,生成两种盐A和B.已知A和B具有相同的阴离子,而阳离子都为直线型.A、B的含Se量分别为54.1%、51.3%.
1.确定A、B的化学式;
2.写出生成A、B的化学反应方程式;
(NO)2Se4O13;B(NO2)2Se4O13
(2)2N2O4+8SeO3=(NO)2SeO13+(NO2)2Se4O13
请给出分析或过程. honestchen1年前1
honestchen1年前1 -
 湖哈 共回答了23个问题
湖哈 共回答了23个问题 |采纳率91.3%N2O4是提供氮氧离子的,就是NOx(y+)
题目说阳离子都为直线型,而NOx(y+)中为直线形的只有NO2(+).
所以另外一种只能是双原子的了.
所以分别是NO(+)和NO2(+)
然后考虑阴离子.硒酸酐SeO3.
设A、B分别是NOSexOy、NO2SexOy.根据Se的质量分数列方程
79x / (14+16+79x+16y) = 0.541
79x / (14+16*2+79x+16y) = 0.513
解得x = 2,y = 6.5
所以A、B分别是NOSe2O6.5、NO2Se2O6.5,即NO)2Se4O13、(NO2)2Se4O13
方程式就容易了.产物、反应物都有了.1年前查看全部
- 一道关于分子结构的化学题下列分子或离子,属于直线型的有:A.OF2 B.SCl2 C.O3 D.ICl- E.NO2-
一道关于分子结构的化学题
下列分子或离子,属于直线型的有:
A.OF2 B.SCl2 C.O3 D.ICl- E.NO2-
求详解.
数字都是右下角标,DE选项是阴离子别看错了哦 fenixyang1年前5
fenixyang1年前5 -
 aacb_93dgh6_b5_5 共回答了21个问题
aacb_93dgh6_b5_5 共回答了21个问题 |采纳率90.5%ABCE都是折线型,或者V型
其中的OF2、SCl2,都可以看成是H2O、H2S中的H被F、Cl取代
O3是V型,是要记住的,是SO2的等电子体
而SO2、NO2^-都是可以用价层电子对互斥理论计算的1年前查看全部
- 二氧化碳和二氧化硫到底是极性的还是非极性的?是不是直线型
二氧化碳和二氧化硫到底是极性的还是非极性的?是不是直线型
二氧化碳是含极性键的非极性分子 那二氧化硅为什么不是?2009-6-9
查看同主题问题:二氧化碳 二氧化硫 极性 dongwenwen19861年前1
dongwenwen19861年前1 -
 wafbpc 共回答了18个问题
wafbpc 共回答了18个问题 |采纳率100%二氧化碳、二氧化硫均含有极性键,但二氧化碳为直线型分子,即键角为180度,此时正负电荷中心重合,故二氧化碳为非极性分子.(这和甲烷四氯化碳二硫化碳为非极性分子同样道理).
二氧化硫中硫原子采取sp2不等性杂化与两个O原子以σ键结合,还有一个p轨道与它们形成三中心4电子大π键,两个硫氧键之间的键角大约为119.5度,故正负电荷中心不重合,二氧化硫为非极性分子.1年前查看全部
- 英语翻译1.英美人的思维方式大多为直线型,习惯开门见山,直截了当地提出问题,将最关键的内容放在最前面.表现在语言上,英美
英语翻译
1.英美人的思维方式大多为直线型,习惯开门见山,直截了当地提出问题,将最关键的内容放在最前面.表现在语言上,英美人一般先点出话语的中心信息,再一一补叙其他外围环境.而***人的思维方式大多为螺旋型,说话喜欢“绕弯子”,常常避开主题而言其他,把一些关键文体保留到最后含蓄地表达出来.汉语是象形文字,从文字出现的最初就试图用象形符号去表达复杂的客观存在和自然事实,采用的是一种以形代形,以形指形的策略,纯粹意义的抽象思维并不重要.汉语习惯于使用具体形象的词汇来表达抽象的概念,
2.分析型与综合型思维在语言上最直观的表现就是形合与意合.“英汉语言之间最重要的区别莫过于形合与意合的区分”.形合要求严密的逻辑推理,讲求形式、结构上的完整和严谨.语言学家以“竹节句法”来比喻英语句子,即英语句子是由不可或缺的各种连接词衔接而成,宛如节节相连的竹子.英语要求个句子成分之间的结合关系必须从形态上体现出来;意合则更注重整体的表达效果,连词成句、连句成章往往依靠说话者的形象思维或者灵感,句子成分的功能往往处于次要地位,只要求可以意会,很多连接词可以省略,语言学家将其比喻为“流水句法”,所谓的流水就是指少用甚是不用连接词仍然可使行文流畅.
怎么还没有人回答啊 祺祺_kiki1年前1
祺祺_kiki1年前1 -
 爱商丘甜的叶子 共回答了17个问题
爱商丘甜的叶子 共回答了17个问题 |采纳率70.6%1. westerners tend to think in a linear way, they like to see and say things directly. in their conversations, the most important contents usually appear first. in the expression of their languages, westerners always like to state their points of view first and make them the topic sentences. the examples and explanations of these points will be given and elaborated later on. unlike the westerners, the Chinese way of thinking is much more complex, we can actually use the word 'spiral' to describe it. Chinese like to beat around the bush. when they speak, they tend to express it in a way that the main subjects and key words are usually avoided or hided in the beginning, they will hint you and eventually tell you what they wanted to say at the end of the conversation. Chinese language is actually derived from the shapes of the objects, with the initial intentions of using symbolic words to express some complex, objective but natural matters in such a way that absolute abstraction does not seem to be the main consideration. apparently, chinese tends to depict abstractive matters in a concrete and symbolic way.
2. analytical and integrated thinking skills can mainly be represented in two ways--hypotaxis and parataxis. the differences between the two are also the main differences between the english and chinese languages. hypotaxis require deep and accurate logics, both forms and structures of the representation must be fully connected, exactly the reason why linguists would use 'bamboo syntax' to describe english language. as every sentence of it is closely connected with various words and phrases just like the structure of bamboo. english require each components of the sentences to form a relation that will reflect itself as a whole or complete sentence. whereas, parataxis focuses more on the entire expression of the meaning, conjunctions or any other similar phrases
would only be used on impulse by the speakers, meaning these words may not be so critical or even necessary and can be removed so long as the coherences of the sentences are not affected, this is also the reason why linguists would describe it as 'water syntax' , that is without using any connecting words or phrases still can make the coherence of the meaning of the entire sentence to flow like water.
.绝对纯人脑原创. 我是从整体翻译的...heihei.1年前查看全部
- 第1讲 小数的计算技巧 第2讲 直线型的行程问题 第3讲 环形路的行程问题 第4讲 比和比例 第5讲 图解法与表解法 第
第1讲 小数的计算技巧 第2讲 直线型的行程问题 第3讲 环形路的行程问题 第4讲 比和比例 第5讲 图解法与表解法 第6讲 一元一次方程的解法 第7讲 列方程解应用题 第8讲 三角形的等积变换 第9讲 利用割补求面积 第10讲 利用方程求面积 第11讲 第12讲 统筹与规划 第13讲 从反面考虑问题 第14讲 换个角度想一想 第15讲 同中存异 第16讲 异中求同 第一学期期末测试 第二学期 第1讲 长方体、正方体的表面积与体积 第2讲 长方体、正方体的切拼与涂色 第3讲 发挥空间想象力 第4讲 数的整除 第5讲 质数、合数和分解质因数 第6讲 奇数和偶数 第7讲 公约数与公倍数 第8讲 辗转相除法 第9讲 第10讲 分数的拆分与巧算 第11讲 分数大小的比较 第12讲 第13讲 枚举与筛选 第14讲 规律与归纳 第15讲 构造法与对应法 第16讲 整体思考与分类讨论
 cxl2581年前1
cxl2581年前1 -
 滴萃阁阁主 共回答了8个问题
滴萃阁阁主 共回答了8个问题 |采纳率75%如果是书的话《小冠军》不错.我们六年级老师现在不买书,她从很多书上挑几道题,剪下来打印出来,每天让我们抄在本子上做.她说买了奥数书就是跟着书转了,自己抄题目可以捡东一些重要的.1年前查看全部
- CO2分子是直线型,其C原子的成键轨道是
CO2分子是直线型,其C原子的成键轨道是
A2个sp杂化轨道 B2个p轨道 C2个sp杂化轨道及2个p轨道D1个sp杂化轨道及1个p轨道
求答案及原因 wangwang48211年前1
wangwang48211年前1 -
 beauva0 共回答了20个问题
beauva0 共回答了20个问题 |采纳率95%D.C原子的1个s轨道,2个p轨道有电子,只有sp杂化为直线型,所以还剩下1个p轨道的两个电子与氧形成π键.1年前查看全部
- 实验测得CS2是直线型结构的分子,则分子中共有4个σ键.
 世人皆睡吾独1年前1
世人皆睡吾独1年前1 -
 xyqs521 共回答了18个问题
xyqs521 共回答了18个问题 |采纳率83.3%CS2和CO2构型相同,含有两个碳硫双键,一个双键的话就是一个σ键和一个π键,σ键的电子云是圆柱形,所以双键不会是两个σ键组成.所以CS2中有2个σ键2个π键1年前查看全部
- 水分子的结构为何成V型硫化氢结构却好像为直线型,氧硫是同一主足,为何两者氢化物结构却不同
 第N个啊熊1年前3
第N个啊熊1年前3 -
 娃哈哈sdti 共回答了9个问题
娃哈哈sdti 共回答了9个问题 |采纳率66.7%硫化氢的结构也是角形,氢原子之间有一种叫做氢键的相互作用力.1年前查看全部
- 干冰中的共价键为什么是极性的?CO2不是直线型吗?为什么会是极性键?
 12358891561年前1
12358891561年前1 -
 恋上你的人 共回答了12个问题
恋上你的人 共回答了12个问题 |采纳率91.7%你把键的极性和分子的极性混起来了.
CO2是极性键形成的非极性分子1年前查看全部
- 对一斜率为正且先于价格轴(纵轴)再与数量轴(横轴)相交的直线型供给曲线,其供给价格弹性是大于1还是小于1?还是等于1?为
对一斜率为正且先于价格轴(纵轴)再与数量轴(横轴)相交的直线型供给曲线,其供给价格弹性是大于1还是小于1?还是等于1?为什么呢?能不能画图说明一下?
 bbggbbgg1年前1
bbggbbgg1年前1 -
 youthman102 共回答了21个问题
youthman102 共回答了21个问题 |采纳率85.7%小于11年前查看全部
- 二氟化氙直线型结构为什么直线型
 看见怒1年前1
看见怒1年前1 -
 小鱼儿蹦过 共回答了18个问题
小鱼儿蹦过 共回答了18个问题 |采纳率94.4%二个F之间的斥力最小呀1年前查看全部
- 碘三负离子空间构型为直线型原因
 我也是凉粉1年前2
我也是凉粉1年前2 -
 ytrr1980 共回答了15个问题
ytrr1980 共回答了15个问题 |采纳率93.3%I3-
sp3d杂化
5对电子是三棱双锥
其中两对成键(直线)1年前查看全部
- 一道平面几何题(直线型)在平行四边形ABCD中,AB=16,AD=10,BE=4,则FC等于多少
 nounours31年前3
nounours31年前3 -
 就变天了 共回答了23个问题
就变天了 共回答了23个问题 |采纳率82.6%因为平行四边形中BCAD,
BC平行且等于AD
三角形AED与三角形BEF相似
BE:AE=BF:AD,
BF=2,
CF=BC-BF=10-2=81年前查看全部
- "氯化汞,氯化亚汞均为直线型分子,其中心金属原子均以sp杂化轨道形式成键" 这句话对吗
 eric08091年前1
eric08091年前1 -
 huanxubb 共回答了17个问题
huanxubb 共回答了17个问题 |采纳率94.1%不对
氯化亚汞是直线型分子式sp杂化 但是氯化汞是V型,为sp2杂化1年前查看全部
- 直线型,V型的分子都哪些?
 xxxucoco1年前1
xxxucoco1年前1 -
 在水一F 共回答了18个问题
在水一F 共回答了18个问题 |采纳率94.4%直线型的有:二氧化碳
V型的有:水、二氧化硫
高中常见的就是这几种了吧,1年前查看全部
- 我们看一根放在半杯水中的筷子,感觉不是直线型,这是因为光的折射.那么我们看游泳池的水下地面,感觉会与其真实情况一样高吗?
我们看一根放在半杯水中的筷子,感觉不是直线型,这是因为光的折射.那么我们看游泳池的水下地面,感觉会与其真实情况一样高吗?
A.一样高 B.比真实情况高 C.比真实情况深 atgc761年前1
atgc761年前1 -
 山西戾hh 共回答了18个问题
山西戾hh 共回答了18个问题 |采纳率88.9%选B ,因为我们看到的杯水中的筷子其实是筷子的折射光所成的虚像,它比实际的筷子更浅.可以画光路图就一目了然.1年前查看全部
- NH3是三角锥形还是三角锥型,记得这两个xing有区别的,直线形还是直线型
 szbbye1年前3
szbbye1年前3 -
 hzd306 共回答了14个问题
hzd306 共回答了14个问题 |采纳率78.6%三角锥型
一个是平面的形
一个是立体的型1年前查看全部
- 一辆汽车在直线型的公路AB山由A向B行驶,C和D
 yuxuan7181年前1
yuxuan7181年前1 -
 wellsj 共回答了21个问题
wellsj 共回答了21个问题 |采纳率95.2%过C,D作 CM,DN垂直AB
因为垂线是最短距离1年前查看全部
- CH≡CCH3是直线型分子么
 wawa20500ray1年前4
wawa20500ray1年前4 -
 新ff 共回答了12个问题
新ff 共回答了12个问题 |采纳率75%三个碳在一条直线上,可以看成直线型分子~1年前查看全部
- 正四面体型分子,三角锥型分子,直线型,V型分子 ,谁可以给我说说么?
 zhangtong5221年前1
zhangtong5221年前1 -
 游走流苏 共回答了26个问题
游走流苏 共回答了26个问题 |采纳率92.3%正四面体:CH4、CCl4、NH4+
三角锥:NH3、PH3、H3O+
直线形:BeCl2、CO2、CH≡CH
V形:H2O、H2S
学了价层电子对互斥理论,就能自己判断构型了.不用硬记住1年前查看全部
- 用价电子对互斥理论CO2的分子结构是直线型,为什么SiO2不是直线型?
 zhongbeu5201年前1
zhongbeu5201年前1 -
 妖精小新娘 共回答了14个问题
妖精小新娘 共回答了14个问题 |采纳率92.9%SIO2是原子晶体,是不存在SIO2分子的.所以不能用价电子互斥理论去解释他、1年前查看全部
- 直线型分子一定是非极性分子错在哪了?直线也算对称啊
 云化羽1年前1
云化羽1年前1 -
 test1137 共回答了20个问题
test1137 共回答了20个问题 |采纳率90%直线不对称1年前查看全部
- 已知乙烯分子是平面结构,乙炔分子是直线型结构.由此推断:
已知乙烯分子是平面结构,乙炔分子是直线型结构.由此推断:
CH3—CH==CH—C C—CF3分子结构的下列叙述中正确的是( )
A.6个碳原子可能都在一条直线上 B.6个碳原子中有5个在一条直线上
C.6个碳原子可能都在一个平面上 D.6个碳原子不可能都在一个平面上
要说明原因 fxyule1年前6
fxyule1年前6 -
 江河大浪 共回答了22个问题
江河大浪 共回答了22个问题 |采纳率86.4%碳碳双键决定六个原子共面,包括双键连接的两个碳原子以及碳原子上再各自连接的两个原子
碳碳三键决定四个原子共线,包括三键连接的两个碳原子以及碳原子上再个子连接的那个原子
单键可以旋转,判断可能共面的时候可以旋转单键,让某些原子旋转到某个平面
饱和碳原子(链接四个单键的碳原子)上连接的四个原子一定不共面,因为四根键是伸向四面体的四个顶点,所以判断不共面的时候可以去找寻饱和碳原子的踪迹
对于本题:共六个碳原子,暂且从后往前给碳原子编号1-6,双键可以决定四个碳原子(3、4、5、6号)共面,三键决定了四个碳原子(1、2、3、4号)共线,根据数学几何知识,如果一条直线有两点在一个平面,那么这条直线一定在这个平面内,从碳号上你会发现,3、4号两个共线的碳原子在双键决定的平面内,因此碳碳三键决定的直线一定在碳碳双键决定的平面内,所以六个碳原子全部共面,但是只有四个共线,因此选择C1年前查看全部
- 简述判断时间序列是否为直线型的方法?
 qhg81年前1
qhg81年前1 -
 bacmilano 共回答了19个问题
bacmilano 共回答了19个问题 |采纳率84.2%电大作业吧 直接复制即可
时间顺序有成动态数列,他是由反映市场现象在不同时间上的数量特征的一系列观察值按时间先后顺序排列后形成的数列,市场现象的发展变化收到多种因素的影响,不同因素的影响会是时间序列呈现不同的变动特征.有些因素对现象的发展起着长期的 决定性作用,致使现象的发展趋势呈现出某种倾向或规律性;有些因素则对现象的发展起着短期的 非决定性做用,致使现象呈现出某种不规则性 所以 时间序列不是直线型方法1年前查看全部
大家在问
- 1在语文中感受大自然 作文
- 2宝贝狗狗,一路走好 作文
- 3小明和小丽同住一幢大楼.小明家住在六楼,每天回家要走80个台阶.小丽回家32个台阶,小丽家住几楼?
- 4帮忙编几条短一点的绕口令,像这条以“化肥”为中心的绕口令一样:黑化肥挥发发灰会花飞;灰化肥挥发发黑会飞花编一条以“台绣”
- 5哪位好心的人帮我解决一下这个英文短文判断(“对”或者“错”)
- 6猜一猜(各打一字)很容易的猜一猜(各打一字)1、海军.( )2、红上加红.( )3、山边河水流.( )4、池里无水,地里
- 7听录音,给下列图片标号(用数字)
- 8课文《金色花》中,"你到哪里去了,你这坏孩子?"这句话中的"坏"是什么意思?
- 9在复数范围内解方程 3x^2+2x+1=0
- 10当海鸥低低的在海面上飞翔,用什么成语形容?
- 11认一认.(1)体育馆在动物园的______面,少年宫在图书馆的______面.(2)学校的东南面是______,西北面是
- 12怎样做频数分布直方图
- 13144分等于几时
- 14画出下图各力的力臂请画出图\(≧▽≦)/
- 15500ml盐水.质量600克密度1.2克每立方厘米加多少水变成密度1.1克每立方厘米