在样品水中检测到大肠菌群说明了什么?
 山丹丹开花红艳艳2022-10-04 11:39:541条回答
山丹丹开花红艳艳2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 棉签儿 共回答了23个问题
棉签儿 共回答了23个问题 |采纳率87%- 由于大肠菌群主要存在于人和动物的肠道中,如果在样品水中检测到大肠菌群,则说明水样直接或间接受到粪便的污染.
- 1年前
相关推荐
- (2014•江宁区二模)为了测定某样品中氧化铁(Fe2O3)的质量分数(杂质不含铁元素,且不溶于水和酸),某兴趣小组的同
(2014•江宁区二模)为了测定某样品中氧化铁(Fe2O3)的质量分数(杂质不含铁元素,且不溶于水和酸),某兴趣小组的同学进行了如下的实验,请你参与过程分析.
【查阅资料】
1草酸(H2C2O4)在浓硫酸作用下受热分解,化学方程式为H2C2O4
CO2↑+CO↑+H2O浓硫酸 .△
2碱石灰能吸收二氧化碳和水蒸气
【实验设计及操作】用如图所示装置进行实验:
【问题讨论】
(1)装药品前应先______,实验中观察到E中现象是:固体颜色______;
(2)进入E中的气体是纯净、干燥的CO,则B、C、D中依次是______(填序号).
①浓硫酸、石灰水、氢氧化钠溶液 ②石灰水、氢氧化钠溶液、浓硫酸
③氢氧化钠溶液、石灰水、浓硫酸
(3)G的作用是______;E中反应的化学方程式是3CO+Fe2O3
2Fe+3CO2高温 .3CO+Fe2O3;
2Fe+3CO2高温 .
(4)当E中固体完全反应后,先熄灭______灯(A、E);
(5)实验装置有一明显缺陷是:______.
【数据处理】称取样品8.0g,用上述装置进行实验,充分反应后称量F装置增重4.4g.则样品中氧化铁质量分数为______.
【实验反思】当观察到E中固体全部变黑后,若立即停止通CO,则测得的样品中氧化铁的质量分数______(填“偏大”,“偏小”,“无影响”). 神奇之神1年前1
神奇之神1年前1 -
 鹿惊 共回答了22个问题
鹿惊 共回答了22个问题 |采纳率100%解题思路:【问题讨论】
(1)凡是有气体参加或产生的实验,实验前一定要检查装置的气密性,以防装置漏气影响实验结果;
氧化铁是红色的,和一氧化碳反应能生成黑色的铁粉和二氧化碳;
(2)氢氧化钠溶液能够吸收二氧化碳气体,二氧化碳能使澄清石灰水变浑浊,浓硫酸具有吸水性,可以用来干燥一氧化碳;
(3)G的作用是防止空气中的二氧化碳和水蒸气干扰实验;
一氧化碳和氧化铁在高温条件下反应能生成铁和二氧化碳;
(4)当E中固体完全反应后,为了防止液体倒吸入A装置,应该先熄灭E处的酒精灯;
(5)一氧化碳有毒,扩散到空气中会污染环境;
【数据处理】
F装置增重的部分即为生成二氧化碳的质量,根据二氧化碳的质量可以计算氧化铁的质量,进一步可以计算样品中氧化铁的质量分数;
【实验反思】
当观察到E中固体全部变黑后,若立即停止通CO,则反应生成的二氧化碳不能被F装置完全吸收.【问题讨论】
(1)装药品前应先检查装置气密性,实验中观察到E中现象是:固体颜色由红色变成黑色.
故填:检查装置气密性;由红色变成黑色.
(2)进入E中的气体是纯净、干燥的CO,则B、C、D中依次是氢氧化钠溶液、石灰水、浓硫酸.
故填:③.
(3)G的作用是防止空气中的二氧化碳和水蒸气进入F;E中反应的化学方程式是3CO+Fe2O3
高温
.
2Fe+3CO2.
故填:防止空气中的二氧化碳和水蒸气进入F;3CO+Fe2O3
高温
.
2Fe+3CO2.
(4)当E中固体完全反应后,先熄灭E处的酒精灯.
故填:E.
(5)实验装置明显缺陷是没有处理尾气.
故填:没有处理尾气.
【数据处理】
设氧化铁的质量为x,
3CO+Fe2O3
高温
.
2Fe+3CO2,
160 132
x 4.4g
[160/x]=[132/4.4g],
x=5.3g,
则样品中氧化铁质量分数为:[5.3g/8.0g]×100%=66.7%,
故填:66.7%.
【实验反思】
当观察到E中固体全部变黑后,若立即停止通CO,会导致生成的二氧化碳不能被F装置完全吸收,则测得的样品中氧化铁的质量分数会偏小.
故填:偏小.点评:
本题考点: 实验探究物质的组成成分以及含量;常见气体的检验与除杂方法;一氧化碳的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.1年前查看全部
- 燃烧热的测定中样品为什么要压片
 dakxx1年前2
dakxx1年前2 -
 忍不到白头 共回答了19个问题
忍不到白头 共回答了19个问题 |采纳率94.7%排除空气等气体杂质的同时,节省了样品在氧弹中所占体积,减小误差.同时,压片后的样品燃烧会更充分.1年前查看全部
- “此票样品的型号修改为……”,这句英语怎么说合适,
 小叮说事儿1年前3
小叮说事儿1年前3 -
 chensi0513 共回答了14个问题
chensi0513 共回答了14个问题 |采纳率92.9%此票样品的型号修改为……
The sample model of this batch has been revised to...
The sample model of this batch has been changed to...
The sample model of this batch has been modified to...
都可以的1年前查看全部
- 一道令人发疯的化学题某课外兴趣小组对一批铁样品(含有杂质,杂质不溶于水,也不与盐酸反应)进行分析.甲乙丙三位同学分别进行
一道令人发疯的化学题
某课外兴趣小组对一批铁样品(含有杂质,杂质不溶于水,也不与盐酸反应)进行分析.甲乙丙三位同学分别进行试验,其中只有一位同学所取用的稀硫酸与铁样品恰好反应.实验数据如下(烧杯的质量为25.4g).
甲 乙 丙
烧杯+稀硫酸 200g 150g 150g
加入的铁样品 9g 9g 14g
充分反映后,烧杯+剩余物 208.7g 158.7g 163.7g
1、那位同学所取用的稀硫酸与铁样品恰好完全反应
2、计算样品中铁的质量分数
3、计算恰好完全反应后所得溶液中溶质的质量分数
先谢谢答题的哥哥姐姐了!
还请来点步骤 歪歪大虾1年前1
歪歪大虾1年前1 -
 honje2000 共回答了13个问题
honje2000 共回答了13个问题 |采纳率92.3%(1)乙同学
(2)设铁的质量分数为x,FeSO4质量为y
Fe + H2SO4 = FeSO4 + H2↑
56 154 2
9×x y 150+9-158.7
x=93.3%
y=23.1
铁中的杂质为:9×(1-93.3%)=0.603g
所以恰好完全反应后所得溶液中溶质的质量分数为:
23.1÷(158.7-25.4-0.603)=17.4%1年前查看全部
- 小雨同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉末搅拌溶解,静置一会儿,采用如图所示装置进行过滤,请回答过滤后仍然浑浊的
 小雨同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉末搅拌溶解,静置一会儿,采用如图所示装置进行过滤,请回答过滤后仍然浑浊的原因是什么?(至少写出三条)
小雨同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉末搅拌溶解,静置一会儿,采用如图所示装置进行过滤,请回答过滤后仍然浑浊的原因是什么?(至少写出三条)  步履无需匆匆1年前1
步履无需匆匆1年前1 -
 janesn 共回答了15个问题
janesn 共回答了15个问题 |采纳率80%解题思路:根据过滤(“一贴、二低、三靠”的原则)操作的注意事项进行分析解答即可.过滤后滤液仍浑浊,可能原因是滤纸破损(会使得液体中的不溶物进入下面的烧杯,从而使得滤液浑浊)、液面高于滤纸边缘(会使部分液体未经过滤纸的过滤直接流下,该操作会使滤液仍然浑浊)或盛接滤液的烧杯不干净等.
故答案为:(1)滤纸破损;(2)液面高于滤纸边缘;(3)仪器不干净.
故答案为:(1)滤纸破损;(2)滤液边缘高于滤纸边缘;(3)盛接滤液的烧杯不干净.点评:
本题考点: 过滤的原理、方法及其应用.
考点点评: 本题难度不大,掌握过滤操作(“一贴、二低、三靠”的原则)的注意事项等即可正确解答本题.1年前查看全部
- 有一块20m3的矿石,为了测出它的质量,从它上面取10cm3样品,测得样品的质量为26g,根据以上数据求出矿石的密度和质
有一块20m3的矿石,为了测出它的质量,从它上面取10cm3样品,测得样品的质量为26g,根据以上数据求出矿石的密度和质量?
 姜平平1年前0
姜平平1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 向16g黄铜(由锌、铜形成的合金)样品中加入稀硫酸充分反应,所加稀硫酸与生成气体的质量关系如图所示,求:
向16g黄铜(由锌、铜形成的合金)样品中加入稀硫酸充分反应,所加稀硫酸与生成气体的质量关系如图所示,求:
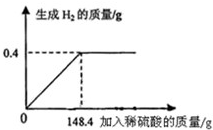
(1)样品中锌的质量分数.(保留一位小数)
(2)所用的稀硫酸中溶质的质量.
(3)恰好完全反应时,所得反应后溶液中溶质的质量分数. 1jxw1年前1
1jxw1年前1 -
 xysth 共回答了23个问题
xysth 共回答了23个问题 |采纳率87%解题思路:本题涉及的反应Zn+H2SO4═ZnSO4+H2↑,图象为充分反应所生成氢气的质量随加入稀硫酸质量的变化情况.根据曲线可确定加入148.4g稀硫酸时与锌恰好完全反应放出0.4g氢气,运用化学方程式可求反应的硫酸的质量,由氢气质量计算参加反应锌的质量及生成硫酸锌的质量,最后由质量守恒定律计算反应后所得溶液质量,完成所得溶液中溶质的质量分数的计算.设样品中锌的质量为x,生成硫酸锌的质量为y.反应的硫酸的质量是z,由图分析可知产生氢气0.4g.
Zn+H2SO4═ZnSO4+H2↑
6598161 2
xzy 0.4g
[65/x=
98
z=
161
y=
2
0.4g]
x=13g y=32.2g z=19.6g
(1)样品中锌的质量分数为[13g/16g]×100%=81.25%
(2)所用的稀硫酸中溶质的质量为19.6g;
(3)恰好完全反应时,所得溶液中溶质的质量分数=[32.2g/13g+148.4g-0.4g]×100%=20%
答:(1)样品中锌的质量分数为81.25%;(2)所用的稀硫酸中溶质的质量为19.6g;(3)所得硫酸锌溶液中溶质的质量分数为20%.点评:
本题考点: 根据化学反应方程式的计算;有关溶质质量分数的简单计算.
考点点评: 解答此类问题的根本点在于对反应图象的曲线进行分析,曲线的折点表示此时恰好完全反应.1年前查看全部
- 英语翻译翻译:我会在周一确认后尽快给你回复.我们可以根据你的尺寸做这个盒子,你可以提供一个样品给我们参考吗?或者你提供我
英语翻译
翻译:我会在周一确认后尽快给你回复.我们可以根据你的尺寸做这个盒子,你可以提供一个样品给我们参考吗?或者你提供我们盒子的内部的图稿给我们参考. 专砸YY毒妇1年前1
专砸YY毒妇1年前1 -
 百诗02 共回答了16个问题
百诗02 共回答了16个问题 |采纳率93.8%I will on Monday after the confirmation reply to you as soon as possible. We can do this box according to your size, you can provide us with reference to asample? Or if you provide us with the box art...1年前查看全部
- 某化学小组利用如图所示装置测定铜锌合金样品中锌的质量分数(图中固定装置已略去)探究过程如下:
 某化学小组利用如图所示装置测定铜锌合金样品中锌的质量分数(图中固定装置已略去)探究过程如下:
某化学小组利用如图所示装置测定铜锌合金样品中锌的质量分数(图中固定装置已略去)探究过程如下:
I连接实验装置并检查装置气密性
II向B中加入质量为m的铜锌合金粉末,由注射器A向B缓缓加入稀硫酸,待B中不再有气体产生气体时,夹紧弹簧夹,立即移出D中导管,准确读取并记录量筒内水的体积.
III经过滤等操作,准确称量并记录B中剩余固体物质的质量.
IV该小组的甲同学根据反应前后B中固体物质的质量计算样品中锌的质量分数;乙同学认定量筒内测得水的体积
即为反应生成气体的体积,并利用该气体在常温下的密度,根据化学方程式进行相关计算,得到样品中锌的质量分数.请回答下列问题:
(1)Ⅲ中,正确的操作顺序是:过滤、______、______、称量.
(2)通过误差分析,化学小组发现乙同学所用数据不可靠.造成该数据不可靠的原因及其对计算结果的影响是:
①II中,移出D中的导管内留存有水,导致计算结果偏小.
②______.
…
(3)日常生活中为方便使用通常将金属制成合金,伍角币为钢芯镀铜、一元币为钢芯镀镍(Ni)合金
①铸造以上硬币用到的材料都是______材料
②选择铸造硬币的材料不需要考虑的因素是______(填序号).
A.金属的导电性B.金属的耐腐蚀性
C.金属的硬度D.金属价格与硬币面值的吻合度
③以上硬币涉及到Fe、Cu、Al、Ni(镍),已知Ni能够发生如下反应:
Ni+H2SO4=NiSO4+H2↑Fe+NiCl2=Ni+FeCl2
四种金属活动性由强到弱的顺序为______(用元素符号表示). bobolin1年前1
bobolin1年前1 -
 aicrebecca 共回答了19个问题
aicrebecca 共回答了19个问题 |采纳率100%(1)从铜和硫酸锌溶液的混合物中得到铜,先进行过滤,得到沾有硫酸锌溶液的铜,再进行洗涤除去表面的硫酸锌,再进行干燥除去水即可;(2);由于锌与硫酸反应生成硫酸锌和氢气时,放出热量,如果没等冷却到室温,根...1年前查看全部
- xrd样品表面为什么要平整
 红星足球11号1年前1
红星足球11号1年前1 -
 zhang7peng 共回答了15个问题
zhang7peng 共回答了15个问题 |采纳率93.3%xrd的原理是根据布拉格方程计算d值,要求样品平面(衍射面)必须位于布拉格方程的焦点上,这样计算所得的d值才是准确的,否则就不准了.1年前查看全部
- 某同学去吃火锅发现了一种固体燃料,他对其产生了浓厚的兴趣,便取了这种固体样品46g,燃烧后测其产物质量
某同学去吃火锅发现了一种固体燃料,他对其产生了浓厚的兴趣,便取了这种固体样品46g,燃烧后测其产物质量
发现生成二氧化碳88g,水54g.
(1)该燃料含有哪些元素?
(2)若该物质的相对分子质量为46,求其化学式.
(3)帮助该同学想一想该物质的其他一种用途. 红黄蓝xyl1年前3
红黄蓝xyl1年前3 -
 spider102 共回答了19个问题
spider102 共回答了19个问题 |采纳率89.5%1、根据质量守恒定律可知可燃物在氧气中燃烧生成生成CO2与H2O,生成物中的碳元素、氢元素都是燃料中所含的元素
m(C)=88g×12/44=24g m(H)=54g×2/18=6g
参加反应的固体燃烧的质量为46g,而碳、氢元素的质量之和为30g,说明这各物质中还含有氧元素.
2、m(O)=46g-24g-6g=16g
m(C):m(H):m(O)=24g:6g:16g=12:3:8
设该物质的化学式为CxHyOz,则12x :1y :16z=12:3:8 x:y:z=2:6:1
所以它的化学式是C2H6O (C2H5OH)
3、医疗上用作消毒剂1年前查看全部
- 生产加碘盐通常是在氯化钠中加入碘酸钾(KIO3).为检验某食用盐样品中是否含有碘元素,某同学采用以下反应进行实验:KIO
生产加碘盐通常是在氯化钠中加入碘酸钾(KIO3).为检验某食用盐样品中是否含有碘元素,某同学采用以下反应进行实验:KIO3+5KI+3H2SO4═3K2SO4+3H2O+3X,则物质X的化学式为下列的( )
A. O2
B. H2
C. I2
D. I2O5 qzhq8171年前1
qzhq8171年前1 -
 88006044 共回答了15个问题
88006044 共回答了15个问题 |采纳率86.7%解题思路:根据质量守恒定律的微观解释:化学反应前后原子的种类和数目不变.可知在化学反应方程式中,反应物和生成物中所含的原子的种类和数目相同.由此可推断化学反应方程式中反应物或生成物的化学式.根据质量守恒定律和化学方程式可得,X的化学式中含有K的个数为:(1+5-3×2)÷3=0,含有I的个数为:(1+5)÷3=2,含有O的个数为:(3+3×4-3×4-3)÷3=0,含有H的个数为:(3×2-3×2)÷3=0,含有S的个数为:(3-3)÷3=0;则X的化学式为:I2.
故选C.点评:
本题考点: 有关化学式的计算和推断;质量守恒定律及其应用.
考点点评: 本题主要考查学生运用质量守恒定律进行推断的能力.利用质量守恒定律可以计算出元素的原子个数,据此推断出化学式.1年前查看全部
- 问一道化学题,急!某校化学兴趣小组用下图所示装置测定铜粉样品(含杂质碳)中铜的质量分数。 (1)装置A中发生反应的化
问一道化学题,急!
某校化学兴趣小组用下图所示装置测定铜粉样品(含杂质碳)中铜的质量分数。

(1)装置A中发生反应的化学方程式为 。
(2)装置B的作用是 。
(3) 装置C增重2g,装置D增重4.4g,装置D发生反应的化学方程式为 。
(4)样品中铜的质量分数为 。(结果保留一位小数)
(5)该实验存在一定误差,导致误差的原因有 。(写一条即可)
答案我知道,主要是求(4)的具体过程,应该是91.4%,我算不出来。
 钰泉1年前1
钰泉1年前1 -
 sailormu 共回答了13个问题
sailormu 共回答了13个问题 |采纳率92.3%C + O2 = CO2;D装置增重4.4g,说明含碳1.2g。
2Cu + O2 = 2CuO;C装置增重2g,说明增重氧的质量是:2+1.2=3.2g,
被氧化的铜的质量就是12.8g。
Cu%=12.8/(12.8+1.2)=91.4%1年前查看全部
- 某碳酸钾样品中含有碳酸钠、硝酸钾和硝酸钡三种杂质中的一种或两种.现将13.8g样品加入到足量水中,样品全部溶解.再加入过
某碳酸钾样品中含有碳酸钠、硝酸钾和硝酸钡三种杂质中的一种或两种.现将13.8g样品加入到足量水中,样品全部溶解.再加入过量的氯化钙溶液,得到9g沉淀.对样品所含杂质的正确的判断是( )
A. 肯定有硝酸钾,肯定没有碳酸钠
B. 肯定有硝酸钡,可能还含有碳酸钠
C. 肯定没有硝酸钡,肯定有硝酸钾
D. 肯定没有硝酸钡和碳酸钠 李梦雯1年前1
李梦雯1年前1 -
 wangkkk1 共回答了20个问题
wangkkk1 共回答了20个问题 |采纳率95%解题思路:取样品加入水中,全部溶解,则不可能硝酸钡,因为硝酸钡能与碳酸钾反应生成碳酸钡的沉淀,加入氯化钙能产生沉淀,然后根据沉淀的质量进一步确定碳酸钠和硝酸钾的存在.样品加入水中,全部溶解,说明一定无硝酸钡,因为硝酸钡能与碳酸钾反应生成碳酸钡的沉淀;
假设13.8g纯碳酸钾产生碳酸钙的质量为x,则有
K2CO3+CaCl2═CaCO3↓+2KCl
138 100
13.8g x
[138/13.8g=
100
x]
x=10g
假设13.8g为纯碳酸钠则设产生碳酸钙的质量为y,则有
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100
13.8gy
[106/13.8g=
100
y]
y≈13g
若含有碳酸钠则得到沉淀的质量应该大于10g小于13g,而实际只得到9g,故可能含有碳酸钠,一定含有硝酸钾,观察选项,B、C的判断合适.
故选:BC;点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 本题考查了物质共存的问题以及根据化学方程式的计算,完成此题,可以依据已有的知识进行,判断混合物的组成时,要采用极值法和平均值法.1年前查看全部
- 有一根在空气中放置一段时间的镁条样品,其质量为2.56g,将该样品投入到50g足量稀盐酸中,充分反应后称得混合物的质量为
有一根在空气中放置一段时间的镁条样品,其质量为2.56g,将该样品投入到50g足量稀盐酸中,充分反应后称得混合物的质量为52.38g.(1)样品中未被氧化的没镁的质量是多少(2)该镁条未被氧化时的质量是多少
 wtuynfce7501年前1
wtuynfce7501年前1 -
 一柄断剑 共回答了22个问题
一柄断剑 共回答了22个问题 |采纳率90.9%生成氢气的质量为 2.56g+50g-52.38g=0.18g
Mg+2HCl=MgCl2+H2
24 2
x 0.18g
24/x=2/0.18g
x=2.16g
(1)样品中未被氧化的镁的质量是 2.16g
氧化镁中镁的质量为 (2.56g-2.16g)*24/40=0.24g
(2)该镁条未被氧化时的质量是 2.16g+0.24g=2.4g1年前查看全部
- 为了研究物质的某种特性,某同学选用了三种不同材料制成的长方体样品,他用实验中测得和经过计算的数据见下表.
为了研究物质的某种特性,某同学选用了三种不同材料制成的长方体样品,他用实验中测得和经过计算的数据见下表.
(1)在表中空白处填上适当的数据;实验次数 样品 质量
(g)体积
(cm3)质量/体积
(g/cm3)1 铝块1 21.6 8.0 2.7 2 铝块2 43.2 16.0 2.7 3 松木1 4.0 8.0 0.5 4 松木2 16.0 32.0 ______ 5 钢块 71.2 8.0 8.9
(2)对实验1、2或3、4中的实验数据进行比较,可以得的结论是,同种物质,它的质量跟体积成______质量与体积的比值______;
(3)比较1、3、5中的实验数据,可以得出的结论是;相同体积的不同物质,质量______,不同物质的______一般不相同. ihaigh1年前0
ihaigh1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 英语翻译简单的英文翻译,1)此样品(样板)仍未通过总部验证,我们过几天后会寄样品到总部验证,等结果出来后再通知你.2)由
英语翻译
简单的英文翻译,
1)此样品(样板)仍未通过总部验证,我们过几天后会寄样品到总部验证,等结果出来后再通知你.
2)由于此样品(样板)还在开发中,需要等待一段时间,开发出来后我们会尽快寄给你.
3)由于LINDA在休婚假(15天),由于我不是负责开发样板,你所提的问题我不是很清楚,所以不能给你答复,我会将你的问题告知LINDA,等她回来再给你回复.
4)产品我们正在生产当中,需花费几天时间.给你带来不便非常抱歉
5)8号我们已寄出6件样品给你(少6件),今天我们再补6件给你,请查收. 浮生心若羽1年前1
浮生心若羽1年前1 -
 点点星光片片云 共回答了18个问题
点点星光片片云 共回答了18个问题 |采纳率88.9%1) this sample (pattern) still haven't verified by headquarters, we had a few days later they will send you samples to headquarters validated, until the result and notify your
2) for this sample (pattern) still in development, the need for a period of time, developed, we will send to you as soon as possible.
3) linda's on holiday to the marriage () 15 days because i am not responsible for developing pattern. the questions i am not quite clear, so i can't give you an answer. i will you let us know linda until she came back and call you back.
4) product we are the production costs of several days. i'm very sorry to cause you inconvenience1年前查看全部
- 还原糖测定时乳制品样品处理添加乙酸锌和亚铁氰化钾的目的是什么
还原糖测定时乳制品样品处理添加乙酸锌和亚铁氰化钾的目的是什么
这两种试剂在样品处理中有什么作用吗? 数学课1年前1
数学课1年前1 -
 huawel 共回答了21个问题
huawel 共回答了21个问题 |采纳率100%沉淀蛋白1年前查看全部
- 在做重氮化分析时,用NaNO2和HCL与氨基进行重氮反应,而分析条件中要求加入溴化钾溶液或溴化钾,且不同的样品要求加入溴
在做重氮化分析时,用NaNO2和HCL与氨基进行重氮反应,而分析条件中要求加入溴化钾溶液或溴化钾,且不同的样品要求加入溴化钾的量也不同,请问溴化钾在重氮化反应中起什么作用?为何用量又大不相同?
 大灰狼东东1年前1
大灰狼东东1年前1 -
 qiuqingxu 共回答了17个问题
qiuqingxu 共回答了17个问题 |采纳率88.2%主要是防止NaNO2(氧化剂,有强氧化性)的过量,一旦NaNO2过量将会对反应产生不利影响,为减少这种副反应根据对合成参数(收率,产量,温度,原料的质量的多少)的要求会加入适量的KBr(有还原性,作还原剂)NO2-+Br-+H+----N2+Br2(BrO3-)+H2O1年前查看全部
- 英语翻译1、由于时间很紧张,加上现在这个交易会的季节,工厂无太多精力去为我们大量制作样品,所以,每款风格只能提供2-3s
英语翻译
1、由于时间很紧张,加上现在这个交易会的季节,工厂无太多精力去为我们大量制作样品,所以,每款风格只能提供2-3set的样品,请见谅.
2、需要重新修改的样品已经完成,明天可以寄出.包括以下:
3、各3套 预计10月6日前可以寄出,这次我们会稍微修改,浮雕部分会更加明显,效
果会更加好. 德莫克休思1年前1
德莫克休思1年前1 -
 流浪在kk 共回答了16个问题
流浪在kk 共回答了16个问题 |采纳率93.8%手工翻译,希望对你有帮助,祝你工作顺利O(∩_∩)O哈!
Dear Amy,
Please kindly note below points:
1)As the time is very tension and we are at the season of trade fair. The factory could not do a large number of samples for us. So the samples for each style could only provide 2-3pcs samples to you. Please understand.
2)The samples needed to be revised has finished at present and will be sent out. It includes as follows:
3)It is expected that three sets for each style will be sent our on 6th October and we will make minor amendment for this time, the embossed part will be more abvious as well, but also the effect will be better than before.
Thanks for your early reply.
Best Regards,
Tony1年前查看全部
- (2009•大庆)某研究性学习小组的同学为了解某地区的地质情况,从实地取回两块样品A和B,进行如下图所示的实验(图中部分
(2009•大庆)某研究性学习小组的同学为了解某地区的地质情况,从实地取回两块样品A和B,进行如下图所示的实验(图中部分反应产物被略去).

(1)请你根据上图实验现象推断下列物质的化学式.A:______;B:______.
(2)写出下列转化的化学方程式.
E→G:CO2+C
2CO高温 .CO2+C;
2CO高温 .
C→D:______;
A+G→I:3CO+Fe2O3
2Fe+3CO2高温 .3CO+Fe2O3.
2Fe+3CO2高温 .
(3)所加试剂X可能是氧化物、酸、碱、盐中的______. 闲时逛逛1年前1
闲时逛逛1年前1 -
 水果布丁6 共回答了23个问题
水果布丁6 共回答了23个问题 |采纳率82.6%解题思路:(1)根据J溶液是浅绿色,所以J中有亚铁离子,金属单质和X会生成亚铁离子,所以I就是铁,D是红褐色的沉淀,所以D是氢氧化铁,H是碱,C是黄色的溶液,是由红色固体A和盐酸反应生成的,所以C是氯化铁,A就是氧化铁;氧化铁和气体G会生成铁单质,G是由E和碳高温生成的,所以G是一氧化碳,E是二氧化碳,F会与水生成碱,所以F是氧化钙,B主要成分是碳酸钙,将推出的物质验证即可;
(2)根据(1)中推出的反应物、生成物书写方程式;
(3)根据铁和X反应生成的是亚铁离子进行分析.(1)J溶液是浅绿色,所以J中有亚铁离子,金属单质和X会生成亚铁离子,所以I就是铁,D是红褐色的沉淀,所以D是氢氧化铁,H是碱,C是黄色的溶液,是由红色固体A和盐酸反应生成的,所以C是氯化铁,A就是氧化铁;氧化铁和气体G会生成铁单质,G是由E和碳高温生成的,所以G是一氧化碳,E是二氧化碳,F会与水生成碱,所以F是氧化钙,B主要成分是碳酸钙,经过验证各种物质都满足转换关系,故答案为:Fe2O3CaCO3
(2)二氧化碳和碳在高温的条件下生成一氧化碳,故答案为:CO2+C
高温
.
2CO
氯化铁和氢氧化钙反应生成氢氧化铁沉淀和氯化钙,故答案为:2FeCl3+3Ca(OH)2═2Fe(OH)3↓+3CaCl2
氧化铁和一氧化碳在高温的条件下生成铁和二氧化碳,故答案为:3CO+Fe2O3
高温
.
2Fe+3CO2
(3)铁在置换反应中才能转化成亚铁离子,所以X是酸或盐,故答案为:酸或盐.
故答案为:
(1)Fe2O3CaCO3
(2)CO2+C
高温
.
2CO
2FeCl3+3Ca(OH)2═2Fe(OH)3↓+3CaCl2;3CO+Fe2O3
高温
.
2Fe+3CO2
(3)酸或盐点评:
本题考点: 物质的鉴别、推断;化学式的书写及意义;书写化学方程式、文字表达式、电离方程式.
考点点评: 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质题中的转换关系推导剩余的物质,最后进行验证即可.1年前查看全部
- (2012•湘潭)有一包固体粉末样品,含有Na2CO3、CaCO3、Zn三种物质.为进一步确定其组成,某实验小组进行了以
(2012•湘潭)有一包固体粉末样品,含有Na2CO3、CaCO3、Zn三种物质.为进一步确定其组成,某实验小组进行了以下探究活动.
【思考与交流】
(1)上述物质中,能溶于水的是______(填化学式).
(2)它们均能与盐酸反应,写出锌与盐酸反应的化学方程式______.
【活动与探究】
经过讨论,他们设计并完成了下列实验:
(3)用托盘天平(1g以下用游码)称取37.7g样品.称量时砝码应置于______(填“左”或“右”)盘,则所称固体的实际质量为______g.
(4)往37.7g样品中加入足量稀盐酸,可观察到产生大量气体,其组成为氢气和______(填化学式.注意:少量氯化氢和水蒸气忽略不计);将所得气体缓慢通入足量氢氧化钠溶液中,待反应完全后,称得该溶液增重13.2g;再将剩余气体通过足量灼热氧化铜粉末,充分反应后冷却称重,发现该粉末反应后比反应前减轻1.6g.
【分析与总结】
(5)上述过程中氧化铜粉末减轻1.6g是由于氢气与氧化铜反应所致,该反应的化学方程式为CuO+H2
Cu+H2O△ .CuO+H2,由此可推知反应中氢气的质量为______g.
Cu+H2O△ .
(6)根据以上数据计算并确定37.7g样品中三种物质的质量. 孤云自闲1年前1
孤云自闲1年前1 -
 tellnothing 共回答了15个问题
tellnothing 共回答了15个问题 |采纳率86.7%解题思路:(1)碳酸钙、锌不溶于水,碳酸钠易溶于水;
(2)根据反应物、生成物及其质量守恒定律可以书写化学方程式;
(3)用天平称量时,要注意的是应该左物右砝;
(4)碳酸钠、碳酸钙和稀盐酸反应都能够生成二氧化碳气体;
(5)通过计算可以确定物质的组成情况.(1)上述物质中,能溶于水的是碳酸钠,化学式是Na2CO3.
故填:Na2CO3.
(2)锌与盐酸反应能生成氯化锌和氢气,反应的化学方程式为:Zn+2HCl═ZnCl2+H2↑.
故填:Zn+2HCl═ZnCl2+H2↑.
(3)称量时砝码应置于右盘,则所称固体的实际质量为37.7g.
故填:右;37.7.
(4)往37.7g样品中加入足量稀盐酸,可观察到产生大量气体,其组成为氢气和二氧化碳,二氧化碳的化学式是CO2.
故填:CO2.
(5)氧化铜和氢气在加热条件下反应能生成铜和水,反应的化学方程式为:CuO+H2
△
.
Cu+H2O.
故填:CuO+H2
△
.
Cu+H2O.
由氧化铜和氢气反应的化学方程式可知,当参加反应的氢气的质量是2份时,固体质量减少的是16份,
设氢气的质量为X,
则有:2:16=X:1.6g,
X=0.2g.
故填:0.2.
(6)设锌的质量为Y,
Zn+2HCl═ZnCl2+H2↑,
65 2
Y 0.2g
[65/2]=[Y/0.2g],
Y=6.5g,
将所得气体缓慢通入足量氢氧化钠溶液中,待反应完全后,称得该溶液增重13.2g,说明生成的二氧化碳的质量是13.2g,
碳酸钙和碳酸钠的质量和为:37.7g-6.5g=31.2g,
设碳酸钙的质量为m,生成二氧化碳的质量为n,
CaCO3+2HCl=CaCl2+H2O+CO2↑,Na2CO3+2HCl=2NaCl+H2O+CO2↑,
1004410644
mn31.2g-m13.2g-n
[100/44]=[m/n],[106/44]=[31.2g−m/13.2g−n],
m=10g,n=4.4g,
碳酸钠的质量为:31.2g-10g=21.2g,
碳酸钠、碳酸钙、锌的质量分别为21.2g、10g、6.5g.点评:
本题考点: 实验探究物质的组成成分以及含量;称量器-托盘天平;酸的化学性质;酸碱盐的溶解性;书写化学方程式、文字表达式、电离方程式;根据化学反应方程式的计算.
考点点评: 差量法在计算中经常遇到,要掌握差量法计算的技巧,并且能够熟练运用,对解答计算方面的题目帮助很大.1年前查看全部
- 某化学兴趣小组为测定生铁样品中单质铁的质量分数,取一只烧杯,称得其质量为70.4g,加入一定量生铁样品碎屑,称得烧杯和样
某化学兴趣小组为测定生铁样品中单质铁的质量分数,取一只烧杯,称得其质量为70.4g,加入一定量生铁样品碎屑,称得烧杯和样品的总质量为102.4g,向产有生铁样品的烧杯中加入稀硫酸,边加边搅拌,直到烧杯中不再产生气泡,共用去稀硫酸247.3g,此时称得烧杯和剩余物质的总质量为348.7g,试计算改生铁样品中单质铁的质量分数,
 不平则鸣5151年前1
不平则鸣5151年前1 -
 cd0925 共回答了20个问题
cd0925 共回答了20个问题 |采纳率90%生成氢气质量为 102.4g+247.3g-348.7g=1g
Fe + H2SO4 === FeSO4 + H2↑
56 2
x 1g
56/x=2/1g
x=28g
生铁样品中单质铁的质量分数 28g/(102.4g-70.4g)*100%=87.5%1年前查看全部
- 某样品为铜和氧化铜混合物为测定样品中氧化铜质量分数,称10克样品在空气中充分加热直至固体质量不再变化
某样品为铜和氧化铜混合物为测定样品中氧化铜质量分数,称10克样品在空气中充分加热直至固体质量不再变化
冷却后称量反应后固体质量为11.6克
计算样品中氧化铜的质量分数? lijinxing20021年前1
lijinxing20021年前1 -
 宁波圣豹行者无疆 共回答了22个问题
宁波圣豹行者无疆 共回答了22个问题 |采纳率81.8%铜和氧气高温生成氧化铜,增加的1.6g质量也就是原来铜的质量10g-1.6g就是样品中氧化铜的质量,再除10就能算出质量分数了Cu + O2 = CuO2
56 88
10-X 11.6-X
56(11.6-X)=(10-X)88
x=7.21年前查看全部
- 某矿石样品中可能含有碳酸钙、二氧化硅、氧化铝、氧化镁等化合物,
某矿石样品中可能含有碳酸钙、二氧化硅、氧化铝、氧化镁等化合物,
经测定各元素质量分数的模型如图甲,由此可推测,该样品中不可能含有的化合物是 .

某矿石样品中吭含有碳酸钙、二氧化钙,氧化铝、氧化镁等化合物. 糗gg你1年前1
糗gg你1年前1 -
 haogui123456 共回答了17个问题
haogui123456 共回答了17个问题 |采纳率88.2%一定没有碳酸钙
因为这图里根本就没有碳元素的质量分数
没有碳元素怎么会有碳酸钙呢.1年前查看全部
- 某化学探究小组称取6g镁铜合金样品于烧杯中,然后将80g稀硫酸分四次加入,充分反映后过滤,洗涤,干燥,称重,得到的实验过
某化学探究小组称取6g镁铜合金样品于烧杯中,然后将80g稀硫酸分四次加入,充分反映后过滤,洗涤,干燥,称重,得到的实验过程中有关物质的用量及质量测定记录如下.
第一次加入稀硫酸的质量 20g
剩余固体的质量4.8g
第二次加入稀硫酸的质量 20g
剩余固体的质量mg
第三次加入稀硫酸的质量 20g
剩余固体的质量2.4g
第四次加入稀硫酸的质量 20g
剩余固体的质量1.8g
问题:
1.上述表格中m的值
2.该合金中Mg的质量分数
3.实验操作结束后的溶液中溶质的化学式
4.所用稀硫酸中溶质的质量分数
5.反映后所得溶液的总质量
希望能有人给出解答过程,不要只给答案,谢谢.
 发骚男人1年前1
发骚男人1年前1 -
 zihuoyanyan 共回答了13个问题
zihuoyanyan 共回答了13个问题 |采纳率100%第四次加入稀硫酸,剩余固体的质量还减小,所以第三次加入稀硫酸,镁还过量,
前后次加入稀硫酸,每次减小0.12克,所以
1.上述表格中m=3.6克
2.该合金中Mg的质量分数=(6-1.8)/6=70%
3.实验操作结束后的溶液中溶质的化学式:MgSO4
Mg + H2SO4 = MgSO4 + H2
24 98
6-4.8=1.2 X
X=4.9g
4.所用稀硫酸中溶质的质量分数=1.2/20=6%
Mg + H2SO4 = MgSO4 + H2
24 120 2
6-1.8=4.2 Y Z
Y=21g
Z=0.35g
5.反映后所得溶液的总质量=4.8+80-0.35=84.45g1年前查看全部
- 弹簧材料选用,本司有一产品应用到弹簧,样品线径分别为5.5与5mm的组合弹簧,
弹簧材料选用,本司有一产品应用到弹簧,样品线径分别为5.5与5mm的组合弹簧,
在使用过程中受压缩处理,通过测试弹力来判定合格性能,要求在使用5000次后弹簧弹力在5%内符动,现有两种材料选用60si2mn 50CrV材料.大弹簧自由长度133,最大压缩长度为75
请问材料如何选择,如果进行验收呢.其它常规材料可否代替呢.
使用情况是在室外使用,应该可以满足要求的,另外你说的这些在设计手册上都能查到呀,我这些零件应用于高压开关里面的,利用弹簧的储能与释放,而释放的时间只有0.8秒,要达到这一要求更难了; nnmm1441年前1
nnmm1441年前1 -
 正在充值中deIQ卡 共回答了13个问题
正在充值中deIQ卡 共回答了13个问题 |采纳率100%60Si2Mn 50CrV 是弹簧钢
化学成分分别为:
60Si2Mn C:0.56-0.64 Si:1.50-2.00 Mn:0.60-0.90 Cr:0.35
50CrV C:0.46-0.54 Si:0.17-0.37 Mn:0.50-0.80 Cr:0.80-1.10 V:0.10-0.20
直径稍大,需用热成型工艺生产的弹簧多采用60Si2Mn,如汽车板簧,铁路车辆的缓冲簧.
对于高应力的重要弹簧可采用50CrV,常用于高级轿车板簧,发动机气门弹簧等.
至于验收的话,你要做疲劳试验来检验其是否符合要求
要是替代的话建议你用琴钢线,力值和抗疲劳度可以达到,但是使用环境适不适合就不知道了1年前查看全部
- 蔗糖的还原糖反应原理有人说空白应该比样品多但 我有过样品比空白多的时候请问 反应原理是什么?谢谢!请问1、加碱性枸橼酸铜
蔗糖的还原糖反应原理
有人说空白应该比样品多
但 我有过样品比空白多的时候
请问 反应原理是什么?
谢谢!
请问
1、加碱性枸橼酸铜后加热 为什么?
怎么生成的氧化亚铜?
2、之后 加碘化钾溶液和硫酸 产生了什么?
3、用硫代硫酸钠 是和那个基团反应?
谢谢!!! 家有棋子1年前1
家有棋子1年前1 -
 鞋店之王 共回答了20个问题
鞋店之王 共回答了20个问题 |采纳率95%一个蔗糖与一个水分子反应生两个葡萄糖
碱性枸橼酸铜,复分解反应氧化性不足以把铜氧化到+2
析出金属铜同时生成KIO3,方程式自己写吧,输入不方便
和H+反应!
生成沉淀和气体1年前查看全部
- 紫外线吸收法测核酸含量实验时为何加了钼酸铵-过氯酸沉淀剂后的样品在260nm处消光值更大大
 htywh1年前1
htywh1年前1 -
 gaoqi77 共回答了24个问题
gaoqi77 共回答了24个问题 |采纳率83.3%钼酸铵-过氯酸在260nm处有较大的吸收值.具体的请参阅文献 年燕兰《关于RNA定量测定方法中存在的问题和改进》.
导致这一现象的原因可能是因为①提取的核酸量较少,②钼酸铵-过氯酸用量过大.
个人意见,仅供参考.1年前查看全部
- 英语翻译因这次的样品尺寸的精密度要求更高,过多的手工样品报废.现因欠料,仅有195PCS良品,请知悉!
 keaigeren91年前4
keaigeren91年前4 -
 dd的树懒 共回答了24个问题
dd的树懒 共回答了24个问题 |采纳率79.2%a lot more handmade samples are scrapped because of the higher requirement of the sample size this time.because of the lack of material,there are only 195PCS good products.just let you know1年前查看全部
- 已知测得50克石灰水样品中含钙元素10克,求石灰水的纯度?
 Jolly1年前3
Jolly1年前3 -
 我爱何剑峰 共回答了14个问题
我爱何剑峰 共回答了14个问题 |采纳率85.7%石灰水的纯度:10*(74/40)/50=0.37=37%1年前查看全部
- 工业上制漂白粉的化学方程式为2Cl2+2Ca(OH)=Ca(ClO)2+CaCl2+2H2O.某干燥样品中有效成分(接下
工业上制漂白粉的化学方程式为2Cl2+2Ca(OH)=Ca(ClO)2+CaCl2+2H2O.某干燥样品中有效成分(接下)
(接上)Ca(ClO)2的质量分数为55%,则生产过程中Ca(OH)2的利用率为? A96.1% B86.4% C77.8% D71.3% 过程? 操之有道1年前1
操之有道1年前1 -
 pandoraeb 共回答了19个问题
pandoraeb 共回答了19个问题 |采纳率100%n(Ca(ClO)2)=55/143=0.3846mol
m(CaCl2)=0.3846*111=42.69g
m(Ca(OH)2)=100-55-42.69=2.3g
m(Ca(OH)2反应)=0.3846*2*74=56.9g
Ca(OH)2%=56.9/(56.9+2.3)=96.1%
A1年前查看全部
- 电泳时loading buffer和样品DNA比例多少?实验室常用6x的,为毛有人用1:5,有人1:1呢?3Q~
 眼小聚光1年前1
眼小聚光1年前1 -
 热带袋鼠 共回答了14个问题
热带袋鼠 共回答了14个问题 |采纳率78.6%这玩意,说白了就是溴酚蓝做一个参照,你不加都一样的能够跑出条带来,我从来都是1:10加的,没问题.所谓6X就是稀释6倍使用,你如果严格的话按1:5加.1年前查看全部
- 求一道化学计算题,尿素是一种肥效高的常用氮肥,其化学式为CO(NH2)2.现有一种尿素样品,测得氮元素的质量分数为43.
求一道化学计算题,
尿素是一种肥效高的常用氮肥,其化学式为CO(NH2)2.现有一种尿素样品,测得氮元素的质量分数为43.5%,试通过计算说明这份尿素样品室纯净物还是混合物. bboyyang1年前1
bboyyang1年前1 -
 泥宝 共回答了17个问题
泥宝 共回答了17个问题 |采纳率88.2%首先计纯尿素物质的N元素的质量分数:分子量N=14,O=16,H=1,C=12,CO(NH2)2总分析量=60,N%=(14*2)/60=46.6%,也就是说,纯尿素的N质量分数是46.6%,而实际是43.5%,因此不是纯净物1年前查看全部
- 纯碱样品(少量)溶于水,再加上过量CaCL2反应公式
 gtnygzz1年前2
gtnygzz1年前2 -
 fmanager1911 共回答了19个问题
fmanager1911 共回答了19个问题 |采纳率84.2%Na2CO3 + CaCl2 = CaCO3↓ + 2NaCl1年前查看全部
- 已知某种NH4NO3样品中混有不含氮元素的杂质,测得该NH4NO3样品中含氮的质量分数为24.5%,则样品中NH4NO3
已知某种NH4NO3样品中混有不含氮元素的杂质,测得该NH4NO3样品中含氮的质量分数为24.5%,则样品中NH4NO3的质量分数为( )
A. 24.5%
B. 49%
C. 70%
D. 80% 阿努夏农1年前1
阿努夏农1年前1 -
 月下刀 共回答了13个问题
月下刀 共回答了13个问题 |采纳率92.3%解题思路:欲正确解答本题,需计算出NH4NO3中氮元素的质量分数,再让NH4NO3样品中含氮的质量分数和它比较,即可计算出样品中NH4NO3的质量分数,然后从选项中选出符合的一项即可.NH4NO3中氮元素的质量分数为:
28
80×100%=35%,24.5%÷35%=70%,
故选C.点评:
本题考点: 混合物中某元素的质量计算.
考点点评: 本题主要考查学生对元素的质量分数的计算能力.1年前查看全部
- 含有元素M的某化合物的化学式为MNO3,已知它的相对分子质量为99,若有MNO3样品中M的质量分数为38.4%,求
含有元素M的某化合物的化学式为MNO3,已知它的相对分子质量为99,若有MNO3样品中M的质量分数为38.4%,求
样品中MNO3的质量分数为多少?(已算出M的相对原子质量为37) zp01081年前1
zp01081年前1 -
 蝶舞梦影 共回答了21个问题
蝶舞梦影 共回答了21个问题 |采纳率95.2%化学式为MNO3,已知它的相对分子质量为99,M=99-62=37.
37/99=37.4%,38.4%-37.4%=1%,该物质为M和MNO3的混合物,含有1%的单质M,含有99%的MNO3.1年前查看全部
- 若反应液显色时超过分光光度计的测定范围,应如何处理样品才能得到准确的总胆固醇含量
 谢仕玉1年前1
谢仕玉1年前1 -
 sf2qi 共回答了16个问题
sf2qi 共回答了16个问题 |采纳率87.5%稀释你的样品··直到落定范围或曲线的可计算范围·
譬如稀释50倍~
然后得出的结果X50就好1年前查看全部
- 用酚试剂测定空气中甲醛样品含量为1μg,采样体积为10L,采样时气温为20℃,大气压为
用酚试剂测定空气中甲醛样品含量为1μg,采样体积为10L,采样时气温为20℃,大气压为
麻烦要具体的公式~
用酚试剂测定空气中甲醛样品含量为1μg,采样体积为10L,采样时气温为20℃,大气压为0.973×105Pa,计算空气中甲醛的浓度 容若19791年前1
容若19791年前1 -
 vacuumwasa 共回答了24个问题
vacuumwasa 共回答了24个问题 |采纳率87.5%甲醛的物质的量=10^-6/30=3.33*10^-8mol
空气中甲醛的浓度=3.33*10^-8/10=3.33*10^-9mol/L1年前查看全部
- 跑蛋白的样品缓冲液每次都得现配吗
 红菡萏11年前1
红菡萏11年前1 -
 z1979312 共回答了22个问题
z1979312 共回答了22个问题 |采纳率86.4%跑蛋白是跑蛋白电泳(SDS-PAGE)吗?
如果是SDS-PAGE的样品缓冲液(一般是用5×Loading buffer)的话
不需要现配的,可以配置完成后放置在-20度保存.只需要在使用前加入2-ME就可以了
如果是加好2-ME的Loading buffer可以在室温下保存1个月左右1年前查看全部
- 了测定黄铜(铜,锌混合物)的组成,某研究性学习小组称取黄铜样品10g,向其中加入19.5百分号的稀硫酸50g
了测定黄铜(铜,锌混合物)的组成,某研究性学习小组称取黄铜样品10g,向其中加入19.5百分号的稀硫酸50g
完全反应后,称得烧杯中剩余的物质质量为59.9g.
①10g+50g-59.9g=0.1g表示( )的质量
②样品中铜的质量分数为( )
③通过计算反应后的溶液溶质中有无硫酸
麻烦哪位高手给我细细讲解下,我的化学真的不好~ 2727843451年前1
2727843451年前1 -
 clmmiky 共回答了17个问题
clmmiky 共回答了17个问题 |采纳率76.5%①10g+50g-59.9g=0.1g表示( 生成氢气 )的质量
铜与稀硫酸不反应
Zn+H2SO4=ZnSO4+H2
65 98 2
x y 0.1g
65/x=98/y=2/0.1g
x=3.25g
y=4.9g
②样品中铜的质量分数为(10g-3.25g)/10g*100%=67.5%
50g*19.5%=9.75g>4.9g
③反应后的溶液溶质中有硫酸1年前查看全部
- 有一座石碑,底面积为3㎡,高为5m,为测其质量,先取质量是54g,体积为20立方厘米的样品,
有一座石碑,底面积为3㎡,高为5m,为测其质量,先取质量是54g,体积为20立方厘米的样品,
求出石碑的质量 wyg401841年前3
wyg401841年前3 -
 allenarlen 共回答了20个问题
allenarlen 共回答了20个问题 |采纳率100%密度=m/v=54/20=2.7(g/立方厘米)=2.7×10^(-3)(kg/立方米)
V=S×h=3×5=15立方米
m=V×密度=15×2.7×10^(-3)=0.0405kg1年前查看全部
- 化学题有一种含有水的过氧化氢的样品 题目
化学题有一种含有水的过氧化氢的样品 题目
化学题有一种含有水的过氧化氢的样品.
有一种含有水的过氧化氢的样品100克,在二氧化锰的催化作用下,完全分解得到氧气3.2克.求:
(1)含有水的过氧化氢中,纯过氧化氢的质量是多少克?
(2)求该样品中过氧化氢的质量分数是多少?
初三的题 要详细解答过程 谢谢
 liuyanysl1年前1
liuyanysl1年前1 -
 望涯秋水 共回答了12个问题
望涯秋水 共回答了12个问题 |采纳率83.3%(1)氧气物质的量n=m/M=3.2/32=0.1 mol
2H2O2=(催化剂MnO2)2H2O+O2(气体)
n:0.2mol 0.1mol
过氧化氢的质量m=M×n=34×0.2=6.8g
(2)过氧化氢的质量分数为μ=6.8/100×100%=6.8%1年前查看全部
- 某硫酸铵样品中混有一种其他氮肥 经分析样品中含有百分之20.5的氮 则该样品中可能混有的氮肥是
某硫酸铵样品中混有一种其他氮肥 经分析样品中含有百分之20.5的氮 则该样品中可能混有的氮肥是
A尿素B硝酸铵C碳酸氢铵D氯化铵 飘摇jane1年前1
飘摇jane1年前1 -
 清新绿茶827 共回答了16个问题
清新绿茶827 共回答了16个问题 |采纳率93.8%(NH4)2SO4中N的质量分数为:21.2% 〉20.5% 所以混入的化肥中N的质量分数要小于20.5% 只能选C1年前查看全部
- 问一个关于薄层色谱的题样品在薄层色谱上展开,10MIN时有一RF值,则20MIN时展开的结果是()A 、RF值加倍 B.
问一个关于薄层色谱的题
样品在薄层色谱上展开,10MIN时有一RF值,则20MIN时展开的结果是()
A 、RF值加倍 B.RF不变 C.样品移行距离加倍 D.样品移行距离增加,但小于2倍
E,样品移行距离增加但大于2倍 ghs_721年前2
ghs_721年前2 -
 dgyclhytj 共回答了14个问题
dgyclhytj 共回答了14个问题 |采纳率85.7%BD:比移值是定性参数,在同一块板和相同条件下是定值,而样品的移行速度一般是先快后慢的.1年前查看全部
- 取某铁样品12g加入到盛有50g稀盐酸的烧杯(烧杯质量60g)中,在反应过程中对烧杯进行了四次称量,数据如下
取某铁样品12g加入到盛有50g稀盐酸的烧杯(烧杯质量60g)中,在反应过程中对烧杯进行了四次称量,数据如下
反应时间: T0 T2 T3 T4
烧杯和药品的质量:122 121.8 121.6 121.6
问:1.反应中产生氢气为?
2.列式计算:工业上要冶炼出上述铁24t,需要含氧化铁为百分之80的铁矿石多少吨?
 佳崴1年前1
佳崴1年前1 -
 一个可怜的小nn 共回答了17个问题
一个可怜的小nn 共回答了17个问题 |采纳率100%1、当质量恒定时,说明反应已经完成.
因此氢气质量m=12+50+60-121.6=0.4g
2、由2HCl+Fe==FeCl2+H2得到样品中的铁的质量为m1=0.4/2*56=11.2g
24t样品中含纯铁量为24*11.2/12=22.4t
含氧化铁为百分之80的铁矿石中纯铁的含量为56*2/(56*2+16*3)*80%=56%
所以需要含氧化铁为百分之80的铁矿石22.4/0.56=40t1年前查看全部
- 某液体样品中含有乳酸链球菌、枯草芽孢杆菌、和酿酒酵母菌,设计一个实验方案,将它们分离纯化出来?
 鲥绱囝囝1年前1
鲥绱囝囝1年前1 -
 坚定的探索者 共回答了22个问题
坚定的探索者 共回答了22个问题 |采纳率77.3%我对乳酸链球菌和酿酒酵母不太熟悉,不过普通的菌株分离纯化方法应该可以帮助你.
首先,选择一种合适的培养基,原则是这三种菌株可以正常生长,同时可以抑制其他菌株的生长.
第二,将液体样品稀释适当的梯度,涂板.涂板的标准以每个平板上200个菌落为准.
第三,挑取平板上的目标菌株于另外的平板上.
第四,对挑取的菌株划线培养,在挑取单菌落,进行鉴定.
这样基本可以得到分离的目的,不过还要看你的目标菌落的特性.枯草芽孢杆菌可以产生芽孢,在显微镜下可以清楚的看到,较为容易分辨.1年前查看全部
- 向10.6克可能含有碳酸钠、硝酸钠、硝酸钡的样品加水,全部溶解
向10.6克可能含有碳酸钠、硝酸钠、硝酸钡的样品加水,全部溶解
再将溶液加入过量氯化钙溶液有10克沉淀 判断样品组成 qq的人是不是我1年前2
qq的人是不是我1年前2 -
 Ж阿哟 共回答了15个问题
Ж阿哟 共回答了15个问题 |采纳率93.3%10克沉淀必定全为碳酸钙,故其物质的量为0.1mol,
由碳酸根守恒,知
碳酸钠的物质的量为0.1mol,
所以碳酸钠的质量为106*0.1=10.6g
故样品全为碳酸钠.
打这么多字不容易,1年前查看全部
- 有12g赤铁矿的样品经分析化验检测地其中汗三氧化二铁,质量为9.6g,求赤铁矿中铁元素的质量分数.其中含三氧化二铁(Fe
有12g赤铁矿的样品
经分析化验检测地其中汗三氧化二铁,质量为9.6g,求赤铁矿中铁元素的质量分数.
其中含三氧化二铁(Fe₂O₃) 幽冥妖蝶1年前1
幽冥妖蝶1年前1 -
 水果木斯里 共回答了25个问题
水果木斯里 共回答了25个问题 |采纳率84%先求铁元素质量 已知Fe2O3有9.6g 那么含铁为
9.6x 112/160=6.72g 也就是赤铁矿12g中含6.72g铁元素 所以质量分数为6.72/12=56%1年前查看全部
大家在问
- 1下列关于常见酸碱的说法,错误的是( )
- 2台湾岛是地壳的什么运动形成的?是地壳的上升运动还是下降运动?
- 3求一道一元函数利用导数求极限 最值的例题!
- 4如图是a、b、c三种物质的溶解度曲线,下列说法不正确的是( )
- 5手写信的好处英文作文
- 6关于三角函数!关于x的方程cosX+sinX=m在x∈[0,π]内有二解,则实数m的取值范围为______?
- 7作文:我不在粗心(420
- 8土壤中含有无机盐的证据是
- 96. Where’s Li Ming ? He ____________ (go) to the teacher’s o
- 1018.______ the light of what you have told me,I will say that
- 11.一个密闭铝盒,恰能悬浮在7℃的水中,在水温从7℃下降到1℃的过程中,关于铝盒的运动,某同学根据在相同的条件下,固体膨胀
- 12比地球角速度大的卫星相对于地球上的物体是怎么转的
- 1321、23、34、38、39
- 14已知,直线Y1=K1X+B1经过点(1,6)及(-2,-3),它和X轴,Y轴的交点是A,B,直线Y2=K2X+B2经过点
- 15有一只箩筐盛有几只西瓜,放在粗糙的水平地面上,箩筐与水平地面间的动摩擦因数为μ,若给箩筐一个水平初速度v0,让整筐西瓜在
