HCLO漂白的原因
 rugrats2022-10-04 11:39:549条回答
rugrats2022-10-04 11:39:549条回答
已提交,审核后显示!提交回复
共9条回复
 wrvhgphfik 共回答了11个问题
wrvhgphfik 共回答了11个问题 |采纳率100%- 次氯酸具有强氧化性,(Cl+1价),能和有色物质发生氧化还原反应,而使有色物质褪色.
- 1年前
 7135817 共回答了2个问题
7135817 共回答了2个问题 |采纳率- 次氯酸具有强氧化性,(Cl+1价),能和有色物质发生氧化还原反应,而使有色物质褪色。
- 1年前
 划图的铅笔 共回答了38个问题
划图的铅笔 共回答了38个问题 |采纳率- HCLO漂白是因为CLO-具有强氧化性
- 1年前
 失恋的感觉真--- 共回答了351个问题
失恋的感觉真--- 共回答了351个问题 |采纳率- 1价氯,强氧化性
- 1年前
 aicsnow99 共回答了147个问题
aicsnow99 共回答了147个问题 |采纳率- 次氯酸的漂白性主要是因为有强氧化性,如果写方程式的化,就是其分解的方程式:2HClO=2HCl+O2,这种新生成的氧非常活泼,如果你细心的话会联系到很多强氧化性的物质如浓硝酸,也可以分解释放氧气,所以也有强氧化性
- 1年前
 xiaozhu1221 共回答了95个问题
xiaozhu1221 共回答了95个问题 |采纳率- CL的化合价是+1,可以升高,有很强的氧化性质,所以具备漂白的作用
- 1年前
 BraveHeart1013 共回答了2个问题
BraveHeart1013 共回答了2个问题 |采纳率- HClO(光照)==HCl + O
这新生的‘原子氧’,具有强的氧化性。 这就决定了HClO的强氧化性,因而具漂白作用。 - 1年前
 朴正雨 共回答了14个问题
朴正雨 共回答了14个问题 |采纳率- 次氯酸根离子具有很强的氧化性,其中氯显正一价.
- 1年前
 zd3344 共回答了9个问题
zd3344 共回答了9个问题 |采纳率- 一楼那位....化合价升高体现的是还原性吧......
具体原因因该是CLO-是含氧酸根离子,有较高氧化性,比较活泼,可与有色物质反应使其变色.... - 1年前
相关推荐
- 5.用漂白粉溶液浸泡过的有色布条,如晾置在空气中,过一段时间后,其漂白效果更好的原因是
5.用漂白粉溶液浸泡过的有色布条,如晾置在空气中,过一段时间后,其漂白效果更好的原因是
A.漂白粉被氧化了
B.有色布条被空气中的氧气氧化了
C.漂白粉和空气中的CO2充分反应生成了HClO
D.漂白粉分解了 sjq80231年前3
sjq80231年前3 -
 xiangjiantan 共回答了20个问题
xiangjiantan 共回答了20个问题 |采纳率80%C.漂白粉和空气中的CO2充分反应生成了HClO
HClO漂白性质更好1年前查看全部
- 氯气为什么要制成漂白粉?A.增强漂白作用 B.转化成较稳定的物质,便于运输和保存C.转化成较易溶于水的物质D.增加氯的百
氯气为什么要制成漂白粉?
A.增强漂白作用
B.转化成较稳定的物质,便于运输和保存
C.转化成较易溶于水的物质
D.增加氯的百分含量,有利于漂白,消毒 kevinch1年前2
kevinch1年前2 -
 zl175409339 共回答了18个问题
zl175409339 共回答了18个问题 |采纳率94.4%B.转化成较稳定的物质,便于运输和保存
漂白的是次氯酸根
氯气是制造的原料!1年前查看全部
- 根据漂白粉漂白的原理,为了让它和水和二氧化碳反应,是不是先要让它放在空气中一段时间呢,那怎么又说这是变质(失效)了呢?好
根据漂白粉漂白的原理,为了让它和水和二氧化碳反应,是不是先要让它放在空气中一段时间呢,那怎么又说这是变质(失效)了呢?好奇怪诶.
 gaorxkk1年前1
gaorxkk1年前1 -
 果果正妆店 共回答了19个问题
果果正妆店 共回答了19个问题 |采纳率100%漂白粉漂白的原理:
漂白粉的主要成分是次氯酸钙和氯化钙,有效成分是次氯酸钙.漂白粉的漂白原理是次氯酸钙与酸反应产生有漂白性的物质次氯酸:
Ca(ClO)2+2HCl(稀)=CaCl2+2HClO
Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO
次氯酸是弱酸,可以氧化色素,从而达到漂白目的
失效原理:
漂白粉的有效成分是次氯酸钙
所以,漂白粉失效应该从次氯酸根的角度分析
Ca(ClO)2+CO2+H2O=CaCO3+HClO(强酸制弱酸)
2Hclo=2Hcl+O2↑
次氯酸根都没有了,当然就失效了1年前查看全部
- 棉花脱脂漂白工艺对水质有什么要求吗,水质不好的话该怎么处理
 云天7601年前1
云天7601年前1 -
 天空刮风下雨 共回答了28个问题
天空刮风下雨 共回答了28个问题 |采纳率78.6%棉花脱脂漂白使用软水就可以了.没有什么特殊要求.
如果原水浑浊(地表水)可以先沉淀,在精炼漂白时添加 1克/公升的六偏磷酸钠作为软水剂(螯合剂).如果使用的是地下水一般比较干净,没有必要经过沉淀,但是原水硬度偏高,可以按照以上方法软化(添加螯合剂).1年前查看全部
- 过氧化钠、过氧化氢、NaClO、HClO、ClO2、SO2、O3、活性炭等物质与漂白粉的漂白原
 面生树影1年前1
面生树影1年前1 -
 bbbb16 共回答了19个问题
bbbb16 共回答了19个问题 |采纳率89.5%二氧化硫:溶于水后生成的亚硫酸跟有机色质直接结合成无色的化合物.加热又能恢复成原色(不稳定的,暂时的)
活性炭:吸附性漂白(物理漂白)
过氧化钠、过氧化氢、NaClO、HClO、ClO2、O3以及漂白粉CaCl2.Ca(ClO)2是因为强氧化性(化学漂白)1年前查看全部
- 如图是中学化学中常见物质之间的相互转化关系.其中C可用于漂白,空气中M含量增加会导致温室效应.反应③常用于实验室制取气体
如图是中学化学中常见物质之间的相互转化关系.其中C可用于漂白,空气中M含量增加会导致温室效应.反应③常用于实验室制取气体B.

请回答下列问题:
(1)C的分子式为______,J的电子式为______.
(2)写出反应①的离子方程式2Cl-+2H2O
2OH-+Cl2↑+H2↑电解 .2Cl-+2H2O.
2OH-+Cl2↑+H2↑电解 .
(3)写出反应②的化学方程式3Cl2+6KOH
5KCl+KClO3+3H2O△ .3Cl2+6KOH.
5KCl+KClO3+3H2O△ .
(4)C、M有相似的化学性质,但也有区别,如C有漂白性、M五漂白性. C、M具有其他不同化学性质的原因是______. 切格瓦拉1年前1
切格瓦拉1年前1 -
 win4000 共回答了15个问题
win4000 共回答了15个问题 |采纳率86.7%解题思路:H是黄绿色气体,应为Cl2,J焰色反应为紫色,则含K元素,对G的溶液电解,可以联想电解饱和食盐水,从而确定出G为KCl,J为KOH,I为H2,反应③为实验室制取气体的反应,其条件为含有MnO2的加热反应,则不难得出K为KClO3,B为O2,G为KCl,由元素守恒知,反应②H与J的加热产物E为水.A为淡黄色粉未,C用于漂白,由B为O2,可推断出A为S,C为SO2,D为SO3,F为H2SO4.M含量增加会导致温室效应,则为CO2气体,故L为碳.H是黄绿色气体,应为Cl2,J焰色反应为紫色,则含K元素,对G的溶液电解,可以联想电解饱和食盐水,从而确定出G为KCl,J为KOH,I为H2,反应③为实验室制取气体的反应,其条件为含有MnO2的加热反应,则不难得出K为KClO3,B为O2,G为KCl,由元素守恒知,反应②H与J的加热产物E为水.A为淡黄色粉未,C用于漂白,由B为O2,可推断出A为S,C为SO2,D为SO3,F为H2SO4.M含量增加会导致温室效应,则为CO2气体,故L为碳,则:
(1)由上述分析可知,C的分子式为SO2,J为KOH,由钾离子与氢氧根离子构成,其电子式为 ,
,
故答案为:SO2; ;
;
(2)反应①为电解KCl溶液生成氯气、氢气与KOH,离子方程式为:2Cl-+2H2O
电解
.
2OH-+Cl2↑+H2↑,
故答案为:2Cl-+2H2O
电解
.
2OH-+Cl2↑+H2↑;
(3)反应②为氯气与KOH在加热条件下生成KCl、氯酸钾与水,反应化学方程式为:3Cl2+6KOH
△
.
5KCl+KClO3+3H2O,
故答案为:3Cl2+6KOH
△
.
5KCl+KClO3+3H2O;
(4)SO2中S为+4价,是中间价态,既有还原性又有氧化性,而CO2中C为+4价,只有氧化性,
故答案为:SO2中S为+4价,是中间价态,既有还原性又有氧化性,而CO2中C为+4价,只有氧化性.点评:
本题考点: 无机物的推断.
考点点评: 本题以无机的框图的形式,考查元素化合物的推断,物质的颜色是推断突破口,关键是利用电解与二氧化锰条件下制取气体,难度中等.1年前查看全部
- 高中化学漂白作用石蕊 酚酞 和品红都是有机色素吧,SO2具有漂白性,可以使品红褪色,但为什么不能使酚酞和石蕊褪色啊?只能
高中化学漂白作用
石蕊 酚酞 和品红都是有机色素吧,SO2具有漂白性,可以使品红褪色,但为什么不能使酚酞和石蕊褪色啊?只能使它们变色?
如果可以的话,希望能给我详细讲下,在次谢谢! Boyplunger1年前5
Boyplunger1年前5 -
 yygszhy 共回答了18个问题
yygszhy 共回答了18个问题 |采纳率100%二氧化硫的氧化性太弱了!只能品红氧化成一种不移定的显色基团!这种显色基团受热易分解!但由于其他两种显色其团稳定以二氧化硫的氧化性还未能将其显色1年前查看全部
- 漂白粉漂白这个反应能说明次氯酸是比碳酸弱的酸么?
 gghgfff1年前1
gghgfff1年前1 -
 高档面料 共回答了13个问题
高档面料 共回答了13个问题 |采纳率84.6%不能,漂白是因为次氯酸氧化性很强,跟酸性没有关系!1年前查看全部
- 漂白粉漂白时,向溶液中滴加少量盐酸,会降低漂白效果吗?
 誓与ee比高低1年前1
誓与ee比高低1年前1 -
 东雨西晴301 共回答了23个问题
东雨西晴301 共回答了23个问题 |采纳率91.3%因为漂白粉的原理就是通过其有效成分次氯酸钠水解生成次氯酸,再利用次氯酸的氧化性将物体漂白,而在溶液中加入HCl后更加速了次氯酸钠的水解,这样还可以加速漂白效果,但HCl一定要适量1年前查看全部
- 1.有时打开自来水龙头,会闻到一股刺激性气味,为什么?2.直接用氯气来漂白、杀菌消毒有什么不利因
1.有时打开自来水龙头,会闻到一股刺激性气味,为什么?2.直接用氯气来漂白、杀菌消毒有什么不利因
1.有时打开自来水龙头,会闻到一股刺激性气味,为什么?
2.直接用氯气来漂白、杀菌消毒有什么不利因素?如何改进? limin10111年前1
limin10111年前1 -
 gonewithstone 共回答了20个问题
gonewithstone 共回答了20个问题 |采纳率90%自来水中的刺激性气味是次氯酸的味道,用来给自来水消毒的
这样生产的自来水有比较刺鼻的氯气的气味,并且一部分溶解在水中的氯气会与水发生化学反应,生成少量的次氯酸(起到消毒作用),次氯酸不稳定又分解为盐酸.
改进:曝气(即把空气通入水中,再用阳光晒晒)1年前查看全部
- 下列关于SO 2 的说法中,错误的是( ) A.二氧化硫能漂白某些物质,说明它具有氧化性 B.二氧化硫的水溶液能使紫色
下列关于SO 2 的说法中,错误的是( ) A.二氧化硫能漂白某些物质,说明它具有氧化性 B.二氧化硫的水溶液能使紫色石蕊溶液变红,说明它能与水反应生成H 2 SO 3 C.实验室可用氢氧化钠溶液处理含有二氧化硫的尾气 D.将足量二氧化硫通入酸性高锰酸钾溶液中,溶液褪色,说明二氧化硫具有还原性  蹉跎又一年1年前1
蹉跎又一年1年前1 -
 ysmzx 共回答了17个问题
ysmzx 共回答了17个问题 |采纳率94.1%解;A、二氧化硫能漂白某些物质,是结合有机色素为无色不稳定物质说明它具有漂白性,没有表现氧化性.故A错误;
B、二氧化硫是酸性氧化物,水溶液能使紫色石蕊溶液变红,是因为二氧化硫与水反应生成H 2 SO 3 ,故B正确;
C、二氧化硫是污染性气体,具有酸性氧化物的性质,和碱反应,实验室可用氢氧化钠溶液处理含有二氧化硫的尾气,故C正确;
D、将足量二氧化硫通入酸性高锰酸钾溶液中,溶液褪色,说明二氧化硫的还原性被高锰酸钾氧化,故D正确;
故选A.1年前查看全部
- 氢氧化钾能代替氢氧化钠吗我是用在漂白方面的,我是和双氧水一起用的可以代替吗
 纳兰容若MM1年前2
纳兰容若MM1年前2 -
 蝶舞飞儿 共回答了16个问题
蝶舞飞儿 共回答了16个问题 |采纳率100%别说代替 氢氧化钠本身就不能用来漂白 会腐蚀衣物
碳酸氢钠才对
那就可以了 双氧水和氢氧化钠漂白原理是利用反应生成的过氧化钠 代替后生成过氧化钾 漂白原理是一样的 都是过氧根的氧化漂白1年前查看全部
- 干燥氯气为什么不能漂白?次氯酸漂白是因为他的氧化性,氯气 大于次氯酸啊
 Ilovesweetbox1年前7
Ilovesweetbox1年前7 -
 职业司机 共回答了26个问题
职业司机 共回答了26个问题 |采纳率80.8%酸性条件下,Cl2ClO-.
乾燥氯气无法漂白是因为无法产生HClO1年前查看全部
- 下列叙述正确的是( )A.HClO可以使有色物质漂白,所以具有氧化性物质可作漂白剂B.Na的金属活动性比Mg强,故可用
下列叙述正确的是( )
A.HClO可以使有色物质漂白,所以具有氧化性物质可作漂白剂
B.Na的金属活动性比Mg强,故可用Na与MgCl2溶液反应制Mg
C.浓硝酸中的HNO3,见光会分解,故有时在实验室看到的浓硝酸呈黄色
D.因为SO2具有较强还原性,所以不能用浓硫酸来干燥它 yologocn1年前1
yologocn1年前1 -
 宝贝vs天天 共回答了18个问题
宝贝vs天天 共回答了18个问题 |采纳率83.3%解题思路:A.具有氧化性的物质不一定能做漂白剂;
B.Na与MgCl2溶液反应生成氢氧化镁和氢气;
C.硝酸分解生成二氧化氮,二氧化氮溶于水;
D.二氧化硫与浓硫酸不反应.A.具有氧化性的物质不一定能做漂白剂,如浓硫酸,一般来说,用作漂白剂的物质通常可生成氧气,故A错误;
B.Na性质活泼,可与水反应,钠与MgCl2溶液反应生成氢氧化镁和氢气,故B错误;
C.硝酸分解生成红棕色二氧化氮,二氧化氮溶于水导致浓硝酸呈黄色,故C正确;
D.二氧化硫与浓硫酸不反应,同种元素相邻化合价,氧化剂和还原剂之间不发生氧化还原反应,故D错误.
故选C.点评:
本题考点: 氯、溴、碘及其化合物的综合应用;硝酸的化学性质;二氧化硫的化学性质;钠的化学性质.
考点点评: 本题考查较为综合,涉及物质的漂白性、钠、硝酸以及二氧化硫的性质,为高考常见题型,侧重元素化合物知识的综合理解和运用的考查,有利于学习良好的科学素养的培养,难度中等,注意相关基础知识的积累.1年前查看全部
- 下列物质都具有漂白性,其中一种与其它物质的漂白原理不相同,这种物质是 A. HClO B. H 2 O 2 C. O 3
下列物质都具有漂白性,其中一种与其它物质的漂白原理不相同,这种物质是
A. HClO B. H 2 O 2 C. O 3 D. SO 2  符熙敏1年前1
符熙敏1年前1 -
 有害书籍爱好者 共回答了13个问题
有害书籍爱好者 共回答了13个问题 |采纳率92.3%D
1年前查看全部
- 漂白粉溶于水后,受空气中的热氧化碳作用,即产生有漂白,杀菌作呕难过的次氯酸,
 fearboy1年前1
fearboy1年前1 -
 林晓小 共回答了15个问题
林晓小 共回答了15个问题 |采纳率93.3%Ca(ClO)2 + H2O + CO2 === CaCO3沉淀 + 2HClO1年前查看全部
- 第一个,NaOH中加酚酞变红,然后加H2O2变成无色,现在想证明是NaOH与H2O2中和还是H2O2将酚酞漂白.我和同学
第一个,NaOH中加酚酞变红,然后加H2O2变成无色,现在想证明是NaOH与H2O2中和还是H2O2将酚酞漂白.我和同学在这里产生了争论,我说继续加酚酞,如果酚酞变红,则是H2O2漂白.他说继续加NaOH,如果不变红,则是漂白.我们谁说得对?还是都对?
第二个,HClO漂白的东西加热后会变回来吗? 废物点心1291年前7
废物点心1291年前7 -
 景_ 共回答了12个问题
景_ 共回答了12个问题 |采纳率83.3%答:是由于双氧水的漂白作用.双氧水的漂白作用是由于它和一些有色物质作用,因为双氧水中+1价的氯使得双氧水有强氧化性,因此,双氧水把有色物质氧化成了无色的物质,这就是双氧水漂白的原理.它的漂白性区别于二氧化硫的漂白性,二氧化硫的漂白性是由于二氧化硫和有色物质反应生成了不稳定的无色物质,因此,加热的时候,无色物质又会转变成有色物质.而由双氧水漂白得到的无色物质是不会因为加热而转变成原来的.
他的说法是正确的,因为如果是氢氧化钠和双氧水发生了中和反应的话,再继续滴加酚酞的同时,因为氢氧化钠已经反应掉了,所以酚酞不会变红,而如果是因为双氧水的漂白作用,继续滴加酚酞,因为双氧水的漂白作用,酚酞还是不会变红的,两种情况的现象一样.因此,你的方法还是无法证明.
他的方法:
继续加NaOH,如果是因为中和作用,在滴加氢氧化钠,因为溶液中原先有滴加的酚酞,所以,新滴加的氢氧化钠和原来溶液中的酚酞结合,使得酚酞变成红色.而如果是由于漂白作用,在滴加氢氧化钠,因为双氧水的漂白,所以,酚酞是不会发生变红的,因此,这两种情况的现象是不同的,所以,可以证明.1年前查看全部
- 过氧化氢常用于消毒、杀菌、漂白等,是中学化学中的一种重要的试剂.
过氧化氢常用于消毒、杀菌、漂白等,是中学化学中的一种重要的试剂.
(1)一种制备过氧化氢的流程如图1,此过程的总化学方程式为H2+O2
H2O2催化剂 .H2+O2.
H2O2催化剂 .
(2)质量分数为5%的H2O2水溶液(密度为1g•mL-1)的物质的量浓度为______.
(3)某实验小组设计下表3组实验研究溶液的酸碱性对H2O2分解反应速率的影响,绘制生成氧气的体积随时间变化的关系如图2.
分析该图能够得出的实验结论是______.实验编号 反应物(室温) 催化剂 a 10mL5%H2O2溶液+1mLH2O 0.1gMnO2粉末 b 10mL5%H2O2溶液+1mL稀HCl 0.1gMnO2粉末 c 10mL5%H2O2溶液+1mL稀NaOH溶液 0.1gMnO2粉末
(4)实验室常用酸性高锰酸钾标准溶液测定双氧水的浓度,反应中MnO4-被还原为Mn2+.
①请用离子方程式表示该滴定原理______.
②准确量取20.00mL某过氧氢试样置于锥形瓶中,用0.1000mol•L-1的酸性KMnO4标准溶液滴定,平行滴定三次,消耗酸性KMnO4溶液的平均体积为18.00mL.则该试样中过氧化氢的浓度为______mol•L-1.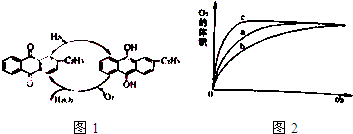
 RP12561年前1
RP12561年前1 -
 Google测试员4629 共回答了24个问题
Google测试员4629 共回答了24个问题 |采纳率91.7%解题思路:(1)根据反应物和生成物结合反应历程判断;
(2)根据c=[1000ρω/M]计算;
(3)由图象可知,碱性条件下分解速率最大;
(4)①发生氧化还原反应生成氧气和Mn2+;
②根据反应的方程式计算.(1)通过图示可知,用乙基蒽醌作催化剂制取双氧水,反应的方程式为H2+O2
催化剂
.
H2O2,故答案为:H2+O2
催化剂
.
H2O2;
(2)c=[1000ρω/M]=[1000×1g/L×5%/34g/mol]=1.47 mol/L,故答案为:1.47 mol/L;
(3)由图象可知,碱性条件下分解速率最大,可知保持其他条件不变,溶液的pH越大,双氧水分解速度越快,故答案为:保持其他条件不变,溶液的pH越大,双氧水分解速度越快;
(4)①发生氧化还原反应生成氧气和Mn2+,离子方程式为2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑,
故答案为:2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑;
②根据反应2MnO4-+5H2O2+6H+═2Mn2++8H2O+5O2,n(H2O2)=2.5×n(MnO4-)=2.5×0.1000mol•L-1×0.018L,c(H2O2)=[2.5×0.1000×0.018/0.02]=0.225 mol/L,
故答案为:0.225 mol/L.点评:
本题考点: 化学反应速率的影响因素;化学方程式的有关计算.
考点点评: 本题考查较为综合,涉及多方面知识,为高考常见题型,侧重于学生的分析、实验和计算能力的考查,注意知识的归纳和梳理是解题的关键,难度不大.1年前查看全部
- 具有漂白作用的物质有①氯气②二氧化硫③活性炭④过氧化钠,其漂白原理相同的是( )
具有漂白作用的物质有①氯气②二氧化硫③活性炭④过氧化钠,其漂白原理相同的是( )
A. ①③
B. ②③
C. ①④
D. ②④ ct998881年前1
ct998881年前1 -
 gvgcafeg1 共回答了16个问题
gvgcafeg1 共回答了16个问题 |采纳率87.5%解题思路:几种漂白剂的比较
漂白剂 HClO Na2O2(H2O2) SO2 活性炭 漂白原理 氧化漂白 氧化漂白 化合漂白 吸附漂白 氯气漂白实际上是氯气与水反应生成的次氯酸起漂白作用,次氯酸和过氧化钠漂白原理都是利用了强氧化性,故C选项正确,故选C.
点评:
本题考点: 氯气的化学性质;二氧化硫的化学性质;钠的重要化合物.
考点点评: 本题考察了不同物质的漂白原理.了解漂白物质的性质,是解决此题的基础.1年前查看全部
- 为什么漂白粉在潮湿条件下和水溶液中才具有漂白和消毒杀菌作用
 pengzubian1年前3
pengzubian1年前3 -
 大丛 共回答了12个问题
大丛 共回答了12个问题 |采纳率91.7%因为漂白粉杀菌原理,必须在一定水分条件下,才能产生杀菌物质,漂白粉洒在干燥处就不易起到消毒作用.即:漂白粉遇水放出有强氧化性的原子氧:Ca(OCl) 2→CaCl2+2[O].1年前查看全部
- 起漂白作用的是HClO还是ClO-
 jayjay031年前1
jayjay031年前1 -
 narcissusysh 共回答了19个问题
narcissusysh 共回答了19个问题 |采纳率89.5%是次氯酸应为首先次氯酸属于不是很强的酸
电离氢离子的能力不强
所以产生ClO-的数量相对的酒不是很多了啊
而漂白粉的漂白作用相当好
说明并不是少量的ClO-影响漂白的效果
说以是大量的HCLO的分子没有完全电离的Hclo才有漂白作用1年前查看全部
- 氯气与氢氧化钠、氯气与氢氧化钙、次氯酸的分解、漂白粉的漂白原理反应方程式与离子方程式
氯气与氢氧化钠、氯气与氢氧化钙、次氯酸的分解、漂白粉的漂白原理反应方程式与离子方程式
氯气与溴化钾、碘化钾,溴与碘化钾、硫与氧气、铁、氢气,二氧化硫与水、氧气、氧化钙、硫化氢反应的方程式与离子方程式,急用! 白水祀1年前1
白水祀1年前1 -
 和乌龟赛跑 共回答了21个问题
和乌龟赛跑 共回答了21个问题 |采纳率95.2%Cl2+NaOH=NaCl+NaClO+H2O Cl2+2OH-=Cl- +ClO- +H2O
2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O Cl2+2OH-=Cl- +ClO- +H2O
2HClO=2HCl+O2↑ 2HClO=2H+ +Cl-+O2↑
Ca(ClO)2+CO2+H2O=2HClO+CaCO3↓ Ca2+ +2ClO-+CO2+H2O=2HClO+CaCO3↓
Cl2+2KBr=2KCl+Br2 Cl2+2Br-=2Cl-+Br2
Cl2+2KI=2KCl+I2 Cl2+2I-=2Cl-+I2
Br2+2KI=2KBr+I2 Br2+2I-=2Br-+I2
_______________________________________________
S+O2=点燃=SO2
S+Fe=加热=FeS
S+H2=加热=H2S
SO2+H2O=H2SO3
2SO2+O2=2SO3
CaO+SO2=CaSO3
SO2+2H2S=3S↓+2H2O
分界线以下的反应都没有离子方程式,因为没有离子参加反应.1年前查看全部
- 漂白粉的漂白、失效原理各是什么是不是同一个啊?用化学方程式表示
 三十等一回1年前1
三十等一回1年前1 -
 烟火逍遥 共回答了21个问题
烟火逍遥 共回答了21个问题 |采纳率90.5%漂白粉漂白的原理:
漂白粉的主要成分是次氯酸钙和氯化钙,有效成分是次氯酸钙.漂白粉的漂白原理是次氯酸钙与酸反应产生有漂白性的物质次氯酸:
Ca(ClO)2+2HCl(稀)=CaCl2+2HClO
Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO
次氯酸是弱酸,可以氧化色素,从而达到漂白目的
失效原理:
漂白粉的有效成分是次氯酸钙
所以,漂白粉失效应该从次氯酸根的角度分析
Ca(ClO)2+CO2+H2O=CaCO3+HClO(强酸制弱酸)
2Hclo=2Hcl+O2↑
次氯酸根都没有了,当然就失效了1年前查看全部
- 漂白粉的漂白原理、84消毒液失效原理(用化学方程式表示)
 zhentamanioub1年前1
zhentamanioub1年前1 -
 bwbpb 共回答了24个问题
bwbpb 共回答了24个问题 |采纳率79.2%漂白粉的主要成分是次氯酸钙和氯化钙,有效成分是次氯酸钙.漂白粉的漂白原理是次氯酸钙与酸反应产生有漂白性的物质次氯酸:
Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO
84消毒液是一种以次氯酸钠为主的高效消毒剂,主要成分为次氯酸钠(NaClO).
失效原理:2NaCIO +CO2+H2O ==Na2CO3 +2HCIO 2HClO=2HCl+O2↑
次氯酸根都没有了,当然就失效了1年前查看全部
- 为了增强漂白粉的漂白能力,常在漂白粉溶于水时,滴入少量的
为了增强漂白粉的漂白能力,常在漂白粉溶于水时,滴入少量的
A:NaOH
B:稀盐酸
C:生石灰
D:NaCl 川灵湘秀1年前2
川灵湘秀1年前2 -
 李-玲-玲 共回答了9个问题
李-玲-玲 共回答了9个问题 |采纳率100%楼上正解
NaOH和生石灰会使漂白粉丧失漂白能力
NaCl没什么作用1年前查看全部
- 漂白原理:Ca(ClO)2——HClO,实际上是HClO起漂白作用,当Ca(ClO)2遇水和二氧化碳时,会产生HClO,
漂白原理:Ca(ClO)2——HClO,实际上是HClO起漂白作用,当Ca(ClO)2遇水和二氧化碳时,会产生HClO,那么为什么漂白粉还要密封包装,避光,隔热存放,它直接与空气接触反而能产生HCIO漂白作用更好.
 雾中de风景1年前4
雾中de风景1年前4 -
 wxh580210 共回答了19个问题
wxh580210 共回答了19个问题 |采纳率84.2%原理的方程式你应该知道吧 是Ca(ClO)2+H2O+CO2----CaCO3+2HClO
如你所说是生成的次氯酸氧化漂白 所以在保存的时候 一定要和 水 空气隔开 如果在保存的时候和水 空气接触了 那么就会使其变质 变成没有用的 CaCO3 而次氯酸在这个时候发挥不了作用 而且很容易分解掉 等你用的时候 那漂白粉早就不是你想要的漂白粉了 而成了如假包换的碳酸钙了 所谓的密封包装 是为了隔水(蒸汽) 隔二氧化碳 避光 隔热是为了 减缓变质的速度1年前查看全部
- 有色物质所含色素的化学共性强氧化性物质可以氧化漂白、SO2可以与有色物质结合漂白.这些物质都能漂白有色物质而一般不论是什
有色物质所含色素的化学共性
强氧化性物质可以氧化漂白、SO2可以与有色物质结合漂白.这些物质都能漂白有色物质而一般不论是什么颜色或什么色素.
这说明一般的有色物质,无论什么颜色或什么色素,都存在化学上的共性.请说明和解释这个共性. xiaokan8611年前3
xiaokan8611年前3 -
 sancofirst 共回答了20个问题
sancofirst 共回答了20个问题 |采纳率95%一楼不全面,共性是都含有重金属离子(硫酸铜,高锰酸钾,铅白,钛白,铅铬绿),这一类就具有氧化性,最典型的高锰酸钾,他褪色是因为被还原!1年前查看全部
- 1.漂白粉在溶液中存在下列平衡:ClO-+H20=HClO+OH-(可逆),下列措施能提高其漂白效率的是:
1.漂白粉在溶液中存在下列平衡:ClO-+H20=HClO+OH-(可逆),下列措施能提高其漂白效率的是:
A.加水,B 通入CO2,C 通入SO2
2.常温下一定浓度的某溶液,由水电离出的c(OH-)=10^-4 mol/L 则该溶液中的溶质可能是:A.Al2(SO4)3,B.CH3COONa,C.NaOH.D KHSO4
3.A.饱和石灰水中加入一定量生石灰,温度明显升高,所得溶液的pH增大
B.AgCl悬浊液中存在平衡:AgCl(s) Ag+(aq)+Cl-(aq),往其中加入少量NaCl
粉末,平衡向左移动,溶液中离子的总浓度会减小
D,硬水中含有较多的Ca2+、Mg2+、HCO-3、SO2-4,加热煮沸可以完全除去其中的Ca2+、Mg2+
讲讲这三个为什么错了.. hugoo1234561年前3
hugoo1234561年前3 -
 9789764 共回答了25个问题
9789764 共回答了25个问题 |采纳率80%1,搞清楚漂白粉的本质是靠HClO,作用机理是氧化.别的都不好使
A加水没用,第一本来就有很多水了,再加水对反应的影响不大.第二,加水稀释了浓度反而漂白效率变低.得不偿失
B,加入CO2 既可以理解为强酸制备弱酸,由较强的H2CO3制备了较弱的HClO .也可以认为CO2和OH-反应,促使平衡右移.生成更多HClO 效果增加
C,看起来SO2和CO2差不多,但是SO2有还原性和HClO反应,消耗了HClO,也是得不偿失.
2,本人认为选CH3COONa,B不是C
第一水电离出的H+,OH-一定是相等的.第二点,水解促进水的电离,加入酸碱移植水的电离.这题中水电离出的OH太多了,说明被促进,排除CD,又A中Al可以结合OH-所以也不多.如果OH-是10^-14就选NaOH
3,A Ca(OH)2虽然强碱,但是溶解度随着温度升高而减小,加入生石灰,会有更多的Ca(OH)2析出.高温下的饱和溶液浓度反而不如低温下的.PH下降.错
B AgCl 本来就难容.而Ag+和 Cl-有一项肯定会很小,否则有更多沉淀.假设Ag+多,加入Cl-消耗掉一个Ag+就多出来一个Na+,不会减少离子总浓度,假设Cl-很多,加入NaCl基本会无影响,离子就更多了.
D,只含碳酸根,碳酸氢跟的是暂时硬水,可以通过加热煮沸除去.但是一旦含有硫酸根就是永久硬水,无法再通过加热出去,不能生成沉淀或气体,除非使用蒸馏的方法,那又是另外一回事了.1年前查看全部
- 把a在b中充分燃烧生成c和水蒸气,c能漂白有色潮湿花朵.问abc各是什么物质.
 bingshui111年前1
bingshui111年前1 -
 fzpz 共回答了23个问题
fzpz 共回答了23个问题 |采纳率95.7%a是H2S(硫化氢),b是氧气,c是二氧化硫1年前查看全部
- so2和cl2的漂白原理相同吗?它能使紫色石蕊试液变色吗?为什么?
 mixxion1年前1
mixxion1年前1 -
 秋木哈骨 共回答了23个问题
秋木哈骨 共回答了23个问题 |采纳率100%SO2与Cl2的漂泊原理不同.SO2是与有色物质结合生成不稳定的无色物质;Cl2是将色素氧化成无色物质.
SO2和Cl2都能使紫色石蕊试剂变色.原理是:SO2与水反应生成的亚硫酸使石蕊变红;Cl2与水反应生成HCl和HClO,石蕊先变红(酸使之变红),然后变成白色(HClO将石蕊氧化成白色).1年前查看全部
- (2012•资阳)漂白粉常用于灾区消毒杀菌,其有效成分为Ca(ClO)2,其中氯元素的化合价为______;工业上制漂白
(2012•资阳)漂白粉常用于灾区消毒杀菌,其有效成分为Ca(ClO)2,其中氯元素的化合价为______;工业上制漂白粉,是将氯气通入石灰乳发生如下反应制得:2Ca(OH)2+2Cl2=X+Ca(ClO)2+2H2O,产物中X的化学式为______;漂白粉易吸收空气中的水分和二氧化碳而硬化变质,最终生成的硬化物是(填写化学式)______,所以漂白粉要密封保存,开封及时使用.
 hainan-hx1年前1
hainan-hx1年前1 -
 Antigone_H 共回答了15个问题
Antigone_H 共回答了15个问题 |采纳率93.3%解题思路:根据在化合物中正负化合价代数和为零,结合Ca(ClO)2的化学式进行解答.
由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式.
根据漂白粉的有效成分、质量守恒定律进行分析解答.钙元素显+2价,氧元素显-2价,设氯元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+2)+2x+(-2)×2=0,则x=+1.
根据反应的化学方程式2Ca(OH)2+2Cl2=X+Ca(ClO)2+2H2O,反应物中钙、氧、氢、氯原子个数分别为2、4、4、4,反应后的生成物中钙、氧、氢、氯原子个数分别为1、4、4、2,根据反应前后原子种类、数目不变,则每个X分子由1个钙原子和2个氯原子构成,则物质X的化学式为CaCl2.
漂白粉的有效成分为Ca(ClO)2,吸收空气中的水分和二氧化碳而硬化变质,最终生成的硬化物是碳酸钙.
故答案为:+1;CaCl2;CaCO3.点评:
本题考点: 有关元素化合价的计算;质量守恒定律及其应用.
考点点评: 本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法、原子守恒来确定物质的化学式等即可正确解答.1年前查看全部
- 二氧化硫和氯气同样可以漂白有色物质,如果将二氧化硫漂白过的有色物质加热,现象______________________
二氧化硫和氯气同样可以漂白有色物质,如果将二氧化硫漂白过的有色物质加热,现象________________________,如果将氯气漂白过的有色物质加热,现象________________________.
 长得帅zz得快1年前3
长得帅zz得快1年前3 -
 abbccde 共回答了14个问题
abbccde 共回答了14个问题 |采纳率78.6%1 现象就是 变回原来的颜色
2 现象就和 上面的相反
原因:SO2里的 漂白性是暂时的 而CL2的则是永久的
举个例子吧.一般农民买回来的草帽都是用SO2熏成黄色的
在太阳下工作带久了会退色 这是个很明显的例子1年前查看全部
- cl2和so2 都具有漂白作用,能使品红溶液褪色,若将等物质的量的cl2 so2 混合后 在通入品红与 bacl2混合溶
cl2和so2 都具有漂白作用,能使品红溶液褪色,若将等物质的量的cl2 so2 混合后 在通入品红与 bacl2混合溶液 能观察到得现象 (多选)
A溶液很快褪色 B溶液不退色 C出现沉淀 D不出现沉淀 朵朵绿1年前3
朵朵绿1年前3 -
 lanhuomiao 共回答了30个问题
lanhuomiao 共回答了30个问题 |采纳率90%BC
Cl2会氧化SO2为SO4 2-
SO2+Cl2+H2OBaSO4↓+2HCl
由于SO2和Cl2全部消耗完,所以溶液不退色,出现白色沉淀.1年前查看全部
- 被次氯酸钠漂白的衣服,是否能染回来
被次氯酸钠漂白的衣服,是否能染回来
衣服用84消毒液洗了,退色了,怎么恢复 带刀御猫1年前4
带刀御猫1年前4 -
 flightflight 共回答了17个问题
flightflight 共回答了17个问题 |采纳率88.2%不可以了,次氯酸钠的漂白是不可恢复的,特是把染料给氧化了,所以不能还原,估计唯一的补救方法就是你DIY一下吧,看看能不能把那个褪色的地方变成特点了.1年前查看全部
- 氢氧化钠能漂白衣服吗
 5em5gl1年前1
5em5gl1年前1 -
 沙漠中小蚂蚁 共回答了25个问题
沙漠中小蚂蚁 共回答了25个问题 |采纳率92%不能
因为氢氧化钠的碱性太强腐蚀性也太强衣服会被腐蚀坏的.
氯化钠没有漂白效果1年前查看全部
- 下列物质均具有漂白作用,其中一种与另外三种的漂白原理不同的是 [ ] A
下列物质均具有漂白作用,其中一种与另外三种的漂白原理不同的是 [ ]A.HClO
B.H 2 O 2
C.SO 2
D.O 3 风色男孩1年前1
风色男孩1年前1 -
 qiutian1222 共回答了15个问题
qiutian1222 共回答了15个问题 |采纳率93.3%C1年前查看全部
- 漂粉精漂白的反应方程式.不是制取.
 lampard5201年前3
lampard5201年前3 -
 softuser888 共回答了19个问题
softuser888 共回答了19个问题 |采纳率89.5%漂粉精主要成份:Ca(ClO)2
Ca(ClO)2 +CO2 + H2O ===CaCO3 + 2HClO
HClO有强氧化性,所以可以漂白,漂白后自身变成了HCl
2HClO=== 2HCl +O21年前查看全部
- 为什么二氧化硫不能漂白石蕊
 czq03391年前2
czq03391年前2 -
 j538h 共回答了23个问题
j538h 共回答了23个问题 |采纳率95.7%这个你要清楚SO2漂白性的原理
能漂白石蕊的物质都是具有强氧化性的 比如湿润的Cl2等等 SO2漂白品红是由于它和品红反应生成了无色的物质 这个反应是可以逆转的 所以加热就又还原了
如果还有疑问 百度HI找我 详谈1年前查看全部
- (2010•青岛模拟)目前,生产自来水常使用适量的氯气,因为:Cl2+H2O=HCl+HClO,HClO有漂白作用,还能
(2010•青岛模拟)目前,生产自来水常使用适量的氯气,因为:Cl2+H2O=HCl+HClO,HClO有漂白作用,还能用于消毒杀菌.而新型净水剂高铁酸钠(Na2FeO4)效果更好,且对人体无害.则下列说法错误的是( )
A.氯气与水发生的反应属于置换反应
B.HClO中氯元素的化合价为+1价
C.用自来水养鱼需要先晒上一段时间
D.Na2FeO4中高铁酸根(FeO4)的化合价为-2价 哭的女人1年前1
哭的女人1年前1 -
 9909077 共回答了17个问题
9909077 共回答了17个问题 |采纳率100%解题思路:本题利用HClO和Na2FeO4的化学式及在化合物中H、0、Na等元素的化合价根据正负化合价的代数和为0来分析Cl元素和FeO4的化合价,利用化学反应Cl2+H2O=HCl+HClO来分析反应类型及用自来水养鱼需要先晒的原因.A、因只有氯气为单质,单质与化合物反应生成单质与化合物的反应属于置换反应,则反应Cl2+H2O=HCl+HClO不属于置换反应,则A说法错误,故A正确.
B、HClO中,H为+1价,O为-2价,则由正负化合价的代数和为0,Cl元素的化合价为+1价,则B说法正确,故B错误;
C、自来水中含有氯气,HClO能用于消毒杀菌,阳光照射可使HClO分解,减小氯气的含量,增大氧气的含量,则用自来水养鱼需要先晒上一段时间,说法正确,故C错误;
D、Na2FeO4中,Na元素为+1价,则高铁酸根(FeO4)的化合价为-2价,说法正确,故D错误;
故选A.点评:
本题考点: 有关元素化合价的计算;常见元素与常见原子团的化合价;化合价规律和原则;置换反应及其应用.
考点点评: 本题考查化合价及化学反应,学生正确把握化学式在解题中的重要作用,了解化学与生活的紧密联系.1年前查看全部
- 下列物质在水溶液中没有漂白作用的是 [ ] A.NaOH
下列物质在水溶液中没有漂白作用的是 [ ]A.NaOH
B.Na 2 O 2
C.Cl 2
D.SO 2 伊黛1年前1
伊黛1年前1 -
 WJJJCJC 共回答了23个问题
WJJJCJC 共回答了23个问题 |采纳率87%A1年前查看全部
- 下列物质中,不具有漂白作用的是( )
下列物质中,不具有漂白作用的是( )
A.氮气
B.氯水
C.二氧化硫
D.过氧化钠 12358921年前1
12358921年前1 -
 布林蛋糕 共回答了23个问题
布林蛋糕 共回答了23个问题 |采纳率91.3%解题思路:具有漂白性的物质:次氯酸、氯水、次氯酸盐、二氧化硫、双氧水等.A、氮气性质稳定,不具有漂白性,故A正确;
B、氯水中含有次氯酸,具有漂白性,故B错误;
C、二氧化硫具有漂白性,能使品红退色,故C错误;
D、过氧化钠具有氧化性,具有漂白性,故D错误.
故选A.点评:
本题考点: 氯气的化学性质;二氧化硫的化学性质;钠的重要化合物.
考点点评: 本题考查学生物质的性质,注意归纳整理具有漂白性的物质,知识的归纳和梳理是关键,难度不大.1年前查看全部
- 二氧化硫可以漂白品红溶液是有强氧化性但它应该是有弱氧化性啊
 一面湖水8881年前2
一面湖水8881年前2 -
 风飞飘 共回答了15个问题
风飞飘 共回答了15个问题 |采纳率100%SO2的漂白性,不是因为它有氧化性,而是能与“某些”有色物质化合,生成“不稳定”的无色物质,所以褪色.
也因为无色物质不稳定,加热或者时间长了还会分解,恢复原来的颜色.1年前查看全部
- 硫代硫酸钠(Na 2 S 2 O 3 )俗称保险粉,可用作定影剂,也可用于纸浆漂白、脱氯剂等。
硫代硫酸钠(Na 2 S 2 O 3 )俗称保险粉,可用作定影剂,也可用于纸浆漂白、脱氯剂等。
Na 2 S 2 O 3 易溶于水,不溶于乙醇,常温下溶液中析出晶体通常为Na 2 S 2 O·5H 2 O。实验室制备保险粉的装置如下图所示。涉及的总化学方程式如下: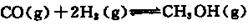

(1)检查虚线框内装置气密性的方法是 。
(2)反应前仪器a中加入的药品为 ,仪器c中加入的药品为 。
(3)仪器b的名称是 。
(4)在制备过程中,持续通人气体时,观察到B装置中先有大量浅黄色沉淀析出,反应一段时间,沉淀逐渐减少;待浅黄色沉淀消失时反应完成,停止加热。反应的离子方程式为 。
(5)反应完成后,为了从混合溶液中获取产品,操作如下:
操作②为 。
(6)为了测产品的纯度,称取8.000 g粗产品,配制成250 mL溶液,用移液管移取25.00 mL于锥形瓶中,再用0.05000 mol·L -l 的碘标准溶液进行滴定(2S 2 O 3 2- +I 2 =S 4 O 6 2- +2I - ),
平行3次实验,平均消耗碘标准溶液的体积为30.00mL。
①测得产品的纯度为 。
②关于上述实验的有关操作,以下表述正确的是 。(填编号)A.用碱式滴定管盛装碘标准溶液 B.用移液管移取25.00mL溶液于锥形瓶中,移液管的尖嘴和锥形瓶内壁要接触 C.如果滴定终点没有控制好,碘标准溶液滴加过量,则必须重新进行滴定 D.滴定过程中若剧烈摇动锥形瓶(溶液不外溅),则所测得的纯度将会偏高  bailinghua1年前1
bailinghua1年前1 -
 新重庆遮阳扇 共回答了20个问题
新重庆遮阳扇 共回答了20个问题 |采纳率95%(1)关闭蒸馏烧瓶右端活塞,往分液漏斗中加水,打开分液漏斗的活塞,水开始下滴,一段时间后,如果水不再下滴,表明气密性良好。反之则气密性不好。
(2)Na 2 SO 3 固体 NaOH溶液(或KMnO 4 溶液等)
(3)三颈烧瓶
(4)S 2 O 3 2- +SO 2 +H 2 O=S↓+2HSO 3 2-
(5)蒸发浓缩、冷却结晶
(6)①93.00% ②B
1年前查看全部
- 下列漂白原理相同的是A氯水A氯水B二氧化硫C过氧化钠D活性炭为什么?
 jiangxiqusi1年前1
jiangxiqusi1年前1 -
 94ai 共回答了14个问题
94ai 共回答了14个问题 |采纳率85.7%氯水和过氧化钠都是通过氧化还原反应达到漂白作用 ,而二氧化硫则是和有机物质生成不稳定物质,但并没有发生氧化还原反应,活性炭则是简单的通过结构上的物理吸附达到的,所以A和C相同1年前查看全部
- 因他打开光明之路,"漂白了的四壁“.的含义
 爱飞的鱼771年前1
爱飞的鱼771年前1 -
 df300aF828 共回答了8个问题
df300aF828 共回答了8个问题 |采纳率87.5%"漂白了的四壁“是失眠和熬夜的意思.1年前查看全部
- Cl2可否使酸碱指示剂褪色?(漂白作用)
 唐钧1年前1
唐钧1年前1 -
 zqy20000 共回答了22个问题
zqy20000 共回答了22个问题 |采纳率95.5%可以;Cl2为气体且有漂白性,Cl2的漂白原理:Cl2 溶于水生成的HClO具有强氧化性,将有色物质氧化成无色物质,褪色后不能恢复原来的颜色.1年前查看全部
- 写化学方程式和离子方程式 1.漂白粉起漂白效用 2.向偏铝酸钠通入二氧化碳
 rfgergyrty1年前2
rfgergyrty1年前2 -
 我现在很矛盾 共回答了19个问题
我现在很矛盾 共回答了19个问题 |采纳率84.2%Ca(ClO)2+CO2+H2O===2HClO+CaCO3沉淀
NaAlO2+CO2+2H2O===Al(OH)3沉淀+NaHCO3 3Cl2+I–+3H2O=6H++6Cl–+IO3–
5Cl2+I2+6H2O===2HIO3+10HCl
5Cl2+I2+6H2O=10Cl–+IO3–+12H+
Cl2+Na2S===2NaCl+S↓ Cl2+S2–=2Cl–+S↓
Cl2+H2S===2HCl+S↓ (水溶液中:Cl2+H2S=2H++2Cl–+S↓
Cl2+SO2+2H2O===H2SO4+2HCl
Cl2+SO2+2H2O=4H++SO42–+2Cl–
Cl2+H2O2===2HCl+O2 Cl2+H2O2=2H++Cl–+O21年前查看全部
- 漂白粉生产方程式和漂白原理
 大渔夫1年前1
大渔夫1年前1 -
 gaoyu0011 共回答了20个问题
gaoyu0011 共回答了20个问题 |采纳率100%2CA(OH)2+2cl2=CA(CLO)2+CACL2+2H2O
CA_CLO)2=CA+2+2CLO-1
CLO-1中的氯离子为正一甲具有强氧化性、表现为漂白性1年前查看全部
- 漂白粉能漂白所有物质吗
 雷星1年前2
雷星1年前2 -
 mingshan11 共回答了15个问题
mingshan11 共回答了15个问题 |采纳率93.3%不能,因为漂白粉只能氧化.
比如一些双键、苯环之类
比如一些最高价金属配合物就再怎么氧化也还是那个颜色
最简单的,Fe3+,KMnO4,就不能被这种氧化剂氧化变色1年前查看全部
大家在问
- 1下列词语中没有错别字的一项是( ) A.瞋视杜撰纨绔敛声摒气潦
- 2小明去文具店购买2B铅笔,店主说:“如果多买一些,给你打8折“,小明测算了一下.如果买50支,比按原价购买可以便宜6元,
- 3如图,在5×5的正方形网格,每个小正方形的边长都为1,线段AB的端点落在格点上,要求画一个四边形,所作的四边形为中心对称
- 4用数学归纳法证明:1+2平方+2的3次方+.+2的N-1次方=2N次方-1
- 5You were so great意思
- 6请问大家一下这个英语表达 lead other people by the nose 是什么意思 应该怎么应用呢 非常感
- 7甲乙两数的和是7.15,甲数 的小数点向右移动一位后与乙数相等.求甲乙两数.
- 8用酚酞鉴别氢氧化钙溶液 盐酸 蒸馏水
- 9英语情态动词the basketball player is not good with words and he __
- 10为什么化学中C=1000*q*a/M?是如何推导出的?
- 11将X4+X2+2X-1因式分解
- 12若代数式x的平方+3X-9和5-2x的值相等则x的值为?快.
- 13月夜忆舍弟这首诗描写了什么样的景象?渲染了怎样的气氛?
- 14某种药品两次降价后,每盒售价从6.4元降到4.9元.平均每次降价百分之几?
- 15求帮忙计算一道关于债券的现值的一道计算题
