供氧与微生物代谢的关系,如何控制溶氧
 SS跳舞2022-10-04 11:39:541条回答
SS跳舞2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 夜郎退士 共回答了24个问题
夜郎退士 共回答了24个问题 |采纳率79.2%- 如果是摇瓶机(摇床),无法控制溶氧.
如果是培养罐或发酵罐,一般是通过调节通风量来控制溶氧.通常控制溶氧在5-8ppm就行了,低于此数值,就加大通风量.高于此数值,就减少通风量.用测量排气中二氧化碳含量的方法调节通风量,也可以控制溶氧. - 1年前
相关推荐
- 给鱼苗供氧为什么用过氧化钙,而不用过氧化钠?
 bland9191年前1
bland9191年前1 -
 kugu77 共回答了13个问题
kugu77 共回答了13个问题 |采纳率84.6%用过氧化钙的原因是产物氢氧化钙溶解度很小,且很容易和水中溶解的CO2作用形成更难溶的碳酸钙,这样水中的离子浓度、ph值不会有太大变化,对鱼苗的存活有好处.1年前查看全部
- 某瓶氧气的密度是6kg/m 3 ,它表示的物理意义是______.若给人供氧用去了氧气质量的1/3,则瓶内剩余氧气的密度
某瓶氧气的密度是6kg/m 3 ,它表示的物理意义是______.若给人供氧用去了氧气质量的1/3,则瓶内剩余氧气的密度是______kg/m 3 ;容积是10L的瓶子装满了煤油,已知煤油的密度是0.8×10 3 kg/m 3 ,则瓶内煤油的质量是______kg,将煤油倒去4kg后,瓶内剩余煤油的密度是______kg/m 3 .  海南人11年前1
海南人11年前1 -
 大船东 共回答了8个问题
大船东 共回答了8个问题 |采纳率100%①某瓶氧气的密度是6kg/m 3 ,它表示的物理意义是体积是1m 3 氧气的质量为6kg;
②若给人供氧用去了氧气质量的1/3,但气瓶的容积一定,也就是氧气体积不变,则瓶内剩余氧气的密度是原来的
2
3 ,为
2
3 ×6kg/m 3 =4kg/m 3 ;
③瓶内煤油的质量是m=ρV=0.8×10 3 kg/m 3 ×0.01m 3 =8kg;
④将煤油倒去4kg后,瓶内剩余煤油的质量、体积发生变化,但状态没有变化,所以密度仍然是0.8×10 3 kg/m 3 .
故答案为:体积是1m 3 氧气的质量为6kg;4;8;0.8×10 3 .1年前查看全部
- 某瓶氧气的密度是5千克每立方米,给人供氧用去了氧气质量的一半,则瓶内剩余氧气的密度是___________;容积式10升
某瓶氧气的密度是5千克每立方米,给人供氧用去了氧气质量的一半,则瓶内剩余氧气的密度是___________;容积式10升的瓶子装满了内有,已知煤油的密度是0.8*10的三次方㎏每立方米,则瓶内煤油的质量是________,将煤油倒去4㎏后,瓶内剩余煤油的密度是________
我想知道每一个空答案的过程,因为实在让我很一愣的、拜托各位啦, 00_霗_001年前1
00_霗_001年前1 -
 爱已黄昏 共回答了17个问题
爱已黄昏 共回答了17个问题 |采纳率88.2%5/2=2.5
10/1000*0.8*1000=8kg
煤油是液体,密度不变1年前查看全部
- 呼吸面具和潜水艇中可用过氧化钠(Na 2 O 2 )作为供氧剂。为了探究其反应原理,兴趣小组同学在老师的指导下,进行了如
呼吸面具和潜水艇中可用过氧化钠(Na 2 O 2 )作为供氧剂。为了探究其反应原理,兴趣小组同学在老师的指导下,进行了如下探究,请你一起参与。
[查阅资料]过氧化钠在常温下与水、二氧化碳反应分别生成氢氧化钠、碳酸钠和氧气。
[设计实验]浩明同学想通过下图所示装置探究过氧化钠与二氧化碳的反应,并验证反应产物。
(1)下列是实验室常用的仪器:
①A是二氧化碳气体的发生装置,装配该装置时,应选用的仪器除带导管的双孔橡皮塞外,还需要的仪器有(填名称) 、 。实验室制取二氧化碳的化学方程式 。该装置在实验室还可以用来制取氧气,写出用该装置制取氧气的化学方程式 。
②实验室选择制取气体的发生装置,主要依据是 、 。
(2)用D所示的方法收集氧气,其依据是 ;收集氧气时,还可以选用 法收集。检验D装置试管内收集到中的气体是否氧气的方法、现象及结论是:待D中气体集满后,把试管移出水面,然后
。
(3)C中氢氧化钠的作用是吸收没有参与反应的CO 2 ,如果没有连接这个装置,可能导致的后果是 。
(4)检验B中反应后剩余固体的成分。实验步骤 实验现象 实验结论及方程式 ①取少量A中反应后的固体于试管中;
② ;
③
。
②
③反应后生成的固体是碳酸钠。写出步骤③的化学方程式
[反思与评价](1)通过上述实验,明明同学认为Na 2 O 2 与CO 2 反应除了生成Na 2 CO 3 和O 2 ,还有可能生成NaHCO 3 。你认为他的结论 (选填“正确”或“不正确”),理由是 。写出Na 2 O 2 与二氧化碳反应的化学方程式 。
请说说呼吸面具或潜水艇用过氧化钠作为供氧剂的最大的是优点 。 沈天陌1021年前1
沈天陌1021年前1 -
 红棕竹 共回答了18个问题
红棕竹 共回答了18个问题 |采纳率100%1年前查看全部
- (2014•东城区二模)鱼塘供氧时常向水中撒固体过氧化钙(CaO2),它与水反应可释放氧气:2CaO2+2H2O═2Ca
(2014•东城区二模)鱼塘供氧时常向水中撒固体过氧化钙(CaO2),它与水反应可释放氧气:2CaO2+2H2O═2Ca(OH)2+O2↑.若将108gCaO2投入到鱼塘中,试计算可生成氧气的质量.
 spring07281年前1
spring07281年前1 -
 tomkansky 共回答了13个问题
tomkansky 共回答了13个问题 |采纳率84.6%解题思路:根据CaO2的质量,找出已知量和未知量,计算出相对分子质量,列出比例式进行计算设可生成氧气的质量为x.
2CaO2+2H2O═2Ca(OH)2+O2↑.
14432
108gx
[144/32]=[108g/x]
X=24 g
答:可生成氧气的质量为24g.点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 本题考查了根据方程式计算的基本步骤,解答时要注意格式规范.1年前查看全部
- (11分)在面具和潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验用品、用下图中的实验装置进行实验,证明过氧化
(11分)在面具和潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验用品、用下图中的实验装置进行实验,证明过氧化钠可作供氧剂。

(1)A是制取CO 2 的装置。写出A中发生反应的化学方程式: 。
(2)填写表中空格:
(3)写出过氧化钠与二氧化碳反应的化学方程式: 。仪器 加入试剂 加入该试剂的目的 B 饱和NaHCO 3 溶液 C D
(4)试管F中收集满气体后,下一步实验操作是 。 宁仇1年前1
宁仇1年前1 -
 山外树青 共回答了22个问题
山外树青 共回答了22个问题 |采纳率95.5%(1)CaCO 3 +2HCl===CaCl 2 +H 2 O+CO 2 ↑
(2)
仪器
加入试剂
加入该试剂的目的
B
除去CO 2 气体中混入的HCl
C
过氧化钠
与CO 2 和水蒸气反应,产生O 2
D
NaOH溶液
吸收未反应的CO 2 气体
(3)2Na 2 O 2 +2CO 2 ===2Na 2 CO 3 +O 2
(4)把E中的导管移出水面,关闭分液漏斗活塞,用拇指堵住试管口,取出试管,将试管正立,松开拇指,立即把带火星的木条伸入。
1年前查看全部
- (2013•崇明县二模)Na2O2是一种淡黄色固体,常用作潜水艇的供氧剂.下列关于Na2O2的描述正确的是( )
(2013•崇明县二模)Na2O2是一种淡黄色固体,常用作潜水艇的供氧剂.下列关于Na2O2的描述正确的是( )
A.Na2O2晶体中阴阳离子个数之比为1:1
B.Na2O2晶体中既有离子键又有非极性共价键
C.Na2O2在空气中加热可以得到更稳定的Na2O
D.Na2O2长期露置于空气中最终转变成NaOH konji1231年前1
konji1231年前1 -
 群体无意识 共回答了19个问题
群体无意识 共回答了19个问题 |采纳率89.5%解题思路:A.Na2O2晶体中阳离子为Na+、阴离子为O22-;
B.一般金属元素与非金属元素形成离子键,同种非金属元素之间形成非极性键,不同种非金属元素之间形成极性共价键;
C.Na2O2比Na2O稳定;
D.Na2O2易与水反应生成NaOH,NaOH吸收空气中的水和CO2生成Na2CO3•xH2O,Na2CO3•xH2O风化脱水生成Na2CO3.A.Na2O2晶体中阳离子为Na+、阴离子为O22-,所以Na2O2晶体中阴阳离子个数之比为1:2,故A错误;
B.过氧化钠中钠离子和过氧根离子间存在离子键,过氧根离子中氧原子和氧原子之间存在非极性共价键,故B正确;
C.Na2O2比Na2O稳定,所以Na2O在空气中加热可以得到更稳定的Na2O2,故C错误;
D.Na2O2易与水反应生成NaOH,NaOH吸收空气中的水和CO2生成Na2CO3•xH2O,Na2CO3•xH2O风化脱水生成Na2CO3,故D错误;
故选B.点评:
本题考点: 钠的重要化合物.
考点点评: 本题主要考查了Na2O2的组成与结构、化学性质等,难度不大,根据课本知识即可完成.1年前查看全部
- 过氧化钠(Na2O2)因能与二氧化碳反应生成氧气,故可作为呼吸面具中氧气的来源.潜水艇紧急情况时,也使用过氧化钠来供氧,
过氧化钠(Na2O2)因能与二氧化碳反应生成氧气,故可作为呼吸面具中氧气的来源.潜水艇紧急情况时,也使用过氧化钠来供氧,有关反应的化学方程式为:2Na2O2+2CO2═2Na2CO3+O2从该反应获取的以下信息中,正确的是( )
A.过氧化钠属于氧化物
B.该反应属于置换反应
C.反应前后氧元素的化合价发生变化
D.实验室可利用这一原理制取纯净的氧气 太极爱好者1年前1
太极爱好者1年前1 -
 你是闰土我是rain 共回答了17个问题
你是闰土我是rain 共回答了17个问题 |采纳率100%解题思路:A、氧化物是由两种元素组成并且一种元素是氧元素的化合物;
B、根据反应物和生成物的种类可以判断反应类型;
C、氧元素在化合物中一般显负价,在单质中氧元素的化合价为零;
D、二氧化碳和氧气在通常情况下都是气体.A、过氧化钠是由钠元素和氧元素组成的化合物,属于氧化物;故对
B、生成物中,碳酸钠属于化合物,氧气属于单质,但是反应物中,过氧化钠和二氧化碳都是化合物,所以该反应不属于置换反应;故错
C、在过氧化钠中,氧元素的化合价是-1价,在二氧化碳中,氧元素的化合价是-2价,在碳酸钠中,氧元素的化合价是-2价,氧气的化合价为零,反应前后氧元素的化合价发生了变化.故对
D、因为二氧化碳在通常情况下也是气体,用这一原理制取的氧气中一般含有二氧化碳.故错
故选AC.点评:
本题考点: 从组成上识别氧化物;有关元素化合价的计算;置换反应及其应用.
考点点评: 本题主要考查物质的分类和元素化合价方面的知识,解答时要从氧化物和化合价概念方面进行分析、判断,从而得出正确的结论.1年前查看全部
- 青藏铁路已全线贯通,即将投入运营的高原列车有完善的供氧系统和完备的医疗应急系统,这样做是因为 [
青藏铁路已全线贯通,即将投入运营的高原列车有完善的供氧系统和完备的医疗应急系统,这样做是因为 [ ]
A、高原空气稀薄,大气压强小
B、高原空气稀薄,大气压强大
C、高原空气稠密,大气压强小
D、高原空气稠密,大气压强大 jane0253501年前1
jane0253501年前1 -
 一个人在雨中 共回答了16个问题
一个人在雨中 共回答了16个问题 |采纳率81.3%A1年前查看全部
- 某瓶氧气的密度是5kg/m3,给人供氧用去了氧气质量的一半,则瓶内剩余氧气的密度是______kg/m3.伊利牌盒装牛奶
某瓶氧气的密度是5kg/m3,给人供氧用去了氧气质量的一半,则瓶内剩余氧气的密度是______kg/m3.伊利牌盒装牛奶的体积是2.5×10-4m3,若测得该盒牛奶的质量是0.3kg,则该牛奶的密度为______ kg/m3.喝掉一半后,牛奶的密度将______ (选填“变大”“变小”或“不变”)
 小猪仔1231年前1
小猪仔1231年前1 -
 bay108 共回答了22个问题
bay108 共回答了22个问题 |采纳率90.9%解题思路:(1)氧气用掉一半,质量减半,氧气还充满整个氧气瓶,体积保持不变,根据密度公式判断密度的变化.
(2)已知牛奶的体积和质量,根据密度公式求出该牛奶的密度;密度是物质的一种特性,与物质的质量和体积无关.(1)一瓶氧气的密度为5kg/m3,给人供氧用去了氧气质量的一半,但体积保持不变,
根据ρ=[m/V]可知,剩余氧气的密度变为原来的一半,即ρ′=2.5kg/m3.
(2)装牛奶的密度:
ρ=[m/V]=
0.3kg
2.5×10−4m3=1.2×103kg/m3,
∵密度与物质的体积和质量无关,
∴喝掉一半时,牛奶的密度不变.
故答案为:2.5;1.2×103;不变.点评:
本题考点: 密度的计算;密度及其特性.
考点点评: 本题考查了密度的计算和学生对密度特性的理解与掌握,关键是知道氧气瓶的容积不变即所装氧气的体积不变.1年前查看全部
- 下列说法不正确的是( )A.过氧化钠可用作供氧剂B.明矾可用作净水剂C.碳酸氢钠可用焙制糕点发酵粉D.可以用电解熔融的
下列说法不正确的是( )
A.过氧化钠可用作供氧剂
B.明矾可用作净水剂
C.碳酸氢钠可用焙制糕点发酵粉
D.可以用电解熔融的氯化钠、氯化镁、氯化铝分别制取钠、镁、铝 joe_sunjun1年前1
joe_sunjun1年前1 -
 7号劳尔 共回答了11个问题
7号劳尔 共回答了11个问题 |采纳率100%解题思路:A、根据过氧化钠能与二氧化碳反应生成碳酸钠和氧气;
B、根据盐类水解的生成物的性质分析;
C、碳酸氢钠受热分解为碳酸钠、水以及二氧化碳,据此回答;
D、氯化铝不导电.A.过氧化钠能与二氧化碳反应生成碳酸钠和氧气,所以过氧化钠可用作供氧剂,故A正确;
B、明矾是强酸弱碱盐,在水溶液里能发生水解生成氢氧化铝胶体,氢氧化铝胶体具有吸附性,所以能作净水剂,故B正确;
C、碳酸氢钠受热分解为碳酸钠、水以及二氧化碳,可用焙制糕点发酵粉,故C正确;
D、氯化铝不导电,工业上利用电解熔融的氧化铝来得到单质铝,故D错误.
故选D.点评:
本题考点: 金属冶炼的一般原理;钠的重要化合物.
考点点评: 本题考查知识点较多,涉及盐类水解、金属冶炼及化学与生活的知识,注重基础知识的考查,题目难度不大.1年前查看全部
- 供、厌氧菌种生长特性表现在哪里?(在供氧、厌氧的发酵过程中菌种的特点)
 狗aa1年前1
狗aa1年前1 -
 kzhr 共回答了17个问题
kzhr 共回答了17个问题 |采纳率88.2%形成大颗粒活性污泥絮团,结构紧密,沉降性能较好,SV达到30%,SVI达到100mg/L,MLSS达到2000~3000mg/L
钟虫大量出现,轮虫增多1年前查看全部
- 下列反应可以用来制氧气,其中适合潜水员潜水时供氧的反应是:
下列反应可以用来制氧气,其中适合潜水员潜水时供氧的反应是:
A 过氧化氢————水+氧气
B 过氧化钠+二氧化碳————碳酸钠+氧气 河马叔叔龟1年前1
河马叔叔龟1年前1 -
 2d453b15370b7959 共回答了19个问题
2d453b15370b7959 共回答了19个问题 |采纳率94.7%B
不仅能产生氧气还能吸收二氧化碳,一举两得1年前查看全部
- 氧气跟炭、铁丝、蜡烛等物质反应,我们可以看出氧气是一种化学性质______的气体,他在氧化反应中能供氧,具有______
氧气跟炭、铁丝、蜡烛等物质反应,我们可以看出氧气是一种化学性质______的气体,他在氧化反应中能供氧,具有______性,是一种常用的氧化剂.
 超级兔子飞1年前1
超级兔子飞1年前1 -
 hyh2 共回答了19个问题
hyh2 共回答了19个问题 |采纳率89.5%解题思路:根据氧气的性质、用途分析回答.氧气的化学性质比较活泼,能够支持燃烧、供给呼吸,是一种常用的氧化剂.在一定条件下,氧气跟炭、铁丝、蜡烛等物质反应,我们可以看出氧气是一种化学性质比较活泼的气体,他在氧化反应中能供氧,具有氧化性,是一种常用的氧化剂.
故答为:比较活泼;氧化.点评:
本题考点: 氧气的化学性质.
考点点评: 本题主要考查物质的性质和用途,比较简单,了解氧气的性质和用途即可解答.1年前查看全部
- 鱼塘供氧时常向水中撒一种微黄色的固体过氧化钙(CaO 2 ).
鱼塘供氧时常向水中撒一种微黄色的固体过氧化钙(CaO 2 ).
(1)将该反应方程式补充完整:2CaO 2 +2H 2 O=2______+O 2 ↑.
(2)若向水中投入72g CaO 2 ,能生成氧气多少克? 棋子691年前1
棋子691年前1 -
 joney128 共回答了26个问题
joney128 共回答了26个问题 |采纳率84.6%(1)反应物中含有2个钙原子、4个氢原子、6个氧原子,生成物中已经有了2个氧原子,还少2个钙原子、4个氢原子、4个氧原子因为待求物质前面系数是2,所以化学式为Ca(OH) 2 ;
(2)设若向水中投入72g CaO 2 ,能生成氧气质量为X则:
2CaO 2 +2H 2 O=2Ca(OH) 2 +O 2 ↑.
144 32
72g X
根据:
144
32 =
72g
X 解得X=16g.
答:若向水中投入72g CaO 2 ,能生成氧气质量为16g.
故答案为:16g.1年前查看全部
- (2013•平谷区一模)化学小组同学在课外读物中看到:“Na2O2广泛应用于潜艇的呼吸供氧和CO2的去除.”他们决定探究
(2013•平谷区一模)化学小组同学在课外读物中看到:“Na2O2广泛应用于潜艇的呼吸供氧和CO2的去除.”他们决定探究CO2与Na2O2反应的产物.提出猜想CO2与Na2O2反应可能生成O2和Na2CO3.查阅资料
①Na2O2是一种淡黄色固体,常温下与CO2、H2O等物质反应,反应的化学方程式分别为:2Na2O2+2CO2=2Na2CO3+O2、2Na2O2+2H2O=4NaOH+O2↑.
②CO2既不与NaHCO3反应,也不溶于饱和的NaHCO3溶液中.
③Na2O2与稀盐酸反应时,生成NaCl、H2O和O2.
实验过程同学们在老师的指导下利用如下图所示装置(部分夹持仪器已略去)进行实验
(1)实验时上述仪器正确的连接顺序为m接______(填接口字母).
(2)检验有氧气产生的方法是将______放在接口______处(填接口字母);证明有氧气产生的实验现象是______.
(3)检验有Na2CO3生成的方法是______.
(4)使气体通过D装置的原因是______. liuyunfei1231年前1
liuyunfei1231年前1 -
 寡人有急 共回答了15个问题
寡人有急 共回答了15个问题 |采纳率86.7%解题思路:(1)分析装置的作用,A是制取二氧化碳,B是干燥二氧化碳,C是除去未反应的二氧化碳,D是除去氯化氢气体,E是二氧化碳与过氧化钠反应,然后结合题意:检验反应产物,确定装置的连接顺序,洗气装置导管是长进短出;
(2)检验氧气可用带火星的木条,若复燃则有氧气;
(3)依据碳酸钠可用稀盐酸检验是否生成二氧化碳进行分析;
(4)D是除去氯化氢气体.(1)根据题意,Na2O2是一种淡黄色固体,常温下与CO2、H2O等物质反应,Na2O2与稀盐酸可反应,生成NaCl、H2O和O2,CO2既不与NaHCO3反应,也不溶于饱和的NaHCO3溶液中;所以要让二氧化碳与过氧化钠反应,先要排除可能稀盐酸挥发的氯化氢气体,将生成的二氧化碳通过D,由于气体从溶液中出来时要带来水蒸气,故要通过浓硫酸除去水蒸气,然后将除杂后的二氧化碳通入过氧化钠,通过氢氧化钠溶液除去未反应的二氧化碳,最后检验生成的气体是否是氧气;
(2)检验是否有氧气可用带火星的木条放于接口d处,若复燃则说明生成了氧气;
(3)检验有Na2CO3生成的方法是:取E中反应后的固体放于试管,滴加稀盐酸,将生成的气体通入澄清的石灰水,若澄清的石灰水变浑浊,说明有碳酸钠生成;
(4)使气体通过D装置的原因是除去氯化氢气体,防止进入E装置与过氧化钠固体反应造成干扰;
故答案为:(1)e,f接a,b接g,h接c;
(2)带火星的木条;d;带火星的木条复燃;
(3)取E中反应后的固体放于试管,滴加稀盐酸,将生成的气体通入澄清的石灰水,澄清的石灰水变浑浊;
(4)除去氯化氢气体.点评:
本题考点: 实验探究物质的性质或变化规律.
考点点评: 分析装置的作用,能正确分析题目所蕴含的信息,并能依据题意分析解答相关问题是解题的关键.1年前查看全部
- 青藏铁路已全线贯通,即将投入运营的高原列车有完善的供氧系统和完备的医疗应急系统,这样做是因为 [
青藏铁路已全线贯通,即将投入运营的高原列车有完善的供氧系统和完备的医疗应急系统,这样做是因为 [ ]
A、高原空气稀薄,大气压强小
B、高原空气稀薄,大气压强大
C、高原空气稠密,大气压强小
D、高原空气稠密,大气压强大 我不要来生1年前1
我不要来生1年前1 -
 睦平 共回答了17个问题
睦平 共回答了17个问题 |采纳率88.2%A1年前查看全部
- 过氧化钠(Na2O2)因能与二氧化碳反应生成氧气,故可作为呼吸面具中氧气的来源.潜水艇紧急情况时,也使用过氧化钠来供氧,
过氧化钠(Na2O2)因能与二氧化碳反应生成氧气,故可作为呼吸面具中氧气的来源.潜水艇紧急情况时,也使用过氧化钠来供氧,有关反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2从该反应获取的以下信息中,正确的是( )
①过氧化钠属于氧化物
②该反应属于化合反应
③反应前后氧元素的化合价发生变化
④实验室可利用这一原理制取纯净的氧气.
A.①③
B.②④
C.②③④
D.①②③ summer81041年前1
summer81041年前1 -
 nn太无眼 共回答了20个问题
nn太无眼 共回答了20个问题 |采纳率85%解题思路:根据已有的知识进行分析,氧化物是指由两种元素组成且其中一种是氧元素的化合物;化合反应是由两种或两种以上的物质生成一种物质的化学反应;根据反应的化学方程式以及物质的化学式进行分析解答即可.①过氧化钠是由钠元素和氧元素两种元素组成的化合物,属于氧化物;
②该反应生成的是两种物质,不属于化合反应;
③反应前氧元素是化合态的,反应后生成了氧气,氧气是单质,氧元素的化合价为零,氧元素的化合价发生变化;
④实验室可利用这一原理可以制取氧气,但是有气体二氧化碳参与,得到的不是纯净的氧气;
观察选项,故选A.点评:
本题考点: 从组成上识别氧化物;有关元素化合价的计算;反应类型的判定.
考点点评: 本题考查了物质的类别以及反应类型的判断,完成此题,可以依据已有的知识进行.1年前查看全部
- 在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.请选用适当的化学试剂和实验用品、用图中的实验装置进行实验,证明过氧化钠可作供
 在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.请选用适当的化学试剂和实验用品、用图中的实验装置进行实验,证明过氧化钠可作供氧剂.
在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.请选用适当的化学试剂和实验用品、用图中的实验装置进行实验,证明过氧化钠可作供氧剂.
(1)A是实验室制取CO2的装置.写出A中发生反应的离子方程式:______.
(2)B装置中装有饱和的NaHCO3溶液,其作用是:______.
(3)写出过氧化钠与二氧化碳反应的化学方程式:______.该反应中氧化剂是______,还原剂是______,反应过程中氧化剂与还原剂的物质的量之比为______. ee有眼6666661年前1
ee有眼6666661年前1 -
 brkb 共回答了15个问题
brkb 共回答了15个问题 |采纳率93.3%解题思路:(1)二氧化碳的实验室制法:用稀盐酸与大理石反应,根据离子方程式的书写方法来回答;
(2)根据实验目的来分析仪器B加入饱和的NaHCO3溶液的目的;
(3)根据化学方程式书写的步骤:写配注等,写出反应方程式,根据化合价的升降来确定氧化剂和还原剂以及物质的量之比.(1)二氧化碳的实验室制法是用稀盐酸与大理石反应,发生反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,改为离子方程式为:CaCO3+2H+=Ca2++H2O+CO2↑,故答案为:CaCO3+2H+=Ca2++H2O+CO2↑;(2)用稀盐酸与大理...
点评:
本题考点: 钠的重要化合物;氧化还原反应.
考点点评: 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.1年前查看全部
- 下列各组物质与其用途的关系不正确的是 [ ] A.过氧化钠:供氧剂
下列各组物质与其用途的关系不正确的是 [ ]A.过氧化钠:供氧剂
B.烧碱:治疗胃酸过多的一种药剂
C.小苏打:发酵粉主要成分
D.明矾:净水剂 第N类1年前1
第N类1年前1 -
 ac1899 共回答了20个问题
ac1899 共回答了20个问题 |采纳率90%B1年前查看全部
- 必修一 请问潜水艇与防毒面具 供氧的原理各是什么 原理相同吗
 板板1221年前2
板板1221年前2 -
 98765432104 共回答了22个问题
98765432104 共回答了22个问题 |采纳率100%一样的1年前查看全部
- 在呼吸面具和潜水艇中可用过氧化钠(Na2O2)作为供氧剂.甲、乙两同学选用适当的化学试剂和实验用品,利用下图中的实验装置
在呼吸面具和潜水艇中可用过氧化钠(Na2O2)作为供氧剂.甲、乙两同学选用适当的化学试剂和实验用品,利用下图中的实验装置进行实验,证明过氧化钠可用于制取氧气.(友情提示:过氧化钠常温下与二氧化碳反应时生成氧气和一种盐,与水反应时生成氧气和一种碱,NaHCO3与Na2CO3性质相似)

(1)A是用大理石制取CO2的装置.写出A中发生反应的化学方程式:______;
(2)按要求填写下表中的空格:
(3)试管F中收集满气体后,把E中的导管移出水面,关闭分液漏斗活塞,用姆指堵住试管口,取出试管;则证明此气体为氧气的方法是______.
(4)乙同学说“上述装置不能证明O2只是由过氧化钠与CO2反应产生的”,若证明“是…”,你认为应如何改进上述装置?______. gaoxin204195121年前1
gaoxin204195121年前1 -
 jay75262315 共回答了11个问题
jay75262315 共回答了11个问题 |采纳率54.5%解题思路:(1)A是用大理石制取CO2的装置,反应物和生成物知道,可以实现化学方程式.
(2)B试剂:饱和碳酸氢钠溶液,是吸收混在二氧化碳中的氯化氢气体的;D试剂:NaOH溶液,吸收未反应的二氧化碳.
(3)①注意步骤:把E中的导管移出水面,关闭分液漏斗活塞,用姆指堵住试管口,取出试管.②掌握检验氧气的方法:把带火星的木条伸入试管口内,木条复燃.
(4)已知“过氧化钠常温下与二氧化碳反应时生成氧气和一种盐,与水反应时生成氧气和一种碱,”所以应保证进出C装置的气体中都无水,从而排除水的影响,(1)反应物为大理石(CaCO3)和盐酸,则根据复分解反应的规律实现化学方程式.
(2)B试剂:吸收混在二氧化碳中的氯化氢气体;D试剂:NaOH溶液,吸收未反应完的二氧化碳.
(3)检验氧气的方法:把带火星的木条伸入试管口内,木条复燃.
(4)在B、C和C、D装置之间,各加上一个干燥装置,则保证C装置的气体一定只为二氧化碳.所以便可“证明O2只是由过氧化钠与CO2反应产生的.”
故答为:(1)CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)B、除去CO2气体中混入的HCl;D、NaOH溶液;
(3)把带火星的木条伸入试管口内,木条复燃,证明试管中的气体是氧气;
(4)在B、C和C、D装置之间,各加上一个干燥装置.点评:
本题考点: 实验探究物质的性质或变化规律;氧气的检验和验满;二氧化碳的实验室制法;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查了如何探究物质的性质和变化规律,掌握反应现象与本质的联系和制取二氧化碳方法和氧气的检验方法.1年前查看全部
- 在潜艇和消防员的呼吸面具中,常用Na2O2作供氧剂.某潜水艇上有50人,如果每人每分钟消耗的O2在标准状况下的体积为0.
在潜艇和消防员的呼吸面具中,常用Na2O2作供氧剂.某潜水艇上有50人,如果每人每分钟消耗的O2在标准状况下的体积为0.80L,则一天需要多少kgNa2O2?
 xw19771年前1
xw19771年前1 -
 路人甲1988 共回答了15个问题
路人甲1988 共回答了15个问题 |采纳率100%解题思路:反应的相关方程式为2Na2O2+2CO2═2Na2CO3+O2,一天共需要氧气的体积为50×0.80L×60×24=57600L,物质的量为[57600L/22.4L/mol]=2571.4mol,结合反应的方程式计算.一天共需要氧气的体积为50×0.80L×60×24=57600L,物质的量为[57600L/22.4L/mol]=2571.43mol,
则2Na2O2+2CO2═2Na2CO3+O2
2mol 1mol
x 2571.4mol
x=5142.86mol,
m(Na2O2)=5142.86mol×78g/mol=401143.08g=401.143kg,
答:一天需要401.143kgNa2O2.点评:
本题考点: 化学方程式的有关计算.
考点点评: 本题考查化学方程式的计算,侧重于学生的分析能力和计算能力的考查,难度不大注意根据方程式计算该题.1年前查看全部
- 下列说法不正确的是( )A.钠在氧气中燃烧生成淡黄色的固体Na2O2,可做为呼吸面具的供氧剂B.液氯是氯气的水溶液,它
下列说法不正确的是( )
A.钠在氧气中燃烧生成淡黄色的固体Na2O2,可做为呼吸面具的供氧剂
B.液氯是氯气的水溶液,它能使干燥的有色布条褪色
C.氯气能与大多数金属化合,生成金属氯化物(盐)
D.氯水具有杀菌、漂白作用是因氯水中含有强氧化性的次氯酸 zicha1年前1
zicha1年前1 -
 Diwint 共回答了19个问题
Diwint 共回答了19个问题 |采纳率78.9%解题思路:A、钠在氧气中燃烧生成淡黄色的固体Na2O2,会和二氧化碳、水反应生成氧气,所以可以做供氧剂;
B、液氯是液态的氯气,是纯净物,不能使干燥的有色布条褪色;
C、氯气是一种强氧化剂,可以氧化大多数具有还原性的金属生成金属氯化物;
D、氯水是氯气溶于水形成的,既有溶解的氯气,也有和水反应生成的次氯酸和盐酸,其中次氯酸具有杀菌、漂白作用;A、过氧化钠和人呼出的二氧化碳气体发生反应:2Na2O2+2CO2=Na2CO3+O2↑可作为呼吸面具中的供氧剂,故A正确;
B、液态氯是纯净物,没有水不能生成次氯酸,不能使干燥的有色布条褪色,故B错误;
C、氯气是典型的具有强氧化性的非金属单质,易与大多数金属化合生成氯化物,故C正确;
D、氯水中发生反应Cl2+H2O=HCl+HClO,次氯酸是一种强氧化性的漂白剂,具有杀菌、消毒、漂白的作用,故D正确;
故选B.点评:
本题考点: 氯气的化学性质;钠的重要化合物.
考点点评: 本题考查了过氧化钠、氯气、次氯酸的化学性质应用.1年前查看全部
- 呼吸面具和潜水艇中可用过氧化钠(Na2O2)作为供氧剂.查资料是:过氧化钠在常温下与二氧化碳反应生成一种盐和氧气;其化学
呼吸面具和潜水艇中可用过氧化钠(Na2O2)作为供氧剂.查资料是:过氧化钠在常温下与二氧化碳反应生成一种盐和氧气;其化学方程式为______.与实验室用KmnO4制氧气的方法相比,用过氧化钠作为呼吸面具供氧剂的主要优点是(写2条)______;______.
 Hunter_731年前1
Hunter_731年前1 -
 liban 共回答了16个问题
liban 共回答了16个问题 |采纳率81.3%解题思路:按照书写化学方程式的步骤,先写化学式,然后配平,再注明条件.从过氧化钠能与二氧化碳反应生成氧气角度考虑.Na2O2与二氧化碳反应生成碳酸钠和氧气,化学方程式为:2Na2O2+2CO2=2Na2CO3+O2;与我们学过的制氧气方法相比,过氧化钠作为呼吸面具和潜水艇的供氧剂,装置简单,反应能在常温下进行;与CO2反应产生供人呼吸的氧气.
故答案为:2Na2O2+2CO2=2Na2CO3+O2;装置简单,反应在常温下进行;与CO2反应产生供人呼吸的氧气.点评:
本题考点: 化学实验方案设计与评价;书写化学方程式、文字表达式、电离方程式.
考点点评: 该实验题具有实际意义,属于身边的化学,要平时多留心,多积累,做到触类旁通.1年前查看全部
- 等质量时,KO2供氧能力是Na2O2的多少倍?
 砖瓦厂kk1年前1
砖瓦厂kk1年前1 -
 茜草忧伤 共回答了17个问题
茜草忧伤 共回答了17个问题 |采纳率88.2%等质量 先算KO2、Na2O2 摩尔数 按化学方程式算产生氧气多少 得出答案 5年多没接触化学了 相对分子质量忘光了 楼主自己算下 .1年前查看全部
- 在呼吸面具和潜水艇中可用过氧化纳作为供氧剂.请选用适当的化学试剂和实验用品、用如图中的实验装置进行实验,证明过氧化钠可作
在呼吸面具和潜水艇中可用过氧化纳作为供氧剂.请选用适当的化学试剂和实验用品、用如图中的实验装置进行实验,证明过氧化钠可作供氧剂.

(1)A是制取CO2的装置.写出A中发生反应的化学方程式:______.
(2)填写表中空格:
(3)写出过氧化钠与二氧化碳反应的化学方程式:______.仪器 加入试剂 加入该试剂的目的 B 饱和NaHCO3溶液 ______ C ______ ______ D ______ ______
(4)试管F中收集满气体后,下一步实验操作是:______.
(5)每生成1mol D同时生成______mol E. 寒风子1年前1
寒风子1年前1 -
 qwrjrnnr 共回答了18个问题
qwrjrnnr 共回答了18个问题 |采纳率94.4%解题思路:由实验装置可知,本实验首先由CaCO3和盐酸反应生成CO2,产生气体通过饱和NaHCO3溶液,以除去CO2气体中混入的HCl,然后过氧化钠与CO2和水气反应,产生O2,用排水法收集O2,最后取出试管,立即把带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气;依据化学方程式计算物质的量;(1)A为由CaCO3和盐酸反应生成CO2,反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,
故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)产生气体通过饱和NaHCO3溶液,以除去CO2气体中混入的HCl,然后过氧化钠与CO2和水气反应,产生O2,由于生成的氧气中混有二氧化碳气体,应用NaOH溶液洗气,吸收未反应的
CO2气体,用排水法收集O2,
故答案为:
仪器 加入试剂 加入该试剂的目的
B 除去CO2气体中混入的HCl
C 过氧化钠 与CO2和水气反应,产生O2
D NaOH溶液 吸收未反应的CO2气体(3)过氧化钠与二氧化碳反应生成碳酸钠和氧气,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2;
故答案为:2Na2O2+2CO2=2Na2CO3+O2;
(4)本实验的目的为证明过氧化钠可作供氧剂,收集气体后要验证是否为氧气,为防止倒吸,应先把E中的导管移出水面,然后关闭分液漏斗活塞,用带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气,
故答案为:把E中的导管移出水面,关闭分液漏斗活塞,用拇指堵住试管口,取出试管,立即把带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气;
(5)D为氢氧化钠,E为氧气,反应生成的化学方程式为:2Na2O2+2H2O=4NaOH+O2;生成4mol氢氧化钠同时生成氧气1mol,所以生成1mol氢氧化钠,同时生成0.25mol氧气;
故答案为:0.25mol;点评:
本题考点: 碱金属及其化合物的性质实验.
考点点评: 本题考查过氧化钠的性质的实验设计,题目难度不大,解答本题注意把握实验原理和相关实验的基本操作,注意除杂的先后顺序和检验氧气的操作方法.1年前查看全部
- 举例说明供氧与微生物代谢有何关系?
 Phantom1981年前1
Phantom1981年前1 -
 wtx136 共回答了24个问题
wtx136 共回答了24个问题 |采纳率95.8%比如,酵母菌在无氧和缺氧的环境下进行有氧呼吸,代谢产生酒精,在有氧环境下进行有氧呼吸,生成二氧化碳和水,还有就是氧气的浓度会影响代谢的速度,就是方程式从左向右进行的速度,这个可以由化学平衡来解释··望采纳1年前查看全部
- (2007•苏州)青藏铁路已全线贯通,已经投入运营的高原列车有完善的供氧系统和完备的医疗应急系统,这样做主要是因为(
(2007•苏州)青藏铁路已全线贯通,已经投入运营的高原列车有完善的供氧系统和完备的医疗应急系统,这样做主要是因为( )
A.高原空气稀薄,大气压强小 B.高原空气稀薄,大气压强大 C.高原空气稠密,大气压强小 D.高原空气稠密,大气压强大  abby_45141年前1
abby_45141年前1 -
 三jgt 共回答了15个问题
三jgt 共回答了15个问题 |采纳率93.3%解题思路:高原反应指的是人到高原后由于气压随地理高度的增高而减小,体内压强大于外界的大气压,从而引起头痛、恶心、胸闷等现象。
高原上空气比较稀薄,大气压强减小
A
1年前查看全部
- 在密封居室中使用煤炉取暖做饭,由于通风不良,供氧不充分,可产生大量的什么气体积蓄在室内?
在密封居室中使用煤炉取暖做饭,由于通风不良,供氧不充分,可产生大量的什么气体积蓄在室内?
A.二氧化碳
B.一氧化碳
C.氮气
D.氧气 sunhaitian1年前1
sunhaitian1年前1 -
 无灰世界 共回答了16个问题
无灰世界 共回答了16个问题 |采纳率93.8%选 B一氧化碳1年前查看全部
- 在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验用品,用下图中的实验装置进行实验,证明过氧化钠可作
在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验用品,用下图中的实验装置进行实验,证明过氧化钠可作供氧剂。 
(1)A是制取CO 2 的装置。写出A中发生反应的化学方程式:______________________。
(2)填写表中空格。
(3)写出过氧化钠与二氧化碳反应的化学方程式:_______________________。
(4)试管F中收集满气体后,下一步实验操作是:_______________________。 xiaoqingo1年前1
xiaoqingo1年前1 -
 gmyzlp 共回答了25个问题
gmyzlp 共回答了25个问题 |采纳率100%(1)CaCO 3 +2HCl = CaCl 2 + H 2 O + CO 2 ↑
(2)除去CO 2 中混入的HCl;过氧化钠;与CO 2 和水蒸气反应,产生O 2 ;NaOH溶液;吸收未反应的CO 2 气体
(3)2Na 2 O 2 +2CO 2 =2NaCO 3 +O 2
(4)把E中导管移出水面,关闭分液漏斗活塞,用拇指堵住试管口,取出试管,立即将带火星的木条伸入试管口内,若带火星的木条复燃,则证明试管中收集的气体是O 21年前查看全部
- ko2和na2o2那个适合做供氧剂
 dawh20081年前1
dawh20081年前1 -
 寒萧轩 共回答了22个问题
寒萧轩 共回答了22个问题 |采纳率100%假设同样质量为m的ko2和na2o2
4KO2+2CO2═2K2CO3+3O2↑
4 3
m/71 x
2Na2O2+2CO2=2Na2CO3+O2↑
2 1
m/78 y
求得x/y=107/71>1 因此 相同质量的两种物质KO2生成更多的氧气
同时4molKO2产生3mol氧气,4molNa2O2产生2mol氧气,相对来说KO2产生氧气多,而且重量轻,反应速度更快更适合做供氧剂,宇宙飞船也用,但相对价格高些1年前查看全部
- 下列说法不正确的是( )A.Na2O2能与CO2反应,可用作呼吸面具的供氧剂B.SiO2有导电性,可用于制备光导纤维C
下列说法不正确的是( )
A.Na2O2能与CO2反应,可用作呼吸面具的供氧剂
B.SiO2有导电性,可用于制备光导纤维
C.硅胶常用作实验室和食品、药品等的干燥剂,也可作催化剂载体
D.小苏打是一种膨松剂,可用于制作馒头和面包 xiongxiong3131年前1
xiongxiong3131年前1 -
 matchbox1997 共回答了21个问题
matchbox1997 共回答了21个问题 |采纳率100%解题思路:A.Na2O2能与CO2反应生成氧气;
B.SiO2不能导电,但具有较好的折光性;
C.根据硅胶表面积大,吸附性强的性质判断;
D.小苏打不稳定,可分解生成二氧化碳气体.A.Na2O2能与CO2反应生成氧气,可用作呼吸面具的供氧剂,故A正确;
B.SiO2不能导电,但具有较好的折光性,故B错误;
C.硅胶表面积大,吸附性强,常用作实验室和食品、药品等的干燥剂,也可作催化剂载体,故C正确;
D.小苏打不稳定,可分解生成二氧化碳气体,可用于制作馒头和面包,故D正确.
故选B.点评:
本题考点: 钠的重要化合物;硅和二氧化硅.
考点点评: 本题考查较为综合,侧重于化学与生活的考查,有利于培养学生良好的科学素养,提高学习的积极性,难度不大,注意相关基础知识的积累.1年前查看全部
- 在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验用品。用下图中的实验装置进行实验,证明过氧化钠可作
在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验用品。用下图中的实验装置进行实验,证明过氧化钠可作供氧剂。 
(1)A是制取CO 2 的装置。写出A中发生反应的化学方程式:____________________。
(2)填写表中空格
(3)写出过氧化钠与二氧化碳反应的化学方程式:____________________。
(4)试管F中收集满气体后,下一步实验操作是:____________________。 bpine1年前1
bpine1年前1 -
 wllbb 共回答了26个问题
wllbb 共回答了26个问题 |采纳率84.6%1年前查看全部
- 过氧化钠与二氧化碳的反应为什么可以在呼吸面具作供氧剂
 西域亡魂1年前3
西域亡魂1年前3 -
 风已失 共回答了24个问题
风已失 共回答了24个问题 |采纳率83.3%生成了氧气啊
2Na2O2+2CO2=2Na2CO3+O21年前查看全部
- (2010•清远)过氧化钠(Na2O2)因为能与水、CO2等反应产生氧气而作为供氧剂.现将39克Na2O2投入到足量的水
(2010•清远)过氧化钠(Na2O2)因为能与水、CO2等反应产生氧气而作为供氧剂.现将39克Na2O2投入到足量的水中,发生如下反应:
2Na2O2+2H2O═4NaOH+O2↑
(1)请计算生成NaOH和O2的质量.
(2)若反应开始时水的质量为69克,求反应后所得溶液的溶质的质量分数. 一个人想像1年前1
一个人想像1年前1 -
 haohaotong 共回答了17个问题
haohaotong 共回答了17个问题 |采纳率94.1%解题思路:(1)根据反应的化学方程式,由Na2O2的质量可以求出生成的NaOH和O2的质量;
(2)根据溶质质量分数的计算公式可以求出反应后所得溶液的溶质的质量分数;设生成NaOH的质量为x,生成O2的质量为y
2Na2O2+2H2O═4NaOH+O2↑
156 16032
39g x y
[156/160]=[39g/x] 解得:x=40g
[156/32]=[39g/y] 解得:y=8g
据题意:溶液质量为:69g+39g-8g=100g,溶液中溶质的质量分数:[40g/100g]×100%=40%
答:(1)生成NaOH的质量为40g,生成O2的质量为8g;
(2)反应后所得溶液的溶质的质量分数 40%.点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 根据反应的化学方程式进行计算时,所使用的物质的质量必须为完全反应的物质的质量,未参加反应的物质质量不能代入化学方程式进行计算.1年前查看全部
- 如图所示装置,有洗气、储气等用途.医院给病人输氧气时,也利用了类似的装置.以下说法不正确的是( ) A.B导管连接供氧
如图所示装置,有洗气、储气等用途.医院给病人输氧气时,也利用了类似的装置.以下说法不正确的是( ) A.B导管连接供氧钢瓶 B.B导管连接病人吸氧导气管 C.该装置可用来观察是否有氧气输出 D.该装置可用来观察输出氧气的速度 
 清风剑客1年前1
清风剑客1年前1 -
 apple_pie 共回答了19个问题
apple_pie 共回答了19个问题 |采纳率94.7%这个地方水的作用有二:一是便于观察流速,二是增加氧气的湿度(先前为液态的,转化为气态时干燥而冷,所以要加湿).
A、B导管连接供氧钢瓶,则A端为气体输出端,这样会首先把水排出,显然这种做法是错误的.故A错.
B、A导管为气体流入端,使氧气从B端流出,连接病人吸氧导气管.故B正确.
C、气体从A流入,会产生气泡从而判断有无气体.故C正确.
D、因进气管通入到了蒸馏水中,气泡越明显,气体的流入速度就越快,因此,可判断输出氧气的速度,D正确.
故答案选A.1年前查看全部
- (2013•安顺)潜水员使用的供氧装置是用过氧化钠(Na2O2)和呼出的CO2反应来制取氧气提供呼吸.某实验小组为验证这
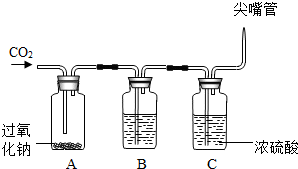 (2013•安顺)潜水员使用的供氧装置是用过氧化钠(Na2O2)和呼出的CO2反应来制取氧气提供呼吸.某实验小组为验证这一原理,进行了实验探究.
(2013•安顺)潜水员使用的供氧装置是用过氧化钠(Na2O2)和呼出的CO2反应来制取氧气提供呼吸.某实验小组为验证这一原理,进行了实验探究.
【查阅资料】在常温常压下过氧化钠是淡黄色固体,在不需要加热的情况下能和二氧化碳反应生成碳酸钠和氧气.
【设计装置】实验小组设计了如图所示的装置进行实验探究,B装置中盛装NaOH溶液.
【实验过程】向装置A中通入足量CO2气体,观察到A瓶中的淡黄色固体逐渐变为白色粉末,同时见到B、C装置中有气泡出现.
【实验分析】
(1)为验证过氧化钠和二氧化碳反应生成氧气,实验小组采用的验证方法是用一根带火星的木条______;
(2)装置C中浓硫酸的作用是______,这是根据浓硫酸具有______的原理;
(3)写出过氧化钠和二氧化碳反应的化学方程式:______;
【实验结论】
(4)实验证明:Na2O2和CO2在不需要加热的情况下反应可得到氧气.通过探究同学们认为:在实验室不用加热的方法,用气体也可制得氧气.按你在实验室制取氧气的经验,你采用的方法是:2H2O2
2H2O+O2↑MnO2 .2H2O2(用一个化学方程式表示).
2H2O+O2↑MnO2 . 1653492141年前1
1653492141年前1 -
 chrislo328 共回答了15个问题
chrislo328 共回答了15个问题 |采纳率93.3%解题思路:(1)氧气具有助燃性,可以使带火星的木条复燃,可以据此解答该题;
(2)浓硫酸具有吸水性,可以用作一些气体的干燥剂,可以据此解答;
(3)过氧化钠和二氧化碳反应生成碳酸钠和氧气,可以据此写出该反应的化学方程式;
(4)过氧化氢溶液在二氧化锰的催化作用之下能够快速的分解产生氧气,可以据此解答.(1)氧气具有助燃性,可以使带火星的木条复燃,所以为验证过氧化钠和二氧化碳反应生成氧气,将一根带火星的木条放在尖嘴管口,若发现木条复燃,则说明反应生成了氧气;
(2)浓硫酸具有吸水性,可以用作一些气体的干燥剂,所以C中浓硫酸的作用是干燥氧气;
(3)过氧化钠和二氧化碳反应生成碳酸钠和氧气,该反应的化学方程式为:2Na2O2+2CO2═2Na2CO3+O2;
(4)过氧化氢溶液在二氧化锰的催化作用之下能够快速的分解产生氧气,该反应的化学方程式为:2H2O2
MnO2
.
2H2O+O2↑.
故答案为:(1)放在尖嘴管口,若发现木条复燃,则说明反应生成了氧气;
(2)干燥氧气;吸水性,;
(3)2Na2O2+2CO2═2Na2CO3+O2;
(4)2H2O2
MnO2
.
2H2O+O2↑.点评:
本题考点: 制取气体的反应原理的探究;气体的干燥(除水);氧气的检验和验满;书写化学方程式、文字表达式、电离方程式.
考点点评: 选用干燥剂应根据气体的性质和干燥剂的性质而定,其原则是干燥剂只能吸收气体中的水分,而不能与气体发生反应.1年前查看全部
- 下列说法不正确的是( )A.Na2O2能与CO2反应,可用作呼吸面具的供氧剂B.Al2O3熔点高,可用于制作耐高温仪器
下列说法不正确的是( )
A.Na2O2能与CO2反应,可用作呼吸面具的供氧剂
B.Al2O3熔点高,可用于制作耐高温仪器
C.明矾能水解生成Al(OH)3胶体,可用作净水剂
D.SiO2有导电性,可用于制备光导纤维 小小小小布丁1年前1
小小小小布丁1年前1 -
 drib 共回答了20个问题
drib 共回答了20个问题 |采纳率90%解题思路:A.Na2O2能与CO2反应生成氧气;
B.制作耐高温仪器所用材料熔点高;
C.明矾含有铝,易水解生成氢氧化铝胶体;
D.SiO2不具有导电性.A.Na2O2能与CO2反应生成氧气,常用于供氧剂,故A正确;
B.Al2O3熔点高,硬度大,可用于制作耐高温仪器,故B正确;
C.明矾含有铝,易水解生成氢氧化铝胶体,具有吸附性,可用于净水,故C正确;
D.SiO2不具有导电性,故D错误;
故选D.点评:
本题考点: 钠的重要化合物;盐类水解的应用;硅和二氧化硅;镁、铝的重要化合物.
考点点评: 本题考查物质的性质与用途,侧重于化学与生活的考查,有利于培养学生的良好的科学素养,提高学生学习的积极性,难度不大,注意相关基础知识的积累.1年前查看全部
- 青藏铁路是世界上海拔最高的铁路,于2006年7月建成通车.青藏线上运行的旅客列车实行全封闭,有列车供氧供暖,其原因有哪些
青藏铁路是世界上海拔最高的铁路,于2006年7月建成通车.青藏线上运行的旅客列车实行全封闭,有列车供氧供暖,其原因有哪些?
 wlc198332451年前1
wlc198332451年前1 -
 huangzhaoming0 共回答了24个问题
huangzhaoming0 共回答了24个问题 |采纳率91.7%主要原因是缺氧1年前查看全部
- 一道简单的生物题判断题将酵母菌由供氧条件转变为厌氧条件培养,葡萄糖的利用加快,丙酮酸的氧化加快 ( )理由?
 alive881年前3
alive881年前3 -
 hawkeyeszy 共回答了26个问题
hawkeyeszy 共回答了26个问题 |采纳率92.3%对的~~~~无氧条件下,进行糖酵解反应,有葡萄糖生成丙酮酸,丙酮酸的氧化加快 是因为进一生成乳酸,1年前查看全部
- 蜡烛加氧气 是氧气供氧的氧化反应 还是缓慢氧化?
 梦回凤阙1年前2
梦回凤阙1年前2 -
 残阳卧雪 共回答了24个问题
残阳卧雪 共回答了24个问题 |采纳率91.7%是氧气供氧的氧化反应1年前查看全部
- 超氧化钾(ko2)和二氧化碳反应生成氧气.在医院矿井潜水高空飞行中作供氧剂.13.2L(标准状况)CO2和KO2反应后,
超氧化钾(ko2)和二氧化碳反应生成氧气.在医院矿井潜水高空飞行中作供氧剂.13.2L(标准状况)CO2和KO2反应后,气体体积变为18.8L,计算反映消耗的KO2质量
补充:方程式4KO2+2CO2=2K2CO3+302 拥抱自然1年前2
拥抱自然1年前2 -
 奇娅 共回答了18个问题
奇娅 共回答了18个问题 |采纳率88.9%反应后气体体积增加18.8-13.2=5.6升
设气体增加5.6升需KO2 X克
4KO2+2CO2=2K2CO3+302
284-----------体积增加22.4升
X-------------------5.6
X=71克
反映消耗的KO2质量=71克1年前查看全部
- 某淡黄色粉末常用作潜水员的供氧剂,在供氧反应中,被氧化和被还原的物质的质量比为?答案好像1比1,为什
某淡黄色粉末常用作潜水员的供氧剂,在供氧反应中,被氧化和被还原的物质的质量比为?答案好像1比1,为什
可不可以讲解下 渡口等船1年前3
渡口等船1年前3 -
 浪漫左右 共回答了21个问题
浪漫左右 共回答了21个问题 |采纳率90.5%黄色粉末为过氧化钠,其中1个氧被氧化,另一个被还原,属典型歧化反应,答案1:1 .
过氧化钠中两个氧化合价均为-1,和潜水员呼出的二氧化碳反应后生成碳酸钠和氧气,即一个氧从-1变为0价,另一个变为-2价!1年前查看全部
- 过氧化钙(CaO2)用于鱼池供氧剂,同时有熟石灰生成. ①写出过氧化钙与水反应的化学方程式
过氧化钙(CaO2)用于鱼池供氧剂,同时有熟石灰生成. ①写出过氧化钙与水反应的化学方程式
过氧化钙(CaO2)用于鱼池供氧剂,同时有熟石灰生成.
①写出过氧化钙与水反应的化学方程式
2CaO2+2H2O=2Ca(OH)2+O2↑
②现将7.2g过氧化钙放入36.0g水中,使之充分反应,所得混合物中氧元素的质量是多少?
求第二问啊 我爱迪士尼1年前1
我爱迪士尼1年前1 -
 庸俗 共回答了19个问题
庸俗 共回答了19个问题 |采纳率100%由方程式可看成氧气是由过氧化钙产生的,水中氧气含量不变
水中氧气含量:36/18*16=32g
过氧化钙产生的氧气量=过氧化钙留在水里的氧气量:7.2/(72*2)*32=16g
溶液中总的氧气量:32+16=48g1年前查看全部
- 金鱼有听觉吗?我同屋的一个呆子每天24小时给4条金鱼供氧,我看在眼里笑在心里—这哪是养鱼,简直在“煮鱼”——气泡把几条可
金鱼有听觉吗?
我同屋的一个呆子每天24小时给4条金鱼供氧,我看在眼里笑在心里—这哪是养鱼,简直在“煮鱼”——气泡把几条可怜的鱼儿团团围住.原来还是6条,它们最后都会被. _ture1ove_1年前1
_ture1ove_1年前1 -
 没事逛着玩 共回答了16个问题
没事逛着玩 共回答了16个问题 |采纳率81.3%有很长时间人们认为鱼什么都听不见,因鱼不长外耳,从外面看鱼好像没有耳朵.但是鱼确实有耳朵,且多数鱼听力甚好.
人类耳朵里有鼓膜,声音进入耳朵使鼓膜振动,这种振动传到耳朵内的听觉部分,就能听见声音了.
声音在水中传播要比在空气中容易得多.鱼的体内有大量的水,声音直接穿过鱼的身体,到达耳朵,因为鱼没有鼓膜,事实上多数鱼的耳朵根本不与外界相通,而是被保护在头两侧的囊中,囊就在眼睛后面.
许多种鱼能用另一种方式收集声音.它们的耳朵与鳔相连,水中的声音使鳔壁振动,就像声音穿过空气使鼓膜振动一样.然后这种振动通常沿着与鳔相连的一串小骨头传到耳朵里.有些鱼不是靠小骨头传送振动,而是靠从鳔延伸出的管状器官.
声音对鱼很重要.许多鱼能彼此发出有力的叫声,几公里以外都能听见.有些鱼通过磨牙发声,另一些鱼在身上磨擦鳍发声.许多鱼用鳔发声辨声.特殊的可敲击肌肉振动鳔发出声音.1年前查看全部
- 已知 2Na2O2+2CO2=2Na2CO3+O2,因此Na2O2可在呼吸面具和潜水艇里作供氧剂.
已知 2Na2O2+2CO2=2Na2CO3+O2,因此Na2O2可在呼吸面具和潜水艇里作供氧剂.
(1)请在答卷上用双线桥法标出上述方程式的电子转移方向和数目______.
(2)______是还原剂,______是还原产物.
(3)若转移3mol电子,则所产生的氧气在标准状况下的体积为______. meilaiyou1年前0
meilaiyou1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 为什么Na2O2能做供氧剂
 星空4111年前3
星空4111年前3 -
 ewoq_k 共回答了24个问题
ewoq_k 共回答了24个问题 |采纳率87.5%那供养瓶来说~当人呼出的是二氧化碳~二氧化碳与氧气瓶中过氧化钠结合生成氢氧化钠和氧气!人呼吸需要氧气!就这么简单!
方程式:2Na2O2+2H2O=4NaOH+O21年前查看全部
- 某瓶氧气的密度是5kg/m3,给人供氧用去了氧气质量的一半,则瓶内剩余氧气的密度是______kg/m3.伊利牌盒装牛奶
某瓶氧气的密度是5kg/m3,给人供氧用去了氧气质量的一半,则瓶内剩余氧气的密度是______kg/m3.伊利牌盒装牛奶的体积是2.5×10-4m3,若测得该盒牛奶的质量是0.3kg,则该牛奶的密度为______ kg/m3.喝掉一半后,牛奶的密度将______ (选填“变大”“变小”或“不变”)
 全宇宙最帅的男人1年前1
全宇宙最帅的男人1年前1 -
 zcfboss 共回答了16个问题
zcfboss 共回答了16个问题 |采纳率81.3%解题思路:(1)氧气用掉一半,质量减半,氧气还充满整个氧气瓶,体积保持不变,根据密度公式判断密度的变化.
(2)已知牛奶的体积和质量,根据密度公式求出该牛奶的密度;密度是物质的一种特性,与物质的质量和体积无关.(1)一瓶氧气的密度为5kg/m3,给人供氧用去了氧气质量的一半,但体积保持不变,
根据ρ=[m/V]可知,剩余氧气的密度变为原来的一半,即ρ′=2.5kg/m3.
(2)装牛奶的密度:
ρ=[m/V]=
0.3kg
2.5×10−4m3=1.2×103kg/m3,
∵密度与物质的体积和质量无关,
∴喝掉一半时,牛奶的密度不变.
故答案为:2.5;1.2×103;不变.点评:
本题考点: 密度的计算;密度及其特性.
考点点评: 本题考查了密度的计算和学生对密度特性的理解与掌握,关键是知道氧气瓶的容积不变即所装氧气的体积不变.1年前查看全部
大家在问
- 1矢量与三角形在三角形ABC中,已知矢量AB与AC满足{(AB/|AB|)+(AC/|AC|)}*BC=0,三角形ABC是
- 2中国重返联合国的主要原因是什么?
- 3(2011•和平区模拟)下化学方程式符合题意且书写正确的是( )
- 4爷爷买来一只锅,直径是45厘米,爷爷想做一个木锅盖,半径比锅盖多0.5厘米,锅盖的面积是多少?
- 5再加减法算式中,被减数,减数与差的和是16.8,差与减数的比是3比4.差是( ),减数是( )
- 6路基横断面里的坡,比如是3:1,那么这个3和1各是什么意思?怎么算路基中线到坡脚线的距离?
- 7【税务问题】甲企业(增值税一般纳税人)为某市一家酒厂,生产各种酒类产品.
- 8若方程3X的3+2N次方-1=0是关于X的一元一次方程则N=多少
- 9地球母亲的保护措施倡议书
- 10烦恼用英语怎么说
- 11绳子把密度为500KG每立方,体积为0.06立方米;的木块挂起来,则绳子对木块的拉力是多少?
- 12你正要去哪儿和你打算去哪儿英语怎么说
- 13急呀....三个英语问题1.The museum is two kilometres________.A.wide B.
- 14序数词的缩略形式有什么规律
- 15如图是一个几何体的三视图,其中正视图与左视图都是全等的腰为3的等腰三角形,俯视图是边长为2的正方形,


