制氧厂采用分离空气的方法制取大量的工业和医疗用氧.医用氧气瓶大瓶通常为四十升容积规格,装满时可装...
 尺语2022-10-04 11:39:541条回答
尺语2022-10-04 11:39:541条回答制氧厂采用分离空气的方法制取大量的工业和医疗用氧.医用氧气瓶大瓶通常为四十升容积规格,装满时可装压缩氧气一百千克.标准状况下氧气的密度约为1.43克每升,若制得这样一瓶医用氧气,需分离标准状况下的空气多少立方米?

已提交,审核后显示!提交回复
共1条回复
 134adf 共回答了13个问题
134adf 共回答了13个问题 |采纳率92.3%- V(O2) = 100Kg / 1.43g/L = 69930.1L
因为氧气空气体积的21%,所以V(空气) = 69930.1L / 21% = 333000.3 L = 333m3
答:…………………………………………………… - 1年前
相关推荐
- 初三化学制氧方程式我只要制氧的方程式会的+271578213M我 谢谢 (3)个制氧的方程
 ouyangzui1年前1
ouyangzui1年前1 -
 拖鞋过河 共回答了19个问题
拖鞋过河 共回答了19个问题 |采纳率78.9%2KMnO4〓▲K2MnO4+MnO2+O2↑(▲是加热符) 再给你几个制氧气的方程式吧.2H2O2〓2H2O+O2↑ (要加MnO2做催化剂) 2KClO3〓▲2KCl+3O2↑ (也要加MnO2做催化剂) 氧气的工业制法:工业上主要用分离液态空气的方法来制氧气,过程可简单表示为:空气→(加压降温)液态空气→(蒸发分离)氮气、液氧(因为氧气的凝固点高,氮气先汽化)1年前查看全部
- 用高锰酸钾和氯化钾制氧,哪个的制氧速度快
用高锰酸钾和氯化钾制氧,哪个的制氧速度快
氯酸钾加热不加催化剂,高锰酸钾加热 shenghcai1年前1
shenghcai1年前1 -
 酗烟的鬼 共回答了16个问题
酗烟的鬼 共回答了16个问题 |采纳率87.5%氯化钾制不了氧气,氯酸钾可以,如果不加二氧化锰做催化剂的话,氯酸钾需要的时间长.
【高锰酸钾加热制取氧气比氯酸钾加热不加催化剂制取氧气快!】1年前查看全部
- 制氧实验中,怎样做才能不浪费氯酸钾?
 fangzq1年前1
fangzq1年前1 -
 黄爱东西 共回答了12个问题
黄爱东西 共回答了12个问题 |采纳率75%1.加入一些高锰酸钾.高锰酸钾受热可以生成氧气和二氧化锰,二氧化锰是氯酸钾反应生成氧气的催化剂.
2.用双氧水制氧是实验室制氧的最好方法.1年前查看全部
- 在潜水艇中普通使用的制氧剂是一种呈黄色的固体氧化物,它能与二氧化碳反应产生氧气,供人们呼吸之用.
在潜水艇中普通使用的制氧剂是一种呈黄色的固体氧化物,它能与二氧化碳反应产生氧气,供人们呼吸之用.
它的化学式为RO2,其中含氧量为45。1%,求R的相对原子质量及RO2的化学式 一新1年前2
一新1年前2 -
 橼枷 共回答了23个问题
橼枷 共回答了23个问题 |采纳率91.3%拿32/0.451=71,相对原子质量(R)=71-32=39,为KO21年前查看全部
- 高中化学题过氧化钠是一种淡黄色固体,它能与二氧化碳反应生成氧气,在潜水艇中用作制氧剂,供人类呼吸之用。某学生为了验证这一
高中化学题
过氧化钠是一种淡黄色固体,它能与二氧化碳反应生成氧气,在潜水艇中用作制氧剂,供人类呼吸之用。某学生为了验证这一实验,以足量的大理石、足量的盐酸和过氧化钠样品为原料,制取O2,设计出如下实验装置

(1)A中制取CO2 的装置,应从下列图①、②、③中选哪个图:?并说明理由!!

我卷子上的答案给的是图3
但网上貌似都是2呵
 小伊ai猪猪1年前3
小伊ai猪猪1年前3 -
 太阳底下无新事 共回答了20个问题
太阳底下无新事 共回答了20个问题 |采纳率85%3中能放隔板,利于控制反应速率1年前查看全部
- 根据下列实验装置图回答问题: (1)请填写标号仪器的名称:a.______,b.______;(2)实验室利用装置B制氧
根据下列实验装置图回答问题: 
(1)请填写标号仪器的名称:a.______,b.______;
(2)实验室利用装置B制氧气时,长颈漏斗的下端要插入液面以下,其目的是:______;
(3)实验室用氯酸钾和二氧化锰的混合物制氧气,发生反应的符号表达式为______;
(4)已知颗粒状的锌和液态稀硫酸在常温下反应可制得氢气,可选择的制取装置是______;(填序号)如果用如图2装置来收集氢气,氢气应从______端进入(填“①”或“②”). 不叫甜甜1年前1
不叫甜甜1年前1 -
 lpzy7 共回答了20个问题
lpzy7 共回答了20个问题 |采纳率85%(1)锥形瓶是常用的反应容器,水槽是盛水的仪器,故答案为:锥形瓶;水槽
(2)长颈漏斗的下端要插入液面以下,其目的是:防止气体从长颈漏斗逸出,故答案为:防止气体从长颈漏斗逸出
(3)氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,故答案为:2KClO 3
Mn O 2
.
△ 2KCl+3O 2 ↑
(4)实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集.如果用如图2装置来收集氢气,氢气应从②进入,因为氢气的密度比水的密度小;故答案为:BD或BE;②1年前查看全部
- 在化学实验室常用KMnO4制氧器某905班做完实验后,老师发现有8支试管破了,破了的原因有 1’2‘3’
 zhangqing8407191年前1
zhangqing8407191年前1 -
 yufanfang 共回答了17个问题
yufanfang 共回答了17个问题 |采纳率94.1%1加热药品时没有预热
2试管外壁有水珠
3试管触及焰芯
4加热固体药品试管口没向下倾斜1年前查看全部
- 为长时间潜航,在潜水艇中配备氧气发生装置,其制氧方法是利用过氧化钠Na2o2与二氧化碳在常温下生成碳酸钠和氧气而制得其反
为长时间潜航,在潜水艇中配备氧气发生装置,其制氧方法是利用过氧化钠Na2o2与二氧化碳在常温下生成碳酸钠和氧气而制得其反应的化学方程式为2Na2o2+2Co2==2Na2co3+o2
若得到48g氧气,需过氧化钠的质量是多少?
Na-23 o-16 lobster20031年前1
lobster20031年前1 -
 KINGFJBOB 共回答了16个问题
KINGFJBOB 共回答了16个问题 |采纳率75%设需过氧化钠的质量为x
2Na2o2+2Co2==2Na2co3+o2
156 32
x 48g
解得x=234g1年前查看全部
- (2011•嘉兴)如图所示,有人制作了一个家庭制氧装置.该制氧装置由2个饮料瓶、2根软管和药剂构成,整套装置成本不到3块
 (2011•嘉兴)如图所示,有人制作了一个家庭制氧装置.该制氧装置由2个饮料瓶、2根软管和药剂构成,整套装置成本不到3块钱.药剂包括过氧碳酸钠(2Na2CO3•3H2O2)和二氧化锰.制氧时,先在两个饮料瓶中加入适量的水,再往甲瓶中加入药剂,产生的气体通过B管从乙瓶导出,即可供人吸氧.
(2011•嘉兴)如图所示,有人制作了一个家庭制氧装置.该制氧装置由2个饮料瓶、2根软管和药剂构成,整套装置成本不到3块钱.药剂包括过氧碳酸钠(2Na2CO3•3H2O2)和二氧化锰.制氧时,先在两个饮料瓶中加入适量的水,再往甲瓶中加入药剂,产生的气体通过B管从乙瓶导出,即可供人吸氧.
(1)为了顺利地导出甲瓶中产生的氧气,A软管在甲瓶中应不伸入液面不伸入液面.
(选填“不伸入液面”或“伸入液面”)
(2)药剂加入水中后会发生以下两个反应:
2Na2CO3•3H2O2=2Na2CO3+3H2O2;2H2O2
2H2O+O2↑MnO2 .
从化学反应的基本类型来看,它们都属于分解分解反应.
(3)已知总质量为110克的药剂可产生34克过氧化氢,则这包药剂完全反应会生成多少克氧气? 丹姐1年前1
丹姐1年前1 -
 无声1314 共回答了21个问题
无声1314 共回答了21个问题 |采纳率81%(1)如果A软管在甲瓶中深入液面以下,就无法导出气体.为了顺利地导出甲瓶中产生的氧气,A软管在甲瓶中应不伸人液面.故答案为:不伸人液面;
(2)根据化学反应式可知,这两种反应式都是由一种物质生成其他两种其他物质的分解反应.故答案为:分解;
(3)设可生成氧气质量为m
2H2O2
MnO2
.
2H2O+O2↑
68 32
34g m
68
34g=
32
m
m=16g
答:可生成氧气质量为16g.1年前查看全部
- 过氧化钠(Na 2 O 2 )是潜水艇氧气再生装置中制氧剂,它是一种淡黄色粉末,能与二氧化碳反应生成氧气,反应的化学方程
过氧化钠(Na 2 O 2 )是潜水艇氧气再生装置中制氧剂,它是一种淡黄色粉末,能与二氧化碳反应生成氧气,反应的化学方程式是  ,则Na 2 O 2 中氧元素的化合价为__________,X的化学式为__________,反应后固体粉末变为_________色。
,则Na 2 O 2 中氧元素的化合价为__________,X的化学式为__________,反应后固体粉末变为_________色。 芳草57551年前1
芳草57551年前1 -
 mxe66 共回答了17个问题
mxe66 共回答了17个问题 |采纳率82.4%-1 价,Na 2 CO 3 ,白1年前查看全部
- 实验室制氧原理的化学方程式
 快乐网事_dy1年前3
快乐网事_dy1年前3 -
 我爱依然 共回答了15个问题
我爱依然 共回答了15个问题 |采纳率100%.加热高锰酸钾,化学式为:2KMnO4===(△)K2MnO4+MnO2+O2↑
2.用催化剂MnO2并加热氯酸钾,化学式为:2KClO3===(△,MnO2) 2KCl+3O2↑
3.双氧水(过氧化氢)在催化剂MnO2(或红砖粉末,土豆,水泥,铁锈等)中,生成O2和H2O,化学式为: 2H2O2===(MnO2) 2H2O+O2↑1年前查看全部
- 过氧化钠是一种淡黄色固体,在潜水艇中用作制氧剂,供人类呼吸之用.某学生为了验证这一实验,以足量的大理石、足量的盐酸和1.
过氧化钠是一种淡黄色固体,在潜水艇中用作制氧剂,供人类呼吸之用.某学生为了验证这一实验,以足量的大理石、足量的盐酸和1.95g过氧化钠样品为原料,制取O2,设计出如下实验装置:

(1)请写出过氧化钠与二氧化碳反应的化学方程式,并标明电子转移的方向和数目:______;
(2)A中制取CO2的装置,应从下列图①、②、③中选哪个图:______;
(3)B装置的作用是______;
(4)为了检验E中收集到的气体,在取出集气瓶后,用______的木条伸入集气瓶内,木条会出现______;
(5)若E中石灰水出现轻微白色浑浊,请说明原因:______;
(6)当D中的1.95g过氧化钠样品接近反应完毕时,你预测E装置内有何现象?______;
(7)反应完毕时,若测得E中的集气瓶收集到的气体为250mL,又知氧气的密度为1.43g/L,当装置的气密性良好的情况下,实际收集到的氧气体积比理论计算值______(大或小),相差约______mL(取整数值,所用数据均在标准状况下测定),这是由于______. hello_boboan1年前1
hello_boboan1年前1 -
 温柔一瓢 共回答了16个问题
温柔一瓢 共回答了16个问题 |采纳率100%解题思路:(1)过氧化钠和二氧化碳反应生成碳酸钠和氧气,注意该反应中过氧化钠既是氧化剂又是还原剂.
(2)根据反应物的状态及反应条件选取反应装置.
(3)根据二氧化碳中的杂质气体判断碳酸氢钠的作用.
(4)使带火星的木条复燃的气体是氧气.
(5)二氧化碳和澄清石灰水反应生成碳酸钙白色沉淀.
(6)根据装置内气体的压强判断现象.
(7)根据过氧化钠的质量可以生成氧气的体积,理论生成气体的体积-实际氧气的体积=差值.(1)过氧化钠和二氧化碳反应生成碳酸钠和氧气,

故答案为:
(2)该反应的药品是固体和液体,且不需加热,所以所需装置为固液混合不加热型,故选②.
(3)大理石和盐酸的反应是放热反应,盐酸具有挥发性,所以制取的二氧化碳中含有氯化氢气体,氯化氢和碳酸氢钠能反应生成二氧化碳,二氧化碳和碳酸氢钠不反应,所以B装置的作用是除二氧化碳中的氯化氢.
故答案为:除CO2中的HCl.
(4)过氧化钠和二氧化碳反应生成氧气,氧气能使带火星的木条复燃.
故答案为:故带火星;复燃.
(5)二氧化碳能使澄清的石灰水变浑浊,若E中石灰水出现轻微白色浑浊,说明未反应的二氧化碳与石灰水反应所致.
故答案为:未反应的二氧化碳与石灰水反应所致.
(6)当D中的1.95g过氧化钠样品接近反应完毕时,由于生成氧气的量减少,压强变小,所以E中可能会因二氧化碳与石灰水反应而倒吸.
故答案为:由于生成氧气的量减少,E中可能会因二氧化碳与石灰水反应而倒吸.
(7)1.95g过氧化钠完全反应生成氧气的体积为v.
2Na2O2----O2;
2mol22.4L
[1.95g/78g/mol] v
v=0.28L=280mL>250mL,所以实际收集到的氧气体积比理论计算值小.
280mL-250mL=30mL;
原因是Na2O2可能含有其它杂质;D装置可能有氧气未被排出.
故答案为:小;30;Na2O2可能含有其它杂质;D装置可能有氧气未被排出.点评:
本题考点: 碱金属及其化合物的性质实验;性质实验方案的设计.
考点点评: 本题考查了钠及其化合物的性质,难度不大,注意过氧化钠和二氧化碳反应中过氧化钠既是氧化剂又是还原剂.1年前查看全部
- 化学制氧实验 哪个装置易漏气
 我也是海角1年前3
我也是海角1年前3 -
 sk112 共回答了12个问题
sk112 共回答了12个问题 |采纳率100%额.其实这个没有太明确的,如果说最容易漏气的话,应该是过氧化氢溶液和二氧化锰的那个吧.因为一般这个反应是把过氧化氢滴入盛有二氧化锰的锥形瓶中,用的主要是分液漏斗或者是长颈漏斗.如果长颈漏斗没有形成液封或者是...1年前查看全部
- H2O2制氧化学表达式像这样:通电 H2 O〓〓H2↑+O2↑
 dyname_19821年前10
dyname_19821年前10 -
 RIKICHEN110 共回答了20个问题
RIKICHEN110 共回答了20个问题 |采纳率95%-----MnO2(cui)
2H2O2===2H2O+O2↑1年前查看全部
- 过氧化钠是一种淡黄色固体,它能与二氧化碳反应生成氧气,在潜水艇中用作制氧剂,供人类呼吸之用.它与二氧化碳反应的化学方程式
过氧化钠是一种淡黄色固体,它能与二氧化碳反应生成氧气,在潜水艇中用作制氧剂,供人类呼吸之用.它与二氧化碳反应的化学方程式为:2Na2O2+2CO2═2Na2CO3+O2.某学生为了验证这一实验,以足量的大理石、足量的盐酸和1.95g过氧化钠样品为原料,制取O2,设计出如下实验装置:

(1)A中制取CO2的装置,应从下列图①、②、③中选哪个图:______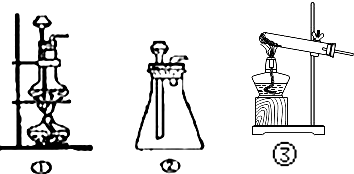
B装置的作用是______,C装置内可能出现的现象是______.为了检验E中收集到的气体,在取出集气瓶后,方法是______.
(2)若E中的石灰水出现出现轻微白色浑浊,请说明原因:______.
(3)若D中的1.95g过氧化钠样品接近反应完毕时,你预测E装置内有何现象?______.
(4)反应完毕时,若测得E中的集气瓶收集到的气体为250mL,又知氧气的密度为1.43g/L,当装置的气密性良好的情况下,实际收集到的氧气体积比理论计算值______(答大或小),相差约______mL(取整数值,所用数据均在标准状况下测定),这是由于______. 别吐o可惜1年前1
别吐o可惜1年前1 -
 松松宝贝 共回答了11个问题
松松宝贝 共回答了11个问题 |采纳率90.9%解题思路:(1)实验室用碳酸钙和稀盐酸反应制备二氧化碳,反应无需加热,且反应需要较多二氧化碳,应用②装置制备;实验中要依次进行除杂、干燥收集等操作;
(2)二氧化碳和澄清石灰水反应生成碳酸钙白色沉淀;
(3)如过氧化钠完全反应,则E中产生大量沉淀,且产生倒吸;
(4)根据过氧化钠的质量可以生成氧气的体积,理论生成气体的体积-实际氧气的体积=差值;(1)该反应的药品是固体和液体,且不需加热,所以所需装置为固液混合不加热型,所以排除①;③中只能制取少量二氧化碳而不能制取大量二氧化碳,所以排除③,故选②;
大理石和盐酸的反应是放热反应,盐酸具有挥发性,所以制取的二氧化碳中含有氯化氢气体、水蒸气,氯化氢和碳酸氢钠能反应生成二氧化碳,所以B装置的作用是吸收A装置中产生的盐酸酸雾,除去HCl气体;
二氧化碳和碳酸氢钠不反应,水蒸气能使无水硫酸铜由白色变蓝色,所以C装置内可能出现的现象是白色固体变蓝色;
过氧化钠和二氧化碳反应生成氧气,氧气能使带火星的木条复燃,检验时,可用带火星的木条放在管口,木条复燃说明收集到的气体为氧气,
故答案为:②;吸收A装置中产生的盐酸酸雾;白色固体变蓝色;用带火星的木条放在管口,木条复燃说明收集到的气体为氧气;
(2)二氧化碳能使澄清的石灰水变浑浊,若E中石灰水出现轻微白色浑浊,说明未反应的二氧化碳与石灰水反应,D中有部分未反应的二氧化碳与E中石灰水反应生成沉淀所致;
故答案为:D中有部分未反应的二氧化碳与E中石灰水反应生成沉淀所致;
(3)当D中的1.95g过氧化钠样品接近反应完毕时,E中石灰水的不是浑浊明显增加,瓶内液面接近停止,由于生成氧气的量减少,压强变小,所以E中可能会因二氧化碳与石灰水反应而倒吸.
故答案为:E中石灰水的白色浑浊明显增加,瓶内液面接近停止,由于生成氧气的量减少,E中可能会因二氧化碳与石灰水反应而倒吸;
(4)1.95g过氧化钠完全反应生成氧气的体积为v.
2Na2O2----O2;
2mol 22.4L
[1.95g/78g/mol] V
V=0.28L=280mL>250mL,所以实际收集到的氧气体积比理论计算值小.
280mL-250mL=30mL;
原因是Na2O2可能含有与二氧化碳不反应的其它杂质;D装置可能有氧气未被排出.
故答案为:小;30;Na2O2可能含有不与二氧化碳反应的其它杂质,D装置可能有氧气未被排出.点评:
本题考点: 碱金属及其化合物的性质实验.
考点点评: 本题以钠的化合物为载体综合考查学生的分析能力和实验能力,为高频考点,注意把握实验的原理和注意事项,结合物质的性质把握实验,难度中等.1年前查看全部
- 做制氧实验时,导管口开始有气泡放出时,不宜立即收集,原因是什么
 herbguo10061年前1
herbguo10061年前1 -
 不扑猫 共回答了19个问题
不扑猫 共回答了19个问题 |采纳率84.2%刚排出来的是空气,不是氧气,如果收集的话会影响氧气纯度,就有可能使后面的实验失败.应等气泡连续且均匀的时候再收集,那是就是氧气了.1年前查看全部
- 工业制氧的原理及方法
 xiuloveleehom1年前1
xiuloveleehom1年前1 -
 月未漾 共回答了14个问题
月未漾 共回答了14个问题 |采纳率92.9%工业用分离空气法制氧,是个物理变化,利用氮气沸点低于氧气.
在低温条件下加压,使空气转变为液态,然后蒸发.由于氮的沸点是-196℃,比液态氧(-183℃)低,因此氮气首先从液态空气中蒸发出来,剩下的主要就是液态氧了.1年前查看全部
- (2014•武汉)某化学兴趣小组的同学对呼吸面具的制氧原理产生好奇心,通过查阅资料得知,呼吸面具中制取氧气的主要原料是固
(2014•武汉)某化学兴趣小组的同学对呼吸面具的制氧原理产生好奇心,通过查阅资料得知,呼吸面具中制取氧气的主要原料是固体过氧化钠(Na2O2).过氧化钠分别能和二氧化碳、水反应,都生成氧气,反应的化学方程式为:
2Na2O2+2H2O═4NaOH+O2↑2Na2O2+2CO2═2Na2CO3+O2
为了测定呼吸面具中过氧化钠的质量分数,该小组的同学在老师的指导下,利用如图所示装置(固定装置一略去)开展探究,并得到正确的结论.
已知,装置B中盛有饱和NaHCO3溶液(NaHCO3不与CO2反应),碱石灰是由固体NaOH和CaO组成的混合物.整套装置气密性良好,反应所需试剂均足量.
请回答下列问题: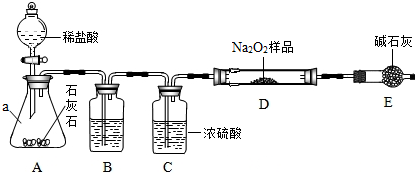
(1)仪器a的名称是______,装置A的作用是______;
(2)不用装置E代替装置C的理由是______.
(3)装置D中过氧化钠药品的质量为m g,装置D在反应前后的总质量n1 g和n2 g.若药品中所含杂质既不溶于水也不参加化学反应,则药品中过氧化钠的质量分数=
%1950(n2−n1) 7m .
%1950(n2−n1) 7m  caxel1年前1
caxel1年前1 -
 往事成烟 共回答了21个问题
往事成烟 共回答了21个问题 |采纳率95.2%解题思路:(1)熟悉常用仪器的名称和用途,根据装置的特点分析作用;
(2)根据碱石灰的性质分析;
(3)根据过氧化钠与二氧化碳的反应,由二氧化碳的质量求出过氧化钠的质量,在求出质量分数.(1)由于图示可知,仪器a的名称是锥形瓶,由装置可知,装置A的作用是制取二氧化碳气体;
(2)由于装置E中的碱石灰能与二氧化碳反应,不能用装置E代替装置C.
(3)设过氧化钠的质量为x
2Na2O2+2CO2═2Na2CO3+O2 增加量
156 88 32 56
xn2g-n1g
[156/56=
x
n2g−n2g] 解得:x=
156(n2g−n1g)
56
药品中过氧化钠的质量分数为:
156(n2g−n1g)
56
mg×100%=
1950(n2−n1)
7m%
故答为:(1)锥形瓶,产生实验所需的二氧化碳;(2)碱石灰还能与二氧化碳反应;(3)
1950(n2−n1)
7m%.点评:
本题考点: 实验探究物质的组成成分以及含量;气体的净化(除杂);二氧化碳的实验室制法;根据化学反应方程式的计算.
考点点评: 该题根据查阅资料提供的信息并结合实验步骤和现象解决问题.主要考查读题能力,能把题目所给信息与所学知识进行牵连.知道性质决定用途,用途体现性质1年前查看全部
- 用过氧化氢制氧 为什么用分液漏斗
 异域娃娃1年前2
异域娃娃1年前2 -
 fan163 共回答了13个问题
fan163 共回答了13个问题 |采纳率100%过氧化氢制氧的步骤为:
1.取一个烧瓶,一个分液漏斗.
2.组装装置,检查装置气密性.
3.在烧瓶里加入MnO2,组装好装置,在分液漏斗中加入H2O2.
4.连接其它装置(净化,收集).
5.缓慢旋开分液漏斗活塞,让H2O2缓慢滴下即可.
使用分液漏斗的目的是能够定量控制加入的过氧化氢的量.并且随时开始反应,随时终止反应.1年前查看全部
- 初三化学题把干燥纯净的氯酸钾把干燥纯净的氯酸钾和二氧化锰混合物15.5g,装入试管,加热制氧,待完全反映后,冷却称量,剩
初三化学题把干燥纯净的氯酸钾
把干燥纯净的氯酸钾和二氧化锰混合物15.5g,装入试管,加热制氧,待完全反映后,冷却称量,剩余固体10.7g.问:1、生成氧气质量 2、10.7g固体中有哪些物质,各多少克? hwgandhwg19781年前1
hwgandhwg19781年前1 -
 正理平治 共回答了17个问题
正理平治 共回答了17个问题 |采纳率88.2%氧气质量4.8g 固体中有氯化钾个二氧化锰 追问:我在给分 回答:根据质量守恒反应前的质量等于反映后的,生成物氧气+剩余固体的质量=15.5g 剩余的固体为反应生成的 氯化钾 和催化剂二氧化锰 追问:详细点,我可以加分,急啊 回答:15.5-10.7=4.8g 童鞋1年前查看全部
- 在潜水艇中普遍使用的制氧剂是一种呈黄色的固体氧化物,它能与二氧化碳反应产生氧
 et-yt1年前4
et-yt1年前4 -
 不会说话的猴子 共回答了18个问题
不会说话的猴子 共回答了18个问题 |采纳率94.4%是问方程式吗?2Na202+2CO2=2Na2CO3+O21年前查看全部
- 如图所示,有人制作了一个家庭制氧装置.该制氧装置由2个饮料瓶、2根软管和药剂构成,整套装置成本不到3块钱.药剂包括过氧碳
如图所示,有人制作了一个家庭制氧装置.该制氧装置由2个饮料瓶、2根软管和药剂构成,整套装置成本不到3块钱.药剂包括过氧碳酸钠(2Na2CO3•3H2O2)和二氧化锰.制氧时,先在两个饮料瓶中加入适量的水,再往甲瓶中加入药剂,产生的气体通过B管从乙瓶导出,即可供人吸氧.
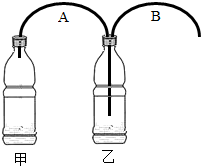
(1)为了顺利地导出甲瓶中产生的氧气,A软管在甲瓶中应______.
(选填“不伸入液面”或“伸入液面”)
(2)药剂加入水中后会发生以下两个反应:
2Na2CO3•3H2O2=2Na2CO3+3H2O2;2H2O2
2H2O+O2↑MnO2 .
从化学反应的基本类型来看,它们都属于______反应.
(3)已知总质量为110克的药剂可产生34克过氧化氢,则这包药剂完全反应会生成多少克氧气? bb_con1年前5
bb_con1年前5 -
 123周围们 共回答了18个问题
123周围们 共回答了18个问题 |采纳率88.9%解题思路:(1)如果A软管在甲瓶中深入液面以下,就无法导出气体;
(2)先观察两个化学反应式的特点,再根据四种反应类型的定义判断;
(3)根据产生34克过氧化氢,和过氧化氢分解生成氧气的化学反应式,设生成氧气的质量为m计算即可.(1)如果A软管在甲瓶中深入液面以下,就无法导出气体.为了顺利地导出甲瓶中产生的氧气,A软管在甲瓶中应不伸人液面.故答案为:不伸人液面;
(2)根据化学反应式可知,这两种反应式都是由一种物质生成其他两种其他物质的分解反应.故答案为:分解;
(3)设可生成氧气质量为m
2H2O2
MnO2
.
2H2O+O2↑
68 32
34g m
[68/34g]=[32/m]
m=16g
答:可生成氧气质量为16g.点评:
本题考点: 实验室制取氧气的反应原理;反应类型的判定;根据化学反应方程式的计算.
考点点评: 本题以实验探究的形式考查反应的类型和相关计算,较为容易,同时是学生了解到,许多的化学知识在生活中的运用.1年前查看全部
- 关于高锰酸钾制氧地震后 如果被埋在废墟里 环境狭小 空间有限 如果氧气被消耗光 后果很严重我已经在公文包中准备好水 食物
关于高锰酸钾制氧
地震后 如果被埋在废墟里 环境狭小 空间有限 如果氧气被消耗光 后果很严重
我已经在公文包中准备好水 食物 保温毯 急救包等等工具 但想来想去还是觉得这个问题必须解决
考虑到双氧水不稳定 而且属于易爆物品 通不过地铁安检 所以我想用高锰酸钾来制氧
但在这种情况下制氧需要面临几个问题
1 高锰酸钾必须加热才能产生氧气 但燃烧本身就需要消耗氧气 假设我把高锰酸钾溶液放在一个罐头里 用一跟蜡烛加热 制造出的氧气能否抵得上燃烧消耗的氧气并维持我们的呼吸
2 高锰酸钾是否需要配成溶液制氧 水同样是很宝贵的 所以如果必须要液体的话我想用尿来配制 请问这样配出的溶液可以制氧吗?会不会产生什么不良的化学反应
3 基于以上原因 是否可以在不燃烧的情况下直接用固体的高锰酸钾制氧 比如拿着手电筒对着药粉照 qq248617811年前3
qq248617811年前3 -
 vivirat 共回答了28个问题
vivirat 共回答了28个问题 |采纳率85.7%1.首先,你可以将h2o2转化成固态的过碳酸钠晶体(其化学式为:2na2co3·3h2o2).它比较稳定,且具有二者的性质.其次,即使燃烧本身就需要消耗氧气小于生成的氧气,所剩余的氧气也根本不够人呼吸只用.
2.高锰酸钾加热制氧无需配成溶液.
3.不行,高锰酸钾加热制氧所需的温度较高,约在270 ℃ .
最后,你见过地震导致人被埋,最后死因是氧气不足的吗?先然没有!所以不必考虑这么多,水 食物 保温毯 急救包已经绰绰有余了.1年前查看全部
- 实验室用KClO3制氧催化剂可用什么代替MnO2?
 首席ff1年前4
首席ff1年前4 -
 laizioran 共回答了9个问题
laizioran 共回答了9个问题 |采纳率88.9%,四种金属元素铜的元素活泼性最差1年前查看全部
- 氯酸钾反应为什么制氧纯,而氯酸钾与二氧化锰不纯
 ertijiao19691年前4
ertijiao19691年前4 -
 这么一个人 共回答了12个问题
这么一个人 共回答了12个问题 |采纳率83.3%有影响,原因很简单,因为二氧化锰催化的过程中经历了复杂的中间过程,
之间生成了氯气,而生成的氯气大多数反应掉最终变回氯化钾而得到氧气,
但有极少量的氯气并没有反应完全,因此产物不纯.1年前查看全部
- 化学制氧
 john0010191年前7
john0010191年前7 -
 去天三百 共回答了19个问题
去天三百 共回答了19个问题 |采纳率100%很多中方法 在高中化学中 最典型的就是 过氧化钠Na2O2 和二氧化碳或者水都可以放应成氧气 前者生成碳酸钠和氧气 后者是氢氧化钠和氧气.
初中介绍了加热高氯酸钾 生成氧气和氯化钾 或者用二氧化锰做催化剂催化双氧水分解成水和氧气 还有一个是高锰酸钾分解 2KMnO4 == K2MnO4 + O2↑ + MnO21年前查看全部
- 实验室用氯酸钾与二氧化锰的混合物制氧器并用排水法收集,加热一会儿试管破裂
实验室用氯酸钾与二氧化锰的混合物制氧器并用排水法收集,加热一会儿试管破裂
分析其原因 youwj20001年前2
youwj20001年前2 -
 KEITA520YY 共回答了16个问题
KEITA520YY 共回答了16个问题 |采纳率100%受热不均匀,一块地方太热,一块地方太冷,所以炸裂了
或者是先熄灭了酒精灯,没有撤离导管,使冷凝水倒吸入试管,使试管冷热不均匀,使试管炸裂
或者是碰到了酒精灯的灯芯
反正根本原因就是冷热不均匀1年前查看全部
- 用过氧化氢制氧时,分液漏斗中的过氧化氢溶液必须缓缓的滴入锥形瓶中,这是为了什么?
 ChinaSars1年前2
ChinaSars1年前2 -
 mychair 共回答了20个问题
mychair 共回答了20个问题 |采纳率90%防止反应过于激烈,气液混合物冲出锥形瓶1年前查看全部
- 氯酸钾与二氧化锰混合加热制氧为什么导管口不能塞棉花?
 jenny30121年前1
jenny30121年前1 -
 何胖 共回答了17个问题
何胖 共回答了17个问题 |采纳率76.5%用氯酸钾与二氧化锰制氧气时,氯酸钾会融化成液态,并将二氧化锰包裹在液态氯酸钾里,所以不会有固态物质同氧气一起进入瓶中.而高锰酸钾制氧气时不会融化,会有一部分高锰酸钾随氧气进入瓶中导致氧气不纯,变为淡红色.1年前查看全部
- 空分制氧纯度化学检测方法
 windedfish1年前1
windedfish1年前1 -
 skywinning 共回答了13个问题
skywinning 共回答了13个问题 |采纳率84.6%采用铜氨溶液吸收法进行测定.吸收液与氧气反应,根据样品气体体积的减少测定氧含量.1年前查看全部
- 过氧化钠是潜水艇氧气再生装置中制氧剂,它能与二氧化碳反应制成氧气,反应后固体粉末变成什么色
过氧化钠是潜水艇氧气再生装置中制氧剂,它能与二氧化碳反应制成氧气,反应后固体粉末变成什么色
详细的问题说明,有助于回答者给出准确的答案 崔雨13141年前1
崔雨13141年前1 -
 152654 共回答了23个问题
152654 共回答了23个问题 |采纳率95.7%白色Na2CO31年前查看全部
- 为什么工业制氧要用分离液态空气法
为什么工业制氧要用分离液态空气法
工业制氧不可以用加热高锰酸钾.分解双氧水.等方法来制氧么?为什么? 云归客1年前0
云归客1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 氯酸钾与二氧化锰混合加热制氧为什么导管口不能塞棉花?
 開心everyday1年前1
開心everyday1年前1 -
 xiou1366 共回答了19个问题
xiou1366 共回答了19个问题 |采纳率89.5%用氯酸钾与二氧化锰制氧气时,氯酸钾会融化成液态,并将二氧化锰包裹在液态氯酸钾里,所以不会有固态物质同氧气一起进入瓶中.而高锰酸钾制氧气时不会融化,会有一部分高锰酸钾随氧气进入瓶中导致氧气不纯,变为淡红色.1年前查看全部
- 制氧时试管口为什么要向下略微倾斜
 sxxwei1年前2
sxxwei1年前2 -
 soonerhong 共回答了19个问题
soonerhong 共回答了19个问题 |采纳率100%防止加热时,水蒸气在较冷的导管壁上凝结成的小水滴回流进试管底部,导致试管炸裂.1年前查看全部
- 在高锰酸钾加热制氧的实验中.先熄灭酒精灯火焰,再将导气管从水槽里抽出水面会有什么结果?
 男欢不尽轮1年前2
男欢不尽轮1年前2 -
 沉浸回忆 共回答了15个问题
沉浸回忆 共回答了15个问题 |采纳率100%水倒吸至试管中,引起试管炸裂.1年前查看全部
- 1、 下列变化属于化学变化的是:A、双氧水制氧气 B、蜡烛燃烧 C、湿衣服经太阳晒后变干 D、分离空气制氧
1、 下列变化属于化学变化的是:A、双氧水制氧气 B、蜡烛燃烧 C、湿衣服经太阳晒后变干 D、分离空气制氧
正确答案是A 可B不也是化学变化 dytsl1年前7
dytsl1年前7 -
 JacieNL 共回答了17个问题
JacieNL 共回答了17个问题 |采纳率94.1%A、双氧水制氧气 B、蜡烛燃烧
选 AB 答案错了1年前查看全部
- 在高锰酸钾加热制氧的实验中,反映完毕,先熄灭酒精灯火焰,再将导气管从水槽里抽出水面会有什么结果?为
 油焖茄子1年前1
油焖茄子1年前1 -
 hunanyonxing 共回答了13个问题
hunanyonxing 共回答了13个问题 |采纳率84.6%先熄灭酒精灯的话,试管内温度下降,管内气压低于管外气压,会导致水槽内的水通过导气管流进试管.1年前查看全部
- 人教版初三化学上册第二单元课题三.过氧化氢制氧试验.
人教版初三化学上册第二单元课题三.过氧化氢制氧试验.
还有实验的注意点.要全面一些,语言比较规范. 谢佑艺1年前4
谢佑艺1年前4 -
 惠连 共回答了18个问题
惠连 共回答了18个问题 |采纳率94.4%1.在试管中加入5ml 5% 的过氧化氢溶液,把带火星的木条伸入试管,木条是否复燃?
2.向上述试管中加入少量二氧化锰,把带火星的木条伸入试管.观察发生的现象.
实验1 现象:有很少的气泡,但木条没有复燃(原因:氧气量太少)
结论:过氧化氢常温下缓慢分解,产生氧气和水.
实验2 现象:有大量气泡,带火星木条伸进,很快复燃
结论:二氧化锰使反应变快,加速过氧化氢分解
讲述:如果在反应前称量二氧化锰质量,反应完后过滤并干燥后再称量,二氧化锰质量不变,再加入过氧化氢,继续反应,可重复使用.说明二氧化锰在反应前后质量和化学性质没有发生变化.1年前查看全部
- 如何验证二氧化锰在过氧化氢制氧中只做催化剂?要具体操作步骤!
如何验证二氧化锰在过氧化氢制氧中只做催化剂?要具体操作步骤!
验证反映前后化学性质和质量都没有变化!
 信大男生1年前1
信大男生1年前1 -
 我并不921 共回答了25个问题
我并不921 共回答了25个问题 |采纳率84%做到催化剂的条件是:①反应前后质量不变,②物质的化学性质(注意是化学性质,答题时不能只答性质)不变.
也就是分别验证质量和化学性质不变.
质量:进行试验前用托盘天平称量催化剂的质量,记为m1.反应结束后,过滤、洗涤、烘干固体,再次称量m2,若质量相等即m1=m2(或质量差小于等于0.1g也可以),则质量不变.
化学性质:将过滤、洗涤、烘干后的固体与浓盐酸混合加热,看能否生成黄绿色,能使有色布条褪色的气体(Cl2).1年前查看全部
- 实验室加热纯净物制氧,化学方程式怎么写
 yy人涛1年前1
yy人涛1年前1 -
 hsg0005 共回答了10个问题
hsg0005 共回答了10个问题 |采纳率70%2H²O²△=2H²O十O²个1年前查看全部
- 初中常见的5种制氧方法
 neverove1年前1
neverove1年前1 -
 rap_anson 共回答了18个问题
rap_anson 共回答了18个问题 |采纳率72.2%2KMnO4〓▲K2MnO4+MnO2+O2↑(▲是加热符)
2H2O2〓2H2O+O2↑ (要加MnO2做催化剂)
2KClO3〓▲2KCl+3O2↑ (也要加MnO2做催化剂)
过氧化钠与水反应
还有电解水分解成氧和H2↑1年前查看全部
- 常见的三种制氧的方法
 shirley0211年前1
shirley0211年前1 -
 思远_河流 共回答了19个问题
思远_河流 共回答了19个问题 |采纳率94.7%一 加热氯酸钾和二氧化锰的混合物 ,采用固固加热装置,用排水法收集 ,原理 :2 KClO3 ===加热 MnO2 === 2 KCl + 3 O2 ,二 加热高锰酸钾 ,装置同上 ,原理 :2 KMnO4 === 加热 ==== K2MnO4 + MnO2 + O2 ,三 在二氧化锰的催化下分解过氧化氢 ,装置采用固液型,用排水法 ,原理 :2 H2O2 == MnO2 === 2 H2O + O2 ,以上均是初中常见的实验室制取氧气的方法,至于还有一些其他的方法(如过氧化钠和二氧化碳 ,超氧化钾和二氧化碳等.1年前查看全部
- 过氧化钠是一种淡黄色固体,在潜水艇中用作制氧剂,供人类呼吸之用.某学生为了验证这一实验,以足量的大理石、足量的盐酸和1.
过氧化钠是一种淡黄色固体,在潜水艇中用作制氧剂,供人类呼吸之用.某学生为了验证这一实验,以足量的大理石、足量的盐酸和1.95g过氧化钠样品为原料,制取O 2 ,设计出如下实验装置: 
(1)请写出过氧化钠与二氧化碳反应的化学方程式,并标明电子转移的方向和数目:______;
(2)A中制取CO 2 的装置,应从下列图①、②、③中选哪个图:______;
(3)B装置的作用是______;
(4)为了检验E中收集到的气体,在取出集气瓶后,用______的木条伸入集气瓶内,木条会出现______;
(5)若E中石灰水出现轻微白色浑浊,请说明原因:______;
(6)当D中的1.95g过氧化钠样品接近反应完毕时,你预测E装置内有何现象?______;
(7)反应完毕时,若测得E中的集气瓶收集到的气体为250mL,又知氧气的密度为1.43g/L,当装置的气密性良好的情况下,实际收集到的氧气体积比理论计算值______(大或小),相差约______mL(取整数值,所用数据均在标准状况下测定),这是由于______. 神枪手0071年前1
神枪手0071年前1 -
 守夜tt 共回答了13个问题
守夜tt 共回答了13个问题 |采纳率84.6%(1)过氧化钠和二氧化碳反应生成碳酸钠和氧气,
故答案为:
(2)该反应的药品是固体和液体,且不需加热,所以所需装置为固液混合不加热型,故选②.
(3)大理石和盐酸的反应是放热反应,盐酸具有挥发性,所以制取的二氧化碳中含有氯化氢气体,氯化氢和碳酸氢钠能反应生成二氧化碳,二氧化碳和碳酸氢钠不反应,所以B装置的作用是除二氧化碳中的氯化氢.
故答案为:除CO 2 中的HCl.
(4)过氧化钠和二氧化碳反应生成氧气,氧气能使带火星的木条复燃.
故答案为:故带火星;复燃.
(5)二氧化碳能使澄清的石灰水变浑浊,若E中石灰水出现轻微白色浑浊,说明未反应的二氧化碳与石灰水反应所致.
故答案为:未反应的二氧化碳与石灰水反应所致.
(6)当D中的1.95g过氧化钠样品接近反应完毕时,由于生成氧气的量减少,压强变小,所以E中可能会因二氧化碳与石灰水反应而倒吸.
故答案为:由于生成氧气的量减少,E中可能会因二氧化碳与石灰水反应而倒吸.
(7)1.95g过氧化钠完全反应生成氧气的体积为v.
2Na 2 O 2 ----O 2 ;
2mol22.4L
1.95g
78g/mol v
v=0.28L=280mL>250mL,所以实际收集到的氧气体积比理论计算值小.
280mL-250mL=30mL;
原因是Na 2 O 2 可能含有其它杂质;D装置可能有氧气未被排出.
故答案为:小;30;Na 2 O 2 可能含有其它杂质;D装置可能有氧气未被排出.1年前查看全部
- 过氧化钠(Na2O2)是潜水艇氧气再生装置中制氧剂,它是一种淡黄色粉末,能与二氧化碳反应生成氧气,反应的化学方程式是
过氧化钠(Na2O2)是潜水艇氧气再生装置中制氧剂,它是一种淡黄色粉末,能与二氧化碳反应生成氧气,反应的化学方程式是
2Na2O2+2CO2═O2+2X,则Na2O2中氧元素化合价为______,X的化学式为______. 毒71年前1
毒71年前1 -
 runrain 共回答了19个问题
runrain 共回答了19个问题 |采纳率89.5%解题思路:根据常见元素的化合价及化合物中正负化合价的代数和为0来计算过氧化钠中氧元素的花合计,再利用化学反应方程式和质量守恒定律来推断X的化学式.在Na2O2中Na元素的化合价为+1价,
设O元素的化合价为x,
根据化合物中正负化合价的代数和为0,则
(+1)×2+x×2=0,解得x=-1;
在2Na2O2+2CO2═O2+2X中,
根据质量守恒定律可知,反应前后元素种类、原子个数和种类相等,
反应前共4个Na原子、2个C原子、8个O原子,
反应后有氧气生成,
则X中应共含有4个Na原子、2个C原子、6个O原子,
又X的化学计量数为2,则X的化学式为Na2CO3,
故答案为:-1;Na2CO3.点评:
本题考点: 有关化学式的计算和推断;有关元素化合价的计算.
考点点评: 本题考查元素化合价的计算和利用化学反应方程式来推断物质的化学式,学生应熟悉常见元素的化合价及守恒法来分析解答.1年前查看全部
- 加热ag氯酸钾和bg二氧化锰的混合物制氧器,到固体质量不在减少为止,得到cg氯化钾,根据质量守恒定律
加热ag氯酸钾和bg二氧化锰的混合物制氧器,到固体质量不在减少为止,得到cg氯化钾,根据质量守恒定律
可知生成氧气的质量为? sunshine12451年前2
sunshine12451年前2 -
 evachaung 共回答了13个问题
evachaung 共回答了13个问题 |采纳率84.6%生成氧气的质量=a-c (g)
反应前后二氧化锰的质量没变
反应物是:ag的氯酸钾,生成物是O2和cg的氯化钾
根据质量守恒定律知:ag=O2的质量+cg
所以:O2的质量=a-c (g)1年前查看全部
- 潜艇中的氧气再生装置,有以下几种制氧的方法:
潜艇中的氧气再生装置,有以下几种制氧的方法:
①加热高锰酸钾②电解水③在常温下过氧化钠固体与二氧化碳反应生成碳酸纳和氧气
其中第______种方法最好.
反应原理是______
优点______. LTSCOOL1年前1
LTSCOOL1年前1 -
 hpj158 共回答了18个问题
hpj158 共回答了18个问题 |采纳率83.3%解题思路:本题考查氧气的制法,在潜艇中制氧气,需要考虑实际情况,要本着方便快捷,节约能源等原则来反应.
①实验装置复杂,且需要加热;
②电解需要消耗电能;
③装置简便,在常温下可反应,不需要消耗其它能源,原料易得,
所以第③种方法最好.①2KMnO4
△
.
K2MnO4+MnO2+O2↑实验装置复杂,且需要加热
②水
通电
氢气+氧气,消耗大量的能源,装置较复杂;
③过氧化钠+二氧化碳→碳酸钠+氧气,装置简便,在常温下可反应,不需要消耗其它能源,原料易得
故答案为:③;过氧化钠+二氧化碳→碳酸钠+氧气;不消耗其它能源,操作简单.点评:
本题考点: 氧气的工业制法;实验室制取氧气的反应原理.
考点点评: 学生要熟悉氧气的制取原理和相应的装置,①是固固加热装置,②是电解装置,③是固固反应且不需加热装置,另外还要知道双氧水制取氧气是固液反应装置,针对不同的问题采取相应的答案.1年前查看全部
- 碳硫磷铁镁燃烧,过氧水 二氧化锰、高锰酸钾 加热制氧 的化学表达式.
碳硫磷铁镁燃烧,过氧水 二氧化锰、高锰酸钾 加热制氧 的化学表达式.
例:(碳)C+O2 点燃 CO2 流浪的人儿1年前3
流浪的人儿1年前3 -
 郭芙蓉背着洋娃娃 共回答了13个问题
郭芙蓉背着洋娃娃 共回答了13个问题 |采纳率76.9%(硫)S+O2 点燃 SO2
(磷)P+O2 点燃 P2O5
(铁)Fe+O2 点燃 Fe3O4
(镁)Mg+O2 点燃 MgO
(过氧化氢)H2O2 MnO2 H2O+O2
(高锰酸钾) KMnO4 加热 K2MnO4 +MnO2+O21年前查看全部
- 过氧化氢制氧为什么所制氧气纯?
 szfssj1年前3
szfssj1年前3 -
 风中的恋情 共回答了29个问题
风中的恋情 共回答了29个问题 |采纳率89.7%过氧化氢分解,生成的是水和氧气两种物质,水很好分离出去,氧气就比较纯的,不含其他气体1年前查看全部
- (2009•常熟市模拟)超氧化钾(KO2)是一种黄色固体,它能与二氧化碳反应生成氧气,在潜水艇中用它作制氧剂,供人们呼吸
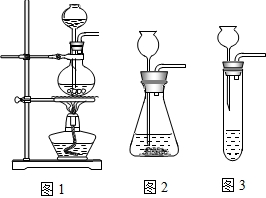 (2009•常熟市模拟)超氧化钾(KO2)是一种黄色固体,它能与二氧化碳反应生成氧气,在潜水艇中用它作制氧剂,供人们呼吸之用,它与二氧化碳反应的化学方程式为:4KO2+2CO2═2K2CO3+3O2,某学生为了验证这一实验,以大理石,足量的盐酸和超氧化钾为原料制取O2,设计如下实验装置:
(2009•常熟市模拟)超氧化钾(KO2)是一种黄色固体,它能与二氧化碳反应生成氧气,在潜水艇中用它作制氧剂,供人们呼吸之用,它与二氧化碳反应的化学方程式为:4KO2+2CO2═2K2CO3+3O2,某学生为了验证这一实验,以大理石,足量的盐酸和超氧化钾为原料制取O2,设计如下实验装置: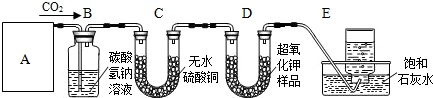
(1)A是制取CO2的装置,应从下图1~3中选择______.C装置内可能出现的现象是______.为了检验E中收集到的气体,可以在取出集气瓶后,用______,现象是______.
(2)若E中的石灰水出现少量的白色沉淀,这是因为______.
(3)表明D中的超氧化钾样品接近反应完毕时的现象是______. Oath吻1年前1
Oath吻1年前1 -
 gg甲1 共回答了29个问题
gg甲1 共回答了29个问题 |采纳率89.7%解题思路:抓住实验室中制取二氧化碳的药品是石灰石(或大理石)和稀盐酸,固液混合而且不需要加热,因此在反应装置的选择上应该注意,二氧化碳和氧气的检验方法主要是根据这两种物质的性质来决定,认真分析资料从中获取有用的信息:4KO2+2CO2═2K2CO3+3O2,超氧化钾是一种黄色固体.(1)由于在实验室中制取二氧化碳是用大理石(或石灰石)和稀盐酸反应,是固液混合且不需要加热;硫酸铜是白色固体,遇到水就会和水反应生成蓝色的五水硫酸铜;氧气能支持燃烧,能使带火星的木条复燃,因此常用带火星的木条来检验氧气,故答案为:图2,白色固体变成蓝色,带火星的木条插入集气瓶内,木条复燃
(2)E中的石灰水出现少量的白色沉淀,说明氧气中混有二氧化碳,即二氧化碳没有全部参与化学反应,故答案为:在D中有少量的二氧化碳没有参与反应随氧气进入到E中,生成了碳酸钙
(3)D中的超氧化钾样品接近反应完毕时,说明超氧化钾全部变成了碳酸钾,已经不能再和二氧化碳发生反应,因此会看到E中的浑浊现象越来越严重,故选D中的黄色固体全部变成白色,且E中浑浊明显点评:
本题考点: 二氧化碳的实验室制法;实验探究物质的性质或变化规律;氧气的检验和验满;化学性质与物理性质的差别及应用.
考点点评: 主要考查了实验室中制取二氧化碳的有关的知识,培养学生分析资料、解决问题的能力.1年前查看全部
大家在问
- 1已知实数A和B分别满足等式A的平方=4A-3和B的平方=4B-3,求代数式B/A+A/B的值
- 2读某半球经纬网示意图,完成下列问题。
- 3晶体在熔化过程中不断从外界______,温度______;熔化时的温度叫做晶体的______.
- 4What_(do)next Sunday?I_(milk)cows..怎么写?
- 5不惑 垂髫 花甲 弱冠 而立 古稀 半百 分别 是多少岁
- 6一个圆柱体高20cm,他被载去5cm后,圆柱的表面积减少了31.4平方cm,原来圆柱体的表面积是多少平方厘米?
- 7填空题 :有关于 抛物线1.抛物线y^2=2px(p>0)上一点M到焦点的距离是a(a>p/2),则点M到准线的距离是(
- 8在胡萝卜根的韧皮部细胞中,把ADP转变成ATP的酶分布在( )
- 9附加题:材料:股票市场,买、卖股票都要分别交纳印花税等有关税费.以沪市A股的股票交易为例,除成本外还要交纳:①印花税:按
- 103.Fish can`t live without water or air (改为条件句) Firsh can`t l
- 11(2008•旅顺口区模拟)小刚家里连接热水器的插头与插座接触不良,在热水器使用一段时间后发现插头与插座过热.下列关于插头
- 12直线y=kx+2与曲线y=根号(-x^2+2x) (0≤x≤2)存在两个交点,则实数k的取值范围是
- 13可在化学反应中不是的电子的是还原剂吗?
- 14军惊而坏都舍是什么意思
- 15发电机的功率一定,负载(电瓶)并联越多,电阻就越小,电流就大,进而就会损坏发电机.
