(2013•润州区二模)碳酸镁晶须(MgCO3•nH2O,n=1~5的整数)广泛应用于冶金、耐火材料及化工产品等领域.为
 000gg0002022-10-04 11:39:541条回答
000gg0002022-10-04 11:39:541条回答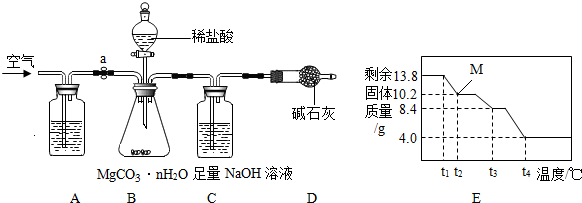
【查阅资料】:
a、碳酸镁晶须受热分解,生成3种氧化物;
b、相对分子质量:[Mr(MgCO3):84、Mr(H2O):18、Mr(MgO):40、Mr(CO2):44]
【实验步骤】
①______;
②准确称取3.45g MgCO3•nH2O放在B装置中,连接仪器;
③打开弹簧夹a,鼓入一段时间空气,称量C装置的质量;
④关闭弹簧夹a,打开分液漏斗活塞,缓缓滴入稀盐酸至不再产生气体为止;
⑤打开弹簧夹a,______;
| 编号 | 1 | 2 | 3 |
| 实验前 | 228.00 | 228.00 | 228.00 |
| 实验后 | 229.10 | 229.11 | 229.09 |
⑦重复上述步骤;
⑧根据数据进行计算.
【实验分析及数据处理】
(1)A装置中盛放的溶液是______,其目的是______
(2)D装置的作用是______;
(3)计算碳酸镁晶须中的n值:(要有计算过程)
【实验反思】
(4)实验结果与理论值有偏差,可以在B、C增加一个______装置以减少误差;
(5)下列选项中,会造成实验结果偏大的是______;偏小的是______;
①反应结束后,没有通空气; ②称量C装置前,没有通空气;
③没有A装置; ④没有D装置;
⑤稀盐酸滴加速率太快; ⑥C装置中NaOH溶液浓度过大;
(6)为精确测定n的值,在老师指导下,小组同学称取13.8g MgCO3•nH2O进行热重分析,并绘制出图E所示的热重曲线示意图.则:
①t2℃时,剩余固体为______(填化学式);
②最终剩余的4.0g物质是______(填化学式);
③MgCO3•nH2O完全分解的化学方程式为:
| ||
| ||

已提交,审核后显示!提交回复
共1条回复
 吾将上下求索 共回答了18个问题
吾将上下求索 共回答了18个问题 |采纳率66.7%- 解题思路:通过实验装置和实验分析可知:第一步骤首先是检查装置的气密性,这是保证实验成功的关键;第⑤步中,打开弹簧夹a,缓缓鼓入空气,是为了把整个装置中的二氧化碳排出去;A装置中盛放的溶液是NaOH(浓)溶液,是用来吸收鼓入空气中的二氧化碳,可以减少误差;D装置的作用是:防止空气中的CO2进入C装置,造成误差.
【实验步骤】第一步骤首先是检查装置的气密性,这是保证实验成功的关键;第⑤步中,打开弹簧夹a,缓缓鼓入空气,是为了把整个装置中的二氧化碳排出去;故答案为:①检查气密性;⑤缓缓鼓入空气
【实验分析及数据处理】
(1)A装置中盛放的溶液是NaOH(浓)溶液,是用来吸收鼓入空气中的二氧化碳,可以减少误差,故答案为:NaOH(浓)溶液;吸收鼓入空气中的二氧化碳
(2)D装置的作用是:防止空气中的CO2进入C装置,造成误差,故答案为:防止空气中的CO2进入C装置,造成误差
(3)故答案为:3次实验C装置平均增重(1.1+1.11+1.09)g/3=3g
MgCO3•nH2O~CO2
84+18n 44
3.45g3g
(4)故答案为:除去氯化氢气体的
(5)故答案为:②③④;①;
(6)故答案为:①MgCO3和MgO;②MgO;③MgCO3•nH2O
△
.
MgO+H2O+CO2↑;点评:
本题考点: 实验探究物质的组成成分以及含量;气体的净化(除杂);酸的化学性质;化学式的书写及意义;书写化学方程式、文字表达式、电离方程式.
考点点评: 本考点既考查了实验步骤的设计,又考查了化学方程式的书写和有关的计算等,还对实验进行了评价,综合性比较强.实验探究题是近几年中考的热点之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过实验资料和实验分析,得到了正确的结论,属于结论性探究.同学们要具体分析,综合掌握. - 1年前
相关推荐
- (2014•润州区二模)下列CO2的制备装置中,不能起到“随开随制,随关随停”效果的是( )
(2014•润州区二模)下列CO2的制备装置中,不能起到“随开随制,随关随停”效果的是( )
A.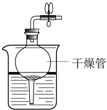
B.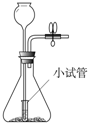
C.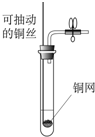
D.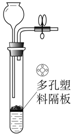
 鼠唛王子1年前1
鼠唛王子1年前1 -
 yeyee 共回答了22个问题
yeyee 共回答了22个问题 |采纳率95.5%解题思路:根据实际操作分析装置是否具有控制反应的发生和停止的效果.A、用弹簧夹夹住橡胶管时气体排不出去,球形瓶中的气体压强变大从而迫使稀盐酸排出干燥管并与大理石分离,反应停止.放开弹簧夹时,稀盐酸进入干燥管,并和烧杯中的液面相平同时与大理石接触,发生化学反应.所以该装置可以通过控制弹簧夹来达到使盐酸和大理石分离,从而控制反应的发生和停止,不符合题意;
B、固体放在大试管中酸放在小试管中,酸和固体不能分离,故无法控制反应发生和停止,符合题意;
C、该装置将固体放于铜网上,铜网放入液体,反应生成气体,将铜网拉出,固液分离,反应停止,故不符合题意;
D、大理石反放于隔板上,通过长颈漏斗添加液体,长颈漏斗下端在液面以上,即使夹上弹簧夹液体也无法压入长颈漏斗,故无法控制反应的发生和停止,符合题意;
故选BD.点评:
本题考点: 常用气体的发生装置和收集装置与选取方法.
考点点评: 通过回答本题掌握了控制反应的发生和停止的实验装置的设计方法,培养了学生分析解决问题的能力.1年前查看全部
- (它0o7•润州区j模)如图所示电源电压U=o8得,小灯泡Le额定电压为m得,当滑动变阻器e滑片P移至t点时,小灯泡L正
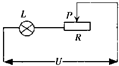 (它0o7•润州区j模)如图所示电源电压U=o8得,小灯泡Le额定电压为m得,当滑动变阻器e滑片P移至t点时,小灯泡L正常发光;当滑片P移至最右端时,小灯泡e实际功率为人W,则小灯泡e额定功率和滑动变阻器e最大阻值分别为( )
(它0o7•润州区j模)如图所示电源电压U=o8得,小灯泡Le额定电压为m得,当滑动变阻器e滑片P移至t点时,小灯泡L正常发光;当滑片P移至最右端时,小灯泡e实际功率为人W,则小灯泡e额定功率和滑动变阻器e最大阻值分别为( )
A.13.5W6Ω
B.13.5W12Ω
C.6W 27Ω
D.6W12Ω kyi20051年前1
kyi20051年前1 -
 吴里头9号 共回答了20个问题
吴里头9号 共回答了20个问题 |采纳率90%(1)P在中点时(连入电阻为
1
24),灯泡正常发光,说明此时灯泡两端的电压为9V,变阻器两端的电压为9V,
即变阻器的最大阻值4为灯泡电阻4L的两倍,4L=4′=
1
24.
(2)当P移动到最右端时(电阻全连入为4),
I=
U
4+4L=
P
4L,即:
18V
4+
1
24=
6W
1
24,
解得:4=12Ω
4L=4′=
1
2=6Ω.
P额=
U2额
4L=
(9V)2
6Ω=14.5W.
故选B.1年前查看全部
- (2012•润州区二模)下列实验操作不正确的是( )
(2012•润州区二模)下列实验操作不正确的是( )
A.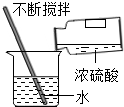
稀释浓硫酸
B.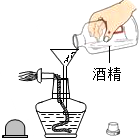
添加酒精
C.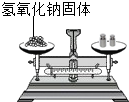
称量NaOH的质量
D.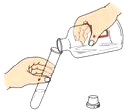
液体倾倒 alexmix1年前1
alexmix1年前1 -
 54cc101 共回答了16个问题
54cc101 共回答了16个问题 |采纳率93.8%解题思路:A、根据浓硫酸的稀释方法进行分析判断.
B、根据向酒精灯内添加酒精的方法进行分析平.
C、根据氢氧化钠具有腐蚀性进行分析判断.
D、根据向试管中倾倒液体药品的方法进行分析判断.A、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;一定不能把水注入浓硫酸中;图中所示操作正确.
B、可用漏斗向酒精灯内添加酒精,图中所示操作正确.
C、氢氧化钠具有腐蚀性,不能放在纸上称量,应放在烧杯中称量,图中所示操作错误.
D、向试管中倾倒液体药品时,瓶塞要倒放,标签要对准手心,瓶口紧挨,图中所示操作正确.
故选C.点评:
本题考点: 浓硫酸的性质及浓硫酸的稀释;称量器-托盘天平;加热器皿-酒精灯;液体药品的取用.
考点点评: 本题难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.1年前查看全部
- (2014•润州区二模)下列设计方案可行,且化学方程式书写正确的是( )
(2014•润州区二模)下列设计方案可行,且化学方程式书写正确的是( )
A.用Al(OH)3治疗胃酸过多症:Al(OH)3+3HCl═AlCl3+3H2O
B.实验室用稀硫酸与铜片反应制取H2:Cu+H2SO4═CuSO4+H2↑
C.用铁粉从含硝酸银的废水中提取金属银:Fe+3AgNO3═Fe(NO3)3+3Ag
D.用点燃的方法除去二氧化碳气体中混有的少量一氧化碳:2CO+O2
2CO2点燃 . 焦嘛鸟1年前1
焦嘛鸟1年前1 -
 不懒猫 共回答了20个问题
不懒猫 共回答了20个问题 |采纳率85%解题思路:A、设计方案可行,且化学方程式书写正确;
B、铜的金属活动性较差,不能与酸反应制取氢气;
C、用适量的铁粉与硝酸银反应,生成物为氯化亚铁,而非氯化铁;
D、二氧化碳气体中混有的少量一氧化碳,是不能点燃的,设计方案不可行.A、用Al(OH)3治疗胃酸过多症:Al(OH)3+3HCl=AlCl3+3H2O,故A正确;
B、铜的金属活动性较差,不能与酸反应制取氢气,化学方程式错误,故B错误;
C、生成物为氯化亚铁,而非氯化亚铁,改为“Fe+2AgNO3═Fe(NO3)2+2Ag”,故C错误;
D、用点燃的方法除去二氧化碳气体中混有的少量一氧化碳:2CO+O2
点燃
.
2CO2,设计方案不可行,故D错误.
故选A.点评:
本题考点: 书写化学方程式、文字表达式、电离方程式.
考点点评: 掌握化学方程式的书写方法与技巧;掌握二氧化碳的化学性质和金属活动性顺序及其应用;学会结合课本知识,学会进行知识的大胆迁移的方法.1年前查看全部
- (2014•润州区二模)一个标有“12V xxW“字样额定功率未知的灯泡,在室内测得其灯丝电阻R随
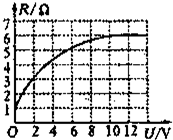 (2014•润州区二模)一个标有“12VxxW“字样额定功率未知的灯泡,在室内测得其灯丝电阻R随灯泡两端电压U变化的关系图线如图所示.则灯泡正常发光时的电阻为______Ω;xx代表的数字是______W;假如灯丝电阻与其热力学温度成正比,室温为300K(K是热力学温度单位),那么在灯泡正常发光的情况下,灯丝的温度为______K.
(2014•润州区二模)一个标有“12VxxW“字样额定功率未知的灯泡,在室内测得其灯丝电阻R随灯泡两端电压U变化的关系图线如图所示.则灯泡正常发光时的电阻为______Ω;xx代表的数字是______W;假如灯丝电阻与其热力学温度成正比,室温为300K(K是热力学温度单位),那么在灯泡正常发光的情况下,灯丝的温度为______K.  yyyc691年前1
yyyc691年前1 -
 diefool 共回答了22个问题
diefool 共回答了22个问题 |采纳率86.4%解题思路:(1)灯泡正常发光时的电压和额定电压相等,根据图象读出对应的电阻,根据P=
求出灯泡的额定功率;U2 R
(2)图可知室温下灯丝的电阻为1Ω,根据灯丝电阻与其热力学温度成正比得出R与热力学温度T的表达式,再根据表达式求出当灯泡正常发光时灯丝的温度.(1)灯泡正常发光时的电压U=12V,由图象可知灯泡的电阻R=6Ω,
则灯泡的额定功率:
P=
U2
R=
(12V)2
6Ω=24W;
(2)由图可知室温下灯丝的电阻为1Ω,
因灯丝电阻与其热力学温度成正比,即R=kT,
则1Ω=k×300K,
解得:k=[1/300]Ω/K,
当灯泡正常发光时,灯泡的电阻:
R=kT,即6Ω=[1/300]Ω/K×T,
解得:T=1800K.
故答案为:6;24;1800.点评:
本题考点: 电功率的计算.
考点点评: 本题考查了电功率的计算和灯丝温度的计算,关键是根据图象读出电阻和利用好“灯丝电阻与其热力学温度成正比”.1年前查看全部
- 英文翻译怎么写:镇江市润州区万达广场写字楼A座803
 swnazi791年前2
swnazi791年前2 -
 伤心天Y涯伤心客 共回答了21个问题
伤心天Y涯伤心客 共回答了21个问题 |采纳率90.5%镇江市润州区万达广场写字楼A座803
Room 803,Tower A,Wanda Plaza Office Building,Runzhou District,Zhenjiang City,Jiangsu Province,China1年前查看全部
- (2014•润州区二模)若n边形的内角和等于外角和,则n=______.
 pzq93111年前1
pzq93111年前1 -
 luzhehui 共回答了20个问题
luzhehui 共回答了20个问题 |采纳率95%由n边形的内角和等于外角和,得
(n-2)180°=360°,
解得n=4,
故答案为;4.1年前查看全部
- (2014•润州区二模)将正方形图1做如下操作:第1次:分别连结各边中点如图2,得到5个正方形;第2次:将图2左上角正方
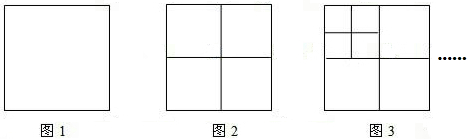
(2014•润州区二模)将正方形图1做如下操作:第1次:分别连结各边中点如图2,得到5个正方形;第2次:将图2左上角正方形按上述方法在分割如图3,得到9个正方形…,依此类推,根据以上操作,若要得到2013个正方形,则需要操作______次.
 abingwin1年前1
abingwin1年前1 -
 深夜的思念 共回答了23个问题
深夜的思念 共回答了23个问题 |采纳率87%解题思路:根据正方形的个数变化可设第n次得到2013个正方形,则4n+1=2013,求出即可.∵第1次:分别连接各边中点如图2,得到4+1=5个正方形;
第2次:将图2左上角正方形按上述方法再分割如图3,得到4×2+1=9个正方形…,
以此类推,根据以上操作,若第n次得到2013个正方形,则4n+1=2013,
解得:n=503.
故答案为:503.点评:
本题考点: 规律型:图形的变化类.
考点点评: 此题主要考查了图形的变化类,根据已知得出正方形个数的变化规律是解题关键.1年前查看全部
- (2014•润州区二模)如图是某燃煤发电厂处理废气的装置示意图.
 (2014•润州区二模)如图是某燃煤发电厂处理废气的装置示意图.
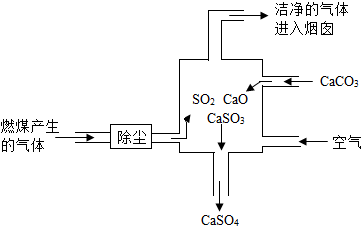
(2014•润州区二模)如图是某燃煤发电厂处理废气的装置示意图.
(1)使用此废气处理装置,可减少______的排放,从而减少酸雨对环境造成的危害;
(2)写出该电厂处理废气的总的化学反应方程式:______. iixxm1年前1
iixxm1年前1 -
 crazysushu 共回答了18个问题
crazysushu 共回答了18个问题 |采纳率100%解题思路:(1)根据二氧化硫是形成酸雨的重要物质,此装置处理的是二氧化硫分析;
(2)根据反应过程可以书写反应的化学方程式.(1)二氧化硫是形成酸雨的重要物质,经过处理后二氧化硫消失,能减少酸雨的形成;
(2)整个过程中,二氧化硫与碳酸钙和氧气反应生成了硫酸钙和二氧化碳,化学反应式可表示为:2SO2+2CaCO3+O2=2CaSO4+2CO2.
故答案为:①二氧化硫;②2SO2+2CaCO3+O2═2CaSO4+2CO2.点评:
本题考点: 酸雨的产生、危害及防治;书写化学方程式、文字表达式、电离方程式.
考点点评: 解答本题要充分理解处理废气的过程,只有这样才能对相关方面的问题做出正确的判断.1年前查看全部
- (2013•润州区二模)同学们对一包放置在外面一段时间的“504双吸剂”固体样品很好奇,设计实验进行探究. 品名:504
(2013•润州区二模)同学们对一包放置在外面一段时间的“504双吸剂”固体样品很好奇,设计实验进行探究.
【提出问题】固体的成分是什么?品名:504双吸剂
成分:铁粉、生石灰等
【查阅资料】铁与氯化铁溶液在常温下发生反应
生成氯化亚铁,反应的方程式为Fe+2FeCl3=3FeCl2
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【实验探究1】甲同学的方案:
【实验质疑】乙,丙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,他们的理由是______.实验操作 实验现象 实验结论 (1)取少量固体放于试管中,加足量蒸馏水溶解. 固体溶解时试管外壁发烫,试管底部有不溶物. 固体中一定含有______ (2)另取少量固体放于试管中,滴加足量的______. 固体逐渐消失,有大量无色气体产生,将气体通入石灰水,石灰水变浑浊,并得到浅绿色溶液. 固体中一定含有______,
一定不含Fe2O3
【实验探究2】乙、丙同学设计如下实验方案继续验证: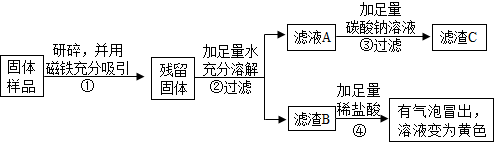
(1)③中反应的化学方程式是______.
(2)乙、丙同学实验中又能得出固体样品中一定还含有______,仍有一种物质不能确定,该物质是______.
(3)乙、丙同学又经过实验测得上述残留固体中含钙物质的总质量为1.6g,滤渣B中CaCO3的质量为1.0g,滤渣C的质量为1.0g.
【实验结论】综合上述实验及给数据,同学们的猜想______(填“成立”或“不成立”) seanily1年前1
seanily1年前1 -
 泷泽云枫 共回答了20个问题
泷泽云枫 共回答了20个问题 |采纳率90%解题思路:甲同学的实验方案中,通过实验分析可知:取少量固体放于试管中,加足量蒸馏水溶解,固体溶解时试管外壁发烫,说明固体溶于水放热,该固体中一定含有CaO;另取少量固体放于试管中,滴加足量的稀盐酸,固体逐渐消失,有大量无色气体产生,将气体通入石灰水,石灰水变浑浊,并得到浅绿色溶液,说明该固体中一定含有CaCO3和Fe;乙,丙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,他们的理由是:铁与氯化铁溶液在常温下发生反应生成氯化亚铁.由流程图可知:滤液A是氢氧化钙溶液,氢氧化钙与碳酸钠溶液反应生成碳酸钙白色沉淀和氢氧化钠,配平即可;因为溶液变为黄色,因此该固体中一定含有氧化铁;不能确定物质是氢氧化钙,因为氧化钙和水反应生成氢氧化钙.乙、丙同学又经过实验测得上述残留固体中含钙物质的总质量为1.6g,滤渣B中CaCO3的质量为1.0g,滤渣C的质量为1.0g;根据滤渣C中碳酸钙是1.0g求氧化钙,据CaO→Ca(OH)2→CaCO3可知:氧化钙的质量是0.56g,因此残留固体中含钙物质的总质量=1.0g+0.56g≈1.6g,因此同学们的猜想成立.【实验探究1】通过实验分析可知:取少量固体放于试管中,加足量蒸馏水溶解,固体溶解时试管外壁发烫,说明固体溶于水放热,该固体中一定含有CaO;另取少量固体放于试管中,滴加足量的稀盐酸,固体逐渐消失,有大量无色气体产生,将气体通入石灰水,石灰水变浑浊,并得到浅绿色溶液,说明该固体中一定含有CaCO3和Fe;故答案为:
实验操作 实验现象 实验结论
固体中一定含有CaO
(2)另取少量固体放于试管中,滴加足量的稀盐酸(或稀HCl). 固体中一定含有CaCO3和Fe,一定不含Fe2O3【实验质疑】乙,丙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,他们的理由是:铁与氯化铁溶液在常温下发生反应生成氯化亚铁,故答案为:铁与氯化铁溶液在常温下发生反应生成氯化亚铁
【实验探究2】
(1)由流程图可知:滤液A是氢氧化钙溶液,氢氧化钙与碳酸钠溶液反应生成碳酸钙白色沉淀和氢氧化钠,配平即可,故答案为:Na2CO3+Ca(OH)2=2NaOH+CaCO3↓
(2)由流程图可知:滤液A是氢氧化钙溶液,氢氧化钙与碳酸钠溶液反应生成碳酸钙白色沉淀和氢氧化钠,配平即可;因为溶液变为黄色,因此该固体中一定含有氧化铁;不能确定物质是氢氧化钙,因为氧化钙和水反应生成氢氧化钙,故答案为:Fe2O3,Ca(OH)2.
(3)【实验结论】乙、丙同学又经过实验测得上述残留固体中含钙物质的总质量为1.6g,滤渣B中CaCO3的质量为1.0g,滤渣C的质量为1.0g;根据滤渣C中碳酸钙是1.0g求氧化钙,据CaO→Ca(OH)2→CaCO3可知:氧化钙的质量是0.56g,因此残留固体中含钙物质的总质量=1.0g+0.56g≈1.6g,因此同学们的猜想成立.故答案为:成立点评:
本题考点: 实验探究物质的组成成分以及含量;金属锈蚀的条件及其防护;生石灰的性质与用途;酸的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 本考点既考查了实验步骤的设计,又考查了化学方程式的书写,还对实验进行了评价,综合性比较强.实验探究题是近几年中考的热点之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过实验资料和实验分析,得到了正确的结论,属于结论性探究.同学们要具体分析,综合掌握.1年前查看全部
- (2014•润州区二模)电热水器内部简化电路如图所示,R1和R2均为电热丝.该电热器有高温、中温、低温三档,中温档的电流
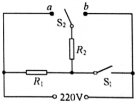 (2014•润州区二模)电热水器内部简化电路如图所示,R1和R2均为电热丝.该电热器有高温、中温、低温三档,中温档的电流是5A,电热丝R2的阻值是66Ω.
(2014•润州区二模)电热水器内部简化电路如图所示,R1和R2均为电热丝.该电热器有高温、中温、低温三档,中温档的电流是5A,电热丝R2的阻值是66Ω.
(1)中温档正常工作10分钟产生的热量是______J;
(2)低温档的电流是______A;
(3)高温档时,开关S1、S2的状态是______,电路功率是______. zz铃1年前1
zz铃1年前1 -
 Ironforce 共回答了21个问题
Ironforce 共回答了21个问题 |采纳率90.5%解题思路:(1)已知中温挡通过电路的电流,根据Q=W=UIt即可求出中温档正常工作10分钟产生的热量;
(2)先根据中温档电路的结构和欧姆定律的变形公式求出R1的阻值,然后根据串联电路电阻的特点求出R1、R2串联后的总电阻,再根据欧姆定律即可求出低温档的电流;
(3)当S1闭合,S2接a时,电热水器处于高温挡;先由根据并联电路电阻的特点求出总电阻,然后根据欧姆定律高温档时电路的电流,最后根据P=UI求出此时电路的功率.(1)电热水器工作时消耗的电能转化为了内能,因此中温档正常工作10分钟产生的热量:Q=W=UIt=220V×5A×10×60s=6.6×105J;
(2)S1闭合,S2接b时,电阻R1接入电路,电热水器处于中温档;由I=[U/R]可知,电阻R1的阻值:R1=[U/I]=[220V/5A]=44Ω;
S1断开,S2接b时,电阻R1与R2串联,电热水器处于低温档;此时电路的总电阻:R=R1+R2=44Ω+66Ω=110Ω;
此时电路中的电流:I′=[U/R]=[220V/110Ω]=2A;
(3)当S1闭合,S2接a时,电阻R1与R2并联,由P=
U2
R可知,电热水器处于高温挡;
此时通过R1的电流:I1=[U
R1=
220V/44Ω]=5A;
通过R2的电流:I2=[U
R2=
220V/66Ω]=[10/3]A;
由于并联中,干路电流等于各支路电流之和,故干路电流:I2=5A+[10/3]A=[25/3]A,
则电路功率:P=UI=220V×[25/3]A≈1833.3W.
故答案为:(1)6.6×105;(2)2;(3)S1闭合,S2接a;1833.3W.点评:
本题考点: 电功与热量的综合计算.
考点点评: 本题考查电流、电阻、电功及电功率的计算以及欧姆定律的应用,关键是公式及其变形的应用,难点是结合电路图判断高温档位、中温挡位和低温档位.1年前查看全部
- (2014•润州区二模)小明用如图所示的装置,探究摩擦力的大小与哪些因素有关.
(2014•润州区二模)小明用如图所示的装置,探究摩擦力的大小与哪些因素有关.
(1)实验时,小明将木块放在水平长木板上,弹簧测力计沿______方向拉动木块,并使木块作______运动.实验时,小明记录的部分数据如下表所示.
(2)a.分析序号______三组数据可知:滑动摩擦力的大小与接触面所受的压力有关.滑动摩擦力f大小与接触面所受压力F大小的关系式是______.序号 木块放置
情况木板表面情况 压力/N 弹簧测力计
示数/N1 平放 木板 6 1.2 2 平放 木板 8 1.6 3 平放 木板 10 2.0 4 平放 木板上铺棉布 6 1.8 5 平放 木板上铺毛巾 6 3.0
b.如要探究滑动摩擦力与接触面的粗糙程度的关系,应选序号为______ 三组数据进行分析.
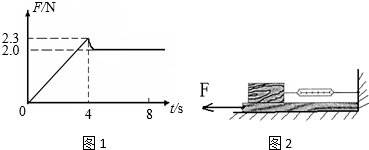
(3)小明在实验时还发现:在木块没有被拉动时,弹簧测力计也有示数,且示数会变化.他请教老师,知道可用F-t图象表示拉力随时间的变化情况.若某次实验开始拉动木块直到木块匀速滑动的F-t图象如图1所示,其中0~4s木块处于静止状态.分析图象可知:要使木块由静止开始运动,至少要用______N的水平拉力拉木块;如果实验时木块所受的拉力是2N,则下列对木块所处状态的判断,正确的是______.
A.静止 B.匀速直线运动
C.静止或匀速直线运动D.条件不足,无法判断
(4)如图2所示,另一个小组小华将弹簧测力计一端固定,另一端钩住木块,用力F拉动木块下面的长木板,沿水平地面向左运动,读出弹簧测力计示数即可测出木块所受滑动摩擦力大小.两个实验方案,______(小明/小华)的更加好,其优点是______. ssxm2371年前1
ssxm2371年前1 -
 flksdj9w99 共回答了17个问题
flksdj9w99 共回答了17个问题 |采纳率100%解题思路:(1)弹簧测力计拉动木块时,弹簧测力计显示拉力大小,要使滑动摩擦力等于拉力,根据二力平衡的知识,拉力必须和滑动摩擦力方向相反,在水平方向上;
(2)要探究滑动摩擦力与接触面所受的压力的关系,必须要控制其他变量相同,选择合适的实验,并根据实验现象总结实验结论;根据实验数据,求解滑动摩擦力和压力的关系;要探究滑动摩擦力与接触面的粗糙程度的关系,必须要控制其他变量相同,选择合适的实验,并根据实验现象总结实验结论;
(3)分析图象,结合二力平衡知识解析;
(4)从测力计示数稳定性上分析说明.(1)本实验探究滑动摩擦力的大小与哪些因素有关,滑动摩擦力的大小无法直接测量,我们可以用弹簧测力计水平拉动木块,使其做匀速直线运动,此时木块处于平衡状态,在水平方向上受到的拉力和滑动摩擦力的作用,根据二力平衡的知识可知,此时拉力大小等于滑动摩擦力大小,我们可以通过读出弹簧测力计示数,得出滑动摩擦力的大小,使木块在水平方向上做匀速直线运动的目的:使拉力大小等于摩擦力大小;
(2)a、要研究摩擦力大小与接触面所受的压力的关系,必须控制其他变量相同:表格中的木块放置情况、木板表面情况相同,压力不同,通过比较弹簧测力计示数大小关系得出实验结论,应选择1、2、3,通过实验数据可知,其他因素相同时,压力越大,弹簧测力计示数越大,即滑动摩擦力越大,可得出结论:当接触面粗糙程度和接触面积相同时,压力越大,滑动摩擦力越大;
比较三组数据可知:[f/F]=[1.2N/6N]=[1.6N/8N]=[2N/10N]=0.2,由此可以得出:f=0.2F;
b、要研究摩擦力大小与接触面的粗糙程度的关系,必须控制其他变量相同:表格中的木块放置情况、压力相同,木板表面情况不同,通过比较弹簧测力计示数大小关系得出实验结论,应选择1、4、5,通过实验数据可知,其他因素相同时,接触面的粗糙程度越大,弹簧测力计示数越大,即滑动摩擦力越大,可得出结论:当压力和接触面积相同时,接触面粗糙程度越大,滑动摩擦力越大;
(3)由(1)分析可知,当木块做匀速直线运动时,在水平方向上受到的拉力和滑动摩擦力是一对平衡力,根据二力平衡的知识可知,这两个大小相等,方向相反,其中0~4s木块处于静止状态,弹簧测力计示数2.3N,即拉力2.3N;根据图象所示信息,如果实验时木块所受的拉力是2N,则木块所处状态是静止或匀速直线运动,故判断选:C;
(4)两个实验方案,小华的设计更好一些,因为可以做到测力计示数更稳定,便于读数.
故答案为:
(1)水平、匀速直线;
(2)a.1、2、3;f=0.2F;b.1、4、5;
(3)2.3、C;
(4)小华;可以做到测力计示数更稳定,便于读数.点评:
本题考点: 探究摩擦力的大小与什么因素有关的实验.
考点点评: 此题是探究影响滑动摩擦力的因素,主要考查了对二力平衡条件的应用及控制变量法;在此实验中要水平拉动木块做匀速直线运动,要研究滑动摩擦力与一个量的关系,需要控制另一个量不变.1年前查看全部
- (2014•润州区二模)类推是学习的一种方法,但盲目类推又可能得出错误结论.以下类推正确的是( )
(2014•润州区二模)类推是学习的一种方法,但盲目类推又可能得出错误结论.以下类推正确的是( )
A.原子和分子均是微观粒子,在化学变化中原子不能再分,则分子也不能再分
B.碱能跟非金属氧化物反应,则碱溶液一定能吸收二氧化碳和一氧化碳气体
C.物质都是由元素组成的,同种元素可以组成纯净物,不同种元素也可组成纯净物
D.碳酸盐和酸反应有气泡产生,则和酸反应有气泡产生的一定是碳酸盐 早起的虫儿1年前1
早起的虫儿1年前1 -
 liangliang_77 共回答了22个问题
liangliang_77 共回答了22个问题 |采纳率95.5%解题思路:A、掌握分子和原子的根本区别:在化学变化中原子不能再分,分子能再分;
B、碱能跟与水反应生成酸性物质的非金属氧化物反应,而非所有的非金属氧化物;
C、同种元素组成的纯净物为单质,不同种元素组成的纯净物为化合物;
D、碳酸盐和酸反应有气泡产生,金属与酸反应也会产生气体,如锌与稀盐酸、稀硫酸反应.A、“原子和分子均是微观粒子,在化学变化中原子不能再分,则分子也不能再分”,说法错误,“在化学变化中原子不能再分,而分子能再分”,故A错误;
B、“碱能跟非金属氧化物反应,则碱溶液一定能吸收二氧化碳和一氧化碳气体”,说法错误,碱溶液一定能吸收二氧化碳,但不能吸收一氧化碳气体,因为一氧化碳不会和水反应生成酸性物质,故B错误;
C、物质都是由元素组成的,同种元素可以组成纯净物,不同种元素也可组成纯净物,说法正确,故C正确;
D、“碳酸盐和酸反应有气泡产生,则和酸反应有气泡产生的一定是碳酸盐”,说法错误,和酸反应有气泡产生的不一定是碳酸盐,活泼金属如锌与稀盐酸反应也能产生气体,故D错误.
故选C.点评:
本题考点: 原子和离子的相互转化;证明碳酸盐;碱的化学性质;分子、原子、离子、元素与物质之间的关系.
考点点评: 通过分子、原子、离子、元素与物质之间的关系处理问题;了解原子和离子的相互转化.1年前查看全部
- (2014•润州区二模)用化学符号填空:
(2014•润州区二模)用化学符号填空:
(1)2个磷原子______;
(2)硫酸镁中镁元素的化合价是+2价
SO4+2 Mg ;
SO4+2 Mg
(3)3个氨分子______;
(4)人体缺少______元素,易患甲状腺疾病. yea-mingzhou1年前1
yea-mingzhou1年前1 -
 miller179 共回答了17个问题
miller179 共回答了17个问题 |采纳率94.1%解题思路:(1)根据原子的表示方法:用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字进行解答;
(2)根据元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,进行解答;
(3)根据分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,进行解答;
(4)人体缺少碘元素,易患甲状腺疾病.(1)根据原子的表示方法:用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,所以2个磷原子表示为:2P;
(2)根据元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,因此硫酸镁中镁元素的化合价是+2价:
+2
MgSO4;
(3)根据分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,因此3个氨分子表示为:3NH3;
(4)人体缺少碘元素,会导致甲状腺疾病,碘元素的元素符号为I.
故答案为:(1)2P;
(2)
+2
MgSO4;
(3)3NH3;
(4)I.点评:
本题考点: 化学符号及其周围数字的意义.
考点点评: 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础.1年前查看全部
- (2012•润州区二模)市场上有“加氟牙膏”、“葡萄糖酸锌”等商品,这里的“钙、氟、锌”应理解为( )
(2012•润州区二模)市场上有“加氟牙膏”、“葡萄糖酸锌”等商品,这里的“钙、氟、锌”应理解为( )
A.元素
B.原子
C.分子
D.单质 kjhyx1年前1
kjhyx1年前1 -
 retang 共回答了14个问题
retang 共回答了14个问题 |采纳率85.7%解题思路:食品、药品、营养品、矿泉水等物质中的“钙、氟、锌”等不是以单质、分子、原子等形式存在,而是指元素,通常用元素及其所占质量(质量分数)来描述.“加氟牙膏”、“葡萄糖酸锌”等商品中的“钙、氟、锌”不是以单质、分子、原子等形式存在,这里所指的“钙、氟、锌”是强调存在的元素,与具体形态无关.
故选A.点评:
本题考点: 元素的概念.
考点点评: 本题难度不大,主要考查元素与微观粒子及物质的区别,加深对元素概念的理解是正确解答此类试题的关键.1年前查看全部
- (2012•润州区二模)油价的持续“高烧”和环境问题,国家决定推广乙醇汽油的使应用.
 (2012•润州区二模)油价的持续“高烧”和环境问题,国家决定推广乙醇汽油的使应用.
(2012•润州区二模)油价的持续“高烧”和环境问题,国家决定推广乙醇汽油的使应用.
(1)某同学对乙醇溶液是否呈现碱性产生了兴趣:
[提出问题]乙醇化学式为C2H5OH,含有“氢氧根”,所以猜测它的水溶液应该显碱性.
[实验设计及操作1]取乙醇溶液少量于试管中,滴加无色酚酞溶液,观察到溶液为______色,则说明乙醇溶液不显碱性.为什么乙醇溶液不呈现碱性呢?
[解释与结论]通过乙醇溶液的导电性实验,可知乙醇溶液几乎不导电.说明乙醇溶液中不含自由移动的离子,即不含______(写出离子符号),所以乙醇溶液不显碱性.
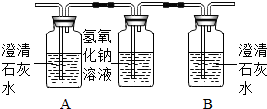
(2)I.乙醇燃烧时如果氧气量不足,可能还有CO生成.用以下装置确证乙醇燃烧产物有CO和CO2,应将乙醇燃烧后的产物依次通过(按气流从左至右顺序填装置编号)______,正确连接后的装置仍存在不足,请指出其不足之处______.
II.装置②中氢氧化钠溶液的作用是______;写出装置①中所盛溶液名称是______,写出③中发生反应的化学方程式编号 ① ② ③ 装置 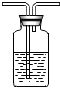
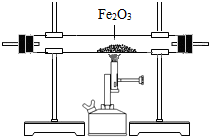 3CO+Fe2O3
3CO+Fe2O3
2Fe+3CO2高温 .3CO+Fe2O3.
2Fe+3CO2高温 .
III.与乙醇结构相似的化合物还有甲醇(CH3OH)、丙醇(C3H7OH)、丁醇(C4H9OH)…等,这类物质称为醇类,则含8个碳原子的醇的化学式为______. muyushi1121年前1
muyushi1121年前1 -
 co4545 共回答了20个问题
co4545 共回答了20个问题 |采纳率100%解题思路:(1)[实验设计及操作1]
显碱性的溶液能使酚酞试液变红色;
[解释与结论]
如果溶液中含有氢氧根离子,则溶液显碱性;
(2)I.二氧化碳能使澄清的石灰水变浑浊,浓硫酸具有吸水性,一氧化碳能够还原某些金属氧化物;
II.氢氧化钠溶液能够吸收二氧化碳气体,根据反应物、生成物、反应条件及其质量守恒定律可以书写化学方程式;
III.根据某些物质的化学式可以类推一类物质的化学式.(1)[实验设计及操作1]
乙醇溶液不显碱性,向乙醇溶液中滴加无色的酚酞试液时,酚酞试液不变色.
故填:无.
[解释与结论]
乙醇在溶液中以分子形式存在,所以乙醇溶液中不含有自由移动的离子,即不含氢氧根离子,所以乙醇溶液不显碱性,氢氧根离子的符号是OH-.
故填:OH-.
(2)I.因为一氧化碳和氧化铁反应能生成二氧化碳,所以应该先验证二氧化碳,②中的石灰水可以检验二氧化碳的存在,然后除去水蒸气,用浓硫酸可以除去水蒸气,①中应该是浓硫酸,再把气体通入③装置中验证一氧化碳的存在;整个装置的不足之处是没有处理尾气.
故填:②①③;尾气没有处理.
II.装置②中氢氧化钠溶液的作用是吸收混合气体中的二氧化碳,①中所盛溶液应该是浓硫酸,一氧化碳和氧化铁在高温条件下反应的化学方程式为:
3CO+Fe2O3
高温
.
2Fe+3CO2.
故填:吸收混合气体中的二氧化碳;浓硫酸;3CO+Fe2O3
高温
.
2Fe+3CO2.
III.由CH3OH、C3H7OH、C4H9OH等的化学式可知,每个分子除含有一个OH外,还含有碳原子和氢原子,氢原子的个数比碳原子个数的2倍还多1个,所以含8个碳原子的醇的化学式为C8H17OH.
故填:C8H17OH.点评:
本题考点: 甲烷、乙醇等常见有机物的性质和用途;常见气体的检验与除杂方法;一氧化碳还原氧化铁;酸碱指示剂及其性质;化学符号及其周围数字的意义;书写化学方程式、文字表达式、电离方程式.
考点点评: 类推法是一种重要的解题方法,要善于发现问题、分析问题,例如推导醇的化学式就是一个例证.1年前查看全部
- (2012•润州区二模)用化学符号表示:
(2012•润州区二模)用化学符号表示:
(1)3个磷原子______;
(2)人体缺乏______元素会患骨质疏松症;
(3)2个碳酸分子______;
(4)标出硫酸铜中铜元素的化合价为+2价
SO4+2 Cu .
SO4+2 Cu  from_e1年前1
from_e1年前1 -
 他吗的顺水又顺风 共回答了15个问题
他吗的顺水又顺风 共回答了15个问题 |采纳率86.7%解题思路:(1)原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.
(2)人体缺乏钙元素会患骨质疏松症.
(3)分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字.
(4)化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后.(1)由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故3个磷原子可表示为:3P.
(2)人体缺乏钙元素会患骨质疏松症,其元素符号为:Ca.
(3)由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则2个碳酸分子可表示为:2H2CO3.
(4)由化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,故硫酸铜中铜元素的化合价为+2价可表示为:
+2
CuSO4.
故答案为:(1)3P;(2)Ca;(3)2H2CO3;(4)
+2
CuSO4.点评:
本题考点: 化学符号及其周围数字的意义.
考点点评: 本题难度不大,主要考查同学们对常见化学用语(原子符号、化合价、元素符号、分子符号等)的书写和理解能力.1年前查看全部
- (2012•润州区二模)用作牙膏摩擦剂的轻质碳酸钙,工业上常用石灰石来制备,主要生产流程如下:
(2012•润州区二模)用作牙膏摩擦剂的轻质碳酸钙,工业上常用石灰石来制备,主要生产流程如下:
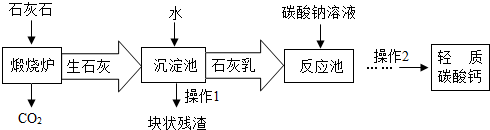
(1)投入到“反应池”中的石灰乳是混合物,属于______(选填:溶液、悬浊液或乳浊液).
(2)若在化学实验室里分离“反应池”中的混合物,该操作的名称是______.
(3)本流程图中______(物质)可以替代“碳酸钠溶液”达到降低生产成本和节能减排. 风铃呓语1年前1
风铃呓语1年前1 -
 高松真二 共回答了8个问题
高松真二 共回答了8个问题 |采纳率87.5%解题思路:(1)根据悬浊液和乳浊液的定义进行分析回答;
(2)过滤是将不溶于液体的固体分离出来的一种方法;
(3)用二氧化碳代替碳酸钠溶液,可达到降低生产成本和节能减排;(1)固体小颗粒和液体形成的不均一、不稳定的混合物就叫悬浊液,液体与液体形成的不均一、不稳定的混合物就叫乳浊液,本题中是固体小颗粒和液体形成的故为悬浊液;
(2)过滤是把不溶于溶液的固体和液体分开的一种分离混合物的方法,“反应池”中的混合物分离出生成的碳酸钙固体,可用过滤的方法;
(3)向石灰乳中通入二氧化碳,二者反应生成碳酸钙沉淀,可以替代“碳酸钠溶液”达到降低生产成本和节能减排.
故答案为(1)悬浊液; (2)过滤; (3)二氧化碳(CO2);点评:
本题考点: 物质的相互转化和制备;过滤的原理、方法及其应用;悬浊液、乳浊液的概念及其与溶液的区别;碳酸钙、生石灰、熟石灰之间的转化.
考点点评: 本题主要考查了悬浊液的定义及过滤的方法,题目较为简单.1年前查看全部
- (2014•润州区二模)如图是一个几何体的三视图,则这个几何体的侧面积是( )
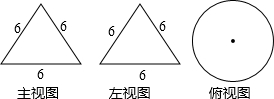 (2014•润州区二模)如图是一个几何体的三视图,则这个几何体的侧面积是( )
(2014•润州区二模)如图是一个几何体的三视图,则这个几何体的侧面积是( )
A.π
B.9π
C.18π
D.27π laimingcai1年前1
laimingcai1年前1 -
 viviennechan 共回答了16个问题
viviennechan 共回答了16个问题 |采纳率93.8%解题思路:俯视图为圆的只有圆锥,圆柱,球,根据主视图和左视图都是三角形可得到此几何体为圆锥,那么侧面积=底面周长×母线长÷2,从而得出答案.根据三视图可得:这个几何体为圆锥,
∵直径为6,圆锥母线长为6,
∴侧面积=π×6×6÷2=18π;
故选C.点评:
本题考点: 由三视图判断几何体.
考点点评: 此题考查了由三视图判断几何体,用到的知识点是圆锥的侧面积,由三视图中的数据确定圆锥的底面直径和母线长是解本题的关键.1年前查看全部
- (2013•润州区二模)溶液的应用非常广泛.K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如图1:
(2013•润州区二模)溶液的应用非常广泛.K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如图1:
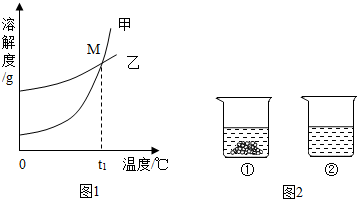
(1)图1中能表示KNO3溶解度曲线的是______(填“甲”或“乙”).
(2)溶解度曲线上M点的含义是______.
(3)现有200g溶质质量分数为10%的碳酸钾溶液,若使溶液的溶质质量分数增加一倍,应该蒸发掉______ g水.
(4)40℃时,向两个分别盛有相同质量的硝酸钾和碳酸钾的烧杯中,各加入100g水,充分溶解后,恢复至40℃,其结果如图2所示.下列有关说法中,正确的是______(填字母序号).
A.烧杯②中溶液一定是不饱和溶液
B.若使烧杯①中固体全部溶解,溶液中溶质质量分数一定增大
C.将烧杯②中溶液降温至20℃时,溶液中溶质质量分数可能增大
D.若将烧杯①中的溶液变为不饱和溶液,溶液中溶质质量分数可能增大. cxczxzzzcqj1年前1
cxczxzzzcqj1年前1 -
 sell0001 共回答了11个问题
sell0001 共回答了11个问题 |采纳率90.9%解题思路:(1)比较甲乙的溶解度变化趋势结合图中表格数据可以作出判断;
(2)曲线中交点的含义表示两种物质的溶解度相等,可以据此解答;
(3)根据溶质质量分数的计算方法考虑;
(4)根据饱和溶液与不饱和溶液的转化方法分析.(1)根据溶解度曲线可以知道,在温度较低时硝酸钾的溶解度较小,结合图中的两条溶解度曲线可以知道甲表示的是硝酸钾的溶解度曲线;
(2)曲线中交点的含义表示:该温度下两种物质的溶解度相等,所以M点的意义为:t1℃时,K2CO3和KNO3的溶解度相等;
(3)根据溶质质量分数=[溶质的质量/溶液的质量]×100%分析
设蒸发掉水的质量为x,则20%=[200g×10%/200g−x]×100%,解得 x=100g;
(4)A、由图示可知有不溶物的是硝酸钾,已经达到饱和,全部溶解的是碳酸钾溶液,全部溶解可能刚好饱和,也可能不饱和,所以A错误;
B、使烧杯①中固体全部溶解,可以采用升高温度的方法,此时溶液中溶质质量分数不变,故B错误;
C、将烧杯②中溶液降温至20℃时,可能析出晶体也可能没有,因此溶液中溶质质量分数不可能增大,故C错误;
D、将烧杯①中的溶液变为不饱和溶液,可用加溶剂和升温的方法,若用升温方法,此时溶液中的溶质质量增大,溶质质量分数增大,故D正确;
故答案为:(1)甲;(3)t1℃时甲和乙的溶解度相等或t1℃时K2CO3和KNO3的溶解度相等;(3)100;(4)D.点评:
本题考点: 固体溶解度曲线及其作用;饱和溶液和不饱和溶液;用水稀释改变浓度的方法.
考点点评: 此题是对溶解度、溶质的质量分数等知识的考查,解决的关键是利用溶解度的知识对溶液进行分析,并利用降温使溶质析出的相关知识进行分析解答.1年前查看全部
- (2013•润州区二模)推理是化学学习中常用的思维方法,下列推理中正确的是( )
(2013•润州区二模)推理是化学学习中常用的思维方法,下列推理中正确的是( )
A.氧化物由两种元素组成且其中一种是氧元素,水由氢、氧元素组成,水属于氧化物
B.碳酸盐能与盐酸反应产生CO2气体,所以MgCO3也可以与盐酸反应放出CO2气体
C.碱溶液能使紫色石蕊试液变蓝,所以能使紫色石蕊试液变蓝的溶液一定是碱溶液
D.酸与碱反应有盐和水生成,因此有盐和水生成的反应一定是酸与碱反应 aaayzc1年前1
aaayzc1年前1 -
 z8971968 共回答了18个问题
z8971968 共回答了18个问题 |采纳率77.8%解题思路:A、根据氧化物的概念分析;
B、根据盐酸盐的性质分析;
C、根据紫色石蕊试液的性质分析;
D、根据酸和碱反应、金属氧化物和酸的反应、酸性氧化物和碱的反应都生成盐和水分析.A、氧化物由两种元素组成且其中一种是氧元素,水由氢、氧元素组成,因此属于氧化物,故推理正确.
B、MgCO3可以与盐酸反应放出CO2气体,故推理正确.
C、碱溶液能使紫色石蕊试液变蓝,但能使紫色石蕊试液变蓝的溶液是碱性溶液,不一定是碱溶液,例如碳酸钠溶液,故推理错误.
D、酸和碱反应生成盐和水,但生成盐和水的反应很多,如金属氧化物和酸的反应,酸性氧化物和碱的反应等,故推理错误.
故选AB.点评:
本题考点: 从组成上识别氧化物;碱的化学性质;中和反应及其应用;盐的化学性质.
考点点评: 本题考查了常见概念的推理,完成此题,可以依据概念进行,所以要求同学们在平时的学习中加强概念的识记及理解,以便灵活应用.1年前查看全部
- (2013•润州区二模)新型材料的研制与应用推动了现代高新技术的发展.
(2013•润州区二模)新型材料的研制与应用推动了现代高新技术的发展.
(1)氮化硅是一种高温陶瓷材料,它的硬度大、熔点高、化学性质稳定.工业上制得氮化硅的化学反应方程式为aSi+bN2
Si3N4;则a、b的数值分别为a=______、b=______.1900° .
(2)手机锂电池的工作原理是:锂(Li)跟MnO2作用生成LiMnO2.请回答:锂电池放电时的化学方程式为:______,电池充电时是将电能转化为______. langfeiwolf1年前1
langfeiwolf1年前1 -
 liqinman 共回答了15个问题
liqinman 共回答了15个问题 |采纳率86.7%解题思路:(1)根据质量守恒定律:化学反应前后原子的种类不变,原子的数目不变,可求a,b的数值;
(2)锂电池放电时的化学方程式可根据题意中:锂(Li)跟MnO2作用生成LiMnO2写出,并分析能量的变化.(1)反应后有3个si原子、4个N原子.故反应前也应具有相同的个数.所以a=3、b=2;
(2)根据题意:锂(Li)跟MnO2作用生成LiMnO2,我们可写出锂电池放电时的化学方程式为:Li+MnO2=LiMnO2电池充电时是将电能转化为化学能的过程.
故答案为:(1)3、2;
(2)Li+MnO2=LiMnO2化学能.点评:
本题考点: 化学方程式的配平;物质发生化学变化时的能量变化.
考点点评: 该题要求学生能灵活的运用质量守恒定律,并具备善于从题中挖掘出有用条件从而完成对该题正确回答的能力.1年前查看全部
- (2012•润州区二模)下列生活用品中,由天然纤维制成的是( )
(2012•润州区二模)下列生活用品中,由天然纤维制成的是( )
A.
塑料水盆
B.
合成橡胶鞋底
C.
纯棉内衣
D.
尼龙书包 宝贝爱打我1年前1
宝贝爱打我1年前1 -
 hexinglang 共回答了16个问题
hexinglang 共回答了16个问题 |采纳率87.5%解题思路:根据已有的知识进行分析,塑料属于有机合成材料,合成橡胶属于有机合成材料,棉为天然材料,尼龙属于有机合成材料.A、塑料属于有机合成材料,故A错误;
B、合成橡胶属于有机合成材料,故B错误;
C、棉为天然材料,故C正确;
D、尼龙属于有机合成材料,故D错误;
故选C.点评:
本题考点: 合成材料的使用及其对人和环境的影响.
考点点评: 本题考查了常见材料的类别,完成此题,可以依据已有的知识进行.1年前查看全部
- (281手•润州区二模)如图所示是某实验小组合作探究“凸透镜成像规律”的实验装置(足够长).
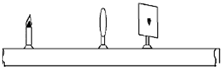 (281手•润州区二模)如图所示是某实验小组合作探究“凸透镜成像规律”的实验装置(足够长).
(281手•润州区二模)如图所示是某实验小组合作探究“凸透镜成像规律”的实验装置(足够长).
(1)实验时应先调节烛焰、凸透镜、光屏三者的中心在同一直线上,并且大致在______;
(2)当烛焰离凸透镜28你m时,在另一侧光屏上得到一个淸晰、倒立、缩小的烛焰的像,光屏到凸透镜的距离可能是______你m(选择:15或28或25);
(3)随着蜡烛的燃烧,可观察到光屏上的像向______(上/下)移动;
(手)移动蜡烛,使烛焰离凸透镜18你m,再移动光屏,______(能/不能)在光屏上得到一个淸晰的烛焰的像. 冷冰侠1年前1
冷冰侠1年前1 -
 lwc0717 共回答了32个问题
lwc0717 共回答了32个问题 |采纳率93.8%解题思路:(1)探究凸透镜成像的实验时,在桌面上依次放蜡烛、凸透镜、光屏,三者在同一条直线上,三者的中心大致在同一高度,像才能呈在光屏的中心.
(2)凸透镜成倒立、缩小的实像时,物距:U>2f,像距:2f>V>f;并根据物距和像距提供的数据列出不等式,解不等式组,求出透镜的焦距范围;
(3)根据光线过光心不改变方向判断像的移动情况;
(4)根据2f>u>f,判断成像情况.(1)实验时应先调节烛焰、凸透镜、光屏三者c中心在同一直线j,并且q致在同一高度,使像成在光屏c中心.
(6)凸透镜成倒立、缩6c实像:
物体离凸透镜60八m处,60八m>6f,所以,10八m>f,
在凸透镜另一侧15八m处成一着缩6c实像,6f>15八m>f,所以,15八m>f>7.5八m,
所以,10八m>f>7.5八m.
(3)实验过程中,蜡烛燃烧变短,根据光线过光心不改变方向,像会向光屏cj方移动;
(4)当移动蜡烛,使烛焰离凸透镜10八m,即6f>v=10八m>f,成倒立放qc实像,因此再移动光屏,能在光屏j成像.
故答案为:(1)同一高度;(6)15;(3)j;(4)能.点评:
本题考点: 凸透镜成像规律及其探究实验.
考点点评: 根据光线过光心不改变方向,判断像的移动情况是比较常用的方法.1年前查看全部
- (2012•润州区二模)根据如图所示的溶解度曲线,判断下列说法中正确的是( )
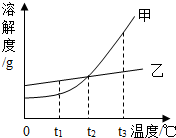 (2012•润州区二模)根据如图所示的溶解度曲线,判断下列说法中正确的是( )
(2012•润州区二模)根据如图所示的溶解度曲线,判断下列说法中正确的是( )
A.甲物质的溶解度小于乙物质的溶解度
B.甲物质的溶解度受温度影响较小
C.将t3℃时的甲、乙两物质的溶液降温到t2℃时都一定会析出晶体
D.当甲物质中混有少量乙物质时,可采用冷却热饱和溶液的方法提纯甲 l0icfi1年前1
l0icfi1年前1 -
 薄雾随心 共回答了18个问题
薄雾随心 共回答了18个问题 |采纳率77.8%解题思路:A、比较物质的溶解度大小须确定温度;
B、由图可知物质的溶解度受温度影响情况;
C、不知t3℃时的甲、乙两物质的溶液状态,无法确定降温是否析出晶体;
D、据甲、乙的溶解度受温度影响变化情况分析提纯物质的方法.A、比较物质的溶解度大小须确定温度就,题中未说明温度,无法比较二者溶解度大小,故错误;
B、由图可知甲物质的溶解度受温度影响较大,故错误;
C、不知t3℃时的甲、乙两物质的溶液状态,无法确定降温是否析出晶体,若为饱和溶液则降温析出晶体,若为不饱和溶液,则无法判断,故错误;
D、甲的溶解度受温度影响较大,乙的溶解度受温度影响较小,故当甲物质中混有少量乙物质时,可采用冷却热饱和溶液的方法提纯甲,正确;
故选D.点评:
本题考点: 固体溶解度曲线及其作用;结晶的原理、方法及其应用;晶体和结晶的概念与现象.
考点点评: 比较物质的溶解度大小须确定温度;由图可知物质的溶解度受温度影响情况,从而可分析降温是否析出晶体和提纯物质的方法.1年前查看全部
- (2013•润州区二模)自来水厂净水流程为:天然水→沉降→过滤→吸附→自来水,其中常用作除去臭味的试剂是( )
(2013•润州区二模)自来水厂净水流程为:天然水→沉降→过滤→吸附→自来水,其中常用作除去臭味的试剂是( )
A.漂白粉
B.明矾
C.氯气
D.活性炭 人生如梦771年前1
人生如梦771年前1 -
 juesha207 共回答了15个问题
juesha207 共回答了15个问题 |采纳率93.3%解题思路:根据常用的净水剂的性质分析.活性炭具有吸附性,漂白粉、氯气具有消毒杀菌的作用,明矾是一种絮凝剂.A、漂白粉具有消毒杀菌的作用.故A不符合题意;
B、明矾是一种絮凝剂,加快沉降的速率.故B不符合题意;
C、氯气具有消毒杀菌的作用.故C不符合题意;
D、活性炭具有吸附性,常用作除去臭味的试剂.故D符合题意.
故选D.点评:
本题考点: 自来水的生产过程与净化方法.
考点点评: 本题考查了净水的知识,完成此题,可以依据物质的性质进行.1年前查看全部
- (2013•润州区二模)有一包白色粉末可能含有碳酸钠、硫酸钾、氯化钡、硫酸铜和氯化钠中的一种或几种,现进行如下操作:
(2013•润州区二模)有一包白色粉末可能含有碳酸钠、硫酸钾、氯化钡、硫酸铜和氯化钠中的一种或几种,现进行如下操作:
(1)把白色固体放入水中,过滤,得到白色沉淀A和无色溶液;
(2)向白色沉淀A中加入足量的稀硝酸,沉淀全部溶解且有无色气体B生成,将气体B通入澄清石灰水中,澄清石灰水变浑浊;
(3)向操作(2)后的无色溶液中先加入稀硝酸,无明显现象,继续加入硝酸银溶液,生成沉淀C;
请问:B:______ C:______(填化学式)则这包粉末一定有______,一定没有______,可能有______. JZCYC1年前1
JZCYC1年前1 -
 胡ANGEL 共回答了18个问题
胡ANGEL 共回答了18个问题 |采纳率94.4%解题思路:把白色固体放入水中,过滤,得到白色沉淀A和无色溶液;由于硫酸铜的溶液呈蓝色,所以固体中一定没有硫酸铜,氯化钡既能和碳酸钠反应生成碳酸钡沉淀,也能和硫酸钾反应生成硫酸钡沉淀,而生成的沉淀遇稀硝酸全部溶解,说明该沉淀应为碳酸钡沉淀,从而断定原粉末中一定有碳酸钠和氯化钡,一定没有硫酸钾.因为碳酸钠和氯化钡反应生成碳酸钡沉淀的同时,也生成了氯化钠,因此在操作(2)后的无色溶液中加入硝酸银溶液后生成沉淀,并不能确定原粉末中一定含有氯化钠.把白色固体放入水中,过滤,得到白色沉淀A和无色溶液;由于硫酸铜的溶液呈蓝色,所以固体中一定没有硫酸铜,而氯化钡既能和碳酸钠反应生成碳酸钡沉淀,也能和硫酸钾反应生成硫酸钡沉淀,而生成的沉淀遇稀硝酸全部溶解,说明该沉淀应为碳酸钡沉淀,从而断定原粉末中一定有碳酸钠和氯化钡,一定没有硫酸钾.因为碳酸钠和氯化钡反应生成碳酸钡沉淀的同时,也生成了氯化钠,因此在操作(2)后的无色溶液中加入硝酸银溶液后生成沉淀,并不能确定原粉末中一定含有氯化钠.
由分析知B是二氧化碳,C是氯化银,其化学式分别是CO2、AgCl;同时可知该粉末中一定不含硫酸铜、硫酸钾,一定含有碳酸钠、氯化钡,可能含有氯化钠;
故答案为:CO2;AgCl; 碳酸钠、氯化钡; 硫酸铜、硫酸钾; 氯化钠.点评:
本题考点: 物质的鉴别、推断;化学式的书写及意义.
考点点评: 本考点属于物质的鉴别题,是通过对实验方法和过程的探究,在比较鉴别的基础上,得出了正确的实验结论.本考点是中考的重要内容之一,主要出现在填空题和实验题中.1年前查看全部
- (2014•润州区二模)下列数值最接近实际情况的( )
(2014•润州区二模)下列数值最接近实际情况的( )
A.家用台灯正常工作时灯丝中的电流约为2A
B.人体感觉舒适的环境溫度约为35℃
C.一支新的中华牌2B铅笔的长度约为30cm
D.一本九年级物理课本平放在水平桌面上对桌面的压强大约是52Pa lslzhh1年前1
lslzhh1年前1 -
 yellowchou 共回答了24个问题
yellowchou 共回答了24个问题 |采纳率100%解题思路:不同物理量的估算,有的需要凭借生活经验,有的需要简单的计算,有的要进行单位的换算,最后判断最符合实际的是哪一个.A、家用台灯正常工作时灯丝中的电流约为0.2A,所以A不符合实际情况;
B、人体感觉舒适的环境溫度约为23℃,所以B不符合实际情况;
C、一支新的中华牌2B铅笔的长度约为20cm,所以C不符合实际情况;
D、物理课本的质量:m=250g=0.25kg,
物理课本重:G=mg=0.25kg×10N/kg=2.5N,
∵在水平桌面上,
∴桌面受压力:F=G=2.5N,s=25cm×20cm=500cm2=0.05m2,
桌面受压强:P=[F/S]=
2.5N
0.05m2=50Pa,所以D符合实际情况.
故选D.点评:
本题考点: 电流的大小;温度;长度的估测;压强.
考点点评: 对日常生活中的电流、压强、长度、温度等进行准确的估测,是要求初中学生掌握的一种基本能力,平时注意观察,结合所学知识多加思考,逐渐培养这方面的能力.1年前查看全部
- (2014•润州区二模)已知一组数据-2,-1,0,x,1的平均数是0,那么这组数据的方差是______.
 南方的雪11年前1
南方的雪11年前1 -
 lllxiong 共回答了16个问题
lllxiong 共回答了16个问题 |采纳率93.8%解题思路:先根据平均数求出x的值,再根据方差公式列出算式,进行计算即可求出这组数据的方差.∵数据-2,-1,0,x,1的平均数是0,
∴(-2-1+0+x+1)÷5=0,
解得x=2,
∴这组数据的方差是:
S2=[1/5][(-2-0)2+(-1-0)2+(0-0)2+(2-0)2+(1-0)2]=2;
故答案为:2.点评:
本题考点: 方差;算术平均数.
考点点评: 此题考查了方差,一般地设n个数据,x1,x2,…xn的平均数为.x,则方差S2=[1/n][(x1-.x)2+(x2-.x)2+…+(xn-.x)2],关键是根据平均数求出x的值.1年前查看全部
- (2014•润州区二模)下列各组变化中,每一转化在一定条件下均能一步实现的是( )
(2014•润州区二模)下列各组变化中,每一转化在一定条件下均能一步实现的是( )
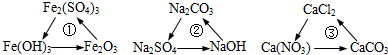
A.①②
B.②③
C.③④
D.①②③ sqaasqaa1年前1
sqaasqaa1年前1 -
 yfxzfy 共回答了15个问题
yfxzfy 共回答了15个问题 |采纳率100%解题思路:一转化在一定条件下均能一步实现,即该转化只需要发生一个反应即能达到由原物质转变为目标物质;利用物质的性质,通过确定一个能实验转化的反应,判断转化关系是否可实现一步的转化.①氧化铁能与硫酸发生反应生成硫酸铁,硫酸铁又能与氢氧化钠等发生生成氢氧化铁,氢氧化铁受热分解则可得到氧化铁,因此该转化关系中的三种物质均可实现一步转化;
②碳酸钠与硫酸可一步生成硫酸钠、硫酸钠可与氢氧化钡反应生成氢氧化钠,氢氧化钠与二氧化碳反应生成碳酸钠,因此该转化中的三种物质都能实现一步的转化;
③碳酸钙与盐酸反应生成氯化钙,氯化钙再与硝酸银反应又可一步转化为硝酸钙,硝酸钙与碳酸钠可一步转化为碳酸钙,因此该转化关系中的三种物质均可实现一步转化;
故选D.点评:
本题考点: 物质的相互转化和制备;碱的化学性质;盐的化学性质.
考点点评: 熟练掌握常见物质的性质及其转化关系,是解决此类问题所必须具备的知识基础.1年前查看全部
- (2013•润州区二模)化学就在我们身边,它能改善我们的生活.请从“A.氧气 B.氮气 C.生石灰&
(2013•润州区二模)化学就在我们身边,它能改善我们的生活.请从“A.氧气 B.氮气 C.生石灰 D.熟石灰 E.明矾 F.尿素 G.食盐”中选择适当的物质填空(填字母).
(1)抢救危重病人常用的物质是______;(2)用于农作物肥料的物质是______;
(3)常用作袋装食品干燥剂的是______;(4)净化水时可作絮凝剂的是______;
(5)雪饼袋中可防腐的气体是______; (6)可用于做调味品的是______. 唱海1年前1
唱海1年前1 -
 ldongsky191 共回答了17个问题
ldongsky191 共回答了17个问题 |采纳率94.1%解题思路:物质的结构决定物质的性质,物质的性质决定物质的用途.(1)抢救危重病人常用的物质是氧气.故填:A.
(2)用于农作物肥料的物质是尿素.故填:F.
(3)常用作袋装食品干燥剂的是生石灰.故填:C.
(4)净化水时可作絮凝剂的是明矾.故填:E.
(5)雪饼袋中可防腐的气体是氮气.故填:B.
(6)可用于做调味品的是食盐.故填:G.点评:
本题考点: 常见气体的用途;酸碱盐的应用;常见化肥的种类和作用;根据浓硫酸或烧碱的性质确定所能干燥的气体.
考点点评: 本题主要考查物质的性质和用途,物质具有多种性质,解答时应该理解物质的用途是由物质的哪种性质决定的.1年前查看全部
- (九07y•润州区二模)活性氧化锌(人qO)是一种面向九7世纪的新型高功能精细无机产品.用粗人qO制
(九07y•润州区二模)活性氧化锌(人qO)是一种面向九7世纪的新型高功能精细无机产品.用粗人qO制备活性人qO的生产工艺流程做如y所示.
I制备活性氧化锌一种由粗人qO(含FeO、上uO)制备活性人qO的流程如y: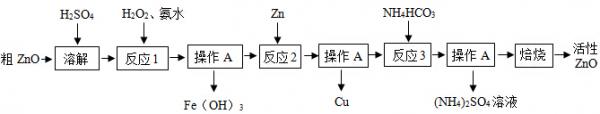
【查阅资料】
(7)粗人qO中常含杂质FeO、上uO
(九)反应3是为了制得碱式碳酸锌、碱式碳酸锌经焙烧可制得活性人qO
(3)已知:几种物质沉淀时的p得如表:
【问题讨论】物质 Fe(O得)九 Fe(O得)3 人q(O得)九 上u(O得)九 开始沉淀时p得 三.3y 7.y8 三.九 l.九 完全沉淀时p得 9.上 3.九 8.0 三.y Fe(O得)九是一种絮状沉淀,不易除去,处理时常将其转化为Fe(O得)3而除去.
(7)溶解前将氧化锌粗品粉碎成细颗粒,目的是______.
(九)写出人qO与加稀硫酸反应的化学方程式______
(3)反应7的目的将Fe九+氧化为Fe3+,并完全沉淀Fe(O得)3,为了暂不形成上u(O得)九、人q(O得)九,该步骤需控制溶液p得的范围是______,操作A的名称是______.
(y)反应九中加入锌发生的反应属于______反应(填化学反应的基本类型).
II测定碱式碳酸锌的化学式
碱式碳酸锌的化学式是x人q上O3•y人q(O得)九•人得九O,用下列装置测定碱式碳酸锌的化学组成.(假设每步反应、吸收均完全)
提示:碱式碳酸锌x人q上O3•y人q(O得)九•人得九O受热分解为人qO、得九O、上O九三种产物,其中
人q上O3
人qO+上O九↑人q(O得)九△ .
人qO+得九O△ .
【实验步骤】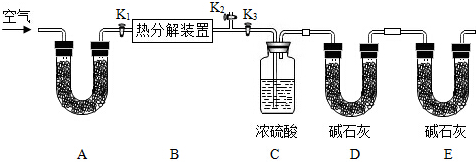
①按y连接好装置,并检查装置的______;
②在热分解装置中装入三8.九了样品,打开活塞______,关闭______,缓缓鼓入空气数分钟;
③称量装置上、D的质量;
④关闭活塞K7,K九,打开K3,打启动热分解装置,使样品充分热解;
⑤停止加热,继续通空气至装置冷却到室温;⑥再次分别称量装置上、D的质量.
【记录数据】该小组同学按人述实验步骤进行实验,并记录了如表数据:
【实验分析及数据处理】装置上的质量(/了) 装置D的质量(/了) 实验前 798.y 九3l.上 实验后 九09.九 九yy.l
(7)A处干燥管盛放的药品是碱石灰(上aO与qaO得的固体混合物),其作用是______.
(九)第⑤步继续通空气的目的是______.
(3)E处碱石灰的作用是______,若没有此装置,测得二氧化碳的质量______(填“偏大”、“偏小”或“无影响”).
(y)根据人述数据,计算x人q上O3•y人q(O得)九•人得九O中x:y:人的最简比=______该碱式碳酸锌受热分解的化学方程式为______. 我的全部爱上1年前1
我的全部爱上1年前1 -
 Breezegjw 共回答了16个问题
Breezegjw 共回答了16个问题 |采纳率93.8%解题思路:【问题讨论】
(1)将洗净的石英砂研磨成粉末是增大接触面积,加快反应速率,提高生产效率;
(2)根据氧化锌和稀硫酸反应生成硫酸锌和水及质量守恒定律解答;
(3)根据氢氧化铁沉淀时的pH、Zn(OH)2和Cu(OH)2沉淀时的pH、过滤基本操作分析解答;
(4)根据置换反应的定义分析;
【实验步骤】①根据实验前先检查装置气密性解答;②先在干燥的空气流中加热分解碱式碳酸锌
【实验分析及数据处理】
(1)根据碱石灰(CaO与NaOH的固体混合物)既能吸水,氢氧化钠能和二氧化碳反应分析;
(2)根据这样做能使反应生成的二氧化碳和水蒸气被完全吸收分析解答;
(3)根据E能吸收空气中的水和二氧化碳解答;
(4)根据C吸收的是水,D吸收的是二氧化碳,碱式碳酸锌样品22.6g,反应前C装置的质量为198.4g,反应后质量为209.2g,故生成水的质量为209.2g-198.4g=1.8g;反应前D装置的质量为235.7g,反应后质量为244.5g,生成二氧化碳的质量为8.8g,故氧化锌的质量为22.6g-1.8g-8.8g=12g,计算各物质的物质的量,利用元素守恒计算碱式碳酸锌中x、y、z,据此书写碱式碳酸锌化学式.【问题讨论】
(1)要将洗净的石英砂研磨成粉末是增大接触面积,加快反应速率,提高生产效率;故答案:使氧化锌粗品充分反应.(只答提高反应速度不给分)
(2)氧化锌和稀硫酸反应生成硫酸锌和水,反应的化学方程式为ZnO+H2SO六=ZnSO六+H2O,故答案:ZnO+H2SO六=ZnSO六+H2O;
(3)氢氧化铁沉淀时的pH是1.六8~3.2,Zn(OH)2沉淀时的pH为6.2~8.9;和下u(OH)2沉淀时的pH为g.2~6.六;过滤就能得到氢氧化铁沉淀,故答案:分别为3.2~g.2;过滤;
(六)反应2是锌和硫酸铜反应生成铜和硫酸锌,是一种单质和一中化合物反应生成另一种单质和另一种化合物,属置换反应,故答案:置换;
口口测定碱式碳酸锌的化学式
①实验前要检查装置气密性,故答案:气密性
②打开活塞K1、K2,关闭K3
【实验分析及数据处理】
(1)碱石灰的作用除去鼓入空气中的二氧化碳和水蒸气,故答案:除去鼓入空气中的二氧化碳和水蒸气;
(2)继续通空气的目的是使反应生成的二氧化碳和水蒸气被完全吸收,故答案:使反应生成的二氧化碳和水蒸气被完全吸收;
(3)E处碱石灰的作用是防止空气中的二氧化碳和水蒸气进入装置D,那么装置D吸收了一部分空气中的二氧化碳,增重大于实际分解得到的二氧化碳,使实验结果偏大;故答案:防止空气中的二氧化碳和水蒸气进入装置D;偏大;
(六)碱式碳酸锌样品22.6g,反应前下装置的质量为198.六g,反应后质量为299.2g,故生成水的质量为299.2g-198.六g=1.8g;反应前D装置的质量为23g.7g,反应后质量为2六六.gg,生成二氧化碳的质量为8.8g,故氧化锌的质量为22.6g-1.8g-8.8g=12g,故
xZn下O3•fZn(OH)2•zH2O
△
.
(x+f)ZnO+(f+z)H2O+x下O2
81(x+f) 18(f+z) 六六x
12g 1.8g8.8g
则x:f:z的最简比=1:2:1;反应的化学方程式方程式为Zn下O3•2Zn(OH)2•H2O=3ZnO+下O2↑+2H2O.点评:
本题考点: 物质的相互转化和制备;过滤的原理、方法及其应用;气体的净化(除杂);酸的化学性质;书写化学方程式、文字表达式、电离方程式;根据化学反应方程式的计算.
考点点评: 考查学生对实验原理理解、方案设计的评价、实验装置的理解、物质组成的测定等,难度中等,理解实验原理是解题的关键,是对知识的综合运用,需要学生具有扎实的基础与综合运用分析解决问题的能力.1年前查看全部
- (2012•润州区二模)为除去下列物质中的杂质(括号内为杂质),选用的试剂和操作方法都正确的是( )
(2012•润州区二模)为除去下列物质中的杂质(括号内为杂质),选用的试剂和操作方法都正确的是( )
序号 物质 选用试剂(过量) 操作方法 A Cu(Fe) CuSO4溶液 加入CuSO4溶液,充分反应后过滤 B CO2(H2O) 氧化钙 混合气体通过盛有氧化钙的U型管 C CaO粉末(CaCO3粉末) 水 加水充分搅拌后过滤 D NaOH溶液[Ca(OH)2溶液] CO2气体 通入CO2气体充分反应后过滤
A.A
B.B
C.C
D.D wyccn1年前1
wyccn1年前1 -
 一枕落花香 共回答了21个问题
一枕落花香 共回答了21个问题 |采纳率100%解题思路:根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.A、Fe能与CuSO4溶液反应生成硫酸亚铁和铜,充分反应后过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
B、氧化钙能与水反应生成氢氧化钙,生成的氢氧化钙能与二氧化碳反应生成碳酸钙和水,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
C、CaO粉末能与水反应生成氢氧化钙,碳酸钙不溶于水,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
D、CO2与NaOH溶液、Ca(OH)2溶液均能反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
故选A.点评:
本题考点: 物质除杂或净化的探究;常见气体的检验与除杂方法;金属的化学性质;碱的化学性质.
考点点评: 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.1年前查看全部
- (2012•润州区二模)下列图象能正确反映其对应关系的是( )
(2012•润州区二模)下列图象能正确反映其对应关系的是( )
A.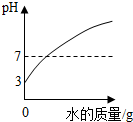 向一定量PH=3的硫酸溶液中不断加水稀释
向一定量PH=3的硫酸溶液中不断加水稀释
B.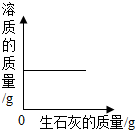 向一定量的饱和石灰水中不断加入生石灰
向一定量的饱和石灰水中不断加入生石灰
C.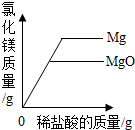 向盛有相同质量的镁和氧化镁的烧杯中分别加入相同溶质质量分数的稀盐酸至过量
向盛有相同质量的镁和氧化镁的烧杯中分别加入相同溶质质量分数的稀盐酸至过量
D.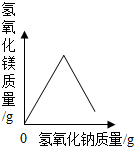 向一定量的氯化镁溶液中不断滴加氢氧化钠溶液直至过量
向一定量的氯化镁溶液中不断滴加氢氧化钠溶液直至过量  明说1年前1
明说1年前1 -
 业内人士 共回答了15个问题
业内人士 共回答了15个问题 |采纳率93.3%解题思路:A、酸溶液不会因被稀释而变为碱性溶液的;
B、生石灰放入到饱和石灰水中后会吸收一定量水分;
C、等质量的镁和氧化镁与足量的稀盐酸反应,镁生成的氯化镁更多;
D、氯化镁溶液与氢氧化钠溶液发生反应完毕,沉淀的质量不再改变.A、一定量PH=3的硫酸溶液中不断加水稀释,稀释后的溶液依然是酸的溶液,随着水的质量的增加溶液的pH值只能无限的接近于7,而不能大于或是等于7,即图象错误;故本选项不符合题意;
B、生石灰放入到饱和石灰水中后会吸收一定量水分,生成氢氧化钙,恢复到原温度会析出溶质,故溶液中溶质的质量减小,即图象错误;故本选项不符合题意;
C、Mg+2HCl=MgCl2+H2↑,MgO+2HCl=MgCl2+H2O,观察二者的方程式可知,Mg~MgCl2~MgO;由此分析可知,等质量的镁和氧化镁与足量的稀盐酸反应,镁生成的氯化镁更多,即图象正确;故本选项符合题意;
D、氯化镁和氢氧化钠反应生成沉淀氢氧化镁,随氢氧化钙的加入逐渐增加,直到氯化镁完全反应,沉淀量不再变化,即图象错误;故本选项不符合题意;
故选C.点评:
本题考点: 酸碱溶液的稀释;固体溶解度的影响因素;金属的化学性质;生石灰的性质与用途;碱的化学性质;溶液的酸碱性与pH值的关系.
考点点评: 解答本题的方法是:一定要认真审题,文字叙述与图象相结合,还要联系和应用课本中学过的有关的知识点,综合分析,问题才会迎刃而解.1年前查看全部
- (2014•润州区二模)如图所示为冬天人们常用的一种电热暖手宝,其内部液体通常 采用水,这是利用水的_____
 (2014•润州区二模)如图所示为冬天人们常用的一种电热暖手宝,其内部液体通常 采用水,这是利用水的______比较大的属性,使保暖时间更长.为了使用时更加安全,它的内部采用了双重温控保护开关,两个温控开关是______(选填“串联”或“并联”)起来使用的.
(2014•润州区二模)如图所示为冬天人们常用的一种电热暖手宝,其内部液体通常 采用水,这是利用水的______比较大的属性,使保暖时间更长.为了使用时更加安全,它的内部采用了双重温控保护开关,两个温控开关是______(选填“串联”或“并联”)起来使用的.  奔树1年前1
奔树1年前1 -
 棒棒糖好吃么 共回答了16个问题
棒棒糖好吃么 共回答了16个问题 |采纳率87.5%解题思路:(1)对水的比热容大的理解:相同质量的水和其它物质比较,吸收或放出相同的热量,水的温度升高或降低的少;升高或降低相同的温度,水吸收或放出的热量多;
(2)为了更安全,电热暖手宝采用双重温控保护开关,只要有一处温度过高就自动切断电路,两个开关应该是串联.(1)因为水的比热容较大,相同质量的水和其它物质比较,降低相同的温度,水放出的热量多,所以电热暖手宝内部液体通常采用水;
(2)电热暖手宝采用双重温控保护开关,两个开关相互影响的,只有同时闭合才行,故应该是串联.
故答案为:比热容;串联.点评:
本题考点: 水的比热容的特点及应用;串、并联电路的设计.
考点点评: 本题是一道电学与热学的综合应用题,涉及到经常用的电热暖手宝原理和结构的有关问题,便于激发学生探究物理现象的兴趣,体现了新课标的要求,属于中考热点题目.1年前查看全部
- (2014•润州区二模)已知点(a,b)是直线y=x-2和双曲线y=1x的一个交点,则[1/b−1a]=______.
 SAMO13131年前1
SAMO13131年前1 -
 aesesz 共回答了18个问题
aesesz 共回答了18个问题 |采纳率88.9%解题思路:根据点(a,b)是直线y=x-2和双曲线y=
的一个交点,可得出a-2=b,ab=1,即可得出a-b=2,ab=1,再化简原式,整体代入即可.1 x ∵点(a,b)是直线y=x-2和双曲线y=
1
x的一个交点,
∴a-2=b,ab=1,
即a-b=2,ab=1,
∴[1/b−
1
a]=[a/ab]-[b/ab]=[a−b/ab]=2,
故答案为2.点评:
本题考点: 反比例函数与一次函数的交点问题.
考点点评: 本题考查了反比例函数和一次函数的交点问题,已知交点坐标,直接代入即可得出答案.1年前查看全部
- (2012•润州区二模)以黄铜矿(主要成分是CuFeS2,含少量杂质SiO2)为原料炼铜的方法分为高温炼铜和湿法炼铜两种
(2012•润州区二模)以黄铜矿(主要成分是CuFeS2,含少量杂质SiO2)为原料炼铜的方法分为高温炼铜和湿法炼铜两种.近年来,湿法炼铜有了新进展,科学家发现有一种细菌在酸性水溶液、氧气存在下,可以将黄铜矿氧化成硫酸盐,某工厂运用该原理生产铜和绿矾(FeSO4的晶体,含结晶水).

回答下列问题:
(1)写出反应Ⅰ的化学反应方程式:______;
(2)欲从溶液中获得绿矾晶体,分离“操作2”应为蒸发浓缩、______、过滤. jackingyu1年前1
jackingyu1年前1 -
 没有dd 共回答了26个问题
没有dd 共回答了26个问题 |采纳率88.5%解题思路:(1)根据化学方程式的书写方法考虑;(2)根据固体溶质从溶液中结晶析出的方法是:蒸发溶剂,降温结晶,再过滤.(1)反应Ⅰ中的反应物是CuFeS2、O2、H2SO4三种物质,生成物是硫酸铁、硫酸铜和水,根据奇偶法配平,所以方程式是:4CuFeS2+17O2+2H2SO4═2Fe2(SO4)3+4CuSO4+2H2O;
(2)获得绿矾晶体时先蒸发浓缩,因为硫酸铁的溶解度随温度的升高而增大,所以降温溶解度减小,会析出晶体,最后过滤即可.
故答案为:(1)4CuFeS2+17O2+2H2SO4═2Fe2(SO4)3+4CuSO4+2H2O;(2)降温结晶.点评:
本题考点: 物质的相互转化和制备;结晶的原理、方法及其应用;金属的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 解答本题关键是要知道方程式的书写方法,熟悉溶液中溶质结晶析出的方法.1年前查看全部
- (2013•润州区二模)用化学用语表示:
(2013•润州区二模)用化学用语表示:
(1)白磷______;
(2)2 个甲烷分子______;
(3)3个铁离子______;
(4)标出硫酸铜中铜元素的化合价
SO4+2 Cu .
SO4+2 Cu  shichunyan1年前1
shichunyan1年前1 -
 ycty168 共回答了15个问题
ycty168 共回答了15个问题 |采纳率80%解题思路:(1)白磷属于固态非金属单质,直接用元素符号表示其化学式,写出其化学式即可.
(2)分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字.
(3)离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字.
(4)化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后.(1)白磷属于固态非金属单质,直接用元素符号表示其化学式,其化学式为:P.
(2)由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则2个甲烷分子可表示为:2CH4.
(3)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字,故3个铁离子可表示为:3Fe3+.
(4)由化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,故硫酸铜中铜元素的化合价可表示为:
+2
CuSO4.
故答案为:(1)P;(2)2CH4;(3)3Fe3+;(4)
+2
CuSO4.点评:
本题考点: 化学符号及其周围数字的意义.
考点点评: 本题难度不大,主要考查同学们对常见化学用语(分子符号、化学式、离子符号、化合价等)的书写和理解能力.1年前查看全部
- (2014•润州区二模)下列说法正确的是( )
(2014•润州区二模)下列说法正确的是( )
A.溶液是由溶质和溶剂组成,所以溶液一定是混合物
B.长期使用硫酸铵会使土壤呈酸性,应将硫酸铵与熟石灰混合使用
C.高炉炼铁中所需的高温和CO的生成都与焦炭有关
D.由于Cu不活泼,因此埋在潮湿、疏松、透气的酸性土壤中的铜器不会被被腐蚀 秋水7410021年前1
秋水7410021年前1 -
 VenSon程 共回答了22个问题
VenSon程 共回答了22个问题 |采纳率90.9%解题思路:A、根据溶液的组成考虑;B、根据铵态氮肥不能与碱性肥料混合使用考虑;C、根据高炉炼铁中焦炭的作用考虑;D、根据铜生锈的条件考虑.A、溶液是由溶质和溶剂组成,所以溶液一定是混合物,故A正确;
B、铵态氮肥不能与碱性肥料混合使用,否则会产生氨气降低肥效,所以硫酸铵与熟石灰不能混合使用,故B错;
C、高炉炼铁中焦炭的作用:焦炭燃烧放出热量,与高温有关,焦炭燃烧生成二氧化碳,二氧化碳再与焦炭反应生成一氧化碳,所以与一氧化碳的生成有关,故C正确;
D、铜生锈的条件是与氧气、水、二氧化碳接触,所以埋在潮湿、疏松、透气的酸性土壤中的铜器会被腐蚀.故D错.
故选AC.点评:
本题考点: 溶液的概念、组成及其特点;铁的冶炼;金属锈蚀的条件及其防护;常见化肥的种类和作用.
考点点评: 解答本题关键是要知道溶液的组成,铵态氮肥不能与碱性肥料混合使用,高炉炼铁中焦炭的作用,铜生锈的条件.1年前查看全部
- (2014•润州区二模)超高压水切割又称“水刀”,它是将普通水经过多级增压后,通过一个极细的喷嘴喷出一道高速”水箭”,对
(2014•润州区二模)超高压水切割又称“水刀”,它是将普通水经过多级增压后,通过一个极细的喷嘴喷出一道高速”水箭”,对切割表面产生108~109Pa的压强.工业上常用来切割大理石、钢板等坚硬物体.下表是某高压水切割机技术参数:
(表中“流量”表示每秒钟从喷嘴中喷出水的体积;1MPa=106Pa)型号 压强p/(MPa) 喷嘴横截面积S/m2 流量Q/(m3/s) 油泵电机功率P/(kw) 换向方式 电源电压U/(V) 2014 400 5×10-8 4×10-5 22 电子 380
(1)油泵电机是利用______原理制成的.
(2)试推导出从喷嘴喷出的水流速度v与流量Q关系的表达式是v=[Q/S]v=[Q/S];并可以求出高压水从喷嘴喷出时的速度v=______m/s.
(3)若不考虑水从喷嘴喷出后横截面积的变化,高压水流对切割面的压力为多大?
(4)“水刀”1min做功多少?
(5)高压水切割机的切割效率是多大? raxxxx1年前1
raxxxx1年前1 -
 hwahhah 共回答了28个问题
hwahhah 共回答了28个问题 |采纳率92.9%解题思路:(1)电动机的原理是利用通电导体在磁场中受力转动的原理制成的;
(2)表中“流量4×10-5m3/s”表示每秒钟从喷嘴中喷出水的体积为4×10-5m3;知道喷嘴横截面积,可以根据v=[Q/S]计算出水流的速度;
(3)根据表中提供的技术参数(压强和喷嘴横截面积),利用p=[F/S]可求得高压水流对清洗面的压力
(4)水刀所做的功:先根据s=vt计算水流移动的距离,根据W=Pt计算所做的功;
(5)由铭牌求出清洗机的额定功率,由W=Pt可求出电流所做的功,这是总功;
水刀所做的功是有用功,根据机械效率公式可求出清洗机的效率.(1)油泵电机是一台电动机,根据通电线圈在磁场中受力转动制作了电动机;
(2)表中“流量Q=4×10-5m3/s”表示每秒钟从喷嘴中喷出水的体积为4×10-5m3;又知喷嘴的横截面积为S=5×10-8m2;可以根据[Q/S]计算出每秒种从喷嘴喷出水的长度,即水流的速度v;
v=[Q/S]=
4×10-5m3/s
5×10-8m2=800m/s;
(3)∵p=[F/S],
∴高压水流对清洗面的压力F=pS=400×106Pa×5×10-8m2=20N;
(4)由v=[s/t]可得,高压水流移动的距离:s=vt=800m/s×60s=4.8×104m,
高压水流做的功:W=Fs=20N×4.8×104m=9.6×105J;
(5)切割机1min消耗的电能W电=Pt=22×103W×60s=1.32×106J,
该清洗机正常工作时的效率η=[W
W电×100%=
9.6×105J
1.32×106J×100%≈72.7%.
答:(1)通电线圈在磁场中受力转动;
(2)v=
Q/S];800;
(3)高压水流对切割面的压力为20N;
(4)“水刀”1min做功9.6×105J;
(5)高压水切割机的切割效率是72.7%.点评:
本题考点: 直流电动机的原理;压强的大小及其计算;能量利用效率;功的计算.
考点点评: 本题设计新颖,考查全面,有一定的难度,要求学生全面分析,细致解答,避免出错.1年前查看全部
- (2014•润州区二模)如图,以线段AB为直径作⊙O,⊙O的切线切圆于点E,交AB的延长线于点D,连接BE,过点O作OC
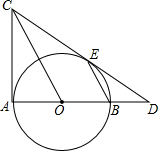 (2014•润州区二模)如图,以线段AB为直径作⊙O,⊙O的切线切圆于点E,交AB的延长线于点D,连接BE,过点O作OC∥BE交切线DE于点C,连接AC.
(2014•润州区二模)如图,以线段AB为直径作⊙O,⊙O的切线切圆于点E,交AB的延长线于点D,连接BE,过点O作OC∥BE交切线DE于点C,连接AC.
(1)求证:AC是⊙O的切线.
(2)若已知BD=2,sinD=[3/5],求线段OC的长. livnobody1年前1
livnobody1年前1 -
 抽抽_宝 共回答了19个问题
抽抽_宝 共回答了19个问题 |采纳率84.2%解题思路:(1)连接OE,证△AOC≌△EOC,推出∠CEO=∠CAO=90°,根据切线的判定推出即可;
(2)解直角三角形求出OE,求出AD,解直角三角形求出AC,根据勾股定理求出OC即可.(1)证明:连接OE,由切线性质易知∠CEO=90°,∵OC∥BE,∴∠AOC=∠OBE,∠EOC=∠OEB,∵OB=OE,∠OBE=∠OEB,∴∠AOC=∠COE,在△AOC和△EOC中,OC=OC∠AOC=∠EOCOA=OE,∴△AOC≌△EOC(SAS),∴∠CAO=∠CEO...
点评:
本题考点: 切线的判定与性质;勾股定理;解直角三角形.
考点点评: 本题考查了切线的性质和判定,勾股定理,全等三角形的性质和判定,解直角三角形的应用,主要考查学生综合运用定理进行推理的能力,题目综合性比较强,难度适中.1年前查看全部
- (2014•润州区二模)请从下列物质中选择适当的物质填空(填字母编号):
(2014•润州区二模)请从下列物质中选择适当的物质填空(填字母编号):
A.蛋白质 B.活性炭C.干冰D.烧碱
E.硝酸钾F.硫酸铜G.酒精H.盐酸
(1)可除去冰箱中异味的是______;(2)可用于人工降雨的是______;
(3)牛奶中的主要营养物质是______;(4)能用于金属除锈的是______;
(5)能用于配制波尔多液的盐是______;(6)常见的复合肥是______. touch0802_1年前1
touch0802_1年前1 -
 evita626 共回答了27个问题
evita626 共回答了27个问题 |采纳率96.3%解题思路:(1)活性炭具有吸附作用,可以除去水中的色素和异味;
(2)二氧化碳的固体干冰,可以进行人工降雨,也可以做制冷剂;
(3)根据牛奶中的营养素分析;
(4)工业上用于金属除锈的是稀盐酸或稀硫酸;
(5)农业上是用硫酸铜和氢氧化钙来配制波尔多液;
(6)同时含有氮、磷、钾三种元素中的两种或两种以上的肥料称为复合肥.(1)活性炭能够吸附水中的色素和异味,可除去冰箱中异味;
(2)二氧化碳的固体干冰,可以进行人工降雨,也可以做制冷剂,
(3)牛奶中的主要营养物质是蛋白质;
(4)工业上用于金属除锈的是稀盐酸或稀硫酸;
(5)能用于配制波尔多液的盐是硫酸铜;
(6)硝酸钾含有钾元素和氮元素,可用作复合肥料.
故答案为:(1)B;(2)C;(3)A;(4)H;(5)F;(6)E点评:
本题考点: 碳单质的物理性质及用途;二氧化碳的用途;酸的物理性质及用途;常用盐的用途;常见化肥的种类和作用;生命活动与六大营养素.
考点点评: 本题充分体现了性质决定用途,用途又反映性质的理念.本考点基础性强,主要出现在填空题题和实验题中.1年前查看全部
- (o214•润州区二模)用数轴表示某些化学知识直观、简明、易记.下列数轴表示错误的是( )
(o214•润州区二模)用数轴表示某些化学知识直观、简明、易记.下列数轴表示错误的是( )
A.物质形成溶液的pH: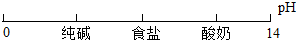
B.银、铜、铁的金属活动性强弱:
C.硫及其化合物与化合价的关系: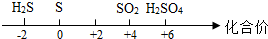
D.形成溶液时的温度:
 longlong58550151年前1
longlong58550151年前1 -
 贝贝猫 共回答了21个问题
贝贝猫 共回答了21个问题 |采纳率71.4%解题思路:本题把溶液的酸碱度、金属活动性、化合物中元素化合价、物质溶于水的吸放热现象,放在数轴上进行对比,结合数轴的变化规律及位置关系判断是否符合物质的性质特点,不相符即错误.A、食盐为中性溶液,其pH=六,而酸奶为酸性其pH<六、纯碱呈碱性其pH>六,这二种物质的性质与所处位置不对应,所以此图关系错误;
2、铁铜银你种金属活动性由强到弱的顺序为铁铜银,与数轴关系一致,表示的关系是正确的;
C、利用化合价代数和为零的原则,根据H为+少、O为-2价,可计算H2S中S为-2价、SO2中S为+4价、H2SO4中S为+下价,单质S中化合价规定为6,四种物质在数轴上的位置正确;
D、硝酸铵溶于水吸热,温度降低;氯化钠溶于水,溶液温度几乎不变;氢氧化钠溶于水,温度升高,数轴关系正确;
故选A.点评:
本题考点: 溶液的酸碱性与pH值的关系;溶解时的吸热或放热现象;金属活动性顺序及其应用;有关元素化合价的计算.
考点点评: 本题考查了常见的用数轴法表示化学知识,完成此题,可以依据已有的知识进行,所以要求同学们在平时的学习中加强基础知识的储备,以便能够灵活应用.1年前查看全部
- (2014•润州区二模)某固体混合物由Mg和MgO组成,取该混合物6.4g与一定量稀硫酸恰好完全反应(反应后溶液中无晶体
(2014•润州区二模)某固体混合物由Mg和MgO组成,取该混合物6.4g与一定量稀硫酸恰好完全反应(反应后溶液中无晶体析出),所得溶液中溶质的质量为24g,则原混合物中氧元素的质量为( )
A.4.8g
B.1.6g
C.3.2g
D.2.56g l_ch1年前1
l_ch1年前1 -
 孤单宝bei 共回答了17个问题
孤单宝bei 共回答了17个问题 |采纳率82.4%解题思路:镁和稀硫酸反应生成硫酸镁和氢气,氧化镁和稀硫酸反应生成硫酸镁和水,根据所得溶液中溶质硫酸镁的质量为24g,可以计算镁元素的质量,进一步可以计算原混合物中氧元素的质量.24g硫酸镁中,镁元素的质量为:24g×[24/120]×100%=4.8g,
则原混合物中氧元素的质量为:6.4g-4.8g=1.6g,
故选:B.点评:
本题考点: 根据化学反应方程式的计算;化合物中某元素的质量计算.
考点点评: 本题主要考查学生进行计算和推断的能力,比较简单,计算时要注意规范性和准确性.1年前查看全部
- (2014•润州区二模)分解因式:mx2-2mx+m=______.
 二教重上1年前1
二教重上1年前1 -
 紫静轩 共回答了8个问题
紫静轩 共回答了8个问题 |采纳率87.5%解题思路:首先提取公因式m,进而利用完全平方公式分解因式得出即可.mx2-2mx+m=m(x2-2x+1)=m(x-1)2.
故答案为:m(x-1)2.点评:
本题考点: 提公因式法与公式法的综合运用.
考点点评: 此题主要考查了提取公因式法和公式法分解因式,熟练应用完全平方公式是解题关键.1年前查看全部
- (2014•润州区二模)下列现象中,由动能转化为重力势能的是( )
(2014•润州区二模)下列现象中,由动能转化为重力势能的是( )
A.
动车匀速上坡
B.
脚踩滑板从高处滑下
C.
滚摆自下而上运动
D.
火箭加速升空 好帅哥1年前1
好帅哥1年前1 -
 天若有情天仪老 共回答了24个问题
天若有情天仪老 共回答了24个问题 |采纳率95.8%解题思路:本题考查了动能与重力势能的转化,动能与质量和速度有关,重力势能与高度和质量有关.若是由动能转化为重力势能,即该过程中动能一定减小,重力势能一定增加;A、动车匀速上坡,所处高度增大,速度不变,重力势能增大,动能不变,不符合题意;
B、小孩滑下,所处高度减小,速度变大,重力势能转化为动能,不符合题意.
C、滚摆上升时,速度越来越小,所处高度增大,动能转化为重力势能,符合题意;
D、火箭加速上升,速度增大,所处高度增大,其动能和重力势能都增大,不符合题意;
故选C.点评:
本题考点: 动能和势能的转化与守恒.
考点点评: 分析能量转化时,就看什么能量减少了,什么能量增加,总是减少的能量转化为增加的能量.1年前查看全部
- (2014•润州区二模)工业上用甲、乙制备化学肥料丙,同时有丁生成.根据下列微观示意图得出的结论中,正确的是( )
(2014•润州区二模)工业上用甲、乙制备化学肥料丙,同时有丁生成.根据下列微观示意图得出的结论中,正确的是( )
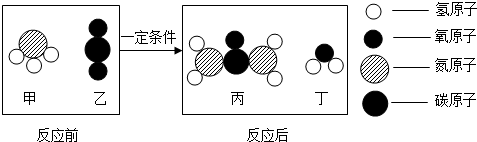
①甲的化学式为NH3②乙、丙、丁都是氧化物
③丙中氮、氢元素质量比为7:1④参加反应的甲、乙质量比为17:44.
A.①
B.①③
C.①④
D.②④ sunxiaochuan1年前1
sunxiaochuan1年前1 -
 南瓜思远 共回答了14个问题
南瓜思远 共回答了14个问题 |采纳率85.7%解题思路:根据微观示意图分析反应物、生成物的构成,判断物质的化学式、类别,写出反应的方程式,再根据方程式进行有关的分析及计算.观察微观示意图,可知反应物、生成物甲、乙、丙、丁分别是:NH3、CO2、CO(NH2)2、H2O,因此反应的方程式是:2NH3+CO2
一定条件
.
CO(NH2)2+H2O,由此可知:
①甲的化学式为:NH3,故正确;
②4种物质中只有CO2、H2O属于氧化物,而CO(NH2)2不是氧化物,故错误;
③丙为CO(NH2)2,其中氮、氢元素的质量比为(14×2):(1×4)=7:1,故正确;
④参加反应的甲、乙质量比为:(2×17):44=34:44,故错误;
所以,①③正确,②④错误.
故选B.点评:
本题考点: 微粒观点及模型图的应用;从组成上识别氧化物;元素质量比的计算.
考点点评: 本题属于微观示意图的考查,解答本题的关键由分子微观示意图确定分子构成,利用分子构成写出物质的化学式,重点考查了知识运用能力.1年前查看全部
- (2014•润州区二模)某化工企业生产流程示意图如图所示,下列说法中正确的是( )
(2014•润州区二模)某化工企业生产流程示意图如图所示,下列说法中正确的是( )

A.钛酸亚铁(FeTiO3)中钛元素为+3价
B.①中反应:2FeTiO3+6C+7Cl2
2X+2TiCl4+6CO,则X为FeCl3一定条件 .
C.②中反应说明金属钛比金属镁的化学性质活泼,氩气起保护气的作用
D.③中反应要使原料全部转化为甲醇,理论上CO和H2投料的质量比是7:1 爱心1001年前1
爱心1001年前1 -
 pangrunyu 共回答了19个问题
pangrunyu 共回答了19个问题 |采纳率84.2%解题思路:A、根据在化合物中正负化合价代数和为零考虑;
B、根据质量守恒定律推断x的化学式;
C、根据强的置换弱的和氩气化学性质稳定判断;
D、根据氢气和一氧化碳反应的方程式考虑质量比;A、设FeTiO3中P的化合价是x.FeTiO3中Fe的化合价是+2价,O的化合价是-2价,利用化合物中各元素的化合价的代数和为零的原则得到方程(+2)+x+(-2)×3=0
解得,x=+4 所以钛酸亚铁(FeTiO3)中钛元素的化合价是+4价,故A错误;
B、根据质量守恒定律,在反应前后各元素原子的个数不变.从2FeTiO3+6C+7Cl2=2X+2TiCl4+6CO看钛原子、氧原子、碳原子反应前后除物质x外个数已经相等,故x中无钛原子、氧原子、碳原子.铁反应前共有2个,反应后只有x有,所以2x中有2个,从而x中有1个;氯原子反应前有14个,反应后x除外有8个,所以2x中有6个,因此x中有3个,因此x的化学式是FeCl3,故B正确;
C、TiCl4与Mg反应的反应物是TiCl4与Mg,生成物是Ti和MgCl2;说明镁比钛活泼,氩气化学性质稳定可做保护气,C错误;
D、根据从化学方程式2H2+CO═CH3OH
4 28
由此可知一氧化碳和氢气的质量比是:28:4=7:1,故D正确;
故选:BD.点评:
本题考点: 物质的相互转化和制备;有关元素化合价的计算;质量守恒定律及其应用.
考点点评: 本题主要考查了化合价的计算、化学方程式的书写以及质量守恒定律的应用,同时考查了学生从题目中获取信息并运用的能力.计算元素的化合价时一定要注意,一定不要忘记填上正号.1年前查看全部
- (2012•润州区二模)下列物质的名称、俗称、化学式相符的是( )
(2012•润州区二模)下列物质的名称、俗称、化学式相符的是( )
A.碳酸氢钠苏打NaHCO3
B.氢氧化钠烧碱NaOH
C.水银汞Ag
D.氯化钠食盐NaCl2 pqoig1年前1
pqoig1年前1 -
 着青石顶 共回答了19个问题
着青石顶 共回答了19个问题 |采纳率94.7%解题思路:根据常见化学物质的名称、俗称、化学式进行分析判断即可.A、碳酸氢钠俗称小苏打,其化学式为NaHCO3,其名称、俗称、化学式不相符.
B、氢氧化钠俗称火碱、烧碱、苛性钠,其化学为NaOH,其名称、俗称、化学式相符.
C、水银是金属汞的俗称,其化学式为Hg,其名称、俗称、化学式不相符.
D、氯化钠的俗称是食盐,其化学式为NaCl,其名称、俗称、化学式不相符.
故选B.点评:
本题考点: 化学式的书写及意义.
考点点评: 本题难度不大,熟练掌握常见化学物质的名称、俗称、化学式是正确解答此类题的关键.1年前查看全部
大家在问
- 1——How are you feeling?——I feel much better.Thank you.A.right
- 2小明要制作一个圆锥模型,其侧面是由一个半径为9cm,圆心角为240°的扇形纸板制成的,还需要一块圆形纸板做底面,那么这块
- 3高中必背古诗文
- 4张掖市人口约128万,面积为4.2万平方千米,则其人口密度约为( )
- 5花园里有一群蜜蜂,其中五分之一落在杜鹃花上,三分之一落在栀子花上,而落在这两种花上的蜜蜂相差数的3倍飞向月季花,最后剩下
- 6背诵一首课外读过的描写春天的古诗,写下来?
- 7中诗人借“弱小的草”抒发了怎样的情?阐明了怎样的理呢?
- 8导体中______会在空中激起电磁波,某电视台发射的电磁波频率为300MHz,该电磁波的波长是______米.
- 9修改病句,虽然明天天气好,但是我们去春游
- 10与科举制的成语和诗句
- 11对溶液平衡条件的困惑!我看了高中化学书上的“溶液平衡条件”.上面说到溶液和溶质处于平衡状态时,一方面不断在溶解,另一方面
- 12已知椭圆E:x2a2+y2b2=1(a>b>0)的离心率为32,且过点(3,[1/2]).
- 13我要一美元的英语怎么写
- 14英语句子中,天气后面什么时候加修饰词?
- 15I am accustomed to getting up early
