电镀液的成分?
 hnjishou2022-10-04 11:39:542条回答
hnjishou2022-10-04 11:39:542条回答
已提交,审核后显示!提交回复
共2条回复
 sanji90123 共回答了18个问题
sanji90123 共回答了18个问题 |采纳率88.9%- 你是要问什么镀液的成分.说都没有说清楚.全都要的话可以去买本电镀书看看就知道了
- 1年前
 春天太短暂 共回答了1个问题
春天太短暂 共回答了1个问题 |采纳率- 三价铬 镍 酸铜 碱铜等
- 1年前
相关推荐
- (10分)铜是重要金属,Cu的化合物在科学研究和工业生产中具有许多用途,如CuSO 4 溶液常用作电解液、电镀液等。请回
(10分)铜是重要金属,Cu的化合物在科学研究和工业生产中具有许多用途,如CuSO 4 溶液常用作电解液、电镀液等。请回答以下问题:
(1)用惰性电极电解硫酸铜溶液时,若某电解质量增加16g,则另一电极的电极方程式为___________;该电极可收集到标况下气体____________L。
(2)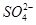 的立体构型是________,其中S原子的杂化轨道类型是_______;
的立体构型是________,其中S原子的杂化轨道类型是_______;
(3))元素金(Au)处于周期表中的第六周期,与Cu同族,Au原子最外层电子排布式为______;一种铜合金晶体具有立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子数量之比为_______。 风飞久久1年前1
风飞久久1年前1 -
 中源一 共回答了16个问题
中源一 共回答了16个问题 |采纳率81.3%(1)4OH -- - 4e - ==2H 2 O + O 2 ; 2.8L。(2)正四面体,sp 3 ;
(3))5d 10 6s 1 ; 3:1
(1) 惰性电极电解硫酸铜溶液,阴极和阳极的反应式分别为2Cu 2 + +4e - =2Cu、4OH - -4 e - ==2H 2 O + O 2 ↑,铜的物质的量是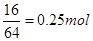 ,根据电荷守恒定律知气体的体积是
,根据电荷守恒定律知气体的体积是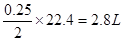 。
。
(2)根据价层电子对互斥模型知,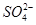 中中心原子的孤对电子数是0,价层电子对数是4,所以是正四面体构型,采用sp 3 杂化。
中中心原子的孤对电子数是0,价层电子对数是4,所以是正四面体构型,采用sp 3 杂化。
(3)立方体有6个面8个顶点,所以1个晶胞中含有的铜原子和金原子数分别为6×1/2=3,8×1/8=1,所以合金中Cu原子与Au原子数量之比为3:1。
(3)根据构造原理知Au原子最外层电子排布式为5d 10 6s 1 (全充满或半充满最稳定)。1年前查看全部
- 电镀时,将镀层金属作阴极,待镀金属制品作阳极,含有镀层金属离子的溶液为电镀液进行电解
 披着羊皮的狼5211年前2
披着羊皮的狼5211年前2 -
 天天添婪 共回答了18个问题
天天添婪 共回答了18个问题 |采纳率88.9%错.电镀时,将镀层金属作阳极,待镀金属制品作阴极,含有镀层金属离子的溶液为电镀液进行电解1年前查看全部
- 电镀池形成条件阳极一定要是镀层金属吗?仅仅电镀液中含有镀层金属离子不行?阳极是惰性电极不行吗?
 我爱射门1年前2
我爱射门1年前2 -
 天空yy 共回答了14个问题
天空yy 共回答了14个问题 |采纳率78.6%对于电镀池的话,应该是这样的,因为他的本质是消耗某金属并使其在阳极析出,形成电镀,至于电镀液,先不说电镀液就是根据他来配置的,但说若仅仅在电镀液中有的话,有可能会造成无法电镀和混有杂质等情况 若是惰性电极的话,会因为电镀液逐渐减少的问题而使反应终止1年前查看全部
- 100分求废电镀液的提金办法-还有加分--有收购的也请告知
100分求废电镀液的提金办法-还有加分--有收购的也请告知
朋友做电镀生意有好多废电镀液想将其中的金提取出来,不知哪位能帮助出个好办法.
曾经使用了直接加锌粉后硫酸煮的办法但获得的液体是深棕色,没能析出换色的金子沉淀,怎样处理才好呢,其他还有什么更好的办法吗,有收购废液的吗. lingge21年前2
lingge21年前2 -
 微笑的小太阳 共回答了24个问题
微笑的小太阳 共回答了24个问题 |采纳率91.7%一 将含金废液加热到80—90℃,不断搅拌下缓慢加入氯化亚铁溶液,反应如下;
Au3++3Fe2+==3Fe3++Au↓随着金离子不断被还原,溶液的颜色由黄色逐渐变为综红色,金粉沉于底部.继续加入过量的氧化亚铁溶液,静置数小时.取静止分层液两滴,加1%赤血盐两滴,现蓝色,表明金已被全部还原.倒去上部清液,减压法抽滤,下部为土黄色金粉沉淀.
酸洗、水洗:将1∶2.5的盐酸溶液加入金粉中煮沸,搅拌5分钟,倾去上部溶液,如此反复3—5次,至不呈现黄色为止.用蒸馏水多次冲洗金粉,至洗出的水pH值约为7时为止
烘干:将水洗后的金粉置于烘干箱中烘干,得桔黄色海绵粒状金渣.
溶铸:将金粉置于石英坩埚内,在高温管式电炉内加热到1200℃左右,溶化后注入石墨模中铸为金锭.若金粉不钝,溶化时可加入硼砂,但不宜用石英坩埚,可将金粉置石墨坩埚中熔铸.
二 在良好的通风条件下,把废金镀液注入瓷皿中,加热蒸发至粘稠状,用五倍蒸馏水稀释,在不断搅拌下加入用盐酸酸化过的硫酸亚铁,直至不再析出沉淀为止.金呈现黑色的粉状沉淀在瓷皿底部.将沉淀物先用盐酸,后用硝酸煮一下,然后清洗烘干.若能在700—800℃焙烧30分钟更好.
三 在良好的通风条件下,用盐酸调废金镀液的PH=1左右.把溶液加热到70—80℃在不断搅拌下加入锌粉,至溶液变成透明黄白色,有大量金粉被沉淀下来为止.在这过程中,保持PH=1左右.此后的处理方法与二相同.
参考别人的,试一下吧!1年前查看全部
- 电镀是金属防锈的方法之一.某电镀厂有三个分别给金属表面镀锌、镀铜、镀银的车间,每个车间电镀液的溶质中只含有易溶的锌盐、铜
电镀是金属防锈的方法之一.某电镀厂有三个分别给金属表面镀锌、镀铜、镀银的车间,每个车间电镀液的溶质中只含有易溶的锌盐、铜盐和银盐中的一种物质.现取三个车间的电镀液于烧杯中,标为1、2、3号,某小组同学通过实验对三种电镀液中溶质成分进行探究.
【提出问题】三种电镀液中溶质的成分是什么?
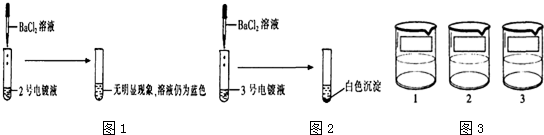
【探究实验1】如图1
【表达与交流】甲同学认为2号电镀液中的溶质一定不是硫酸铜,你认为他的结论______(填“正确”或“不正确”).
【探究实验2】如图2
【反思与评价】乙同学认为3号电镀液中的溶质一定是硫酸锌,请你对乙同学的结论给予评价______.
【探究实验3】根据上述实验,丙同学取少量的1号电镀液与少量的2号电镀液混合,立即出现有______生成的明显现象,由此小组同学确定了三种电镀液中分别含有的溶质的成分.
【解释与结论】请帮助他们将三种电镀液中溶质成分的化学式填写在烧杯的标签上. goolit1年前1
goolit1年前1 -
 ξИīъуп 共回答了19个问题
ξИīъуп 共回答了19个问题 |采纳率89.5%解题思路:【表达与交流】硫酸铜和氯化钡反应会生成白色沉淀;
【反思与评价】可溶性的银盐、硫酸盐均和氯化钡反应生成白色沉淀;
【探究实验3】银盐中只有硝酸银是易溶的,氯化银是常见的难溶性白色沉淀,硝酸银和氯化铜反应会生成白色沉淀;
【解释与结论】根据实验现象来判断具体的物质.【表达与交流】2号电镀液中的溶质如果是硫酸铜,则硫酸铜和氯化钡反应会生成白色沉淀,和题中的无现象矛盾,所以2号电镀液中的溶质一定不是硫酸铜,故答案为:正确;
【反思与评价】3号电镀液中加入氯化钡溶液出现白色沉淀,溶液中可能含有硫酸锌,也可能含硝酸银,因为硫酸锌与氯化钡反应生成硫酸钡是白色沉淀,硝酸银与氯化钡反应生成氯化银是白色沉淀;故答案为:不正确;3号电镀液中加入氯化钡溶液出现白色沉淀,溶液中可能含有硫酸锌,硫酸锌与氯化钡反应生成硫酸钡是白色沉淀,也可能含硝酸银,硝酸银与氯化钡反应生成氯化银是白色沉淀(或产生白色沉淀只能证明3号溶液中含有硫酸根离子或银离子),因此乙同学认为3号电镀液中的溶质一定是硫酸锌是不正确的;
【探究实验3】根据题目中的实验现象,2号电镀液一定含有铜离子,3号电镀液一定含有硫酸根离子,1号电镀液是可溶的银盐,即硝酸银,则2号电镀液为氯化铜,3号电镀液为硫酸锌,1号电镀液与少量的2号电镀液混合,会生成白色沉淀,故答案为:白色沉淀;
【解释与结论】1号电镀液是硝酸银,则2号电镀液为氯化铜,3号电镀液为硫酸锌,贴上标签后为: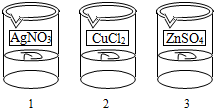 ,故答案为:
,故答案为: .
.点评:
本题考点: 实验探究物质的组成成分以及含量;盐的化学性质;化学式的书写及意义.
考点点评: 本题是一道化学综合试验知识题目,要求学生具有分析和解决问题的能力,难度较大.1年前查看全部
- 以KCl和ZnCl2混合液为电镀液在铁制品上镀锌,下列说法正确的是( )
以KCl和ZnCl2混合液为电镀液在铁制品上镀锌,下列说法正确的是( )
A. 未通电前上述镀锌装置可构成原电池,电镀过程是该电池的充电过程
B. 因部分电能转化为热能,电镀是通过的电量与锌的析出量无确定关系
C. 电镀时保持电流恒定,升高温度不改变电解反应速率
D. 镀锌层破损后即对铁制品失去保护作用 秋日寒流1年前1
秋日寒流1年前1 -
 麦加叮叮 共回答了16个问题
麦加叮叮 共回答了16个问题 |采纳率81.3%解题思路:根据Zn的金属性强于Fe,未通电前上述镀锌装置可构成原电池,其正极反应为:O2+4e-+2H2O═4OH-,与电镀时所发生的反应为不同的两个反应,故电镀过程不是该原电池的充电过程;
电镀时,每转移2mol电子析出1molZn,通过的电量与析出的锌的量存在确定的关系,与能量的其他转化无关;电镀时保持单位时间内转移的电子数恒定,则消耗的反应物与产生的生成物的量恒定,也就是反应速率恒定,与温度无关;镀锌铁制品的镀层破损后,易形成Zn-Fe原电池,Zn作负极优先被腐蚀,铁制品仍能受到保护.A、未通电前上述镀锌装置可构成原电池,因原电池反应与电镀时所发生的反应为不同的两个反应,故电镀过程不是该原电池的充电过程,故A错误;
B、电解过程中确实存在电能转化成热能的情况,但电镀时通过的电量与析出的锌的量存在确定的关系,与能量的其他转化无关,故B错误;
C、电镀时保持电流恒定,即单位时间内转移的电子数恒定,则消耗的反应物与产生的生成物的量恒定,也就是反应速率恒定,与温度无关,故C正确;
D、镀锌层破损后,能形成锌铁原电池,铁为正极,锌为负极,同样起到保护铁的作用,故D错误.
故选C.点评:
本题考点: 电解原理的应用实验.
考点点评: 此题考查了原电池与电解池的工作原理及应用.重在突出应用及电路中的电量与析出物质的守恒关系,解答本题时应明确电池或电解工作原理,对于其应用也要掌握.1年前查看全部
- 电镀的电镀液为什么要采用含有镀层金属离子的盐溶液?具体点,why一定要有镀层金属离子?
 胡涂小仙女1年前3
胡涂小仙女1年前3 -
 嘈如急雨小 共回答了18个问题
嘈如急雨小 共回答了18个问题 |采纳率83.3%电镀是一个阳极氧化、阴极还原的过程,阳极金属被氧化后形成金属离子进入镀液,在阴极,金属阳离子得到电子被还原到镀件上,但电镀中存在浓差极化,存在液相传质的过程,不是电镀一开始,金属离子就直接能从阳极到达阴极;...1年前查看全部
- 电镀液混进盐酸怎么除去盐酸?注:主要成分有氟硼酸亚希,硼酸,氟硼酸
 JUNS011年前2
JUNS011年前2 -
 zhuxu7011 共回答了13个问题
zhuxu7011 共回答了13个问题 |采纳率92.3%这种溶液混迹盐酸无法去除,因为既不能电解除去,也不能沉淀除去,加银离子可生成氯化银沉淀除去,但这样做得不偿失,氯化亚铜也可以沉淀除去,但无法加进亚铜离子.1年前查看全部
- 电镀的电镀液为什么要采用含有镀层金属离子的盐溶液?具体点,谢谢!
 jc8i1年前2
jc8i1年前2 -
 小丸子很懦弱 共回答了18个问题
小丸子很懦弱 共回答了18个问题 |采纳率77.8%在电镀液中,金属离子是正价缺电子游离状态,在得到电子的时候就会变成金属附着,也就是电镀上了这种金属.1年前查看全部
- 在电镀池中电镀液的质量会改变吗?为什么?
 风之女妖1年前5
风之女妖1年前5 -
 155245497 共回答了13个问题
155245497 共回答了13个问题 |采纳率92.3%这个问题要客观考虑,在人类正常的生活条件下,电镀过程中电镀液的质量是会减少的,但是有的情况,例如理想状态会有不变的情况.
我简单解释下,很多人认为由于金属上镀导致镀液中金属离子浓度降低,但是如果阳极所挂为上镀金属,其会同时不断的补充到镀液中去,所以单从这个方面不能简单的就判定电镀液质量减低.
但是,很多电镀过程中有副反应存在,例如碱性镀锌析出氢气,这样的话电镀液质量肯定减少,再加之生产过程中反应放热,水也会挥发,有些电镀主盐会和空气中的成份缓慢反应,导致析出,这些都会导致电镀液质量减少,所以实际生产中才需要不断的添加主盐,添加剂等等.
当然,如果这是道普通的学校考试题目,也许会考虑不放热,真空状态、不考虑副反应等等理想情况,那样的话,会有可能质量恒定.
另外,LZ可以考虑质量守恒定律来解释,希望回答对LZ有帮助1年前查看全部
- 电镀液被硝酸污染怎么处理
 刘艳1年前2
刘艳1年前2 -
 侯禀鹊 共回答了13个问题
侯禀鹊 共回答了13个问题 |采纳率92.3%除硝酸根可以采用电解法,电解去除镀镍液中的硝酸根以低pH值和高温为好.低pH值有利于硝酸根在阴极上的还原,高温可以使硝酸根还原产生的气体在溶液中的溶解度降低,防止它溶入后重新污染镀镍液,所以一般电解去除硝酸根的条件为:镀液pH=1~2,温度60℃~70℃,阴极电流密度先用lA/dm2~2A/dm2,使NO3-在阴极还原为NH3逸出,然后逐渐降低至0.2A/dm2,直至镀液正常为止.
但是此法缺点是电解费时费工,对连续生产的自动线或手工生产应付急件,都令人头痛;镀镍液调低pH值容易,要调回到允许值则很麻烦,要么加碳酸钡后彻底过滤,要么用5%以下苛性钠稀溶液在强烈搅拌下慢慢加入.此时,镀液冲稀不少,体积大增;要么急于求成,主盐镍离子成氢氧化镍沉淀损失不少.有人加人对镀液无害的还原剂(NaHSO3稀溶液),靠氧化还原反应直接去除硝酸根取得了很好效果:第一步,通过霍耳槽试验确定应加入的NaHSO3量;第二步,按计算量的110%在不断强烈搅拌下慢慢加入稀NaHSO3溶液(以减少因生成SO2而过量消耗的HSO3-),继续搅拌约5min;第三步,按lmL/L~2mL/L量加入30%的H2O2,加温(也可直接在热的镀镍液中处理)到55℃~60℃;搅拌反应约lh,氧化残存的NaHS03并分解多余的H2O2.无需过滤、调pH值到工艺范围即可试镀(光亮剂依情况调整).大生产应用效果良好,处理一次耗时2h左右,物耗也很小.1年前查看全部
- 将电镀液中的铬离子除去,但要保留铜和镍离子,且PH保持3-5之间
 mp4fan_snoopy001年前3
mp4fan_snoopy001年前3 -
 潇潇林枫 共回答了20个问题
潇潇林枫 共回答了20个问题 |采纳率80%控pH = 3-5可以使Cr(3+)生成Cr(OH)3沉淀,而Cu(2+)、Ni(2+)不沉淀.1年前查看全部
- 有一个长方体形的电镀槽,槽内有一圆柱形的零件完全浸在电镀液中,已知电镀槽的长2米,宽为1米.
有一个长方体形的电镀槽,槽内有一圆柱形的零件完全浸在电镀液中,已知电镀槽的长2米,宽为1米.
电镀液面高0.5米.零件的底面直径为0.4米.当零件从电镀液中取出后液面下降了0.03米,那么零件的高是多少?
 华南人1年前1
华南人1年前1 -
 流水依扬 共回答了15个问题
流水依扬 共回答了15个问题 |采纳率86.7%小毛鼠:您好.
零件体积:2m×1m×0.03m=0.06m³
零件高:0.06m³÷[(0.2m)²×3.14)]=0.06m³÷0.1256m²=0.4777m
答:零件高约0.48米
祝好,再见.1年前查看全部
- 以KCl和ZnCl2混合液为电镀液在铁制品上镀锌,下列说法正确的是( )
以KCl和ZnCl2混合液为电镀液在铁制品上镀锌,下列说法正确的是( )
A. 未通电前上述镀锌装置可构成原电池,电镀过程是该电池的充电过程
B. 因部分电能转化为热能,电镀是通过的电量与锌的析出量无确定关系
C. 电镀时保持电流恒定,升高温度不改变电解反应速率
D. 镀锌层破损后即对铁制品失去保护作用 刀上飞1年前3
刀上飞1年前3 -
 太阳的爱 共回答了21个问题
太阳的爱 共回答了21个问题 |采纳率85.7%解题思路:根据Zn的金属性强于Fe,未通电前上述镀锌装置可构成原电池,其正极反应为:O2+4e-+2H2O═4OH-,与电镀时所发生的反应为不同的两个反应,故电镀过程不是该原电池的充电过程;
电镀时,每转移2mol电子析出1molZn,通过的电量与析出的锌的量存在确定的关系,与能量的其他转化无关;电镀时保持单位时间内转移的电子数恒定,则消耗的反应物与产生的生成物的量恒定,也就是反应速率恒定,与温度无关;镀锌铁制品的镀层破损后,易形成Zn-Fe原电池,Zn作负极优先被腐蚀,铁制品仍能受到保护.A、未通电前上述镀锌装置可构成原电池,因原电池反应与电镀时所发生的反应为不同的两个反应,故电镀过程不是该原电池的充电过程,故A错误;
B、电解过程中确实存在电能转化成热能的情况,但电镀时通过的电量与析出的锌的量存在确定的关系,与能量的其他转化无关,故B错误;
C、电镀时保持电流恒定,即单位时间内转移的电子数恒定,则消耗的反应物与产生的生成物的量恒定,也就是反应速率恒定,与温度无关,故C正确;
D、镀锌层破损后,能形成锌铁原电池,铁为正极,锌为负极,同样起到保护铁的作用,故D错误.
故选C.点评:
本题考点: 电解原理的应用实验.
考点点评: 此题考查了原电池与电解池的工作原理及应用.重在突出应用及电路中的电量与析出物质的守恒关系,解答本题时应明确电池或电解工作原理,对于其应用也要掌握.1年前查看全部
- 电镀液的测定误差问题用重铬酸钾法测定电镀液中的甲基磺酸锡含量:步骤如下:称样0.7g加25ml硫酸铁铵,加10ml浓硫酸
电镀液的测定误差问题
用重铬酸钾法测定电镀液中的甲基磺酸锡含量:步骤如下:称样0.7g加25ml硫酸铁铵,加10ml浓硫酸,反应2min,加70ml水,加10ml浓磷酸,反应2min,以二苯胺磺酸钠为指示剂,用重铬酸钾滴定至溶液由绿色变蓝紫色为终点。在实验中平行样间误差较大,求教高手,各步骤的反应机理和实验中所需注意的细节问题 ,以减少平行样间的误差问题。
 青草饭团1年前1
青草饭团1年前1 -
 Bernadette 共回答了19个问题
Bernadette 共回答了19个问题 |采纳率89.5%找找看有没有国标方法或ISO方法,或甲基磺酸锡产品的标准分析方法1年前查看全部
- 欲在金属表面镀银,应把镀件挂在电镀池的阴极.下列各组中,选用的阳极金属和电镀液均正确的是( )
欲在金属表面镀银,应把镀件挂在电镀池的阴极.下列各组中,选用的阳极金属和电镀液均正确的是( )
A. Ag和AgCl溶液
B. Ag和AgNO3溶液
C. Pt和Ag2CO3溶液
D. Pt和Ag2SO4溶液 组织361年前2
组织361年前2 -
 adsl5231 共回答了21个问题
adsl5231 共回答了21个问题 |采纳率81%解题思路:电镀时,镀层金属为阳极,镀件金属为阴极,电镀液是含有镀层金属阳离子的盐溶液.在金属表面镀银,应把镀件挂在电镀池的阴极,镀层金属银作阳极,电镀液是含有银离子的可溶性的盐溶液硝酸银即可.
故选B.点评:
本题考点: 电解原理.
考点点评: 本题考查学生电镀池的工作原理知识,注意知识的梳理和应用是关键,难度不大.1年前查看全部
- 电镀是金属防锈的方法之一.某电镀厂有三个分别给金属表面镀锌、镀铜、镀银的车间,每个车间电镀液的溶质中只含有易溶的锌盐、铜
电镀是金属防锈的方法之一.某电镀厂有三个分别给金属表面镀锌、镀铜、镀银的车间,每个车间电镀液的溶质中只含有易溶的锌盐、铜盐和银盐中的一种物质.现取三个车间的电镀液于烧杯中,标为1、2、3号,某小组同学通过实验对三种电镀液中溶质成分进行探究.
[提出问题]三种电镀液中溶质的成分是什么?
[探究实验1]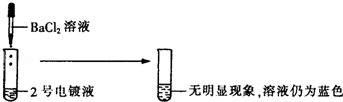
[表达与交流]甲同学认为2号电镀液中的溶质一定不是硫酸铜,你认为他的结论(1) (填“正确”或“不正确”).
[探究实验2]
[反思与评价]乙同学认为3号电镀液中的溶质一定是硫酸锌,请你对乙同学的结论给予评价(2) .
[探究实验3]根据上述实验,丙同学取少量的1号电镀液与少量的2号电镀液混合,立即出现有(3) 生成的明显现象,由此小组同学确定了三种电镀液中分别含有的溶质的成分.
解释与结论:探究实验3中发生反应的化学方程式为(4) ,请帮助他们将三种电镀液中溶质成分的化学式填写在烧杯的标签上(5). 厦忆1年前1
厦忆1年前1 -
 垂裳 共回答了14个问题
垂裳 共回答了14个问题 |采纳率100%(1)正确;(2)不正确;3号电镀液中加入氯化钡溶液出现白色沉淀,溶液中可能含有硫酸锌,硫酸锌与氯化钡反应生成硫酸钡是白色沉淀,也可能含硝酸银,硝酸银与氯化钡反应生成氯化银是白色沉淀(或产生白色沉淀只能证明3号溶液中含有硫酸根离子或银离子),因此乙同学认为3号电镀液中的溶质一定是硫酸锌是不正确的;
(3)白色沉淀;(4)CuCl 2 +2AgNO 3 =2AgCl↓+Cu(NO 3 ) 2 ;(5)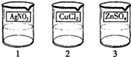
(1)2号电镀液中的溶质如果是硫酸铜,则硫酸铜和氯化钡反应会生成白色沉淀,和体重的无现象矛盾,,所以2号电镀液中的溶质一定不是硫酸铜,故答案为:正确;
(2)3号电镀液中加入氯化钡溶液出现白色沉淀,溶液中可能含有硫酸锌,也可能含硝酸银,因为硫酸锌与氯化钡反应生成硫酸钡是白色沉淀,硝酸银与氯化钡反应生成氯化银是白色沉淀,故答案为:不正确;3号电镀液中加入氯化钡溶液出现白色沉淀,溶液中可能含有硫酸锌,硫酸锌与氯化钡反应生成硫酸钡是白色沉淀,也可能含硝酸银,硝酸银与氯化钡反应生成氯化银是白色沉淀(或产生白色沉淀只能证明3号溶液中含有硫酸根离子或银离子),因此乙同学认为3号电镀液中的溶质一定是硫酸锌是不正确的;
(3)根据题目中的实验现象,2号电镀液一定含有铜离子,3号电镀液一定含有硫酸根离子,1号电镀液是可溶的银盐,即硝酸银,则2号电镀液为氯化铜,3号电镀液为硫酸锌,1号电镀液与少量的2号电镀液混合,会生成白色沉淀,故答案为:白色沉淀;
(4)氯化铜和硝酸银发生复分解反应,即CuCl 2 +2AgNO 3 =2AgCl↓+Cu(NO 3 ) 2 ,故答案为:CuCl 2 +2AgNO 3 =2AgCl↓+Cu(NO 3 ) 2 ;
(5)1号电镀液是硝酸银,则2号电镀液为氯化铜,3号电镀液为硫酸锌,故答案为: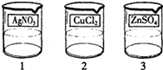 .
1年前查看全部
.
1年前查看全部
- (2012•哈尔滨)电镀是金属防锈的方法之一.某电镀厂有三个分别给金属表面镀锌、镀铜、镀银的车间,每个车间电镀液的溶质中
(2012•哈尔滨)电镀是金属防锈的方法之一.某电镀厂有三个分别给金属表面镀锌、镀铜、镀银的车间,每个车间电镀液的溶质中只含有易溶的锌盐、铜盐和银盐中的一种物质.现取三个车间的电镀液于烧杯中,标为1、2、3号,某小组同学通过实验对三种电镀液中溶质成分进行探究.
[提出问题]三种电镀液中溶质的成分是什么?
[探究实验1]
[表达与交流]甲同学认为2号电镀液中的溶质一定不是硫酸铜,你认为他的结论(1)______(填“正确”或“不正确”).
[探究实验2]
[反思与评价]乙同学认为3号电镀液中的溶质一定是硫酸锌,请你对乙同学的结论给予评价(2)______.
[探究实验3]根据上述实验,丙同学取少量的1号电镀液与少量的2号电镀液混合,立即出现有(3)______生成的明显现象,由此小组同学确定了三种电镀液中分别含有的溶质的成分.
解释与结论:探究实验3中发生反应的化学方程式为(4)______,请帮助他们将三种电镀液中溶质成分的化学式填写在烧杯的标签上(5). hh帮你顶1年前1
hh帮你顶1年前1 -
 5016021 共回答了14个问题
5016021 共回答了14个问题 |采纳率85.7%解题思路:(1)硫酸铜和氯化钡反应会生成白色沉淀;
(2)可溶性的银盐、硫酸盐均和氯化钡反应生成白色沉淀;
(3)银盐中只有硝酸银是易溶的,氯化银是常见的难溶性白色沉淀,硝酸银和氯化铜反应会生成白色沉淀;
(4)硝酸银和氯化铜之间发生复分解反应,会生成白色沉淀;
(5)根据实验想先来判断具体的物质.(1)2号电镀液中的溶质如果是硫酸铜,则硫酸铜和氯化钡反应会生成白色沉淀,和题中的无现象矛盾,所以2号电镀液中的溶质一定不是硫酸铜,故答案为:正确;
(2)3号电镀液中加入氯化钡溶液出现白色沉淀,溶液中可能含有硫酸锌,也可能含硝酸银,因为硫酸锌与氯化钡反应生成硫酸钡是白色沉淀,硝酸银与氯化钡反应生成氯化银是白色沉淀,故答案为:不正确;3号电镀液中加入氯化钡溶液出现白色沉淀,溶液中可能含有硫酸锌,硫酸锌与氯化钡反应生成硫酸钡是白色沉淀,也可能含硝酸银,硝酸银与氯化钡反应生成氯化银是白色沉淀(或产生白色沉淀只能证明3号溶液中含有硫酸根离子或银离子),因此乙同学认为3号电镀液中的溶质一定是硫酸锌是不正确的;
(3)根据题目中的实验现象,2号电镀液一定含有铜离子,3号电镀液一定含有硫酸根离子,1号电镀液是可溶的银盐,即硝酸银,则2号电镀液为氯化铜,3号电镀液为硫酸锌,1号电镀液与少量的2号电镀液混合,会生成白色沉淀,故答案为:白色沉淀;
(4)氯化铜和硝酸银发生复分解反应,即CuCl2+2AgNO3=2AgCl↓+Cu(NO3)2,故答案为:CuCl2+2AgNO3=2AgCl↓+Cu(NO3)2;
(5)1号电镀液是硝酸银,则2号电镀液为氯化铜,3号电镀液为硫酸锌,贴上标签后为: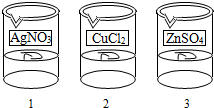 ,故答案为:
,故答案为: .
.点评:
本题考点: 实验探究物质的组成成分以及含量;盐的化学性质;常见离子的检验方法及现象;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题是一道化学综合试验知识题目,要求学生具有分析和解决问题的能力,难度较大.1年前查看全部
- 电镀是金属防锈的方法之一.某电镀厂有三个分别给金属表面镀锌、镀铜、镀银的车间,每个车间电镀液的溶质中只含有易溶的锌盐、铜
电镀是金属防锈的方法之一.某电镀厂有三个分别给金属表面镀锌、镀铜、镀银的车间,每个车间电镀液的溶质中只含有易溶的锌盐、铜盐和银盐中的一种物质.现取三个车间的电镀液于烧杯中,标为1、2、3号,某小组同学通过实验对三种电镀液中溶质成分进行探究.
[提出问题]三种电镀液中溶质的成分是什么?
[探究实验1]
[表达与交流]甲同学认为2号电镀液中的溶质一定不是硫酸铜,你认为他的结论(1)______(填“正确”或“不正确”).
[探究实验2]
[反思与评价]乙同学认为3号电镀液中的溶质一定是硫酸锌,请你对乙同学的结论给予评价(2)______.
[探究实验3]根据上述实验,丙同学取少量的1号电镀液与少量的2号电镀液混合,立即出现有(3)______生成的明显现象,由此小组同学确定了三种电镀液中分别含有的溶质的成分.
解释与结论:探究实验3中发生反应的化学方程式为(4)______,请帮助他们将三种电镀液中溶质成分的化学式填写在烧杯的标签上(5). toproad1年前1
toproad1年前1 -
 ziweixing 共回答了15个问题
ziweixing 共回答了15个问题 |采纳率80%解题思路:(1)硫酸铜和氯化钡反应会生成白色沉淀;
(2)可溶性的银盐、硫酸盐均和氯化钡反应生成白色沉淀;
(3)银盐中只有硝酸银是易溶的,氯化银是常见的难溶性白色沉淀,硝酸银和氯化铜反应会生成白色沉淀;
(4)硝酸银和氯化铜之间发生复分解反应,会生成白色沉淀;
(5)根据实验想先来判断具体的物质.(1)2号电镀液中的溶质如果是硫酸铜,则硫酸铜和氯化钡反应会生成白色沉淀,和题中的无现象矛盾,所以2号电镀液中的溶质一定不是硫酸铜,故答案为:正确;
(2)3号电镀液中加入氯化钡溶液出现白色沉淀,溶液中可能含有硫酸锌,也可能含硝酸银,因为硫酸锌与氯化钡反应生成硫酸钡是白色沉淀,硝酸银与氯化钡反应生成氯化银是白色沉淀,故答案为:不正确;3号电镀液中加入氯化钡溶液出现白色沉淀,溶液中可能含有硫酸锌,硫酸锌与氯化钡反应生成硫酸钡是白色沉淀,也可能含硝酸银,硝酸银与氯化钡反应生成氯化银是白色沉淀(或产生白色沉淀只能证明3号溶液中含有硫酸根离子或银离子),因此乙同学认为3号电镀液中的溶质一定是硫酸锌是不正确的;
(3)根据题目中的实验现象,2号电镀液一定含有铜离子,3号电镀液一定含有硫酸根离子,1号电镀液是可溶的银盐,即硝酸银,则2号电镀液为氯化铜,3号电镀液为硫酸锌,1号电镀液与少量的2号电镀液混合,会生成白色沉淀,故答案为:白色沉淀;
(4)氯化铜和硝酸银发生复分解反应,即CuCl2+2AgNO3=2AgCl↓+Cu(NO3)2,故答案为:CuCl2+2AgNO3=2AgCl↓+Cu(NO3)2;
(5)1号电镀液是硝酸银,则2号电镀液为氯化铜,3号电镀液为硫酸锌,贴上标签后为: ,故答案为:
,故答案为: .
.点评:
本题考点: 实验探究物质的组成成分以及含量;盐的化学性质;常见离子的检验方法及现象;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题是一道化学综合试验知识题目,要求学生具有分析和解决问题的能力,难度较大.1年前查看全部
- 以KCL和ZnCL2混合液为电镀液在铁制品上镀锌,下列说法正确的是
以KCL和ZnCL2混合液为电镀液在铁制品上镀锌,下列说法正确的是
A.未通电前上述镀锌装置可构成原电池,电镀过程是该原电池的充电过程
我知道这项是错的,答案里说可以构成原电池,上网有些人又说不可以,到底前半句说的话有没正确,可以构成原电池吗?
我书上的答案是说可以构成原电池 其中 Zn - 2e- = Zn2+,还有一极是 发生O2+H2O+4e=4OH-
能不能构成原电池,可以的话为什么我答案说是发生O2+H2O+4e=4OH-
而不是H+ +2e=H2 老陈牛1年前2
老陈牛1年前2 -
 ffffffsdaa 共回答了19个问题
ffffffsdaa 共回答了19个问题 |采纳率89.5%不能构成原电池
构成的是腐蚀电池(吸氧腐蚀)1年前查看全部
- 配制电镀液的时候为什么要加入PH缓冲剂
配制电镀液的时候为什么要加入PH缓冲剂
如铁钉上镀锌,电镀液的配制中要加入硼酸,使其PH稳定,为什么电镀时,要加入ph缓冲剂呢 odinmmboy1年前3
odinmmboy1年前3 -
 林少 共回答了15个问题
林少 共回答了15个问题 |采纳率93.3%因为在电镀过程中,发生各种化学反应,导致酸碱度变化,酸碱度影响到各个物质的电极电势,造成电镀电流密度变化,析出物组成变化,电镀质量就会不好.浙大哲博检测回答1年前查看全部
- 电镀的原理是镀层金属做阳极,有镀层金属离子的电解质配电镀液.利用阳极溶解提供镀层金属,那么在用惰性电极材料作阳极,镀层金
电镀的原理是镀层金属做阳极,有镀层金属离子的电解质配电镀液.利用阳极溶解提供镀层金属,那么在用惰性电极材料作阳极,镀层金属由电镀液提供时,惰性电极是否也失去电子被氧化?如果惰性电极(比如石墨,非金属做阳极)不失去电子,那么电镀液中的金属离子被还原时需要的电子从哪里来?
谢 gavinchen_gogogo1年前1
gavinchen_gogogo1年前1 -
 waozichaolaoda 共回答了17个问题
waozichaolaoda 共回答了17个问题 |采纳率82.4%电镀时,电流通过两类导体(第一类导体外电路金属导体和第二类导体内电路电解质溶液)形成回路,在第一类导体中是电子导电,在第二类导体中是离子导电.只要有电流通过,电解池的两极必发生氧化还原反应,阳极上失去电子,发生氧化反应,阴极得到电子,发生还原反应,这实质上是外加电场强行从阳极上夺得电子,再通过外电路送给阴极.当阳极是可溶性金属时,电子是该金属提供的,当阳极是惰性金属时,电子是溶液中的阴离子提供的,比如氢氧根离子,它在阳极失去电子变成氧气,再如氯离子,在阳极失去电子变成氯气等等.需指出,阳极必须是导体,不导电的非金属不能作阳极,.1年前查看全部
- 电镀是金属防锈的方法之一.某电镀厂有三个分别给金属表面镀锌、镀铜、镀银的车间,每个车间电镀液的溶质中只含有易溶的锌盐、铜
电镀是金属防锈的方法之一.某电镀厂有三个分别给金属表面镀锌、镀铜、镀银的车间,每个车间电镀液的溶质中只含有易溶的锌盐、铜盐和银盐中的一种物质.现取三个车间的电镀液于烧杯中,标为1、2、3号(如图1),某小组同学通过实验对三种电镀液中溶质成分进行探究.
【提出问题】三种电镀液中溶质的成分是什么?
【探究实验1】如图2: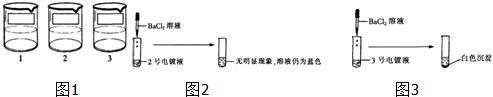
【表达与交流】甲同学认为2号电镀液中的溶质一定不是硫酸铜,你认为他的结论(1)______(填“正确”或“不正确”).
【探究实验2】如图3:
【反思与评价】乙同学认为3号电镀液中的溶质一定是硫酸锌,请你对乙同学的结论给予评价且说明理由(2)______.
【探究实验3】根据上述实验,丙同学取少量的1号电镀液与少量的2号电镀液混合,立即出现有(3)______生成的明显现象,由此小组同学确定了三种电镀液中分别含有的溶质的成分.3号电镀液中的溶质是(4)______.
【解释与结论】探究实验3中发生反应的化学方程式为(5)______. BLF123451年前1
BLF123451年前1 -
 hot555 共回答了17个问题
hot555 共回答了17个问题 |采纳率94.1%解题思路:(1)向2号电镀液中滴加BaCl2溶液,无明显现象,溶液仍为蓝色,说明该溶液中含有铜离子,不含硫酸根离子;
(2)向3号电镀液中滴加BaCl2溶液,有白色沉淀,由此仅能判断3号电镀液中的溶质可以是硫酸锌,也可以是硝酸银;
(3)若1号电镀液为锌盐,取少量的1号电镀液与少量的2号电镀液混合,不会立即出现有明显现象;
(4)由分析(3)可推出3号电镀液中的溶质只能是硫酸锌(ZnSO4);
(5)依据实验中存在的反应事实书写化学方程式.(1)向2号电镀液中滴加BaCl2溶液,无明显现象,溶液仍为蓝色,说明该溶液中含有铜离子,不含硫酸根离子;故填正确;
(2)向3号电镀液中滴加BaCl2溶液,有白色沉淀,由此仅能判断3号电镀液中的溶质可以是硫酸锌,也可以是硝酸银;故填不正确,也有可能溶质是硝酸银;
(3)若1号电镀液为锌盐,取少量的1号电镀液与少量的2号电镀液混合,不会立即出现有明显现象;故1号电镀液溶质为硝酸银,故填白色沉淀;(4)由分析(3)可推出3号电镀液中的溶质只能是硫酸锌(ZnSO4);故填硫酸锌(ZnSO4);
(5)依据实验中存在的反应事实书写化学方程式:CuCl2+2AgNO3═2AgCl↓+Cu(NO3)2
故答案为:
(1)正确;
(2)不正确,也有可能溶质是硝酸银;
(3)白色沉淀;
(4)硫酸锌(ZnSO4);
(5)CuCl2+2AgNO3═2AgCl↓+Cu(NO3)2点评:
本题考点: 实验探究物质的组成成分以及含量;盐的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 通过实验现象判断反应事实,一定要联想各种可能性,防止挂一漏万,判断失误.1年前查看全部
- 电镀液各种成分的作用是什么.
 奏乐的丁香1年前1
奏乐的丁香1年前1 -
 孤独薰衣草 共回答了17个问题
孤独薰衣草 共回答了17个问题 |采纳率94.1%1.主盐是指能在阴极上沉积出所要求的镀层金属的盐.
2.导电盐是指能提高溶液的电导率,对放电金属离子不起络合作用的碱金属或碱土金属的盐类(包括铵盐).
3.缓冲剂 加入溶液中,能使溶液在遇到酸或碱时,溶液的pH值变化幅度缩小.
4.阳极去极化剂 是指在电解时能使阳极电位变负、促进阳极活化的物质.
5.络合剂在电镀生产中,一般将能络合主盐中金属离子的物质称为络合剂.
6.添加剂 为了改善电镀溶液性能和镀层质量,往往在电镀溶液中加入少量的某些有机物,这些物质叫做添加剂.
除有机添加剂外,还有某些无机添加剂.无机添加剂多数是硫、硒、碲、铅、铋和锑的化合物.1年前查看全部
- 2011年山东高考理综 第15题以KCI和ZnCI2混合液为电镀液在铁制品上镀锌,A选项
2011年山东高考理综 第15题以KCI和ZnCI2混合液为电镀液在铁制品上镀锌,A选项
未通电时是原电池,但电镀过程并不是原电池的充电过程.我的疑问是:没有通电时,原电池是怎样进行的,也就是谁是正负极?求细解
A选项是 未通电前上述镀锌装置可构成原电池,电镀过程是该原电池的充电过程
“未通电前上述镀锌装置可构成原电池”此句不明白.其中有没有涉及到盐桥?在这先谢谢了 zszblue1年前1
zszblue1年前1 -
 我爱我乖 共回答了19个问题
我爱我乖 共回答了19个问题 |采纳率94.7%组成原电池的基本条件:
1.将两种活泼性不同的金属(或导电单质)(Pt和石墨为惰性电极,即本身不会得失电子)(一种是相对较活泼金属一种是相对较不活泼金属)2.用导线连接后插入电解质溶液中,形成闭合回路.3.要发生自发的氧化还原反应.
原电池工作原理
原电 原电池池是将一个能自发进行的氧化还原反应的氧化反应和还原反应分别在原电池的负极和正极上发生,从而在外电路中产生电流.负极发生氧化反应,正极发生还原反应,简易记法:负失氧,正得还.
原电池的电极的判断:
负极:电子流出的一极;化合价升高的一极;发生氧化反应的一极;活泼性相对较强(有时候也要考虑到电解质溶液对两极的影响)金属的一极.
正极:电子流入的一极;化合价降低的一极;发生还原反应的一极;相对不活泼(有时候也要考虑到电解质溶液对两极的影响)的金属或其它导体的一极.
在原电池中,外电路为电子导电,电解质溶液中为离子导电.
原电池的判定: (1)先分析有无外接电路,有外接电源的为电解池,无外接电源的可能为原电池;然后依据原电池的形成条件分析判断,主要是“四看”:看电极——两极为金属或导电单质且存在活泼性差异(燃料电池的电极一般为惰性电极);看溶液——两极插入电解质中;看回路——形成闭合回路或两极直接接触;看本质——有无氧化还原反应.
(2)多池相连,但无外接电源时,两极活泼性差异最大的一池为原电池,其他各池可看做电解池.
------------------------------------分割线----------------------------------------------------------------------
没有涉及盐桥!
盐桥:作用原理
在两种溶液之间插入盐桥以代替原来的两种溶液的直接接触,减免和稳定液接电位(当组成或活度不同的两种电解质接触时,在溶液接界处由于正负离子扩散通过界面的离子迁移速度不同造成正负电荷分离而形成双电层,这样产生的电位差称为液体接界扩散电位,简称液接电位),使液接电位减至最小以致接近消除. 防止试液中的有害离子扩散到参比电极的内盐桥溶液中影响其电极电位.
此题是电镀:
在盛有电镀液的镀槽中,经过清理和特殊预处理的待镀件作为阴极,用镀覆金属制成阳极,两极分别与直流电源的负极和正极联接.电镀液由含有镀覆金属的化合物、导电的盐类、缓冲剂、pH调节剂和添加剂等的水溶液组成.通电后,电镀液中的金属离子,在电位差的作用下移动到阴极上形成镀层.阳极的金属形成金属离子进入电镀液,以保持被镀覆的金属离子的浓度.在有些情况下,如镀铬,是采用铅、铅锑合金制成的不溶性阳极,它只起传递电子、导通电流的作用.电解液中的铬离子浓度,需依靠定期地向镀液中加入铬化合物来维持.电镀时,阳极材料的质量、电镀液的成分、温度、电流密度、通电时间、搅拌强度、析出的杂质、电源波形等都会影响镀层的质量,需要适时进行控制.1年前查看全部
- 电镀液中添加的络合剂的目的是什么
电镀液中添加的络合剂的目的是什么
是为了与金属离子结合防止金属离子沉淀稳定电镀液还是为了控制放点金属离子的放电沉积速度? Linda761年前1
Linda761年前1 -
 自古不留名 共回答了23个问题
自古不留名 共回答了23个问题 |采纳率100%其实你的理解很对,络合剂其实是与镀液主盐络合,形成更稳定的金属络合离子,这样就增加了浓度极化和电化学极化,使金属沉积速度减慢,镀层更为细致.也就是说你的两个猜测都对,可能理解的侧重点有所不同.1年前查看全部
- 关于电解和电镀的放电顺序电镀是用ZnCl2作电镀液是锌得电子 电解时ZnCl2溶液中却是氢得电子是为什么
 arthurzhou1年前1
arthurzhou1年前1 -
 szfssj 共回答了19个问题
szfssj 共回答了19个问题 |采纳率100%影响离子放电顺序的因素有多种,如离子本性,离子浓度,电极材料,电流密度等等.中学所学习的放电顺序涉及了"离子本性".而未提离子浓度的影响.
你上面所说就是这样的问题.
电镀时用的ZnCl2浓溶液,浓度大时,Zn2+放电能力强(得电子能力强)于水中的H+,故是Zn2+得电子被还原.
中学做电解ZnCl2水溶液实验时,用的是ZnCl2稀溶液,浓度小时,Zn2+放电能力弱,故是溶液中的H+被还原生成H2.1年前查看全部
- 在铁制品上镀铜时,镀件为阳极,铜盐为电镀液.为什么不对
 浪客剑心_林枫1年前2
浪客剑心_林枫1年前2 -
 wokankkkk 共回答了17个问题
wokankkkk 共回答了17个问题 |采纳率94.1%镀件应在阴极,放在阳极镀件就溶解了1年前查看全部
- 应用题(今天必须写完)又一个长方形电镀槽,槽内有一圆柱形的零件完全侵在电镀槽中,已知电渡槽的长为2米,宽为1米,电镀液面
应用题(今天必须写完)
又一个长方形电镀槽,槽内有一圆柱形的零件完全侵在电镀槽中,已知电渡槽的长为2米,宽为1米,电镀液面高为0.5米,零件的底面直径为0.4米,当零件从电镀液中取出后液面下降了0.03米,那么零件高为多少米?(派=3.14) cockxxx1年前2
cockxxx1年前2 -
 xxfvitop 共回答了18个问题
xxfvitop 共回答了18个问题 |采纳率88.9%公式:V=abh
=2*1*0.3
=0.06(平方米)
3.14*[(0.4/2)*(0.4/2)]=0.125
0.06/0.125=0.48(m)1年前查看全部
- 用铜电镀铁时,可以用碳棒作阳极,氯化铜溶液作电镀液,铁作阴极吗?为什么?电镀的本质是什么?
 陽光魅力1年前3
陽光魅力1年前3 -
 O四鲜烤麸O 共回答了15个问题
O四鲜烤麸O 共回答了15个问题 |采纳率86.7%可以 阳极 4氢氧根离子-4e——2H2O+O2
阴极2铜离子+4e——2Cu
阳极的镀层金属失去电子,形成金属阳离子进入溶液,在溶液中的金属阳离子在阴极待镀物品上得到电子,表面覆盖一层镀层金属1年前查看全部
- 电镀时为什么必须用含有镀层离子溶液做电镀液
 fjtiti1年前1
fjtiti1年前1 -
 ksgimi 共回答了19个问题
ksgimi 共回答了19个问题 |采纳率94.7%因为阳极金属不纯 要消耗电镀液里的金属阳离子1年前查看全部
- 电镀铜实验中,详细的反应过程是怎么样的?(电镀液是CuSO4、待镀铁制品、铜片)
 ee下的混蛋1年前2
ee下的混蛋1年前2 -
 vicky0718 共回答了17个问题
vicky0718 共回答了17个问题 |采纳率94.1%首先按照金属活动性顺序排
阳极活泼金属>I->Cl->OH-〉含氧酸根
阴极Ag+>Fe3+>Cu2+>H+>Fe2+
按此顺序谁大谁先消耗(但不会消耗干净,出的顺序与浓度也有关)出(OH-出的O2)
阴极铁片:Cu2+ + 2e- = Cu
阳极铜片:Cu - 2e- = Cu2+
阴极接电源负极
另一个同理1年前查看全部
- 电镀液一般使用金属离子的配合物溶液的原因
 gaoaidong1年前1
gaoaidong1年前1 -
 最爱扇子 共回答了16个问题
最爱扇子 共回答了16个问题 |采纳率81.3%电镀时,镀层的质量和电镀速度与溶液中该金属例子的浓度有关.
如果电镀时不使用配合物(即络合物),随着电镀的进行,溶液里金属例子的浓度会发生变化,不利于电镀过程的控制.使用了络合物,让络合剂先把金属例子保护起来,电镀时再慢慢释放,就能缓和电镀时金属离子浓度的变化,有利于电镀过程的控制.1年前查看全部
- 铁钉镀锌的电镀液电镀液的成分是氯化锌、氯化钾、硼酸.用氯化锌是显然的,但为什么要用氯化钾和硼酸呢?如果硼酸是为了调节PH
铁钉镀锌的电镀液
电镀液的成分是氯化锌、氯化钾、硼酸.用氯化锌是显然的,但为什么要用氯化钾和硼酸呢?如果硼酸是为了调节PH为酸性,为什么不用盐酸? 遭遇健忘1年前1
遭遇健忘1年前1 -
 kinghuang08 共回答了14个问题
kinghuang08 共回答了14个问题 |采纳率85.7%氯化锌是主盐,氯化钾是导电盐,又是锌离子的弱配位体氯离子的来源.硼酸是缓冲剂,调节PH在5左右.稀盐酸也可以调节ph1年前查看全部
- 以KCL和ZnCL2混合液为电镀液在铁制品上镀锌
以KCL和ZnCL2混合液为电镀液在铁制品上镀锌
因部分电能转化为热能,电镀时通过的电量与锌的析出量无确定关系 这句话为什么是错的?
我这么想的,本来一定的电子,被导线的电阻消耗掉一部分后,不能确定多少能通过去啊? luoyuping853331年前2
luoyuping853331年前2 -
 空荡荡的秋千 共回答了23个问题
空荡荡的秋千 共回答了23个问题 |采纳率87%根据法拉第定律,电镀时通过的电量与析出的金属量有确定关系.1年前查看全部
- 怎样用碘滴定电镀液中锡离子?
 送别孤独1年前3
送别孤独1年前3 -
 vasusnerve 共回答了20个问题
vasusnerve 共回答了20个问题 |采纳率95%具体是什么镀液?二价锡:移取镀液V ml(移取的体积根据含锡量决定)至碘量瓶中,加水50ml,盐酸10ml,淀粉指示剂5ml,用碘标准溶液滴至变蓝为终点,二价锡含量(g/L)=碘标液摩尔浓度*碘标液体积*118.7/V.总锡移取镀液V ml(移取的体积根据含锡量决定)至碘量瓶中,加水50ml,盐酸20ml,缓慢加铝片3G,盖上盖式漏斗,反应完全,冷却后,用碘标准溶液滴至变蓝为终点,锡含量(g/L)=碘标液摩尔浓度*碘标液体积*118.7/V1年前查看全部
- 铜金合金用途广泛,而且Cu的化合物在科学研究和工业生产中具有许多用途,如CuSO4溶液常用作电解液、电镀液等.金稳定性强
铜金合金用途广泛,而且Cu的化合物在科学研究和工业生产中具有许多用途,如CuSO4溶液常用作电解液、电镀液等.金稳定性强,常作为首饰.请回答以下问题:
(1)CuSO4可由金属铜与浓硫酸反应制备,该反应的化学方程式为Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O△ .Cu+2H2SO4(浓);
CuSO4+SO2↑+2H2O△ .
(2)CuSO4粉末常用来检验一些有机物中的微量水分,其原因是______;SO42-中S原子的杂化轨道类型是______;
(3)元素金(Au)处于周期表中的第六周期,与Cu同族,Au原子最外层电子排布式为______;一种铜金合金晶体具有面心立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子数量之比为______;该晶体中,原子之间的作用力是______;若该晶体的晶胞边长为a nm,则合金的密度为[0.65a3  求不他1年前0
求不他1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
大家在问
- 1猴子分桃有一堆桃,每只猴子分3个余1个,分4个余2个,分5个余3个,分6个余4个,这堆桃子至少有多少个?
- 2设Sn是等比数列{an}的前n项的和,若a3+2a6=0,则S6S3的值是______.
- 3请问50%氯化铝溶液怎么配制?最近看到一篇文献,里面写着50% (w/v) AlCl3 cross-linker sol
- 4Last year I _ my dad to give up smoking,but failed.A.advised
- 5请用化学符号、元素符号的意义或数字“2”的意义填写下列空白:
- 6如图,在正方形ABCD中,点E、F分别在AB、DC上,点G、H分别在AD、BC上,且EF与GH所夹的
- 7he lives in shanghai 变反义疑问句
- 82010年六年级一单元语文试题
- 919+199+1999+……+199……99(2002个9)
- 10下雨的时候我们会听见什么声音
- 11小明在探究利用杠杆做功的实践活动中,所用的杠杆是一根质量均匀、重为5N的硬棒,他将棒的一端固定,把重为15N的物体挂在棒
- 12p是双曲线x的平方/a的平方-y的平方/b的平方=1右支上一点,F为右焦点,F1、F2分别为其左右焦点且焦距为2c
- 13你有2个罐子,装者50个红色玻璃求和50个兰色的玻璃球.随意拿起个罐子拿出一个玻璃球,怎样最大程度的增加拿红球的机会,利
- 14请各位英语达人们帮我把英语30-40分提高到及格
- 15某年有52个星期零2天,这一年共有几天

