(2012•斗门区一模)物理知识在平时的生产、生活中有着广泛的应用,下列说法中正确的是( )
 yugang4682022-10-04 11:39:541条回答
yugang4682022-10-04 11:39:541条回答A.手机备用电池不能与硬币放在一起,主要是为了防止电池两极被硬币短路而损坏
B.有些家用电器使用三脚插头和三孔插座主要是为了增强三脚插头使用时的稳定性
C.电线的芯线外面包一层塑料,主要是为了保护里面的芯线不受腐蚀
D.电工用的尖嘴钳钳柄装有橡胶套,主要是为了使劲握钳柄时不至于太痛

已提交,审核后显示!提交回复
共1条回复
 大约在冬季yy 共回答了21个问题
大约在冬季yy 共回答了21个问题 |采纳率95.2%- 解题思路:根据导电性的不同,材料可分为导体,半导体,绝缘体三大类,容易导电的物体叫导体,不容易导电的物体叫绝缘体,导电性能介于导体与绝缘体之间的叫半导体.根据物质的导电性分析各个选项.
A、硬币是导体,说法正确;
B、家用电器使用三脚插头和三孔插座主要是为了让用电器的金属外壳与大地相连,防止发生触电事故,说法错误;
C、电线的芯线外面包一层塑料,主要是为了漏电或造成触电,说法错误;
D、电工用的尖嘴钳钳柄通常都装有橡胶套,是利用橡胶是绝缘体,不会导电,可以防止触电,说法错误.
故选A.点评:
本题考点: 电路的三种状态;绝缘体;插座的构造与工作方式.
考点点评: 本题考查了导体和绝缘体的应用,属于基础题目. - 1年前
相关推荐
- 斗门区民族特色(作文)400字左右
斗门区民族特色(作文)400字左右
斗门区民族特色(作文)400字左右
3月13日上午之前要。 elvadoki1年前2
elvadoki1年前2 -
 liluye925 共回答了11个问题
liluye925 共回答了11个问题 |采纳率90.9%舞龙醒狮
斗门舞龙醒狮为民间绝技,斗门县莲溪镇的舞龙队曾代表斗门县到珠海市参加过各类巡游演出,龙生虎猛,当然要大显身手.醒狮在斗门更是平常,大小庆典都要出动,春节几天,各村镇的醒狮队伍纷纷进城来表演,为各商铺祈求好运,同时也采得一些过年利是,在一阵阵锣鼓声中完成各种高难度的动作,并非一件容易的事,图个新年大吉大利,纵使辛苦一点亦无所谓.
斗门莲洲舞龙于2007年被列入珠海市非物质文化遗产保护名录,这项传统文化得到更好的传承和发扬.今年参加巡游的莲洲金龙、银龙均为特意定制的新龙.金龙代表“龙公”,银龙代表“龙母”,每条均超过50米,有“猪仔笼”23个,每个间隔2米,每支龙队由40人组成表演队伍.
斗门醒狮:驱邪避害迎吉祥
斗门区民间醒狮活动最早出现在明朝中叶,距今已有400多年的历史,至清末民初醒狮表演日渐兴盛,成为一门传统艺术活跃于民间.现全区共有32支醒狮队,队员600多人.斗门醒狮属于南狮技艺,融武术、舞蹈、音乐为一体,曾多次在省、市级的各类醒狮比赛中获得优异的成绩.在本次巡游中,斗门醒狮艺人向更高难度挑战他们将在最高达4米的移动高桩和高梯上,一展醒狮的高超技艺.
元宵大巡游
正月+五珠海元宵大巡游是展示本土传统文化尤其是非物质文化遗产的最好窗口.斗门水上婚嫁、三灶鹤舞、乾务飘色,咸水歌、鹤歌鹤舞等,影响力越来越大,是珠海民间艺术的缩影.据了解,几年来,大巡游的演员队伍和巡游规模一年比一年大,观众也一年比一年多,不少外地观众特地赶来观看,尤其澳门市民一直关注大巡游,港澳也派出表演方阵参加,凸显出大巡游的影响力也一年比一年大.形成‘元宵节到珠海看民间艺术大巡游’的概念,大巡游打造成整个珠三角的节庆文化品牌,一个特别热闹的节日.珠海打造传统节庆文化和推动经济发展得到了很好的结合.大巡游不仅是一个文化品牌项目,更是一个旅游和商业项目,带动了本地旅游业的发展.它和沙滩音乐派对等一起,为珠海城市文化影响力发挥了重要作用.大巡游在弘扬传统艺术、引导民间风俗、活跃社区文化、增添节日喜庆气氛上,都能起到正面的鼓舞作用.
珠海飘色是传统民间艺术,起源于明朝天启年间,(珠海乾务镇人)梁国栋任江西省彭泽县令时由江西传入,至今已有300多年的历史.乾务飘色多取材于民间故事,造型奇特,制作工艺精致.至今保留人工抬色的传统,每队飘色均辅有领路牌、罗伞、护色等,阵容庞大,色彩夺目,观赏性强.1年前查看全部
- (2012•斗门区一模)人类生活离不开金属.
 (2012•斗门区一模)人类生活离不开金属.
(2012•斗门区一模)人类生活离不开金属.
(1)铁是生活中常用的金属.如图是某“取暖片”外包装的图片.该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热.
①发热剂需接触到空气才会发热,原因是铁要与______、______等物质共同作用才会生锈.
②推测发热剂成分中氯化钠的作用是______.
(2)应用金属活动性顺序能帮助我们进一步学习金属性质.
已知下列各组物质间均能发生置换反应.
A.Fe 和CuSO4溶液B.Mg和MnSO4溶液C.Mn和FeSO4溶液
①写出Fe 和CuSO4溶液反应的化学方程式______.
②Mn、Fe、Mg、Cu四种金属的活动性由强到弱的顺序______. happybabyhappy1年前1
happybabyhappy1年前1 -
 wabd 共回答了18个问题
wabd 共回答了18个问题 |采纳率77.8%解题思路:(1)铁与水和氧气充分接触时容易生锈,盐溶液能够促进铁生锈;
(2)铁和硫酸铜容易反应能生成铜和硫酸亚铁;由置换反应可以判断金属的活泼性顺序.(1)①发热剂需接触到空气才会发热,原因是铁要与水、氧气等物质共同作用才会生锈.故答案为:水、氧气.
②发热剂成分中氯化钠的作用是加速铁粉生锈,更快地放出热量.故答案为:加速铁粉生锈,更快地放出热量.
(2)①铁和硫酸铜反应的化学方程式为:Fe+CuSO4═FeSO4+Cu.
②在金属活动性顺序中,排在前面的金属能够把排在后面的金属从它的盐溶液中置换出来,由下列各组物质间均能发生置换反应可知,Mn、Fe、Mg、Cu四种金属的活动性由强到弱的顺序为:Mg、Mn、Fe、Cu.
故答案为:Mg、Mn、Fe、Cu.点评:
本题考点: 金属锈蚀的条件及其防护;金属活动性顺序及其应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题主要考查铁生锈的条件和化学方程式的书写等方面的知识,书写化学方程式时要注意遵循质量守恒定律.1年前查看全部
- (2013•中山一模)斗门区今年的春夏季节举办以“油菜花”、“龙舟比赛”等为主题的活动.当游客漫步在金黄色的油菜花的海洋
 (2013•中山一模)斗门区今年的春夏季节举办以“油菜花”、“龙舟比赛”等为主题的活动.当游客漫步在金黄色的油菜花的海洋,到处都弥漫着花的清香,从物理学的角度看,这是______现象,这种现象说明______;而划龙舟比赛中(如图),运动员使用的船桨属于______(填“省力”或“费力”)杠杆.
(2013•中山一模)斗门区今年的春夏季节举办以“油菜花”、“龙舟比赛”等为主题的活动.当游客漫步在金黄色的油菜花的海洋,到处都弥漫着花的清香,从物理学的角度看,这是______现象,这种现象说明______;而划龙舟比赛中(如图),运动员使用的船桨属于______(填“省力”或“费力”)杠杆.  冰镇可乐的夏天1年前1
冰镇可乐的夏天1年前1 -
 沉水沉舟 共回答了14个问题
沉水沉舟 共回答了14个问题 |采纳率92.9%解题思路:(1)组成物质的分子永不停息地做无规则的运动,扩散现象证明了分子不停地做无规则运动;
(2)根据杠杆的平衡条件:动力×动力臂=阻力×阻力臂,知道阻力臂大于动力臂时,动力大于阻力,杠杆是费力杠杆.(1)到处都弥漫着花的清香,是因为组成荷花的分子不停地做无规则的运动,分子通过扩散现象使周围空气充满花香分子,所以游客会闻到花的清香;
(2)运动员使用的杠杆阻力臂大于动力臂,属于费力杠杆.
故答案为:扩散,分子不停做无规则运动;费力.点评:
本题考点: 扩散现象;杠杆的分类.
考点点评: 本题考查了扩散现象、分子动理论、杠杆等物理知识,是一道学科综合题;题目难度不大,只要熟练掌握基础知识即可解答.1年前查看全部
- (2012•斗门区一模)第六次全国人口普查数据显示珠海市常住人口约为1560000人,用科学记数法表示这个数为( )
(2012•斗门区一模)第六次全国人口普查数据显示珠海市常住人口约为1560000人,用科学记数法表示这个数为( )
A.1.56×104
B.15.6×105
C.1.56×106
D.0.156×107 dkjz9981年前1
dkjz9981年前1 -
 微风无澜 共回答了14个问题
微风无澜 共回答了14个问题 |采纳率100%解题思路:科学记数法的表示形式为a×10n的形式,其中1≤|a|<10,n为整数.确定n的值是易错点,由于1560000万有7位,所以可以确定n=7-1=6.1 560 000=1.56×106.
故选C.点评:
本题考点: 科学记数法—表示较大的数.
考点点评: 此题考查科学记数法表示较大的数的方法,准确确定a与n值是关键.1年前查看全部
- (2012•斗门区一模)如图甲所示,塑料挂钩的吸盘能“吸”在平滑的墙面上,是由于______的存在.挂钩能够承受一定的拉
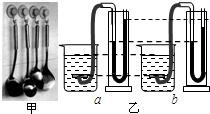 (2012•斗门区一模)如图甲所示,塑料挂钩的吸盘能“吸”在平滑的墙面上,是由于______的存在.挂钩能够承受一定的拉力而不脱落,是由于吸盘受到墙面的______力作用.如图乙所示,有两个完全相同的容器,分别盛有适量的水和浓盐水,某同学用压强计鉴别这两种液体,则图______(a/b)中装的是盐水.
(2012•斗门区一模)如图甲所示,塑料挂钩的吸盘能“吸”在平滑的墙面上,是由于______的存在.挂钩能够承受一定的拉力而不脱落,是由于吸盘受到墙面的______力作用.如图乙所示,有两个完全相同的容器,分别盛有适量的水和浓盐水,某同学用压强计鉴别这两种液体,则图______(a/b)中装的是盐水.  dillai1年前1
dillai1年前1 -
 qq战旗 共回答了16个问题
qq战旗 共回答了16个问题 |采纳率81.3%解题思路:塑料吸盘是挤出里面的空气后,在大气压的作用下才被压在墙面上的;物体对它的拉力是向下的,而阻碍其向下的力是吸盘与墙面间的摩擦力;判断图乙中两容器内的液体应注意观察U形管中液面的高度差.是大气压的存在使吸盘被压在了墙面上的;阻碍拉力的力是吸盘与墙面之间的摩擦力;
读图乙可知,a、b两容器中,金属盒的深度相同,U形管中的液面高度差a大于b,因此,a中装的是盐水.
故答案为:大气压;静摩擦力(摩擦力);a.点评:
本题考点: 探究液体压强的特点实验;大气压的综合应用.
考点点评: 吸盘是利用大气压工作的典型实例,但值得注意的是,它能承受一定的向下的拉力,则是由于拉力与摩擦力是相互平衡的;比较液体内部压强时,要学会观察金属盒的深度与U形管中的液面高度差,这是判断压强大小的关键.1年前查看全部
- (2012•斗门区一模)建设城市,市政府向市民征集到的下列措施中,你认为不可行的是( )
(2012•斗门区一模)建设城市,市政府向市民征集到的下列措施中,你认为不可行的是( )
A.使用清洁能源代替煤和石油
B.实施绿化工程,防治扬尘污染
C.分类回收垃圾,并露天焚烧
D.使用燃煤脱硫技术,减少SO2污染 sadgjklawlkrhger1年前1
sadgjklawlkrhger1年前1 -
 发条99 共回答了12个问题
发条99 共回答了12个问题 |采纳率100%解题思路:A、根据化石燃料的污染性考虑;
B、根据绿化工程的作用做题;
C、垃圾的处理方法考虑;
D、根据燃煤脱硫技术的意义.A、煤和石油属于化石燃料,燃烧后产生大量的空气污染物,使用清洁能源代替煤和石油就减少了空气污染,故A正确;
B、绿化工程是植树造林对空气有净化作用,防治扬尘污染,故B正确;
C、分类回收垃圾是正确的,露天焚烧就不行了污染了空气,故C错误;
D、使用燃煤脱硫技术,减少SO2污染,也就减少了对空气的污染,故D正确.
故选:C.点评:
本题考点: 防治空气污染的措施;"三废"处理的必要性和一般原则.
考点点评: 通过回答本题知道了减少污染的方法有:使用清洁能源代替煤和石油,实施绿化工程,分类回收垃圾,使用燃煤脱硫技术.1年前查看全部
- (2012•斗门区一模)下面是钠元素和氯元素在元素周期表中的信息和4种粒子的结构示意图.请回答下列问题:
(2012•斗门区一模)下面是钠元素和氯元素在元素周期表中的信息和4种粒子的结构示意图.请回答下列问题:

(1)钠元素的原子序数为______,它与氯元素组成的化合物的化学式为:______.
(2)A、B、C、D属于同种元素的粒子是______(填字母).
(3)D粒子的化学性质与A、B、C中哪一种粒子的化学性质相似______(填字母). swwgg1年前1
swwgg1年前1 -
 也不会再迷惘 共回答了18个问题
也不会再迷惘 共回答了18个问题 |采纳率94.4%解题思路:(1)元素周期表信息中最左上角的数字表示原子序数,依据最外层电子数确定元素的化合价,并所学化学式;
(2)质子数相同的粒子属于同一种元素;
(3)最外层电子数相同的粒子具有相似的化学性质.(1)根据钠元素在元素周期表中信息可知,钠元素的原子序数为11;钠原子的最外层电子数是1个,易失去1个电子,显+1价,氯元素的原子最外层电子数是7个,易得1个电子,化合价显-1价,故二者形成的化学式是NaCl;
(2)质子数相同的粒子属于同一种元素,由图可知A、B种粒子的质子数相同;
(3)最外层电子数相同的粒子具有相似的化学性质.D粒子的最外层电子数为7,与其相同的是C;
故答案为:
(1)11;NaCl;
(2)A、B;
(3)C.点评:
本题考点: 元素周期表的特点及其应用;核外电子在化学反应中的作用;原子结构示意图与离子结构示意图.
考点点评: 本题主要考查对元素周期表中信息的了解和应用,以及粒子结构示意图所表示出的信息和意义.1年前查看全部
- (2006•斗门区二模)在我们的生活中,许多现象与化学有着密切的联系,从下列物质中选择恰当物质的序号填空:①氯化钠 ②食
(2006•斗门区二模)在我们的生活中,许多现象与化学有着密切的联系,从下列物质中选择恰当物质的序号填空:①氯化钠 ②食醋 ③硫酸 ④熟石灰 ⑤活性炭 ⑥CO ⑦甲醇
(1)生理盐水是医疗上常用的溶液,该溶液的溶质是______.
(2)使用铁锅可以有效地预防缺铁性贫血的发生,专家建议在炒菜时加入适量的______效果更好.
(3)农业技术人员对某些菜地的土壤进行分析,发现土壤呈酸性,不利于作物生长.你认为应当施用适量的______来改良土壤结构.
(4)用于除去冰霜异味的是______.
(5)饮用假酒引起中毒导致眼睛失明,原因是假酒中含有______.
(6)用煤炉取暖时易发生中毒,主要是由于室内______排放不畅而引起的. maop61年前1
maop61年前1 -
 爱尚呆呆 共回答了21个问题
爱尚呆呆 共回答了21个问题 |采纳率100%解题思路:根据物质的性质进行分析,氯化钠常用于配制生理盐水,食醋具有酸性,能与铁反应生成易被人体吸收的亚铁盐,硫酸具有酸性,可用于金属去锈,熟石灰具有碱性,能用于改良酸性土壤,活性炭具有吸附性,能吸附异味和色素,一氧化碳具有毒性,能引起煤气中毒,工业酒精中含有的甲醇有毒.(1)氯化钠常用于配制生理盐水,所以本题答案为:①;
(2)食醋具有酸性,能与铁反应生成易被人体吸收的亚铁盐,所以本题答案为:②;
(3)熟石灰具有碱性,能用于改良酸性土壤,所以本题答案为:④
(4)活性炭具有吸附性,能吸附异味和色素,所以本题答案为:⑤;
(5)工业酒精中含有的甲醇有毒,饮用能引起失明,所以本题答案为:⑦;
(6)一氧化碳具有毒性,能引起煤气中毒,所以本题答案为:⑥.点评:
本题考点: 常用盐的用途;常见碱的特性和用途;醋酸的性质及醋酸的含量测定;碳单质的物理性质及用途;常见中毒途径及预防方法.
考点点评: 本题考查了常见物质的用途,完成此题,可以依据物质的性质进行.1年前查看全部
- (2006•斗门区二模)如图是几种常见的实验装置:
(2006•斗门区二模)如图是几种常见的实验装置:
(1)指出仪器名称:甲酒精灯酒精灯乙水槽水槽.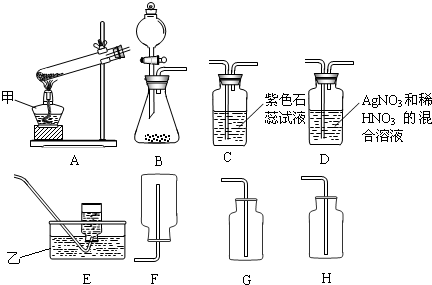
(2)如果用A装置加热固体制取氧气,请指出其中的错误:①试管口没向下倾斜试管口没向下倾斜②试管口少棉花团试管口少棉花团
(3)如果要收集干燥的氧气,通常可选用上述装置中的G或HG或H(填写序号)
(4)实验室制取CO2应选择的发生装置是(填装置编号)BB将药品装入试管之前必须要进行的实验操作是检验装置的气密性检验装置的气密性如果小李准备收集一瓶CO2气体,所选用的收集装置是G或HG或H(填编号)
(5)小李同学将制得的CO2通入澄清石灰水中,未见浑浊.
提出假设1:石灰水可能已变质.
措施:重新配制澄清的石灰水.取5g新买的氢氧化钙粉末放入干净的250mL烧杯中倒入约100mL蒸馏水,搅拌,静置,得到浑浊液.采用过滤的方法除去未溶解的氢氧化钙,除了滤纸,小李还需要哪些仪器?烧杯、漏斗、玻璃棒、铁架台烧杯、漏斗、玻璃棒、铁架台
过滤后,如果所得液体仍然浑浊,小李应该怎样操作?检查实验装置是否严密,改进后再过滤检查实验装置是否严密,改进后再过滤最后所得的澄清的液体是氢氧化钙的饱和饱和(填饱和或不饱和)溶液.
(6)实验与问题:小李同学将制得的CO2通入新制的澄清石灰水中,仍然未见浑浊.
提出假设2:可能错用了较浓的盐酸,使制得的CO2中混入氯化氢气体.
(查资料知道:AgCl是一种白色的固体,它既不溶于水也不溶于稀硝酸)
设计实验方案:甲、乙两组同学选择图中的C或D装置与发生装置连接进行实验.
讨论与交流:
①甲组同学选择C装置,他们不能不能(填“能”或“不能”)证实假设2,理由是二氧化碳的水溶液也能使石蕊溶液变红.二氧化碳的水溶液也能使石蕊溶液变红.
②乙组同学选择D装置,他们能能(填“能”或“不能”)证实假设2,理由是氯化氢的水溶液通入酸化的硝酸银溶液中能产生白色沉淀,二氧化碳的水溶液通入酸化的硝酸银溶液中不能产生白色沉淀氯化氢的水溶液通入酸化的硝酸银溶液中能产生白色沉淀,二氧化碳的水溶液通入酸化的硝酸银溶液中不能产生白色沉淀. DDllee1年前1
DDllee1年前1 -
 weking 共回答了14个问题
weking 共回答了14个问题 |采纳率85.7%(1)图中甲是酒精灯,乙是水槽,故答案为:酒精灯、水槽;
(2)为防止加热时固体中的水蒸气倒流入试管,引起试管的炸裂,试管口要向下倾斜;为防止试管中的固体药品进入导管,要在试管口放一团棉花.故答案为:试管口没向下倾斜、试管口少棉花团;
(3)用排空气法可收集到干燥的氧气,再根据氧气的密度大约空气的密度,我们可知要用向上排空气法收集.故答案为:G或H;
(4)制取二氧化碳不需加热,所以可选用B作为发生装置;二氧化碳密度大于空气的密度,易溶于水,所以我们可以向上排空气法收集二氧化碳;为能保证实验的顺利进行,在放入药品之前一定要检验装置的气密性.故答案为:B、检验装置的气密性、G或H;
(5)过滤实验要用的仪器有:烧杯、漏斗、玻璃棒、铁架台;过滤后,如果所得液体仍然浑浊,要看是否符合“一贴二底三靠”,检查无误后再重新过滤;因为有未溶解的氢氧化钙,所以最后所得的澄清的液体是氢氧化钙的饱和溶液.
故答案为:烧杯,漏斗,玻璃棒,铁架台、检查实验装置是否严密,改进后再过滤、饱和;
(6)①甲组同学选择C装置,他们不能.理由是:二氧化碳的水溶液也能使石蕊溶液变红.故答案为:不能、二氧化碳的水溶液也能使石蕊溶液变红;
②乙组同学选择D装置,他们能.理由是:氯化氢的水溶液通入酸化的硝酸银溶液中能产生白色沉淀,二氧化碳的水溶液通入酸化的硝酸银溶液中不能产生白色沉淀.1年前查看全部
- (2012•斗门区一模)近年来,世界各地地震频发,造成了很大的人员伤亡和财产损失.结合图含钙化合物间的相互转化关系,回答
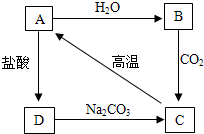 (2012•斗门区一模)近年来,世界各地地震频发,造成了很大的人员伤亡和财产损失.结合图含钙化合物间的相互转化关系,回答下列问题:
(2012•斗门区一模)近年来,世界各地地震频发,造成了很大的人员伤亡和财产损失.结合图含钙化合物间的相互转化关系,回答下列问题:
(1)B的化学式是______.写出D→C反应的化学方程式______.该反应属于______ 反应(填基本类型)
(2)化学反应常伴有能量变化.A与水反应时会______(“吸收”或“放出”)热量.
(3)地震发生的成因很复杂,据有关研究,孕震过程中比较活跃的物质有二氧化碳、氢等.图中C→A就是孕震过程中地壳岩层发生的重要反应之一,该反应的化学方程式是:CaCO3
CaO+CO2↑高温 .CaCO3.
CaO+CO2↑高温 .
(4)氢在目前的地震预测中被公认为是一种灵敏元素.一般认为,高温下地壳中水蒸气和氧化亚铁(FeO)作用会产生氢气和氧化铁(Fe2O3),该反应的化学方程式2FeO+H2O
Fe2O3+H2↑.高温 .2FeO+H2O.
Fe2O3+H2↑.高温 . 爱情的尽头1年前1
爱情的尽头1年前1 -
 donne21 共回答了20个问题
donne21 共回答了20个问题 |采纳率90%解题思路:根据题意,由于A、B、C、D为含钙化合物,又A能与水发生反应,可判断物质A为氧化钙,以此为突破口,可依次判断B为氢氧化钙、C为碳酸钙、D为氯化钙;据此结果,根据题意即物质之间的转变关系,完成问题的解答.(1)由题意可知,含钙的物质A与水反应生成B,根据与水发生反应的常见物质,可判断A为氧化钙,则B为氢氧化钙,其化学式为Ca(OH)2;物质A氧化钙与盐酸反应生成的含钙物质D为氯化钙,因此D→C反应为氯化钙与碳酸钠通过交换成分而生成氯化钠和碳酸钙的复分解反应,反应的化学方程式为CaCl2+Na2CO3=CaCO3↓+2NaCl;
(2)A物质氧化钙遇水反应生成氢氧化钙,放出大量的热;
(3)由题意可知,图中C→A的反应就是碳酸钙在高温条件下分解成氧化钙和二氧化碳,反应的方程式是:CaCO3
高温
.
CaO+CO2↑;
(4)由题意可知,高温下地壳中水蒸气和氧化亚铁(FeO)作用会产生氢气和氧化铁(Fe2O3),该反应的化学方程式是:2FeO+H2O
高温
.
Fe2O3+H2↑.
故答为:(1)Ca(OH)2,CaCl2+Na2CO3=CaCO3↓+2NaCl,复分解;(2)放出;(3)CaCO3
高温
.
CaO+CO2↑;
(4)2FeO+H2O
高温
.
Fe2O3+H2↑.点评:
本题考点: 物质的相互转化和制备;物质发生化学变化时的能量变化;反应类型的判定;书写化学方程式、文字表达式、电离方程式.
考点点评: 熟悉能与水发生反应的物质在本题的解答中相当重要:在初中化学中能与水反应的物质主要为金属氧化物与非金属氧化物两类.1年前查看全部
- (2006•斗门区二模)据报道:2005年5月12日上午7时许,某地的湖面上出现奇怪“景观“,上万条黄鳝笔直地“站“在水
(2006•斗门区二模)据报道:2005年5月12日上午7时许,某地的湖面上出现奇怪“景观“,上万条黄鳝笔直地“站“在水中喘气,吸引许多晨练市民驻足观看,以下分析中不正确的是( )
A.表明近期该湖的水质可能发生了变化
B.水中氨氮成分增加使水体溶氧量大幅减少,黄鳝只有浮上水面“透口气“
C.夜间湖内水生植物的呼吸作用,使得水中含氧量进一步下降的缘故
D.清晨水面气压大,迫使黄鳝浮出水面吸气 聚蓝之心1年前1
聚蓝之心1年前1 -
 angelo211 共回答了15个问题
angelo211 共回答了15个问题 |采纳率86.7%黄鳝的这一呼吸现象是因为水中含氧量降低的缘故
A、水质的改变有可能是水中的含氧量降低,故此选项错误.
B、氨氮成分可使水中的含氧量降低,故此选项错误.
C、呼吸作用会消耗氧气,夜间湖内水生植物的呼吸作用,使得水中含氧量进一步下降,故此选项错误.
D、水面气压大会使水中的气体溶解度变大,因此这不是正确的.故此选项正确.
故选D1年前查看全部
- (2013•斗门区一模)实验室用浓盐酸(质量分数为37%,密度1.19g/cm3)配制100g质量分数为10%的稀盐酸.
(2013•斗门区一模)实验室用浓盐酸(质量分数为37%,密度1.19g/cm3)配制100g质量分数为10%的稀盐酸.其操作步骤是:
a.计算:需要量取浓盐酸______ mL;
b.量取:用规格为______ mL的量筒量取______ mL的浓盐酸倒入烧杯里.
c.溶解:用量筒量取______ mL水倒入盛有浓盐酸的烧杯里,边加边用玻璃棒搅拌,以使盐酸和水______. 70223111年前1
70223111年前1 -
 wintersi 共回答了19个问题
wintersi 共回答了19个问题 |采纳率100%解题思路:配制溶质质量分数一定的盐酸溶液的基本步骤:
a.计算,根据稀释前后溶质的量不变计算浓盐酸的体积;
b.量取,根据a的计算选用合适的量筒,量取浓盐酸;
c.溶解,用量筒量取所需水的体积,溶解.用溶质质量分数为37%浓盐酸配制100g质量分数为10%的稀盐酸,操作步骤为:
a.计算:需量取浓盐酸的体积=100g×10%÷(37%×1.19g/cm3)=22.7mL,所需水的质量=100g-25mL×1.19g/cm3≈73g,即73mL;
b.量取:选用规格为50mL的量筒量取22.7mL的浓盐酸倒入烧杯中;
c.溶用量筒量取73mL水倒入盛有浓盐酸的烧杯里,边加边用玻璃棒搅拌,以便混合均匀.
故答案为:a.22.7;b.50;22.7;c.73;混合均匀.点评:
本题考点: 一定溶质质量分数的溶液的配制.
考点点评: 该考点的命题方向通过设置实验情景,让学生根据所学知识,计算出溶质和溶剂的质量,选用适当的仪器,配制一定溶质质量分数的溶液1年前查看全部
- (2006•斗门区二模)据报道:2005年5月12日上午7时许,某地的湖面上出现奇怪“景观“,上万条黄鳝笔直地“站“在水
(2006•斗门区二模)据报道:2005年5月12日上午7时许,某地的湖面上出现奇怪“景观“,上万条黄鳝笔直地“站“在水中喘气,吸引许多晨练市民驻足观看,以下分析中不正确的是( )
A.表明近期该湖的水质可能发生了变化
B.水中氨氮成分增加使水体溶氧量大幅减少,黄鳝只有浮上水面“透口气“
C.夜间湖内水生植物的呼吸作用,使得水中含氧量进一步下降的缘故
D.清晨水面气压大,迫使黄鳝浮出水面吸气 verca1年前1
verca1年前1 -
 罐头旗子 共回答了11个问题
罐头旗子 共回答了11个问题 |采纳率90.9%解题思路:黄鳝湖面呼吸说明水中含氧量变小,任何使水的含氧量变小的分析都是正确的,D选项中的水面气压大会使水中的气体溶解度变大,因此这不是正确的分析.黄鳝的这一呼吸现象是因为水中含氧量降低的缘故
A、水质的改变有可能是水中的含氧量降低,故此选项错误.
B、氨氮成分可使水中的含氧量降低,故此选项错误.
C、呼吸作用会消耗氧气,夜间湖内水生植物的呼吸作用,使得水中含氧量进一步下降,故此选项错误.
D、水面气压大会使水中的气体溶解度变大,因此这不是正确的.故此选项正确.
故选D点评:
本题考点: 光合作用与呼吸作用.
考点点评: 此题是对生活中的化学知识的应用考查,解题的关键是抓住水中氧气含量降低这一实质性的原因即可.1年前查看全部
- (2012•斗门区一模)小华同学测滑轮组机械效率时所用的实验装置如图所示,小华同学对同一滑轮组进行实验探究,得到了下表中
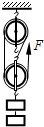 (2012•斗门区一模)小华同学测滑轮组机械效率时所用的实验装置如图所示,小华同学对同一滑轮组进行实验探究,得到了下表中的数据
(2012•斗门区一模)小华同学测滑轮组机械效率时所用的实验装置如图所示,小华同学对同一滑轮组进行实验探究,得到了下表中的数据
(1)将表中数据补充完整.a处填______;b处填______;c处填______项目
次数1 2 3 钩码重/N 4 6 8 钩码上升高度/m 0.1 0.1 0.1 绳端拉力/N 1.8 a 3 绳端上移的距离/m 0.3 b 0.3 机械效率 74% 80% c
(2)实验中拉动弹簧测力计时,要注意匀速直线沿______.
(3)小华用弹簧测力计测力时发现示数有忽大忽小现象,为改变这种现象,小华让弹簧测力计静止下来读数,这样他测得的机械效率将______(选填“变大”、“变小”或“不变”).
(4)分析比较表中的数据,你认为同一滑轮组机械效率发生变化的主要原因是______.
(5)若将此滑轮组换一种绕绳方法,不计摩擦及绳重,滑轮组的机械效率______(选填“变大”、“变小”或“不变”). y4p6d1年前1
y4p6d1年前1 -
 罗小梅 共回答了21个问题
罗小梅 共回答了21个问题 |采纳率100%解题思路:(1)b数据:由滑轮组的绕法,确定绳子的段数;知道物体升高的距离,知道绳子的段数,求出绳端上移的距离.
a数据:知道机械效率、钩码重力、钩码上升的距离、绳端上移的距离,根据η=
=[Gh/Fs]求出绳端的拉力.W有 W总
c数据:知道钩码重力、钩码上升的距离、绳端的拉力、绳端上移的距离,根据η=
=[Gh/Fs]求出机械效率.W有 W总
(2)用滑轮组竖直拉动物体时,绳端要竖直向上或向下匀速直线拉动.
(3)绳端的拉力匀速直线拉动时拉力大于静止时的拉力.根据η=
=[Gh/Fs]判断机械效率的变化.W有 W总
(4)同一滑轮组,提起的物体越重,滑轮组的机械效率越高.
(5)滑轮组的机械效率跟动滑轮的重、绳重、摩擦、提起物体的重有关,跟滑轮组的绕法、物体升高的距离等都没有关系.(1)b数据:由滑轮组的绕法知,物体有三段绳子承担,物体升高了0.1m,所以绳端上移的距离为:s=3h=3×0.1m=0.3m.
a数据:由η=
W有
W总=[Gh/Fs]得,80%=[6N×0.1m/F×0.3m],所以绳端拉力:F=2.5N.
c数据:η'=
W′有
W′总=[G′h′/F′s′]=[8N×0.1m/3N×0.3m]=89%.
(2)如图,用滑轮组向上提升物体,绳端要竖直向上匀速直线拉动.
(3)用滑轮组拉动物体上升时,当弹簧测力计静止时,绳轮之间的摩擦力为零,故额外功减小,总功减小,根据η=
W有
W总=[Gh/Fs],钩码重、钩码上升的距离、物体升高的距离都不变,总功减小,机械效率会变大.
(4)滑轮组的机械效率跟动滑轮的重、绳重、摩擦、提起物体的重有关,同一滑轮组,动滑轮的重、绳重、摩擦不变,提起的物体越重,机械效率越高.所以同一滑轮组机械效率发生变化的主要原因是改变提起的物体重.
(5)在其它条件相同时,改变绳子的绕法,不能改变滑轮组的机械效率.
故答案为:(1)2.5;0.3;89%;(2)竖直向上拉动;(3)变大;(4)改变提起的物体重;(5)不变.点评:
本题考点: 滑轮(组)机械效率的测量实验.
考点点评: 对于滑轮组机械效率的问题,知道物体的重、物体升高的距离、绳端移动的距离、绳端的拉力、机械效率中的任意四个量,η=W有W总=[Gh/Fs],都能求出第五个量.1年前查看全部
- 英语翻译广东省珠海市斗门区湖心路1111号万威美地3栋4单元101房
 颦湘霜梦1年前2
颦湘霜梦1年前2 -
 茉莉爱上香烟 共回答了17个问题
茉莉爱上香烟 共回答了17个问题 |采纳率94.1%中文地址翻译原则
中文地址的排列顺序是由大到小,如:X国X省X市X区X路X号,而英文地址则刚好相反,是由小到大.如上例写成英文就是:X号,X路,X区,X市,X省,X国.掌握了这个原则,翻译起来就容易多了!室RoomX
X号No.X
X单元UnitX
X号楼BuildingNo.X
X街XStreet
X路XRoad
X区XDistrict
X县XCounty
X镇XTown
X市XCity
X省XProvince
请注意:翻译人名、路名、街道名等,最好用拼音.
中文地址翻译范例:
宝山区示范新村37号403室
Room403,No.37,SiFangResidentialQuarter,BaoShanDistrict
所以,
陕西,西安,高新路,31号 应翻译为:
No.31,GaoxinStreet,Xi'an,Shaanxi
是否可以解决您的问题?1年前查看全部
- 英语翻译珠海市鹏森电子科技有限公司珠海市斗门区井岸镇新青五路2号(厂房C)A面第三层和B面第一层、宿舍楼
 hrdangan1年前1
hrdangan1年前1 -
 qiwz 共回答了18个问题
qiwz 共回答了18个问题 |采纳率88.9%Zhuhai Peng Sen Electronic Technology Co.,Ltd.
Zhuhai city Doumen District Jing An Zhen Xin Qing Road five No.2 (plant C) A surface layer third and B surface of the first layer,dormitory1年前查看全部
- (2012•斗门区一模)分解因式:ab3-ab=______.
 金色白兰地1年前1
金色白兰地1年前1 -
 liliwen1977 共回答了21个问题
liliwen1977 共回答了21个问题 |采纳率95.2%解题思路:先提取公因式ab,再对余下的多项式利用平方差公式继续分解.ab3-ab,
=ab(b2-1),
=ab(b+1)(b-1).点评:
本题考点: 提公因式法与公式法的综合运用.
考点点评: 本题考查了提公因式法与公式法进行因式分解,一个多项式有公因式首先提取公因式,然后再用其他方法进行因式分解,同时因式分解要彻底,直到不能分解为止.1年前查看全部
- (2013•斗门区一模)化学就在我们身边,现有以下常见的物质:①Ne ②H2O
(2013•斗门区一模)化学就在我们身边,现有以下常见的物质:①Ne②H2O③H2SO4④Na2CO3⑤Ca(OH)2
请选择适当物质的序号填空:
(1)最常用的溶剂是______;
(2)可用于制造霓虹灯的是______;
(3)可用于金属表面除锈的是______;
(4)可用于造纸、纺织工业的盐是______;
(5)可用于改良酸性土壤的是______. isabella_yt1年前1
isabella_yt1年前1 -
 redink2007 共回答了21个问题
redink2007 共回答了21个问题 |采纳率85.7%解题思路:物质的性质决定物质的用途,根据常见物质的性质和用途分析回答;(1)水能溶解许多种物质,是最常用的溶剂;
(2)由于稀有气体在通电时能发出有色的光,所以,氖气可用于制造霓虹灯;
(3)由于酸能与某些金属氧化物反应,硫酸可用于金属表面除锈;
(4)碳酸钠是一种可用于造纸、纺织工业的盐;
(5)氢氧化钙是一种碱,能与酸发生中反应,可用于改良酸性土壤.
故答为:(1)②;(2)①;(3)③;(4)④;(5)⑤.点评:
本题考点: 常见的溶剂;常见气体的用途;酸的物理性质及用途;常见碱的特性和用途;常用盐的用途.
考点点评: 本题主要考查了物质的用途,完成此题,可以依据物质的性质进行.1年前查看全部
- (2012•斗门区一模)化学就在我们身边,下列叙述不是化学变化的是( )
(2012•斗门区一模)化学就在我们身边,下列叙述不是化学变化的是( )
A.人吃进的食物逐渐被消化
B.人体的呼吸作用
C.电动车充电时的能量转化
D.水在冰箱里结成冰 被遗忘的条例1年前1
被遗忘的条例1年前1 -
 谁站在谎言背后 共回答了26个问题
谁站在谎言背后 共回答了26个问题 |采纳率80.8%解题思路:化学变化的特征是:有新物质生成.判断物理变化和化学变化的依据是:是否有新物质生成.食物逐渐被消化,生成新物质;人体的呼吸是吸入氧气,呼出二氧化碳;电动车充电时,应该是电能转化为化学能,本质是电池发生了氧化还原反应;水结冰是水分子由液态变为固态.A、食物逐渐被消化,生成新物质,属于化学变化,故选项错误;
B、人体的呼吸是吸入氧气,呼出二氧化碳,属于化学变化,故选项错误;
C、电动车充电时,应该是电能转化为化学能,本质是电池发生了氧化还原反应,属于化学变化,故选项错误;
D、水结冰是水分子由液态变为固态,属于物理变化,故选项正确;
故选D点评:
本题考点: 化学变化和物理变化的判别.
考点点评: 本考点考查了物理变化和化学变化的区别,基础性比较强,只要抓住关键点:是否有新物质生成,问题就很容易解决.本考点主要出现在选择题和填空题中.1年前查看全部
- (2013•斗门区一模)在《我与化学》活动中,某兴趣小组的同学在实验室用含有少量生石灰的NaCl固体配制一定质量分数的N
(2013•斗门区一模)在《我与化学》活动中,某兴趣小组的同学在实验室用含有少量生石灰的NaCl固体配制一定质量分数的NaCl溶液.实验步骤如下图所示:
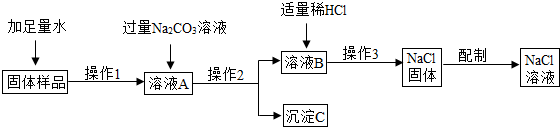
请回答:
(1)在“固体样品”中加入水时所发生反应的化学方程式为______.
(2)“溶液A”中所含溶质为______和______(填化学式),加入“过量Na2CO3”所发生反应的化学方程式为______.
(3)在“操作2”中,要用到的玻璃仪器除玻璃棒、烧杯外,还有______.
(4)加入“适量HCl”的目的是______. xx相处1年前1
xx相处1年前1 -
 84925040 共回答了10个问题
84925040 共回答了10个问题 |采纳率80%解题思路:本题关键是要分析流程图,结合实验基本操作和物质的化学性质进行分析解答.
(1)生石灰就是CaO,它可以与水反应,方程式为:CaO+H2O=Ca(OH)2
(2)CaO与水反应的产物是Ca(OH)2,所以溶液A包括Ca(OH)2和NaCl,Ca(OH)2和Na2CO3符合复分解反应发生的条件,所以两者会发生反应,
(3)操作2是过滤操作,根据过滤操作所要用到的仪器分析即可,
(4)因为溶液A中所加的Na2CO3溶液是过量的,所以溶液B中有剩余的Na2CO3和生成的NaOH,加入适量的盐酸是为了除去Na2CO3和NaOH,同时不引进新的杂质.(1)CaO可以与水反应,方程式为:CaO+H2O=Ca(OH)2
故答案为:CaO+H2O=Ca(OH)2
(2)溶液A中有生成的Ca(OH)2和样品中的NaCl,
Ca(OH)2和Na2CO3发生反应的方程式为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
故答案为:Ca(OH)2和NaCl; Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
(3)因为操作2是过滤操作,所以还需要漏斗,
故答案为:漏斗
(4)溶液B中有杂质NaOH和Na2CO3,NaOH和Na2CO3均会与盐酸反应,所以加入适量盐酸的目的就是除去NaOH和Na2CO3
故答案为:除去过量的Na2CO3和生成的NaOH.点评:
本题考点: 混合物的分离方法;过滤的原理、方法及其应用;物质的相互转化和制备;书写化学方程式、文字表达式、电离方程式.
考点点评: 此题对同学们的要求很高,顺利解答此题的前提条件是会分析流程图,若流程图不会分析,可以说下面的题目是一个也做不出来的,在分析流程图时,需要注意其中所加物质的量的多少,如:过量或适量等.1年前查看全部
- (2006•斗门区二模)久置于空气中的石灰水,其表面会形成一层白膜.此时溶液的pH比变化前溶液的pH( )
(2006•斗门区二模)久置于空气中的石灰水,其表面会形成一层白膜.此时溶液的pH比变化前溶液的pH( )
A.偏大
B.偏小
C.一样
D.无法比较 牌楼1年前1
牌楼1年前1 -
 飞叶覆雪 共回答了15个问题
飞叶覆雪 共回答了15个问题 |采纳率80%解题思路:久置于空气中的石灰水,其表面会形成一层白膜是因为石灰水与空气中的二氧化碳反应生成难溶于水的碳酸钙的原因,其反应的文字表达式为:二氧化碳+氢氧化钙→碳酸钙+水,由于石灰水发生化学变化而变质,故碱性减弱,溶液的pH比变化前溶液的pH会变得偏小.据题给信息,久置于空气中的石灰水发生了如下反应:二氧化碳+氢氧化钙→碳酸钙+水,即形成的白膜就是生成的难溶于水的碳酸钙,由于石灰水发生化学变化而变质,故碱性减弱,溶液的pH比变化前溶液的pH会变得偏小.
故选 B点评:
本题考点: 碱的化学性质;溶液的酸碱性与pH值的关系.
考点点评: 考查学生石灰水与二氧化碳的反应实质,明确溶液的酸碱性与pH值的关系,理论和生活实际慢慢衔接.1年前查看全部
- 〔宇宙银河系地球亚洲中国广东〕珠海香洲区的香洲七小距离斗门区神秘岛有多远.
〔宇宙银河系地球亚洲中国广东〕珠海香洲区的香洲七小距离斗门区神秘岛有多远.
主要问题是路线、走哪路车、需要多长时间 英格丽饱满1年前1
英格丽饱满1年前1 -
 lhn_7804 共回答了20个问题
lhn_7804 共回答了20个问题 |采纳率90%在拱北、拱北口岸下车1年前查看全部
- (2012•斗门区一模)(1)请完成图1中的光路图.
(2012•斗门区一模)(1)请完成图1中的光路图.
(2)请在图2中,作出静止在斜面上重为5N的物体所受重力的示意图.
(3)在图3中,根据通电螺线管的N、S极,分别标出电源的正负极和两小磁针静止时的N、S极.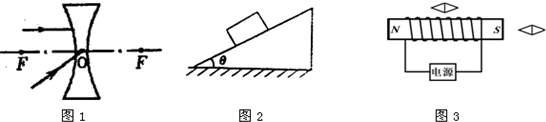
 Ray-8281年前1
Ray-8281年前1 -
 jusanliangyiyi 共回答了23个问题
jusanliangyiyi 共回答了23个问题 |采纳率95.7%解题思路:(1)凹透镜三条特殊光线的作图:
①延长线过另一侧焦点的入射光线经凹透镜折射后将平行于主光轴;
②平行于主光轴的光线经凹透镜折射后变得发散,其折射光线的反向延长线过焦点;
③过光心的光线经凹透镜折射后传播方向不改变.
(2)在受力物体上沿力的方向画一条线段,在线段的末端画一个箭头表示力的方向,线段的起点或终点表示力的作用点;知道力的大小就要标出来;
重力的方向是竖直向下的;重心一般就画在物体的几何中心上.
(3)首先利用螺线管的N、S极,根据安培定则确定螺线管中电流的方向;然后利用磁极间的作用规律确定小磁针的N、S极,从而可以得到答案.(1)平行于主光轴的光线经凹透镜折射后变得发散,其折射光线的反向延长线过焦点;过光心的入射光线,经过凹透镜折射后,其传播方向不变,由此可以画出其折射光线如下图所示:
(2)画重力的示意图时,先找重心,重心就画在物体的几何中心;
重力的方向是竖直向下的,从重心画一竖直向下的线段,标上箭头和字母G,同时标出重力的大小.
故答案为:
(3)从图可知螺线管的N、S极,根据安培定则,伸出右手四指弯曲指向电流的方向,则大拇指所指的方向--通电螺线管的右端为N极,左端为S极.则电源的右端为正极,左端为负极;
根据异名磁极相互吸引、同名磁极相互排斥,上面小磁针的左端为S极,右端为极N.右面小磁针的左端为N极,右端为S极,如图所示: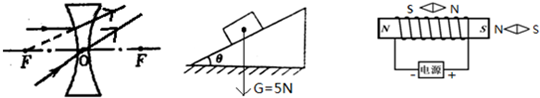
点评:
本题考点: 重力示意图;透镜的光路图;通电螺线管的极性和电流方向的判断.
考点点评: 图3考查了磁极间的相互作用规律和右手螺旋定则的运用.根据安培定则,利用螺线管的NS极和线圈绕向来确定电源的正负极是解决此题的关键.这两个知识点相结合的题目很多,一定要掌握.1年前查看全部
- (2013•斗门区一模)为了测定某品牌纯碱(杂质为氯化钠)中碳酸钠的质量分数,进行了如下实验:①在三个烧杯中都加入了11
(2013•斗门区一模)为了测定某品牌纯碱(杂质为氯化钠)中碳酸钠的质量分数,进行了如下实验:①在三个烧杯中都加入了11g样品及足量的水配成溶液;②向三个烧杯中加入质量不等的CaCl2粉末;③将充分反应后生成的沉淀过滤、洗涤、干燥得到wg的白色固体.实验数据如下:
回答下列问题:烧杯Ⅰ 烧杯Ⅱ 烧杯Ⅲ 加入CaCl2的质量/g 5.55 12 15 W/g 5 10 10
(1)将烧杯Ⅲ中的溶液蒸干,得到______g固体,该固体由______和______组成(只填化学式).
(2)样品中碳酸钠的质量分数是多少? 南加巴瓦1年前1
南加巴瓦1年前1 -
 天籁倾城 共回答了21个问题
天籁倾城 共回答了21个问题 |采纳率76.2%解题思路:本题探究物质的组成是利用碳酸钠和氯化钙的反应,求得11g样品中碳酸钠的质量,由表中数据,5.55g氯化钙不足,10g或12g氯化钙都能使碳酸钠完全反应,所以可根据由10g碳酸钙生成来展开计算.(1)根据表中数据,11g样品中最多生成10g碳酸钙,设11g样品中碳酸钠的质量为X,消耗的氯化钙Yg,
反应生成的氯化钠Zg.则
Na2CO3+CaCl2=CaCO3↓+2NaCl
106111 100 117
XY10gz
106:100=X:10 111:100=Y:10 100:117=10:Z
解得:X=10.6g Y=11.1gZ=11.7g
则11g样品中NaCl为11g-10.6g=0.4g,烧杯Ⅲ中剩余的CaCl2为15g-11.1g=3.9g,生成的氯化钠为11.7g
所以烧杯Ⅲ中的溶液蒸干,得到NaCl和CaCl2
质量为:0.4g+3.9g+11.7g=16g
故答案为:16;NaCl、CaCl2
(2)样品中碳酸钠的质量分数为:[10.6g/11g]×100%=96.4%
故答案为:96.4%点评:
本题考点: 实验探究物质的组成成分以及含量;根据化学反应方程式的计算.
考点点评: 本题思路简单,但计算较繁琐,在确定蒸干烧杯中反应液后的成分时,要注意氯化钠有两部分,原来的和生成的.1年前查看全部
- (2012•斗门区一模)下列是生活中几种常见的镜子:A.平面镜 B.老花镜
(2012•斗门区一模)下列是生活中几种常见的镜子:A.平面镜B.老花镜C.汽车的后视镜D.近视镜.现请你判断其中发生光的折射的是______;能发散光的是______;能会聚光的是______.(填字母代号)
 oliverma_41年前1
oliverma_41年前1 -
 甲猫 共回答了24个问题
甲猫 共回答了24个问题 |采纳率83.3%解题思路:(1)光学器具分成两种镜面:面镜和透镜.面镜利用了光的反射定律,透镜利用了光的折射;
(2)光的反射:光遇到物体时,在物体表面返回到原来介质中的一种现象;穿衣镜、潜望镜、观后镜都是面镜,利用光的反射;
(3)光的折射:光从一种介质斜射入另一种介质或光在不均匀介质中传播时,光的传播方向发生改变的现象;
凸透镜有会聚光线的作用、凹透镜有发散光线的作用,都属于光的折射.A、光照在平面镜上能发生反射,平面镜不能使光发生折射,平面镜对光没有会聚或发散作用;
B、老花镜实际上是凸透镜,光透过平面镜时会发生折射,凸透镜对光线有会聚作用;
C、汽车的观后镜是凸面镜,光照在上面能发生反射,对光具有发散作用,它不能使光发生折射;
D、近视镜是凹透镜,能使光发生折射,对光线有发散作用;
由以上分析可知,能发生光的折射的是B老花镜,D近视镜;能发散光的是C、观后镜,D、近视镜;
能会聚光的是B老花镜;
故答案为:B、D;C、D;B.点评:
本题考点: 光的折射现象及其应用;凸面镜和凹面镜;凸透镜的会聚作用;凹透镜的发散作用.
考点点评: 此题通过几个光学元件考查了学生对光的反射、光的折射的理解.在平时的学习中要善于总结规律,分析各光学元件的制作原理.1年前查看全部
- (2006•斗门区二模)经常对所学知识进行总结和归纳,是学习的一种重要手段.请你根据下列知识的总结和归纳,按要求填空或举
(2006•斗门区二模)经常对所学知识进行总结和归纳,是学习的一种重要手段.请你根据下列知识的总结和归纳,按要求填空或举例:
(1)下列各组物质间均有一定的规律:氧气(O2)和臭氧(O3);红磷和白磷;氧化亚铁(FeO)四氧化三铁(Fe3O4);二氧化硫(SO2)和三氧化硫SO3).
请按此规律再举一例(写化学式):______.
(2)初中化学中有许多有趣的“化学之最”.如:空气中含量最多的气体是氮气;地壳中含量最多的元素是氧元素;相同条件下,密度最小的气体是氢气.请再举一例
______.
(3)化学知识中有很多的“相等”.如化合物中元素化合价的正价总数等于负价总数.请再举一例______. 门下1年前1
门下1年前1 -
 zczxscz 共回答了17个问题
zczxscz 共回答了17个问题 |采纳率94.1%解题思路:(1)组成元素相同,化学式的书写相似的;
(2)“化学之最”:如熔点最高的金属,硬度最大的物质,地壳中含量最多的金属元素等;
(3)化学知识中有很多的“相等”.如元素化合价与该种元素的离子的电荷数绝对值相等;原子中质子数等于核个电子数.(1)组成元素相同,如水与双氧水;一氧化碳与二氧化碳,水(H2O)和双氧水(H2O2);
(2)“化学之最”:如熔点最高的金属为钨,硬度最大的物质为金刚石,地壳中含量最多的金属元素为铝,人体中含量最多的元素是氧元素等;
(3)化学知识中有很多的“相等”.如元素化合价与该种元素的离子的电荷数绝对值相等;原子中质子数等于核外电子数.
故答为:(1)水(H2O)和双氧水(H2O2);
(2)人体中含量最多的元素是氧元素;
(3)原子中质子数等于核外电子数.点评:
本题考点: 物质的元素组成;有关化学之最;原子的定义与构成.
考点点评: 学会对所学知识进行总结和归纳;掌握物质的元素组成;了解有关化学之最;了解原子的定义与构成.1年前查看全部
- (2006•斗门区二模)如图是几种常见的实验装置:
(2006•斗门区二模)如图是几种常见的实验装置:
(1)指出仪器名称:甲______乙______.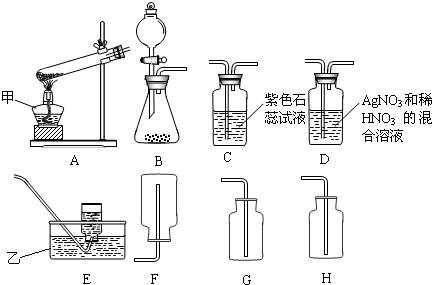
(2)如果用A装置加热固体制取氧气,请指出其中的错误:①______②______
(3)如果要收集干燥的氧气,通常可选用上述装置中的______(填写序号)
(4)实验室制取CO2应选择的发生装置是(填装置编号)______将药品装入试管之前必须要进行的实验操作是______如果小李准备收集一瓶CO2气体,所选用的收集装置是______(填编号)
(5)小李同学将制得的CO2通入澄清石灰水中,未见浑浊.
提出假设1:石灰水可能已变质.
措施:重新配制澄清的石灰水.取5g新买的氢氧化钙粉末放入干净的250mL烧杯中倒入约100mL蒸馏水,搅拌,静置,得到浑浊液.采用过滤的方法除去未溶解的氢氧化钙,除了滤纸,小李还需要哪些仪器?______
过滤后,如果所得液体仍然浑浊,小李应该怎样操作?______最后所得的澄清的液体是氢氧化钙的______(填饱和或不饱和)溶液.
(6)实验与问题:小李同学将制得的CO2通入新制的澄清石灰水中,仍然未见浑浊.
提出假设2:可能错用了较浓的盐酸,使制得的CO2中混入氯化氢气体.
(查资料知道:AgCl是一种白色的固体,它既不溶于水也不溶于稀硝酸)
设计实验方案:甲、乙两组同学选择图中的C或D装置与发生装置连接进行实验.
讨论与交流:
①甲组同学选择C装置,他们______(填“能”或“不能”)证实假设2,理由是______
②乙组同学选择D装置,他们______(填“能”或“不能”)证实假设2,理由是______. 763923821年前1
763923821年前1 -
 zyhf88 共回答了17个问题
zyhf88 共回答了17个问题 |采纳率100%解题思路:(1)熟悉常见仪器,了解名称;
(2)观察图形可知,试管口没向下倾斜,也没放棉花团;
(3)用排空气法可收集到干燥的氧气,再根据氧气的密度大约空气的密度选择即可;
(4)根据制取二氧化碳不需加热选择发生装置;根据二氧化碳密度和溶水性选择收集装置;
(5)过滤实验要用的仪器有:烧杯、漏斗、玻璃棒、铁架台;过滤后,如果所得液体仍然浑浊,要看是否“一贴二底三靠”;根据有未溶解的氢氧化钙判断是哪种溶液;
(6)根据二氧化碳气体和氯化氢气体的性质判断能否证实假设2.(1)图中甲是酒精灯,乙是水槽,故答案为:酒精灯、水槽;
(2)为防止加热时固体中的水蒸气倒流入试管,引起试管的炸裂,试管口要向下倾斜;为防止试管中的固体药品进入导管,要在试管口放一团棉花.故答案为:试管口没向下倾斜、试管口少棉花团;
(3)用排空气法可收集到干燥的氧气,再根据氧气的密度大约空气的密度,我们可知要用向上排空气法收集.故答案为:G或H;
(4)制取二氧化碳不需加热,所以可选用B作为发生装置;二氧化碳密度大于空气的密度,易溶于水,所以我们可以向上排空气法收集二氧化碳;为能保证实验的顺利进行,在放入药品之前一定要检验装置的气密性.故答案为:B、检验装置的气密性、G或H;
(5)过滤实验要用的仪器有:烧杯、漏斗、玻璃棒、铁架台;过滤后,如果所得液体仍然浑浊,要看是否符合“一贴二底三靠”,检查无误后再重新过滤;因为有未溶解的氢氧化钙,所以最后所得的澄清的液体是氢氧化钙的饱和溶液.
故答案为:烧杯,漏斗,玻璃棒,铁架台、检查实验装置是否严密,改进后再过滤、饱和;
(6)①甲组同学选择C装置,他们不能.理由是:二氧化碳的水溶液也能使石蕊溶液变红.故答案为:不能、二氧化碳的水溶液也能使石蕊溶液变红;
②乙组同学选择D装置,他们能.理由是:氯化氢的水溶液通入酸化的硝酸银溶液中能产生白色沉淀,二氧化碳的水溶液通入酸化的硝酸银溶液中不能产生白色沉淀.点评:
本题考点: 气体制取装置的探究;药品是否变质的探究;氧气的制取装置;二氧化碳的实验室制法;二氧化碳的检验和验满.
考点点评: 解答本题的关键是要充分了解制取二氧化碳的方法及其装置,理解二氧化碳和氯化氢的性质,只有这样才能对问题做出正确的判断.1年前查看全部
- (2013•斗门区一模)A、C均由一种或多种金属组成.为确定A的组成,进行下图所示实验(部分产物略去).已知B、E均为只
(2013•斗门区一模)A、C均由一种或多种金属组成.为确定A的组成,进行下图所示实验(部分产物略去).已知B、E均为只含有一种溶质的溶液,B为浅绿色,E为蓝色.
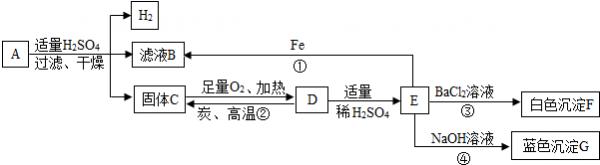
(1)G是______(写物质名称或化学式)
(2)为了分离溶液和不溶固体,在①处应进行的操作是______.
(3)反应①③的化学方程式为:①______. ③______.
(4)比较反应③④,它们的共同点是(写2条):______;______.
(5)根据以上信息,对A的组成可作出的判断是______(填序号).
a.A中只含有Fe b.A中含有Fe和Cu c.A可能是铜锌合金 d.A中一定含有Au. 笑典典1年前1
笑典典1年前1 -
 到达明天075 共回答了20个问题
到达明天075 共回答了20个问题 |采纳率85%解题思路:根据D和硫酸反应会生成E,E只含有一种溶质的溶液,E为蓝色,所以E是硫酸铜,硫酸铜和氢氧化钠反应生成氢氧化铜沉淀和硫酸钠,所以G是氢氧化铜,F就是硫酸钡.硫酸铜和铁反应会生成B,B只含有一种溶质的溶液,B为浅绿色,所以B就是硫酸亚铁.C和D在不同的条件下可以相互转化,D和硫酸反应会生成硫酸铜,所以C就是铜,D就是氧化铜,所以A中含有铁和铜.
(1)根据推导确定G的化学式;
(2)根据过滤操作分离的对象进行分析;
(3)根据推导出的反应物、生成物书写方程式;
(4)根据③④反应的原理进行分析;
(5)根据推导的结果确定A的组成.D和硫酸反应会生成E,E只含有一种溶质的溶液,E为蓝色,所以E是硫酸铜,硫酸铜和氢氧化钠反应生成氢氧化铜沉淀和硫酸钠,所以G是氢氧化铜,F就是硫酸钡,硫酸铜和铁反应会生成B,B只含有一种溶质的溶液,B为浅绿色,所以B就是硫酸亚铁,C和D在不同的条件下可以相互转化,D和硫酸反应会生成硫酸铜,所以C就是铜,D就是氧化铜,所以A中含有铁和铜,
(1)D和硫酸反应会生成E,E只含有一种溶质的溶液,E为蓝色,所以E是硫酸铜,所以G是氢氧化铜,故答案为:Cu(OH)2(或氢氧化铜);
(2)过滤可以将不溶性的物质从液体中进行分离,该题正是为了分离溶液和不溶固体,故答案为:过滤;
(3)①铁和硫酸铜反应生成硫酸亚铁和铜,故答案为:CuSO4+Fe═FeSO4+Cu;
③硫酸铜和氯化钡反应生成氯化铜和硫酸钡沉淀,故答案为:CuSO4+BaCl2═CuCl2+BaSO4↓
(4)③硫酸铜和氯化钡反应生成氯化铜和硫酸钡沉淀,④氢氧化钠和硫酸铜反应上海菜氢氧化铜沉淀和硫酸钠,故答案为:属于复分解反应;有沉淀生成;
(5)从推导可知A是铁和铜组成的,故答案为:b.点评:
本题考点: 物质的鉴别、推断;金属活动性顺序及其应用;盐的化学性质;化学式的书写及意义;书写化学方程式、文字表达式、电离方程式.
考点点评: 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质题中的转换关系推导剩余的物质,最后进行验证即可.1年前查看全部
- (2012•斗门区一模)石墨烯又称单层墨,它仅由一层碳原子组成,具有许多奇特的属性,包括极强的拉力,优 良的导
(2012•斗门区一模)石墨烯又称单层墨,它仅由一层碳原子组成,具有许多奇特的属性,包括极强的拉力,优 良的导电性和导热性,硬度很大,熔点超过 3000℃等,这种高新材料有可能代替硅成为新的半导体材料.根据石墨烯的特性,你认为石墨烯不能用来制成( )
A.高压输电线
B.保温隔热材料
C.发光二极管
D.坚韧的防弹衣 wangbigwei1年前1
wangbigwei1年前1 -
 leeee 共回答了14个问题
leeee 共回答了14个问题 |采纳率100%解题思路:本题的石墨烯是一种新发现的材料,它的物理性质是拉力好、导电性和导热性好、硬度大、熔点高等,根据它的这些特性我们就能知道它的用途.A、高压输电线,利用了它的导电性好的特点,故A正确;但不符合题意;
B、保温隔热材料,要求导热性能差,而石墨烯具有优良的导电性和导热性,故不适合做保温隔热材料,符合题意;
C、发光二极管,利用了它的半导体特性,故C正确;但不符合题意;
D、坚韧的防弹衣,利用了它的拉力好的特点,故D确;但不符合题意;
故选B.点评:
本题考点: 物质的基本属性.
考点点评: 这是一道关心科技发展的一道较简单的基础题.解题时一定要从题目中给出的材料的特性入手.1年前查看全部
- (2012•斗门区一模)(1)实验室中常用氯酸钾和二氧化锰加热制氧气、锌粒与稀硫酸反应制氢气、石灰石与稀盐酸制二氧化碳气
(2012•斗门区一模)(1)实验室中常用氯酸钾和二氧化锰加热制氧气、锌粒与稀硫酸反应制氢气、石灰石与稀盐酸制二氧化碳气体.
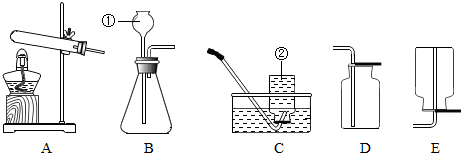
写出标号仪器的名称①______②______
请结合所给药品选择适当的气体发生和收集装置填入下表:(填字母)
(2)由于大量使用一次性塑料方便袋造成的“白色污染”,已成为一个严重的社会问题.某化学研究小组的同学欲对某种塑料袋的组成进行分析探究(资料显示该塑料只含C、H两种元素),他们设计了如图所示的实验装置,使该塑料试样在纯氧中燃烧,观察实验现象,分析有关数据,推算元素含量.气体 发生装置 收集装置 O2 ______ ______ H2 ______ ______ CO2 ______ ______ 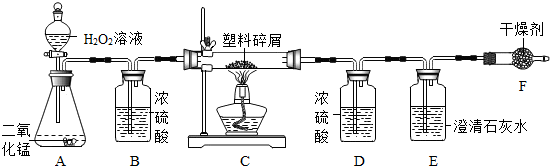
①仪器B的作用是______.
②仪器E中的现象是______.
③若仪器C的玻璃管中放入的塑料试样质量为Wg,塑料试样充分燃烧后,若仪器D增重a g,则Wg该塑料试样中含氢元素的质量为[1/9]a[1/9]ag(计算结果可为分数形式)
④若装置中没有连接仪器B,将使该塑料试样中氢元素的质量测算结果______(填“偏小”、“偏大”、“无影响”中之一). rusiwei1年前1
rusiwei1年前1 -
 我也爱弹吉它 共回答了26个问题
我也爱弹吉它 共回答了26个问题 |采纳率84.6%解题思路:(1)根据发生装置和收集装置的选择依据进行分析解答.
(2)对某种塑料袋的组成元素进行分析探究,用好题中信息,结合课本知识含氢元素的物质燃烧产生水,含碳元素的物质燃烧生成二氧化碳;以上知识再结合题中实验解答该题.另外还用到根据质量守恒定律和化学式计算某元素的质量分数.(1)①长颈漏斗;②集气瓶
(2)装置B中装的是浓硫酸,浓硫酸用于除水蒸气;
(3)装置E中装的是澄清的石灰水,是用来检验二氧化碳的,二氧化碳能使澄清的石灰水变浑浊;
(4)塑料试样充分燃烧后,浓硫酸具有吸水性,故D增重的质量就是W g该塑料试样燃烧生成的水的质量,装置D增重a g,据质量守恒定律,水中氢元素即塑料样品中的氢元素,所以W g该塑料试样中含氢元素的质量为 [1/9]ag;
(5)若整套装置中没有连接仪器B,会使氧气中的水蒸会进入装置D,从而使实验测得的水的质量大于塑料样品燃烧生成的水,故将使该塑料试样中氢元素的质量测算结果偏大.
故答案为:
(1)①长颈漏斗;②集气瓶
气体 发生装置 收集装置
O2 A C或D
H2 B C或E
CO2 B D(2)①除去气体中的水蒸气;②澄清石灰水变浑浊;③[1/9]a;④偏大点评:
本题考点: 常用气体的发生装置和收集装置与选取方法;化学实验方案设计与评价;常见气体的检验与除杂方法;白色污染与防治.
考点点评: 本题是实验探究题,考查了装置的选择依据及化合物中碳元素和氢元素的验证过程和根据化学式的计算,综合性极强,只要看清反应的实质较易解答该题.1年前查看全部
- (2012•斗门区一模)如图,在边长为1个单位长度的小正方形组成的网格中,△ABC与△DFE关于直线MN对称,△ABC与
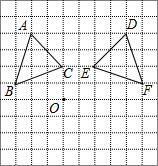 (2012•斗门区一模)如图,在边长为1个单位长度的小正方形组成的网格中,△ABC与△DFE关于直线MN对称,△ABC与△DFE的顶点均在格点上,请按要求完成下列各题.
(2012•斗门区一模)如图,在边长为1个单位长度的小正方形组成的网格中,△ABC与△DFE关于直线MN对称,△ABC与△DFE的顶点均在格点上,请按要求完成下列各题.
(1)在图中画出直线MN;
(2)画出△ABC关于点O中心对称的图形△A1B1C1;
(3)求△A1B1C1的面积. 和我一起漂泊1年前0
和我一起漂泊1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2006•斗门区二模)如图是A和B物质的溶解度曲线,回答下列问题:
 (2006•斗门区二模)如图是A和B物质的溶解度曲线,回答下列问题:
(2006•斗门区二模)如图是A和B物质的溶解度曲线,回答下列问题:
(1)降低温度时,A溶液中析出的晶体比B析出的晶体______(填多、少或无法比较).
(2)20℃时,A物质的饱和溶液中,溶质的质量分数等于[100a/100+a]%[100a/100+a]%.
(3)若要从B的饱和溶液中得到B物质的晶体,通常采用______的方法. 月a_11年前1
月a_11年前1 -
 yflfrank 共回答了12个问题
yflfrank 共回答了12个问题 |采纳率100%解题思路:根据固体物质的溶解度曲线可以:可以查出某物质在一定温度时的溶解度,根据溶解度进行有关的分析与计算;可以查出物质的溶解度随温度变化的变化情况,从而可以确定在降低温度时析出晶体的多少,确定从饱和溶液中析出晶体的方法等.(1)由于A、B溶液的状态、溶液的质量等不确定,无法比较降低温度时析出的晶体的多少;
(2)由A物质的溶解度曲线可知,在20℃时,A物质的溶解度是ag,则溶质的质量分数等于[ag/100g+ag]×100%=[100a/100+a]%;
(3)由B物质的溶解度曲线可知,由于B物质的溶解度受温度的影响不大,所以,若要从B的饱和溶液中得到B物质的晶体,通常采用蒸发溶剂的方法.
故答为:(1)无法比较;(2)[100a/100+a]%;(3)蒸发溶剂.点评:
本题考点: 固体溶解度曲线及其作用;结晶的原理、方法及其应用;溶质的质量分数、溶解性和溶解度的关系.
考点点评: 本题难度不大,主要考查了固体溶解度曲线所表示的意义,通过本题可以加强学生对固体溶解度的理解.1年前查看全部
大家在问
- 1现在是师范生就读,暑假作业要求写一篇教案.请问应该怎么写/有什么注意事项?
- 2下列物质中,其实验式与另外三种不同的是( )
- 3拜财神时点了3只香有两根然到一半灭了什么意思
- 4将纯锌片和纯铜片按图示方式插入同浓度同体积的稀硫酸中一段时间,以下叙述正确的是( ) A.两烧杯中铜片表面均无气泡产生
- 5(1997•苏州)改变物体内能的方法有两种,______和______.
- 6secondary battery是什么意思
- 7写一个表现母爱的句子,用上“凝望”一词。
- 8把一列数1/2,-1/4,1/6,-1/8,…按以下规律排成一个数表如下:
- 9明天我得去理发了用英语怎么说
- 10一桶油重58千克,三天用完.第一天用去三分之一,第二天用去余下的三分之二,第三天用去比前二天用去的总和的七分之三少6千克
- 11以“我的篮球梦” 写一篇不少于600字的作文
- 12to make adjustment along the way ,along the way 做什么成分啊,
- 134)How much is produced________________how hard we work.用depe
- 14某班一次集合,请假人数是出席的人数的 1 9 ,中途又有一人请假离开,这样一来请假人数是出席人数的 3 22 ,那么这个
- 15实验小学上学期评出三好学生180人,恰好占全校学生人数的20分之3,全校有学生多少人
