(2006•都匀市)都匀市区有部分餐馆燃烧含有硫单质的蜂窝煤,产生了大量污染环境的气体.该气体是( )
 水中星cissy2022-10-04 11:39:541条回答
水中星cissy2022-10-04 11:39:541条回答A.H20
B.N2
C.SO2
D.CO2

已提交,审核后显示!提交回复
共1条回复
 雾中飞 共回答了11个问题
雾中飞 共回答了11个问题 |采纳率100%- 解题思路:空气污染的途径主要有两个:有害气体和粉尘.有害气体主要有一氧化碳、二氧化硫、二氧化氮等气体;粉尘主要指一些固体小颗粒.二氧化硫主要来源于煤、石油等燃料的燃烧,工厂排放的废气等.含有硫单质的蜂窝煤燃烧,会生成二氧化硫,污染空气.
A、水不是空气污染物,故选项错误;
B、氮气是空气的主要成分,无污染,故选项错误;
C、含有硫单质的蜂窝煤燃烧,会生成二氧化硫,污染空气.故选项正确;
D、二氧化碳是空气的成分,无污染,故选项错误;
故选C.点评:
本题考点: 空气的污染及其危害;质量守恒定律及其应用.
考点点评: 本题主要是空气的污染及其危害,环保问题已经引起了全球的重视,关于“三废”的处理问题,是中考的热点问题,化学上提倡绿色化学工艺,要从源头上杜绝污染. - 1年前
相关推荐
- (2022•黔南州)都匀市某新修“商业大厦”的一处自动扶梯如图,已知扶梯的长人为20米,该自动扶梯到达的高度h为6米,自
 (2022•黔南州)都匀市某新修“商业大厦”的一处自动扶梯如图,已知扶梯的长人为20米,该自动扶梯到达的高度h为6米,自动扶梯与地面所成的角为θ,则右如nθ的值等于[r/4][r/4].
(2022•黔南州)都匀市某新修“商业大厦”的一处自动扶梯如图,已知扶梯的长人为20米,该自动扶梯到达的高度h为6米,自动扶梯与地面所成的角为θ,则右如nθ的值等于[r/4][r/4]. 向着阳光冲1年前0
向着阳光冲1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2006•都匀市)在太空舱里,为了保持舱内O2和CO2气体含量的相对稳定,常用NiFe2O4作催化剂将宇航员呼出的CO
(2006•都匀市)在太空舱里,为了保持舱内O2和CO2气体含量的相对稳定,常用NiFe2O4作催化剂将宇航员呼出的CO2转化为O2.NiFe2O4中铁为+3价,则Ni的化合价为( )
A.+1
B.+2
C.+3
D.+4 smucel7903231年前1
smucel7903231年前1 -
 TTSOBAG 共回答了17个问题
TTSOBAG 共回答了17个问题 |采纳率94.1%根据在化合物中正负化合价代数和为零,可得NiFe2O4中Ni的化合价为:x+(+3)×2+(-2)×4=0,则x=+2;
故选:B.1年前查看全部
- 在全国初中数学竞赛中,都匀市有40名同学进入复赛,把他们的成绩分为六组,第一组一第四组的人数分别为10,5,7,6,第五
在全国初中数学竞赛中,都匀市有40名同学进入复赛,把他们的成绩分为六组,第一组一第四组的人数分别为10,5,7,6,第五组的频率是0.2,则第六组的频率是______.
 zelda7231年前1
zelda7231年前1 -
 酒吧烂钟 共回答了23个问题
酒吧烂钟 共回答了23个问题 |采纳率87%解题思路:先用数据总数乘第五组的频率得出第五组的频数,再求出第六组的频数,然后根据频率=频数÷数据总数即可求解.∵都匀市有40名同学进入复赛,把他们的成绩分为六组,第一组一第四组的人数分别为10,5,7,6,第五组的频率是0.2,
∴第五组的频数为40×0.2=8,第六组的频数为40-(10+5+7+6+8)=4,
∴第六组的频率是4÷40=0.1.
故答案为:0.1.点评:
本题考点: 频数与频率.
考点点评: 本题考查了频数与频率,用到的知识点:频数=数据总数×频率,频率=频数÷数据总数,各组频数之和等于数据总数.1年前查看全部
- (2006•都匀市)下列实验操作正确的是( )
(2006•都匀市)下列实验操作正确的是( )
A.
制取二氧化碳
B.
称量白磷燃烧前后质量
C.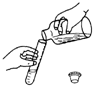
倾倒液体
D.
过滤 FISHFLASH1年前1
FISHFLASH1年前1 -
 轻雨微寒 共回答了24个问题
轻雨微寒 共回答了24个问题 |采纳率87.5%解题思路:制取二氧化碳时,要形成液封,防止漏气;用托盘天平称量时,要注意左物右码;从细口瓶取液体药品,注意事项一般有以下几点:①瓶塞应该倒放②标签要对着手心③试剂瓶口要紧挨中试管口④试管要倾斜⑤试管中的药品一般不超过试管容积的三分之一.过滤中要注意:一贴、二低、三靠.A、制取二氧化碳时,要形成液封,防止漏气,故选项错误;
B、用托盘天平称量时,要注意左物右码,故选项错误;
C、倾倒液体时瓶塞应该倒放,故选项错误;
D、过滤中要注意:一贴、二低、三靠,故选项正确;
故选D.点评:
本题考点: 二氧化碳的实验室制法;液体药品的取用;过滤的原理、方法及其应用;质量守恒定律及其应用.
考点点评: 本考点考查了二氧化碳的制法、物质的称量、液体的取用方法和过滤,考查的知识点比较多,要加强记忆有关的注意事项,并理解应用,本考点主要出现在选择题和填空题中.1年前查看全部
- 英语翻译:贵州省都匀市时代广场1栋14层C户
 benyuwang821年前2
benyuwang821年前2 -
 ldqan 共回答了14个问题
ldqan 共回答了14个问题 |采纳率100%Room C,Floor 14,Building 1,Times Square,Duyun,Guizhou Province,China1年前查看全部
- (2006•都匀市)有一块含杂质(杂质不与盐酸反应、也不溶解于任何溶剂)的锌块与200mL稀盐酸(密度为1.09g/mL
(2006•都匀市)有一块含杂质(杂质不与盐酸反应、也不溶解于任何溶剂)的锌块与200mL稀盐酸(密度为1.09g/mL)完全反应,产生1克氢气,把反应后的液体过滤.求:
(1)稀盐酸中HCl的质量分数;
(2)滤液中溶质的质量分数. fanlir1年前1
fanlir1年前1 -
 下雨了大家收衣服 共回答了19个问题
下雨了大家收衣服 共回答了19个问题 |采纳率94.7%解题思路:根据生成氢气的质量结合锌与盐酸反应的方程式求出稀盐酸中溶质的质量,氯化锌的质量、锌的质量,再根据溶质的质量分数=[溶质的质量/溶液的质量]×100%求稀盐酸中HCl的质量分数和滤液中溶质的质量分数.稀盐酸的质量为:200 X 1.09g/mL=218(g)
(1)设参加反应的HCl质量为x,锌的质量为y,则
Zn+2HCl═ZnCl2+H2↑
65 73 2
y x 1g
[65/y]=[2/1g] [73/x]=[2/1g]
y=32.5g x=36.5g
则稀盐酸中Hcl的质量分数为:[36.5g/218g]×100%=16.7%
(2)过滤后的滤液是氯化锌溶液.
根据质量守恒定律,生成氯化锌的质量是:32.5g+36.5g-1g=68g
滤液的质量为32.5g+218g-1g=249.5g
则氯化锌溶液溶质的质量分数是:[68g/24 9.5g]100%=27.3%
答:稀盐酸中HCl的质量分数是16.7%,滤液中溶质的质量分数是27.3%.点评:
本题考点: 根据化学反应方程式的计算;有关溶质质量分数的简单计算.
考点点评: 本题考查了学生依据化学方程式进行解题的能力,书写正确的方程式、明确溶液的质量=溶液的体积×密度、溶质的质量分数=[溶质的质量/溶液的质量]×100%是解题的关键.1年前查看全部
- (2007•黔南州)在都匀市第二届房车交易会上,主席台上整齐摆放着10台小汽车,其中2台黄色QQ车,3台黑色桑塔纳,5台
(2007•黔南州)在都匀市第二届房车交易会上,主席台上整齐摆放着10台小汽车,其中2台黄色QQ车,3台黑色桑塔纳,5台白色别克,则坐在主席台前方的一名观众抬头第一眼看见是黑色桑塔纳轿车的概率是[3/10][3/10].
 tracylynn1年前0
tracylynn1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2006•都匀市)都匀毛尖茶中含有的单宁酸具有抑制血压上升、清热解毒、抗癌等功效,其化学式为C76H52O46,请根据
(2006•都匀市)都匀毛尖茶中含有的单宁酸具有抑制血压上升、清热解毒、抗癌等功效,其化学式为C76H52O46,请根据单宁酸分子的化学式填空:
(1)单宁酸的一个分子中含有______个原子;
(2)单宁酸的相对分子质量为______;
(3)单宁酸中碳元素的质量分数为______. heiyewu7281年前1
heiyewu7281年前1 -
 沙喇 共回答了15个问题
沙喇 共回答了15个问题 |采纳率80%解题思路:(1)根据标在元素符号右下角的数字表示一个分子中所含原子的个数;进行解答;(2)根据相对分子的质量为组成分子的各原子的相对原子质量之和,进行解答;
(3)根据物质中某元素的质量分数=[该元素相对原子质量×原子个数/物质的相对分子质量]×100%,进行解答.(1)根据标在元素符号右下角的数字表示一个分子中所含原子的个数;可得单宁酸的一个分子中含有:
76+52+46=174;(2)根据相对分子的质量为组成分子的各原子的相对原子质量之和,可得单宁酸的相对分子质量为:12×76+1×52+16×46=1700;
(3)根据物质中某元素的质量分数=[该元素相对原子质量×原子个数/物质的相对分子质量]×100%,可得单宁酸中碳元素的质量分数为:[12×76/1700]×100%=53.65%;
故答案为:(1)174; (2)1700;(3)53.65%.点评:
本题考点: 有关化学式的计算和推断;相对分子质量的概念及其计算;元素的质量分数计算.
考点点评: 本题考查学生对化学式的含义的理解,并能根据化学式进行相应的计算的能力.1年前查看全部
- (2006•都匀市)把A、B、C、D四种物质放在密闭容器中,在一定条件下充分反应,并测得反应物和产物在反应前后各物质的质
(2006•都匀市)把A、B、C、D四种物质放在密闭容器中,在一定条件下充分反应,并测得反应物和产物在反应前后各物质的质量如下表所示:
下列说法错误的是( )物质 A B C D 反应前质量/g 19.7 8.7 21.6 O.4 反应后质量/g 待测 17.4 O 3.6
A.该反应是分解反应
B.反应后密闭容器中A的质量为29.4g
C.该反应是化合反应
D.反应过程中,物质B和物质D质量增加的比为87:32 远航木1年前1
远航木1年前1 -
 cadenza8 共回答了20个问题
cadenza8 共回答了20个问题 |采纳率85%解题思路:根据质量守恒定律,可分析先B、C、D三种物质反应前后的质量变化情况,确定是反应物还是生成物;然后根据质量守恒定律确定A是反应物还是生成物,进而可以确定反应类型.由表中数据分析可知,反应前后,B的质量增加了8.7g,故B是生成物,参加反应的B的质量为8.7g;同理可以确定C是反应物,参加反应的C的质量为21.6g;D的质量增加了3.2g,故D是生成物,参加反应的D的质量为3.2g;由质量守恒定律,A应是反应物,且生成的A的质量为21.6g-8.7g-3.2g=9.7g.
A、该反应的反应物为C,生成物是A、B、D,符合“一变多”的特征,属于分解反应;故选项说法正确.
B、生成的A的质量为9.7g,则待测的值为9.7g+19.7g=29.4g;故选项说法正确.
C、该反应的反应物为C,生成物是A、B、D,符合“一变多”的特征,属于分解反应;故选项说法错误.
D、由质量守恒定律,物质B和物质D质量增加的比为8.7g:3.2g=87:32;故选项说法正确.
故选C.点评:
本题考点: 质量守恒定律及其应用;反应类型的判定.
考点点评: 本题难度不大,考查的是质量守恒定律的应用,解题的关键是分析表中数据、灵活运用质量守恒定律.1年前查看全部
大家在问
- 1下列大写字母按其在字母表中顺序排列错误的是________ A.EMS B.ABC C.RMB D.MTV
- 2我是老外,帮我修改病句.但是大宏觉得在家里养大狗会保护小云,特别是她一个人在家的时候.
- 3已知扇形OAB的圆心角为4/3π弧度,其面积为2/3π平方米,求扇形的周长和弦长
- 4试证当n为正整数时,f(n)=32n+2-8n-9能被64整除.
- 51mg/m³等于多少ppm?空气
- 6一次会议上,每两个参加会议的人都互相握手一次,有人统计一共是握了66次手,则这次会议到会人数是______人.
- 7a>0比较下列算式水的结果最大A a/0.6 B 0.6/a C a+0.6 D 无法确定
- 8一个这样的老师 作文
- 9英语翻译functional words do far more work of expression than con
- 10如果跟一个一年级的小朋友补习数学.一对一的.
- 11化学与生活、社会密切相关,下列说法正确的是( )
- 12x=-8是方程3x+8=四分之x-a的解,求a平方-4a的值
- 13求周长和面积(带图)
- 14有一xOy平面,在x<0的空间内,存在场强为E、与 y轴成θ角的匀强电场,如图所示.在第Ⅲ象限某处有质子源s,
- 15在观察DNA和RNA在细胞中的分布实验中,为什么用百分之8的盐酸?
