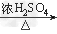铁的导电能力比铜强,
 langly_chang2022-10-04 11:39:543条回答
langly_chang2022-10-04 11:39:543条回答
已提交,审核后显示!提交回复
共3条回复
 天_涯浪_子 共回答了14个问题
天_涯浪_子 共回答了14个问题 |采纳率100%- 不对 铜的电阻比铁小 导线性比铁强
所以我们用的导线都是铜的 - 1年前
 绿水轻飘 共回答了2个问题
绿水轻飘 共回答了2个问题 |采纳率- 铜的比铁强。
- 1年前
 457891 共回答了14个问题
457891 共回答了14个问题 |采纳率- 错
- 1年前
相关推荐
- 在熔融状态下才能导电的电解质有哪些?
在熔融状态下才能导电的电解质有哪些?
我的意思是在水溶液中不能导电的电解质 天笑风1年前5
天笑风1年前5 -
 跑进狼群的小羊 共回答了21个问题
跑进狼群的小羊 共回答了21个问题 |采纳率85.7%强酸(硫酸、盐酸、硝酸等)、强碱(氢氧化钠、氢氧化钾等)、大部分正盐(氯化钠、硝酸银、碳酸钾等)等强电解质.1年前查看全部
- (2010•莆田)2010年4月26日,福厦高铁客运正式开通.动车组与架空电线的接触材料应具有耐高温、不易氧化、能导电的
(2010•莆田)2010年4月26日,福厦高铁客运正式开通.动车组与架空电线的接触材料应具有耐高温、不易氧化、能导电的性质.你认为该材料可选用( )
A.铁
B.石墨
C.金刚石
D.铜 mmmaaaxxx1年前1
mmmaaaxxx1年前1 -
 nolovenopain 共回答了17个问题
nolovenopain 共回答了17个问题 |采纳率82.4%解题思路:物质的结构决定物质的性质,物质的性质决定物质的用途.A、铁在空气中易被氧化,不能用作接触点上的材料,故A错误;
B、石墨具有耐高温,不易氧化,能导电的性质,可以用作接触点上的材料,故B正确;
C、金刚石不导电,不能用作接触点上的材料,故C错误;
D、铜在受热时容易被空气中的氧气氧化,不能用作接触点上的材料,故D错误;
故选B.点评:
本题考点: 碳单质的物理性质及用途.
考点点评: 本题主要考查物质的性质和用途,物质具有多种性质,解答时应该理解物质的用途是由物质的哪种性质决定的.1年前查看全部
- 什么金属长期在水中不会生锈,导电性能又好?
什么金属长期在水中不会生锈,导电性能又好?
我用的是自动抽水装置,水箱里有高,中,低3根导电金属,泡在水中.半年后由于金属生锈,导电性能变差,结果常常把水大的满出去了,不会自动关水了.所以我想找个长期在水中不会生锈,导电性能又好的金属这样就好了.
铝带电放在水里会不会生锈的啊? 股人曰1年前1
股人曰1年前1 -
 yyg120 共回答了16个问题
yyg120 共回答了16个问题 |采纳率100%不要用铝 铝在通电时会发生电化学腐蚀 铜也是 金属许多会生锈 不生锈的又贵 但不锈钢还可以 不过建议你用石墨 锌锰干电池中的那根芯就是 那是碳 导电极好 又不生锈1年前查看全部
- 纯净水为什么不能导电电解质是溶于水溶液中或在熔融状态下就能够导电(电解离成阳离子与阴离子)并产生化学变化的化合物.水是电
纯净水为什么不能导电
电解质是溶于水溶液中或在熔融状态下就能够导电(电解离成阳离子与阴离子)并产生化学变化的化合物.水是电解质为什么不能导电 离离原上火1年前1
离离原上火1年前1 -
 大床头柜 共回答了18个问题
大床头柜 共回答了18个问题 |采纳率88.9%水是弱电解质,只能电离出极少的氢离子和氢氧根离子,所以导电性很弱,但它是可以导电的,只不过用我们实验的导电装置测不到(灯泡不亮),用灵敏电流计可以测到电流.1年前查看全部
- 只要某物质有自由移动的带电粒子,那它就能导电?
 这些图片说明1年前1
这些图片说明1年前1 -
 神仙的腰带 共回答了15个问题
神仙的腰带 共回答了15个问题 |采纳率93.3%不一定 要在水溶液中或者熔融状态下1年前查看全部
- 为了测定不同电解质的水溶液的导电能力是否相同,设计如下图所示的实验,
为了测定不同电解质的水溶液的导电能力是否相同,设计如下图所示的实验,
图为5种溶液连了5个灯泡,灯泡的发光程度不同
请回答下列问题:
(1)本实验取了盐酸、CH3COOH溶液、NaOH溶液、NaCl溶液和氨水五种溶液,若要再增加一种溶液,你认为选取下列哪种溶液最为合适?▲
(A)硫酸钠 (B)氯化钙 (C)氢氧化钡 (D)硝酸钾 忆哥1年前3
忆哥1年前3 -
 67086708 共回答了19个问题
67086708 共回答了19个问题 |采纳率100%D.
个人认为已经有了强酸,弱酸,强碱,弱减,盐,
应该选一个盐,而且离子不重复的.
你有答案吧,希望不会误导你.1年前查看全部
- Ⅰ.对羟基肉桂酸是一种强效的导电材料,在液晶显示器工业中近年来研究广泛。其结构简式如图所示: (
Ⅰ.对羟基肉桂酸是一种强效的导电材料,在液晶显示器工业中近年来研究广泛。其结构简式如图所示: 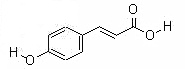
(1)该有机物具有的官能团名称是________________(写出其中的两种)。
(2)该有机物能发生的反应类型是(填写代号)______________。
A.酯化反应 B.消去反应 C.加成反应 D.水解反应
Ⅱ.芳香族化合物C 10 H 10 O 2 有如下的转化关系:
已知E能使Br 2 /CCl 4 溶液褪色。请回答下列问题:
(3)请写出A的结构简式:_______________。
(4)若有机物F与C互为同分异构体,则与有机物B互为同系物的F的同分异构体有______________(用结构简式表示)
(5)请写出B→C反应的化学反应方程式_________________。
(6)请写出D→E反应的化学反应方程式___________________。 玉树随秋风1年前1
玉树随秋风1年前1 -
 大漠沙粒 共回答了12个问题
大漠沙粒 共回答了12个问题 |采纳率100%1年前查看全部
- 液态HCI能不能导电?是不是电解质?
 afhni1年前6
afhni1年前6 -
 zlcjmldbnr 共回答了22个问题
zlcjmldbnr 共回答了22个问题 |采纳率86.4%是的 电解质
熔融状态上不能导电
水溶液能导电
高一化学书上有
总之满足一个就是电解质1年前查看全部
- 什么电解质只有在溶于水时才导电什么电解质只有在熔融状态什么电解质即在融融状态下又在溶于水时导电
 ella22ling1年前2
ella22ling1年前2 -
 不渝至爱 共回答了19个问题
不渝至爱 共回答了19个问题 |采纳率94.7%一些共价化合物电解质只有在溶于水时才导电 如HCl H2SO4等
难溶于水的盐电解质只有在熔融状态时才导电 如BaSO4等
可溶性盐电解质即在融融状态下又在溶于水时导电 如NaCl等1年前查看全部
- 怎样判断一种化合物和其溶液或熔融状态下是否是电解质?能否导电?
怎样判断一种化合物和其溶液或熔融状态下是否是电解质?能否导电?
怎样判断一种 化合物 和 其溶液 或 熔融 状态下 是否是电解质?能否导电呢?
知道者讲解详细点,把通常所用到 看到 的化合物和其溶液或 熔融 状态下 是否是电解质?能否导电的列举出来!
有些化合物在 水溶液中能导电 是电解质 但在 熔融状态下 不是!
有些化合物在 熔融状态下能导电 是电解质但在水溶液中不是!怎样分辨它们呢?知道者能举出通常能用到和能见到的例子! CANRISE1年前5
CANRISE1年前5 -
 触桑三磨堂 共回答了18个问题
触桑三磨堂 共回答了18个问题 |采纳率100%一般来说溶液 或 熔融 状态下能电离(产生)自由移动的离子就是电解质,满足其中的一个条件即可.
就是说这种物质在 熔融或者它的水溶液能导电,那说明这种物质就是电解质.
一般来说共价化合物在水溶液中能导电,熔融时不导电,如HCl,H2SO4等
离子化合物在熔融和水溶液中都能导电,如:NaCl,CaCl2等
有些离子化合物在如果溶解度太小,只有在熔融时导电,如CaCO3等1年前查看全部
- 下列说法中,不正确的是( )A.NH3的水溶液可以导电,说明NH3是电解质B.明矾水解形成Al(OH)3胶体有吸附性,
下列说法中,不正确的是( )
A.NH3的水溶液可以导电,说明NH3是电解质
B.明矾水解形成Al(OH)3胶体有吸附性,可用于水的净化
C.二氧化硅可用于制造光导纤维
D.向淀粉碘化钾溶液中加溴水,溶液变为蓝色,说明Br2的氧化性强于I2 dt9481年前1
dt9481年前1 -
 耗子018382 共回答了18个问题
耗子018382 共回答了18个问题 |采纳率88.9%解题思路:A.电解质指:水溶液中或熔融状态下能够导电的化合物,注意能导电,必须是电解质自身电离出自由移动的离子;在上述两种情况下都不能导电的化合物称为非电解质;
B.明矾中的铝离子水解生成氢氧化铝胶体,具有吸附悬浮杂质的作用;
C.光导纤维的主要成分是二氧化硅;
D.卤素单质的氧化性顺序是:Br2>I2,离子的还原性顺序是:I->Br-,Br2强氧化性比碘强,可与KI发生氧化还原反应生成I2;碘遇淀粉显蓝色;A.氨气是化合物,溶于水,氨气和水反应生成一水和氨,NH3•H2O⇌NH4++OH-导电,但这些离子不是氨气电离,氨气是非电解质,故A错误;
B.明矾中的铝离子水解生成氢氧化铝胶体,具有吸附悬浮杂质的作用;可用于水的净化;故B正确;
C.光导纤维是利用光反射原理制成的,光导纤维的主要成分是二氧化硅,故C正确;
D.碘遇淀粉显蓝色,说明有碘单质生成,这是因为溴强氧化性比碘强,可与KI发生氧化还原反应生成I2,反应的离子方程式为Br2+2I-=2Br-+I2,故D正确;
故选A.点评:
本题考点: 电解质与非电解质;盐类水解的应用;硅和二氧化硅.
考点点评: 本题考查了氨气是非电解质、明矾净水、光导纤维的主要成分、碘遇淀粉显蓝色等知识点,掌握基础知识是解题关键,题目难度不大.1年前查看全部
- 白炽灯的灯丝随温度的升高导电性能变差,则白炽灯不通电时灯丝电阻R 1 与正常发光时电阻R 2 比较应是( ) A.R
白炽灯的灯丝随温度的升高导电性能变差,则白炽灯不通电时灯丝电阻R 1 与正常发光时电阻R 2 比较应是( ) A.R 1 >R 2 B.R 1 <R 2 C.R 1 =R 2 D.无法判断  我是小妖晶1年前1
我是小妖晶1年前1 -
 lacuston 共回答了13个问题
lacuston 共回答了13个问题 |采纳率84.6%白炽灯灯丝由金属钨构成,金属的电阻率随温度的升高而升高,故电阻变大,即白炽灯的灯丝随温度的升高导电性能变差,故通电后温度升高,电阻变大,即R 1 <R 2 .
故选B.1年前查看全部
- 玻璃棒加热后为什么导电?
 mydreamxp1年前1
mydreamxp1年前1 -
 半夜无眠 共回答了15个问题
半夜无眠 共回答了15个问题 |采纳率100%玻璃是石英(二氧化硅)、纯碱(碳酸钠)、长石等的熔融混合物,其没有固定熔点,是因为其中各组分熔点不同.玻璃在加热到600-800度左右开始变软,进一步加热,则发红,普通玻璃在1000度左右完全融化.
之所以红热以后导电,是因为玻璃中部分熔点地的组分已经熔化,熔融状态的化合物阴阳离子发生电离,从而导电.
这个很麻烦~·
玻璃棒中有硅酸盐,加热嘛肯定能电离的.
还有就是原子受热之后最外层电子不稳定,易移动,所以能够导电
这个比较简洁~1年前查看全部
- 下列说法中不正确如是( )A.自由电荷定向移动形成电流B.金属导电的过程中,自由电子移动方向与电流方向相同C.只要是有
下列说法中不正确如是( )
A.自由电荷定向移动形成电流
B.金属导电的过程中,自由电子移动方向与电流方向相同
C.只要是有电源,就一定有电流
D.绝缘体不容易导电的原因是因为绝缘体内缺少自由电子 寒豫1年前1
寒豫1年前1 -
 liboshuism 共回答了18个问题
liboshuism 共回答了18个问题 |采纳率94.4%A、电流是由电荷的定向移动形成的,能够定向移动的电荷一定是自由电荷.故A的说法正确,不合题意.
B、金属导体导电,靠的是自由电子,自由电子带负电,电流的方向是规定正电荷定向移动的方向为电流方向.所以若是负电荷导电,则电流方向与负电荷定向移动的方向相反.故B的说法错误,符合题意.
左、电路中虽然有电源,但 若是断开的电路,电路中仍然没有电流,因为要上到持续电流这两个条件必须同时具备.故左的说法错误,符合题意.
D、绝缘体不导电,是因为绝缘体内缺少自由电荷,有的物体内部虽然没有自由电子,但仍是导体,如酸碱盐的溶液.故D的说法错误,符合题意.
故选B左D.1年前查看全部
- 下列说法中正确的是( )A.导体能导电说明导体内部有多余的电子B.绝缘体不能导电是因为它不能带上电荷C.直接用手拿着金
下列说法中正确的是( )
A.导体能导电说明导体内部有多余的电子
B.绝缘体不能导电是因为它不能带上电荷
C.直接用手拿着金属棒与毛皮摩擦时,金属棒不会带电
D.通常情况下,塑料、玻璃、石蜡、空气都是绝缘体 铷铯钫1年前1
铷铯钫1年前1 -
 www_w2003 共回答了22个问题
www_w2003 共回答了22个问题 |采纳率95.5%解题思路:容易导电的物体是导体,不容易导电的物体是绝缘体,导体导电是因为导体内部有大量的自由电荷,绝缘体不导电是因为绝缘体内部几乎没有自由电荷.常见的导体有金属、石墨、人体、大地、酸碱盐的水溶液.A、导体能导电是因为导体内有能够自由移动的电子,故此选项错误;
B、绝缘体不能导电是因为它内部几乎没有自由电荷,故此选项错误;
C、人体是导体直接用手拿着金属棒与毛皮摩擦时,电荷会从人体导走,金属棒不会带电,故此选项正确;
D、通常情况下,塑料、玻璃、石蜡、空气都是绝缘体,正确.
故选CD点评:
本题考点: 金属导电的实质;绝缘体.
考点点评: 本题考查了导体和绝缘体的概念及导体导电和绝缘体不导电的原因,属于基本内容,比较简单.1年前查看全部
- 问一道竞赛中静电场的题目半径为R2的导电球壳包围着半径为R1的导电金属球,金属球原来是具有电势U,如果让球壳接地,则金属
问一道竞赛中静电场的题目
半径为R2的导电球壳包围着半径为R1的导电金属球,金属球原来是具有电势U,如果让球壳接地,则金属球的电势变为多少? 只好感1年前2
只好感1年前2 -
 guzhuyu 共回答了23个问题
guzhuyu 共回答了23个问题 |采纳率82.6%不接地时,里面的+Q在外面感应出的-Q与外面剩的+Q是在外面均匀分布的,对内电势为零,所以里面的U=kQ/R1,接地后由于球壳电势为零,里面的+Q和球壳上感应出的q在球壳上的总电势为零即
kQ/R2+kq/R2=0,加号前是球在球壳处产生的,加号后是球壳自己在球壳上产生的.
用U表示Q,代入所以q=-UR1/k
所以金属球现在的电势为球自己的U没变,加上球壳在里面的电势,这与球壳的相等因为球壳与其内部为一等势体即kq/R2
U+kq/R2带入上面算出的q得(R2-R1)U/R21年前查看全部
- 有关高一化学电解质的问题课本上关于电解质的概念是“在水溶液中或熔融状态下能导电的化合物”,那么能否改成“在水溶液中或熔融
有关高一化学电解质的问题
课本上关于电解质的概念是“在水溶液中或熔融状态下能导电的化合物”,那么能否改成“在水溶液中或熔融状态下能导电的物质”?为什么?有在水溶液中或熔融状态下能导电的混合物吗?
 vivianlean1年前3
vivianlean1年前3 -
 俗世一尘埃 共回答了13个问题
俗世一尘埃 共回答了13个问题 |采纳率76.9%比如说在水溶液中,能导电,但是叫做电解质溶液,而溶质叫做电解质。而电解质本身不能导电,溶液是混合物,电解质是借助在水溶液或熔融状态下才能导电1年前查看全部
- 像皮 铅笔芯 回形针 铁钉 干木棍 铜丝 塑料棒 铝制钥匙哪个是容易导电的东西
 文心5551年前1
文心5551年前1 -
 zhongliyuan43 共回答了16个问题
zhongliyuan43 共回答了16个问题 |采纳率87.5%铅笔芯 回形针 铁钉 铜丝 铝制钥匙都是容易导电的东西,其中铜丝导电效果最好.1年前查看全部
- 铝用炭素材料导电能力是怎么得来的
 诸葛很靓1年前1
诸葛很靓1年前1 -
 芭乐斯坦 共回答了16个问题
芭乐斯坦 共回答了16个问题 |采纳率81.3%看电阻率,及各种理化指标1年前查看全部
- 物质的量浓度均为1mol/L的下列溶液,盐酸、硫酸、醋酸,导电能力由强到弱
 爱的ww1年前1
爱的ww1年前1 -
 lastwood 共回答了18个问题
lastwood 共回答了18个问题 |采纳率100%硫酸〉盐酸〉醋酸1年前查看全部
- 下列关于弱电解质的说法正确的是: ( ) A.电解质越弱,则其溶液的导电能力就越差 B.同一弱电解质,浓度越
下列关于弱电解质的说法正确的是:()
A.电解质越弱,则其溶液的导电能力就越差 B.同一弱电解质,浓度越大,电离程度越大 C.升高温度,弱电解质的电离程度减小 D.弱电解质的相对强弱可由相同温度下的电离常数值的大小来判断  liangwanru1年前1
liangwanru1年前1 -
 unique830101 共回答了25个问题
unique830101 共回答了25个问题 |采纳率96%D
A错误,电解质的强弱与其在溶液中导电能力的大小没有直接关系,溶液中导电能力大小只与溶液中的离子浓度和离子所带电荷数目有关。
B错误,对于弱电解质,浓度越大,电离程度越小。
C错误,电离过程是吸热,升高温度,弱电解质的电离平衡正向移动,电离程度增大。
D正确。1年前查看全部
- 金属导体导电,为什么电流方向与电荷运动方向不同
 潇湘-juan1年前2
潇湘-juan1年前2 -
 hgh1818 共回答了10个问题
hgh1818 共回答了10个问题 |采纳率90%应该是电子吧~
物理学上规定,以正电荷定向移动的方向为电流方向.
电子带负电,所以电流方向与电子定向移动方向相反.1年前查看全部
- 为什么液氨和无水乙醇是非电解质,它们溶于水不导电吗?
 fancyfreei1年前1
fancyfreei1年前1 -
 ds5f5r5r55 共回答了15个问题
ds5f5r5r55 共回答了15个问题 |采纳率86.7%液氨和乙醇溶于水都不能直接电离出离子(乙醇电离的比水还少视为不电离)
氨分子与水生成的一水合氨能直接电离生成铵离子和氢氧根离子,所以一水合氨是电解质才对.1年前查看全部
- 什么样的物体具有导电性,为什么,下列哪些物体不能导电,为什么1.NACL晶体2.纯硫酸3,融化的碳酸钾 4液态氯化
 dapaojj1年前2
dapaojj1年前2 -
 tackiezhou 共回答了14个问题
tackiezhou 共回答了14个问题 |采纳率92.9%41年前查看全部
- 绝缘体不容易导电的原因
 橘子香烟1年前1
橘子香烟1年前1 -
 thnht 共回答了17个问题
thnht 共回答了17个问题 |采纳率82.4%绝缘体内部的自由电荷极少极少1年前查看全部
- 将40g烧碱溶于水得溶液甲,再向甲中通入1molHCl得溶液乙,则在相同温度下甲和乙的导电能力一样.为什么?
 Phonixsong1年前1
Phonixsong1年前1 -
 兜兜多多 共回答了18个问题
兜兜多多 共回答了18个问题 |采纳率94.4%如果不考虑溶液体积变化,那麼甲有1molNaOH,乙有1molNaCl,大家阴阳离子的总量以及带电都是一样的,那麼导电能力当然相同.1年前查看全部
- 下列说法错误的是( )A. 导体能够导电是因为导体内有自由电荷B. 绝缘体不容易导电是因为绝缘体内没有电荷C. 金属能
下列说法错误的是( )
A. 导体能够导电是因为导体内有自由电荷
B. 绝缘体不容易导电是因为绝缘体内没有电荷
C. 金属能够导电是因为金属内有自由电子
D. 酸、碱、盐的水溶液导电靠正离子和负离子 icerhx1年前3
icerhx1年前3 -
 小小鸟1986 共回答了21个问题
小小鸟1986 共回答了21个问题 |采纳率90.5%解题思路:不同物质的导电能力是不同的,容易导电的称为导体,不容易导电的称为绝缘体.导体容易导电,是因为导体内有能够自由移动的电荷;而绝缘体不容易导电,是因为绝缘体内几乎没有能够自由移动的电荷.A、导体能够导电是因为导体内有大量的自由电荷;故A正确;
B、绝缘体不容易导电是因为绝缘体内的电荷不能够自由移动,故B错;
C、金属能够导电是因为金属导体中存在大量的自由电荷,这些自由电荷就是自由电子;故C正确;
D、酸、碱、盐的水溶液中存在大量的正负离子;它导电就是靠正离子和负离子;故D正确;
故选B.点评:
本题考点: 导体和绝缘体的区别.
考点点评: 明确导体和绝缘体的本质区别(是否含有大量自由电荷),是解答此题的关键.1年前查看全部
- 液态氯化钠导电么注:不是溶液,是液态纯氯化钠
 cgh8301年前2
cgh8301年前2 -
 wangnan1024 共回答了21个问题
wangnan1024 共回答了21个问题 |采纳率90.5%导电的,因为氯化钠是电解质,在熔融状态下即可以导电.1年前查看全部
- 导体容易导电,是因为导体中有大量的自由电子
导体容易导电,是因为导体中有大量的自由电子
这句话为什么错了? wh1001年前2
wh1001年前2 -
 wk2235ads2235 共回答了13个问题
wk2235ads2235 共回答了13个问题 |采纳率92.3%因为并不是所有的导体导电都是靠自由电子导电的
例如,NaOH水溶液导电就不是靠电子,而是靠正负离子1年前查看全部
- 液态的HCL和液氨导电吗
 是过往1年前2
是过往1年前2 -
 heweiwei555 共回答了16个问题
heweiwei555 共回答了16个问题 |采纳率75%不导电的.液态的HCL和液氨是纯净物,里面不含可自由移动的离子.液态的HCL和液氨是HCL和NH3的液态形式1年前查看全部
- 一定温度下,冰醋酸加水稀释过程中溶液的导电能力变化曲线如图所示,请回答:
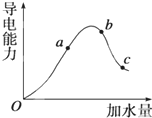 一定温度下,冰醋酸加水稀释过程中溶液的导电能力变化曲线如图所示,请回答:
一定温度下,冰醋酸加水稀释过程中溶液的导电能力变化曲线如图所示,请回答:
(1)O点为什么不导电______.
(2)a、b、c三点的pH由小到大的顺序是______.
(3)H+的物质的量最大的是______(填“a”、“b”或“c”).
(4)若使c点溶液中的c(CH3COO-)增大,可以采取下列措施中的______(填序号).
A.加热B.加很稀的NaOH溶液 C.加NaOH固体 D.加水E.加固体CH3COONa F.加入锌粒. 过去就让它过去1年前1
过去就让它过去1年前1 -
 大鱼头 共回答了22个问题
大鱼头 共回答了22个问题 |采纳率77.3%解题思路:(1)溶液的导电性与离子浓度有关,离子浓度越大,导电性越强;
(2)导电能力越强,离子浓度越大,氢离子浓度越大,pH越小;
(3)溶液越稀,越促进醋酸电离,则溶液中氢离子的物质的量越大;
(4)要使醋酸根离子浓度增大,可以采用加热、加入含有醋酸根离子的物质、加入和氢离子反应的物质.(1)溶液的导电性与离子浓度有关,离子浓度越大,导电性越强,冰醋酸中没有自由移动的离子,所以冰醋酸不导电,故答案为:无自由移动的离子;
(2)导电能力越强,离子浓度越大,氢离子浓度越大,pH越小,则a、b、c三点溶液的pH为b<a<c,故答案为:b<a<c;
(3)溶液越稀,越促进醋酸电离,则溶液中氢离子的物质的量越大,所以氢离子物质的量最大的是c,故选C;
(4)要使醋酸根离子浓度增大,可以采用加热、加入含有醋酸根离子的物质、加入和氢离子反应的物质,
A.加热促进醋酸电离,则溶液中醋酸根离子浓度增大,故正确;
B.加很稀的NaOH溶液,促进醋酸电离,但溶液的体积增大,导致醋酸根离子浓度减小,故错误;
C.加NaOH固体,氢氧化钠和氢离子反应促进醋酸电离,所以醋酸根离子浓度增大,故正确;
D.加水稀释能促进醋酸电离,但醋酸根离子浓度减小,故错误;
E.加固体CH3COONa,能抑制醋酸电离,但醋酸钠电离出的醋酸根离子大于抑制醋酸电离出的醋酸根离子,所以醋酸根离子浓度增大,故正确;
F.加入锌粒,和氢离子反应,促进醋酸电离,所以醋酸根离子浓度增大,故正确;
故选ACEF.点评:
本题考点: 弱电解质在水溶液中的电离平衡.
考点点评: 本题考查电解质的电离,题目难度中等,易错选项是D,加水稀释醋酸,能促进醋酸电离,但溶液中醋酸根离子增大的量远远小于水体积增大的量,所以醋酸根离子浓度减小,为易错点.1年前查看全部
- 下列叙述正确的是()A绿化难溶液在电流作用下电离成钠离子和氯离子所以能导电B二氧化硫的水溶液能导电,所以二氧化硫式电解质
下列叙述正确的是()
A绿化难溶液在电流作用下电离成钠离子和氯离子所以能导电
B二氧化硫的水溶液能导电,所以二氧化硫式电解质
C硫酸钡难容于水,但硫酸钡属于强电解质‘
D固体氯化钠不到点,所以氯化钠是非电解质
下列各组物质的分类正确的是()
A纯净物 :蒸馏水 盐酸 只含氧元素的固体
B非电解质 :CL2 NH3 C2H5OH
C胶体分散系:淀粉溶液 Fe(OH)3胶体 泥沙水
D酸性氧化物:CO2 SO2 SO3
在某些无色同名的酸性溶液中,能共存的例子是()
A Na+ K+ So42- CO32- B Cu2+ K+ So42- No3-
C Na+ K+ Cl- No3- D Ba2+ K+ So42- Cl-
能用H++OH-==H20表示的是()
A氢氧化钡和稀硫酸 B氢氧化铜和稀硝酸
C醋酸和氢氧化钾 D氢氧化钠和硫酸 sqsq5204431年前1
sqsq5204431年前1 -
 液体蜘蛛 共回答了18个问题
液体蜘蛛 共回答了18个问题 |采纳率94.4%1.C
A选项中,氯化钠并非在电流作用下电离,而是在水中解离,形成水和钠离子与水和氯离子;B中二氧化硫溶于水形成亚硫酸,亚硫酸是电解质;C中硫酸钡不溶于水,但也有一小部分溶于水,且完全电离,故是强电解质;固体氯化钠熔融可以导电,是电解质.
2.D
A选项中盐酸和只含氧元素的固体不是纯净物;氯气是纯净物,不符合非电解质是化合物的条件;泥沙水是悬浊液;D中非金属氧化物都是酸性氧化物.
3.C
碳酸根离子和氢离子会生成气体,不能共存;铜离子在水中呈蓝色,不符合;D中钡离子和硫酸根例子生成不溶于水的固体,不符合.
4.D
A中氢氧化钡和硫酸不仅生成水,还生成硫酸钡,不可省去;B中氢氧化铜不可分;醋酸是弱酸,不完全电离,不可分;D中离子前面的计量数可以略去,符合.1年前查看全部
- 熔化的KcL能导电吗?不是溶于水。
 多吃水果蔬菜1年前1
多吃水果蔬菜1年前1 -
 一帖成名天下知 共回答了17个问题
一帖成名天下知 共回答了17个问题 |采纳率88.2%熔化的KCl能导电1年前查看全部
- 哪些物质只能在熔融状态下导电,哪些只能在水溶液
 翻筋斗的云1年前1
翻筋斗的云1年前1 -
 桂鬼鬼 共回答了20个问题
桂鬼鬼 共回答了20个问题 |采纳率85%共价化合物,在液态条件下,共价键不发生断裂,不能形成自由移动的带电离子,因此不能导电.如:液态H2SO4、液态HCL、液氨等.但是,它们虽然液态不能导电,在水溶液中,由于水分子的影响,共价键被破坏,形成阴阳离子,能够导电.
离子化合物在液态下(熔融状态)和在水溶液中,离子键被破坏,形成自由移动的离子,因此都能导电.
所以离子化合物在水溶液中和熔融状态下都能导电,而共价化合物只有在水溶液中才导电.
你理解下这两个电离方程式,其中道理就明白了.
Na2HSO4(硫酸氢钠)的电离:
水溶液中:Na2HSO4==2Na+加H+加SO4 2-(离子键和共价键都断裂)熔融状态:Na2HSO4== 2Na+加HSO4-(离子键断裂,而共价键不断裂)1年前查看全部
- (2008•广东)电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率的变化可以确定滴定反应的终点.如图所示是KO
 (2008•广东)电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率的变化可以确定滴定反应的终点.如图所示是KOH溶液分别滴定HCl溶液和CH3COOH溶液的滴定曲线.下列示意图中,能正确表示用NH3•H2O滴定HCl和CH3COOH混合溶液的滴定曲线的是( )
(2008•广东)电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率的变化可以确定滴定反应的终点.如图所示是KOH溶液分别滴定HCl溶液和CH3COOH溶液的滴定曲线.下列示意图中,能正确表示用NH3•H2O滴定HCl和CH3COOH混合溶液的滴定曲线的是( )
A.
B.
C.
D.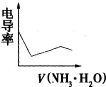
 人在行云里1年前1
人在行云里1年前1 -
 钟小洁 共回答了12个问题
钟小洁 共回答了12个问题 |采纳率83.3%解题思路:醋酸和一水合氨是弱电解质,在溶液里部分电离,氯化氢是强电解质,完全电离,向混合溶液中滴加氨水,氨水先和氯化氢反应生成强电解质氯化铵,氯化氢完全反应后,氨水再和醋酸反应生成强电解质醋酸铵,根据溶液中离子浓度变化与电导率的关系分析解答.氯化氢是强电解质,醋酸是弱电解质,滴加的弱电解质先和氯化氢反应生成强电解质氯化铵,但溶液体积不断增大,溶液被稀释,所以电导率下降;当氯化氢完全被中和后,一水合氨继续电离与弱电解质醋酸反应生成强电解质醋酸铵,所以电导率增大;醋酸也完全反应后,继续滴加氨水,因为溶液被稀释,电导率有下降趋势,故选D.
点评:
本题考点: 电解质溶液的导电性;中和滴定.
考点点评: 本题考查了酸碱中和溶液电导率的变化,明确电导率与离子浓度的关系是解本题关键,根据电解质的强弱、离子浓度的变化来分析解答即可,难度中等.1年前查看全部
- 导体为什么能够导电?绝缘体为什么不导电?
导体为什么能够导电?绝缘体为什么不导电?
Quickly! 隐性的燃烧1年前1
隐性的燃烧1年前1 -
 mxuestc 共回答了16个问题
mxuestc 共回答了16个问题 |采纳率87.5%导体内有自由移动的电子,所以能导电;绝缘体内没有自由移动的电子,所以不导电.1年前查看全部
- 利用原子知识,请解释导体容易导电,绝缘体不容易导电.
 xuesong20051年前1
xuesong20051年前1 -
 出来看上帝 共回答了16个问题
出来看上帝 共回答了16个问题 |采纳率87.5%只能从电子说起 导体中的电子可自由移动 受外电场作用定向移动形成电流就是导电 而绝缘体中的电子不可自由移动1年前查看全部
- 12月16日化学21页:3.下列溶液中加入少量NaOH固体导电能力变化不大的是
12月16日化学21页:3.下列溶液中加入少量NaOH固体导电能力变化不大的是
A 盐酸 B CH3COOH C NH3.H2O D H2O
请问下面网上查的解析里的对于ABD的解释对吗?另外,请帮忙讲解一下C选项,谢谢! 选AA溶液中原有H+与Cl-,加入少量NaOH后H+与OH-中和形成H2O,但少了多少H+就有多少Na+来填补,所以变化不大.B中醋酸原本不易电离,加入NaOH后变成易电离的醋酸钠,所以很有影响C与B类似.D原本几乎不导电,加入NaOH后有阴阳离子易导电了
 wetw423df1年前1
wetw423df1年前1 -
 aspy 共回答了18个问题
aspy 共回答了18个问题 |采纳率83.3%A 是正确的, 导电能力取决于溶液中离子浓度的大小. HCl== H+ + Cl-
与NaOH反应后生成了NaCl和水 , NaCl == Na+ + Cl- 离子数目基本没变,1年前查看全部
- 熔融的氢氧化钠 硝酸钾晶体 这两个哪个能导电 又是电解质?
熔融的氢氧化钠 硝酸钾晶体 这两个哪个能导电 又是电解质?
怎样才能知道 哪种物质导电 哪种不导电呢? sammyhe761年前1
sammyhe761年前1 -
 夜魔之刃 共回答了15个问题
夜魔之刃 共回答了15个问题 |采纳率73.3%能否导电,看其中有无自由移动的离子或自由电子.
熔融的氢氧化钠——有自由移动的钠离子和氢氧根离子——能导电.
硝酸钾晶体——无自由移动的离子——不能导电.
电解质,指的是化合物,且在熔融状态或在溶液中能电离出自由移动的离子,能导电.熔融的氢氧化钠、硝酸钾晶体都属于电解质.
所以,能导电又是电解质的是熔融的氢氧化钠.1年前查看全部
- 为什么固体氧化镁不能导电,而氧化镁水溶液或加热到融化时便能导电
 蝶若停翅1年前1
蝶若停翅1年前1 -
 200739 共回答了21个问题
200739 共回答了21个问题 |采纳率95.2%物体导电需要有可移动的自由电子
固体氧化镁中的电子不可以自由移动 而溶液中氧化镁为离子状态 或加热时可分解
所以固体氧化镁不能导电,而氧化镁水溶液或加热到融化时便能导电1年前查看全部
- 将下列物质分别加入到Ba(OH)2溶液中,溶液导电能力明显减弱的是?为什么
将下列物质分别加入到Ba(OH)2溶液中,溶液导电能力明显减弱的是?为什么
A,.盐酸
B.Na2co3
C.Na2so4
D.H2so4 网络邂逅1年前2
网络邂逅1年前2 -
 liuxiao3322 共回答了18个问题
liuxiao3322 共回答了18个问题 |采纳率94.4%D.H2so4
Ba(OH)2+H2SO4=BaSO4(沉淀)+2H2O
反应完后原溶液中只有水和沉淀了,所以导电能力明显减弱
其他几种方法溶液中都会还有离子存在1年前查看全部
- 超过多少度水银就不能导电了
 rendi1年前2
rendi1年前2 -
 可以哭也可以笑 共回答了14个问题
可以哭也可以笑 共回答了14个问题 |采纳率100%水银是金属汞,它的凝点是-38.8°沸点是356.7°C,它一般状态下是液态可以导电,凝固后成金属固体也可一导电,只有温度超过356.7°C水银成汞蒸气,这种情况下其实也可以导电,只是汞蒸气导电能力非常弱,也就不导电了1年前查看全部
- 怎样判断电解质的导电能力分别向下列各溶液中加入少量NaOH固体,溶液的导电能力变化最小的是( )A、水 B、盐酸 C、醋
怎样判断电解质的导电能力
分别向下列各溶液中加入少量NaOH固体,溶液的导电能力变化最小的是( )
A、水 B、盐酸 C、醋酸溶液 D、NaCl溶液
为什么?
判断导电能力是根据带电荷的多少还是离子的物质的量来判断的?比如1摩尔盐酸和1摩尔硫酸谁的导电能力强 nanlouguyan1年前4
nanlouguyan1年前4 -
 Kelly_775 共回答了24个问题
Kelly_775 共回答了24个问题 |采纳率87.5%分别向下列各溶液中加入少量NaOH固体,溶液的导电能力变化最小的是( )
A、水 变化较大,因为水是弱电解质,加入强电解质后,离子浓度变化较大
B、盐酸
正确.加入少量烧碱后,会和少量盐酸反应,但是生成了氯化钠,相当于反应的那部分盐酸换成了氯化钠,所以离子浓度几乎没有变化.
C、醋酸溶液
答案解释同A
D、NaCl溶液
这样溶液中的离子浓度直接多了加入的氢氧化钠,离子浓度增大,变化较大.
所以以上变化最小的是B.
导电能力的强弱与离子的浓度及离子所带电荷的多少有关,离子浓度越大,导电能力越强,相同浓度下,离子所带电荷越多导电能力越强.
比如都是1mol每升的盐酸与硫酸相比,硫酸的导电能力强.因为所带电荷多.
理解请及时采纳!1年前查看全部
- 强电解质溶液一定比弱电解质溶液的导电能力强吗
 木头果1年前1
木头果1年前1 -
 逆风飞雨 共回答了20个问题
逆风飞雨 共回答了20个问题 |采纳率95%不一定,溶液的导电性取决于溶液中自由离子的浓度,也就是说溶液中离子浓度越大导电性就越强,强电解质在熔融态或水溶液中因为能完全电离,所以离子浓度大,导电性强,但是如碳酸钙,在水中几乎不电离,所以导电性未必有饱和弱点解质的强1年前查看全部
- 什么溶液能离解出自由移动的离子?我才刚上初三,什么离解的我不懂,怎么样才能判断一种溶液能否导电啊?
 王缙1年前3
王缙1年前3 -
 恋恋红尘_boy 共回答了13个问题
恋恋红尘_boy 共回答了13个问题 |采纳率92.3%电解质(酸、碱、盐、部分的有机物)能离解出自由移动的离子,非电解质不能(比如蔗糖溶液等)1年前查看全部
- 强酸 弱酸 一元酸 二元酸 等导电能力由强到弱顺序是怎样的?
 wtt2011年前1
wtt2011年前1 -
 阳光无风 共回答了17个问题
阳光无风 共回答了17个问题 |采纳率94.1%其导电能力由电离电子决定,电离粒子越多,导电性越好,所以强酸大于弱酸,二元酸大于一元酸1年前查看全部
- 1mol/L甲酸(一元酸)溶液的导电性能比同浓度的盐酸的导电性弱 是否正确
 少堂1年前1
少堂1年前1 -
 东洋浪人 共回答了14个问题
东洋浪人 共回答了14个问题 |采纳率92.9%是的.因为甲酸是弱酸,不完全电离
导电能力比较是比较总离子浓度
盐酸是 2mol/L 总的
甲酸不到2mol/L
所以比较弱1年前查看全部
- 12.若地磁场在某区域的磁场强弱和方向处处相同,小明在该区域某处竖直拿着闭合的矩形导电线圈面向南方,则能使线圈中产生感应
12.若地磁场在某区域的磁场强弱和方向处处相同,小明在该区域某处竖直拿着闭合的矩形导电线圈面向南方,则能使线圈中产生感应电流的操作是
A.南北移动线圈 B.将线圈转至水平
C.东西移动线圈 D.上下移动线圈 寄主植物1年前2
寄主植物1年前2 -
 toper1201 共回答了20个问题
toper1201 共回答了20个问题 |采纳率90%选 B答案.要产生感应电流必须要是通过矩形框内的磁通量发生变化1年前查看全部
大家在问
- 1I'M A HUSTLA 中文意思是什么
- 2①读下列语句,写出你的理解(2分)
- 3strReg=/^\w+((-\w+)|(\.\w+))*\@{1}\w+\.{1}\w{2,4}(\.{0,1}\w{
- 4某同学在超市购物时用10N的水平力推着购物车在水平地面上做匀速直线运动,这时小车受到阻力10N
- 5已知b=√4(3a-2)+√2(2-3a)+2,求a分之1+b分之1的值
- 6请种一棵爬山虎 我叫爬山虎,在植物分类中属葡萄科.我的卷须前端的吸盘使我成为爬墙的好手.随着成市的发展,原本住在野外的我
- 7倒影微凉 作文
- 8若整数n满足(n-2012)的2次方+(n-2014)的2次方=4,求n的值
- 9求解4★+3●=45,3★+ 4●=39,★+●=?
- 107和9 9和6 4和8的最小公倍数是?
- 11写一篇去看病的英语作文,要求题目是See doctor 要写我和医生的对话(最好有中文翻译)
- 12英语句型转换1.He used a knife for cutting things.(改为同义句)He ______
- 13there are looking for work__________ and still havent got an
- 14《童趣》的阅读题:你有过类似的经历吗?
- 15Welcome to the neigborhood ,How do you like it so far?