(2011•武清区一模)复分解反应是我们学过的基本反应类型之一.学习时,应注意将知识进行归纳、总结,深刻理解复分解反应发
 luojing10242022-10-04 11:39:541条回答
luojing10242022-10-04 11:39:541条回答(1)下面有三个化学反应,请你写出①反应的化学方程式:
①碳酸钾溶液与石灰水反应______;
②碳酸钾和稀盐酸混合;
③氢氧化钡与稀硝酸混合.
(2)你想到上述复分解反应为什么能够发生吗?这是因为在这些反应物中含有一些“特殊”的阴、阳离子,它们能相互结合.如上述①中,实际参加反应的离子是CO32-和Ca2+,而K+和OH-则是“旁观者”,并没有参加反应.请你分析上述反应②中实际参加反应的离子是______,上述反应③中实际参加反应的离子是______.

已提交,审核后显示!提交回复
共1条回复
 罪里跳凳看贱 共回答了20个问题
罪里跳凳看贱 共回答了20个问题 |采纳率95%- 解题思路:复分解反应的实质是:发生复分解反应的两种物质在水溶液中相互交换离子,结合成难电离的物质----沉淀、气体、水,使溶液中离子浓度降低,化学反应即向着离子浓度降低的方向进行.
[小结]复分解反应发生的条件:
(1)反应物:必须可溶(包括可溶入酸)
(2)生成物:有沉淀、气体或水生成.(1)①根据写配注等写出,碳酸钾溶液与石灰水反应的方程式为:K2CO3+Ca(OH)2═2KOH+CaCO3↓;
故答案为:K2CO3+Ca(OH)2═2KOH+CaCO3↓;
(2)复分解反应发生的条件:生成物中有沉淀、气体或水生成,可知反应②中有二氧化碳气体生成,实际参加反应的离子为:CO32-、、H+; 反应③中有水生成,实际参加反应的离子是:H+、OH-;
故答案为:CO32-、、H+;H+、OH-.点评:
本题考点: 复分解反应的条件与实质;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查学生对复分解反应发生的条件的理解与掌握,并能在解题中灵活应用的能力. - 1年前
相关推荐
- (2014•武清区一模)如图,D是AB边上的中点,将△ABC沿过D的直线折叠,使点A落在BC上F处,若∠B=50°,则∠
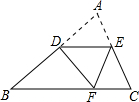 (2014•武清区一模)如图,D是AB边上的中点,将△ABC沿过D的直线折叠,使点A落在BC上F处,若∠B=50°,则∠EDF的度数为( )
(2014•武清区一模)如图,D是AB边上的中点,将△ABC沿过D的直线折叠,使点A落在BC上F处,若∠B=50°,则∠EDF的度数为( )
A.50°
B.40°
C.80°
D.60° wangyulin67671年前1
wangyulin67671年前1 -
 suyangminling 共回答了21个问题
suyangminling 共回答了21个问题 |采纳率95.2%解题思路:先根据图形翻折不变的性质可得AD=DF,根据等边对等角的性质可得∠B=∠BFD,再根据三角形的内角和定理列式计算可得∠BDF的解,再根据平角的定义和折叠的性质即可求解.∵△DEF是△DEA沿直线DE翻折变换而来,
∴AD=DF,
∵D是AB边的中点,
∴AD=BD,
∴BD=DF,
∴∠B=∠BFD,
∵∠B=50°,
∴∠BDF=180°-∠B-∠BFD=180°-50°-50°=80°,
∴∠EDF=(180°-∠BDF)÷2=50°.
故选:A.点评:
本题考点: 翻折变换(折叠问题).
考点点评: 本题考查的是图形翻折变换的图形能够重合的性质,以及等边对等角的性质,熟知折叠的性质是解答此题的关键.1年前查看全部
- (2014•武清区一模)下列各组物质按单质、有机物、混合物顺序排列的是( )
(2014•武清区一模)下列各组物质按单质、有机物、混合物顺序排列的是( )
A.氢气 乙醇 石油
B.生铁 碳酸钙 矿泉水
C.红磷 一氧化碳 空气
D.氨气 葡萄糖 冰水共存物 360872981年前1
360872981年前1 -
 tianya_wuzi 共回答了11个问题
tianya_wuzi 共回答了11个问题 |采纳率100%解题思路:根据具体物质的类别进行分析解答即可,单质是由一种元素组成的纯净物;有机物是指含有碳元素的化合物;混合物是由多种物质组成的,据此解答.A、氢气是单质,乙醇是有机物,石油是混合物,故A正确;
B、生铁是混合物,碳酸钙不是有机物,矿泉水是混合物,故B错误;
C、红磷是单质,一氧化碳不是有机物,空气是混合物,故C错误;
D、氦气是单质,葡萄糖是有机物,冰水共存物是纯净物,故D错误;
故选A.点评:
本题考点: 单质和化合物的判别;纯净物和混合物的判别;有机物与无机物的区别.
考点点评: 本题考查了常见物质的分类,完成此题,可以依据物质的组成进行.1年前查看全部
- (2014•武清区三模)双曲线C:x2a2-y2b2=1(a>0,b>0)的右焦点在直线l:x+y-2=0上,右顶点到直
(2014•武清区三模)双曲线C:
-x2 a2
=1(a>0,b>0)的右焦点在直线l:x+y-2=0上,右顶点到直线l的距离为y2 b2
,则双曲线C的渐近线方程为2 2 y=±
x.3 y=±.
x.3  dgh19811年前1
dgh19811年前1 -
 bindu99 共回答了17个问题
bindu99 共回答了17个问题 |采纳率94.1%解题思路:首先根据右焦点在直线l:x+y-2=0上,求的c=2,再根据点到直线的距离公式求得a的值,最后求出渐近线方程即可.∵直线l:x+y-2=0与x轴的交点夺坐标为(2,0),
∴c=2,
设双曲线的右顶点坐标为(a,0)
根据点到直线的距离公式可得
|a+0−2|
2=
2
2
解得a=1,a=3>2=c(舍去)
∴b=
c2−a2=
3
∵双曲线C:
x2
a2-
y2
b2=1的渐近线方程为y=±
b
ax
∴y=±
3x.
故答案为:y=±
3x.点评:
本题考点: 双曲线的简单性质.
考点点评: 本题主要考查了双曲线的性质,以及渐近线的求法,还有点到直线的距离,属于基础题.1年前查看全部
- (2013•武清区三模)下列说法不正确的是( )
(2013•武清区三模)下列说法不正确的是( )
A.用溴水即可鉴别2,4-已二烯、苯酚溶液和甲苯
B.在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH
C.在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉会溶解
D.在含有FeCl3和BaCl2的酸性混合液中,通入足量SO2气体,有白色沉淀生成,过滤后,向滤液中滴加KSCN溶液,不出现红色,白色沉淀是BaSO4 wislawa1年前1
wislawa1年前1 -
 四季下雨 共回答了14个问题
四季下雨 共回答了14个问题 |采纳率85.7%解题思路:A.溴水可与2,4-已二烯发生加成反应,与苯酚发生取代反应;
B.水解产物是CH3COOH和C2H518OH;
C.NO3-在酸性条件下与Cu发生氧化还原反应;
D.Fe3+与SO2发生氧化还原反应生成Fe2+和SO42-.A.溴水可与2,4-已二烯发生加成反应生成无色油状液体,与苯酚发生取代反应生成白色沉淀,与甲苯不反应,可鉴别,故A正确;
B.在酸性条件下,CH3CO18OC2H5的水解产物是CH3COOH和C2H518OH,故B错误;
C.NO3-在酸性条件下与Cu发生氧化还原反应,铜粉会溶解,故C正确;
D.Fe3+与SO2发生氧化还原反应生成Fe2+和SO42-,则向滤液中滴加KSCN溶液,不出现红色,白色沉淀是BaSO4,故D正确.
故选B.点评:
本题考点: 有机物的鉴别;酯的性质;物质的检验和鉴别的基本方法选择及应用.
考点点评: 本题考查较为综合,涉及有机物的检验、氧化还原反应等知识,注意把握相关物质的性质,题目难度不大.1年前查看全部
- (2014•武清区三模)下列方法正确的是( )
(2014•武清区三模)下列方法正确的是( )
A.[SiO4]的四面体结构: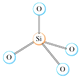
B.C2H5Cl与NaOH溶液混合加热水解后,加入AgNO3溶液,以检验Cl-
C.在MgCl2晶体中含有共价键和离子键
D.0.5g C3H4中含有共用电子对的数目为1×6.02×1023 ii叶情1年前1
ii叶情1年前1 -
 qq修罗 共回答了24个问题
qq修罗 共回答了24个问题 |采纳率87.5%解题思路:A、每个Si与4个O结合形成四面体结构;
B、多余的NaOH与AgNO3溶液会形成沉淀;
C、MgCl2晶体中只有离子键;
D、根据分子中共价键数判断.A、每个Si与4个O结合形成四面体结构,所以[SiO4]的四面体结构:
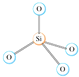 ,故A正确;
,故A正确;
B、C2H5Cl与NaOH溶液混合加热水解后,再加足量稀硝酸中和多余的NaOH,然后加入AgNO3溶液,以检验Cl-,故B错误;
C、MgCl2晶体中镁离子与氯离子形成离子键,晶体中没有共价键,故C错误;
D、1molC3H4中含有4molC-H,1molC-C,1molC≡C,共8mol共用电子对,0.5g C3H4的物质的量为[0.5g/40g/mol]=0.0125mol,则含有共用电子对的数目为0.1×6.02×1023,故D错误;
故选A.点评:
本题考点: 不同晶体的结构微粒及微粒间作用力的区别;常见阴离子的检验.
考点点评: 本题考查了晶体结构、氯代烃中氯原子的检验、离子键、共用电子对数的计算等,题目涉及的知识点较多,侧重于基础知识的考查,难度不大.1年前查看全部
- (2012•武清区一模)命题“∀x∈(1,2),x2>x+1”的否定为( )
(2012•武清区一模)命题“∀x∈(1,2),x2>x+1”的否定为( )
A.∃x0∈(1,2),x02≤x0+1
B.∃x0∈(1,2),x02<x0+1
C.∀x∉(1,2),x2>x+1
D.∀x∉(1,2),x2≤x+1 05440250341年前1
05440250341年前1 -
 呢呢惰 共回答了12个问题
呢呢惰 共回答了12个问题 |采纳率91.7%∵命题“∀x∈(1,2),x2>x+1”的否定,
∵任意的否定为存在,
∴命题的否定为∃x0∈(1,2),x02≤x0+1,
故选A.1年前查看全部
- (2014•武清区三模)阅读如图的程序框图,运行相应的程序,则输出n的值为[4/5][4/5].
 乱侃世家1年前1
乱侃世家1年前1 -
 淡白稚气 共回答了16个问题
淡白稚气 共回答了16个问题 |采纳率100%解题思路:根据题意,模拟程序框图的运行过程,即可得出输出的结果是什么.模拟程序框图的运行过程,如下;
i=1,m=0,n=0,i≤4?,是;
i=2,m=0+1=1,n=0+[1/1×2]=[1/2],i≤4?,是;
i=3,m=1+1=2,n=[1/2]+[1/2×3]=[2/3],i≤4?,是;
i=4,m=2+1=3,n=[2/3]+[1/3×4]=[3/4],i≤4?,是;
i=5,m=3+1=4,n=[3/4]+[1/4×5]=[4/5],i≤4?,否;
输出n=[4/5].
故答案为:[4/5].点评:
本题考点: 程序框图.
考点点评: 本题考查了程序框图的应用问题,解题时应模拟程序框图的运行过程,以便得出正确的答案,是基础题.1年前查看全部
- (2011•武清区一模)下列四种基本反应类型中,可能没有化合物生成的是( )
(2011•武清区一模)下列四种基本反应类型中,可能没有化合物生成的是( )
A.置换反应
B.化合反应
C.分解反应
D.复分解反应 lilin19851985_11年前1
lilin19851985_11年前1 -
 rriew 共回答了17个问题
rriew 共回答了17个问题 |采纳率94.1%解题思路:化合反应是指由两种或两种以上物质反应生成另外一种物质的反应.
分解反应是指由一种物质生成另外两种或两种以上物质的反应.
置换反应是指由一种单质和一种化合物反应,生成另外一种单质和一种化合物的反应.
复分解反应是指由两种化合物相互交换成分,生成另外两种新的化合物的反应.由各种反应类型的概念可知,分解反应的生成物中可能没有化合物生成,例如,电解水能生成氢气和氧气,生成物中没有化合物.
故选C.点评:
本题考点: 反应类型的判定;单质和化合物的判别;化合反应及其应用;分解反应及其应用;置换反应及其应用;复分解反应及其应用.
考点点评: 解答本题要充分理解各种反应类型的特点,只有这样才能对相关方面的问题做出正确的判断.1年前查看全部
- (2014•武清区一模)电路元件A和B中的电流与两端电压关系如图.由图可知,A的电阻是______Ω.若将A、B并联后接
 (2014•武清区一模)电路元件A和B中的电流与两端电压关系如图.由图可知,A的电阻是______Ω.若将A、B并联后接在电压为2V的电源两端,干路中的电流是______A.
(2014•武清区一模)电路元件A和B中的电流与两端电压关系如图.由图可知,A的电阻是______Ω.若将A、B并联后接在电压为2V的电源两端,干路中的电流是______A.  hyesung241年前1
hyesung241年前1 -
 风静音 共回答了14个问题
风静音 共回答了14个问题 |采纳率85.7%解题思路:(1)先根据元件A的U-I图象读出任一电压和对应的电流,根据欧姆定律求出其阻值的大小;
(2)根据并联电路电压特点可知两电阻并联时两端的电压,再根据图象读出对应的电流,根据并联电路的电流特点求出干路电流.(1)由图象可知,当UA=3V,IA=0.6A,
元件A的电阻RA=
UA
IA=[3V/0.6A]=5Ω;
(2)元件A、B并联后接在电压为2V的电源两端时,UA=UB=2V,
由图象可知,IA=0.4A,IB=0.2A,
干路电流I=IA+IB=0.4A+0.2A=0.6A.
故答案为:5;0.6.点评:
本题考点: 欧姆定律的应用.
考点点评: 本题要求学生正确应用图象获得必要信息,并能结合并联电路的特点熟练应用欧姆定律的计算公式.1年前查看全部
- (2010•武清区一模)已知三次函数f(x)=x3+ax2-6x+b,a、b为实数,f(0)=1,曲线y=f(x)在点(
(2010•武清区一模)已知三次函数f(x)=x3+ax2-6x+b,a、b为实数,f(0)=1,曲线y=f(x)在点(1,f(1))处切线的斜率为-6.
(1)求函数f(x)的解析式;
(2)若f(x)≤|2m-1|对任意的x∈(-2,2)恒成立,求实数m的取值范围. 败家生子1年前1
败家生子1年前1 -
 fastghost 共回答了16个问题
fastghost 共回答了16个问题 |采纳率87.5%解题思路:(1)先求函数的导数,进而根据f'(1)=-6求出a的值,然后根据f(0)=1,求出b的值即可求出函数的解析式;
(2)先利用导数判断函数的单调性,进而求出函数在区间(-2,2)内的最大值,再解不等式即可.(1)f'(x)=3x2+2ax-6…(1分)由导数的几何意义,f'(1)=-6∴a=-32 …(2分)∵f(0)=1∴b=1…(3分)∴f(x)=x3-32x2-6x+1…(4分)(2)f'(x)=3x2-3x-6=3(x+1...
点评:
本题考点: 导数的几何意义;函数解析式的求解及常用方法;函数恒成立问题.
考点点评: 本题的考查了导数的几何意义、导数的求法以及函数恒成立问题,对于函数恒成立问题一般转化成求函数的最值问题,属于中档题.1年前查看全部
- (2007•武清区模拟)一个正方形线圈边长a=0.20m,共有n=100匝,其总电阻r=4.0Ω.线圈与阻值R=16Ω的
 (2007•武清区模拟)一个正方形线圈边长a=0.20m,共有n=100匝,其总电阻r=4.0Ω.线圈与阻值R=16Ω的外电阻连成闭合回路,如图甲所示.线圈所在区域存在着分布均匀但强弱随时间变化的磁场,磁场方向垂直线圈平面,其磁感应强度B的大小随时间作周期性变化的周期T=1.0×10-2s,如图乙所示,图象中t1=
(2007•武清区模拟)一个正方形线圈边长a=0.20m,共有n=100匝,其总电阻r=4.0Ω.线圈与阻值R=16Ω的外电阻连成闭合回路,如图甲所示.线圈所在区域存在着分布均匀但强弱随时间变化的磁场,磁场方向垂直线圈平面,其磁感应强度B的大小随时间作周期性变化的周期T=1.0×10-2s,如图乙所示,图象中t1=
T,T2=1 3
T,t3=4 3
T、….求:7 3
(1)0-t1时间内,通过电阻R的电荷量;
(2)t=1.0s内电通过电阻R所产生的热量;
(3)线圈中产生感应电流的有效值. huitian1年前1
huitian1年前1 -
 ourunyang 共回答了26个问题
ourunyang 共回答了26个问题 |采纳率84.6%解题思路:(1)根据法拉第电磁感应定律与闭合电路欧姆定律,并依据电量表达式,即可求解;(2)根据焦耳定律,可求出一个周期内的产生热量,从而可求出1秒内电阻R所产生的热量;(3)通过感应电流的有效值来计算一个周期内的热量,从而即可求解.(1)0-t1时间内的感应电动势E=n
Bma2
t1=60V
通过电阻R的电流I1=[E/R+r]=3.0A
所以在0-t1时间内通过R的电荷量q=I1t1=1.0×10-2C
(2)在一个周期内,电流通过电阻R产生热量Q1=
I21R
T
3=0.48J
在1.0s内电阻R产生的热量为Q=
t
T
Q 1=
1
0.01×0.48J=48J
(3)设感应电流的有效值为I,则一个周期内电流产生的热量
I21Rt1=I2RT
解得I=
t1
TI1=
3A
答:(1)0-t1时间内,通过电阻R的电荷量1.0×10-2C;
(2)t=1.0s内电通过电阻R所产生的热量48J;
(3)线圈中产生感应电流的有效值
3A.点评:
本题考点: 法拉第电磁感应定律;闭合电路的欧姆定律;电磁感应中的能量转化.
考点点评: 考查法拉第电磁感应定律,闭合电路欧姆定律,焦耳定律等规律的应用,掌握交流电的有效值来计算焦耳热.1年前查看全部
- (2011•武清区一模)如图,△ABC是等腰直角三角形,BC是斜边,将△ABP绕点A逆时针旋转后,能与△ACD重合,如果
 (2011•武清区一模)如图,△ABC是等腰直角三角形,BC是斜边,将△ABP绕点A逆时针旋转后,能与△ACD重合,如果AP=
(2011•武清区一模)如图,△ABC是等腰直角三角形,BC是斜边,将△ABP绕点A逆时针旋转后,能与△ACD重合,如果AP=
,那么PD的长等于______.2  wyh206011601年前1
wyh206011601年前1 -
 ge6hjweggew 共回答了16个问题
ge6hjweggew 共回答了16个问题 |采纳率87.5%解题思路:根据等腰直角三角形得到AC=AB,∠BAC=90°,因为△ABP绕点A逆时针旋转后能与△ACD重合,则AB与AC重合,AP与AD重合,根据旋转的性质有AP=AD,∠PAD=∠BAC=90°,得到△APD为等腰直角三角形,则有PD=
AP,然后把AP=2
代入计算即可.2 ∵△ABC是等腰直角三角形,
∴AC=AB,∠BAC=90°,
∵△ABP绕点A逆时针旋转后能与△ACD重合,即AB与AC重合,AP与AD重合,
∴AP=AD,∠PAD=∠BAC=90°,
∴△APD为等腰直角三角形,
∴PD=
2AP,
∵AP=
2,
∴PD=
2×
2=2.
故答案为2.点评:
本题考点: 旋转的性质;等腰直角三角形.
考点点评: 本题考查了旋转的性质:旋转前后两图形全等,即对应角线段,对应线段线段;对应点的连线段所夹的角等于旋转角;对应点到旋转中心的距离相等.也考查了等腰直角三角形的判定与性质.1年前查看全部
- (2014•武清区一模)在Rt△ABC中,∠C=90°,若sinA=[1/2],则∠A的度数是( )
(2014•武清区一模)在Rt△ABC中,∠C=90°,若sinA=[1/2],则∠A的度数是( )
A.30°
B.45°
C.60°
D.90° 龙之剑缘1年前1
龙之剑缘1年前1 -
 zqb17 共回答了17个问题
zqb17 共回答了17个问题 |采纳率88.2%解题思路:根据特殊角的函数值sin30°=[1/2]可得答案.∵sin30°=[1/2],
∴∠A=30°,
故选:A.点评:
本题考点: 特殊角的三角函数值.
考点点评: 此题主要考查了特殊角的函数值,关键时熟练掌握sin30°=[1/2]; cos30°=32;tan30°=33;sin45°=22;cos45°=22;tan45°=1;sin60°=32;cos60°=[1/2]; tan60°=3;代入计算即可.1年前查看全部
- (2014•武清区一模)某遗传病的遗传涉及非同源染色体上的两对等位基因.已知Ⅰ-1基因型为AaBB,且Ⅱ-2与Ⅱ-3婚配
(2014•武清区一模)某遗传病的遗传涉及非同源染色体上的两对等位基因.已知Ⅰ-1基因型为AaBB,且Ⅱ-2与Ⅱ-3婚配的子代不会患病.根据以下系谱图,正确的推断是( )

A.Ⅰ-3的基因型一定为AABb
B.Ⅱ-2的基因型一定为aaBB
C.Ⅲ-1的基因型可能为 AaBb或AABb
D.Ⅲ-2与基因型为AaBb的女性婚配,子代患病的概率为[3/16] 快乐天秤座1年前1
快乐天秤座1年前1 -
 革这伙马马的命 共回答了19个问题
革这伙马马的命 共回答了19个问题 |采纳率94.7%解题思路:“Ⅰ-1基因型为AaBB”而个体不会患病,由此可推知基因型为A_B_的个体表现正常,也可推知患病的个体Ⅱ-2的基因型必为aaB_.由于第Ⅲ代不会患病,第Ⅲ代个体的基因型一定为AaB_,故Ⅱ-3的基因型必为AAbb,同时确定Ⅱ-2的基因型必为aaBB,Ⅲ-1与Ⅲ-2的基因型都是AaBb.A、由于Ⅱ-3的基因型为AAbb,因此Ⅰ-3的基因型可以为AABb或AaBb,A错误;
B、由以上分析可知:Ⅱ-2的基因型一定为aaBB,B正确;
C、Ⅱ-2的基因型只能是aaBB,Ⅱ-3的基因型只能是Aabb,所以III-1的基因型只能是AaBb,C错误;
D、III-2基因型为AaBb,与AaBb的女性婚配,后代患病的概率[7/16],D错误.
故选:B.点评:
本题考点: 基因的自由组合规律的实质及应用.
考点点评: 本题结合系谱图,考查自由组合定律和系谱图的判断,首先要求考生掌握基因自由组合定律的实质,能根据题干信息“已知Ⅰ-1基因型为AaBB,且Ⅱ-2与Ⅱ-3婚配的子代不会患病”,判断出双显性个体才正常的结论,进而推导出Ⅱ-2和Ⅱ-3的基因型,再对选项作出正确的判断.1年前查看全部
- (2012•武清区一模)150辆汽车正在经过某一雷达区,这些汽车行进的时速频率分布直方图如图所示,则时速超过60km/h
 (2012•武清区一模)150辆汽车正在经过某一雷达区,这些汽车行进的时速频率分布直方图如图所示,则时速超过60km/h的汽车数量约为______辆.
(2012•武清区一模)150辆汽车正在经过某一雷达区,这些汽车行进的时速频率分布直方图如图所示,则时速超过60km/h的汽车数量约为______辆.  迷失的孔雀1年前1
迷失的孔雀1年前1 -
 Hai_Gui 共回答了21个问题
Hai_Gui 共回答了21个问题 |采纳率81%解题思路:根据频率分布直方图中小长方形的面积=组距×[频率/组距]=频率,从而求出时速超过60km/h的汽车的频率,再根据频数=频率×样本容量求出频数即可.时速超过60km/h的汽车的频率=(0.028+0.010)×10=0.38
∴时速超过60km/h的汽车的频数=0.38×150=57(辆).
故答案为:57.点评:
本题考点: 频率分布直方图.
考点点评: 本题主要考查了频率分布直方图,小长方形的面积=组距×[频率/组距]=频率,各个矩形面积之和等于1,频数=频率×样本容量,属于基础题.1年前查看全部
- (2008•武清区二模)如图所示,四棱锥P-ABCD的底面ABCD为正方形,PD⊥底面ABCD,PD=AD.
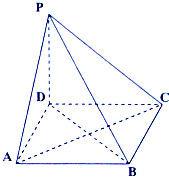 (2008•武清区二模)如图所示,四棱锥P-ABCD的底面ABCD为正方形,PD⊥底面ABCD,PD=AD.
(2008•武清区二模)如图所示,四棱锥P-ABCD的底面ABCD为正方形,PD⊥底面ABCD,PD=AD.
(1)求证:平面PAC⊥平面PBD;
(2)求PC与平面PBD所成角的大小;
(3)在线段PB上找出一点E,使得PC⊥平面ADE,并求出此时二面角A-ED-B的大小. 欧阳海涛1年前1
欧阳海涛1年前1 -
 leileilesure 共回答了24个问题
leileilesure 共回答了24个问题 |采纳率91.7%解题思路:(1)由线面垂直得AC⊥PD,由正方形性质得AC⊥BD,由此能证明平面PAC⊥平面PBD.
(2)记AC与BD相交于O,连结PO,由已知条件得∠CPO就是PC与平面PBD所成的角,由此能求出PC与平面PBD所成的角为30°.
(3)分别以DA,DC,DP为x,y,z轴正方向建立空间直角坐标系,根据PC⊥平面ADE,确定E的位置,求出满足条件的平面ADE与平面BDE的法向量,代入向量夹角公式,即可求出此时二面角A-DE-B的大小.(1)证明:∵PD⊥底面ABCD,AC⊂底面ABCD,∴AC⊥PD,又∵底面ABCD为正方形,∴AC⊥BD,而PD与BD交于点D,∴AC⊥平面PBD,又AC⊂平面PAC,∴平面PAC⊥平面PBD.(2)记AC与BD相交于O,连结PO,由(1)知,AC⊥平面P...
点评:
本题考点: 二面角的平面角及求法.
考点点评: 本题考查的知识点是用空间向量求平面间的夹角,平面与平面垂直的判定,二面角的平面角及求法,熟练掌握空间中直线与平面垂直及平面与平面垂直的判定定理,二面角的求解一般是建立空间坐标系,将空间中直线与平面的垂直关系及二面角问题,转化为向量夹角问题.1年前查看全部
- (2008•武清区二模)已知f1(x)=sinx-cosx,若f2(x)=f1′(x),f3(x)=f2′(x),…,f
(2008•武清区二模)已知f1(x)=sinx-cosx,若f2(x)=f1′(x),f3(x)=f2′(x),…,fn(x)=fn-1′(x)(n∈N*且n>1),则f1([π/2])+f2([π/2])+…+f2008([π/2])等于______.
 辰熙881年前1
辰熙881年前1 -
 2109948 共回答了14个问题
2109948 共回答了14个问题 |采纳率92.9%解题思路:利用导数的运算法则,通过计算即可得出其周期性fn+4(x)=fn(x)进而即可得出答案.∵f1(x)=sinx-cosx,
∴f2(x)=f1′(x)=cosx+sinx,
f3(x)=(cosx+sinx)′=-sinx+cosx,
f4(x)=(-sinx+cosx)′=-cosx-sinx,
f5(x)=(-cosx-sinx)′=sinx-cosx,
依此类推,可得出fn(x)=fn+4(x),即函数fn(x)具备周期性,周期是4.
且f1(x)+f2(x)+f3(x)+f4(x)=0,
∵2008=502×4,
∴f1([π/2])+f2([π/2])+…+f2008([π/2])=502×0=0.
故答案为:0.点评:
本题考点: 导数的运算.
考点点评: 本题考查三角函数的导数、周期性、及观察归纳思想的运用,熟练掌握三角函数的求导法则,利用其中的函数周期性则解决本题的关键.1年前查看全部
- (2010•武清区二模)请结合下列实验室中的常用装置,回答有关问题.
(2010•武清区二模)请结合下列实验室中的常用装置,回答有关问题.
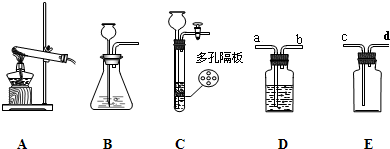
(1)若提供双氧水和二氧化锰制取氧气,应选用的发生装置是______(填“A”、“B”或“C”),该反应的化学方程式是2H2O2
2H2O+O2↑MnO2 .2H2O2;若提供氯酸钾和二氧化锰制取氧气,应选用的发生装置是______(填“A”、“B”或“C”),该反应的化学方程式是
2H2O+O2↑MnO2 .2KClO3
2KCl+3O2↑MnO2 .△ 2KClO3.
2KCl+3O2↑MnO2 .△
(2)若提供石灰石和稀盐酸制取二氧化碳,并且要求可以随时控制反应的进行,应选用的发生装置是______(填“A”、“B”或“C”);若要得到干燥的二氧化碳,还需选用D装置,该装置中应盛放______(填试剂名称). 女神巡礼菜yy1年前1
女神巡礼菜yy1年前1 -
 pennytaoran 共回答了23个问题
pennytaoran 共回答了23个问题 |采纳率69.6%解题思路:制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热,如果可以随时控制反应的进行,就需要C装置;二氧化碳可以用浓硫酸干燥.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.(1)如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;故答案为:B(选C不扣分);2H2O2
MnO2
.
2H2O+O2↑;A; 2KClO3
MnO2
.
△2KCl+3O2↑
(2)制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热,如果可以随时控制反应的进行,就需要C装置;二氧化碳可以用浓硫酸干燥,故答案为:C;浓硫酸点评:
本题考点: 常用气体的发生装置和收集装置与选取方法;气体的干燥(除水);实验室制取氧气的反应原理;二氧化碳的实验室制法;书写化学方程式、文字表达式、电离方程式.
考点点评: 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和气体的干燥等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.1年前查看全部
- (2014•武清区一模)从1、2、3、4这四个数中,任意取两个不同数字组成一个两位数,则这个两位数能被3整除的概率是 [
(2014•武清区一模)从1、2、3、4这四个数中,任意取两个不同数字组成一个两位数,则这个两位数能被3整除的概率是[1/3][1/3].
 zarch20561年前1
zarch20561年前1 -
 lalsw 共回答了21个问题
lalsw 共回答了21个问题 |采纳率95.2%解题思路:先列举出所有满足条件的两位数,然后找出能被3整除的两位数,即可得到能被3整除的概率.可以得到的所有两位数为:12,13,14,23,24,34,43,42,41,32,31,21,共有12个.
能被3整除的有4个,
所以两位数能被3整除的概率是[4/12]=[1/3].
故答案为[1/3].点评:
本题考点: 列表法与树状图法.
考点点评: 本题考查了利用列举法求概率的方法:先列举出所有可能的结果,然后找出某事件发生的结果,利用概念即可求出概率.1年前查看全部
- (2013•武清区一模)碘盐就是在食盐中加入一定量的碘酸钾(KIO3),回答下列问题.
(2013•武清区一模)碘盐就是在食盐中加入一定量的碘酸钾(KIO3),回答下列问题.
(1)碘酸钾的相对分子质量为214214;在碘酸钾中碘元素的质量分数是59.3%59.3%;
(2)42.842.8g 碘酸钾中含碘 25.4g. 西窗听雨雨无声1年前1
西窗听雨雨无声1年前1 -
 baozhuzjk 共回答了17个问题
baozhuzjk 共回答了17个问题 |采纳率94.1%解题思路:(1)根据碘酸钾的化学式KIO3,利用各元素的相对原子质量进行计算;(2)利用一定质量化合物中组成元素的质量=化合物的质量×化合物中该元素的质量分数,由元素碘的质量计算化合物碘酸钾的质量.(1)碘酸钾KIO3的相对分子质量=39+127+16×3=214;碘酸钾KIO3中碘元素的质量分数=
127
214×100%=59.3%;
(2)含碘 25.4g的碘酸钾的质量=25.4g÷
127
214×100%=42.8g
故答案为:(1)214;59.3%;
(2)42.8.点评:
本题考点: 相对分子质量的概念及其计算;元素的质量分数计算;化合物中某元素的质量计算.1年前查看全部
- (2013•武清区一模)碘盐就是在食盐中加入一定量的碘酸钾(KIO3),回答下列问题.
(2013•武清区一模)碘盐就是在食盐中加入一定量的碘酸钾(KIO3),回答下列问题.
(1)碘酸钾的相对分子质量为______;在碘酸钾中碘元素的质量分数是______;
(2)______g 碘酸钾中含碘 25.4g. 北鲲化鹏1年前1
北鲲化鹏1年前1 -
 指下飞舞 共回答了24个问题
指下飞舞 共回答了24个问题 |采纳率87.5%(1)碘酸钾KIO3的相对分子质量=39+127+16×3=214;碘酸钾KIO3中碘元素的质量分数=[127/214]×100%=59.3%;
(2)含碘 25.4g的碘酸钾的质量=25.4g÷[127/214]×100%=42.8g
故答案为:(1)214;59.3%;
(2)42.8.1年前查看全部
- (2010•武清区二模)今年春晚刘谦表演的近景魔术如真似幻,让人大饱眼福,陈老师也在化学晚会上表演如下魔术:用毛笔蘸取一
(2010•武清区二模)

今年春晚刘谦表演的近景魔术如真似幻,让人大饱眼福,陈老师也在化学晚会上表演如下魔术:用毛笔蘸取一种无色液体在一张白纸上书写了“中考必胜”四字,然后再喷上一种无色液体,白纸上立即出现了红色的“中考必胜”四字.你能揭底陈老师他先后所用的无色液体可能是______
A.石蕊溶液、NaOH溶液B.酚酞溶液、“雪碧”饮料
C.澄清石灰水、酚酞溶液D.Fe2(SO4)3溶液、NaOH溶液
碳酸钠俗称纯碱,其溶液能使无色酚酞变红,甲同学想探究是Na+还是CO32-的作用使酚酞试液变红,其设计方案如下:先往Na2CO3溶液中滴加酚酞试液后,再加入适量的Ca(OH)2溶液,观察红色是否消失.资料查询:纯碱是一种盐,其溶液pH>7,氯化钙溶液pH=7.
①老师肯定了乙同学的看法,你认为甲同学方案的不合理之处是______;
②丙同学要证明是CO32-的作用使酚酞试液变红.在下列物质中选用一种最好的试剂是(填序号)______;A.HCl B.NaOHC.CaCl2
③丁同学发现碳酸钠溶液碱性的强弱与溶液的浓度和温度有关,请你帮他完成实验探究.(只要求就一种影响碳酸钠溶液碱性强弱的因素设计实验方案.)
[实验方案]______. 小猴子尾巴1年前1
小猴子尾巴1年前1 -
 ttnn 共回答了15个问题
ttnn 共回答了15个问题 |采纳率93.3%解题思路:由题目的叙述可知两种溶液均为无色,由于A中有紫色石蕊,D中有蓝色的溶液,所以AD均错,雪碧显酸性遇酚酞不变色,故B错误,酚酞遇氢氧化钙溶液会变红,并且两种溶液均无无色.
①Ca(OH)2溶液中含有OH-,而OH-能够使酚酞变红;
②HCl本身也能使溶液变成无色;根据①知,NaOH中的OH-能够使酚酞变红;主要从碳酸钠溶液和氯化钙溶液的反应可以得出,碳酸根离子减少,使红色逐渐消失;
③因为是测定溶液在温度与浓度对PH的影响,因此应先创设温度相同不同浓度的条件,而后再设置温度不同浓度相同的条件进行对比实验.从题目信息可知是两种无色物质混合后呈现红色,石蕊溶液为紫色,Fe2(SO4)3溶液为棕黄色,故A选项和D选项错误;
“雪碧”饮料呈现酸性,遇酚酞不会变色.故B项错误;
澄清石灰水、酚酞溶液均为无色,且澄清石灰水能使酚酞溶液变红,故C选项正确
故答案是:C;
①甲同学所选的试剂Ca(OH)2溶液中含有能使无色酚酞试液变红的OH-.
故答案是:Ca(OH)2溶液与Na2CO3溶液反应后的产物中含有能使无色酚酞试液变红的NaOH,干扰实验;
②HCl本身也能使溶液变成无色,因此,加HCl根本无法证明“是CO32-的作用使酚酞试液变红”;
由①知,OH-能够使酚酞变红,因此,加入NaOH溶液无法证明“是CO32-的作用使酚酞试液变红”;
CaCl2溶液和Na2CO3溶液反应生成碳酸钙沉淀和NaCl,从而除去了CO32-,所以向酚酞试液中滴入Na2CO3溶液,振荡,酚酞试液变红,向变红后的溶液中再逐滴滴入过量的
CaCl2溶液,红色逐渐消失,说明是CO32-的作用使酚酞试液变红;
故答案是:C;
③创设对比实验的前提就是控制相同条件下不同的项目的比较.即定温状态或定溶液状态下进行.
故答案是:在相同的温度下,取两份质量相等浓度不同Na2CO3溶液,分别用pH试纸测出其pH值进行比较,多测几次再下结论.或取两份浓度相等的同种Na2CO3溶液,分别用pH试纸测出其在不同温度时pH值进行比较,多测几次再下结论.点评:
本题考点: 碳酸钠、碳酸氢钠与碳酸钙;酸碱指示剂及其性质.
考点点评: 此题属于易错题,在解答魔术表演的题目时,一定要排除有色溶液的选项.1年前查看全部
- (2010•武清区二模)神仙滩,那里的原始森林每天都在合成一定浓度的臭氧(O3),令那里的空气变得清新宜人.下列关于O3
(2010•武清区二模)神仙滩,那里的原始森林每天都在合成一定浓度的臭氧(O3),令那里的空气变得清新宜人.下列关于O3的说法中你认为错误的是( )
A.O3与O2化学性质完全相同
B.等质量的O3与O2所含的原子个数不同
C.O3和O2所组成的物质是混合物
D.构成O3和O2的原子具有相同的原子结构 天是和1年前1
天是和1年前1 -
 vv的vv 共回答了21个问题
vv的vv 共回答了21个问题 |采纳率95.2%解题思路:A、氧气和臭氧化学性质不完全相同;
B、两者的分子都是由氧原子构成的,因此等质量的O3与O2所含的原子个数相同;
C、臭氧和氧气的化学式不同,构成方式也不同,是属于两种不同的物质;
D、构成O3和O2的原子都是氧原子,具有相同的原子结构.A、氧气和臭氧化学性质不完全相同,故说法错误;
B、两者的分子都是由氧原子构成的,因此等质量的O3与O2所含的原子个数相同,故说法错误;
C、臭氧和氧气的化学式不同,构成方式也不同,是属于两种不同的物质,两者所组成的物质是混合物,故说法正确;
D、构成O3和O2的原子都是氧原子,具有相同的原子结构,故说法正确.
故选AB.点评:
本题考点: 氧元素组成的单质;纯净物和混合物的判别.
考点点评: 本题难度较小,根据题中信息结合所学化学知识进行分析即可.1年前查看全部
- (2014•武清区三模)若k>1,a>0,则k2a2+
(2014•武清区三模)若k>1,a>0,则k2a2+
A.1
B.2
C.2
D.4 lugdy1年前1
lugdy1年前1 -
 爱为你不变 共回答了20个问题
爱为你不变 共回答了20个问题 |采纳率85%∵k>1,a>0,由基本不等式可得
k2a2+
16
(k−1)a2≥2
k2a2•
16
(k−1)a2=
8k
k−1
当且仅当k2a2=
16
(k−1)a2,即a=
2
k
k−1时取等号,
又
8k
k−1=
8(k−1+1)
k−1=8(
k−1+
1
k−1)≥16
当且仅当
k−1=
1
k−1,即k=2时取等号,
∴当k=2即a=
2时,k2a2+
16
(k−1)a2取得最小值
故选:B.1年前查看全部
- (2014•武清区一模)人手指意外触到蜡烛火焰,引起屈肘反射.其反射弧示意图.
 (2014•武清区一模)人手指意外触到蜡烛火焰,引起屈肘反射.其反射弧示意图.
(2014•武清区一模)人手指意外触到蜡烛火焰,引起屈肘反射.其反射弧示意图.
(1)如图中神经元a产生的兴奋传到神经末梢时,引起突触前膜内______释放神经递质,该递质使神经元b兴奋.神经元b的神经冲动进一步引起神经元c兴奋,最终导致屈肌收缩.
(2)肌无力患者的神经细胞和肌肉细胞均正常,但无法完成自主运动功能,其原因最可能是______出现异常而引起的.
(3)图中M点兴奋时,此处神经纤维膜两侧的电位表现为______.若N点受刺激产生兴奋,则在神经元b上______(填“有”或“无”)膜电位的变化,其原因是______.
(4)手指意外触到火焰引起局部皮肤红肿,是因为皮肤毛细血管舒张和通透性增加,
______引起组织间隙液体积聚.若手指伤口感染,可引起体液中吞噬细胞核杀菌物质抵御病菌侵害,此过程属于______免疫. klp2281年前1
klp2281年前1 -
 斌爷 共回答了22个问题
斌爷 共回答了22个问题 |采纳率95.5%解题思路:1、当兴奋传到神经末梢时,引起突触前膜内突触小泡释放神经递质,该递质使神经元b兴奋.
2、肌无力患者的神经细胞和肌肉细胞均正常,但无法完成自主运动功能,其原因最可能是与神经递质结合的(特异性)受体出现异常而引起的.
3、兴奋部位神经纤维膜两侧的电位表现为内正外负,兴奋在突触处只能单向传递.
4、手指意外触到火焰引起局部皮肤红肿,是因为皮肤毛细血管舒张和通透性增加血浆中的蛋白质和液体渗出,引起组织间隙液体积聚.吞噬细胞和杀菌物质抵御病菌侵害,是人体的第二道防线,此过程属于非特异性免疫.(1)如图中神经元a产生的兴奋传到神经末梢时,引起突触前膜内突触小泡释放神经递质,该递质使神经元b兴奋.神经元b的神经冲动进一步引起神经元c兴奋,最终导致屈肌收缩.
(2)肌无力患者的神经细胞和肌肉细胞均正常,但无法完成自主运动功能,其原因最可能是与神经递质结合的(特异性)受体出现异常而引起的.
(3)M点在静息时,膜电位为内负外正,受刺激后变为内正外负.由图可知,手指皮肤下有感受器,a神经元为传入神经,b为神经中枢,c为传出神经,而兴奋在反射弧中各神经元间只能单向传递,所以N点受刺激产生兴奋只能在c神经元内传导,不能引起b神经元的兴奋.
(4)手指意外触到火焰引起局部皮肤红肿,因为皮肤毛细血管舒张和通透性增强,血浆中的蛋白质进入组织液,导致组织液渗透压升高,血浆中的水进入组织液,引起组织水肿.体液中吞噬细胞和杀菌物质抵御病菌为人体的第二道防线,属于非特异性免疫.
故答案为:
(1)突触小泡
(2)与神经递质结合的(特异性)受体
(3)内正外负无兴奋在神经元之间只能单向传递
(4)血浆中的蛋白质和液体渗出非特异性点评:
本题考点: 人体神经调节的结构基础和调节过程;神经冲动的产生和传导;人体免疫系统在维持稳态中的作用.
考点点评: 本 本题综合考查神经调节和免疫调节的基础知识,包括兴奋的产生、传导及传递,人体的三道防线(第二道防线);考查识图能力与获取信息能力.1年前查看全部
- (2013•武清区三模)某含N、O等元素的芳香族化合物A分子,相同状况下,其蒸气的密度为氢气密度的68.5倍.现以苯为原
(2013•武清区三模)某含N、O等元素的芳香族化合物A分子,相同状况下,其蒸气的密度为氢气密度的68.5倍.现以苯为原料合成A,并最终制得F(一种染料中间体),转化关系如下:(一些非主要产物已略去)
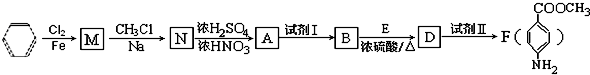
已知: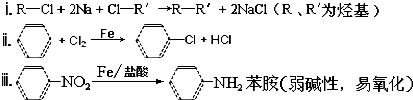
请回答问题:
(1)A的结构简式为______
(2)N→A的反应类型是______
(3)①上述转化中试剂Ⅰ和试剂Ⅱ分别是:试剂Ⅰ______;试剂Ⅱ______(选填字母).
a.KMnO4(H+)b.Fe/盐酸c.NaOH溶液
②若上述转化中物质A依次与试剂Ⅱ、试剂Ⅰ、化合物E(浓硫酸/△)作用,______(能
或否)得到F,原因是______
(4)用核磁共振氢谱可以证明化合物E中含有______种处不同化学环境的氢.
(5)写出同时符合下列要求的两种D的同分异构体的结构简式______
①属于芳香族化合物,分子中有两个互为对位的取代基,其中一个取代基是硝基
②分子中含有 结构
结构
(6)有一种D的同分异构体W,在酸性条件下水解后,可得到的一种能与FeCl3溶液发生显色反应的产物,写出W在酸性条件下水解的化学方程式______
(7)F的水解反应为: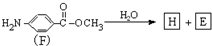
化合物H在一定条件下经缩聚反应可制得高分子纤维,广泛用于通讯、宇航等领域.
请写出该缩聚反应的化学方程式______. a9en1年前1
a9en1年前1 -
 dashano21986 共回答了17个问题
dashano21986 共回答了17个问题 |采纳率88.2%解题思路:苯与氯气发生取代反应生成M为氯苯(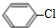 ),氯苯与一氯甲烷发生信息i的反应生成N为甲苯(
),氯苯与一氯甲烷发生信息i的反应生成N为甲苯( ),甲苯发生硝化反应生成A,A的密度为氢气密度的68.5倍,则N的相对分子质量为68.5×2=133,故A为一硝基取代,根据转化关系中F的结构可知,A为
),甲苯发生硝化反应生成A,A的密度为氢气密度的68.5倍,则N的相对分子质量为68.5×2=133,故A为一硝基取代,根据转化关系中F的结构可知,A为 ,A被酸性高锰酸钾氧化生成B为
,A被酸性高锰酸钾氧化生成B为 ,由F的结构可知,B与甲醇在浓硫酸作用下反应生成D为
,由F的结构可知,B与甲醇在浓硫酸作用下反应生成D为 ,故E为甲醇,D与HCl/Fe发生还原反应生成F,结合有机物的结构和性质解答该题.
,故E为甲醇,D与HCl/Fe发生还原反应生成F,结合有机物的结构和性质解答该题.
苯与氯气发生取代反应生成M为氯苯(
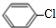 ),氯苯与一氯甲烷发生信息i的反应生成N为甲苯(
),氯苯与一氯甲烷发生信息i的反应生成N为甲苯(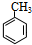 ),甲苯发生硝化反应生成A,A的密度为氢气密度的68.5倍,则N的相对分子质量为68.5×2=133,故A为一硝基取代,根据转化关系中F的结构可知,A为
),甲苯发生硝化反应生成A,A的密度为氢气密度的68.5倍,则N的相对分子质量为68.5×2=133,故A为一硝基取代,根据转化关系中F的结构可知,A为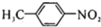 ,A被酸性高锰酸钾氧化生成B为
,A被酸性高锰酸钾氧化生成B为 ,由F的结构可知,B与甲醇在浓硫酸作用下反应生成D为
,由F的结构可知,B与甲醇在浓硫酸作用下反应生成D为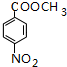 ,故E为甲醇,D与HCl/Fe发生还原反应生成F,
,故E为甲醇,D与HCl/Fe发生还原反应生成F,
(1)由以上分析可知A为 ,故答案为:
,故答案为: ;
;
(2)N为 ,在浓硫酸作用下与硝酸发生取代反应生成
,在浓硫酸作用下与硝酸发生取代反应生成 ,
,
故答案为:取代反应;
(3)①由题给信息结合以上分析可知试剂I和试剂Ⅱ分别是KMnO4(H+)、Fe/盐酸,
故答案为:a;b;
②若先还原后氧化,则还原生成的氨基又被氧化,所以不能得到F,
故答案为:否;若先还原后氧化,则还原生成的氨基又被氧化;
(4)E为CH3OH,含有两种不同的H原子,故答案为:2;
(5)D为 ,对应的属于芳香族化合物,分子中有两个互为对位的取代基,其中一个取代基是硝基;且分子中含有
,对应的属于芳香族化合物,分子中有两个互为对位的取代基,其中一个取代基是硝基;且分子中含有 结构的同分异构体有:
结构的同分异构体有: ,
,
故答案为: 任意2种;
任意2种;
(6)D的同分异构体w,在酸性条件下水解后,可得到一种能与FeCl3溶液发生显色反应的产物,说明分子中含有酚羟基,应为 ,水解的方程式为:
,水解的方程式为: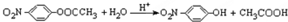 ,
,
故答案为: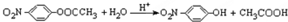 ;
;
(7)F的水解产物为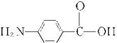 和CH3OH,化合物H在一定条件下经缩聚反应可制得高分子纤维,广泛用于通讯、导弹、宇航等领域,则H为
和CH3OH,化合物H在一定条件下经缩聚反应可制得高分子纤维,广泛用于通讯、导弹、宇航等领域,则H为 ,可发生缩聚反应,方程式为:
,可发生缩聚反应,方程式为: ,
,
故答案为: .
.点评:
本题考点: 有机物的推断;有机物的合成.
考点点评: 本题考查有机物的推断和合成,题目难度较大,本题注意把握题给信息,为解答该题的关键,注意有机物官能团的性质和变化,较好的考查学生的自学能力、逻辑推理能力,是热点题型.1年前查看全部
- (2010•武清区二模)A、B、C、D都是九年级化学中的物质,它们存在右下图所示的关系(该反应无条件或反应条件未注明).
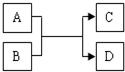 (2010•武清区二模)A、B、C、D都是九年级化学中的物质,它们存在右下图所示的关系(该反应无条件或反应条件未注明).
(2010•武清区二模)A、B、C、D都是九年级化学中的物质,它们存在右下图所示的关系(该反应无条件或反应条件未注明).
(1)如图代表的反应不可能属于基本反应类型中的______和分解反应;
(2)若A为蓝色溶液,C为Cu(OH)2,则B溶液的pH______7
(填“<”、“>”或“=”);
(3)若A为常见金属,C的溶液呈浅绿色,则D物质可能是______;
(4)若D是水,请写出一个对应的化学反应方程式:______;
(5)若C为CuSO4,该反应______中和反应(填写序号).
①一定是;②可能是;③一定不是. 美味冰激凌1年前1
美味冰激凌1年前1 -
 我就是葫芦娃3 共回答了16个问题
我就是葫芦娃3 共回答了16个问题 |采纳率81.3%解题思路:(1)依据四种基本反应类型的反应特点,对转化关系所代表的反应进行反应类型判断;
(2)由反应物和生成物的物质类别,推断转化关系的反应规律,进一步推断另一反应物溶液的酸碱性.由A为蓝色溶液可知A为可溶性铜盐,反应后生成的Cu(OH)2属于碱,可知此反应为盐与碱生成新盐和新碱的复分解反应,则反应物B应为可溶性碱;
(3)C的溶液呈浅绿色,则C为亚铁盐;A为常见金属,可猜测金属A可能为铁;推测反应为:铁与物质B生成亚铁盐和物质D,此反应存在为置换反应的可能;
(4)A+B→C+D,其生成物之一为水,符合此反应特点的反应有:氢气还原金属氧化物如氧化铜,酸碱中和,金属氧化物与酸的反应,非金属氧化物与碱溶液的反应;
(5)A+B→C+D,其生成物之一为硫酸铜属于盐类物质,即能生成盐的反应.(1)A+B→C+D,两种物质发生反应生成两种物质,此类型的反应不可能是“一变多”的分解反应,也不可能是“多变一”的化合反应;
故答:化合反应;
(2)反应物B应为可溶性碱,其溶液的pH>7;
故答:>;
(3)铁的性质表明,有铁参加的置换反应有:铁可与酸生成亚铁盐和氢气,铁与盐溶液反应生成亚铁盐和金属;所以物质D可能为氢气或金属单质;
故答:H2或金属单质;
(4)在下列反应中任意选取一类反应,都符合题意:氢气还原金属氧化物如氧化铜,酸碱中和,金属氧化物与酸的反应,非金属氧化物与碱溶液的反应.此问具有开放性;
故答:H2+CuO≜Cu+H2O或CuO+2HCl═CuCl2+H2O等等(其它合理答案也可)
(5)此时反应的特点为:A+B→盐+另一种物质,中和反应生成盐和水,但生成盐的反应并不是只有中和反应,比如碱和盐反应生成新盐新碱,等等
故答:②.点评:
本题考点: 物质的鉴别、推断;化合反应及其应用.
考点点评: 根据反应的特点,分析满足条件的反应.本题开放度较大,分析时不必追求面面俱到穷尽所有结果.1年前查看全部
- (2013•武清区一模)(1)水烧开时,壶嘴有大量“白气”产生,仔细观察,可以发现在最靠近壶嘴的地方反而不出现“白气”,
 (2013•武清区一模)(1)水烧开时,壶嘴有大量“白气”产生,仔细观察,可以发现在最靠近壶嘴的地方反而不出现“白气”,为什么呢?
(2013•武清区一模)(1)水烧开时,壶嘴有大量“白气”产生,仔细观察,可以发现在最靠近壶嘴的地方反而不出现“白气”,为什么呢?
(2)小明同学将如图所示的玻璃管装置接到水流稳定的自来水管上,当水在玻璃管中流动时,可看到两个竖直管中液面的高度并不相同.从图中可以看出在A、B两处管的粗细不同,因而A处流速小,B处流速大.可见流体的压强与流速之间有着一定的关系.如图所示的实验,可以得出流体的压强与流速之间有什么关系? 快乐王子1999991年前1
快乐王子1999991年前1 -
 匿名的天使 共回答了8个问题
匿名的天使 共回答了8个问题 |采纳率100%解题思路:(1)物质由气态变为液态叫液化,液化现象一般发生在温度低的环境中,或发生在降温时.(2)液体和气体压强中,流速快的地方压强小.答:(1)水烧开时,壶嘴有大量“白气”,这“白气”实质上是壶嘴喷出的水蒸气遇冷发生了液化现象,形成了小液滴.高温的水蒸气在遇冷时才发生液化现象,而在靠近壶嘴的地方,温度高,水蒸气不会液化,仍是无色的水蒸气,故我们什么也看不见.水蒸气离开壶嘴一段距离以后,由于遇冷而发生液化;形成“白气”.
(2)图中所示的实验,可以得出流体的压强与流速之间的关系为:流速越大,压强越小.点评:
本题考点: 液化及液化现象;流体压强与流速的关系.
考点点评: 明确液化时温度的变化情况,理解流体压强与流速的关系;是解答此题的关键.1年前查看全部
- (2013•武清区三模)图中晨昏线k和纬线M相切于0点,其坐标为(700S,1200大).完成1-2题.
 (2013•武清区三模)图中晨昏线k和纬线M相切于0点,其坐标为(700S,1200大).完成1-2题.
(2013•武清区三模)图中晨昏线k和纬线M相切于0点,其坐标为(700S,1200大).完成1-2题.
l.若此时8rrN处于极昼状态,其正午太阳高度为( )
我.若0点此时夜长最短,则北京的地方时为:( )
A.12时
B.0时
C.11时44分
D.23时44分 xgdyyh3783664711年前1
xgdyyh3783664711年前1 -
 liz214 共回答了11个问题
liz214 共回答了11个问题 |采纳率100%解题思路:图中晨昏线L和纬线M相切于0点,其坐标为(70°S,120°E),若0点此时夜长最短,70°S及其以南地区出现极昼,0点地方时为0时,根据“东早西晚、东加西减”求算北京的地方时.图地晨昏线L和纬线M相切于d点,其坐标为(7d°S,1xd°E),若d点此时夜长最短,7d°S及其以南地区出现极昼,d点地方时为d时,d点的经度为1xd°E,北京的经度为116°E,根据“东早西晚、东加西减”,北京的地方时为x3时44分.
故选:D.点评:
本题考点: 地方时与区时的区别及计算.
考点点评: 本题难度适中,属于知识性试题,解题的关键是掌握太阳光照图的判读和地方时的计算.1年前查看全部
- (2014•武清区一模)下列图形中,不是中心对称图形的是( )
(2014•武清区一模)下列图形中,不是中心对称图形的是( )
A.
B.
C.
D.
 告别什么呢1年前1
告别什么呢1年前1 -
 明事999大爷 共回答了23个问题
明事999大爷 共回答了23个问题 |采纳率82.6%解题思路:根据中心对称图形的概念求解.A、是中心对称图形.故本选项错误;
B、是中心对称图形.故本选项错误;
C、不是中心对称图形.故本选项正确;
D、是中心对称图形.故本选项错误.
故选C.点评:
本题考点: 中心对称图形.
考点点评: 本题考查了中心对称图形的概念:中心对称图形关键要寻找对称中心,旋转180度后与原图重合.1年前查看全部
- (2013•武清区一模)某学习小组的同学在做碳酸钠溶液和澄清石灰水反应的实验后,将反应后的浑浊液进行过滤,得到澄清的滤液
(2013•武清区一模)某学习小组的同学在做碳酸钠溶液和澄清石灰水反应的实验后,将反应后的浑浊液进行过滤,得到澄清的滤液,对于滤液的组成同学们做出如下猜想:
(1)【猜想与假设】大家一致认为滤液中一定有氢氧化钠,生成氢氧化钠的化学方程式是______;小明猜想还可能有氢氧化钙,小丽猜想还可能有氢氧化钙和碳酸钠,你还能做出的猜想是______.
(2)【活动与探究】请你设计一个实验方案验证你的猜想.
(3)现有一样品,经分析含氢氧化钠、碳酸钠和水三种物质,向该样品中加入溶质质量分数为9.8%的稀硫酸100g,恰好完全反应得到中性溶液.蒸干该溶液得到______g固体.实验步骤 实验现象 实验结论  newman451年前1
newman451年前1 -
 lliioonn12345678 共回答了16个问题
lliioonn12345678 共回答了16个问题 |采纳率81.3%解题思路:根据已有的知识进行分数,碳酸钠与氢氧化钙反应时,可能存在物质过量的情况,要设计实验证明物质的存在,可以依据物质的性质进行,根据反应的化学方程式即可计算出生成的硫酸钠的质量,据此解答即可.(1)碳酸钠能与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,碳酸钠和氢氧化钙反应时,可能存在碳酸钠过量,也可能存在氢氧化钙过滤,故填:Na2CO3+Ca(OH)2=2NaOH+CaCO3↓,可能有碳酸钠;
(2)碳酸钠能与盐酸反应生成二氧化碳气体,可以向反应后的滤液中加入过量的稀盐酸,观察到气泡产生,说明猜想成立,故填:
实验步骤 实验现象 实验结论
取样于试管中,滴入足量稀盐酸 有气体产生 猜想成立(3)2NaOH+H2SO4=Na2SO4+2H2O,Na2CO3+H2SO4=Na2SO4+H2O+CO2↑,根据反应的化学方程式可以看出,反应后所得的溶液中溶质是硫酸钠,设生成硫酸钠的质量为x
H2SO4------Na2SO4
98 142
100g×9.8% x
[98/100g×9.8%=
142
x] x=14.2g
故填:14.2.点评:
本题考点: 实验探究物质的组成成分以及含量;盐的化学性质.
考点点评: 本题考查了反应后溶液中物质成分的推断,完成此题,可以依据物质的性质进行,进行化学方程式计算时,可以依据硫酸与硫酸钠的质量比为定值进行.1年前查看全部
- (2012•武清区二模)如图表示治理汽车尾气所涉及反应的微观过程.下列说法正确的是( )
(2012•武清区二模)如图表示治理汽车尾气所涉及反应的微观过程.下列说法正确的是( )
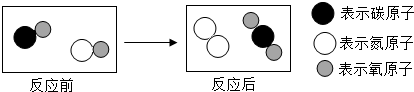
A.图中有两种单质和两种氧化物
B.生成单质与化合物的质量比为7:22
C.反应物和生成物均含有毒气体
D.反应物的分子个数比为1:1 rwtb1年前1
rwtb1年前1 -
 贝贝35 共回答了22个问题
贝贝35 共回答了22个问题 |采纳率100%解题思路:根据反应的微观过程,分析反应物、生成物写出反应的方程,根据方程式分析判断有关的问题.由反应的微观过程可知,反应物是一氧化氮和一氧化碳,生成物是氮气和二氧化氮,反应的化学方程式式:2CO+2NO═N2+2CO2;
A、根据该反应的化学方程式2CO+2NO═N2+2CO2可知,氮气由同种元素组成,属于单质,一氧化氮、一氧化碳、二氧化碳由两种元素组成,其中一种元素是氧元素,属于氧化素属于氧化物.故A不正确;
B、根据该反应的化学方程式2CO+2NO═N2+2CO2可知,单质N2与化合物CO2的质量比=28:(2×44)=7:22.故B正确;
C、该反应的生成物为N2和CO2,两种气体均不是有毒气体.故C不正确;
D、根据该反应的化学方程式2CO+2NO═N2+2CO2可知,反应物的分子个数比为1:1.故D正确.
故选BD.点评:
本题考点: 微粒观点及模型图的应用.
考点点评: 分子由原子构成,同种原子构成的分子为单质分子,不同种原子构成的分子为化合物分子.1年前查看全部
- (2014•武清区三模)如图所示,上、下表面平行的玻璃砖置于空气中,一束复色光斜射到上表面,穿过玻璃后从下表面射出,分成
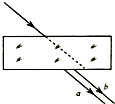 (2014•武清区三模)如图所示,上、下表面平行的玻璃砖置于空气中,一束复色光斜射到上表面,穿过玻璃后从下表面射出,分成a、b两束单色光.下列说法中正确的是( )
(2014•武清区三模)如图所示,上、下表面平行的玻璃砖置于空气中,一束复色光斜射到上表面,穿过玻璃后从下表面射出,分成a、b两束单色光.下列说法中正确的是( )
A.a、b两束单色光相互平行
B.a光在玻璃中的传播速度大于b光
C.在玻璃中a光全反射的临界角小于b光
D.用同一双缝干涉装置进行实验a光的条纹间距小于b光 Sunnyxyyun1年前1
Sunnyxyyun1年前1 -
 kevin-zhu 共回答了23个问题
kevin-zhu 共回答了23个问题 |采纳率87%解题思路:一束复色光从空气斜射到厚平板玻璃(上、下表面平行)的上表面,穿过玻璃后从下表面射出,变为a、b两束平行单色光,从而可确定折射率大小.由n=[c/v]可得两束光在玻璃中的速度与折射率成反比;由临界角公式sinC=[1/n],分析临界角的大小.由折射率的大小,确定波长的大小,即可分析干涉条纹间距的大小.A、由几何知识可知光射到玻璃砖下表面时的入射角等于上表面的折射角,由光路可逆原理得知光射出玻璃砖下表面时的折射角等于上表面的入射角,由几何知识可知出射光线与入射光线平行,所以a、b两束单色光相互平行.故A正确.
B、由图看出,光线通过平板玻璃后,a光的侧移大于b光的侧移,说明玻璃对a光的折射率大于b光的折射率.由n=[c/v]可知a光在玻璃中的传播速度小于b光,故B错误.
C、由sinC=[1/n],知折射率越大,临界角越小,所以在玻璃中a光的全反射临界角小于b光.故C正确.
D、玻璃对a光的折射率大于b光的折射率,则a光的波长小于b光的波长,用同一双缝干涉装置做干涉实验时,干涉条纹间距与波长成正比,则a光的干涉条纹间距比b光的小.故D正确.
故选:ACD.点评:
本题考点: 光的折射定律.
考点点评: 此题关键要理解玻璃砖的光学特性,知道光线通过平板玻璃后,其侧移与折射率有关,同样条件下折射率越大,侧移越大.1年前查看全部
- (2011•武清区一模)已知某无色溶液中含有盐酸,则该溶液中还可能含有( )
(2011•武清区一模)已知某无色溶液中含有盐酸,则该溶液中还可能含有( )
A.纯碱
B.烧碱
C.氯化锌
D.氯化铜 便再没见你笑过1年前1
便再没见你笑过1年前1 -
 adam20051003 共回答了18个问题
adam20051003 共回答了18个问题 |采纳率77.8%解题思路:A、碳酸根离子会与酸反应生成二氧化碳和水,
B、氢氧根离子会和氢离子发生中和反应生成水,
C、氯化锌是盐,和盐酸不会反应,
D、铜离子显蓝色,A、纯碱中含有碳酸根离子,会与氢离子反应生成二氧化碳和水,所以不能存在于盐酸中,故A错误,
B、烧碱中含有氢氧根离子,会与氢离子发生中和反应生成水,所以不能存在于盐酸中,故B错误,
C、氯化锌和盐酸不会反应,因为它们之间的反应不满足复分解反应的条件,故C正确,
D、氯化铜中的铜离子显蓝色,溶液是无色的,故D错误,
故选:C.点评:
本题考点: 离子或物质的共存问题;酸的化学性质.
考点点评: 本题主要考查了离子之间的共存问题,以及初中阶段的带色离子,要加强记忆.1年前查看全部
- (2012•武清区一模)曲线y=x2与直线y=6x围成的封闭图形的面积为______.
 matianyu1年前1
matianyu1年前1 -
 judy1001 共回答了17个问题
judy1001 共回答了17个问题 |采纳率94.1%解题思路:先联立方程,组成方程组,求得交点坐标,可得被积区间,再用定积分表示出曲线y=x2与直线y=6x围成的封闭图形的面积,即可求得结论.由
y=x2
y=6x,可得
x=0
y=0或
x=6
y=36
∴曲线y=x2与直线y=6x围成的封闭图形的面积为
∫60(6x−x2)dx=(3x2−
1
3x3)
|60=36
故答案为:36点评:
本题考点: 定积分在求面积中的应用.
考点点评: 本题考查利用定积分求面积,解题的关键是确定被积区间及被积函数.1年前查看全部
- (2014•武清区三模)图中一组平行实线可能是电场线也可能是等势面,一个电子只在电场力作用下从a点运动到b点的轨迹如图中
 (2014•武清区三模)图中一组平行实线可能是电场线也可能是等势面,一个电子只在电场力作用下从a点运动到b点的轨迹如图中虚线所示,下列说法中正确的是( )
(2014•武清区三模)图中一组平行实线可能是电场线也可能是等势面,一个电子只在电场力作用下从a点运动到b点的轨迹如图中虚线所示,下列说法中正确的是( )
A.如果实线是电场线,则a点的电势比b点的电势高
B.如果实线是等势面,则a点的电势比b点的电势低
C.如果实线是电场线,则电子在a点的电势能比在b点的电势能大
D.如果实线是等势面,则电子在a点的电势能比在b点的电势能大 白糖茶叶1年前1
白糖茶叶1年前1 -
 这又是我的 共回答了25个问题
这又是我的 共回答了25个问题 |采纳率80%解题思路:根据曲线运动的条件判断出电场力的方向,可以判断电场力做功的正负情况,而电场力做功等于电势能的减小量.A、如果实线是电场线,根据曲线运动的条件,电场力水平向右,则场强向左,则a点的电势比b点的电势低;故A错误;
B、如果实线是等势面,电场线与等势面垂直,根据曲线运动的条件,电场力竖直向下,电场线向上,故a点的电势比b点的电势高,故B错误;
C、如果实线是电场线,根据曲线运动的条件,电场力水平向右,电场力做正功,电势能降低,即电子在a点的电势能比在b点的电势能大,故C正确;
D、如果实线是等势面,电场线与等势面垂直,根据曲线运动的条件,电场力竖直向下,故电场力做负功,电势能增加,即电子在a点的电势能比在b点的电势能小,故D错误;
故选:C.点评:
本题考点: 电势;电势能.
考点点评: 根据轨迹的弯曲方向,根据合力指向轨迹的内侧,可判断质点的合力方向.根据电场力做功的正负判断电势能的变化,基础问题.1年前查看全部
- (2014•武清区三模)已知数列{an}满足,anan+1=n(n-1)(an+1-an),且a1=0,a2=1.
(2014•武清区三模)已知数列{an}满足,anan+1=n(n-1)(an+1-an),且a1=0,a2=1.
(1)求证:数列{an}是等差数列;
(2)设bn=2 an-34,求数列{|bn|}的前n项和Sn. chenfeng2531年前1
chenfeng2531年前1 -
 jacob110 共回答了19个问题
jacob110 共回答了19个问题 |采纳率89.5%解题思路:(1)a1=0,a2=1,依题意只需证明∀n∈N*,只需证an2+an−n(n−1)=0,即只需证an=n-1或an=-n,由此利用分析法能证明数列{an}是等差数列.
(2)由an=n-1,知bn=2n−1−34,由此能求出数列{|bn|}的前n项和Sn.(1)证明:∵a1=0,a2=1,依题意只需证明∀n∈N*,
an+1-an=a2-a1=1,…(1分)
∵anan+1=n(n-1)(an+1-an),
∴an+1=
n(n−1)an
n(n−1)−an,n>1,
∴只需证an+1−an=
an2
n(n−1)−an=1,n>1.…(3分)
即只需证an2=n(n−1)−an,即只需证an2+an−n(n−1)=0,
即只需证an=n-1或an=-n,…(5分)
∵an=-n不符合a2=1,∴只需证an=n-1.
数列{n-1}是等差数列,且满足a1=0,a2=1,以上各步都可逆
∴数列{an}是等差数列 …(7分)
(2)由(1)可知an=n-1,∴bn=2n−1−34,…(8分)
设数列{bn}的前n项和为Tn,
数列{2n-1}是首项为1,公比为2的等比数列,数列{34}是常数列
∴Tn=b1+b2+…+bn=
1−2n
1−2−34n=2n-34n-1,…(9分)
令bn=2n−1−34>0,∴n>6,∵数列{bn}是递增数列
∴数列{bn}前6项为负,以后各项为正 …(10分)
∴当n≤6时,Sn=-Tn=-2n+34n+1,…(11分)
当n>6时,Sn=Tn-2T6=2n-34n-283.…(12分)
∴Sn=
−2n+34n+1,n≤6
2n−34n−283,n>6.…(13分)点评:
本题考点: 数列的求和;等差关系的确定.
考点点评: 本题考查等差数列的证明,考查数列的前n项和的求法,解题时要认真审题,注意分类讨论思想的合理运用.1年前查看全部
- (2013•武清区一模)碘盐就是在食盐中加入一定量的碘酸钾(KIO3),回答下列问题.
(2013•武清区一模)碘盐就是在食盐中加入一定量的碘酸钾(KIO3),回答下列问题.
(1)碘酸钾的相对分子质量为214214;在碘酸钾中碘元素的质量分数是59.3%59.3%;
(2)42.842.8g 碘酸钾中含碘 25.4g. 思绪放飞1年前1
思绪放飞1年前1 -
 studentff1973 共回答了24个问题
studentff1973 共回答了24个问题 |采纳率83.3%(1)碘酸钾KIO3的相对分子质量=39+127+16×3=214;碘酸钾KIO3中碘元素的质量分数=
127
214×100%=59.3%;
(2)含碘 25.4g的碘酸钾的质量=25.4g÷
127
214×100%=42.8g
故答案为:(1)214;59.3%;
(2)42.8.1年前查看全部
- (2012•武清区一模)某校生物兴趣小组在玻璃温室里进行植物栽培实验,为此他们对室内空气中的CO2含量进行了24小时测定
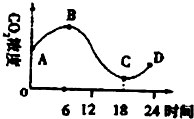 (2012•武清区一模)某校生物兴趣小组在玻璃温室里进行植物栽培实验,为此他们对室内空气中的CO2含量进行了24小时测定,并根据数据绘制出了如图曲线.以下说法正确的是( )
(2012•武清区一模)某校生物兴趣小组在玻璃温室里进行植物栽培实验,为此他们对室内空气中的CO2含量进行了24小时测定,并根据数据绘制出了如图曲线.以下说法正确的是( )
A.该植物进行光台合作用的时间区段是BC
B.B、C点表示光合速率等于呼吸速率
C.在AB区段,产生ATP的场所是细胞质基质、线粒体
D.CD段CO2浓度的持续变化主要受光照强度的影响 choicerey1年前1
choicerey1年前1 -
 跳蹦跳 共回答了8个问题
跳蹦跳 共回答了8个问题 |采纳率87.5%解题思路:图形解读:①AB段玻璃温室内的二氧化碳浓度增加,说明呼吸作用强度大于呼吸作用强度;②B点,二氧化碳的浓度既不增加也不减少,说明光合作用强度等于呼吸作用强度;③BC段二氧化碳的浓度降低,说明光合作用强度大于呼吸作用强度;④CD段二氧化碳浓度增加,说明呼吸作用强度大于呼吸作用强度;⑤C点,二氧化碳的浓度既不增加也不减少,说明光合作用强度等于呼吸作用强度.A、由于在B、C点上,二氧化碳的浓度既不增加也不减少,说明光合作用强度等于呼吸作用强度,说明在B点之前和C点之后,也进行光合作用,故A错误;
B、在B、C点上,二氧化碳的浓度既不增加也不减少,说明光合作用强度等于呼吸作用强度,故B正确;
C、在AB区段的靠近B点时,进行光合作用,所以植物产生ATP的场所是细胞质基质、线粒体和叶绿体,故C错误;
D、CD段在夜晚,由于温度下降,呼吸作用速率就下降,所以CO2浓度的变化主要受温度的影响,故D错误.
故选B.点评:
本题考点: 影响光合作用速率的环境因素;细胞呼吸的过程和意义.
考点点评: 本题考查光合作用与细胞呼吸,意在考查学生用文字、图表以及数学方式等多种表达形式准确的描述生物学方面的内容的能力.1年前查看全部
- (2010•武清区一模)将杨辉三角中的奇数换成1,偶数换成0,便可以得到如下的“0-1三角”.在“0-1三角”中,从第1
 (2010•武清区一模)将杨辉三角中的奇数换成1,偶数换成0,便可以得到如下的“0-1三角”.在“0-1三角”中,从第1行起,设第n(n∈N*)次出现全行为1时,1的个数为an,则a3等于( )
(2010•武清区一模)将杨辉三角中的奇数换成1,偶数换成0,便可以得到如下的“0-1三角”.在“0-1三角”中,从第1行起,设第n(n∈N*)次出现全行为1时,1的个数为an,则a3等于( )
A.26
B.27
C.7
D.8 萝驼铃1年前1
萝驼铃1年前1 -
 pengpen_999 共回答了23个问题
pengpen_999 共回答了23个问题 |采纳率91.3%解题思路:先由条件找到全行的数都为1的前几项,利用前几项的规律来求出全行的数都为1的行的通项,从而求出第3次出现全行为1的是第几行,从而求出a3的值.由题意,将杨辉三角中的奇数换成1,偶数换成0,可得第1次全行的数都为1的是第1行,第2次全行的数都为1的是第3行,…,
由此可知全奇数的行出现在2n-1的行数,即第n次全行的数都为1的是第2n-1行.
∴第3次出现全行为1的是第7行,第7行有8个1,故a3=8
故选D.点评:
本题考点: 进行简单的合情推理.
考点点评: 本题是借助于杨辉三角求数列的通项公式,本题的关键点是熟悉杨辉三角以及常见数列的通项公式,属于基础题.1年前查看全部
- (2007•武清区模拟)如图所示,一边长为h的正方形线圈A,其电流I大小方向均固定不变,用两条长度恒为h的细绳静止悬挂于
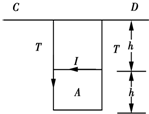 (2007•武清区模拟)如图所示,一边长为h的正方形线圈A,其电流I大小方向均固定不变,用两条长度恒为h的细绳静止悬挂于水平长直导线CD的正下方.当导线CD中无电流时,两细绳中张力均为T,当通过CD的电流为i1时,两细绳中张力均降为aT(0<a<1=,而当CD上的电流为i2时,细绳中张力恰好为零.已知长直通电导线的磁场的磁感应强度B与电流强度成正比,与场点到导线的距离r成反比(即B=ki/r,k为常数).由此可知,CD中的电流方向和电流之比i1/i2分别为( )
(2007•武清区模拟)如图所示,一边长为h的正方形线圈A,其电流I大小方向均固定不变,用两条长度恒为h的细绳静止悬挂于水平长直导线CD的正下方.当导线CD中无电流时,两细绳中张力均为T,当通过CD的电流为i1时,两细绳中张力均降为aT(0<a<1=,而当CD上的电流为i2时,细绳中张力恰好为零.已知长直通电导线的磁场的磁感应强度B与电流强度成正比,与场点到导线的距离r成反比(即B=ki/r,k为常数).由此可知,CD中的电流方向和电流之比i1/i2分别为( )
A.向左1+a
B.向右1+a
C.向左1-a
D.向右1-a sanny0091年前1
sanny0091年前1 -
 冰飞焰舞 共回答了20个问题
冰飞焰舞 共回答了20个问题 |采纳率85%解题思路:根据对线圈受力分析,依据受力平衡,则可分别来确定电流大小关系,从而即可求解.由题目中给出的信息可知,当CD中通电流时,细绳中的张力减小,故正方形线圈受到的安培力的合力一定向上.当通过CD的电流为i时,对线圈进行受力分析,受到重力、向上和向下的安培力、细绳的拉力,故G
k
2hilh=2aT+
k
hilh①;
当通过CD的电流为i′时,对线圈进行受力分析,受到重力、向上和向下的安培力、细绳的拉力,故G+
k
2hi′lh=
k
hi′lh②;
当通过CD中无电流时,对线圈进行受力分析,受到重力和细绳的张力,故G=2T③.
解①②③可得
i
i′=1−a.
故选C点评:
本题考点: 安培力;力的合成与分解的运用;通电直导线和通电线圈周围磁场的方向.
考点点评: 本题以信息题的形式出现考查了电磁感应现象、安培力的计算、左手定则、受力分析等知识点.1年前查看全部
- (2014•武清区三模)如图所示,质量M=0.8kg、长L=0.9m、高h=0.45m的矩形滑块置于水平地面上,滑块与地
 (2014•武清区三模)如图所示,质量M=0.8kg、长L=0.9m、高h=0.45m的矩形滑块置于水平地面上,滑块与地面间动摩擦因数μ=0.4;滑块上表面光滑,其右端放置一质量m=0.2kg的小球.现给滑块一水平向右的瞬时冲量I=4N•s,经过一段时间后小球落地.求小球落地时距滑块左端的水平距离.
(2014•武清区三模)如图所示,质量M=0.8kg、长L=0.9m、高h=0.45m的矩形滑块置于水平地面上,滑块与地面间动摩擦因数μ=0.4;滑块上表面光滑,其右端放置一质量m=0.2kg的小球.现给滑块一水平向右的瞬时冲量I=4N•s,经过一段时间后小球落地.求小球落地时距滑块左端的水平距离.  beyondzhu1年前1
beyondzhu1年前1 -
 月夜风飞 共回答了24个问题
月夜风飞 共回答了24个问题 |采纳率87.5%对滑块根据动能定理有:I=Mv0
可得滑块获得的初速度为:v0=
I
M=
4
0.8m/s=5m/s
小球未离开滑块之前滑块受到的摩擦力为:μ(M+m)g=Ma
解得加速度的大小:a=
μ(m+M)g
M=
0.4×(0.2+0.8)×10
0.8m/s2=5m/s2
因为滑块做匀减速运动,由速度位移关系有:
v2−
v20=−2aL
可得小球离开滑块时,滑块的速度为:v=
v20−2aL=
52−2×5×0.9m/s=4m/s
小球离开滑块以后做自由落体运动有:
h=
1
2gt2
得小球运动时间为:t=
2h
g=
2×0.45
10s=0.3s
滑块的加速度为:a'=-μg=-0.4×10m/s2=4m/s2
根据运动学公式为:x=vt+
1
2a′t2
可得:x=4×0.3+
1
2×4×0.32m=1.02m
答:小球落地时距滑块左端的水平距离为1.02m.1年前查看全部
- (2013•武清区一模)完成下列化学方程式
(2013•武清区一模)完成下列化学方程式
(1)实验室加热高锰酸钾制氧气2KMnO4
K2MnO4+MnO2+O2↑△ .2KMnO4
K2MnO4+MnO2+O2↑△ .
(2)碳还原氧化铜C+2CuO
2Cu+CO2↑高温 .C+2CuO
2Cu+CO2↑高温 .
(3)甲烷燃烧CH4+2O2
CO2+2H2O点燃 .CH4+2O2
CO2+2H2O点燃 .
(4)用盐酸除铁锈______. 网通小灵通1年前1
网通小灵通1年前1 -
 jiangxueli 共回答了28个问题
jiangxueli 共回答了28个问题 |采纳率89.3%解题思路:根据方程式的书写步骤:一写二配三注明四等号来回答本题.(1)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为 2KMnO4
△
.
K2MnO4+MnO2+O2↑
(2)碳在高温条件下还原氧化铜生成铜和二氧化碳,化学方程式为 C+2CuO
高温
.
2Cu+CO2↑
(3)甲烷燃烧生成二氧化碳和水,化学方程式为 CH4+2O2
点燃
.
CO2+2H2O
(4)铁锈的主要成分是氧化铁,氧化铁与盐酸反应生成氯化铁和水,化学方程式为 Fe2O3+6HCl═2FeCl3+3H2O
故答案为:(1)2KMnO4
△
.
K2MnO4+MnO2+O2↑
(2)C+2CuO
高温
.
2Cu+CO2↑
(3)CH4+2O2
点燃
.
CO2+2H2O
(4)Fe2O3+6HCl═2FeCl3+3H2O点评:
本题考点: 书写化学方程式、文字表达式、电离方程式.
考点点评: 通过回答本题进一步巩固了方程式的书写步骤,要灵活运用方程式的书写步骤去写方程式1年前查看全部
- (2012•武清区一模)某大学共有A、B、C三个学生食堂,一个宿舍共有四名学生,在一段时间内,他们每天中午都在学生食堂用
(2012•武清区一模)某大学共有A、B、C三个学生食堂,一个宿舍共有四名学生,在一段时间内,他们每天中午都在学生食堂用餐,且每个学生到这三个食堂中的任一食堂用餐的可能性都相等.用X表示这个宿舍每天中午在A食堂用餐的人数.根据这一时间段该宿舍学生的就餐情况解决下列问题:
(1)求每天中午每个学生食堂中至少有这个宿舍一名学生用餐的概率;
(2)求随机变量X的数学期望和方差. 扎萨格dd天堂1年前1
扎萨格dd天堂1年前1 -
 59223807 共回答了16个问题
59223807 共回答了16个问题 |采纳率81.3%(1)每天中午每个学生食堂中至少有这个宿舍一名学生用餐的情况有
C24•
A33种,
四名学生到食堂用餐的情况共有34种,
∴每天中午每个学生食堂中至少有这个宿舍一名学生用餐的概率P=
C24•
A33
34=
4
9.
(2)由题设知X的可能取值为0,1,2,3,4,
P(X=0)=
24
34=
16
81,
P(X=1)=
C14•23
34=
32
81,
P(X=2)=
C24•22
34=
24
81,
P(X=3)=
C34•2
34=
8
81,
P(X=4)=
C44
34=
1
81,
∴X的分布列为:
X 0 1 2 3 4
P
16
81
32
81
24
81
8
81
1
81∴EX=0×
16
81+1×
32
81+2×
24
81+3×
8
81+4×
1
81=
4
3.
DX=(0-
4
3)2×
16
81+(1-
4
3)2×
32
81+(2-
4
3)2×
24
81+(3-
4
3)2×
8
81+(4-
4
3)2×
1
81=
8
9.1年前查看全部
- 武清区六年级练什么题
 ly8au1年前2
ly8au1年前2 -
 小飘鱼 共回答了8个问题
小飘鱼 共回答了8个问题 |采纳率87.5%武清区六年级的书可以直接去新华书店看看,或者咨询下老师,1年前查看全部
- (2014•武清区一模)下列说法正确的是( )
(2014•武清区一模)下列说法正确的是( )
A.在气体和液体中,流速越大的位置压强越大
B.汽油机工作时,做功冲程是内能转化为机械能
C.“神州八号”发射升空过程中内能全部转化为势能
D.电风扇工作时将机械能转化为电能 常来侃侃1年前1
常来侃侃1年前1 -
 dalehongliu119 共回答了17个问题
dalehongliu119 共回答了17个问题 |采纳率94.1%解题思路:A、气体和液体都属于流体,在流体中,流速大的地方压强小,流速小的地方压强大.
B、做功冲程中,火花塞冒出电火花,将混合气体点燃,混合气体剧烈燃烧,产生高温高压的燃气,推动活塞运动,燃气的内能转化为活塞运动的动能.
C、燃料的化学能转化成火箭的动能和重力势能,还有一部分以内能的形式散发了.
D、用电器消耗电能的过程,是电流做功的过程,也是电能转化成其他形式能的过程.A、气体的压强与流速的关系:在气体和液体中,流速越大的位置压强越小,故A错误;
B、在做功冲程中,两个气门关闭,活塞下行带动曲轴转动做功,气体的内能转化为机械能,故B正确;
C、“神州八号”发射升空过程中内能没有全部转化为势能,还有一部分以内能的形式散发了,故C错误;
D、电风扇通过电流做功将电能转化为机械能.故D错误.
故选B.点评:
本题考点: 流体压强与流速的关系;能量的相互转化;内燃机的四个冲程.
考点点评: 此题涉及到了流体压强与流速的关系,能量的相互转化,内燃机的四个冲程等多个知识点的理解和掌握,是一道综合性较强的题目.1年前查看全部
- (2012•武清区二模)实验室用6.5g锌与足量稀盐酸反应,可制得氢气多少克?这些氢气在标准状况下为多少升?(氢气的密度
(2012•武清区二模)实验室用6.5g锌与足量稀盐酸反应,可制得氢气多少克?这些氢气在标准状况下为多少升?(氢气的密度是0.09g/L)计算结果保留至0.01.
 020tianhe1年前1
020tianhe1年前1 -
 colorsz-y 共回答了21个问题
colorsz-y 共回答了21个问题 |采纳率81%设生成氢气的质量为x
Zn+2HCl═ZnCl2+H2↑
65 2
6.5g x
[65/6.5g=
2
x]
x=0.2g
氢气在标准状况下的体积为
[0.2g/0.09g/L]=2.22l
答:生成氢气0.2g,在标准状况下2.22升1年前查看全部
- (2014•武清区三模)下列实验现象及其对应的结论正确的是( )
(2014•武清区三模)下列实验现象及其对应的结论正确的是( )

实验 现象 结论 A 锥形瓶中有气体产生,烧杯中液体变浑浊 Cl、C、Si非金属性依次减弱 B 右边试管中冒出的气泡快 FeCl3能加快H2O2分解速率 C 试管中橙色溶液变为绿色 乙醇发生消去反应生成乙烯 D 试管中溶液依次出现白色、淡黄色、黑色沉淀 溶解度:AgCl<AgBr<Ag2S
A.A
B.B
C.C
D.D waxwork8311011年前1
waxwork8311011年前1 -
 飞红的QQ群 共回答了13个问题
飞红的QQ群 共回答了13个问题 |采纳率100%解题思路:A.制取的二氧化碳中含有HCl,HCl干扰二氧化碳的反应;
B.催化剂能加快反应速率;
C.重铬酸钾具有强氧化性,能氧化乙醇;
D.发生沉淀的转化,向更难溶的方向移动.A.盐酸易挥发,与碳酸钠、硅酸钠均发生化学反应,制取的二氧化碳中含有HCl,图中装置不能说明二氧化碳与硅酸钠溶液反应,则不能比较碳酸与硅酸的酸性,故A错误;
B.右边试管中冒出的气泡快,说明氯化铁作催化剂,加快双氧水分解,故B正确;
C.重铬酸钾具有强氧化性,能氧化乙醇,自身被还原,所以溶液颜色发生变化,故C错误;
D.发生沉淀的转化,向更难溶的方向移动,则由白色固体先变为淡黄色,后变为黑色,可知溶解性:AgCl>AgBr>Ag2S,故D错误;
故选B.点评:
本题考点: 化学实验方案的评价.
考点点评: 本题考查了实验方案评价,涉及沉淀的转化、氧化还原反应、催化剂等知识点,明确实验原理是解本题关键,易错选项是A,要排除HCl的干扰.1年前查看全部
- (2010•武清区二模)如图,点C在反比例函数y=kx的图象上,过点C作CD⊥y轴,交y轴负半轴于点D,且△ODC的面积
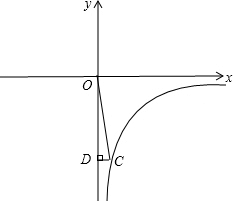 (2010•武清区二模)如图,点C在反比例函数y=
(2010•武清区二模)如图,点C在反比例函数y=
的图象上,过点C作CD⊥y轴,交y轴负半轴于点D,且△ODC的面积是3.k x
(1)求反比例函数y=
的解析式;k x
(2)将过点O且与OC所在直线关于y轴对称的直线向上平移2个单位后得到直线AB,如果CD=1,求直线AB的解析式. 言先生1年前1
言先生1年前1 -
 lfg520 共回答了19个问题
lfg520 共回答了19个问题 |采纳率94.7%解题思路:(1)在反比例函数的图象上任意一点象坐标轴作垂线,这一点和垂足以及坐标原点所构成的三角形的面积是
,且保持不变,再根据反比例函数的图象所在的象限确定k的值,即可求出反比例函数的解析式.|k| 2
(2)由已知条件易得C的坐标,根据对称可求得C关于y轴对称的点的坐标,从而求得OC所在直线关于y轴对称的直线的解析式,根据平移k不变,b值加减即可得出答案.(1)∵△ODC的面积是3,
∴OD•DC=6
∵点C在y=
k
x的图象上,
∴xy=k.(1分)
∴(-y)x=6,
∴k=xy=-6.
∴所求反比例函数解析式为y=−
6
x.(2分)
(2)∵CD=1,即点C(1,y),
把x=1代入y=−
6
x,得y=-6.
∴C(1,-6).
∴C点关于y轴对称点为C′(-1,-6).
∴过点O且与OC所在直线关于y轴对称的直线为y=6x.
∴将直线y=6x向上平移2个单位后得到直线AB的解析式为y=6x+2.点评:
本题考点: 反比例函数综合题.
考点点评: 本题综合考查了反比例函数.用到的知识点为:待定系数法求函数解析式,反比例函数图象和性质,及上下平移直线解析式只改变常数项,上加,下减;左右平移不改变直线解析式中的k,关键是得到平移后经过的一个具体点;求关于某条直线对称的直线解析式,难点是得到新直线解析式上的2个具体点.1年前查看全部
大家在问
- 1若2x的a-b+1次方*y的3a-2b-5次方与-3x的b-1次方*y是同类项,那a的b次方=?
- 2某溶液中存在Mg2+ ,Ag+,Ba2+ 三种金属离子,现用NaOH(1),NaCl(2),Na2CO3(3)三种溶液是
- 3设数列an的前n项和为Sn,已知a1=1,(2Sn)/n=a(n+1)-1/3n^2-n-2/3,
- 41.Which season is it now?什么意思? 2.What's the weather like tod
- 5写几题.在三角形ABC中,角C=90度,a=5,b=12,则c等于
- 6The exercises翻译成中文
- 7(2010•嘉定区一模)熟石灰的溶解度在30℃为a克/100克水,60℃为b克/100克水,且已知60℃时饱和溶液的浓度
- 8如图,∠O=48°PA∥OM,PB∥ON PH⊥PB 求∠的度数
- 9填空:I __in Shanghai since I was born in 1995.A.live B.lived C
- 10对于数据1,2,3,4,5其中众数是什么?1,1,2,2其中众数是什么?
- 11(2011•上饶模拟)请从Ca、C、H、O、Fe、Cl、N七种元素中选择适当的元素按要求填空:(用化学用语填空)
- 12根据短文内容,完形填 根据短文内容,完形填空.(每空一词) There are _______ (1) mon
- 13我是 中队长 用英语怎么说明天就要面试了,
- 14硫酸的相对分子质量不是100吗 为什么是98
- 15为什么秋天的叶子有的会变黄,有的会变红
