碘-131的半衰期是多长?
 benyho2022-10-04 11:39:541条回答
benyho2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 山风水影之二 共回答了16个问题
山风水影之二 共回答了16个问题 |采纳率93.8%- 完全衰变完在理论上是不可能的,并非经过两个半衰期所有辐射都将消失.放射性是一种概率现象,每经过一个半衰期,初始原子会消失50%,即辐射的危险会降低一半,但还能延续很多个半衰期.只要还有最后一个放射性原子,辐射就不可能完全消失.不过通常来说,在经过30个半衰期后,辐射已减至原来的十亿分之一,基本无法被探测到,也就没有危害了.
计算:经过N个半衰期后剩余的放射性原子为1/2的N次幂. - 1年前
相关推荐
- (2011•海淀区一模)2011年3月,日本海啸引发福岛第一核电站的放射性物质外泄,有关131I(碘-131)的相关报道
(2011•海淀区一模)2011年3月,日本海啸引发福岛第一核电站的放射性物质外泄,有关131i(碘-131)的相关报道成为热门话题.请回答下列问题:
(1)碘元素在体内发挥重要作用,但过量补碘也会引起甲亢等疾病.目前***各地检测出的131i含量很小,根据京津等地检出的数值,吃上2000kg的菠菜才相当于照一张x光片的辐射量.根据以上资料分析,下列说法正确的是______.
a.盲目服用碘片等预防辐射对身体可能造成负面作用
b.我们应尽可能主动多摄入含碘食品,多多益善
c.以目前***检测出的131i含量来看,对身体健康影响很小,不必恐慌
(2)131i原子中含有53个质子,78个中子.
①131i原子的核外电子数为______.
②自然界中普遍存在另一种稳定的碘原子127i,它和131i同属于碘元素.127i原子的质子数为______.
(3)专家指出,服用碘片(有效成分为ki)可以治疗131i造成的辐射,但服用碘酒(有效成分为i2)却会引起碘中毒.ki和i2性质的不同的原因是______.
(4)①食盐中常添加碘酸钾(kio3)以补充碘元素.已知kio3中钾元素的化合价为+1,其中碘元素的化合价为______.
②服用碘片治疗131i辐射的推荐服用剂量是每日摄入ki为130-170mg,假设服用某碘片每日补充166mg ki.已知每千克某品牌碘盐中kio3的加入量为42.8mg,如果用该食盐替代碘片提供治疗辐射所需的碘元素,则每日需食用该食盐的质量为______kg. 有印良屿1年前1
有印良屿1年前1 -
 restcool 共回答了17个问题
restcool 共回答了17个问题 |采纳率94.1%解题思路:(1)利用题中的信息结合所学的化学知识解决.
(2)①根据原子中质子数=核外电子数回答.
②根据元素的种类是由质子数决定的回答.
(3)根据物质的结构决定物质的性质回答.
(4)①利用化合物中元素的化合价代数和等于零解决②根据每日需要补充166mgKI的质量计算所需碘元素的质量,根据碘元素的质量求出碘酸钾的质量,再根据已知每千克某品牌碘盐中KIO3的加入量为42.8mg计算碘盐的质量.(1)由题中的信息可以看出,过量服碘有害无益.
(2)①131I原子中含有53个质子,根据原子中质子数=核外电子数,131I原子的核外电子数为53.
②由于元素的种类是由质子数决定的,碘原子127I和131I同属于碘元素,故127I原子的质子数为53.
(3)物质的性质是由物质的结构决定的,KI和I2的性质不同是因构成物质的微粒(分子)不同.
(4)①碘酸钾中碘的化合价可通过钾的化合价是+1氧的化合价是-2,再结合相关的化合物中化合价代数和是零的原则完成,求得碘的化合价是+5;
②KI中碘的质量分数为 [127/39+127]×100%=76.5%,每日需要补充166mg KI,则含碘元素的质量为166mg×76.5%=127mg;KIO3中碘的质量分数为 [127/39+127+16×3]×100%=59.35%,则需碘酸钾[127mg/59.35%]=214mg,已知每千克某品牌碘盐中KIO3的加入量为42.8mg,故每日需食用该食盐的质量为:
[214mg/42.8mg/kg]=5kg.
故答案为:(1)ac(2)①53;②53;(3)构成物质的微粒(分子)不同(要点是“结构不同”);(4)①+5②5.点评:
本题考点: 原子的定义与构成;分子、原子、离子、元素与物质之间的关系;有关元素化合价的计算;混合物中某元素的质量计算;人体的元素组成与元素对人体健康的重要作用.
考点点评: 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.学生分析问题的思维跨度较大,强调了学生整合知识的能力,以及对信息的分析、提炼、加工、运用的能力.1年前查看全部
- 2011年3月11日,在日本福岛发生了震惊世界的核泄漏事件,关于核电站泄漏的放射性碘-131( 53 131 I)、铯-
2011年3月11日,在日本福岛发生了震惊世界的核泄漏事件,关于核电站泄漏的放射性碘-131( 53 131 I)、铯-137( 55 137 Cs)的各种说法正确的是( ) A.碘-131的中子数为78 B.碘-131质量数为53 C.碘与铯互称同位素 D.铯-137的放射性是化学性质  847559451年前1
847559451年前1 -
 小磊_NIU8682 共回答了21个问题
小磊_NIU8682 共回答了21个问题 |采纳率90.5%A、碘-131的中子数=质量数-质子数=131-53=78,故A正确.
B、碘-131的质量数为131,故B错误.
C、碘和铯是不同的元素,所以不是同位素,故C错误.
D、铯-137的放射性是物理性质,故D错误.
故选A.1年前查看全部
- 今年3月12日riben福岛核电站因发生特大地震出现放射性物质泄露.碘元素有20多种原子,质子数都是53.碘-131(相
今年3月12日riben福岛核电站因发生特大地震出现放射性物质泄露.碘元素有20多种原子,质子数都是53.碘-131(相对原子质量为131)是一人工合成的元素遇到适宜条件,粒子就会从原子核内散逸出去,同时释放出射线,碘-131的放射性由此而来.研究人员还发现,碘-131的半衰期为8.02天,也就是每过8天放射物质会衰减一半,30个半衰期过后,辐射强度已减至原来的十亿分之一,基本无法被探测到.变成了稳定的其它元素.
(1)碘-131原子核内中子个数有______.
(2)碘盐中的碘是稳定的碘-127以KIO3存在,一个KIO3分子中电子个数有______. 乖乖_叶_ll1年前1
乖乖_叶_ll1年前1 -
 jianzhu117 共回答了20个问题
jianzhu117 共回答了20个问题 |采纳率85%解题思路:(1)依据原子中质子数与中子数之和约等于其相对原子质量分析解答;
(2)利用分子中质子总数等于电子总数分析解答:(1)由于原子中质子数与中子数之和约等于其相对原子质量,所以53+中子数=131,则中子数为78;
(2)依据分子中质子总数等于电子总数,可知由于KIO3分子中的质子数=19+53+8×3=96,所以其核外电子总数为96;
故答案为:(1)78;(2)96;点评:
本题考点: 原子的有关数量计算.
考点点评: 本题主要考查了原子的构成,会根据构成原子的微粒数目关系,判断一些微粒的数目,是解题的关键.1年前查看全部
- 我们已知的放射物质,是一些物质的原子核能发生衰变.如碘-131衰变为氙131.
我们已知的放射物质,是一些物质的原子核能发生衰变.如碘-131衰变为氙131.
如果我们在衰变之前,用化学方式进行中和发生物理沉淀,或者利用带有放射性的元素进行化学反应,能否有效的控制放射性污染物的泄露啊什么的?或者一开始在进行人工放射性元素的时候,选取较为容易产生物理沉淀的钡137. gb1980071年前2
gb1980071年前2 -
 legend_zx 共回答了23个问题
legend_zx 共回答了23个问题 |采纳率82.6%衰变与化学状态,物理作用无关.选择何种放射性物质并不是人说了算.因为并不是说有放射性物质都能作为核燃料.比如说钡137就不能,钴60也不能,碳14也不行.目前可作为核燃料比较现实的是钚和铀.镭以及很多人造元素虽然也可以,但是成本极高得不常失,而且危害也不一定就小.处理液体核废料,确实有人在研究如何将其固化.然后封存,记得是八十年代加拿大有人在研究.就是不知道有没有取得成功1年前查看全部
- 碘片(碘-127)以降低放射性对人体的伤害,已知放射性碘(碘-131)的核电荷数为53,中子数为78,碘-131和
碘片(碘-127)以降低放射性对人体的伤害,已知放射性碘(碘-131)的核电荷数为53,中子数为78,碘-131和
碘-127的化学性质是否不同 zdlec1年前1
zdlec1年前1 -
 budeannin 共回答了16个问题
budeannin 共回答了16个问题 |采纳率81.3%化学性质看的只是元素种类.
都是碘元素,就没有不同1年前查看全部
- (2011•徐州)2011年3月,日本地震引发福岛第一核电站的放射性物质碘-131外泄.人体的甲状腺会吸收放射性碘-13
(2011•徐州)2011年3月,日本地震引发福岛第一核电站的放射性物质碘-131外泄.人体的甲状腺会吸收放射性碘-131,并对甲状腺造成损伤.碘片可减少甲状腺对碘-131的吸收.
请回答下列问题
{1}碘-131原子的原子核带53个单位的正电荷,则该原子的核外电子数为______
{2}我国在一些极少数地区也检测到极少量的碘-131,这说明微粒是______
{3}碘片中的“碘”指的是______{选填“分子”,“原子”或“元素”},如果人体内缺碘会导致______.
{4}福岛第一核电站机组反应堆芯释放出的高温氢气接触外界的氧气发生剧烈反应,导致连续爆炸.氢气爆炸时的化学方程式为2H2+O2
2H2O高温 .2H2+O2;反应的基本类型为______.
2H2O高温 . yuquan02341年前1
yuquan02341年前1 -
 星月夜光 共回答了16个问题
星月夜光 共回答了16个问题 |采纳率81.3%解题思路:(1)根据原子核带53个单位的正电荷,在原子中质子带正电,利用原子中质子数等于核外电子数来解答;
(2)根据在一些极少数地区也检测到极少量的碘-131,则说明微粒可以运动到偏远的地方,利用微粒的性质来解答;
(3)根据碘片中碘的存在形态来分析,并利用碘片可减少甲状腺对碘-131的吸收来分析;
(4)根据反应物与生成物书写化学反应方程式,并利用物质的种类和多少来分析反应的类型.(1)因该原子的原子核带53个单位的正电荷,则质子数为53,且在原子中质子数等于核外电子数,则核外电子数为53,故答案为:53;
(2)由在不同的地方都可以检测到碘-131,则说明该微粒是不断运动的,从一个地方能运动到另一个地方,故答案为:不断运动的;
(3)因碘片中的碘是以碘酸盐的形式存在的,则碘是指碘元素,由碘片可减少甲状腺对碘-131的吸收可知人体内缺碘会导致甲状腺肿大,故答案为:元素;甲状腺肿大;
(4)因反应物为氢气和氧气,生成物为水,则反应为2H2+O2
高温
.
2H2O,该反应是两种物质反应生成一种物质,则属于化合反应;故答案为:2H2+O2
高温
.
2H2O;化合反应.点评:
本题考点: 原子的有关数量计算;利用分子与原子的性质分析和解决问题;元素的概念;反应类型的判定;书写化学方程式、文字表达式、电离方程式;微量元素、维生素与健康的关系及摄取方法.
考点点评: 本题属于信息习题,学生应学会利用信息中的关键性信息并结合所学知识来解答问题,较好的考查了学生分析解决问题的能力.1年前查看全部
- 2011年3月,日本强烈地震后,海啸引发福岛第一核电站的放射性物质外泄,有关131I(碘-131)的相关报道成为热门话题
2011年3月,日本强烈地震后,海啸引发福岛第一核电站的放射性物质外泄,有关131I(碘-131)的相关报道成为热门话题.请回答下列问题:
(1)131I原子中含有53个质子,78个中子.
①131I原子的核外电子数为______.
②自然界中普遍存在另一种稳定的碘原子127I,它和131I同属于碘元素.127I原子的质子数为______.
(2)专家指出,服用碘片(有效成分为KI)可以治疗131I造成的辐射,但服用碘酒(有效成分为I2)却会引起碘中毒.KI和I2的性质不同的原因是______. unreally1年前1
unreally1年前1 -
 gg五筒 共回答了23个问题
gg五筒 共回答了23个问题 |采纳率87%解题思路:(1)根据在原子中,核内质子数=核外电子数,同种元素的原子质子数相同分析填空.
(2)根据构成物质的微粒分析物质的性质,结构决定性质.(1)①在原子中,核内质子数=核外电子数,由于131I原子中含有53个质子,所以131I原子的核外电子数为53;②同种元素的原子质子数相同,131I原子中含有53个质子,所以127I原子的质子数为53.(2)物质的结构决定物质...
点评:
本题考点: 原子的定义与构成.
考点点评: 本题主要考查了原子中有关数量计算.原子序数=核内质子数=核电荷数=核外电子数.1年前查看全部
- 碘-131与碘-127均为碘在自然界中稳定存在的同位素,3Q
 不想睡1年前1
不想睡1年前1 -
 公主指标 共回答了19个问题
公主指标 共回答了19个问题 |采纳率89.5%碘-131是元素碘的一种放射性同位素,为人工放射性核素(核裂变产物),符号为I-131,半衰期为8.3天.正常情况下自然界是不会存在.1年前查看全部
- 日本核泄漏事故释放的放射性物质中含有碘-131,下列关于 13153 I的说法正确的是( ) A. 13153 I和
日本核泄漏事故释放的放射性物质中含有碘-131,下列关于
I的说法正确的是( )13153 A.
I和13153
I是同一种核素13453 B.
I和13153
I互为同位素13453 C.
I和13153
I都含有53个电子13453 D.
I和13153
I都含有53个中子13453  囿点笨1年前1
囿点笨1年前1 -
 sanheidan 共回答了15个问题
sanheidan 共回答了15个问题 |采纳率80%A.
13153 I和
13453 I中子数不相同,不是同一种核素,故A错误;
B.
13153 I和
13453 I质子数相同,中子数不同,互为同位素,故B正确;
C.
13153 I和
13453 I质子数=核外电子数=53,故C正确;
D.中子数=质量数-质子数,
13153 I和
13453 I中中子数分别为78、81,故D错误.
故选BC.1年前查看全部
- 2011年3月,日本强烈地震后,海啸引发福岛第一核电站的放射性物质外泄,有关131I(碘-131)的相关报道成为热门话题
2011年3月,日本强烈地震后,海啸引发福岛第一核电站的放射性物质外泄,有关131I(碘-131)的相关报道成为热门话题.请回答下列问题:
(1)131I原子中含有53个质子,78个中子.自然界中普遍存在另一种稳定的碘原子127I,它和131I同属于碘元素.127I原子的质子数为______.
(2)专家指出,服用碘片(有效成分为KI)可以治疗131I造成的辐射,但服用碘酒(有效成分为I2)却会引起碘中毒.KI和I2的性质不同的原因是______.
(3)日本地震后,个别居民抢购食盐.假设某人经医生确认,每日需要补充166mg KI.已知每千克某品牌碘盐中KIO3的加入量为42.8mg,如果用该食盐替代碘片提供治疗辐射所需的碘元素,则每日需食用该食盐的质量为______kg. 悠悠沧海1年前2
悠悠沧海1年前2 -
 zqpczj 共回答了13个问题
zqpczj 共回答了13个问题 |采纳率100%解题思路:(1)根据元素的种类是由质子数决定的回答;(2)根据物质的结构决定物质的性质回答;(3)根据每日需要补充166mgKI的质量计算所需碘元素的质量,根据碘元素的质量求出碘酸钾的质量,再根据已知每千克某品牌碘盐中KIO3的加入量为42.8mg计算碘盐的质量.(1)由于元素的种类是由质子数决定的,碘原子127I和131I同属于碘元素,故127I原子的质子数为53;
(2)物质的性质是由物质的结构决定的,KI和I2的性质不同是因构成物质的微粒不同;
(3)每日需要补充166mg KI,则含碘元素的质量为166mg×[127/39+127]×100%═127mg;
则需碘酸钾127mg÷[127/39+127+16×3]×100%=214mg,已知每千克某品牌碘盐中KIO3的加入量为42.8mg,故每日需食用该食盐的质量为214mg÷42.8mg/kg=5kg.(根据计算结果可以看出,利用加碘食盐来防辐射是不可行的,因为人不能吃那么多的食盐).
故答案为:(1)53;(2)构成物质的微粒不同;(3)5.点评:
本题考点: 元素的概念;利用分子与原子的性质分析和解决问题;化合物中某元素的质量计算.
考点点评: 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.学生分析问题的思维跨度较大,强调了学生整合知识的能力,以及对信息的分析、提炼、加工、运用的能力.1年前查看全部
- 碘-131(质子数与中子数之和)具有放射性,对人体有害.而生活中的碘盐、碘酒所含的碘-127对人体无害.碘-131和碘-
碘-131(质子数与中子数之和)具有放射性,对人体有害.而生活中的碘盐、碘酒所含的碘-127对人体无害.碘-131和碘-127是同种元素的不同原子,核电荷数均为53.下列说法正确的是( ) A.碘是一种金属元素 B.碘-127原子核外有74个电子 C.碘-131原子核内有78个质子 D.碘-131和碘-127核内中子数不同  高空微笑1年前1
高空微笑1年前1 -
 wangtao5211314 共回答了17个问题
wangtao5211314 共回答了17个问题 |采纳率88.2%A、碘是一种非金属元素,符合非金属元素的书写特征,故此选项错误.
B、由于在原子中质子数等于电子数,所以碘的核外电子数是53,故此选项错误.
C、原子中质子数等于电子数等于核电荷数,所以碘原子核内部质子数是53,故此选项错误.
D、131与127是质子数与中子数之和,两者质子数相同中子数一定不同,故此选项正确.
故选D1年前查看全部
- 据报道,日本福岛核电站发生泄漏事故后,在我市环境空气中检测出一种微量的放射性核素“碘-131”,含量为每立方米0.4毫贝
据报道,日本福岛核电站发生泄漏事故后,在我市环境空气中检测出一种微量的放射性核素“碘-131”,含量为每立方米0.4毫贝克(这种元素的半衰期是8天,即每8天含量减少一半,如8天后减少到0.2毫贝克),那么要使含量降至每立方米0.0004毫贝克以下,下列天数中,能达到目标的最少天数是( )
A.64
B.71
C.82
D.104 香雪鱼鱼1年前1
香雪鱼鱼1年前1 -
 chuasy 共回答了13个问题
chuasy 共回答了13个问题 |采纳率100%解题思路:根据这种元素的半衰期是8天,即每8天含量减少一半,设经过n次半衰期,由0.4毫贝克到0.0004毫贝克以下,可列出不等式求出n,进而求出天数.设经过n次半衰期,
2n>[0.4/0.0004],
n>10.
10×8=80.
故能达到目标的最少天数是82天.
故选C.点评:
本题考点: 一元一次不等式的应用.
考点点评: 本题理解题意的能力,先求出经过几次半衰期,然后求出天数,即可找到答案.1年前查看全部
- 碘-131和碘-127的化学性质是否相同?
 傻小女人1年前2
傻小女人1年前2 -
 lengyuegushuang 共回答了12个问题
lengyuegushuang 共回答了12个问题 |采纳率91.7%碘-131是放射性元素,常用来治疗甲状腺疾病,其化学性质于常见同位素碘-127相同.1年前查看全部
- 2011年3月,日本强烈地震后,海啸引发福岛第一核电站的放射性物质外泄,有关 131 I(碘-131)的相关报道成为热门
2011年3月,日本强烈地震后,海啸引发福岛第一核电站的放射性物质外泄,有关 131 I(碘-131)的相关报道成为热门话题。请回答下列问题:
(1) 131 I原子中含有53个质子,78个中子。
① 131 I原子的核外电子数为__________。
②自然界中普遍存在另一种稳定的碘原子 127 I,它和 131 I同属于碘元素。127I原子的质子数为________。
(2)专家指出,服用碘片(有效成分为KI)可以治疗 131 I造成的辐射,但服用碘酒(有效成分为I 2 )却会引起碘中毒。KI和I 2 的性质不同的原因是_________。
(3)日本地震后,个别居民抢购食盐。假设某人经医生确认,每日需要补充166mgKI。已知每千克某品牌碘盐中KIO 3 的加入量为42.8mg,如果用该食盐替代碘片提供治疗辐射所需的碘元素,则每日需食用该食盐的质量为__________kg。 亲1切1年前1
亲1切1年前1 -
 坠天nn 共回答了17个问题
坠天nn 共回答了17个问题 |采纳率94.1%(1)①53、②53
(2)构成物质的微粒(分子)不同(要点是“结构不同”)
(3)51年前查看全部
- 据报道:日本大地震引发福岛核电站爆炸后泄漏出放射性物质碘-131.碘-131是质子数为53、中子数为78的一种碘原子,则
据报道:日本大地震引发福岛核电站爆炸后泄漏出放射性物质碘-131.碘-131是质子数为53、中子数为78的一种碘原子,则该原子的核电荷数为( )
A. 53
B. 78
C. 131
D. 184 fzhawl1年前1
fzhawl1年前1 -
 肖十一郎诚交友 共回答了21个问题
肖十一郎诚交友 共回答了21个问题 |采纳率90.5%解题思路:根据原子中:核电荷数=质子数=电子数、相对原子质量=质子数+中子数,结合题意进行分析解答.由题意碘-131是质子数为53、中子数为78的一种碘原子,因为原子中,核电荷数=质子数=电子数,故该原子的核电荷数为为53.
故选A.点评:
本题考点: 原子的有关数量计算.
考点点评: 本题难度不是很大,解题的关键是理解题意、灵活运用原子中核电荷数=质子数=电子数、相对原子质量=质子数+中子数.1年前查看全部
- (2011•遵义)2011年日本福岛核电站发生核泄漏所产生的污染物之一“碘-131”,其原子核内有53个质子,78个中子
(2011•遵义)2011年日本福岛核电站发生核泄漏所产生的污染物之一“碘-131”,其原子核内有53个质子,78个中子,则该原子的核电荷数为( )
A.53
B.131
C.78
D.127 8102071年前1
8102071年前1 -
 cj_0908 共回答了13个问题
cj_0908 共回答了13个问题 |采纳率92.3%解题思路:在原子中,核电荷数=核内质子数=核外电子数=原子序数.在原子中,核电荷数等于质子数,也等于核外电子数,故该原子的核电荷数为53.
故选A.点评:
本题考点: 原子的定义与构成.
考点点评: 此题是对原子知识的考核,解题的关键是对有关原子知识的掌握,属基础性知识考查题.1年前查看全部
- 日本大地震引发的福岛第一核电站核泄漏事故,造成放射性物质碘-131和铯-137( Cs)向外界泄漏。下列相关说
日本大地震引发的福岛第一核电站核泄漏事故,造成放射性物质碘-131和铯-137( Cs)向外界泄漏。下列相关说法错误的是 [ ]A.每个 Cs原子中有82个中子
B.CsOH的碱性比KOH强
C.HI比HF还原性强
D.KIO 3 是碘的最高价含氧酸的盐 想想再說吧1年前1
想想再說吧1年前1 -
 forseasons 共回答了17个问题
forseasons 共回答了17个问题 |采纳率94.1%D1年前查看全部
- 2011年3月,日本地震引发福岛第一核电站的放射性物质碘-131(131是碘的相对原子质量)外泄.人体甲状腺会吸收放射性
2011年3月,日本地震引发福岛第一核电站的放射性物质碘-131(131是碘的相对原子质量)外泄.人体甲状腺会吸收放射性碘-131,并对甲状腺造成损伤.碘-131原子含有53个质子,则该原子的中子数为______,自然界中普遍存在另一种稳定的碘原子碘-127,它和碘-131同属于碘元素,它的质子数为______,中子数为______.
 71302511年前1
71302511年前1 -
 断弦 共回答了24个问题
断弦 共回答了24个问题 |采纳率79.2%解题思路:根据原子中:相对原子质量=质子数+中子数,决定元素种类的是核内质子数,结合题意进行分析解答.根据题意,碘-131(131是碘的相对原子质量),碘-131原子含有53个质子,由相对原子质量=质子数+中子数,则中子数=131-53=78.
碘原子碘-127,它和碘-131同属于碘元素,同种元素的原子是核内质子数相同,碘-131原子含有53个质子,则碘-127的质子数为53;由相对原子质量=质子数+中子数,则中子数=127-53=74.
故答案为:78;53;74.点评:
本题考点: 原子的有关数量计算.
考点点评: 本题难度不大,解题的关键是掌握并灵活运用原子中核电荷数=核内质子数=核外电子数、相对原子质量=质子数+中子数.1年前查看全部
- (2011•贺州)2011年3月,日本大地震引发福岛核电站的放射性物质发泄,有关碘-131(131I)、碘-127(12
(2011•贺州)2011年3月,日本大地震引发福岛核电站的放射性物质发泄,有关碘-131(131I)、碘-127(127I)等碘原子.请回答下列问题:
(1)131I原子中含有53个质子,78个中子
①131I原子中核外电子数为______;
②127I是自然界中普遍存在的一种稳定的碘原子,它和131I同属于碘元素.127I原子的质子数为______;
(2)食盐中常添碘酸钾(KIO3)以补充碘元素.KIO3中碘的化合价为______;
(3)专家指出服用碘片(有效成分为KI)可以治疗131I造成的核辐射,但服用碘酒(有效成分为I2)却会引起碘中毒.KI和I2化学性质不同的原因是______. s42235331年前1
s42235331年前1 -
 yufan2149 共回答了16个问题
yufan2149 共回答了16个问题 |采纳率68.8%解题思路:(1)依据元素种类相同则质子数相同以及原子中质子数等于电子数分析解决;
(2)依据化合物中各元素的化合价代数和为零分析判断;
(3)依据物质的结构决定物质的性质分析判断;(1)①在原子中,核内质子数=核外电子数,由于131I原子中含有53个质子,所以131I原子的核外电子数为53;
②同种元素的原子质子数相同,131I原子中含有53个质子,所以127I原子的质子数为53.
(2)因为在KIO3中各元素的化合价代数和为零,而钾的化合价为+1,氧的化合价为-2,所以碘的化合价为+5;
(3)物质的结构决定物质的性质,碘酒中的碘是由碘分子构成的,KI中的碘是碘离子,构成物质的微粒不同,所以,KI和I2的性质不同.
故答案为:(1)①53;②53;+5;(3)构成物质的微粒不同;点评:
本题考点: 原子的有关数量计算;元素的概念;化学性质与物理性质的差别及应用.
考点点评: 本题主要考查了原子中有关数量计算.掌握原子序数=核内质子数=核电荷数=核外电子数是解题的关键.1年前查看全部
- (4分)2011年3月,日本大地震引发福岛核电站的放射性物质发泄,有关碘-131( 131 I)、碘-127( 127
(4分)2011年3月,日本大地震引发福岛核电站的放射性物质发泄,有关碘-131( 131 I)、碘-127( 127 I)等碘原子。请回答下列问题:
⑴ 131 I原子中含有53个质子,78个中子
① 131 I原子中核外电子数为 ;
② 127 I是自然界中普遍存在的一种稳定的碘原子,它和 131 I同属于碘元素。 127 I原子的质子数为 ;
⑵食盐中常添碘酸钾(KIO 3 )以补充碘元素。KIO 3 中碘的化合价为 ;
⑶专家指出服用碘片(有效成分为KI)可以治疗 131 I造成的核辐射,但服用碘酒(有效 成分为I 2 )却会引起碘中毒。KI和I 2 化学性质不同的原因是 ; baobeisy1年前1
baobeisy1年前1 -
 雪花有情8681 共回答了19个问题
雪花有情8681 共回答了19个问题 |采纳率94.7%(1)① 53 ;② 53 ;
+5 ;(3) 构成物质的分子不同
(1)在原子中质子数等于核外电子数,则核外电子数为53, 127 I和 131 I同属于碘元素。 127 I原子的质子数也为53
根据在化合物中正负化合价代数和为零,钾元素显+1,氧元素显-2,设碘元素的化合价是x,可知碘酸钾(KIO 3 )中碘元素的化合价:(+1)+x+(-2)×3=0,则x=+5.
(3)物质的性质是由物质的结构决定的,KI和I 2 的性质不同是因构成物质的微粒(分子)不同1年前查看全部
- 碘一127和碘-131是同种元素的不同原子,核电荷数均为53.碘-131(质子数与中子数之和)具有放射性,对人体有害.而
碘一127和碘-131是同种元素的不同原子,核电荷数均为53.碘-131(质子数与中子数之和)具有放射性,对人体有害.而生活中的碘盐、碘酒所含的碘-127对人体无害.下列说法正确的是( )
A.碘是一种金属元素
B.碘-127原子核外有74个电子
C.碘-131原子核内有78个质子
D.碘-127和碘-131核内中子数不同 向日葵88871年前1
向日葵88871年前1 -
 一米阳光336 共回答了20个问题
一米阳光336 共回答了20个问题 |采纳率95%解题思路:A、依据碘是一种非金属元素分析解答.
B、依据原子中质子数和核外电子数相同分析解答;
C、依据核电荷数等于核外电子数分析解答;
D、131与127是质子数与中子数之和,两者质子数相同中子数一定不同.A、碘是一种非金属元素,符合非金属元素的书写特征,故此选项错误.
B、由于在原子中核电荷数等于质子数等于核外电子数,所以碘的核外电子数是53,故此选项错误.
C、原子中质子数等于电子数等于核电荷数,所以碘原子核内部质子数是53,故此选项错误.
D、相对原子质量等于质子数与中子数之和,故131与127是两种原子中质子数与中子数之和,两者质子数相同,所以两者中子数一定不同,故此选项正确.
故选:D.点评:
本题考点: 原子的有关数量计算;元素的简单分类.
考点点评: 此题是一道原子知识的考查题,解题的关键是对原子内一些量的关系的了解.1年前查看全部
- 2011年3月,日本海啸引发福岛第一核电站的放射性物质外泄,有关131I(碘-131)的相关报道成为热门话题.请回答下列
2011年3月,日本海啸引发福岛第一核电站的放射性物质外泄,有关131i(碘-131)的相关报道成为热门话题.请回答下列问题:
(1)碘元素在体内发挥重要作用,但过量补碘也会引起甲亢等疾病.目前***各地检测出的131i含量很小,根据京津等地检出的数值,吃上2000kg的菠菜才相当于照一张x光片的辐射量.根据以上资料分析,下列说法正确的是______.
a.盲目服用碘片等预防辐射对身体可能造成负面作用
b.我们应尽可能主动多摄入含碘食品,多多益善
c.以目前***检测出的131i含量来看,对身体健康影响很小,不必恐慌
(2)131i原子中含有53个质子,78个中子.131i原子的核外电子数为______.
(3)专家指出,服用碘片(有效成分为ki)可以治疗131i造成的辐射,但服用碘酒(有效成分为i2)却会引起碘中毒.ki和i2性质的不同的原因是______.
(4)①食盐中常添加碘酸钾(kio3)以补充碘元素.已知kio3中钾元素的化合价为+1,其中碘元素的化合价为______.
②服用碘片治疗131i辐射的推荐服用剂量是每日摄入ki为130-170mg,假设服用某碘片每日补充166mg ki.已知每千克某品牌碘盐中kio3的加入量为42.8mg,如果用该食盐替代碘片提供治疗辐射所需的碘元素,则每日需食用该食盐的质量为______kg. 沙鱼D1年前1
沙鱼D1年前1 -
 可能是我爱的不够 共回答了20个问题
可能是我爱的不够 共回答了20个问题 |采纳率100%解题思路:(1)依据题中信息解决.
(2)原子中质子数等于电子数,已知质子数可知电子数.
(3)结构决定物质的性质,性质不同结构一定不同.
(4)①依据化合物中元素的化合价代数和等于零解决.
②分别对不同含碘的化合物进行碘量的计算解决,可先求出每天补充的碘量,然后再利用食盐中的含碘量求需要多少食盐即可.(1)由题中信息可知过量服碘对身体无益,少量辐射对人体无害.
(2)原子中质子数等于电子数,其质子数是53,核外电子数也是53.
(3)结构决定性质,KI和I2性质的不同,是因为其构成的微粒不同导致的.
(4)①已知KIO3中钾元素的化合价为+1,氧的化合价为-2价,依据化合物中元素的化合价等于零可知碘的化合价是+5价.
②166mgKI中碘元素的质量为166mg×碘化钾中碘的质量分数=166×[127/166]=127mg
每千克食盐中含42.8mgKIO3中碘元素的质量为42.8mg×碘酸钾中碘的质量分数=42.8×[127/214]=25.4mg
要提供127mg碘元素,需要食盐的质量为 [127/25.4]kg=5kg
故答案为:
(1)ac;
(2)①53,②53;
(3)构成物质的微粒(分子)不同;
(4)①+5;②5.点评:
本题考点: 原子的定义与构成;利用分子与原子的性质分析和解决问题;有关元素化合价的计算;混合物中某元素的质量计算;人体的元素组成与元素对人体健康的重要作用.
考点点评: 此题是一道多点知识考查题,解题的关键是对相关知识点的掌握与理解,属基础性知识考查题.1年前查看全部
- 碘化钾的化学式碘-131原子核内有几个中子
 whg9543211年前1
whg9543211年前1 -
 leon0324 共回答了21个问题
leon0324 共回答了21个问题 |采纳率100%KI,
碘131的中子数为:131-53=78.
如果你是初中的 ,那你要注意同位素、元素的概念和相对原子质量,这是今年考点.1年前查看全部
- 日本地震引发的核电站泄漏引起了全球人们的恐慌,核电站泄漏物质中包含放射性元素碘-131.如图是元素周期表中碘元素的某些信
 日本地震引发的核电站泄漏引起了全球人们的恐慌,核电站泄漏物质中包含放射性元素碘-131.如图是元素周期表中碘元素的某些信息,下列说法中不正确的是( )
日本地震引发的核电站泄漏引起了全球人们的恐慌,核电站泄漏物质中包含放射性元素碘-131.如图是元素周期表中碘元素的某些信息,下列说法中不正确的是( )
A.碘-131和图示中的碘是不同的元素
B.碘元素的原子的核电荷数为53
C.碘-131的核内中子数为78
D.碘元素是非金属元素 想飞10191年前1
想飞10191年前1 -
 小罡炮 共回答了12个问题
小罡炮 共回答了12个问题 |采纳率100%解题思路:由题意可知“在元素周期表中,碘元素的某些信息如图所示”,可知碘元素的相对原子质量;由碘的汉语名称,可知其元素种类;根据“原子序数=核内质子数=核外电子数=核电荷数”,可知其他信息.A、由图示信息知碘元素的核电荷数为53,而碘-131和图示中的碘都是碘元素,因而属于同种元素,只是两者的核内中子数不同,属于不同的碘原子,故A错误;
B、由图示信息知碘元素的核电荷数为53,故B正确;
C、碘-131的相对原子质量为131,故其中子数为131-53=78,故C正确;
D、由碘元素的元素名称“碘”可知,该元素属于非金属元素,故D正确.
故选:A.点评:
本题考点: 元素周期表的特点及其应用.
考点点评: 了解元素周期表的特点及其应用;核外电子在化学反应中的作用;了解元素的简单分类.1年前查看全部
- 碘-131是原子质数,中指数
 chaiminghua1年前2
chaiminghua1年前2 -
 secret116 共回答了18个问题
secret116 共回答了18个问题 |采纳率77.8%131是指质量数,碘是53号元素,所以质子数=53,中子数=131-53=78 .1年前查看全部
- 2011年3月11日,日本福岛核电站因为9.0级大地震引发的海啸受损,产生严重的核泄漏.核泄漏物中含放射性元素碘-131
2011年3月11日,日本福岛核电站因为9.0级大地震引发的海啸受损,产生严重的核泄漏.核泄漏物中含放射性元素碘-131,则有关碘-131(
I)和碘-127(13153
I)说法正确的是( )12753
A.
I和13153
I的中子数相同,是同一种核素12753
B.
I和13153
I的质子数相同,互为同位素12753
C.
I和13153
I的核外电子排布方式不同12753
D.
I有放射性而13153
I无放射性,说明两者化学性质不同12753 nbzou1年前1
nbzou1年前1 -
 焦咖啡 共回答了12个问题
焦咖啡 共回答了12个问题 |采纳率91.7%解题思路:A.中子数=质量数-质子数;
B.质子数相同中子数不同的同种元素的不同原子互为同位素;
C.质子数=核外电子数;
D.放射性是物理性质.A.中子数=质量数-质子数,
13153I和
12753I的中子数不同,故A错误;
B.127I与131I符合同位素概念,互为同位素,故B正确;
C.质子数=核外电子数,
13153I和
12753I的核外电子排布方式相同,故C错误;
D.二者是同种元素,化学性质相同,故D错误.
故选B.点评:
本题考点: 核素;质量数与质子数、中子数之间的相互关系.
考点点评: 本题考查了核素、同位素的定义,题目较为基础,注意一种不同的原子就是一种核素.1年前查看全部
- (2011•安溪县质检)2011年3月11日,日本发生强烈地震造成了福岛核电站核泄漏,其中放射性碘-131的有关信息如图
 (2011•安溪县质检)2011年3月11日,日本发生强烈地震造成了福岛核电站核泄漏,其中放射性碘-131的有关信息如图所示,下列有关碘-131的说法正确的是( )
(2011•安溪县质检)2011年3月11日,日本发生强烈地震造成了福岛核电站核泄漏,其中放射性碘-131的有关信息如图所示,下列有关碘-131的说法正确的是( )
A.碘-131在自然界的含量是53%
B.碘属于非金属元素
C.碘-131的相对原子质量为131g
D.碘的相对原子质量为53 zhongrengg1年前1
zhongrengg1年前1 -
 405154475 共回答了12个问题
405154475 共回答了12个问题 |采纳率100%解题思路:由题意可知“在元素周期表中,碘元素的某些信息如图所示”,可知碘元素的相对原子质量;由碘的汉语名称,可知其元素种类;根据“原子序数=核内质子数=核外电子数=核电荷数”,可知其他信息A、由碘的有关信息不能确定其在自然界中的含量;
B、由碘的汉语名称可知碘属于非金属元素.正确.
C、由信息可知碘的相对原子质量为131,不能带单位g,错误;
D、碘的相对原子质量为131,质子数为53,错误.
故选B点评:
本题考点: 元素周期表的特点及其应用;元素的简单分类.
考点点评: 本题考查学生熟练掌握应用元素周期表所提供的信息进行分析解题的能力.1年前查看全部
- (2012•通州区二模)2011年3月,受地震影响,riben福岛第一核电站反应堆发生放射性元素碘-131泄漏事故.已知
(2012•通州区二模)2011年3月,受地震影响,riben福岛第一核电站反应堆发生放射性元素碘-131泄漏事故.已知碘-131的原子核内质子数为53,质子数与中子数之和为131,则下列关于该原子的说法正确的是( )
A.中子数为88
B.核外电子数位53
C.核电荷数为131
D.1个该原子的质量为131g 爱有天意-雨1年前1
爱有天意-雨1年前1 -
 晚儿的净土 共回答了21个问题
晚儿的净土 共回答了21个问题 |采纳率100%解题思路:在原子中,核内质子数=核电荷数=核外电子数,相对原子质量=质子数+中子数,相对原子质量是原子的相对的质量,不是实际质量,据此分析解答即可;A、已知碘-131的原子核内质子数为53,质子数与中子数之和为131,则中子数是78;故A不正确;
B、在原子中,核内质子数=核电荷数=核外电子数,再根据题意知其核外电子数是53;故B正确;
C、在原子中,核内质子数=核电荷数=核外电子数,再根据题意知其核电荷数是53;故C不正确;
D、由题意知1个该原子的相对原子质量是131,不是原子的实际质量是131g.故D不正确;
故选B点评:
本题考点: 原子的有关数量计算.
考点点评: 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.学生分析问题的思维跨度较大,强调了学生整合知识的能力,以及对信息的分析、提炼、加工、运用的能力.1年前查看全部
- 2011年3月11日,日本大地震引起发福岛核电站核泄漏,其中一种主要放射性元素碘-131.碘-131的原子核内质子数为5
2011年3月11日,日本大地震引起发福岛核电站核泄漏,其中一种主要放射性元素碘-131.碘-131的原子核内质子数为53,质子数和中子数之和是131,则下列关于该原子的说法错误的是( )
A.核外电子数为53
B.一个该原子的质量是131g
C.相对原子质量为131
D.中子数为78 卡内齐1年前1
卡内齐1年前1 -
 bluemoon7783 共回答了11个问题
bluemoon7783 共回答了11个问题 |采纳率100%解题思路:在原子中,核内质子数=核电荷数=核外电子数,相对原子质量=质子数+中子数,相对原子质量是原子的相对的质量,不是实际质量,据此分析解答即可;A、在原子中,核内质子数=核电荷数=核外电子数,故其核外电子数是53;
B、由题意知该原子的相对原子质量是131,不是原子的实际质量是131g.
C、原子中相对原子质量=质子数+中子数,故由题意知该原子的相对原子质量为131;
D、已知碘-131的原子核内质子数为53,质子数与中子数之和为131,则中子数是131-53=78;
故选:B.点评:
本题考点: 原子的有关数量计算.
考点点评: 熟练掌握在原子中的两个等量关系:原子序数=质子数=核外电子数=核电荷数和相对原子质量=质子数+中子数,常是解决此类问题的关键;1年前查看全部
- 碘-131是如何产生的?
 sangyeqing1年前1
sangyeqing1年前1 -
 nivana999 共回答了17个问题
nivana999 共回答了17个问题 |采纳率82.4%放射性核燃料在衰变过程中,会转变为多种物质.其中就有碘131,碘131易于挥发,又易溶于水,所以就扩散开来,也不是稳定的碘,具有放射性,所以检测其扩散情况就是检测了核辐射的扩散情况1年前查看全部
- 2011年3月,日本海啸引发福岛第一核电站的放射性物质外泄,有关131I(碘-131,即131I原子中含有53个质子,7
2011年3月,日本海啸引发福岛第一核电站的放射性物质外泄,有关131I(碘-131,即131I原子中含有53个质子,78个中子)的相关报道成为热门话题.请回答下列问题:
(1)131I原子的核外电子数为______.
(2)自然界中普遍存在另一种稳定的碘原子127I,它和131I同属于碘元素.127I原子的质子数为______.
(3)食盐中常添加碘酸钾(KIO3)以补充碘元素.已知KIO3中钾元素的化合价为+1,其中碘元素的化合价为______. rr苹果落地1年前1
rr苹果落地1年前1 -
 都市放狗人 共回答了15个问题
都市放狗人 共回答了15个问题 |采纳率80%解题思路:(1)根据原子中质子数=核外电子数回答.
(2)根据元素的种类是由质子数决定的回答.
(3)根据在化合物中正负化合价代数和为零,进行解答.(1)131I原子中含有53个质子,根据原子中质子数=核外电子数,131I原子的核外电子数为53.
(2)由于元素的种类是由质子数决定的,碘原子127I和131I同属于碘元素,131I原子中含有53个质子,故127I原子的质子数为53.
(3)根据在化合物中正负化合价代数和为零,在KIO3中钾元素的化合价为+1价,氧元素的化合价为-2价,设KIO3中碘的化合价为x,则(+1)+x+(-2)×3=0,解得 x=+5.
故答案为:(1)53;(2)53;(3)+5.点评:
本题考点: 原子的有关数量计算;有关元素化合价的计算.
考点点评: 掌握原子中的两个等量关系:核电荷数=质子数=电子数、相对原子质量=质子数+中子数,并能够熟练的应用.1年前查看全部
- 2011年3月,日本强烈地震后,海啸引发福岛第一核电站的放射性物质外泄,有关131I(碘-131)的相关报道成为热门话题
2011年3月,日本强烈地震后,海啸引发福岛第一核电站的放射性物质外泄,有关131I(碘-131)的相关报道成为热门话题.请回答下列问题:
(1)131I原子中含有53个质子,78个中子.
①131I原子的核外电子数为______.
②自然界中普遍存在另一种稳定的碘原子127I,它和131I同属于碘元素.127I原子的质子数为______.
(2)专家指出,服用碘片(有效成分为KI)可以治疗131I造成的辐射,但服用碘酒(有效成分为I2)却会引起碘中毒.KI和I2的性质不同的原因是______.
(3)针对上述事件下列说法错误的是______.
A.科学、安全地利用核能B.充分利用风能、地热能和太阳能
C.尽可能多使用石油、煤等化石能源D.寻找可循环利用的生物能源. antemei888841年前1
antemei888841年前1 -
 缚茧 共回答了13个问题
缚茧 共回答了13个问题 |采纳率100%解题思路:(1)①根据原子中质子数=核外电子数回答.②根据元素的种类是由质子数决定的回答.
(2)根据物质的结构决定物质的性质回答.
(3)根据叙述的内容的优缺点分析解答;(1)①131I原子中含有53个质子,根据原子中质子数=核外电子数,131I原子的核外电子数为53.
②由于元素的种类是由质子数决定的,碘原子127I和131I同属于碘元素,故127I原子的质子数为53.
(2)物质的性质是由物质的结构决定的,KI和I2的性质不同是因构成物质的微粒(分子)不同.
(3)A、科学、安全地利用核能可有效的防止核泄露的危害,故正确;
B、风能、地热能和太阳能是新型能源,新型能源的使用可有效地缓解能源紧张且保护环境;
C、大量使用石油、煤等化石能源会造成严重的环境污染,故错误;
D、寻找可循环利用的生物能源,可有效地缓解能源紧张且保护环境;
故答案为:(1)①53;②53;(2)构成物质的微粒(分子)不同;(3)C;点评:
本题考点: 原子的有关数量计算;资源综合利用和新能源开发.
考点点评: 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.学生分析问题的思维跨度较大,强调了学生整合知识的能力,以及对信息的分析、提炼、加工、运用的能力.1年前查看全部
- 日本福岛第一核电站发生核泄漏释放出放射性-碘131( 13153I).下列关于碘-131说法正确的是( )
日本福岛第一核电站发生核泄漏释放出放射性-碘131(
I).下列关于碘-131说法正确的是( )13153
A.质子数为l31
B.中子数为53
C.电子数为78
D.与
I互为同位素12753 茉莉冰蓝1年前1
茉莉冰蓝1年前1 -
 云卷云舒88 共回答了21个问题
云卷云舒88 共回答了21个问题 |采纳率85.7%解题思路:根据原子符号的左下角表示质子数,左上角表示质量数,中子数=质量数-质子数,核外电子数等于核内质子数;质子数相同中子数不同的同一元素互称同位素.碘131(
13153I)的质子数为53,质量数为131,中子数=质量数-质子数=131-53=78,核外电子数为53,
13153I与
12753I的质子数相同,中子数不同,互为同位素,所以A、B、C错误,
故选:D.点评:
本题考点: 质子数、中子数、核外电子数及其相互联系.
考点点评: 本题考查了质子数、中子数、质量数之间的关系,难度不大,注意元素符号周围各数字表示的含义.1年前查看全部
- 碘-131是一种放射性物质,在医疗诊断中常会用到它,下表是20克碘-131在4天内每天衰减的试验数据:
碘-131是一种放射性物质,在医疗诊断中常会用到它,下表是20克碘-131在4天内每天衰减的试验数据:
天数 0 1 2 3 4
剩余克数 20.0 18.34 16.82 15.42 14.14
7天后是否能保证有10克该物质用于治疗?请说明你的理由.
最好有过程.
用数列的过程来做。 fsm60461年前2
fsm60461年前2 -
 wx_46 共回答了22个问题
wx_46 共回答了22个问题 |采纳率81.8%第一天减少:1.66
第二天减少:1.52
第三天减少:1.4
第四天减少:1.28
由上面可以看出 从第三天起,每天比前一天减少的量是一个等差数列,首相是1.52,公差是 -0.12,∴第七天的量=20-前7天减少的总量
a6=1.52-5*0.12=0.92
第二天到第七天减少的总量=(1.52+0.92)*6/2
v =7.32
第七天的量=20-1.66-7.32=11.02(克) ∵11.02>10
七天后可以保证有10克该物质用于治疗!1年前查看全部
- 碘-131(质子数与中子数之和)具有放射性,对人体有害。而生活中的碘盐、碘酒所含的碘-127对人体无害。碘-131和碘-
碘-131(质子数与中子数之和)具有放射性,对人体有害。而生活中的碘盐、碘酒所含的碘-127对人体无害。碘-131和碘-127是同种元素的不同原子,核电荷数均为53。下列说法正确的是 [ ]
A.碘是一种金属元素
B.碘-127原子核外有74个电子
C.碘-131原子核内有78个质子
D.碘-131和碘-127核内中子数不同 曹志良1年前1
曹志良1年前1 -
 x000028 共回答了18个问题
x000028 共回答了18个问题 |采纳率88.9%D1年前查看全部
- 据报道:日本大地震引发福岛核电站爆炸后泄漏出放射性物质碘-131.碘-131是质子数为53、中子数为78的一种碘原子,则
据报道:日本大地震引发福岛核电站爆炸后泄漏出放射性物质碘-131.碘-131是质子数为53、中子数为78的一种碘原子,则该原子的核电荷数为( ) A.53 B.78 C.131 D.184  xzsz1年前1
xzsz1年前1 -
 后胜明 共回答了19个问题
后胜明 共回答了19个问题 |采纳率89.5%由题意碘-131是质子数为53、中子数为78的一种碘原子,因为原子中,核电荷数=质子数=电子数,故该原子的核电荷数为为53.
故选A.1年前查看全部
- 日本大地震引发的福岛第一核电站核泄漏事故,造成放射性物质碘-131和铯-137( 13755Cs)向外界泄漏.
日本大地震引发的福岛第一核电站核泄漏事故,造成放射性物质碘-131和铯-137(
Cs)向外界泄漏.下列相关说法错误的是( )13755
A.每个
Cs原子中有82个中子13755
B.CsOH的碱性比KOH强
C.HI比HF还原性强
D.KIO3是碘的最高价含氧酸的盐 belinda1361年前1
belinda1361年前1 -
 wwjloveyou 共回答了19个问题
wwjloveyou 共回答了19个问题 |采纳率94.7%解题思路:A.中子数=质量数-质子数;
B.在周期表中同主族从上到下金属性逐渐增强;
C.单质的氧化性越强则离子的还原性越弱;
D.碘最外层有7个电子,最高正价为+7价.A.55137Cs原子中质量数是137,质子数是55,中子数=质量数-质子数=137-55=82,故A正确;
B.在周期表中同主族从上到下金属性逐渐增强,金属性越强对应的氢氧化物的碱性越强,故B正确;
C.卤素单质的氧化性强弱顺序为:F2>Cl2>Br2>I2,所以离子的还原性顺序为:F-<Cl-<Br-<I-,故C正确;
D.碘最外层有7个电子,最高正价为+7价,KIO3中碘的化合价为+5,故D错误.
故选D.点评:
本题考点: 核素;质量数与质子数、中子数之间的相互关系.
考点点评: 本题考查质量数与质子数、中子数之间的相互关系、碱性、还原性强弱的比较,难度不大,平时注意知识的积累.1年前查看全部
- (2011•开封一模)2011年3月日本大地震引发了核泄漏事故,核泄漏释放出了放射性碘-131,人体接触碘-131后可能
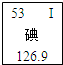 (2011•开封一模)2011年3月日本大地震引发了核泄漏事故,核泄漏释放出了放射性碘-131,人体接触碘-131后可能引发甲状腺疾病.碘元素在元素周期表中的信息如图所示,下列说法正确的是( )
(2011•开封一模)2011年3月日本大地震引发了核泄漏事故,核泄漏释放出了放射性碘-131,人体接触碘-131后可能引发甲状腺疾病.碘元素在元素周期表中的信息如图所示,下列说法正确的是( )
A.碘属于金属元素
B.质子数是126.9
C.相对原子质量是126.9g
D.原子序数是53 海狗肾人参酒1年前1
海狗肾人参酒1年前1 -
 希玄2 共回答了22个问题
希玄2 共回答了22个问题 |采纳率100%解题思路:由元素周期表可知:碘-131的质子数、元素种类、原子序数、相对原子质量等信息.A、右汉语名称可知,碘属于非金属元素,故A错误;
B、质子数=原子序数=53,而非126.9,故B错误;
C、相对原子质量是126.9,因为其单位为“1”,而非“g”,故C错误;
D、原子序数是53,说法正确,故D正确.
故选D.点评:
本题考点: 微粒观点及模型图的应用;原子的定义与构成;原子的有关数量计算;元素周期表的特点及其应用.
考点点评: 试题通过给出微粒的模型,考查学生的观察能力和对基本概念的理解与运用能力;了解原子的定义和构成:原子由原子核和核外电子构成,其中原子核由质子和中子构成的.1年前查看全部
- 1)碘-131 78中子,为什么?2)铜锈和稀硫酸反应方程式?
 yvonne291年前1
yvonne291年前1 -
 旧布娃娃82 共回答了16个问题
旧布娃娃82 共回答了16个问题 |采纳率87.5%1.质量数=质子数+中子数
中子数=质量数-质子数=131-53=78
2.Cu(OH)2CO3+H2SO4=CuSO4 + CO2↑+ H2O1年前查看全部
- (2011•河北)碘-131(质子数与中子数之和)具有放射性,对人体有害.而生活中的碘盐、碘酒所含的碘-127对人体无害
(2011•河北)碘-131(质子数与中子数之和)具有放射性,对人体有害.而生活中的碘盐、碘酒所含的碘-127对人体无害.碘-131和碘-127是同种元素的不同原子,核电荷数均为53.下列说法正确的是( )
A.碘是一种金属元素
B.碘-127原子核外有74个电子
C.碘-131原子核内有78个质子
D.碘-131和碘-127核内中子数不同 云枫雨1年前1
云枫雨1年前1 -
 highlo 共回答了19个问题
highlo 共回答了19个问题 |采纳率84.2%解题思路:A、碘是一种非金属元素.
B、碘的核外电子数是53.
C、碘原子核内部质子数是53.
D、131与127是质子数与中子数之和,两者质子数相同中子数一定不同.A、碘是一种非金属元素,符合非金属元素的书写特征,故此选项错误.
B、由于在原子中质子数等于电子数,所以碘的核外电子数是53,故此选项错误.
C、原子中质子数等于电子数等于核电荷数,所以碘原子核内部质子数是53,故此选项错误.
D、131与127是质子数与中子数之和,两者质子数相同中子数一定不同,故此选项正确.
故选D点评:
本题考点: 原子的定义与构成;元素的简单分类.
考点点评: 此题是一道原子知识的考查题,解题的关键是对原子内一些量的关系的了解.1年前查看全部
- (2011•肇庆二模)2011年3月11日,在日本福岛发生了震惊世界的核泄漏事件,关于核电站泄漏的放射性碘-131(53
(2011•肇庆二模)2011年3月11日,在日本福岛发生了震惊世界的核泄漏事件,关于核电站泄漏的放射性碘-131(53131I)、铯-137(55137Cs)的各种说法正确的是( )
A.碘-131的中子数为78
B.碘-131质量数为53
C.碘与铯互称同位素
D.铯-137的放射性是化学性质 地平线11年前1
地平线11年前1 -
 柯莹工作室 共回答了17个问题
柯莹工作室 共回答了17个问题 |采纳率88.2%解题思路:元素符号的左下角表示质子数,左上角表示质量数,中子数=质量数-质子数,质子数相同中子数不同的同一元素互称同位素,同位素必须是元素不是单质或化合物,放射性是元素的物理性质不是化学性质.A、碘-131的中子数=质量数-质子数=131-53=78,故A正确.
B、碘-131的质量数为131,故B错误.
C、碘和铯是不同的元素,所以不是同位素,故C错误.
D、铯-137的放射性是物理性质,故D错误.
故选A.点评:
本题考点: 质量数与质子数、中子数之间的相互关系;质子数、中子数、核外电子数及其相互联系.
考点点评: 本题考查了质子数、中子数、质量数之间的关系,难度不大,注意元素符号周围各数字表示的含义.1年前查看全部
- 2011年3月,日本强烈地震后,海啸引发福岛第一核电站的放射性物质外泄,有关131I(碘-131)的相关报道成为热门话题
2011年3月,日本强烈地震后,海啸引发福岛第一核电站的放射性物质外泄,有关131I(碘-131)的相关报道成为热门话题.请回答下列问题:
(1)131I原子中含有53个质子,78个中子.自然界中普遍存在另一种稳定的碘原子127I,它和131I同属于碘元素.127I原子的质子数为______.
(2)专家指出,服用碘片(有效成分为KI)可以治疗131I造成的辐射,但服用碘酒(有效成分为I2)却会引起碘中毒.KI和I2的性质不同的原因是______.
(3)日本地震后,个别居民抢购食盐.假设某人经医生确认,每日需要补充166mg KI.已知每千克某品牌碘盐中KIO3的加入量为42.8mg,如果用该食盐替代碘片提供治疗辐射所需的碘元素,则每日需食用该食盐的质量为______kg. 55583681年前1
55583681年前1 -
 buaaiegsxc 共回答了24个问题
buaaiegsxc 共回答了24个问题 |采纳率91.7%解题思路:(1)根据元素的种类是由质子数决定的回答;(2)根据物质的结构决定物质的性质回答;(3)根据每日需要补充166mgKI的质量计算所需碘元素的质量,根据碘元素的质量求出碘酸钾的质量,再根据已知每千克某品牌碘盐中KIO3的加入量为42.8mg计算碘盐的质量.(1)由于元素的种类是由质子数决定的,碘原子127I和131I同属于碘元素,故127I原子的质子数为53;
(2)物质的性质是由物质的结构决定的,KI和I2的性质不同是因构成物质的微粒不同;
(3)每日需要补充166mg KI,则含碘元素的质量为166mg×[127/39+127]×100%═127mg;
则需碘酸钾127mg÷[127/39+127+16×3]×100%=214mg,已知每千克某品牌碘盐中KIO3的加入量为42.8mg,故每日需食用该食盐的质量为214mg÷42.8mg/kg=5kg.(根据计算结果可以看出,利用加碘食盐来防辐射是不可行的,因为人不能吃那么多的食盐).
故答案为:(1)53;(2)构成物质的微粒不同;(3)5.点评:
本题考点: 元素的概念;利用分子与原子的性质分析和解决问题;化合物中某元素的质量计算.
考点点评: 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.学生分析问题的思维跨度较大,强调了学生整合知识的能力,以及对信息的分析、提炼、加工、运用的能力.1年前查看全部
- 铯-134,铯-137,碘-131和碳-12一样,属于A.分子 B.单质 C.原子 D.离子 为什么?
 tt数码1年前3
tt数码1年前3 -
 成森林 共回答了20个问题
成森林 共回答了20个问题 |采纳率85%应选C,应为铯-134,铯-137,碘-131和碳-12都是同位素.同位素是具有相同质子数,不同中子数(或不同质量数)同一元素的不同核素的互称.1年前查看全部
- (2011•雅安)2011年3月,日本强烈地震后,海啸引发福岛第一核电站的放射性物质外泄,有关131I(碘-131)的相
(2011•雅安)2011年3月,日本强烈地震后,海啸引发福岛第一核电站的放射性物质外泄,有关131I(碘-131)的相关报道成为热门话题.请回答下列问题:
(1)131I原子中含有53个质子,78个中子.
①131I原子的核外电子数为______.
②自然界中普遍存在另一种稳定的碘原子127I,它和131I同属于碘元素.127I原子的质子数为______.
(2)专家指出,服用碘片(有效成分为KI)可以治疗131I造成的辐射,但服用碘酒(有效成分为I2)却会引起碘中毒.KI和I2的性质不同的原因是______.
(3)日本地震后,个别居民抢购食盐.假设某人经医生确认,每日需要补充166mg KI.已知每千克某品牌碘盐中KIO3的加入量为42.8mg,如果用该食盐替代碘片提供治疗辐射所需的碘元素,则每日需食用该食盐的质量为______kg. skyhouse991年前1
skyhouse991年前1 -
 shenbo19830723 共回答了22个问题
shenbo19830723 共回答了22个问题 |采纳率95.5%解题思路:(1)①根据原子中质子数=核外电子数回答.
②根据元素的种类是由质子数决定的回答.
(2)根据物质的结构决定物质的性质回答.
(3)根据每日需要补充166mgKI的质量计算所需碘元素的质量,根据碘元素的质量求出碘酸钾的质量,再根据已知每千克某品牌碘盐中KIO3的加入量为42.8mg计算碘盐的质量.(1)①131I原子中含有53个质子,根据原子中质子数=核外电子数,131I原子的核外电子数为53.
②由于元素的种类是由质子数决定的,碘原子127I和131I同属于碘元素,故127I原子的质子数为53.
(2)物质的性质是由物质的结构决定的,KI和I2的性质不同是因构成物质的微粒(分子)不同.
(3)每日需要补充166mg KI,则含碘元素的质量为166mg×
127
39+127×100%═127mg;
则需碘酸钾127mg÷
127
39+127+16×3×100%=214mg,已知每千克某品牌碘盐中KIO3的加入量为42.8mg,故每日需食用该食盐的质量为214mg÷42.8mg/kg=5kg.(根据计算结果可以看出,利用加碘食盐来防辐射是不可行的,因为人不能吃那么多的食盐)
故答案为:
(1)①53;②53;
(2)构成物质的微粒(分子)不同(要点是“结构不同”);
(3)5.点评:
本题考点: 人体的元素组成与元素对人体健康的重要作用;原子的定义与构成;混合物中某元素的质量计算.
考点点评: 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.学生分析问题的思维跨度较大,强调了学生整合知识的能力,以及对信息的分析、提炼、加工、运用的能力.1年前查看全部
- (2011•翔安区质检)碘-131是人工合成的一种放射性同位素,它在元素周期表的信息如图所示,下列关于碘-131的说法不
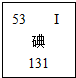 (2011•翔安区质检)碘-131是人工合成的一种放射性同位素,它在元素周期表的信息如图所示,下列关于碘-131的说法不正确的是( )
(2011•翔安区质检)碘-131是人工合成的一种放射性同位素,它在元素周期表的信息如图所示,下列关于碘-131的说法不正确的是( )
A.元素符号为I
B.质子数为53
C.中子数为131
D.其-1价离子可表示为I- zhuzi_01年前1
zhuzi_01年前1 -
 强者zz 共回答了26个问题
强者zz 共回答了26个问题 |采纳率100%解题思路:根据图中元素周期表可以获得的信息:原子序数、相对原子质量、元素符号、元素种类等,元素符号左边的数字表示原子序数,元素名称下方的数字表示相对原子质量,进行分析判断即可.A、根据元素周期表中的一格中获取的信息,该元素的元素符号为I,故选项说法正确.
B、根据元素周期表中的一格中获取的信息,该元素的原子序数为53;根据原子序数=核电荷数=质子数,则该元素的质子数为53,故选项说法正确.
C、根据元素周期表中的一格中获取的信息,可知元素的相对原子质量为131,而不是中子数为131,故选项说法错误.
D、离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,其-1价离子可表示为I-,故选项说法正确.
故选C.点评:
本题考点: 元素周期表的特点及其应用.
考点点评: 本题难度不大,考查学生灵活运用元素周期表中元素的信息及辨别元素种类的方法进行分析解题的能力.1年前查看全部
- 放射性核素,比如碘-131半衰期是8.3天,要完全衰变玩需要多长时间,计算公式是什么
 barbara111年前1
barbara111年前1 -
 dongyu1155 共回答了25个问题
dongyu1155 共回答了25个问题 |采纳率88%完全衰变完在理论上是不可能的,并非经过两个半衰期所有辐射都将消失.放射性是一种概率现象,每经过一个半衰期,初始原子会消失50%,即辐射的危险会降低一半,但还能延续很多个半衰期.只要还有最后一个放射性原子,辐射就不可能完全消失.不过通常来说,在经过30个半衰期后,辐射已减至原来的十亿分之一,基本无法被探测到,也就没有危害了.
计算:经过N个半衰期后剩余的放射性原子为1/2的N次幂.1年前查看全部
- 2011年3月,日本强烈地震后,海啸引发福岛第一核电站的放射性物质外泄,有关131I(碘-131)的相关报道成为热门话题
2011年3月,日本强烈地震后,海啸引发福岛第一核电站的放射性物质外泄,有关131I(碘-131)的相关报道成为热门话题.请回答下列问题:
(1)131I原子中含有53个质子,78个中子.
①131I原子的核外电子数为______.
②自然界中普遍存在另一种稳定的碘原子127I,它和131I同属于碘元素.127I原子的质子数为______.(1分)
(2)专家指出,服用碘片(有效成分为KI)可以治疗,但服用碘酒(有效成分为I2)却会引起碘中毒.KI和I2的性质不同的原因是______.(1分)
(3)假设某人经医生确认,每日需要补充166mg KI.试计算
①KI的相对分子质量是多少?(1分)
②KI中钾元素、碘元素的质量比是多少?(2分)
③KI中碘元素的质量分数是多少?(计算结果精确到0.1%)(2分)
④该人每天补充碘元素的质量为多少?(2分) 特警ss1年前1
特警ss1年前1 -
 风一直吹666 共回答了16个问题
风一直吹666 共回答了16个问题 |采纳率75%解题思路:(1)根据在原子中,核内质子数=核外电子数,同种元素的原子质子数相同分析填空.
(2)根据构成物质的微粒分析物质的性质,结构决定性质.
(3)①依据相对分子质量等于各元素相对原子质量之和求解;
②依据物质中元素的质量比等于各元素相对原子质量和的比解决;
③依据物质中元素的质量分数=[该元素相对原子质量之和/该物质的相对分子质量]×100%分析解决;
④依据元素的质量等于物质的质量与该元素的质量分数的乘积解决;(1)①在原子中,核内质子数=核外电子数,由于131I原子中含有53个质子,所以131I原子的核外电子数为53;
②同种元素的原子质子数相同,131I原子中含有53个质子,所以127I原子的质子数为53.
(2)物质的结构决定物质的性质,碘酒中的碘是由碘分子构成的,KI中的碘是碘离子,构成物质的微粒不同,所以,KI和I2的性质不同.
(3)①由相对分子质量等于各元素相对原子质量之和可知:KI的相对分子质量是39+127=166;
②由物质中元素的质量比等于各元素相对原子质量和的比可知:KI中钾元素、碘元素的质量比是39:127
③因为物质中元素的质量分数=[该元素相对原子质量之和/该物质的相对分子质量]×100%,所以KI中碘元素的质量分数=[127/166]×100%=76.5%;
④因为元素的质量等于物质的质量与该元素的质量分数的乘积;所以该人每天补充碘元素的质量=166mg×[127/166]×100%=127mg
故答案为:(1)53;53;(2)构成物质的微粒不同;
(3)答:①KI的相对分子质量是166;
②KI中钾元素、碘元素的质量比是39:127;
③KI中碘元素的质量分数是76.5%;
④该人每天补充碘元素的质量为127mg;点评:
本题考点: 原子的有关数量计算;元素的概念;相对分子质量的概念及其计算;元素质量比的计算;元素的质量分数计算;化合物中某元素的质量计算.
考点点评: 本题主要考查了与碘元素有关的问题,重点是对学生运用所学化学知识解决实际问题能力的训练.强调了学生整合知识的能力,以及对信息的分析、提炼、加工、运用的能力.1年前查看全部
- 2011年3月11日,日本发生里氏9.0级大地震.地震中引发了福岛核电站的核泄漏,碘-131是本次核泄漏事件中的放射性核
 2011年3月11日,日本发生里氏9.0级大地震.地震中引发了福岛核电站的核泄漏,碘-131是本次核泄漏事件中的放射性核素之一,被人体吸入后可能引发甲状腺疾病.碘在元素周期表中如右图所示.下列说法正确的是( )
2011年3月11日,日本发生里氏9.0级大地震.地震中引发了福岛核电站的核泄漏,碘-131是本次核泄漏事件中的放射性核素之一,被人体吸入后可能引发甲状腺疾病.碘在元素周期表中如右图所示.下列说法正确的是( )
A.加碘食盐中的碘的含量很高,家中应立即储备很多
B.碘原子的质子数是53
C.碘-131的质子数为131
D.碘元素的相对原子质量是126.9 g 朵朵1411年前1
朵朵1411年前1 -
 711448 共回答了20个问题
711448 共回答了20个问题 |采纳率95%解题思路:根据元素周期表中的一个小格所提供的信息是原子序数.元素符号.元素名称.相对原子质量,解答本题.A、加碘食盐中的碘的含量很低,家中应储备很多食盐无实际意义;
B、由图示可知碘的原子序数是53,所以其质子数也是53;
C、碘-131是碘元素的一种,所以其质子数也是53;
D、相对原子质量的单位是“1”不能是克,所以由图示可知碘元素的相对原子质量是126.9;
故选B点评:
本题考点: 元素周期表的特点及其应用.
考点点评: 该题是对元素周期表意义的考查,是对元素周期表中的一个小格信息灵活应用能力的训练,属于基础性知识考查题.1年前查看全部
- 2011年3月,日本海啸引发福岛第一核电站的放射性物质外泄,有关 131 I(碘-131)的相关报道成为热门话题.请回答
2011年3月,日本海啸引发福岛第一核电站的放射性物质外泄,有关 131 i(碘-131)的相关报道成为热门话题.请回答下列问题:
(1)碘元素在体内发挥重要作用,但过量补碘也会引起甲亢等疾病.目前***各地检测出的 131 i含量很小,根据京津等地检出的数值,吃上2000kg的菠菜才相当于照一张x光片的辐射量.根据以上资料分析,下列说法正确的是______.
a.盲目服用碘片等预防辐射对身体可能造成负面作用
b.我们应尽可能主动多摄入含碘食品,多多益善
c.以目前***检测出的 131 i含量来看,对身体健康影响很小,不必恐慌
(2) 131 i原子中含有53个质子,78个中子. 131 i原子的核外电子数为______.
(3)专家指出,服用碘片(有效成分为ki)可以治疗 131 i造成的辐射,但服用碘酒(有效成分为i 2 )却会引起碘中毒.ki和i 2 性质的不同的原因是______.
(4)①食盐中常添加碘酸钾(kio 3 )以补充碘元素.已知kio 3 中钾元素的化合价为+1,其中碘元素的化合价为______.
②服用碘片治疗 131 i辐射的推荐服用剂量是每日摄入ki为130-170mg,假设服用某碘片每日补充166mg ki.已知每千克某品牌碘盐中kio 3 的加入量为42.8mg,如果用该食盐替代碘片提供治疗辐射所需的碘元素,则每日需食用该食盐的质量为______kg. 路扬1011年前1
路扬1011年前1 -
 苍南小白 共回答了19个问题
苍南小白 共回答了19个问题 |采纳率89.5%(1)由题中信息可知过量服碘对身体无益,少量辐射对人体无害.
(2)原子中质子数等于电子数,其质子数是53,核外电子数也是53.
(3)结构决定性质,KI和I 2 性质的不同,是因为其构成的微粒不同导致的.
(4)①已知KIO 3 中钾元素的化合价为+1,氧的化合价为-2价,依据化合物中元素的化合价等于零可知碘的化合价是+5价.
②166mgKI中碘元素的质量为166mg×碘化钾中碘的质量分数=166×
127
166 =127mg
每千克食盐中含42.8mgKIO 3 中碘元素的质量为42.8mg×碘酸钾中碘的质量分数=42.8×
127
214 =25.4mg
要提供127mg碘元素,需要食盐的质量为
127
25.4 kg=5kg
故答案为:
(1)ac;
(2)①53,②53;
(3)构成物质的微粒(分子)不同;
(4)①+5;②5.1年前查看全部
大家在问
- 1光的三原色能混合为黑色吗?颜料的三原色能混合为白色吗
- 2(2009•深圳二模)如图所示,点电荷固定于Q点,一带电粒子仅在库仑力作用下,做以Q为焦点的椭圆运动.M、N为椭圆长轴的
- 3甲乙两车分别同时从相距20千米的A、B两地背向而行,甲每小时行80千米,是乙车速度的2倍,两车开出后5小时相距多少千米?
- 4汽车前杠中的有一个小小的正方形的东西有什么作用
- 5“永远的舞者”英文怎么写
- 6下列加点字解释有误的一项是( ) A.不违农时,谷不可胜食也(尽) B.此所谓战胜于朝
- 71的7.8796584652倍数是多少?
- 8Don’t worry. I’ll help to ______ the guests. A.host B.hold C
- 9根据对话内容, 选择恰当的句子补全下列对话。(每小题1分,共5分)
- 10车以8米每秒的速度运动~一个人在车上发射子弹,子弹的初速度是4米每秒,运动了10秒~子弹的水平位移是多少
- 11诗歌至今有多少年历史?
- 12在复摆的某一位置加一配重时,其振动周期将如何变化
- 13函数y=x+2/x+1图象的对称中心是_____.
- 14一般不会造成水污染的是( ) A.合理放养鱼虾等水产品 B.工厂排放没有经过处理的废水 C.大量的生活污水流入河流 D
- 15,△AOB中,OA=OB,∠AOB=90°,AD平分∠OAB交OB于D,OE⊥AD交AB于E,垂足为F求(AD-OE)÷
