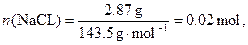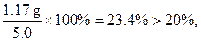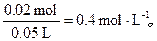谷氨酸钠中钠含量为13.5%,吃一克无盐味精(谷氨酸钠99.9%),不也吃了0.5克的盐了?
 getget7142022-10-04 11:39:541条回答
getget7142022-10-04 11:39:541条回答谷氨酸钠——169,钠——23,氯——36
谷氨酸钠中钠含量为13.5%,如果折算为氯化钠相对于:谷氨酸钠中氯化钠含量为54%,这样吃一克无盐味精(谷氨酸钠99.9%),不也吃了0.5克的盐了?
当味精溶于水(或唾液)时,它会迅速电离为***的钠离子和谷氨酸盐离子。每人每天盐量应不超过6克,是钠离子还是氯离子的问题?胃酸中氯离子应该很多吧?

已提交,审核后显示!提交回复
共1条回复
 wuchiju 共回答了17个问题
wuchiju 共回答了17个问题 |采纳率82.4%- 谷氨酸钠里仅仅是钠元素,你要折算成氯化钠的话,在研究物质中钠含量的时候是可以的,但是食盐是氯化钠,只有钠元素没有氯是不能等同于氯化钠的.只能说吃一克无盐味精也就是吃了0.135克钠元素!
- 1年前
相关推荐
- 味精是烹调菜肴时常用的调味剂,其主要成份是谷氨酸钠.谷氨酸钠有鲜味,易溶于水.小靖发现某品牌味精包装上标注:“谷氨酸钠含
味精是烹调菜肴时常用的调味剂,其主要成份是谷氨酸钠.谷氨酸钠有鲜味,易溶于水.小靖发现某品牌味精包装上标注:“谷氨酸钠含量≥80%,氯化钠含量≤20%”.他想测定此味精中的NaCl的含量(谷氨酸钠的存在不影响NaCl的性质).
(1)下面是他所做实验的有关步骤,请补全实验步骤②.
①称取该味精样品5.0g,并溶于蒸馏水;
②加入过量的______溶液;
③过滤;
④用蒸馏水反复洗涤沉淀多次;
⑤将沉淀烘干、称量,测得固体质量为2.87g.
(2)根据上述实验步骤回答下列有关问题:
①过滤操作中所需要的仪器除了烧杯、铁架台(带铁圈)、玻璃棒外,还需要______;
②检验沉淀是否洗净的方法是______.
③此样品中NaCl的质量分数为______,是否符合其包装上标注的标准?______.
(3)味精的鲜味与溶液的酸碱度有关,当pH为6~7时鲜味最强;味精的鲜味还与温度有关,其水溶液经120℃以上长时间加热,不仅鲜味消失,而且对人体有害.因此试想一下,使用味精时应注意哪些问题?(2条即可)______. 17楼的猫1年前1
17楼的猫1年前1 -
 hhhbdh 共回答了26个问题
hhhbdh 共回答了26个问题 |采纳率73.1%(1)②需要将氯化钠转化为沉淀,通过沉淀的质量以及方程式中的比例关系,计算氯化钠的质量,故答案为:AgNO 3 ;
(2)①过滤操作除了题中提供的仪器外,还需要漏斗,故答案为:漏斗(带滤纸);
②只要检验洗涤液中的成分,就可以判断是否会洗净,故答案为:向洗涤液中滴加NaCl溶液,如果没有沉淀产生,则说明已洗净;
③设样品中的氯化钠为X,
NaCl+AgNO 3 =AgCl↓+NaNO 3
58.5 143.5
x 2.87g
58.5
X =
143.5
2.87g
x=1.17g,
氯化钠的质量分数:
1.17
5 ×100%=23.4%,而氯化钠的质量分数≤20%,故答案为:23.4%,不符合;
(3)味精的鲜味在pH为6~7时鲜味最强,味精水溶液经120℃以上长时间加热,不仅鲜味消失,而且对人体有害,故答案为:加味精时,尽量控制酸碱性呈中性或弱酸性;加味精应在起锅前.1年前查看全部
- (2005•资阳区)味精是谷氨酸钠和氯化钠混合的一种调味剂.某品牌味精包装袋上有如图所示的内容.学校初三“学化学、用化学
(2005•资阳区)味精是谷氨酸钠和氯化钠混合的一种调味剂.某品牌味精包装袋上有如图所示的内容.学校初三“学化学、用化学”兴趣小组同学,设想通过测定味精中NaCl的含量,来探究该味精的有效成分谷氨酸钠是否大于或等于80%的标注含量.他们的实验操作是:用天平准确称量5.88g该味精样品,全部溶解于适量水中,滴加足量的AgNO3溶液,再加入少量稀硝酸(排除杂质干扰检测),将产生的沉淀过滤、洗涤、干燥、称量,得到白色固体AgCl 2.87g.
请你根据他们获得的实验数据,完成探究活动最后的数据分析(要有分析过程)、结果判断工作,最终得出正确的判断结果.XX牌味精
成分:谷氨酸钠(C5H7NO4Na2)≥80%
氧化钠(NaCl)≤20%
净重:100g
生产日期:XX年X月X日
XX味精厂 雨夜清枫1年前1
雨夜清枫1年前1 -
 楚楚爱穆乖 共回答了18个问题
楚楚爱穆乖 共回答了18个问题 |采纳率83.3%解题思路:根据反应的化学方程式,可由生成沉淀氯化银的质量计算出该味精产生中所含氯化钠的质量,味精样品的质量与所计算氯化钠的质量差即为样品中谷氨酸钠的质量,用谷氨酸钠的质量与样品质量比可计算出该味精的有效成分谷氨酸钠的含量,用该含量与包装袋中所标注含量对比,判断谷氨酸钠是否大于或等于80%的标注含量.设味精氯化钠的质量为x
NaCl+AgNO3═AgCl↓+NaNO3
58.5 143.5
x 2.87g
[58.5/x]=[143.5/2.87g] x=1.17g
该味精的有效成分谷氨酸钠的质量分数=[5.88g−1.17g/5.88g]×100%=80.10%>80%
因此,味精的有效成分谷氨酸钠为80.10%,符合包装袋上谷氨酸钠≥80%的标注含量
答:味精的有效成分谷氨酸钠为80.10%,符合包装袋上谷氨酸钠≥80%的标注含量.点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 把化学方程式的计算与生活用品相结合,用计算结果判断生活用品标注是否符合实际,使计算具有现实意义.1年前查看全部
- (2014•淮北模拟)味精是调味料的一种,主要作用是增加食品的鲜味,它的主要成分是谷氨酸钠(C5H8NO4Na).下列关
(2014•淮北模拟)味精是调味料的一种,主要作用是增加食品的鲜味,它的主要成分是谷氨酸钠(C5H8NO4Na).下列关于谷氨酸钠的说法正确的是( )
A.谷氨酸钠中碳、氢、氧、氮元素的个数比为5:8:4:l
B.谷氨酸钠属于化合物
C.一个谷氨酸钠分子中含有4个氢分子
D.谷氨酸钠的相对分子质量为169g professorl1年前1
professorl1年前1 -
 想去云游 共回答了20个问题
想去云游 共回答了20个问题 |采纳率75%A.元素是个宏观概念,只讲种类,不讲个数,故错误;
B.由谷氨酸钠(C5H8NO4Na)的化学式可知,它是由五种元素组成的纯净物,属于化合物,故正确;
C.由谷氨酸钠(C5H8NO4Na)的化学式可知,1个谷氨酸分子中含有5个碳原子、8个氢原子、1个氮原子、4个氧原子和1个钠原子,不存在氢分子,故错误;
D.相对分子质量的单位是“1”,通常省略,而不是“g”,故错误.
故选B.1年前查看全部
- 化学式是C5H8NONa)若某品牌味精包装上标注:8.5克谷氨酸钠谷氨酸钠中C.H.N.O.Na的原子个数比为?拜托各位
 空山灵雨08711年前1
空山灵雨08711年前1 -
 crystalftt 共回答了17个问题
crystalftt 共回答了17个问题 |采纳率94.1%原子个数比只和化学式有关,和质量无关.所以C.H.N.O.Na的原子个数比为5:8:1:1:11年前查看全部
- 在制备味精的时候,将谷氨酸钠水溶液制成晶体,需要浓缩和流加,具体怎么操作呢?
 短暂如爱1年前1
短暂如爱1年前1 -
 shuaipeng84823 共回答了23个问题
shuaipeng84823 共回答了23个问题 |采纳率87%流加,它是以分批加料为基础,间歇或连续地补加新鲜原料的一种加料方法.
操作从上面说明基本上就可以看的出来的1年前查看全部
- 如何分离谷氨酸钠和氯化钠
 专拍垃圾1年前1
专拍垃圾1年前1 -
 tommyqiu 共回答了30个问题
tommyqiu 共回答了30个问题 |采纳率93.3%化学方法:谷氨酸钠是一种氨基酸盐,所以利用强酸制弱酸的原理,可用谷氨酸钠和浓醋酸反应得到谷氨酸,谷氨酸常温下在水中溶解度很小,所以可得到结晶沉淀.而氯化钠和浓醋酸混合无明显现象.将其过滤干燥就行了1年前查看全部
- (2009•普宁市一模)谷氨酸钠是味精的主要成分.研究表明,味精的鲜味与溶液的酸碱度有关系,当pH为6-7时,鲜味最好;
(2009•普宁市一模)谷氨酸钠是味精的主要成分.研究表明,味精的鲜味与溶液的酸碱度有关系,当pH为6-7时,鲜味最好;另外,还与温度有关,其水溶液经120℃以上长时间加热,不仅鲜味消失,而且会生成对身体有害的焦谷氨酸钠.对下列说法不正确的是( )
A.谷氨酸钠能溶于水
B.谷氨酸钠在加热条件下生成焦谷氨酸钠是物理变化
C.菜烧熟起锅后再加味精比炒菜过程中加味精更有利于人体健康
D.加入味精时,应避免在酸性较强或碱性较强的条件下使用 火辣辣的PBJ1年前1
火辣辣的PBJ1年前1 -
 644632826 共回答了17个问题
644632826 共回答了17个问题 |采纳率100%解题思路:A、由题中信息可以知道谷氨酸钠能够形成水溶液,可以据此判断;
B、味精在高温条件下容易发生化学变化;
C、谷氨酸钠在温度较低的条件下较稳定,可以据此解答;
D、根据题意可以知道谷氨酸钠在中性或弱酸性的环境中鲜味更好,可以据此解答.A、由题中信息可以知道谷氨酸钠能够形成水溶液,所以可以判断谷氨酸钠能够溶于水,故A说法正确;
B、味精在高温条件下容易发生化学变化而生成焦谷氨酸钠,故B说法错误;;
C、谷氨酸钠在温度较低的条件下较稳定,所以菜烧熟起锅后再加味精比炒菜过程中加味精更有利于人体健康,故C说法错误;
D、根据题意可以知道谷氨酸钠在中性或弱酸性的环境中鲜味更好,所以加入味精时,应避免在酸性较强或碱性较强的条件下,故D说法正确.
故选B.点评:
本题考点: 化学性质与物理性质的差别及应用;溶液的酸碱性与pH值的关系;化学变化和物理变化的判别.
考点点评: 化学来源于生产、生活,也服务于生产、生活,与生产、生活相关的化学知识,关乎我们的生存、健康和社会的发展,是中考热点之一.1年前查看全部
- 谁知道味精的主要成分谷氨酸钠的化学式 谢谢
 analyoo1年前1
analyoo1年前1 -
 szjsz 共回答了13个问题
szjsz 共回答了13个问题 |采纳率84.6%C5H8NO4Na1年前查看全部
- (2010•永春县质检)调味品味精中的主要成分为谷氨酸钠,化学式为C5H8NO4Na,,谷氨酸钠中氮、氢、氧各元素的质量
(2010•永春县质检)调味品味精中的主要成分为谷氨酸钠,化学式为C5H8NO4Na,,谷氨酸钠中氮、氢、氧各元素的质量比为=______;谷氨酸钠的相对分子质量为______,其中Na的质量分数为______.
 爱在荒野1年前1
爱在荒野1年前1 -
 都督xf 共回答了9个问题
都督xf 共回答了9个问题 |采纳率100%解题思路:根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比;
相对分子的质量为组成分子的各原子的相对原子质量之和;
物质中元素的质量分数=[该元素的相对原子质量×原子个数/该物质相对分子质量]×100%,进行解答.根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比;可得谷氨酸钠中氮、氢、氧各元素的质量比为 14:8:(16×4)=7:4:32;
根据相对分子的质量为组成分子的各原子的相对原子质量之和;可得谷氨酸钠的相对分子质量
为:12×5+1×8+14×1+16×4+23×1=169;
物质中元素的质量分数=[该元素的相对原子质量×原子个数/该物质相对分子质量]×100%,可得谷氨酸钠中Na的
质量分数为:[23/169]×100%=13.6%;
故答案为 7:4:32; 169; 13.6%.点评:
本题考点: 元素质量比的计算;相对分子质量的概念及其计算;元素的质量分数计算.
考点点评: 本题考查学生对物质中元素的质量比与元素的质量分数计算方法的掌握与在解题中的应用.1年前查看全部
- 味精(谷氨酸钠)属哪种晶体(共四种)
 qidshxian1年前1
qidshxian1年前1 -
 bigRookie 共回答了21个问题
bigRookie 共回答了21个问题 |采纳率81%离子晶体1年前查看全部
- 味精是烹制菜肴时常用的调味品,其主要成分是谷氨酸钠(化学式为C 5 H 8 NO 4 Na)。谷氨酸钠有鲜味,易溶于水。
味精是烹制菜肴时常用的调味品,其主要成分是谷氨酸钠(化学式为C 5 H 8 NO 4 Na)。谷氨酸钠有鲜味,易溶于水。某品牌味精包装上标注:“谷氨酸钠含量≥80%,NaCl含量<20%”。
某学校化学科研小组对此味精中NaCl的含量进行测定。
Ⅰ.查阅资料:谷氨酸钠的存在不影响NaCl含量的测定。
Ⅱ.设计实验方案:
(1)实验原理:通过味精与硝酸银反应生成氯化银的质量计算该味精中NaCl的质量分数。
(2)实验试剂:水、AgNO 3 溶液等
(3)实验过程: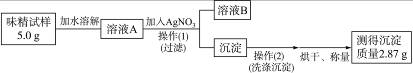
①操作(Ⅰ)所需要的玻璃仪器有____________________。
②通过计算判断该味精中NaCl的质量分数是__________,判断该味精中NaCl __________(填“符合”或“不符合”)其包装上标注的标准。
③若溶液A的体积为50 mL,则其中NaCl的物质的量浓度为____________________。 autoddedit1年前1
autoddedit1年前1 -
 csboyzheng 共回答了15个问题
csboyzheng 共回答了15个问题 |采纳率100%1年前查看全部
- (2012•丹阳市二模)味精是常用的调味品,它的鲜味来自于其中的主要成分“谷氨酸钠”(化学式是C5H8NO4Na,易溶于
(2012•丹阳市二模)味精是常用的调味品,它的鲜味来自于其中的主要成分“谷氨酸钠”(化学式是C5H8NO4Na,易溶于水,与AgNO3不反应),另外还含有NaCl(其他成分不考虑).某兴趣小组配制味精溶液并测定NaCl质量分数,请回答下列问题:
(1)称取5.0g味精配制成50g溶液,量取蒸馏水的量筒规格是BB(填字母).
A.10mL B.50mLC.100mL
(2)如图是配制过程,正确的操作顺序为②②→①①→④④→③③(填序号).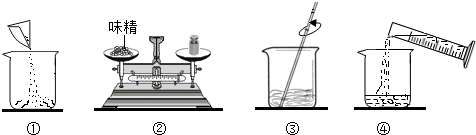
(3)为测定味精中NaCl的质量分数,进行如下实验:向所配制的50g溶液中加入过量的AgNO3溶液充分反应.检验沉淀是否完全的方法是:静置后,在上层清液中加入AgNO3AgNO3溶液(填化学式),观察是否有沉淀生成.过滤后,洗涤、干燥、称量沉淀并计算.
(4)计算后发现NaCl的质量分数偏低,则可能的原因是ABAB(填字母).
A.配溶液时仰视量水B.过滤时待滤液面高于滤纸边缘C.洗涤、干燥沉淀不彻底. woi5741年前1
woi5741年前1 -
 sherylkong 共回答了18个问题
sherylkong 共回答了18个问题 |采纳率94.4%解题思路:(1)根据溶液质量=溶质质量+溶剂质量,由5.0g味精配制成50g溶液,求出配制时所需水的量,然后选择量取蒸馏水的量筒;(2)根据使用固体物质配制溶液的步骤:计算、称量、溶解,判断实验操作图中操作的顺序;(3)溶液中的氯化钠与硝酸银溶液能发生化学反应,生成白色沉淀;可采取再滴加硝酸银溶液的方法,观察是否有沉淀,若无沉淀说明已经沉淀完全;(4)根据溶质的质量分数的计算公式可以知道,若质量分数偏小,则溶质少了,或是溶剂多了.可以据此解答.(1)取5.0g味精配制成50g溶液,则需要水的质量50g-5.0g=45g,45g水合45mL,因此需要选择50mL的量筒.故选B;
(2)图①为称量完毕的味精倒入烧杯,图②为称量味精的质量,图③为进行溶解,图④为量取水后倒入盛有味精的烧杯,因此,正确的操作顺序为②①④③,故答案为:②①④③
(3)氯化钠与硝酸银溶液能发生化学反应,生成白色沉淀,反应化学方程式为AgNO3+NaCl═AgCl↓+NaNO3;向清液中再滴加硝酸银溶液,若观察到无明显现象说明原来已经完全沉淀.故答案为:AgNO3
(4)A、用量筒量取水时仰视读数,则会使量取的液体偏大,从而使溶质的质量分数减小,故A可能;
B、过滤时滤液面高于滤纸边缘会导致测得的氯化银质量减小,从而导致计算出的溶质氯化钠减小,从而使溶质的质量分数减小,故B可能;
C、洗涤、干燥沉淀不彻底会导致测得的氯化银质量增大,从而导致计算出的溶质氯化钠增大,从而使溶质的质量分数增大,故B不可能.
故选AB.点评:
本题考点: 味精中食盐含量的探究;一定溶质质量分数的溶液的配制;盐的化学性质.1年前查看全部
- (2004•厦门)现在,专家否认了“味精致癌”的说法.实验表明,味精在100℃时加热半小时,只有0.3%的味精(谷氨酸钠
(2004•厦门)现在,专家否认了“味精致癌”的说法.实验表明,味精在100℃时加热半小时,只有0.3%的味精(谷氨酸钠)生成焦谷氨酸钠,其对人体的影响甚微.对此下列认识正确的是( )
A.谷氨酸钠受热不分解
B.谷氨酸钠在加热下生成焦谷氨酸钠是物理变化
C.大量食用味精有利于身体健康
D.实验是研究问题的一种有效方法 过路的1111年前1
过路的1111年前1 -
 likexxx_2001 共回答了14个问题
likexxx_2001 共回答了14个问题 |采纳率78.6%解题思路:谷氨酸钠的热稳定性差;
有新物质生成的变化属于化学变化;
大量、长期食用味精对人体有害;
实验是研究问题的最直接、最有效的方法.A、谷氨酸钠受热时能生成焦谷氨酸钠.故选项错误;
B、谷氨酸钠在加热下生成焦谷氨酸钠是化学变化.故选项错误;
C、大量食用味精不利于身体健康.故选项错误;
D、实验是研究问题的最直接、最有效的方法.故选项正确.
故选D.点评:
本题考点: 亚硝酸钠、甲醛等化学品的性质与人体健康;化学变化和物理变化的判别.
考点点评: 本题主要考查物质的性质和用途,物质具有多种性质,解答时应该理解物质的用途是由物质的哪种性质决定的.1年前查看全部
- 谷氨酸钠(MSG)鲜味剂的鲜味与pH值的关系是什么?
 飞帆------1年前1
飞帆------1年前1 -
 anneyanghuie 共回答了20个问题
anneyanghuie 共回答了20个问题 |采纳率75%中性时鲜味最好1年前查看全部
- 食品添加剂(谷氨酸钠\甘氨酸\呈味核苷酸二钠)是什么?对人体有害吗?什么害处?
 漏网的大雨1年前1
漏网的大雨1年前1 -
 late 共回答了14个问题
late 共回答了14个问题 |采纳率92.9%谷氨酸钠甘氨酸呈味核苷酸二钠) 这些都是 盐类!
在体内会水解的
谷氨酸钠 水解产生 谷氨酸
甘氨酸钠水解产生 甘氨酸
呈味核苷酸二钠 水解产生 核苷酸
谷氨酸 甘氨酸 是两种氨基酸 是构成人体 蛋白质的 物质
核苷酸 是构成人体 DNA RNA 的 两种物质
都无害.1年前查看全部
- 谷氨酸钠中心碳原子的杂化类型有
 qiaoqiao86071年前1
qiaoqiao86071年前1 -
 hk26012 共回答了12个问题
hk26012 共回答了12个问题 |采纳率91.7%如果是单键碳为sp3杂化,双键碳为sp2杂化1年前查看全部
- (1)味精的主要成分为谷氨酸钠(化学式为C 5 H 8 NO 4 Na),谷氨酸钠由
(1)味精的主要成分为谷氨酸钠(化学式为C 5 H 8 NO 4 Na),谷氨酸钠由 种元素组成,其中氢元素与氧元素的质量比为 .(最简整数比)
(2)天然气的主要成分是甲烷,甲烷不完全燃烧的方程式为;3CH 4 +5O 2 CO 2 +2CO+6H 2 O反应的两种生成物中,碳元素的化合价分别为 、 .
CO 2 +2CO+6H 2 O反应的两种生成物中,碳元素的化合价分别为 、 . cloudaw1年前1
cloudaw1年前1 -
 ytjyjhhggh 共回答了9个问题
ytjyjhhggh 共回答了9个问题 |采纳率100%
1年前查看全部
- 常温下 氢氧化铝 与 苯甲酸钠 谷氨酸钠 的水溶液会起化学反应吗?生成的物质有毒吗?
 采花的猪1年前1
采花的猪1年前1 -
 vickyong 共回答了14个问题
vickyong 共回答了14个问题 |采纳率92.9%苯甲酸钠 谷氨酸钠的水溶液显弱碱性,PH为8左右.氢氧化铝在水中的几乎不溶,属于两性物质,可以与强碱、强酸反应.本身表现出来的酸性弱于苯甲酸,碱性远弱于氢氧化钠,常温氢氧化铝不会与苯甲酸钠 谷氨酸钠的水溶液起化学反应.1年前查看全部
- (2004•沈阳)味精是烹调菜肴时常用的调味剂,其主要成份是谷氨酸钠.谷氨酸钠有鲜味,易溶于水.小靖发现某品牌味精包装上
(2004•沈阳)味精是烹调菜肴时常用的调味剂,其主要成份是谷氨酸钠.谷氨酸钠有鲜味,易溶于水.小靖发现某品牌味精包装上标注:“谷氨酸钠含量≥80%,氯化钠含量≤20%”.他想测定此味精中的NaCl的含量(谷氨酸钠的存在不影响NaCl的性质).
(1)下面是他所做实验的有关步骤,请补全实验步骤②.
①称取该味精样品5.0g,并溶于蒸馏水;
②加入过量的______溶液;
③过滤;
④用蒸馏水反复洗涤沉淀多次;
⑤将沉淀烘干、称量,测得固体质量为2.87g.
(2)根据上述实验步骤回答下列有关问题:
①过滤操作中所需要的仪器除了烧杯、铁架台(带铁圈)、玻璃棒外,还需要______;
②检验沉淀是否洗净的方法是______.
③此样品中NaCl的质量分数为______,是否符合其包装上标注的标准?______.
(3)味精的鲜味与溶液的酸碱度有关,当pH为6~7时鲜味最强;味精的鲜味还与温度有关,其水溶液经120℃以上长时间加热,不仅鲜味消失,而且对人体有害.因此试想一下,使用味精时应注意哪些问题?(2条即可)______. Edwardsnow1年前1
Edwardsnow1年前1 -
 稀饭鱼 共回答了8个问题
稀饭鱼 共回答了8个问题 |采纳率87.5%解题思路:(1)②根据钠盐都溶于水,需要将氯化钠中的氯离子转化为沉淀,通过沉淀的质量计算氯化钠的质量进行分析;
(2)①根据过滤操作需要的仪器进行分析;
②通过检验洗涤液中是否含有反应剩余的硝酸银进行分析;
③通过计算出氯化钠的质量分数与题中的数据进比较分析;
(3)根据味精具有的性质判断需要注意的事项.(1)②需要将氯化钠转化为沉淀,通过沉淀的质量以及方程式中的比例关系,计算氯化钠的质量,故答案为:AgNO3;
(2)①过滤操作除了题中提供的仪器外,还需要漏斗,故答案为:漏斗(带滤纸);
②只要检验洗涤液中的成分,就可以判断是否会洗净,故答案为:向洗涤液中滴加NaCl溶液,如果没有沉淀产生,则说明已洗净;
③设样品中的氯化钠为X,
NaCl+AgNO3=AgCl↓+NaNO3
58.5 143.5
x 2.87g
[58.5/X]=[143.5/2.87g]
x=1.17g,
氯化钠的质量分数:[1.17/5]×100%=23.4%,而氯化钠的质量分数≤20%,故答案为:23.4%,不符合;
(3)味精的鲜味在pH为6~7时鲜味最强,味精水溶液经120℃以上长时间加热,不仅鲜味消失,而且对人体有害,故答案为:加味精时,尽量控制酸碱性呈中性或弱酸性;加味精应在起锅前.点评:
本题考点: 酸、碱、盐的鉴别;玻璃仪器的洗涤;根据化学反应方程式的计算.
考点点评: 在解此类题时,首先分析题中所考查的问题,然后结合题中提供的知识和学过的知识进分析解答.1年前查看全部
- 味精是烹调菜肴时常用的调味剂,其主要成份是谷氨酸钠.谷氨酸钠有鲜味,易溶于水.小靖发现某品牌味精包装上标注:“谷氨酸钠含
味精是烹调菜肴时常用的调味剂,其主要成份是谷氨酸钠.谷氨酸钠有鲜味,易溶于水.小靖发现某品牌味精包装上标注:“谷氨酸钠含量≥80%,氯化钠含量≤20%”.他想测定此味精中的NaCl的含量(谷氨酸钠的存在不影响NaCl的性质).
(1)下面是他所做实验的有关步骤,请补全实验步骤②.
①称取该味精样品5.0g,并溶于蒸馏水;
②加入过量的______溶液;
③过滤;
④用蒸馏水反复洗涤沉淀多次;
⑤将沉淀烘干、称量,测得固体质量为2.87g.
(2)根据上述实验步骤回答下列有关问题:
①过滤操作中所需要的仪器除了烧杯、铁架台(带铁圈)、玻璃棒外,还需要______;
②检验沉淀是否洗净的方法是______.
③此样品中NaCl的质量分数为______,是否符合其包装上标注的标准?______.
(3)味精的鲜味与溶液的酸碱度有关,当pH为6~7时鲜味最强;味精的鲜味还与温度有关,其水溶液经120℃以上长时间加热,不仅鲜味消失,而且对人体有害.因此试想一下,使用味精时应注意哪些问题?(2条即可)______. 偶尔满足1年前1
偶尔满足1年前1 -
 长春亦友 共回答了10个问题
长春亦友 共回答了10个问题 |采纳率100%解题思路:(1)②根据钠盐都溶于水,需要将氯化钠中的氯离子转化为沉淀,通过沉淀的质量计算氯化钠的质量进行分析;
(2)①根据过滤操作需要的仪器进行分析;
②通过检验洗涤液中是否含有反应剩余的硝酸银进行分析;
③通过计算出氯化钠的质量分数与题中的数据进比较分析;
(3)根据味精具有的性质判断需要注意的事项.(1)②需要将氯化钠转化为沉淀,通过沉淀的质量以及方程式中的比例关系,计算氯化钠的质量,故答案为:AgNO3;
(2)①过滤操作除了题中提供的仪器外,还需要漏斗,故答案为:漏斗(带滤纸);
②只要检验洗涤液中的成分,就可以判断是否会洗净,故答案为:向洗涤液中滴加NaCl溶液,如果没有沉淀产生,则说明已洗净;
③设样品中的氯化钠为X,
NaCl+AgNO3=AgCl↓+NaNO3
58.5 143.5
x 2.87g
[58.5/X]=[143.5/2.87g]
x=1.17g,
氯化钠的质量分数:[1.17/5]×100%=23.4%,而氯化钠的质量分数≤20%,故答案为:23.4%,不符合;
(3)味精的鲜味在pH为6~7时鲜味最强,味精水溶液经120℃以上长时间加热,不仅鲜味消失,而且对人体有害,故答案为:加味精时,尽量控制酸碱性呈中性或弱酸性;加味精应在起锅前.点评:
本题考点: 酸、碱、盐的鉴别;玻璃仪器的洗涤;根据化学反应方程式的计算.
考点点评: 在解此类题时,首先分析题中所考查的问题,然后结合题中提供的知识和学过的知识进分析解答.1年前查看全部
- 酒楼的食品在制作时常加入味精,味精的主要成分是一种有机化合物--谷氨酸钠,其化学式为C5H8NO4Na.根据题
酒楼的食品在制作时常加入味精,味精的主要成分是一种有机化合物--谷氨酸钠,其化学式为C5H8NO4Na.根据题
(1)谷氨酸钠的各元素的原子个数比和相对分子质量?
(2)谷氨酸钠组成各元素的质量比和其中纳的质量分数? jmnyj1年前1
jmnyj1年前1 -
 可爱鼠 共回答了11个问题
可爱鼠 共回答了11个问题 |采纳率100%(1)C:H:N:O:NA=5:8:1:4:1
总相对分子质量=12×5+1×8+14×1+16×4+23×1
(2)1、将加号换成比号
2、=23÷总相对分子质量×百分百1年前查看全部
- 化学酱油是用盐酸分解大豆里的蛋白质,变成单个的氨基酸,再经过过滤、中和、着色等制成,主要成分是谷氨酸钠和食盐.目前,市场
化学酱油是用盐酸分解大豆里的蛋白质,变成单个的氨基酸,再经过过滤、中和、着色等制成,主要成分是谷氨酸钠和食盐.目前,市场上发现有些不合格化学酱油中含有盐酸,请你来检验其中有没有含酸.
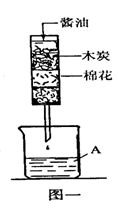
(1)将化学酱油通过图一所示的装置得到A溶液,此操作目的是 .(我的问题还有:这里的碳有什么用?是做活性炭吸附杂质的么?)
(2)从烧杯中取少量的A液体于试管中,用经下提供的 测试,若观察到 现象时,说明此化学酱油中可能含人盐酸.
(供选用的物质:①氯化钡溶液 ②硝酸银溶液 ③PH试纸 ④酚酞试液 ⑤石蕊试液.)
 911我爱1年前6
911我爱1年前6 -
 rainring 共回答了15个问题
rainring 共回答了15个问题 |采纳率93.3%1.除去溶液中的悬浊物,
2,应该选用 (PH 试纸),(变红),一般试纸是算红碱蓝的 下面说原因:
第一,因为 若含有未被中和完的盐酸,那溶液那溶液就应该是酸性; 不选石蕊是因为实际本生颜色太浓,不好区分.
第二,不选硝酸银是因为 题目中已经说过会含有食盐,也就是说会含氯化钠,既然这样那溶液中肯定含有氯离子,若用硝酸银检验,不知道检验出的是实验中的氯离子还是盐酸中的氯离子.1年前查看全部
- 味精的主要成分是谷氨酸钠,它的化学式是HOOCCHNH2(CH2) 2COONa,谷氨酸钠由_______种元素组成,其
味精的主要成分是谷氨酸钠,它的化学式是HOOCCHNH2(CH2) 2COONa,谷氨酸钠由_______种元素组成,其相对分子质量为________.
已知K2MnO4的式量为m,若钾的相对原子质量为a,氧的相对原子质量为b,则锰的相对原子质量(表达式)为x=m-2a-4b. 雨露女孩1年前2
雨露女孩1年前2 -
 五彩气泡 共回答了14个问题
五彩气泡 共回答了14个问题 |采纳率92.9%1.味精的主要成分是谷氨酸钠,它的化学式是HOOCCHNH2(CH2) 2COONa,谷氨酸钠由(5)种元素组成,其相对分子质量为(169).
先对化学式进行合并,得到C5H8NO4Na,含有C、H、N、O、Na五种元素.
相对分子质量是12*5+1*8+14+16*4+23=169
2.已知K2MnO4的式量为m,若钾的相对原子质量为a,氧的相对原子质量为b,则锰的相对原子质量(表达式)为x=m-2a-4b.
式量就是相对分子质量.设Mn的相对原子质量为x.
K2MnO4的式量为m=2a+x+4b,x=m-2a-41年前查看全部
- 有哪些几种味精是加盐加鲜的?主要配料是:谷氨酸钠,氯化钠,呈味核苷酸二钠!有朋友知道吗?
 angel21年前1
angel21年前1 -
 evermd 共回答了17个问题
evermd 共回答了17个问题 |采纳率88.2%市场上销售的加盐味精大部分是一些小品牌或无牌味精,它们价格便宜,大多销售给了饭店餐馆.除此之外,记者还发现它们包装上的执行标准也有问题.1年前查看全部
- (2014•河北区三模)味精是常用的调味品,它的鲜味来自于其中的主要成分“谷氨酸钠”(化学式是C5H8NO4Na,该物质
(2014•河北区三模)味精是常用的调味品,它的鲜味来自于其中的主要成分“谷氨酸钠”(化学式是C5H8NO4Na,该物质易溶于水,与AgNO3不反应).另外还含有NaCl(其他成分不考虑).请回答下列问题:
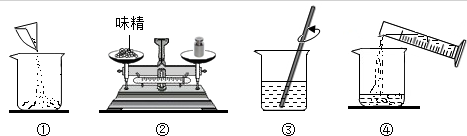
(1)称取5.0g味精配制成50g溶液,量取蒸馏水的量筒规格是______mL (填序号).
A.10mL B.50mL C.100mL
(2)如图是配制过程,正确的操作顺序为______.(填序号)
(3)为测定味精中NaCl的质量分数,进行如下实验:
①向所配置的50g溶液中加入适量的硝酸银溶液,该反应的化学方程式为______,检验该反应是否进行完全的方法是:静置后,在上层清夜中继续滴加硝酸银溶液,观察是否有______产生.
②过滤后,洗涤、干燥,称量氯化银固体,最后计算出氯化钠的质量分数.
③在其他操作均正确的情况下,若在配制溶液过程中,仰视刻度量取蒸馏水,则所配制溶液中谷氨酸钠的质量分数______(填“偏大”、“偏小”或“无影响”).
(4)某注射用药液的配置方法如下:
①把1.0g药品溶于水配制成4.0mL溶液a;
②取0.1mL溶液a,加水稀释至1.0mL,得溶液b;
③取0.1mL溶液b,加水稀释至1.0mL,得溶液c;
④取0.2mL溶液c,加水稀释至1.0mL,得溶液d;
由于在整个配置过程中药液很稀,其密度可近似看做1g/cm3,最终得到的药液(溶液d)中溶质的质量分数为______. 爱鱼儿love1年前1
爱鱼儿love1年前1 -
 ss- 共回答了14个问题
ss- 共回答了14个问题 |采纳率92.9%解题思路:(1)根据溶液质量=溶质质量+溶剂质量,由5.0g味精配制成50g溶液,求出配制时所需水的量,然后选择量取蒸馏水的量筒;
(2)根据使用固体物质配制溶液的步骤:计算-称量-溶解,判断实验操作图中操作的顺序;
(3)①可采取再滴加硝酸银溶液的方法,观察是否有沉淀,若无沉淀说明已经沉淀完全;
③仰视读数时,所读出的体积小于实际液体的体积;
(4)溶质的质量分数=[溶质的质量/溶液的质量]×100%,并利用稀释前后溶质的质量不会改变的知识解决,分步求出各部得到的溶液的溶质质量分数即可.(1)取5.0g味精配制成50g溶液,则需要水的质量=50g-5g=45g合45mL,因此需要选择50mL的量筒;故选B;
(2)图①为称量完毕的味精倒入烧杯,图②为称量味精的质量,图③为进行溶解,图④为量取水后倒入盛有味精的烧杯,因此,正确的操作顺序为②①④③;故填:②①④③;
(3)①氯化钠和硝酸银溶液反应生成氯化银白色沉淀和硝酸钠,该反应的化学方程式为NaCl+AgNO3═AgCl↓+NaNO3;向清液中再滴加硝酸银溶液,若观察到无明显现象说明原来已经完全沉淀;故填:NaCl+AgNO3═AgCl↓+NaNO3;白色沉淀;
③由于实际量取水的体积因仰视而大于配制时所需要水的体积,因此,使所配制的溶液因水量偏大而质量分数偏小;故填:偏小;
(4)因为溶液的密度是1g/cm3,所以可直接看成毫升数即是物质的克数,然后利用溶质的质量分数=[溶质的质量/溶液的质量]×100%计算;
(1)第一步:溶质的质量=1.0g;
溶液的质量=4.0mL×1g/cm3=4.0cm3×1g/cm3=4.0g;
所以,溶液a中溶质的质量分数=[1.0g/4.0g]×100%=25%;
溶液b的质量分数=[0.1g×25%/1g]×100%=2.5%;
溶液c的质量分数=[0.1g×2.5%/1g]×100%=0.25%;
溶液d的质量分数=[0.2g×0.25%/1g]×100%=0.05%.故填:0.05%.点评:
本题考点: 实验探究物质的组成成分以及含量;一定溶质质量分数的溶液的配制;盐的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题具有较大的综合性,在解答时需要涉及较多的基础知识,因此,需要足够的耐心和毅力.1年前查看全部
- (1)味精的主要成分为谷氨酸钠(化学式为C5H8NO4Na),谷氨酸钠由______种元素组成,其中氢元素与氧元素的质量
(1)味精的主要成分为谷氨酸钠(化学式为C5H8NO4Na),谷氨酸钠由______种元素组成,其中氢元素与氧元素的质量比为______.(最简整数比)
(2)天然气的主要成分是甲烷,甲烷不完全燃烧的方程式为;3CH4+5O2
CO2+2CO+6H2O反应的两种生成物中,碳元素的化合价分别为______、______.点燃 . 黑茶壶1年前1
黑茶壶1年前1 -
 teamt 共回答了19个问题
teamt 共回答了19个问题 |采纳率94.7%解题思路:(1)根据谷氨酸钠化学式的含义、化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(2)根据在化合物中正负化合价代数和为零,结合两种含碳元素的生成物的化学式进行解答本题.(1)谷氨酸钠是由碳、氢、氮、氧、钠五种元素组成的;其中氢元素与氧元素的质量比为(1×8):(16×4)=1:8.
(2)氧元素显-2价,设二氧化碳中碳元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(-2)×2=0,则x=+4价.
氧元素显-2价,设一氧化碳中碳元素的化合价是y,根据在化合物中正负化合价代数和为零,可得:y+(-2)=0,则y=+2价.
故答案为:(1)5;1:8.(2)+4价;+2价.点评:
本题考点: 化学式的书写及意义;有关元素化合价的计算;元素质量比的计算.
考点点评: 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.1年前查看全部
- 味精是常见调味料之一,主要成分为谷氨酸钠.谷氨酸钠(C5H8NO4Na)是一种由钠离子与谷氨酸根离子形成的盐.下列说法中
味精是常见调味料之一,主要成分为谷氨酸钠.谷氨酸钠(C5H8NO4Na)是一种由钠离子与谷氨酸根离子形成的盐.下列说法中正确的是( )
A.味精属于纯净物
B.谷氨酸钠中含有19个原子
C.谷氨酸钠分子不显电性
D.谷氨酸钠中碳、氮元素的质量比为30:7 pizzachan1年前1
pizzachan1年前1 -
 sflyb14 共回答了14个问题
sflyb14 共回答了14个问题 |采纳率85.7%解题思路:A、根据味精是常见调味料之一,主要成分为谷氨酸钠,进行分析判断.
B、根据谷氨酸钠的微观构成进行分析判断.
C、根据谷氨酸钠(C5H8NO4Na)是一种由钠离子与谷氨酸根离子形成的盐,进行分析判断.
D、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.A、味精是常见调味料之一,主要成分为谷氨酸钠,还含有其它物质,属于混合物,故选项说法错误.
B、谷氨酸钠(C5H8NO4Na)是一种由钠离子与谷氨酸根离子形成的盐,其1个粒子中含有19个原子,故选项说法错误.
C、谷氨酸钠(C5H8NO4Na)是一种由钠离子与谷氨酸根离子形成的盐,不含谷氨酸钠分分子,故选项说法错误.
D、谷氨酸钠中碳、氮元素的质量比为(12×5):14=30:7,故选项说法正确.
故选:D.点评:
本题考点: 化学式的书写及意义;纯净物和混合物的判别;元素质量比的计算.
考点点评: 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算等进行分析问题、解决问题的能力.1年前查看全部
- 味精的鲜味来自谷氨酸钠,它最早发现于什么汤中?
 小雨19941年前1
小雨19941年前1 -
 wangliliky 共回答了13个问题
wangliliky 共回答了13个问题 |采纳率92.3%应该是海带汤中,绝对正确的!加十分!1年前查看全部
- 生物题:已知谷氨酸钠分子的R基为—C3H5O2,则一份子谷氨酸中
生物题:已知谷氨酸钠分子的R基为—C3H5O2,则一份子谷氨酸中
含有的C, H, O, N原子数依次是
A5,9,4,1
B4,8,5,1
C5,8,4,1
D4,9,4,1 美美3321年前1
美美3321年前1 -
 whch98631 共回答了18个问题
whch98631 共回答了18个问题 |采纳率94.4%A5,9,4,11年前查看全部
- 味精的主要成分是谷氨酸还是谷氨酸钠
 ysy1980ysy1年前1
ysy1980ysy1年前1 -
 昕7号 共回答了21个问题
昕7号 共回答了21个问题 |采纳率95.2%味精的主要成分是谷氨酸钠.谷氨酸是脑组织氧化代谢的氨基酸之一,对改进和维持丘脑的机能是十分重要的.正常人每日摄钠1-2克便可满足生理的需要(联合国推荐每人每天摄入食盐为8克以下,食盐主要成分为氯化钠),如过食则可造成体内水钠潴留,导致血管管腔变细,血管阻力加大,血容量增多,加重心、肾负担,致使血压升高.1年前查看全部
- 一袋250g的含谷氨酸钠85%的味精中,含钠元素的质量为多少 谷氨酸钠C5H8NO4Na
 xiaomei04091年前1
xiaomei04091年前1 -
 匆匆过客0001 共回答了25个问题
匆匆过客0001 共回答了25个问题 |采纳率84%含钠元素 28.92 克
解析:
由谷氨酸钠的化学式 C5H8NO4Na得知
其的相对分子质量 = 12×5 + 8 + 14 + 16×4 + 23 = 169;
所以
谷氨酸钠中钠元素的质量分数为:
23 / 169 * 100% = 13.61%
所以
250g的含谷氨酸钠85%的味精中,含钠元素的质量为:
250 * 85% * 13.61% = 28.92 克1年前查看全部
- 味精是烹饪中不可缺少的调味品,其主要成分为谷氨酸钠(化学式为C5H8NO4Na),著名的“莲花”牌味精,其谷氨酸钠的含量
味精是烹饪中不可缺少的调味品,其主要成分为谷氨酸钠(化学式为C5H8NO4Na),著名的“莲花”牌味精,其谷氨酸钠的含量可达85%以上,请回答:
(1)谷氨酸钠的相对分子质量为______;
(2)一袋包装为50克的“莲花”牌味精中,谷氨酸钠的质量不少于______克. 爱君无悔1年前1
爱君无悔1年前1 -
 hh依归 共回答了18个问题
hh依归 共回答了18个问题 |采纳率83.3%解题思路:根据谷氨酸钠的化学式为C5H8NO4Na:(1)根据相对分子质量的计算方法计算即可;
(2)根据谷氨酸钠的含量为85%以上计算即可.(1)因为谷氨酸钠的化学式为C5H8NO4Na,所以谷氨酸钠的相对分子质量=12×5+1×8+14×1+16×4+23×1=169,
故答案为:169.
(2)因为“莲花”牌味精中谷氨酸钠的含量为85%以上,50g“莲花”牌味精中所以谷氨酸钠的质量≥50×85%=42.5g,
故答案为:42.5.点评:
本题考点: 相对分子质量的概念及其计算;物质组成的综合计算.
考点点评: 本题主要考查了相对分子质量的计算,化合物相对分子质量等于化合物中所有元素分子质量之和.1年前查看全部
- 169克谷氨酸钠中有多少克钠元素?
 lxforevermm1年前1
lxforevermm1年前1 -
 阿焰 共回答了25个问题
阿焰 共回答了25个问题 |采纳率88%谷氨酸钠 相对分子质量169,钠相对原子质量23,所以还有钠元素的质量为169×(23/ 169)=23克1年前查看全部
- 味精的主要成分为谷氨酸钠(化学式为C5H8NO4Na).因增加食品的鲜味、促进食欲而成为家庭常用的调味品.济宁市味精厂生
味精的主要成分为谷氨酸钠(化学式为C5H8NO4Na).因增加食品的鲜味、促进食欲而成为家庭常用的调味品.济宁市味精厂生产的“菱花”牌味精,其谷氨酸钠的含量可达85%以上.请回答:
(1)谷氨酸钠的相对分子质量是______;
(2)一袋包装为50g的“菱花”牌味精中,含谷氨酸钠的质量不少于______克. yashica1年前1
yashica1年前1 -
 在昼为影 共回答了21个问题
在昼为影 共回答了21个问题 |采纳率81%解题思路:(1)根据谷氨酸钠的化学式C5H8NO4Na可知,谷氨酸钠的相对分子质量=(碳的相对原子质量×碳原子个数)+(氢的相对原子质量×氢原子个数)+(氮的相对原子质量×氮原子个数)+(氧的相对原子质量×氧原子个数)+(钠的相对原子质量×钠原子个数);
(2)根据“味精质量×味精中谷氨酸钠的含量”计算即可.(1)根据谷氨酸钠的化学式C5H8NO4Na可知,谷氨酸钠的相对分子质量=12×5+8+14+16×4+23=169;
(2)50g×85%=42.5g.
故答案为:(1)189;(2)42.5g.点评:
本题考点: 化合物中某元素的质量计算;有关化学式的计算和推断.
考点点评: 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.1年前查看全部
- 味精的主要成分是谷氨酸钠,向其中加入盐酸可得谷氨酸,谷氨酸既能与NaOH反应,又能与HCL反应.
 zhoukang121年前4
zhoukang121年前4 -
 polaris俊 共回答了20个问题
polaris俊 共回答了20个问题 |采纳率95%谷氨酸钠(C5H8NO4Na),化学名α-氨基戊二酸一钠,是一种由钠离子与谷氨酸根离子形成的盐.其中谷氨酸是一种氨基酸,而钠是一种金属元素.生活中常用的调味料味精的主要成分就是谷氨酸钠.http://baike.baidu.com/view/296951.htm1年前查看全部
- 请问旋光法测定味精中谷氨酸钠含量时加入盐酸的目的是什么?
 zw03711年前1
zw03711年前1 -
 linxiaoguang 共回答了14个问题
linxiaoguang 共回答了14个问题 |采纳率85.7%主要是为了使维持溶液的PH,使得谷氨酸钠完全电离,稳定谷氨酸钠!1年前查看全部
- 谷氨酸钠、5'-呈味核苷酸二钠、柠檬黄、胭酯红、特丁基对苯二酚、二丁基羟基甲苯.这些物质的分子式?...
谷氨酸钠、5'-呈味核苷酸二钠、柠檬黄、胭酯红、特丁基对苯二酚、二丁基羟基甲苯.这些物质的分子式?...
谷氨酸钠、5'-呈味核苷酸二钠、柠檬黄、胭酯红、特丁基对苯二酚、二丁基羟基甲苯.这些物质的分子式?(说的格式是:物质名称+对应的 分子式) sasbsasb1年前1
sasbsasb1年前1 -
 janbry 共回答了22个问题
janbry 共回答了22个问题 |采纳率86.4%谷氨酸钠 分子式C5H8NO4Na ;
5'-呈味核苷酸二钠 分子式C10H12N5NA2O8P;
柠檬黄 分子式C16H12N4O9S2Na3;
胭酯红 分子式C20H11N2O10S3Na3;
特丁基对苯二酚 分子式10H14O2;
二丁基羟基甲苯 分子式 C10H14O2;1年前查看全部
- 请问:食用糖(葡萄糖、蔗糖、砂糖、绵白糖)、味精(谷氨酸钠)、耗油的分子式是什么?
 伊犁河上1年前1
伊犁河上1年前1 -
 zllbingo 共回答了24个问题
zllbingo 共回答了24个问题 |采纳率75%葡萄糖--C6H12O6 是多羟基醛
蔗糖-----C12H22O11
砂糖------C12H22O11 这两者分子式同但结构不同 是同分异构体
味精-------C5H8NO4Na 化学名谷氨酸钠 谷氨酸是氨基酸中的一种 只是羧基中的氢原子被钠取代
蚝油是混和物 无化学式可写1年前查看全部
- 味精所含的谷氨酸钠是微生物发酵的产物么?
 dcy19851年前2
dcy19851年前2 -
 王豫鲁 共回答了25个问题
王豫鲁 共回答了25个问题 |采纳率84%是 是由谷氨酸棒状杆菌 发酵而成
谷氨酸棒状杆菌
谷氨酸棒状杆菌(Corynebacterium glutamicum)是好氧细菌,为革兰氏阳性.可用于微生物发酵工程生产谷氨酸来制取谷氨酸钠(味精),谷氨酸棒状杆菌在发酵过程中要不断地通入无菌空气,并通过搅拌使空气形成细小的气泡,迅速溶解在培养液中(溶氧);在温度为摄氏30到37度,pH为7到8的情况下,经28到32小时,培养液中会生成大量的谷氨酸.在谷氨酸生产中,培养基中碳氮比为4:1时,菌体大量繁殖而产生的谷氨酸少;当碳氮比为3:1时,菌体繁殖受抑制,但谷氨酸的合成量大增.在发酵过程中,当pH呈酸性时,谷氨酸棒状杆菌就会生成乙酰谷氨酰胺;当溶氧不足时,生成的代谢产物就会是乳酸或琥珀酸.1年前查看全部
- (2006•中山模拟)味精是烹制菜肴时常用的调味品,其主要成分是谷氨酸钠.谷氨酸钠有鲜味,易溶于水.小明发现某品牌味精包
(2006•中山模拟)味精是烹制菜肴时常用的调味品,其主要成分是谷氨酸钠.谷氨酸钠有鲜味,易溶于水.小明发现某品牌味精包装上标注:“谷氨酸钠含量≥80%,NaCl含量≤20%”,他想测定此味精中NaCl的含量.
查资料:NaCl+AgNO3=AgCl↓+NaNO3,谷氨酸钠的存在不影响NaCl性质.
实验过程:
①称取该味精样品5.0g,并溶于蒸馏水;②加入过量的硝酸银溶液;③过滤;④用蒸馏水反复洗涤沉淀物多次;⑤将沉淀物烘干、称量,测得固体质量为2.87g.
根据上述实验步骤回答下列有关问题:
(1)过滤操作所需要的仪器除烧杯、铁架台(带铁圈)、玻璃棒外,还需要的玻璃仪器是______;
(2)此样品中NaCl的质量分数为______,是否符合其包装上标注的标准?______.
应用:最近专家否认了“味精致癌”的说法.实验表明,味精在100℃加热半小时,只有0.3%的味精(谷氨酸钠)生成焦谷氨酸钠(有毒),其对人体的影响甚微.对此下列认识正确的是______.
A.谷氨酸钠受热不发生化学变化
B.谷氨酸钠在加热下生成焦谷氨酸钠是物理变化
C.大量食用味精不利于身体健康
D.研究问题的一种有效方法是通过实验. henson3251年前1
henson3251年前1 -
 dinolovek 共回答了21个问题
dinolovek 共回答了21个问题 |采纳率85.7%解题思路:(1)进行过滤操作最重要的一步就是过滤,需要的仪器较多烧杯(两只)、铁架台(带铁圈)、玻璃棒、漏斗、胶头滴管、洗瓶(塑料)等;
(2)根据生成的氯化银的质量计算出氯化钠的质量,进而求出质量分数,然后进行判断;
应用:根据所给的信息进行判断作出正确的判断.(1)要使液体与固体分离,用过滤的方法进行,缺少的仪器是漏斗(2)设调料味精中混有的氯化钠的质量为x NaCl+AgNO3=AgCl↓+NaNO3 58.514...
点评:
本题考点: 味精中食盐含量的探究;含杂质物质的化学反应的有关计算;酸、碱、盐的鉴别;根据化学反应方程式的计算.
考点点评: 进行解题是我们必须培养的能力,熟练的利用化学方程式根据已知的物质的质量计算求出其它物质的质量.1年前查看全部
大家在问
- 1读《争吵》有感 作文
- 2赞美别人需要真诚,更需要一些合适的语言请你搜集一些恰当的词语填充下表 对象特征
- 3英语翻译1.当她到达的时候,我已经回家了.2,到这个月底,我们已经学了3000个单词.3,我那时不饿,我那时刚吃过早餐.
- 4同义句替换petrol is outging.paul is outgoing too
- 5宾补,直宾,间宾区别MR.SMITH teachs us MATHThe news made us sad哪个是宾语补足
- 6翻译!音乐之声翻译一下《音乐之声》中Do-Re-Mi
- 7That\'s right!Let\'s go!
- 8画一个长方形把平面分成两个部分,那么画三个长方形把平面分成几个部分?
- 9已知A,B,C,D,E是短周期的五种元素,他们的原子序数依次增大.A元素原子形成的离子核外电子数为零;C,D,E三种元素
- 10怎么在搜索框中输入数学平方或立方符号
- 11It在句子中怎么用?只是指物还是指人也可以?如果描写动物的话,It grew and grew 可不可以这么写?
- 12浴室地面铺完瓷砖才发现地面不平,有积水,可以直接在瓷砖上用马赛克再铺一遍吗?
- 13消费者使用信用卡①可以提高支付结算效率 ②可以减少
- 14钱剩的不多了用英语怎么说
- 15读她大板块示意图,完成下列要求.