(2她13•东港市二模)1面是九明同学在实验室所做的证明碳酸铵是由碳酸根和铵根组成的实验.请你帮忙完成1列实验报告内容的
 ladenfish2022-10-04 11:39:541条回答
ladenfish2022-10-04 11:39:541条回答| 实验操作步骤 | 实验现象 | 实验结论 |
| 取少量碳酸铵与适量的稀盐酸混合,将生成的气体通入澄清的石灰水中 | 碳酸铵含有______ | |
| 取少量碳酸铵与适量的熟石灰混合研磨 | 碳酸铵含有______ |

已提交,审核后显示!提交回复
共1条回复
 zhangqing1983 共回答了24个问题
zhangqing1983 共回答了24个问题 |采纳率91.7%- 解题思路:(1)根据碳酸根离子和氢离子结合产生二氧化碳气体分析;
(2)根据铵根离子和氢氧根离子结合产生刺激性气味的氨气分析.解;(1)取少量碳酸铵与适量的稀盐酸混合,会产生二氧化碳,因此将生成的气体通入澄清的石灰水中,会观察到澄清的石灰水变浑浊,说明碳酸铵中含有碳酸根离子;故答案为;澄清的石灰水变浑浊;碳酸根离子;
(2)取少量碳酸铵与适量的熟石灰混合研磨会产生刺激性气味的氨气,因此观察到的实验现象为:有刺激性气味的气体产生,说明碳酸铵中含有铵根离子;故答案为:有刺激性气味的气体产生;铵根离子.点评:
本题考点: 常见离子的检验方法及现象.
考点点评: 本题考查了初中阶段重要的碳酸根离子、铵根离子的检验方法,此外还要掌握硫酸根离子、氯离子等重要离子的检验方法,并且在语言表达方面要严密、准确,步骤要完整. - 1年前
相关推荐
- (2013•东港市二模)如图是某地部分麦田的图片.你认为图中右边(矮小麦苗)的那片麦田应施用下列哪种化肥( )
 (2013•东港市二模)如图是某地部分麦田的图片.你认为图中右边(矮小麦苗)的那片麦田应施用下列哪种化肥( )
(2013•东港市二模)如图是某地部分麦田的图片.你认为图中右边(矮小麦苗)的那片麦田应施用下列哪种化肥( )
A.KCl
B.Ca3(PO4)2
C.NH4Cl
D.KNO3 心悬在梦中1年前1
心悬在梦中1年前1 -
 大家晚上好 共回答了12个问题
大家晚上好 共回答了12个问题 |采纳率75%解题思路:根据题意,该同学要使用氮肥,含有氮元素的化肥是氮肥,能促进植物的茎叶生长茂盛,叶色浓绿.植物比正常的植株矮小瘦弱,叶片发黄,说明土壤中缺乏营养元素氮元素.
A、氯化钾中不含有氮元素,含有钾元素,属于钾肥,故选项错误;
B、磷酸钙中不含有氮元素,含有磷元素,属于磷肥,故选项错误;
C、氯化铵中含有氮元素,属于氮肥,故选项正确;
D、硝酸钾中含有钾元素和氮元素,属于复合肥,故选项错误.
故选C.点评:
本题考点: 常见化肥的种类和作用.
考点点评: 解答本题要掌握各种化肥对植物生长的作用,只有这样才能对问题做出正确的判断.1年前查看全部
- (2013•东港市二模)自然界中存在氧循环和碳循环,其中能将二氧化碳转化为氧气的是( )
(2013•东港市二模)自然界中存在氧循环和碳循环,其中能将二氧化碳转化为氧气的是( )
A.动植物尸体的腐烂
B.动植物的呼吸
C.燃料的燃烧
D.光合作用 tmmg48911年前1
tmmg48911年前1 -
 liuxiaocong 共回答了23个问题
liuxiaocong 共回答了23个问题 |采纳率82.6%解题思路:结合光合作用、呼吸作用、动植物尸体的腐烂、燃烧的常识进行分析解答,自然界中由二氧化碳转化为氧气唯一的方法是光合作用,据此进行分析判断.A、动植物尸体在微生物作用下,与空气中氧气发生缓慢氧化,产生二氧化碳等物质而腐烂,是将氧气转化为二氧化碳,故选项错误.
B、动植物的呼吸,是将氧气在体内发生缓慢氧化释放出二氧化碳,是将氧气转化为二氧化碳,故选项错误.
C、燃料的燃烧,是燃料与氧气反应生成二氧化碳,是将氧气转化为二氧化碳,故选项错误.
D、植物的光合作用是吸收植物吸收二氧化碳释放氧气的过程,能将二氧化碳转化为氧气,故选项正确.
故选D.点评:
本题考点: 自然界中的氧循环.
考点点评: 本题难度不大,了解光合作用、呼吸作用、动植物尸体的腐烂、燃烧的原理是正确解答本题的关键.1年前查看全部
- (2013•东港市二模)已知:在20℃时,硝酸钾的溶解度为31.6g,则下列有关说法不正确的是( )
(2013•东港市二模)已知:在20℃时,硝酸钾的溶解度为31.6g,则下列有关说法不正确的是( )
A.20℃时,饱和硝酸钾溶液中溶液和溶质的质量比为131.6:31.6
B.20℃时,饱和硝酸钾溶液中溶质的质量分数为31.6%
C.20℃时,饱和硝酸钾溶液中溶剂和溶质的质量比为100:31.6
D.20℃时,每100 g水中最多能溶解31.6 g硝酸钾 xiaoxiao小1年前1
xiaoxiao小1年前1 -
 wysh_406 共回答了27个问题
wysh_406 共回答了27个问题 |采纳率92.6%解题思路:溶解度是在一定温度下,某固体溶质在100g溶剂里达到饱和状态所溶解的溶质质量;溶解度定义中的四要素:一定温度、100g溶剂、溶液达到饱和状态、溶解的质量及单位克;据此进行分析判断.在20℃时,硝酸钾的溶解度为31.6g,其涵义是20℃时,100g水中最多溶解31.6g硝酸钾,溶液达到饱和状态.
A、20℃时,饱和硝酸钾溶液中溶液和溶质的质量比为131.6g:31.6g=131.6:31.6,故选项说法正确.
B、20℃时,饱和硝酸钾溶液中溶质的质量分数为
31.6g
31.6g+100g×100%<31.6%,故选项说法错误.
C、20℃时,饱和硝酸钾溶液中溶剂和溶质的质量比为100g:31.6g=100:31.6,故选项说法正确.
D、20℃时,每100g水中最多能溶解31.6g硝酸钾,溶液达到饱和状态,故选项说法正确.
故选B.点评:
本题考点: 固体溶解度的概念;溶质的质量分数、溶解性和溶解度的关系.
考点点评: 本题难度不大,理解溶解度的概念,熟记溶解度的四要素(温度、100g溶剂、饱和状态、单位是克)是正确解答本题的关键.1年前查看全部
- (2013•东港市二模)物质X在一定温度下受热分解:2X═2N2↑+O2↑+4H2O↑ 则物质X化
(2013•东港市二模)物质X在一定温度下受热分解:2X═2N2↑+O2↑+4H2O↑则物质X化学式为( )
A.HNO2
B.HNO3
C.NH3.H2O
D.NH4NO3 不会哭的袜子1年前1
不会哭的袜子1年前1 -
 whitelily 共回答了27个问题
whitelily 共回答了27个问题 |采纳率96.3%解题思路:解此题需根据质量守恒定律,反应前后原子种类和个数都不变,分别统计出反应前后原子种类及个数,比较分析就可以求出所的物质的化学式.反应的化学方程式为2X═2N2↑+O2↑+4H2O↑,反应后反应物种含N、O、H三种元素的原子个数分别为4、6、8,根据反应前后原子种类、数目不变,可判断2X中含4个N原子、6个O原子和8个氢原子,则每个X分子由2个N原子、3个O原子和4个氢原子构成,则物质X的化学式为NH4NO3;
故选D.点评:
本题考点: 质量守恒定律及其应用.
考点点评: 根据反应的化学方程式,利用反应前后原子种类、数目不变,可推断反应中某物质的分子构成、确定该物质的化学式.1年前查看全部
- (2013•东港市二模)将石油加热炼制,不能得到的产品是( )
(2013•东港市二模)将石油加热炼制,不能得到的产品是( )
A.汽油
B.柴油
C.煤油
D.煤焦油 bayb881年前1
bayb881年前1 -
 爱宇小西 共回答了22个问题
爱宇小西 共回答了22个问题 |采纳率90.9%解题思路:石油中含有多种成分,这些成分的沸点不同,根据沸点不同将它们加热分离可得到汽油、煤油、柴油、润滑油、石蜡、溶剂油、沥青等产品;根据石油分馏的产品进行分析判断即可.石油属于混合物,它是由汽油、煤油、柴油、润滑油、机油等沸点不同物质混合而成的,石油通过分馏即可得到上述物质.将煤隔绝空气加强热,可生成焦炭、煤焦油、煤气、焦炉气等产物,煤气、煤焦油、焦炉气均属于煤加工的产品.
A、汽油属于石油加工的产品,故选项错误.
B、柴油属于石油加工的产品,故选项错误.
C、煤油属于石油加工的产品,故选项错误.
D、煤焦油属于煤加工的产品,故选项正确.
故选D.点评:
本题考点: 石油加工的产物.
考点点评: 本题难度不大,了解石油加热炼制得到的产品是正确解答本题的关键.1年前查看全部
- (2013•东港市二模)以下是某化学探究的过程.请在下列横线上填写适当的内容.
(2013•东港市二模)以下是某化学探究的过程.请在下列横线上填写适当的内容.
实验:向NaOH溶液中滴入无色酚酞试液,溶液显红色
(1)提出问题:是什么粒子使无色酚酞试液显红色呢?
(2)查找资料:NaOH溶液中存在的粒子有大量的H2O、Na+、OH-.
(3)猜想:是大量的OH-使无色酚酞试液显红色.
(4)实验探究步骤及其说明:
①在一支干净试管中加入2mL蒸馏水,再滴入几滴无色酚酞试液,溶液几乎不变色,说明______;
②______,说明钠离子Na+(或钠离子)不能使无色酚酞试液变红;
(5)结论:原假设成立
(6)反思:KOH、Ca(OH)2的水溶液,都能使无色酚酞试液显红色,是因为______. fanshen1年前1
fanshen1年前1 -
 wsn111 共回答了14个问题
wsn111 共回答了14个问题 |采纳率92.9%解题思路:根据碱的性质结合碱溶液中存在的微粒进行分析,能使酚酞变红的粒子是OH-,设计实验时要排除水分子和Na+的干扰.(4)①蒸馏水是由水分子构成的,因此在一支干净试管中加入2mL蒸馏水,再滴入几滴无色酚酞试液,溶液几乎不变色,说明水分子不能使无色酚酞试液变红;
②要验证不是钠离子使酚酞试液变色,可以使用氯化钠溶液,操作为:在一支干净试管中加入2mL氯化钠溶液,再滴入几滴无色酚酞试液,溶液几乎不变色,说明钠离子不能使酚酞试液变红;
(6)KOH、Ca(OH)2的水溶液,都能使无色酚酞试液显红色,根据结论氢氧根离子能使酚酞试液变红,而二者的溶液中都存在大量的氢氧根离子;
故答案为:(4)①水分子不能使无色酚酞试液变红;②在一支干净试管中加入2mL氯化钠溶液,再滴入几滴无色酚酞试液,溶液几乎不变色;
(6)KOH、Ca(OH)2的水溶液中都存在大量的氢氧根离子.点评:
本题考点: 碱的化学性质.
考点点评: 本题从微观的角度考查了酚酞试液变色的原因,设计实验往往从排除干扰的角度验证氢氧根离子的作用.1年前查看全部
- (2013•东港市二模)A~G表示初中化学常见的物质,它们之间的转化关系如图所示(部分生成物已略去),其中A为金属氧化物
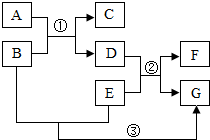 (2013•东港市二模)A~G表示初中化学常见的物质,它们之间的转化关系如图所示(部分生成物已略去),其中A为金属氧化物,B是一种酸,其浓溶液有吸水性,常用作干燥剂,E是一种比较活泼的金属、F为紫红色的单质,G的水溶液为浅绿色.化学反应②和③的基本反应类型相同.请回答下列问题:
(2013•东港市二模)A~G表示初中化学常见的物质,它们之间的转化关系如图所示(部分生成物已略去),其中A为金属氧化物,B是一种酸,其浓溶液有吸水性,常用作干燥剂,E是一种比较活泼的金属、F为紫红色的单质,G的水溶液为浅绿色.化学反应②和③的基本反应类型相同.请回答下列问题:
(1)写出A物质的化学式______;
(2)D的水溶液的颜色是______,它与烧碱溶液反应的化学反应方程式为______;
(3)写出B和E发生反应的化学方程式______;
(4)反应②的基本反应类型是______,该反应可以说明金属活泼性由强到弱的顺序是(用化学式表示)______. 利连1年前1
利连1年前1 -
 anuoyuanyuan 共回答了14个问题
anuoyuanyuan 共回答了14个问题 |采纳率78.6%解题思路:根据题干叙述,本题的解题突破口是F为紫红色的单质,则F是铜;B是一种酸,其浓溶液有吸水性,常用作干燥剂,则B是硫酸;G的水溶液为浅绿色,说明含有亚铁离子,是B-硫酸和E反应产生的硫酸亚铁,而E是一种比较活泼的金属,所以E是铁;E-铁和D反应产生F-铜和硫酸亚铁,因此D是硫酸铜;A为金属氧化物,能与硫酸反应生成硫酸铜,则A是氧化铜,C是水,然后带入完成相关的问题.F为紫红色的单质,则F是铜;B是一种酸,其浓溶液有吸水性,常用作干燥剂,则B是硫酸;G的水溶液为浅绿色,说明含有亚铁离子,是B-硫酸和E反应产生的硫酸亚铁,而E是一种比较活泼的金属,所以E是铁;E-铁和D反应产生F-铜和硫酸亚铁,因此D是硫酸铜;A为金属氧化物,能与硫酸反应生成硫酸铜,则A是氧化铜,C是水,代入框图,推断合理;因此:
(1)A是氧化铜,故填:CuO;
(2)D是硫酸铜溶液,是蓝色的;硫酸铜与烧碱溶液反应的化学反应方程式为:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;故填:蓝色;CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
(3)铁和硫酸反应的方程式为:Fe+H2SO4=FeSO4+H2↑;故填:Fe+H2SO4=FeSO4+H2↑;
(4)硫酸铜与铁反应生成硫酸亚铁和铜,是一种单质和一种化合物反应生成另一种单质和另一种化合物,属于置换反应,故填:置换反应;同时该反应说明了铁的活动性比铜强;故填:置换反应;Fe>Cu.点评:
本题考点: 物质的鉴别、推断;化学式的书写及意义;反应类型的判定;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题为框图式推断题,解题的关键是依据题干的信息,找准推断的突破口,得出有关物质的化学式,然后结合相关的现象通过正推或逆推等完成其它物质的推断,得出结论,验证即可.1年前查看全部
- (2013•东港市二模)请你从①熟石灰 ②小苏打 ③食盐 ④石墨中,选择适当物
(2013•东港市二模)请你从①熟石灰 ②小苏打 ③食盐④石墨中,选择适当物质填空( 填物质对应的序号).
(1)可作干电池电极的是______;
(2)常用于改良酸性土壤的是______;
(3)腌制蔬菜、鱼、肉等常用的调味品是______;
(4)焙制糕点所用的发酵粉的主要成分是______. maodan1231年前1
maodan1231年前1 -
 wangshicc 共回答了18个问题
wangshicc 共回答了18个问题 |采纳率100%解题思路:物质的性质决定物质的用途,石墨具有优良的导电性;熟石灰是氢氧化钙的俗称,具有碱性;食盐是氯化钠的俗称,是常用的调味品;小苏打是碳酸氢钠的俗称;据此结合上述物质的性质与用途进行分析解答.(1)石墨具有优良的导电性,可作干电池电极.
(2)熟石灰是氢氧化钙的俗称,具有碱性,属于碱,可用于改良酸性土壤.
(3)食盐是氯化钠的俗称,腌制蔬菜、鱼、肉等常用的调味品.
(4)小苏打是碳酸氢钠的俗称,是焙制糕点所用的发酵粉的主要成分.
故答案为:(1)④;(2)①;(3)③;(4)②.点评:
本题考点: 碳单质的物理性质及用途;常见碱的特性和用途;常用盐的用途.
考点点评: 本题难度不大,物质的性质决定物质的用途,掌握常见化学物质的性质和用途是正确解答此类题的关键.1年前查看全部
- (2013•东港市二模)实验小组对铁的锈蚀按下表探究.室温时,将包有样品的滤纸包固定在橡胶塞上,迅速塞紧,装置如下图.观
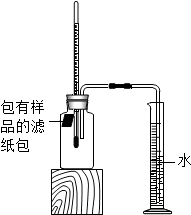 (2013•东港市二模)实验小组对铁的锈蚀按下表探究.室温时,将包有样品的滤纸包固定在橡胶塞上,迅速塞紧,装置如下图.观察到量筒内水沿导管慢慢进入广口瓶(净容积为146mL).当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零).记录起始和最终量筒的读数以及所需时间如下表.
(2013•东港市二模)实验小组对铁的锈蚀按下表探究.室温时,将包有样品的滤纸包固定在橡胶塞上,迅速塞紧,装置如下图.观察到量筒内水沿导管慢慢进入广口瓶(净容积为146mL).当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零).记录起始和最终量筒的读数以及所需时间如下表.
(1)实验①和②说明NaCl可以______ (填“加快”或“减慢”)铁锈蚀的速率.序号 样品 量筒起始读数
/mL量筒最终读数
/mL所需时间
/min① 1g铁粉、0.2g碳和10滴水 100 70 约120 ② l g铁粉、0.2g碳、10滴水和少量NaCl 100 70 约70 ③ ______
(2)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是______(填“放热”或“吸热”)过程.
(3)实验结束后取出滤纸包,观察到有红棕色物质生成,该物质的化学式是______.
(4)实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成. meidong1年前1
meidong1年前1 -
 ring1030 共回答了28个问题
ring1030 共回答了28个问题 |采纳率89.3%解题思路:(1)根据因为广口瓶中铁生锈,是铁和空气中的氧气反应,所以广口瓶中气体压强减小量筒中的水会进入广口瓶,量筒中的水减少30ml所需时间的长短分析.
(2)根据实验开始后,广口瓶内温度有所上升分析.
(3)根据铁生锈是铁和氧气及空气中的水反应分析.
(4)根据实验①和③是探究碳对铁锈蚀速率的影响并比较①方案中实验设计分析.(1)因为广口瓶中铁生锈所以广口瓶中气体压强减小所以量筒中的水会进入广口瓶,量筒中的水减少30ml所需时间的长短,故答案:加快.
(2)实验开始后,广口瓶内温度有所上升,故答案:放热.
(3)铁生锈是铁和空气中的水、氧气反应生成氧化铁等物质,故答案:Fe2O3.
(4)实验①和③是探究碳对铁锈蚀速率的影响并比较①方案中实验设计,控制铁和水的用量再不加碳实验一下铁的锈蚀速度即可.故答案:
③ 1 g铁粉、10滴水点评:
本题考点: 探究金属锈蚀的条件.
考点点评: 本题主要考查了金属生锈的条件的探究方面的内容,注重控制变量法做好对比实验是解答这类题的关键.1年前查看全部
- (2013•东港市二模)正确的化学实验操作对实验结果、人身安全都非常重要.以下是一些实验操作图,其中正确的是( )
(2013•东港市二模)正确的化学实验操作对实验结果、人身安全都非常重要.以下是一些实验操作图,其中正确的是( )
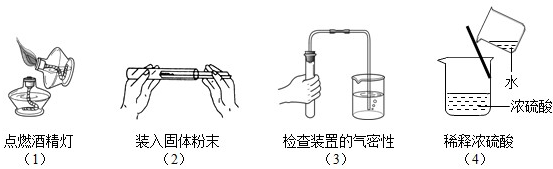
A.只有(1)和(2)
B.只有(1)和(4)
C.只有(3)和(4)
D.只有(2)和(3) 三井美香1年前1
三井美香1年前1 -
 yueyue002 共回答了17个问题
yueyue002 共回答了17个问题 |采纳率94.1%解题思路:(1)根据禁止用一酒精灯去引燃另一酒精灯分析.
(2)根据向试管中取用固体粉末状药品,试管要平放,将药品尽量向试管底部送,.
(3)根据检查装置气密性是现将导管放入水中再用手握住试管外壁看导管处是否有气泡冒出分析.
(4)根据稀释浓硫酸要将浓硫酸慢慢倒入水中不能将水加入浓硫酸中分析.(1)禁止用一酒精灯去引燃另一酒精灯,该操作不正确.
(2)向试管中取用固体粉末状药品,试管要平放,将药品尽量向试管底部送,该操作正确.
(3)检查装置气密性是现将导管放入水中再用手握住试管外壁看导管处是否有气泡冒出,该操作正确.
(4)稀释浓硫酸要将浓硫酸慢慢倒入水中不能将水加入浓硫酸中,该操作不正确.
故答案选D.点评:
本题考点: 加热器皿-酒精灯;固体药品的取用;浓硫酸的性质及浓硫酸的稀释;检查装置的气密性.
考点点评: 化学实验基本操作准确与否是实验取得成功的关键,一定要准确操作才能保证实验的顺利进行.1年前查看全部
大家在问
- 1一个长方体水池长5分米宽4分米深3分米,水面离池口4厘米放一块棱长2.1分米的正主体石块水会溢出多少毫升
- 2已知抛物线的顶点在原点,焦点在Y轴上,抛物线上的一个点的纵坐标为-3,且该点与焦点的距离是5,求此抛物线的方程
- 3PM2.5漂浮多高
- 4关于维生素C水溶液能使高锰酸钾溶液褪色的问题
- 51.She pionted at a strange thing___three legs.啥意思?
- 6英语书面表达又到周末了,你想为全家准备一顿晚饭.请介绍一下你家人想吃的食物.提示词:would like,60词左右.y
- 7黄铜是一种铜与锌的合金,其中铜的含量达到70%.现在一块黄铜含锌21千克,这块黄铜重( )千克?
- 8如图,四棱锥P-ABCD中,PB⊥底面ABCD,CD⊥PD,底面ABCD为直角梯形,AD∥BC,AB⊥BC,AB=AD=
- 9一名考古学家发现了一块古代车轮碎片,你能帮他找出这个车轮的半径吗?说出你的理由
- 10有只有两个字的成语吗?有只有两个字的成语吗?有的话请列举一下
- 11已知函数f(x)=4x+ax(x>0,a>0)在x=3时取得最小值,则a= ___ .
- 12《山中访友》一文中,有哪些好句子.例举一个.
- 13一辆总质量是4乘10的三次方千克的满载的汽车,从静止出发,沿水平路面行驶,汽车的牵引力是6乘10的三次方牛,受到的阻力是
- 14如图,CD∥AF,∠CDE=∠BAF,AB⊥BC,∠C=124°,∠E=80°,则∠F=______度.
- 15据热力学温度T和摄氏度t之间的数据关系,做以下换算
