波义耳实验为什么会违背了守恒定律
 fffwa2022-10-04 11:39:542条回答
fffwa2022-10-04 11:39:542条回答
已提交,审核后显示!提交回复
共2条回复
 明白1 共回答了17个问题
明白1 共回答了17个问题 |采纳率94.1%- 没有违背守恒定律
发生了氧化反应,增加的是容器里的氧气的质量. - 1年前
 大将军88001053 共回答了81个问题
大将军88001053 共回答了81个问题 |采纳率- 不会的
你手对它肯定做功的 - 1年前
相关推荐
- 英国科学家波义耳之所以被称为近代化学的创始人,主要是因为他
英国科学家波义耳之所以被称为近代化学的创始人,主要是因为他
A.通过化学反应提出质量守恒定律
B.把严密的实验方法引入化学
C.确立了物质的分子原子结构学说
D.制定化学元素周期表 瑾儿041年前1
瑾儿041年前1 -
 yix123 共回答了16个问题
yix123 共回答了16个问题 |采纳率93.8%答案B
分析本题考查的知识点是化学发展史的四个阶段.这是一道最佳选择题,它从宏观方面勾画出了17到19世纪化学发展的轨迹,具有较高的综合性.17世纪时,波义耳把严密的实验方法引入化学.没有严密的科学的实验方法,化学只能是中世纪巫术而不能称其为科学,所以波义耳被称为近代化学的创始人.18世纪末,法国科学家拉瓦锡第一个通过化学反应提出了物质不灭定律,即质量守衡定律.19世纪初,英国科学家道尔顿建立了科学的原子论,在此基础上确立了分子一原子结构学说.19世纪60年代,俄国化学家门捷列夫发现了化学元素周期律,制定了化学元素周期表.
评述解这一类型题,应全面了解第一个标志性事件在整个化学发展史中的历史意义,学习时应针对这一类型的选择题全面掌握科技文化发展史.1年前查看全部
- (2010•淄博)英国化学家波义耳做了一个著名的实验,他将金属汞放在密闭的容器里煅烧,煅烧后的立刻打开容器盖进行称量,得
(2010•淄博)英国化学家波义耳做了一个著名的实验,他将金属汞放在密闭的容器里煅烧,煅烧后的立刻打开容器盖进行称量,得出的结论是物质的质量增加了.假设波义耳用铜代替金属汞以同样的方法进行实验,反应后容器内固体物质的质量增加了1g,计算有多少克铜参加了反应?请用简要的语言分析波义耳的实验导致他没有发现质量守恒定律的原因.
 爱你的人是我1年前1
爱你的人是我1年前1 -
 玩玩kk 共回答了25个问题
玩玩kk 共回答了25个问题 |采纳率100%解题思路:金属汞铜放在密闭的容器里煅烧,消耗容器内的氧气生成了氧化铜,根据质量守恒定律,固体增加的质量即参加反应的氧气的质量;利用氧气质量计算参加反应铜的质量;氧气的消耗使得密闭容器中气体减少,当打开容器盖时,空气进入补充消耗氧气的体积而使容器内物质总质量有所增加.由题意分析可知,增加的质量即为参加反应的氧气的质量设参加反应的铜的质量为x2Cu+O2△. 2CuO128 32x 1g128x=321g 解得x=4g答:参加反应的铜的质量为4g.容器打开...
点评:
本题考点: 根据化学反应方程式的计算;质量守恒定律及其应用.
考点点评: 根据反应只有氧气一种气体参加的特点,利用质量守恒定律,由反应前后固体质量变化确定参加反应氧气的质量是进行计算的基础.1年前查看全部
- 著名化学家罗伯特•波义耳在一次实验中,不小心将盐酸溅到紫罗兰花瓣上,过一会儿,发现紫色花瓣出现红点.他对此现
著名化学家罗伯特•波义耳在一次实验中,不小心将盐酸溅到紫罗兰花瓣上,过一会儿,发现紫色花瓣出现红点.他对此现象作出各种假设,经过多次实验验证,探究普遍规律,终于获得成功.以下是验证假设的实验方案,请你据此写出相应的假设:
(1) 将盐酸(HCl)分别滴到其他种类的花瓣上,观察现象.
其假设是__________________________________________________________.
(2) 将NaOH、Ba(OH)2溶液滴到花瓣上,观察现象.
其假设是__________________________________________________________.
(3) 将NaCl、KCl溶液滴到花瓣上,观察现象.
其假设是__________________________________________________________.
(4) 除以上角度,你还可提出什么假设,并写出验证方案.
______________________________________________________________________________________________________________________________________. chuenzhijiaozi1年前2
chuenzhijiaozi1年前2 -
 凌飞宇 共回答了20个问题
凌飞宇 共回答了20个问题 |采纳率95%HCl是否对其他的花瓣有效果.
氢氧根离子是否会有同样效果.
氯离子是否为关键因素.
这种变色的物质在植株的其他部位是否会存在.茎,叶,根等部位分别滴加盐酸.1年前查看全部
- 为什么波义耳的实验失败了 而拉瓦锡的成功了
为什么波义耳的实验失败了 而拉瓦锡的成功了
验证质量守恒的实验 dean781年前1
dean781年前1 -
 菜牙 共回答了15个问题
菜牙 共回答了15个问题 |采纳率100%由于金属在煅烧时会结合空气中的氧气,波义耳在煅烧后打开容器盖进行称量,就使外界的空气进入容器,所以反应后的固体质量增加了,因此导至波义耳未能发现质量守恒定律.
在1756年俄国化学家罗蒙诺索夫把金属锡放在密闭容器里煅烧,锡发生了化学变化,变成了白色的氧化锡,但是容器和容器里的物质的总质量,在锻烧前后并没有发生变化.经过反复的实验,都得到同样的结果,于是他认为在化学变化中物质的质量是守恒的.总结出了质量守恒定律:即参加反应的各物质的质量总和等于反应后生成的各物质的质量总和.
主要原因就是波义耳的实验装置使外界空气进入容器了!1年前查看全部
- (2007•十堰)根据物理学家波义耳1662年的研究结果:在温度不变的情况下,气球内气体的压强p(pa)与它的体积v(m
(2007•十堰)根据物理学家波义耳1662年的研究结果:在温度不变的情况下,气球内气体的压强p(pa)与它的体积v(m3)的乘积是一个常数k,即pv=k(k为常数,k>0),下列图象能正确反映p与v之间函数关系的是( )
A.
B.
C.
D.
 4月19日注册1年前1
4月19日注册1年前1 -
 现代赵热 共回答了19个问题
现代赵热 共回答了19个问题 |采纳率78.9%解题思路:根据题意有:pv=k(k为常数,k>0),故p与v之间的函数图象为反比例函数,且根据实际意义p、v应>0.∵pv=k(k为常数,k>0)
∴p=[k/v](p>0,v>0,k>0)
故选C.点评:
本题考点: 反比例函数的应用.
考点点评: 现实生活中存在大量成反比例函数的两个变量,解答该类问题的关键是确定两个变量之间的函数关系,然后利用实际意义确定其所在的象限.1年前查看全部
- 英国著名化学家波义耳正急匆匆地走向自己的实验室.缩句
 andy200703131年前4
andy200703131年前4 -
 深_海_蓝 共回答了17个问题
深_海_蓝 共回答了17个问题 |采纳率100%波义耳走向实验室.1年前查看全部
- 为探索物质在化学变化前后的质量关系,科学家们做了大量实验.1673年,英国物理学家波义耳做了一个有名的实验,他将金属放在
为探索物质在化学变化前后的质量关系,科学家们做了大量实验.1673年,英国物理学家波义耳做了一个有名的实验,他将金属放在密闭容器里煅烧,煅烧后他立即打开容器盖进行称量,结果发现反应后的固体质量增加了,该实验导致波义耳未能发现质量守恒定律,请你简要分析一下原因是什么?
 俺镇俺最衰1年前4
俺镇俺最衰1年前4 -
 bh1206 共回答了23个问题
bh1206 共回答了23个问题 |采纳率78.3%解题思路:化学反应遵循质量守恒定律,即参加反应的物质的质量之和,等于反应后生成的物质的质量之和.将金属放在密闭容器里煅烧时,金属和氧气反应生成氧化物,煅烧后立即打开容器盖进行称量时,容器外的空气进入,导致发现反应后的固体质量增加.
点评:
本题考点: 质量守恒定律及其应用.
考点点评: 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.1年前查看全部
- 打破沙锅问到底的人有哪些?除了《真理诞生于一百个问号之后》中的谢皮罗、波义耳和那位奥地利医生以外的人还有那些?
 haiboy_csu1年前1
haiboy_csu1年前1 -
 xukun235 共回答了19个问题
xukun235 共回答了19个问题 |采纳率94.7%伽利略 牛顿 鲁班1年前查看全部
- 300多年前,著名化学家波义耳发现了铁盐与没食子酸(结构式如图所示)的显色反应,并由此发明了蓝黑墨水.与制造蓝黑墨水相关
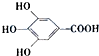 300多年前,著名化学家波义耳发现了铁盐与没食子酸(结构式如图所示)的显色反应,并由此发明了蓝黑墨水.与制造蓝黑墨水相关的基团可能是( )
300多年前,著名化学家波义耳发现了铁盐与没食子酸(结构式如图所示)的显色反应,并由此发明了蓝黑墨水.与制造蓝黑墨水相关的基团可能是( )
A.苯环
B.羧基
C.羧基中的羟基
D.酚羟基 wbc1979981年前1
wbc1979981年前1 -
 yckaixin 共回答了15个问题
yckaixin 共回答了15个问题 |采纳率93.3%解题思路:没食子酸含有酚羟基,可发生取代、氧化和颜色反应,含有羧基,具有酸性,可发生取代反应.没食子酸含有酚羟基,可发生取代、氧化和颜色反应,铁盐与没食子酸(结构式如图所示)的显色反应,应是铁盐与酚羟基发生颜色反应的结果.
故选D.点评:
本题考点: 有机物分子中的官能团及其结构.
考点点评: 本题考查有机物的结构和性质,侧重于有机物官能团的性质的考查,注意根据题给信息结合有机物的官能团的概念进行判断,题目难度不大.1年前查看全部
- 英国化学家波义耳做了一个著名的实验,他将金属汞放在密闭的容器里煅烧,煅烧后立刻打开容器盖进行称量得出的结论是物质的质量增
英国化学家波义耳做了一个著名的实验,他将金属汞放在密闭的容器里煅烧,煅烧后立刻打开容器盖进行称量得出的结论是物质的质量增加了.(1)假设波义耳用铜代替金属汞以同样的方法进行实验,反应后容器内固体物质的质量增加了1g,计算有多少克铜参加了反应?(2)请用简要的语言分析波义耳的实验导致他没有发现质量守恒定律的原因.
设Cu的质量为x
2Cu+O2==== 2CuO
 0卜1年前1
0卜1年前1 -
 ww文化研究社 共回答了19个问题
ww文化研究社 共回答了19个问题 |采纳率84.2%2Cu+O2==== 2CuO
反应后容器内固体物质的质量增加了1g,增加的质量即生成的氧化铜中氧元素的质量
设Cu的质量为x 则CuO的质量为 (X+1)g1年前查看全部
- 真理诞生于一百个问号之后中人物、发现现象、不断疑问、找到真理 谢皮罗教授 化学家波义耳 奥地利的一位医
 free2fly1年前1
free2fly1年前1 -
 transparent_nt 共回答了14个问题
transparent_nt 共回答了14个问题 |采纳率100%你到底想问什么问题?1年前查看全部
- 1673年,英国化学家波义耳做了这样一个实验
1673年,英国化学家波义耳做了这样一个实验
他将全金属汞放入一敞口容器里煅烧,冷却后进行称量,得出的结论是固体物质的质量增加了.该实验导致波义尔与质量守恒定律擦肩而过.1.是什么原因导致波义耳未能发现质量守恒定律?2.总结波义耳的失败经历,如果你在实验室要验证质量守恒定量,你该注意什么? nihaowohao9981年前1
nihaowohao9981年前1 -
 夜卿眸 共回答了19个问题
夜卿眸 共回答了19个问题 |采纳率84.2%在18世纪以前,由于人们对化学的认识非常局限,因此化学的发展是非常缓慢的,化学只是经验规律,直到18世纪末拉瓦锡引入定量化学并证明质量守恒定律后化学才得到突飞猛进的发展,因此,拉瓦锡被世界公认为最伟大的化学家,被称为现代化学之父.
由于对化学规律缺乏认识、实验条件的限制和经验的局限性,导致波义尔在做这个实验时得出了错误的结论,他几次做类似的实验都得到相同的结果,于是他下结论:在加热过程中有一种人看不见的火素(他自己定义的,当然实际上是不存在的)穿过容器壁进入加热物中,火素是有质量的,这样就使得物质的质量增加.这就是火素论,它在定量化学引入以前的一百多年里,一直被奉为经典,统治着化学界.后来被拉瓦锡彻底推翻.
在实验室做验证质量守恒定律时,如果实验条件不是很好,实验仪器不够精密,我觉得比较好的方法是尽量不要做产生气体的实验,如果产生的都是固体,没有气体逸出,那操作会更简单一些,结果也会精确一些.如果试验中有气体产生,就一定要求实验仪器气密性足够好,这样产生的误差就会小一些.1年前查看全部
- 早在17世纪,质量守恒定律发现之前,英国化学家波义耳曾经做过一个实验:在密闭的容器中燃烧金属时,得到了金属灰,然后打开容
早在17世纪,质量守恒定律发现之前,英国化学家波义耳曾经做过一个实验:在密闭的容器中燃烧金属时,得到了金属灰,然后打开容器盖,称量金属灰的质量,发现比原来金属质量增加了.这种变化并没有引起这位科学家的足够重视,也因此错过了一次取得重要科研成果的机会.这个实验的“异常”现象却成就了波义耳的后来者拉瓦锡--一位不畏权威、勇于创新、胆大精细的伟***国科学家.
(1)你认为波义耳实验中的金属灰质量比原金属质量大的原因是______;
(2)波义耳错过了发现质量守恒定律的机会的一个重要原因是称量方法的选择不合理.为此,你改进后的称量方法是______;
(3)你从波义耳的经历中得到的启发是______. linjm6191年前1
linjm6191年前1 -
 由由1314 共回答了27个问题
由由1314 共回答了27个问题 |采纳率88.9%解题思路:在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和,这个规律就叫做质量守恒定律.反应物中的气体的质量、生成物中气体的质量常因气态物质不易察觉而被忽略,形成质量不等的错觉.(1)金属燃烧是金属和氧气发生化合反应,生成金属氧化物.根据质量守恒定律可知,参加反应的金属与氧气的质量之和等于生成的金属氧化物的质量.生成的金属灰是金属氧化物,所以金属灰的质量比原来金属的质量增加了.
(2)不打开容器盖,分别称量反应前后密闭容器的质量.
(3)在研究、学习和工作中不能放过任何一个细节,一定要有科学的精神对待每个细微的变化等.
故答案为:(1)金属燃烧是金属和氧气发生的化合反应,生成金属氧化物.根据质量守恒定律可知,参加反应的金属与氧气的质量之和等于生成的金属氧化物的质量.生成的金属灰是金属氧化物,所以金属灰的质量比原来金属的质量增加了;
(2)分别称量反应前后密闭容器及其内容物的质量;
(3)在研究、学习和工作中不能放过任何一个细节,一定要有科学的精神对待每个细微的变化等.点评:
本题考点: 质量守恒定律及其应用.
考点点评: 在任何与周围隔绝的体系中,不论发生何种变化或过程,其总质量始终保持不变.1年前查看全部
- 英国化学家波义耳做了一个著名的实验,他将金属汞放在密闭的容器里煅烧,煅烧后立刻打开容器盖进行称量得出的结论是物质的质量增
英国化学家波义耳做了一个著名的实验,他将金属汞放在密闭的容器里煅烧,煅烧后立刻打开容器盖进行称量得出的结论是物质的质量增加了.(1)假设波义耳用铜代替金属汞以同样的方法进行实验,反应后容器内固体物质的质量增加了1g,计算有多少克铜参加了反应?(2)请用简要的语言分析波义耳的实验导致他没有发现质量守恒定律的原因.
设Cu的质量为x
2Cu+O2==== 2CuO
128 160
X (X+1)g
128/160=X/X+1
x=4g 艳姬1年前1
艳姬1年前1 -
 -飘渺的心- 共回答了17个问题
-飘渺的心- 共回答了17个问题 |采纳率82.4%2Cu+O2==== 2CuO
反应后容器内固体物质的质量增加了1g,增加的质量即生成的氧化铜中氧元素的质量
设Cu的质量为x 则CuO的质量为 (X+1)g1年前查看全部
- (2000•青岛)为探索物质在化学变化前后的质量关系,科学家做了大量实验.1673年,英国物理学家波义耳做了一个有名的实
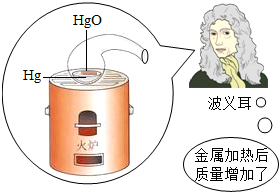 (2000•青岛)为探索物质在化学变化前后的质量关系,科学家做了大量实验.1673年,英国物理学家波义耳做了一个有名的实验,他将金属放在密闭容器里煅烧,煅烧后他立即打开容器进行称量,结果发现反应的固体质量增加了.该实验导致波义耳未能发现质量守恒定律,请你简要分析一下其中的原因是什么?
(2000•青岛)为探索物质在化学变化前后的质量关系,科学家做了大量实验.1673年,英国物理学家波义耳做了一个有名的实验,他将金属放在密闭容器里煅烧,煅烧后他立即打开容器进行称量,结果发现反应的固体质量增加了.该实验导致波义耳未能发现质量守恒定律,请你简要分析一下其中的原因是什么?  yanyanjiaxin1年前1
yanyanjiaxin1年前1 -
 2008mimi2008 共回答了17个问题
2008mimi2008 共回答了17个问题 |采纳率94.1%解题思路:空气中的氧气可以和金属反应生成氧化物使固体质量增加,根据质量守恒定律分析解答即可.密闭容器中有氧气,在加热后会使固体质量增加,由于称量的是反应前后的固体质量而没有考虑气体的质量变化.故答案为:
波义耳没有考虑参加反应的空气中的氧气质量点评:
本题考点: 质量守恒定律的实验探究;空气的成分及各成分的体积分数.
考点点评: 在验证质量守恒定律时,需要考虑反应物质量和生成物质量之间的关系,本题较灵活,难度不大.1年前查看全部
- 课文中所提到的谢皮罗教授,波义耳,奥地利医生,他们都是因为善于提问,思考,最终才有所发现,有所创造.
课文中所提到的谢皮罗教授,波义耳,奥地利医生,他们都是因为善于提问,思考,最终才有所发现,有所创造.
科学史上,这样的示例还有很多,你能举出两例忙?8512(帮我一下) ctcp1年前1
ctcp1年前1 -
 wtydtybk 共回答了18个问题
wtydtybk 共回答了18个问题 |采纳率77.8%英国的牛顿通过苹果落地发现了万有引力,德国的欧姆发现电流规律创立了欧姆定律.希望对你有帮助~1年前查看全部
- 科学家的重要成就波义耳、拉瓦锡、道尔顿、阿伏伽德罗、门捷列夫在化学学科中的重要成就是什么尽量简短
 万木复苏1年前2
万木复苏1年前2 -
 ampop 共回答了18个问题
ampop 共回答了18个问题 |采纳率94.4%波义耳:石蕊试纸和黑墨水的发明建立了元素的新定义:不能用化学方法再分解的简单物质才是元素实验化学的创始人门捷列夫:元素周期律的发现成功地预测了镭的原子数及其性质,且研制了镭制品门氡(液态镭).拉瓦锡:拉...1年前查看全部
- 关于波义耳发现酸碱指示剂的几个问题.明天试卷就交了
关于波义耳发现酸碱指示剂的几个问题.明天试卷就交了
1.当波义耳发现紫罗兰花瓣变成红色是,提出的猜测是______________.
2.波义耳通过各种酸与紫罗兰花的实验,得出的结论是_____
3.你认为波义而耳发现石蕊试剂是偶然的吗?请说明理由.________
4.玻璃清洁剂,洁厕灵,肥皂液,洗发水中可以使石蕊试剂变成红色的是、? lj95021年前1
lj95021年前1 -
 zedu001 共回答了18个问题
zedu001 共回答了18个问题 |采纳率88.9%稀的酸性物质可能会使紫罗兰花瓣变红色
紫罗兰花的浸出液可用于检验溶液是否呈酸性1年前查看全部
- 化学反应后为什么质量会增加波义耳的实验
 kkkkvvvv1年前2
kkkkvvvv1年前2 -
 gdww66 共回答了16个问题
gdww66 共回答了16个问题 |采纳率100%化学反应遵循质量守恒,若是有气体参与反应且气体质量没有被算在反应物质量中,实验测得反应后反应物的质量就会增加.但实际参与反应的反应物的总质量和生成物的重质量是相等的1年前查看全部
- 像谢皮罗、波义耳、奥地利医生,善于提问、思考最终才有所发现、创造的例子。在科学史上,能否举出两例来。谢谢,请快点我急用。
 zhuzhu66361年前1
zhuzhu66361年前1 -
 wcyfr40818 共回答了15个问题
wcyfr40818 共回答了15个问题 |采纳率66.7%鲁班上山,手被树叶划伤,后来发明了锯;牛顿在树下,被苹果砸了头,后来现了万有引力定律。1年前查看全部
- 为探索物质在化学变化前后的质量关系,科学家做了大量实验.1673年,英国物理学家波义耳做了一个有名的实验.他将金属放在密
为探索物质在化学变化前后的质量关系,科学家做了大量实验.1673年,英国物理学家波义耳做了一个有名的实验.他将金属放在密闭容器中煅烧,煅烧后他立即打开容器盖进行称量,结果发现反应后的固体质量增加了.该实验导致波义耳未能发现质量守恒定律.之后俄国化学家罗蒙诺索夫在密闭玻璃瓶内燃烧金属,发现反应后质量不变,由此得出反应前后的质量守恒.
这两位科学家的实验相似,为何结论不同?某研究小组沿着科学家的足迹进行探究,请你完成以下相关内容:
(1)【交流讨论】两位科学家得出不同的结论究竟与哪些实验因素有关呢?
(2)【提出假设】若用同种金属,同一容器进行实验,两位科学家得出不同的结论主要是由于______的缘故.
(3)【实验验证】已知:钠在空气中受热燃烧生成过氧化钠固体.
(4)【得出结论】假设成立.操作步骤及实验现象 简答 (1)在底部铺有细沙的锥形瓶中,放入一小块金属钠,塞紧橡皮塞,称量,用砝码使天平平衡. 称量前需______. (2)取下锥形瓶,放在垫有石棉网的三角架上微热,观察到金属钠着火燃烧,冷却后,再称量. 称量时观察到______. (3)将锥形瓶瓶塞取出一会儿后,盖上瓶塞,再称量. 称量时观察到______.
(5)依据以上实验事实,解释两位科学家的实验结论:______. sunskyjn1年前1
sunskyjn1年前1 -
 爪子印 共回答了19个问题
爪子印 共回答了19个问题 |采纳率94.7%解题思路:(1)根据可能与反应容器是否密闭有关以及可能与反应物有关进行解答
(2)根据用同种金属,同一容器进行实验,两位科学家得出不同的结论主要是由于反应容器敞开与密闭的差异进行解答;
(3)根据称量物质质量的注意事项以及钠燃烧消耗氧气进行解答;
(5)根据实验是否在密闭容器内进行解答.(1)将金属放在密闭容器里煅烧,煅烧后他立即打开容器盖进行称量,发现反应后的固体质量增加了,是因为金属在煅烧时会与空气中的氧气反应产生固体氧化物,增加了氧气的质量,所以两位科学家得出不同的结论究竟可能与反应容器是否密闭有关或可能与反应物有关;
(2)用同种金属,同一容器进行实验,两位科学家得出不同的结论主要是由于反应容器敞开与密闭的差异;
(3)由称量物质质量的注意事项可知,称量前需检查天平是否平衡;由质量守恒定律可知,反应前后物质的质量相等,所以取下锥形瓶,放在垫有石棉网的三角架上微热,观察到金属钠着火燃烧,冷却后,再称量.观察到天平保持平衡;将锥形瓶瓶塞取出一会儿后,空气会进入,所以盖上瓶塞,再称量,称量时观察到天平指针向左偏移;
(5)依据以上实验事实可知,波义尔在敞口容器中实验,消耗氧气后,又不断补充空气,因此质量增加;而罗蒙诺索夫是在密闭容器中进行,质量不变.
故答案为:(1)可能与反应容器是否密闭有关或可能与反应物有关;
(2)反应容器敞开与密闭的差异;
(3)检查天平是否平衡;天平保持平衡;天平指针向左偏移;
(5)波义尔在敞口容器中实验,消耗氧气后,又不断补充空气,因此质量增加;而罗蒙诺索夫是在密闭容器中进行,质量不变.点评:
本题考点: 质量守恒定律的实验探究.
考点点评: 本题考查质量守恒定律的内容以及应用,具有新颖性,同时也考查了学生的分析和应变能力.1年前查看全部
- 波义耳试验在一个密闭的玻璃容器中燃烧金属,得到金属灰,称量后发现金属灰的质量比原质量金属质量增加了.
波义耳试验在一个密闭的玻璃容器中燃烧金属,得到金属灰,称量后发现金属灰的质量比原质量金属质量增加了.
解释增加的原因,和改进他的称量方法以验证质量守恒定律.我有急用. march1841年前1
march1841年前1 -
 js12688 共回答了18个问题
js12688 共回答了18个问题 |采纳率88.9%与氧气反应得的物质有氧气的质量在内,所以大于了原质量.
测出反应前后密闭容器内气体的质量,则金属质量+前气体质量=金属灰质量+后气体质量
望采纳1年前查看全部
- 英国著名化学家波义耳正急匆匆地向自己的实验室走去
英国著名化学家波义耳正急匆匆地向自己的实验室走去
到底是“波义耳走去”还是“波义耳向实验室走去” oo成仙1年前2
oo成仙1年前2 -
 邪神一少 共回答了14个问题
邪神一少 共回答了14个问题 |采纳率100%“波义耳向实验室走去”1年前查看全部
- 为探索物质在化学变化前后的质量关系,科学家们做了大量实验.1673年,英国物理学家波义耳做了一个有名的实验,他将金属放在
为探索物质在化学变化前后的质量关系,科学家们做了大量实验.1673年,英国物理学家波义耳做了一个有名的实验,他将金属放在密闭容器里煅烧,煅烧后他立即打开容器盖进行称量,结果发现反应后的固体质量增加了,该实验导致波义耳未能发现质量守恒定律,请你简要分析一下原因是什么?
 lansono1年前3
lansono1年前3 -
 lona007 共回答了18个问题
lona007 共回答了18个问题 |采纳率100%解题思路:化学反应遵循质量守恒定律,即参加反应的物质的质量之和,等于反应后生成的物质的质量之和.将金属放在密闭容器里煅烧时,金属和氧气反应生成氧化物,煅烧后立即打开容器盖进行称量时,容器外的空气进入,导致发现反应后的固体质量增加.
点评:
本题考点: 质量守恒定律及其应用.
考点点评: 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.1年前查看全部
- 17世纪的一个夏天,英国著名化学家波义耳匆匆地向自己的实验室走去.缩句
 tinytinyman1年前1
tinytinyman1年前1 -
 粉色饭团 共回答了15个问题
粉色饭团 共回答了15个问题 |采纳率66.7%波义耳向实验室走1年前查看全部
- 这一奇怪的现象以及一连串的问题,促进波义耳进行了许多实验这句话怎样修改
 没钱不谈爱1年前1
没钱不谈爱1年前1 -
 曾经最美洪 共回答了24个问题
曾经最美洪 共回答了24个问题 |采纳率79.2%这一奇怪的现象以及一连串的问题,促使波义耳进行了许多实验.(促进改为促使)1年前查看全部
- 早在1673年,英国化学家波义耳在一个敞口容器中加热一种金属,结果发现反应后的质量增加了.
早在1673年,英国化学家波义耳在一个敞口容器中加热一种金属,结果发现反应后的质量增加了.
(1)波义耳的实验结果是否违反质量守恒定律?简析原因.
(2)试从原子的角度解释质量守恒定律.
(3)碘的某种氧化物可以用来测定空气中CO的污染程度.已知1分子的该氧化物可将5分子的CO氧化为CO2,同时生成1分子的I2,则该碘的氧化物的化学式为______. mlwsl1年前4
mlwsl1年前4 -
 kysfnkd 共回答了19个问题
kysfnkd 共回答了19个问题 |采纳率89.5%解题思路:根据质量守恒定律:本题中反应后的容器中物质的质量增加的原因是:金属与氧气结合,所以后来质量会增加,这正是对质量守恒定律的应用.根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.根据在化学反应中,反应前后原子的种类没有改变,数目没有增减.(1)因为参加反应的金属和参加反应的氧气的质量之和等于反应后生成物的质量,因此反应后生成的生成物的质量比反应前的质量大了.这个实验仍然符合质量守恒定律.
(2)化学反应的过程,就是参加反应的各物质(反应物)的原子,重新组合而生成其他物质的过程.在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变.
(3)根据反应物中元素种类及原子个数分别为C,5;O,10;已知生成物中元素种类及原子个数为I,2;比较分析知道X中含有I,2;O,5;从而知道X的化学式为I2O5
故答案为:
(1)不违反.金属与空气中的氧气反应,生成物的质量应该等于金属质量与氧气质量之和.
(2)在一切化学反应中,反应前后原子的种类、数目均没有改变,原子的质量也不改变.
(3)I2O5点评:
本题考点: 质量守恒定律及其应用;有关化学式的计算和推断.
考点点评: 该题要求学生利用化学知识解决实际问题,既考查了学生学以致用的能力,又能让学生感觉到生活中化学的存在,认识到化学的重要性,产生对化学的学习兴趣.1年前查看全部
- 缩句:英国著名化学家波义耳正急匆匆地向自己的实验室走去
 wwlian195511年前12
wwlian195511年前12 -
 liu3213662 共回答了23个问题
liu3213662 共回答了23个问题 |采纳率100%波义耳向实验室走去1年前查看全部
- 1662年波义耳提出,在温度不变的情况下,气体的体积和他所受的压力成正比.19世纪雷尼奥发
1662年波义耳提出,在温度不变的情况下,气体的体积和他所受的压力成正比.19世纪雷尼奥发
1662年波义耳提出,在温度不变的情况下,气体的体积和他所受的压力成正比.19世纪雷尼奥发现,除了不能液化的“真正的”气体即氢气外,其它气体在温度增加到接近其液化点时,这一定律就不适用了.后来人们发现,不能液化的“真正”气体是不存在的,所有气体都可以变成液化状态.但是人们并未因此而抛弃波义耳定律.这一事实说明( )
a 真理与谬误具有同一性
b 人不能获得真理
c 真理总是相对的
d 真理取决于观察者 ynp888881年前2
ynp888881年前2 -
 e55298 共回答了20个问题
e55298 共回答了20个问题 |采纳率90%c当然不对,比如说光速大于声速,这一真理就是绝对正确的1年前查看全部
- 导致波义耳未能发现质量守恒定律的原因
 asml1年前1
asml1年前1 -
 清水无香1 共回答了19个问题
清水无香1 共回答了19个问题 |采纳率94.7%因为金属燃烧后产生了固体的氧化物,这个氧化物的质量等于之前的金属和参加反应的氧气的质量的和,所以反应后质量增加了..
我记得好像是Hg在O2中燃烧,生成HgO,最后他打开密闭容器中测量的,氧气逸出,HgO肯定大于原来Hg的质量啦~1年前查看全部
- 英国著名化学家波义耳正急匆匆地向自己的实验室走去.(缩句)
 h5205021年前4
h5205021年前4 -
 lvxiaoying 共回答了16个问题
lvxiaoying 共回答了16个问题 |采纳率81.3%波义耳向实验室走.1年前查看全部
- 波义耳定理问题压力*体积=一常数那常数为多少,与温度的大小有什么关系
 hellojohnzzy1年前2
hellojohnzzy1年前2 -
 野鹤闲鸥 共回答了16个问题
野鹤闲鸥 共回答了16个问题 |采纳率93.8%PV=nRT
波义耳定理研究的是定量定温,所以n和T是一定的
R是常数,数值为R=8.3141年前查看全部
大家在问
- 1C.D在线段AB上,且三角形PCD是等边三角形,当AC.CD.DB满足什么关系时,三角形ACP相似于三角形PDB
- 2英语倍数怎么表达全面有讲解O(∩_∩)O谢谢
- 3当____太大,_____太低时,波义耳定律就不适用了
- 4如图正三角形ABC中,D、E分别在BC、AC上,AE=CD=6,AD=9.求PE的长度
- 5有氧呼吸是不是就是糖的有氧分解
- 6用苯胺作原料,还可以用其他什么方法制备乙酸苯胺?写出反应方程式
- 7利用铝、盐酸、氢氧化钠来制备氢氧化铝的最节省原料的方法中发生的离子方程式
- 8请问下面这个故事为什么要列举“孙叔敖杀两头蛇”的故事呢?是为了什么?
- 9phone _ a fire engine 1.to 2.for 3.in 4.with
- 10在求二重积分时怎么确定是X型还是Y型?
- 11盐水中为什么更易生锈
- 12英语中倍数如何表达?
- 13简述马克思主义哲学的物质范畴及其意义
- 14HCL与NA2CO3的热化学方程式
- 15育才小学36人去公园玩,公园门口的‘购票须知’写道;‘凭票入园.儿童票没张8元,40张开始按原价的5分之4
