碳酸氢钙在水中的溶解度是多少?如何提高?
 sameo2022-10-04 11:39:541条回答
sameo2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 Baby小天使 共回答了15个问题
Baby小天使 共回答了15个问题 |采纳率93.3%- 碳酸氢钙在水中的溶解度
16.16 g/100 mL (0 °C)
16.6 g/100 mL (20°C)
17.05 g/100 mL (40°C)
17.5 g/100 mL (60°C)
17.95 g/100 mL (80°C)
18.4 g/100 mL (100 °C)
适当升温可提高溶解度 - 1年前
相关推荐
- 硬水中含有较多的可溶性的钙镁化合物,其中钙的化合物为碳酸氢钙……
硬水中含有较多的可溶性的钙镁化合物,其中钙的化合物为碳酸氢钙……
硬水中含有较多的可溶性的钙镁化合物,其中钙的化合物为碳酸氢钙,受热容易分解,若对其加热会生成水和大量的气体,还有一种难溶性化合物,该化合物是水垢的成分之一.
(一)提出问题
探究碳酸氢钙受热分解的生成物.
(二)猜想
小红认为生成物的气体可能是二氧化碳,你认为生成物的固体可能是________.
(三)收集证据
水垢的主要成分是碳酸钙,它能与稀盐酸反应放出使澄清石灰水变浑的气体.
(四)设计实验方案
请你设计出简单的实验方案,来验证上述猜想是否正确.
(1)_____________________
(2)_______________________
(五)观察与结论
(1)如果小红和你的猜想正确,实验现象应该分别是___________、________________.
(2)写出碳酸氢钙受热分解的文字表达式._____________________________________ kk4051年前2
kk4051年前2 -
 孤独风中 共回答了22个问题
孤独风中 共回答了22个问题 |采纳率86.4%(2)碳酸钙
(4)将产生的无嗅气体通入澄清石灰水,在固体里加入稀盐酸,将产生无嗅气体通入澄清石灰水
(5)变浑浊,变浑浊
碳酸氢钙=碳酸钙+二氧化碳+水
条件加热1年前查看全部
- 碳酸钙与碳酸氢钙有什么区别?
 alice_qin1年前1
alice_qin1年前1 -
 dinz79 共回答了24个问题
dinz79 共回答了24个问题 |采纳率87.5%元素组成上:碳酸钙不含氢,而碳酸氢钙含有氢.溶解度:碳酸钙难溶于水,而碳酸氢钙易溶于水.稳定性:碳酸钙的分解温度大于碳酸氢钙.PH:碳酸钙溶液>碳酸氢钙溶液.1年前查看全部
- 碳酸氢钙是强电解质还是弱的
 黑猫市长1年前1
黑猫市长1年前1 -
 yy明月酒 共回答了15个问题
yy明月酒 共回答了15个问题 |采纳率86.7%强电解质1年前查看全部
- 下列物质的不饱和溶液能通过加热蒸发的方法使之变成饱和溶液的是?A氯化钠 B盐酸 C硅酸 D碳酸氢钙
 tobeoding1年前1
tobeoding1年前1 -
 8316472 共回答了14个问题
8316472 共回答了14个问题 |采纳率92.9%A 碳酸氢钠和硅酸加热易分解,而盐酸加热易挥发1年前查看全部
- 饱和碳酸氢钙中加饱和石灰水,这里的饱和起什么说明作用
 周润发之弟1年前1
周润发之弟1年前1 -
 fuf4321 共回答了29个问题
fuf4321 共回答了29个问题 |采纳率96.6%两种饱和溶液浓度不一样,石灰水很稀,相比之下碳酸氢钠更浓即石灰水少量,生成碳酸钙和纯碱和水1年前查看全部
- :碳酸氢钙和碳酸氢钠反应少 量氢氧根反应
:碳酸氢钙和碳酸氢钠反应少 量氢氧根反应
过量:Ca(HCO3)2+2NaOH=
CaCO 3↓+2H2O+Na2CO3,过量
的NaHCO3与Ca(OH)2反应:2NaHCO3
+Ca(OH)2=CaCO3↓+Na2CO3+2 H2O,
,为什么同样是碳酸氢根与氢氧
根反应,一个生成的是碳酸氢钠
,一个却生成碳酸钠? 朵月1年前3
朵月1年前3 -
 幸福由自己创造 共回答了14个问题
幸福由自己创造 共回答了14个问题 |采纳率92.9%①、Ca(HCO3)2和NaOH反应过程理解为两个过程:先HCO3- + OH- =H20+ CO3 2-,后Ca2+ + CO32- =CaCO3↓.由于一个Ca(HCO3)2中有2个HCO3-,而一个NaOH分子中只有一个OH-,故与二者量的相对多少有关.这种方程式在书写时,先抓住中心反应,将量少的取1个分子,由其离子数确定其它离子数目.本题中如果Ca(HCO3)2少时,一个Ca(HCO3)2电离出2个HCO3-和1个Ca2+,2个HCO3-将和2个OH-反应生成2个H20和2个CO3 2-,其中1个CO3 2- 和1个Ca2+反应生成1个CaCO3分子,故总反应为:Ca2+ +2HCO3- + 2OH- =CaCO3↓ +2H20 + CO3 2- .如果NaOH少时,一个NaOH分子电离出一个OH-,一个OH-只与一个HCO3-反应生成1个H20和1个CO3 2-,1个CO3 2-与1个Ca2+生成一个CaCO3分子,总反应为:Ca2+ +HCO3- + OH- =CaCO3↓+H20 .
②、可以根据“取一”的原则:
氢氧化钠少量时,NaOH取一,则
只能消耗1个HCO3-,故
Ca2+ + HCO3- + OH- =CaCO3↓ + H20
氢氧化钠过量时,即碳酸氢钙少量
,因而碳酸氢钙取一,每个碳酸氢
钙中含有2个HCO3-,可消耗2个OH
-,故:
Ca2+ + 2HCO3- + 2OH- =CaCO3↓ + 2H20
+ CO3 2-1年前查看全部
- 含有较多可溶性钙、镁化合物的水称为硬水。这些化合物多以碳酸氢钙、碳酸氢镁的形式溶于水。当加热含有这些物质的硬水时,便生成
含有较多可溶性钙、镁化合物的水称为硬水。这些化合物多以碳酸氢钙、碳酸氢镁的形式溶于水。当加热含有这些物质的硬水时,便生成了碳酸钙沉淀、碳酸镁沉淀、水和二氧化碳,使水中的可溶性钙、镁化合物大大减少,而生成的沆淀可称作锅垢。据此回答下列问题:
(1)生成锅垢的变化,属于____(填“物理”或“化学”)变化,反应的基本类型为____。
(2)向煮沸后的水中滴加肥皂水,很少生成浮渣,为什么?________________________。 AngelPhoebe1年前1
AngelPhoebe1年前1 -
 lhd1018 共回答了20个问题
lhd1018 共回答了20个问题 |采纳率80%(1)化学;分解反应
(2)因溶有的钙、镁化合物煮沸后已经沉降下来,所以很少生成浮渣1年前查看全部
- 怎么样制作碳酸氢钙,什么与碳酸钙反应不与铁反应
怎么样制作碳酸氢钙,什么与碳酸钙反应不与铁反应
有什么化学性质比较稳定的酸,可以是有机酸,其酸性比Ca(HCO3)2(碳酸氢钙)差,比碳酸钙酸性强.
也就是把此酸跟碳酸钙混合,生成碳酸氢钙,而又不会与碳酸氢钙进一步反应生成钙盐.
有什么酸可以跟碳酸钙反应生成盐,而又不与铁反应.或者酸与铁反应生成难溶物,可以阻止与铁的进一步反应.
回答完美追加100. cashchung1年前1
cashchung1年前1 -
 xinruo2008 共回答了21个问题
xinruo2008 共回答了21个问题 |采纳率90.5%氢氰酸、氢硫酸、硼酸酸性比Ca(HCO3)2差,在水溶液中碳酸钙无酸性.不过如果想做碳酸氢钙,最好还是用碳酸(二氧化碳+水)(前两个剧毒,硼酸会四聚成四硼酸,比碳酸强).
第二个可以用磷酸(磷酸盐也用于钢铁防腐(络合作用))
另外纠正一点,质子论中,酸性比酸A差的不能与A的共轭碱反应,故问题应改为:“有什么化学性质比较稳定的酸,可以是有机酸,其酸性比碳酸差,比碳酸氢根酸性强?”(我是按改后回答的)1年前查看全部
- 下列离子方程式正确的是( )A.往碳酸氢钙溶液中滴入少量氢氧化钠溶液:OH-+HCO3-+Ca2+=CaCO3↓+H2
下列离子方程式正确的是( )
A.往碳酸氢钙溶液中滴入少量氢氧化钠溶液:OH-+HCO3-+Ca2+=CaCO3↓+H2O
B.将一小块金属钠投入到硫酸铜溶液中:2Na+Cu2+═Cu+2Na+
C.NaHCO3溶液显碱性:HCO3-+H2O OH-+H2CO3
OH-+H2CO3
D.氯气溶解于水:Cl2+H2O 12H++Cl-+ClO-
12H++Cl-+ClO-  是大鄂人1年前1
是大鄂人1年前1 -
 茉莉花_2004 共回答了10个问题
茉莉花_2004 共回答了10个问题 |采纳率80%解题思路:A、往碳酸氢钙溶液中滴入少量氢氧化钠溶液,碳酸氢根有剩余,反应生成碳酸钙、碳酸氢钠与水.
B、钠不能置换铜,应生成硫酸钠、氢氧化铜与氢气.
C、碳酸氢根水解与电离,碳酸氢根的水解沉淀等于电离程度,使溶液呈碱性.
D、次氯酸是弱电解质,应写成化学式形式.A、往碳酸氢钙溶液中滴入少量氢氧化钠溶液,碳酸氢根有剩余,反应生成碳酸钙、碳酸氢钠与水,离子方程式为OH-+HCO3-+Ca2+=CaCO3↓+H2O,故A正确;
B、钠先与水反应生成氢氧化钠与氢气,氢氧化钠再与硫酸铜反应生成氢氧化铜沉淀与硫酸钠,反应总的离子方程式为2Na+Cu2++2H2O═2Na++Cu(OH)2↓+H2↑,故B错误;
C、碳酸氢根水解HCO3-+H2O OH-+H2CO3,同时碳酸氢根发生电离HCO3-
OH-+H2CO3,同时碳酸氢根发生电离HCO3- H++CO32-,碳酸氢根的水解沉淀等于电离程度,使溶液呈碱性,故C错误;
H++CO32-,碳酸氢根的水解沉淀等于电离程度,使溶液呈碱性,故C错误;
D、次氯酸是弱电解质,应写成化学式,离子方程式应为Cl2+H2O=H++Cl-+HClO,故D错误.
故选:A.点评:
本题考点: 离子方程式的书写.
考点点评: 考查离子方程式的书写与正误判断,难度中等,是对学生综合能力与所学知识运用的考查,掌握元素化合物知识与离子方程式的书写与判断方法.1年前查看全部
- 碳酸氢钙的溶解度是多少?
 一枪甩翻1年前1
一枪甩翻1年前1 -
 aigangqin 共回答了15个问题
aigangqin 共回答了15个问题 |采纳率80%碳酸氢钙的溶解度(16.60/100g纯水)的溶解度比碳酸钙的溶解度(0.003/100g 纯水)大的多1年前查看全部
- C.向偏铝酸钠溶液中通人过量CO2:2AlO2-+CO2+3H2O 2Al(OH)3↓+CO32- D.碳酸氢钙溶液中加
C.向偏铝酸钠溶液中通人过量CO2:2AlO2-+CO2+3H2O 2Al(OH)3↓+CO32- D.碳酸氢钙溶液中加人少量NaOH溶
C.向偏铝酸钠溶液中通人过量CO2:
2AlO2-+CO2+3H2O 2Al(OH)3↓+CO32-
D.碳酸氢钙溶液中加人少量NaOH溶液:
Ca2++2HCO3-+2OH- CaCO3↓+CO32-+2H2O
为什么C、D错 河南文化1年前1
河南文化1年前1 -
 清浊墨 共回答了18个问题
清浊墨 共回答了18个问题 |采纳率94.4%C、过量的二氧化碳的话生成碳酸氢根;
D、少量NaOH的话Ca2++HCO3-+OH- == CaCO3↓+H2O1年前查看全部
- 为什么碳酸氢钙和氢氧化钙能反映?不是都有钙吗
为什么碳酸氢钙和氢氧化钙能反映?不是都有钙吗
老师说阳离子都有Ca,所以不能反映,但是网上都说能反映
这个老师的水平是不是有问题啊?
还有,都知道,向石灰水中通入CO2,产生沉淀,继续通,沉淀与水、CO2反应,生成碳酸氢钙,如果能与氢氧化钙反应,有生成碳酸钙和水,就是又产生沉淀……是不是就会不断循环啊…… rainbowlight1年前1
rainbowlight1年前1 -
 slk2004 共回答了26个问题
slk2004 共回答了26个问题 |采纳率92.3%1 是能反应的 因为碳酸氢根可以电离出氢离子 虽然两很少 但会跟氢氧根反应 产生碳酸根 最终生成碳酸钙 如果你不能理解 那你应该知道碳酸氢根是两性的离子 可以与酸反应 也可以跟碱反应.
2 你的第二个问难题 CO2通入石灰水中 产生沉淀 随着通入量增多 沉淀增多 当完全消耗掉氢氧化钙后 不在产生沉淀.再继续通入CO2,CO2与碳酸钙反应 生成碳酸氢钙 慢慢减少 最终沉淀消失1年前查看全部
- 下列反应的离子方程式正确的是?向碳酸氢钙溶液中加入过量氢氧化钠 的离子方程式是什么?Ca2+ + 2HCO3- + 2O
下列反应的离子方程式正确的是?
向碳酸氢钙溶液中加入过量氢氧化钠 的离子方程式是什么?
Ca2+ + 2HCO3- + 2OH- = CaCO3↓ + CO32- + 2H2O
硫酸溶液中加入氢氧化钡溶液
Ba2+ + SO42- + H+ OH- =BaSO4↓ + H2O
我觉得这两个都对的啊 有哪个错的吗? dicky1311年前6
dicky1311年前6 -
 夕语 共回答了18个问题
夕语 共回答了18个问题 |采纳率88.9%向碳酸氢钙溶液中加入过量氢氧化钠,是对的,氢氧根过量
硫酸溶液中加入氢氧化钡溶液,不对,氢氧化钡里有两个氢氧根,如果完全反应,则钡离子和氢氧根之比应该是1比2,所以方程式中应该是连个氢氧根,同理,也应该是两个氢离子才对.1年前查看全部
- 水中溶解的碳酸氢钙和碳酸钙和碳酸之间起什么样的反应?
 mahui_19801年前1
mahui_19801年前1 -
 wlzwyn661215 共回答了21个问题
wlzwyn661215 共回答了21个问题 |采纳率81%CACO3+H2O+CO2=CA(HCO3)2
CA(HCO3)2=CACO3+H2O+CO21年前查看全部
- 问下哈,那个碳酸氢钙和氢氧化钙反应足量与少量时都反应生成什么?
问下哈,那个碳酸氢钙和氢氧化钙反应足量与少量时都反应生成什么?
那为什么老师给我们出的这套题上有足量和少量两种情况?我们老师很牛X,
碳酸氢钠和碳酸氢钙都有,而且都是和足量少量的氢氧化钙反应,4个! 井龙21年前2
井龙21年前2 -
 yatian9999 共回答了21个问题
yatian9999 共回答了21个问题 |采纳率95.2%抄错了吧.要是碳酸氢钠还是可以的:
NaHCO3+Ca(OH)2=CaCO3↓+NaOH+H2O
2NaHCO3+Ca(OH)2=CaCO3↓+Na2CO3+2H2O
要是碳酸氢钙,只可能有一个,酸式盐可与碱反应生成正盐和水.
像这种老师,一定要好好质疑他,实在不成我跟他说.1年前查看全部
- 哪位好心的娃来教教俺...分别向下列物质的水溶液中加入少量过氧化钠固体,不会出现浑浊现象的是?A氢硫酸溶液B碳酸氢钙溶液
哪位好心的娃来教教俺...
分别向下列物质的水溶液中加入少量过氧化钠固体,不会出现浑浊现象的是?
A氢硫酸溶液
B碳酸氢钙溶液
C饱和碳酸氢钠溶液
D饱和氯化钠溶液
能把每个选项都解释下么.. 安小可1年前3
安小可1年前3 -
 亲亲我们的宝贝 共回答了21个问题
亲亲我们的宝贝 共回答了21个问题 |采纳率90.5%A不会出现混浊,生成水和硫化钠B中碳酸氢根与氢氧根生成碳酸根,碳酸根与钙离子生成难溶的碳酸钙C选项中理论上讲过氧化钠首先与水发生反应,水减少,饱和碳酸氢钠会有少量析出(也可能生成过饱和溶液,根据际情况而定),...1年前查看全部
- 写出下列离子方程式1碘化钾与氯气2氯化铁与氨水3碳酸氢钙与稀硝酸4氯气与冷的氢氧化钠
 eleeke1年前2
eleeke1年前2 -
 滇西女孩 共回答了11个问题
滇西女孩 共回答了11个问题 |采纳率81.8%1.Cl2+2I-=I2+2Cl-
2.Fe3+ +3NH3·H2O=Fe(OH)3↓+3NH4+
3.HCO3- +H+=H2O+CO2↑
4.Cl2+2OH-=Cl- +ClO- +H2O1年前查看全部
- 氢氧化钙一步转化成碳酸氢钙化学方程式和离子方程式
 lzh60699941年前1
lzh60699941年前1 -
 星瓶子 共回答了15个问题
星瓶子 共回答了15个问题 |采纳率93.3%Ca(OH)2 + 2CO2 == Ca(HCO3)2
OH- + CO2 == HCO3-1年前查看全部
- 1.碳酸钠在水中的电离方程式 2.硫酸 3.硝酸 4.硝酸铜 5.碳酸氢钙 6.硝酸铵 7.硫酸铝 8.高锰酸钾 9.氯
1.碳酸钠在水中的电离方程式 2.硫酸 3.硝酸 4.硝酸铜 5.碳酸氢钙 6.硝酸铵 7.硫酸铝 8.高锰酸钾 9.氯酸钾 10.氢氧化钙 11.磷酸钠 12.硝酸钡 13 氯化铁 14.氯化铵
 wyjie20021年前1
wyjie20021年前1 -
 liulimei 共回答了23个问题
liulimei 共回答了23个问题 |采纳率82.6%1.Na2CO3==2Na++HCO3- 2.H2SO4==2H++SO42- 3.HNO3==H++NO3- 4.Cu(NO3)2==Cu2++2NO3- 5.Ca(HCO3)2==Ca2++2HCO3- 6.NH4NO3==NH4++NO3- 7.Al2(SO4)3==2Al3++3SO42- 8.KMnO4==K++MnO4- 9.KCl==K++Cl- 10.Ca(OH)2==Ca2++2OH- 11.Na3PO4==3Na++PO43- 12.Ba(NO3)2==Ba2++2NO3- 13.FeCl3==Fe3++3Cl- 14.NH4Cl==NH4++Cl-1年前查看全部
- 二氧化碳 和漂白粉反应 生成碳酸钙还是碳酸氢钙 已知酸性 H2co3>hclo>hco3-
二氧化碳 和漂白粉反应 生成碳酸钙还是碳酸氢钙 已知酸性 H2co3>hclo>hco3-
二氧化碳 和漂白粉反应 生成碳酸钙还是碳酸氢钙 已知酸性 H2co3>hclo>hco3- we16071年前3
we16071年前3 -
 blame09 共回答了14个问题
blame09 共回答了14个问题 |采纳率92.9%如果从酸性的角度,确实只能生成碳酸氢盐:
如NaClO +CO2 + H2O=NaHCO3 + HClO 即使CO2少量也是这样反应
但是对次氯酸钙,则不一样,因为生成CaCO3沉淀,使HCO3-继续电离:
因此在CO2少量:Ca(ClO)2+CO2+H2O=CaCO3+2HClO
CO2过量:Ca(ClO)2+2CO2+2H2O=Ca(HCO3)2+2HClO1年前查看全部
- 漂白粉失效的反应中为什么不生成碳酸氢钙
漂白粉失效的反应中为什么不生成碳酸氢钙
空气中二氧化碳可以看成无限多的啊,CO2过量后为何不是碳酸氢根 如是我吻1年前1
如是我吻1年前1 -
 wozhongyuan 共回答了26个问题
wozhongyuan 共回答了26个问题 |采纳率88.5%空气中的二氧化碳是可以看成无限多,但是也不能都进入到溶液中啊,二氧化碳总有个溶解的平衡和电离的平衡啊~如果不是人为地通入二氧化碳的话,空气中的二氧化碳本来含量(百分数)也不多~是不够形象横碳酸氢钙的~1年前查看全部
- 漂白粉失效方程式是生成碳酸钙还是碳酸氢钙?
 逍遥_任我行1年前1
逍遥_任我行1年前1 -
 luckylulu 共回答了15个问题
luckylulu 共回答了15个问题 |采纳率86.7%是碳酸钙!
因为有效成分是次氯酸钙,因为和二氧化碳.水反应生成碳酸钙和次氯酸,次氯酸易分解,所以失效!1年前查看全部
- 漂白粉在空气中失效为什么生成碳酸钙而不是碳酸氢钙
 shixinhuizi1年前1
shixinhuizi1年前1 -
 无处躲雨_yoyo 共回答了17个问题
无处躲雨_yoyo 共回答了17个问题 |采纳率94.1%漂白粉是次氯酸钙与碱式氯化钙的混合物,有效成分为次氯酸钙.漂白粉的作用基于次氯酸的氧化性.次氯酸钙只是潜在的强氧化剂,使用时必须加入酸,使之变为次氯酸才具有氧化性.空气中的二氧化碳与漂白粉作用,生成的是碳酸钙与氯化钙.生成酸式盐的碳酸氢钙需要较高浓度的二氧化碳,一般空气中的浓度达不到,而且碳酸氢钙极易分解,30多度就会分解.次氯酸还原后还会生成氯化氢.1年前查看全部
- 碳酸氢钙和氢氧化钙离子方程式为什么氢氧化钙要拆?
 追忆之瞳1年前1
追忆之瞳1年前1 -
 分享黎明 共回答了13个问题
分享黎明 共回答了13个问题 |采纳率92.3%HCO3- + OH- + Ca2+ = H2O + CaCO3(沉淀)
氢氧化钙只有作石灰乳的时候不拆的1年前查看全部
- 碳酸氢钙溶液与少量氢氧化钠反应生成碳酸钙和水,与足量氢氧化钠反应生成碳酸钙,水和碳酸...
碳酸氢钙溶液与少量氢氧化钠反应生成碳酸钙和水,与足量氢氧化钠反应生成碳酸钙,水和碳酸...
碳酸氢钙溶液与少量氢氧化钠反应生成碳酸钙和水,与足量氢氧化钠反应生成碳酸钙,水和碳酸根离子;而碳酸氢钾和不足的氢氧化钙反应生成碳酸钙,水和碳酸根离子,与过量的氢氧化钙反应生成碳酸钙和水.它们都是碳酸氢根和氢氧根反应,为什么当氢氧根不足的时候它们所生成的物质正好相反呢?到底是氢氧根多生成碳酸根离子还是少的时候生成碳酸根离子? yypi1年前1
yypi1年前1 -
 于凌 共回答了20个问题
于凌 共回答了20个问题 |采纳率100%这是高考常考点,具体解答如下
谁不足,设谁的量为1,比如CA(HCO3)2+NAOH(过量)的反应,设CA(HCO3)2为1,则HCO3为2,CA为1,中和NAOH后得到2MOL的CO3,其中一个与CA生成碳酸钙,还剩一个CO3,其余类推.1年前查看全部
- 有关酸式盐的酸式盐是不是水溶液都呈酸性?酸式盐是不是都溶于水?还有如何从碳酸氢钙的水溶液中分离出碳酸氢钙固体是酸式盐,
 chenxisea9191年前8
chenxisea9191年前8 -
 engy4ojf 共回答了23个问题
engy4ojf 共回答了23个问题 |采纳率87%1 不是,NaHCO3的水溶液呈碱性.
2 不是,磷酸一氢盐大多不溶.
3 减压蒸发,使得水蒸发而不至于达到Ca(HCO3)2的分解温度.1年前查看全部
- 碳酸氢钙溶液与氢氧化钠溶液反应.
 千千阕歌20031年前1
千千阕歌20031年前1 -
 奶茶慕斯K 共回答了18个问题
奶茶慕斯K 共回答了18个问题 |采纳率94.4%二氧化碳,水,碳酸钠1年前查看全部
- 氢氧化钙溶液中滴入少量碳酸氢钙离子方程式
 tsyonglin1年前1
tsyonglin1年前1 -
 一壶驶 共回答了19个问题
一壶驶 共回答了19个问题 |采纳率100%Ca2+ + 2HCO3- +2 OH- =2H2O + CaCO3 +HCO3-1年前查看全部
- 下列离子方程式正确的是( )A.用惰性电极电解饱和氯化钠溶液:2Cl-+2H+ 电解 . H2↑+Cl2↑B.碳酸氢钙
下列离子方程式正确的是( )
A.用惰性电极电解饱和氯化钠溶液:2Cl-+2H+
H2↑+Cl2↑电解 .
B.碳酸氢钙溶液与足量澄清石灰水反应:HCO3-+Ca2++OH-═CaCO3↓+H2O
C.溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+═AgBr↓
D.苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- haiyou20071年前1
haiyou20071年前1 -
 ouyf 共回答了14个问题
ouyf 共回答了14个问题 |采纳率100%解题思路:A.用惰性电极电解饱和氯化钠溶液时,阳极上氯离子放电、阴极上氢离子放电,同时阴极附近有氢氧根离子生成;
B.二者反应生成碳酸钙和水;
C.自由移动的溴离子能和硝酸银溶液反应生成溴化银沉淀;
D.苯酚钠和二氧化碳反应生成苯酚和碳酸氢钠.A.用惰性电极电解饱和氯化钠溶液时,阳极上氯离子放电、阴极上氢离子放电,同时阴极附近有氢氧根离子生成,离子方程式为2Cl-+2H2O
电解
.
H2↑+Cl2↑+2OH-,故A错误;
B.二者反应生成碳酸钙和水,离子方程式为HCO3-+Ca2++OH-═CaCO3↓+H2O,故B正确;
C.自由移动的溴离子能和硝酸银溶液反应生成溴化银沉淀,溴乙烷中没有自由移动的溴离子,所以溴乙烷和硝酸银溶液不反应,故C错误;
D.苯酚钠和二氧化碳反应生成苯酚和碳酸氢钠,离子方程式为C6H5O-+CO2+H2O→C6H5OH+HCO3-,故D错误;
故选B.点评:
本题考点: 离子方程式的书写.
考点点评: 本题考查了离子方程式的书写,涉及电解原理、溴代烃中溴元素检验、苯酚的性质等知识点,注意C中溴元素检验方法、步骤,注意D中碳酸氢根离子酸性小于苯酚,无论二氧化碳是否过量,都生成碳酸氢钠,为易错点.1年前查看全部
- 浴室喷头长时间使用会有白色固体附着,这是因为硬水中含有较多的可溶性的钙、镁化合物,其中碳酸氢钙[Ca(HCO 3 ) 2
浴室喷头长时间使用会有白色固体附着,这是因为硬水中含有较多的可溶性的钙、镁化合物,其中碳酸氢钙[ca(hco 3 ) 2 ]受热易分解,生成难溶性的化合物、气体等物质。某小组探究碳酸氢钙受热完全分解后产物的成分。
【提出猜想】从组成物质元素的角度分析:
猜想1:生成的难溶性化合物可能是____。
猜想2:放出的气体可能是o 2 、h 2 、co 2 。
【方案设计】请你设计实验,帮助该组同学确定难溶物的成分。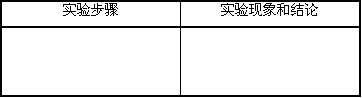
【实验探究】该组同学设计如下实验,继续探究气体的成分。 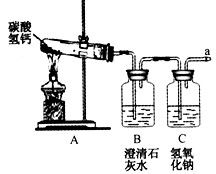
操作1:加热a装置,一段时间后,b装置中的澄清石灰水变浑浊。
操作2:在a处用燃着的木条检验,无明显现象。
【实验结论】结论1:碳酸氢钙分解产生的气体一定有____;一定没有_____。
结论2:碳酸氢钙受热分解的化学方程式为ca(hco 3 ) 2 caco 3 ↓+co 2 ↑
caco 3 ↓+co 2 ↑
【实验交流】交流1:从安全的角度考虑,操作2中存在的实验不足是_____________。
交流2:小组内某同学对上述结论提出***: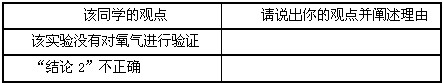
 发财猪哥哥1年前1
发财猪哥哥1年前1 -
 sindy1388 共回答了14个问题
sindy1388 共回答了14个问题 |采纳率92.9%1年前查看全部
- 写出下列物质的化学式碳酸碳酸钠碱式碳酸铜碳酸氢钠碳酸钙碳酸氢钙氯化氢氯气氯化钾二氧化锰氯酸氯酸钾二氧化氯氧化二氯硝酸硝酸
写出下列物质的化学式
碳酸
碳酸钠
碱式碳酸铜
碳酸氢钠
碳酸钙
碳酸氢钙
氯化氢
氯气
氯化钾
二氧化锰
氯酸
氯酸钾
二氧化氯
氧化二氯
硝酸
硝酸钾
硝酸钡
硝酸铵
硝酸铜
硝酸汞
硝酸银
硫酸
硫酸铵
硫酸氢铵
硫酸钡
硫酸铝
硫酸铁
硫酸亚铁
磷酸
磷酸钠
磷酸氢钠
磷酸氢二钠
磷酸氢铵
磷酸钙
磷酸二铵
氮气
硫磺
白磷
金刚石
氦气
二氧化硅
氖气
二氧化氮
氩气
氧化铁
氧化铝
氢氧根离子
硫酸根离子
碳酸根离子
硝酸根离子
铵根离子 lcon011年前2
lcon011年前2 -
 lewis_xuxu 共回答了16个问题
lewis_xuxu 共回答了16个问题 |采纳率100%碳酸 H2CO3
碳酸钠 Na2CO3
碱式碳酸铜 Cu2(OH)2CO3
碳酸氢钠 NaHCO3
碳酸钙 CaCO3
碳酸氢钙 Ca(HCO3)2
氯化氢 HCl
氯气 Cl2
氯化钾 KCl
二氧化锰 MnO2
氯酸 HClO3
氯酸钾 KClO3
二氧化氯 ClO2
氧化二氯 Cl2O
硝酸 HNO3
硝酸钾 KNO3
硝酸钡 Ba(NO3)2
硝酸铵 NH4NO3
硝酸铜 Cu(NO3)2
硝酸汞 Hg(NO3)2
硝酸银 AgNO3
硫酸 H2SO4
硫酸铵 (NH4)2SO4
硫酸氢铵 NH4HSO4
硫酸钡 BaSO4
硫酸铝 Al2(SO4)3
硫酸铁 Fe2(SO4)3
硫酸亚铁 FeSO4
磷酸 H3PO4
磷酸钠 Na3PO4
磷酸氢钠 NaH2PO4
磷酸氢二钠 Na2HPO4
磷酸氢铵 NH4H2PO4
磷酸钙 Ca3(PO4)2
磷酸二铵 (NH4)2HPO4
氮气 N2
硫磺 S
白磷 P
金刚石 C
氦气 He
二氧化硅 SiO2
氖气 Ne
二氧化氮 NO2
氩气 Ar
氧化铁 Fe2O3
氧化铝 Al2O3
氢氧根离子 OH^-
硫酸根离子 SO4^2-
碳酸根离子 CO3^2-
硝酸根离子 NO3^-
铵根离子 NH4^+1年前查看全部
- 酸式盐与碱 离子方程式1.碳酸氢钠与氢氧化钡混合2.硫酸氢钠与氢氧化钡混合3.小苏打治疗胃酸过多4.碳酸氢钙溶液加到醋酸
酸式盐与碱 离子方程式
1.碳酸氢钠与氢氧化钡混合
2.硫酸氢钠与氢氧化钡混合
3.小苏打治疗胃酸过多
4.碳酸氢钙溶液加到醋酸
5.NH4HSO3溶液与NaOH混合加热
6.向Ba(OH)2中加入少量NaHSO3溶液 cx_hm_st1年前0
cx_hm_st1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 高一上的化学方程式,今晚作业碳酸氢钙与氢氧化钠反应的完整化学方程式,在线等,真是想不出来,跪求了太太太太太…感谢了
 wahaha831年前1
wahaha831年前1 -
 坏坏hh 共回答了18个问题
坏坏hh 共回答了18个问题 |采纳率77.8%氢氧化钠的量充分时有:
Ca(HCO3)2+2NaOH=CaCO3(沉淀)+2H2O+Na2CO3
氢氧化钠的不足分时有:
Ca(HCO3)2+NaOH=CaCO3(沉淀)+H2O+NaHCO31年前查看全部
- (2012•乐山)取只含碳酸氢钙的硬水a g,充分加热,发生如下反应:
(2012•乐山)取只含碳酸氢钙的硬水a g,充分加热,发生如下反应:
Ca(HCO3)2
CaCO3↓+CO2↑+H2O,得到沉淀1.0g.回答下列问题:△ .
(1)碳酸氢钙中钙元素与氧元素的质量比为______.
(2)计算此硬水中碳酸氢钙的质量是多少?
(3)将a g这样的硬水充分煮沸,理论上可得到的软水质量为______. booksun1年前1
booksun1年前1 -
 通宵的人 共回答了18个问题
通宵的人 共回答了18个问题 |采纳率100%解题思路:(1)化合物物质元素的质量比的计算方法为:原子个数×相对原子质量的比值,可以据此解答;
(2)根据生成沉淀的质量可以计算出硬水中碳酸氢钙的质量;
(3)除去碳酸钙和二氧化碳气体的质量,即为可得到的软水的质量,可以据此解答.(1)碳酸氢钙中钙元素和氧元素的质量比为:40:(16×6)=5:12;
(2)设Ca(HCO3)2 的质量为x,生成二氧化碳的质量为y
Ca(HCO3)2
△
.
CaCO3↓+CO2↑+H2O
162 10044
x 1.0gy
[162/x=
100
1.0g=
44
y]
解得:x=1.62g,y=0.44g;
答:硬水中碳酸氢钙的质量是1.62g;
(3)将ag这样的硬水充分煮沸,理论上可得到的软水质量为:(a-1.0g-0.44g)=(a-1.44)g.
故答案为:(1)5:12;
(2)1.62g;
(3)(a-1.44)g.点评:
本题考点: 根据化学反应方程式的计算;硬水与软水.
考点点评: 要想解答好这类题目,首先,要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等.然后,根据所给的问题情景或图表信息等,结合所学的相关知识和技能,细致地分析题意(或图表信息)等各种信息资源,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可.1年前查看全部
- 麻烦写出下面反应的离子方程式.1.碳酸氢钠和醋酸溶液反应.2.碳酸氢钙溶液中加盐酸.3.向氯化亚铁溶液中通入氯气.4.磷
麻烦写出下面反应的离子方程式.
1.碳酸氢钠和醋酸溶液反应.
2.碳酸氢钙溶液中加盐酸.
3.向氯化亚铁溶液中通入氯气.
4.磷酸二氢钙溶液与氢氧化钠溶液反应.
5.三氯化铁溶液跟过量氨水反应.
6.小苏打溶液和烧碱溶液反应.
7.用氨水吸收少量二氧化硫.
氯化钾溶液中混有杂质溴化氢。
写一下除杂所用试剂和有关离子方程式。 mtbike851年前1
mtbike851年前1 -
 游悠的鱼 共回答了18个问题
游悠的鱼 共回答了18个问题 |采纳率83.3%1,HCO3- + CH3COOH =CO2↑+ H2O +CH3COO-
2,HCO3- + H+ CO2+ H2O
3,2Fe2+ + Cl2 =2Fe3+ +2Cl-
4,H2PO4- + 2OH- =PO43- +2H2O
5,Fe3+ + 3NH3H2O?Fe(OH)3 +3NH4+
6,HCO3- + OH- =CO2↑ + H2O
7,NH3 +H2O +SO2 NH4+ SO3 2-1年前查看全部
- 碳酸氢钙与少量氢氧化钠溶液反应的离子方程式
碳酸氢钙与少量氢氧化钠溶液反应的离子方程式
要准确的 有能力没人理1年前2
有能力没人理1年前2 -
 zgf1980 共回答了19个问题
zgf1980 共回答了19个问题 |采纳率78.9%HCO3- +Ca2+ +OH- =H2O+CaCO3(沉淀)1年前查看全部
- 碳酸氢钙溶液和氢氧化钠溶液混合的离子方程式
 牛皮癣治老ee1年前2
牛皮癣治老ee1年前2 -
 LKM9876 共回答了18个问题
LKM9876 共回答了18个问题 |采纳率88.9%如果碳酸氢钙过量
Ca2+ +HCO3- +OH-=CaCO3+H20
如果NaOH过量
Ca2+ +2HCO3- +2OH-=CaCO3+CO32- +2H201年前查看全部
- 碳酸氢钙和氢氧化钠反应的化学题目
碳酸氢钙和氢氧化钠反应的化学题目
200mL 1mol/L的碳酸氢钠溶液与120mL 2mol/L的氢氧化钠溶液混合,
求:生成沉淀多少克? 花开的温度1年前2
花开的温度1年前2 -
 rxov 共回答了23个问题
rxov 共回答了23个问题 |采纳率87%题目影视碳酸氢钠溶液和氢氧化钙溶液反应吧
否则是不会有沉淀的
n(NaHCO3)=0.2L×1mol/L=0.2mol
n[Ca(OH)2]=0.12L×2mol/L=0.24mol
所以NaHCO3不足,Ca(OH)2有剩余,由方程式
Ca(OH)2+2NaHCO3==CaCO3+2H2O
0.1mol.0.2mol.0.1mol
故生成0.1molCaCO3沉淀
质量为0.1mol×100g/mol=10g1年前查看全部
- 浴室喷头长时间使用会有白色固体附着,这是因为自来水中含有较多的可溶性的钙、镁化合物,其中碳酸氢钙 Ca(HCO3)2受热
 浴室喷头长时间使用会有白色固体附着,这是因为自来水中含有较多的可溶性的钙、镁化合物,其中碳酸氢钙 ca(hco3)2受热易分解,生成难溶性的化合物、气体等物质.某小组探究碳酸氢钙受热分解后产物的成分.
浴室喷头长时间使用会有白色固体附着,这是因为自来水中含有较多的可溶性的钙、镁化合物,其中碳酸氢钙 ca(hco3)2受热易分解,生成难溶性的化合物、气体等物质.某小组探究碳酸氢钙受热分解后产物的成分.
提出猜想:从组成物质元素的角度分析:
猜想1.生成的难溶性化合物可能是______(填化学式).
猜想2.放出的气体可能是o2、h2、co2.
方案设计:请你设计实验,帮助该组同学确定难溶物的成分.
继续探讨:该组同学设计如图实验,继续探究气体的成分.实验步骤 实验现象和结论 取少量难溶物于试管中,______,然后将燃着的木条伸入试管中 若______且木条火焰熄灭,则证明猜想正确
操作1.加热a装置,一段时间后,b装置中的澄清石灰水变浑浊,c装置氢氧化钠溶液的作用是______.
操作2.在a处用燃着的木条检验,无明显现象.
实验结论:
结论:碳酸氢钙分解产生的气体一定有co2;一定没有o2和h2.
实验交流:
交流1.从安全的角度考虑,操作2中存在的实验不足是______.
交流2.小组内某同学对上述结论提出***,认为该实验没有对氧气进行验证,请说出你的观点并阐述理由:______. 尚程茶社1年前1
尚程茶社1年前1 -
 活动如果是 共回答了11个问题
活动如果是 共回答了11个问题 |采纳率81.8%解题思路:根据质量守恒定律,生成的难溶性化合物可能是碳酸钙;由题目给出的信息可知:碳酸钙可以用稀盐酸检验,碳酸钙与盐酸反应生成氯化钙和水和二氧化碳,因此有气泡冒出,并且木条熄灭.该组同学设计如图实验,继续探究气体的成分,C装置氢氧化钠溶液的作用是吸收二氧化碳;从安全的角度考虑,操作2中存在的实验不足是:氢气具有可燃性,点燃气体前没有先验纯;我认为对氧气已经进行验证了,因此不同意此观点;因为氧气具有助燃性,若有氧气产生,实验操作2中的木条燃烧得会更旺.猜想1.根据质量守恒定律,生成的难溶性化合物可能是碳酸钙;故答案为:CaCO3
【方案设计】碳酸钙可以用稀盐酸检验,碳酸钙与盐酸反应生成氯化钙和水和二氧化碳,因此有气泡冒出,并且木条熄灭;故答案为:实验步骤:加入稀盐酸;实验现象和结论:有气泡产生
【继续探究】操作1.该组同学设计如图实验,继续探究气体的成分,C装置氢氧化钠溶液的作用是吸收二氧化碳;故答案为:除去(或吸收)CO2
【实验交流】交流1.从安全的角度考虑,操作2中存在的实验不足是:氢气具有可燃性,点燃气体前没有先验纯;故答案为:点燃气体前没有先验纯
交流2.我认为对氧气已经进行验证了,因此不同意此观点;因为氧气具有助燃性,若有氧气产生,实验操作2中的木条燃烧得会更旺;故答案为:不同意此观点;因为氧气具有助燃性,若有氧气产生,实验操作2中的木条燃烧得会更旺.(答案合理均给分)点评:
本题考点: 实验探究物质的组成成分以及含量;常见气体的检验与除杂方法;质量守恒定律及其应用;氢气、一氧化碳、甲烷等可燃气体的验纯.
考点点评: 有关实验方案的设计和对实验方案的评价是中考的热点之一,设计实验方案时,要注意用最少的药品和最简单的方法;关于对实验设计方案的评价,要在两个方面考虑,一是方案是否可行,能否达到实验目的;二是设计的方法进行比较,那种方法更简便.1年前查看全部
- 高一 这几个离子方程式怎么写?碳酸氢钙和氢氧化钠溶液的 反应现象和离子方程式 硫酸氢钠 碳酸钠 澄清石灰水
 銀冰1年前2
銀冰1年前2 -
 bsym888 共回答了12个问题
bsym888 共回答了12个问题 |采纳率100%HCO3- + OH- + Ca2+ =H2O+CaCO3↓ 溶液变浑浊产生白色沉淀
HCO3- +H+ +SO42- +Ca2+=CaSO4↓+H2O+CO2↑ 溶液变浑浊产生白色沉淀和大量气泡
Ca2+ +CO32- =CaCO3↓ 溶液变浑浊产生白色沉淀
Ca2+ +HCO3- +OH- =CaCO3↓+H2O 溶液变浑浊产生白色沉淀1年前查看全部
- 过量二氧化碳通入碳酸钙的水溶液生成碳酸氢钙,求离子方程式
 zhdshzh1年前3
zhdshzh1年前3 -
 tianxianl 共回答了16个问题
tianxianl 共回答了16个问题 |采纳率93.8%co2+Co3(2-)+H2o--》2HCo3(-)1年前查看全部
- 写化学方程式和离子方程式CO2过量+氢氧化钙碳酸氢钙少量+氢氧化钠碳酸氢钙+氢氧化钠少量碳酸氢钠+氢氧化钙少量碳酸氢钠少
写化学方程式和离子方程式
CO2过量+氢氧化钙
碳酸氢钙少量+氢氧化钠
碳酸氢钙+氢氧化钠少量
碳酸氢钠+氢氧化钙少量
碳酸氢钠少量+氢氧化钙
第一个氢氧化钙拆不拆? 064231年前4
064231年前4 -
 tengkongyu 共回答了28个问题
tengkongyu 共回答了28个问题 |采纳率96.4%①.CO2过量+氢氧化钙反应可分两步,首先反应生成碳酸钙沉淀.过量的二氧化碳又和碳酸钙反应生成碳酸氢钙,而碳酸氢钙溶于水.
化学方程式:2CO2 + Ca(OH)2 = Ca(HCO3)2
离子方程式:2CO2 + Ca(OH)2 = Ca2+ + 2(HCO3)-
②.碳酸氢钙少量+氢氧化钠.碳酸氢钙是少量的,所以碳酸氢钙完全参加反应.
方程式:Ca(HCO3)2 + 2NaOH = CaCO3 + Na2CO3 + 2H2O
离子式:Ca2+ + 2HCO3- +2OH- = CaCO3 + CO32- +2H2O
③.碳酸氢钙+氢氧化钠少量.氢氧化钠少量的完全参加反应.
方程式:Ca(HCO3)2+NaOH = CaCO3 + NaHCO3 +H2O
离子式:Ca2+ +HCO3- + OH- = CaCO3 + H2O
④.碳酸氢钠+氢氧化钙少量.氢氧化钙少量完全转化为碳酸钙沉淀.
方程式:2NaHCO3+Ca(OH)2=CaCO3 + 2H2O +Na2CO3
离子式:2HCO3- + Ca(OH)2 = CaCO3 +2H2O + CO32-
⑤:碳酸氢钠少量+氢氧化钙.
方程式:NaHCO3 + Ca(OH)2 = CaCO3 + NaOH + H2O
离子式:HCO3- + Ca(OH)2 = CaCO3 + OH- + H2O1年前查看全部
- 家中烧开水的铝壶和盛放开水的暖瓶,使用时间长了易结水垢.因为硬水中含有较多的可溶性的钙、镁化合物,其中碳酸氢钙[Ca(H
家中烧开水的铝壶和盛放开水的暖瓶,使用时间长了易结水垢.因为硬水中含有较多的可溶性的钙、镁化合物,其中碳酸氢钙[Ca(HCO 3 ) 2 ]受热易分解,生成水和大量的气体,还有一种难溶性的化合物,它是水垢的成分之一.
【问题】碳酸氢钙受热分解的另外两种生成物是什么?
【假设】①你认为生成物中的固体可能是______,理由是______.
②小红认为生成物中的气体可能是O 2 ,与你的假设是否一致,说明理由______.
【实验】依据你的假设设计实验方案(注:写清操作步骤、现象、结论)
假设①的方案
假设②的方案
写出假设②方案中涉及的化学方程式______. 酒幕风香1年前1
酒幕风香1年前1 -
 飞子在线 共回答了12个问题
飞子在线 共回答了12个问题 |采纳率91.7%(1)碳酸氢钙[Ca(HCO 3 ) 2 ]受热易分解,生成水和大量的气体,还有一种难溶性的化合物,它是水垢的成分之一.根据质量守恒定律确定该固体是含钙的化合物,又因为该固体是难溶物,所以可能为碳酸钙.故答案为:CaCO 3 ;根据质量守恒定律确定该固体是含钙的化合物,又因为该固体是难溶物,所以可能为碳酸钙.
(2)小红认为生成物中的气体可能是O 2 ,我认为是二氧化碳,因为根据质量守恒定律,反应前后原子的种类和个数不变,若为氧气,反应前后差一个碳原子.故答案为:不一致,气体应为二氧化碳,根据质量守恒定律,反应前后原子的种类和个数不变,若为氧气,反应前后差一个碳原子.
实验:碳酸钙可以用稀盐酸和燃烧的木条检验;二氧化碳可以用澄清的石灰水来检验;二氧化碳和氢氧化钙反应生成碳酸钙白色沉淀和水.故答案为:假设①的方案:取少量难溶物于试管中,加入稀盐酸后,将燃着的木条伸入试管中;若有气泡冒出并且木条火焰熄灭,就证明难溶物是碳酸钙.假设②的方案:将收集的气体通入石灰水中,若石灰水变浑浊,则证明气体为二氧化碳.CO 2 +Ca(OH) 2 =CaCO 3 ↓+H 2 O1年前查看全部
- 碳酸氢钙,碳酸氢钡,硫酸氢钙,硫酸氢钡,哪些不是沉淀?
 wuxiaobin881年前1
wuxiaobin881年前1 -
 sadfsasdf 共回答了16个问题
sadfsasdf 共回答了16个问题 |采纳率100%碳酸氢钙,碳酸氢钡,硫酸氢钡不是1年前查看全部
- 请教下列反应方程式:三氧化硫和水 氧化钠和水 碱式碳酸铜加热 铁和硝酸汞溶液 碳酸氢钙溶液和盐酸
请教下列反应方程式:三氧化硫和水 氧化钠和水 碱式碳酸铜加热 铁和硝酸汞溶液 碳酸氢钙溶液和盐酸
下列物质在水中的电离方程式
碳酸钠 硫酸 硝酸 硝酸铜 碳酸氢钙 硝酸铵 硫酸铝 高锰酸钾 氯酸钾 氢氧化钙 磷酸钠 硝酸钡 氯化铁 氯化铵 口牙1年前2
口牙1年前2 -
 wadeliu 共回答了20个问题
wadeliu 共回答了20个问题 |采纳率100%SO3+H2O=H2SO4
Na2O+H2O=2NaOH
Cu2(OH)2CO3△=2CuO+H2O+CO2↑
Fe+Hg(NO3)2=Hg+Fe(NO3)2
Ca(HCO3)2+2HCl=CaCl2+2H2O+2CO2↑
在水中电离方程式
Na2CO3=Na+ + co32-(钠离子+碳酸根离子)
其余依次写就行(金属离子+酸根离子),注意氯化铵中金属离子是铵根离子1年前查看全部
- 碳酸氢钙 物质类别快 酸 碱 我先写个盐 明天问好老师
 blf6543211年前7
blf6543211年前7 -
 susu_9 共回答了16个问题
susu_9 共回答了16个问题 |采纳率93.8%盐1年前查看全部
- 某碳酸钙与碳酸氢钙的混合物跟足量盐酸 消耗H+和产生CO2的物质的量之比为5:4 该混合物中碳酸钙与碳酸氢钙
某碳酸钙与碳酸氢钙的混合物跟足量盐酸 消耗H+和产生CO2的物质的量之比为5:4 该混合物中碳酸钙与碳酸氢钙
的物质的量之比是多少 SIYUE8402051年前1
SIYUE8402051年前1 -
 lyjchly 共回答了22个问题
lyjchly 共回答了22个问题 |采纳率86.4%解设该混合物中含碳酸钙与碳酸氢钙的物质的量分别为X、Y
CaCO3 + 2HCl =CaCl2 + H2O + CO2↑
1 2 1
X 2X X
Ca(HCO3)2 + 2HCl =CaCl2 + 2H2O + 2CO2↑
1 2 2
Y 2Y 2Y
则(2X+2Y):(X+2Y)=5:4
X:Y=2:3
答:该混合物中含碳酸钙与碳酸氢钙的物质的量之比为2:31年前查看全部
- 碳酸氢钙和氢氧化钠分别以物质的量之比为1:2和1:1发生反应方程式.
 s48741年前1
s48741年前1 -
 彩色恋曲 共回答了17个问题
彩色恋曲 共回答了17个问题 |采纳率94.1%Ca(HCO3)2+2NaOH=CaCO3+Na2CO3+2H2O
Ca(HCO3)2+NaOH=CaCO3+NaHCO3+H2O1年前查看全部
大家在问
- 1轻松自如的近义词和反义词分别是什么?
- 2已知不等式组2x+m>0,2x+6
- 3已知关于x的方程x²-5x+m-1=0的一个根与关于x的方程x²+5x-m+1=0的一个根互为相反数,求m的值
- 4大 师 聂鑫森 至少要10个,
- 5某学校为开展“阳光体育”活动,计划拿出不超过3000元的资金购买一批篮球、羽毛球拍和乒乓球拍,已知篮球、羽毛球拍和乒乓球
- 6凶恶、辨别、呼喊、勤奋、湿润、跟随、精细、探求、的近义词是什么?
- 765Mn弹簧零件的怎样淬火能保证弹性最好?零件厚度0.6-0.7mm.长宽10*20.
- 8这些数学题怎么算?15厘米=米=( )米.6分米=米=( )米.1毫米=厘米=( )厘米.1里面有( )百分之一.10个
- 9小明上山以每小时240千米的速度,5小时到达山顶,又以每小时400千米的速度按原路下山.小明上、下山的平均速度是多少?
- 10一个杯子倒扣在水上,漂浮着,如果将它往下按,直到完全浸入水中,放开手,杯会如何 A一直下沉直到水底
- 11三角形ABC是等腰直角三角形,角BAC等于90度,F为AC中点,CE垂直于BF,三角形BDE面积为36,求CE的长
- 12select which program features you want installed.recommended
- 13请给我一份一天会做的事的英语翻译,好的另给20财富就星期一到星期四.
- 14一块300亩的正方形土地,周长是多少
- 15某物体从高度为125米的地方自由下落,物体落地时刻的速度为多少.