对热力学第二定律,下列理解正确的是( )
 breezesmile2022-10-04 11:39:541条回答
breezesmile2022-10-04 11:39:541条回答A.自然界进行的一切宏观过程都是可逆的
B.自然界进行的涉及热现象的宏观过程都具有方向性,是不可逆的
C.热量不可能由低温物体传递到高温物体
D.第二类永动机违背了能量守恒定律,因此不可能制成

已提交,审核后显示!提交回复
共1条回复
 hjur 共回答了20个问题
hjur 共回答了20个问题 |采纳率80%- 解题思路:自然界进行的涉及热现象的宏观过程都具有方向性,是不可逆的,热量可能由低温物体传递到高温物体,但要产生其它影响,第二类永动机不违背能量守恒,违背了热力学第二定律.
A、自然界进行的一切与热现象有关的宏观过程都是不可逆的,A错误;
B、自然界进行的涉及热现象的宏观过程都具有方向性,是不可逆的,B正确;
C、热量可能由低温物体传递到高温物体,比如冰箱,C错误;
D、第二类永动机违背了热力学第二定律,D错误;
故选:B点评:
本题考点: 热力学第二定律;温度是分子平均动能的标志.
考点点评: 记住热力学第二定律的两种表述,能应用它们进行分析判断问题. - 1年前
相关推荐
- 根据热力学第二定律,可知下列说法中正确的是( ) A.可能从单一热源吸收热量并把它全部用来做功,而不引起其它变化 B.
根据热力学第二定律,可知下列说法中正确的是( ) A.可能从单一热源吸收热量并把它全部用来做功,而不引起其它变化 B.没有冷淋器,只有单一的热源,能将从单一热源吸收的热量全部用来做功,而不引起其它变化的热机是可实现的 C.制冷系统能将冰箱里的热量传给外界较高温度的空气中而不引起其它变化 D.不可能使热量由低温物体传递到高温物体,而不引起其它变化  doctor1年前1
doctor1年前1 -
 ceeo 共回答了13个问题
ceeo 共回答了13个问题 |采纳率84.6%A、B、根据热力学第二定律,不可能从单一热源吸收热量并把它全部用来做功,而不引起其它变化,故A错误,B错误;
C、制冷系统能将冰箱里的热量传给外界较高温度的空气中,但是要消耗电能,故C错误;
D、根据热力学第二定律,不可能使热量由低温物体传递到高温物体,而不引起其它变化,故D正确;
故选D.1年前查看全部
- 热力学第二定律的自发过程产生能量变化不?如气体向真空膨胀过程会不会做功?
 十万个不知道s1年前1
十万个不知道s1年前1 -
 我是啊财 共回答了19个问题
我是啊财 共回答了19个问题 |采纳率89.5%热力学第二定律的自发过程与能量是否变化没有直接关系.热二是关于系统微观状态数多少——熵大小的.尽管系统能量变化有可能影响微观状态数,但它不是唯一的影响因素,故熵与能量并不正相关.系统能量是否变化关键看系统是否是孤立系:若是孤立系,能量就不变;若不是,一般会变.
气体向真空膨胀过程不对外界做机械功,但对本身做机械功——膨胀的动能源于气体的部分内能.此时的气体系统不是一个孤立系,而是一个闭系(与外界交换能量但不交换粒子),因为它可以向外界发出热辐射,气体系统与它发出的辐射的总能量显然不变,但气体系统的能量必定减小;作为不可逆的自发过程,气体系统与它的辐射的总熵必然增大,但气体系统的熵不一定增大,要看具体情况.1年前查看全部
- 用热力学第二定律证明:两条绝热线不能相交.
用热力学第二定律证明:两条绝热线不能相交.
如题. c62xhh1年前2
c62xhh1年前2 -
 wudang88884444 共回答了13个问题
wudang88884444 共回答了13个问题 |采纳率76.9%用反证法.
两条绝热线如果能相交,再加上一条等温线就可以组成一个循环(闭合曲线).这个循环只在等温过程从单一热源吸热,然后对外做功,显然违反了热力学第二定律.
所以,两条绝热线不可能相交.1年前查看全部
- 热力学第二定律的几种表述及关系
 pengxuangui1年前1
pengxuangui1年前1 -
 tz820105 共回答了17个问题
tz820105 共回答了17个问题 |采纳率82.4%热力学第二定律
热力学第二定律有几种表述方式:
克劳修斯表述:
热量可以自发地从较热的物体传递到较冷的物体,但不可能自发地从较冷的物体传递到较热的物体;
开尔文-普朗克表述:
不可能从单一热源吸取热量,并将这热量变为功,而不产生其他影响.熵表述:
随时间进行,一个孤立体系中的熵总是不会减少.关系:
热力学第二定律的每一种表述,揭示了大量分子参与的宏观过程的方向性,使人们认识到自然界中进行的涉及热现象的宏观过程都具有方向性.微观意义
一切自然过程总是沿着分子热运动的无序性增大的方向进行.
第二类永动机(不可能制成)
只从单一热源吸收热量,使之完全变为有用的功而不引起其他变化的热机.
第二类永动机违法了热力学第二定律1年前查看全部
- 根据热力学第二定律,可知下列说法中正确的是( )
根据热力学第二定律,可知下列说法中正确的是( )
A.可能从单一热源吸收热量并把它全部用来做功,而不引起其它变化
B.没有冷淋器,只有单一的热源,能将从单一热源吸收的热量全部用来做功,而不引起其它变化的热机是可实现的
C.制冷系统能将冰箱里的热量传给外界较高温度的空气中而不引起其它变化
D.不可能使热量由低温物体传递到高温物体,而不引起其它变化 南极黑人1年前1
南极黑人1年前1 -
 Carrie_Gong 共回答了19个问题
Carrie_Gong 共回答了19个问题 |采纳率100%解题思路:热力学第二定律的内容:不可能从单一热源吸取热量,使之完全变为有用功而不产生其他影响;不可能使热量由低温物体传递到高温物体,而不引起其他变化.第二定律说明热的传导具有方向性.A、B、根据热力学第二定律,不可能从单一热源吸收热量并把它全部用来做功,而不引起其它变化,故A错误,B错误;
C、制冷系统能将冰箱里的热量传给外界较高温度的空气中,但是要消耗电能,故C错误;
D、根据热力学第二定律,不可能使热量由低温物体传递到高温物体,而不引起其它变化,故D正确;
故选D.点评:
本题考点: 热力学第二定律.
考点点评: 只有熟练掌握热力学第二定律的内容才能顺利解决本题,故一定要注意基本概念的积累.1年前查看全部
- (2006•江苏模拟)(A类题)对热力学第二定律的理解,以下说法正确的是( )
(2006•江苏模拟)(A类题)对热力学第二定律的理解,以下说法正确的是( )
A.它是能量守恒定律的一种具体形式
B.它是反映宏观自然过程的方向性的定律
C.机械能可以全部转化为内能,而内能不能全部转化为机械能
D.热量可以从低温物体传到高温物体,但要引起其他变化 peterwu41年前1
peterwu41年前1 -
 签发成 共回答了23个问题
签发成 共回答了23个问题 |采纳率78.3%解题思路:本题考查热力学第二定律的内容:一种表述:不可能从单一热源吸取热量,使之完全变为有用功而不产生其他影响.另一种表述是:不可能使热量由低温物体传递到高温物体,而不引起其他变化.第二定律说明热的传导具有方向性.A、符合能量守恒的过程不一定符合热力学第二定律,故A错误
B、它是反映宏观自然过程的方向性的定律,故B正确
C、根据热力学第二定律可知,机械能可能全部转化为内能,在没有外界影响时,内能不能全部用来做功以转化成机械能.但是在外界的条件下内能能全部转化为机械能.故C错误
D、热量可以从低温物体传到高温物体,但要引起其他变化,故D正确
故选BD.点评:
本题考点: 热力学第二定律.
考点点评: 只有熟练掌握热力学第二定律的内容才能顺利解决本题,故一定要注意基本概念的积累.1年前查看全部
- 下列说法正确的是( )A. 热力学第二定律只在一定前提条件下才能成立B. 热力学第二定律揭示了一切自然过程总是沿着分子
下列说法正确的是( )
A. 热力学第二定律只在一定前提条件下才能成立
B. 热力学第二定律揭示了一切自然过程总是沿着分子热运动的无序性增大的方向进行
C. 能量耗散是从能量转化的角度反映出自然界中的宏观过程具有方向性
D. 热力学第二定律揭示了有大量分子参与宏观过程的方向性 会飞红猪侠1年前4
会飞红猪侠1年前4 -
 双123 共回答了18个问题
双123 共回答了18个问题 |采纳率72.2%解题思路:热力学定律的两种表述:(1)按传热的方向性表述:热量不能自发地从低温物体传到高温物体,(2)按机械能与内能转化的方向性表述:不可能从单一热源吸收热量,使之完全变成功,而不产生其他影响.熵增加原理的内容:在任何自然过程中,一个孤立系统的总熵不会减小.如果过程可逆,则熵不变;如果过程不可逆,则熵增加.
从微观的角度看,热力学第二定律是一个统计规律:一个孤立系统总是从熵小的状态向熵大的状态发展,而熵值较大代表着较为无序,所以自发的宏观过程总是向无序度更大的方向发展.A、热力学第二定律的成立不需要条件,故A错误.
B、熵增加原理说明一切自然过程总是向着分子热运动的无序性增大的方向进行,故B正确;
C、能量耗散是从能量转化的角度反映出自然界中的宏观过程具有方向性,故C正确.
D、热力学第二定律揭示了有大量分子参与宏观过程的方向性,故D正确.
故选:BCD.点评:
本题考点: 热力学第二定律.
考点点评: 本题综合考查了热力学第二定律的内容,知识点较多,要加强知识的积累.1年前查看全部
- 关于热力学第一定律和热力学第二定律,下列论述正确的是 [ ] A .热力
关于热力学第一定律和热力学第二定律,下列论述正确的是 [ ]A .热力学第一定律指出内能可以与其他形式的能相互转化,而热力学第二定律则指出内能不可能完全转化为其他形式的能,故这两条定律是相互矛盾的
B .内能可以全部转化为其他形式的能,只是会产生其他影响,故两条定律并不矛盾
C.两条定律都是有关能量的转化规律,它们不但不矛盾,而且没有本质区别
D .其实,能量守恒定律已经包含了热力学第一定律和热力学第二定律 九目丁1年前1
九目丁1年前1 -
 qjj1120 共回答了24个问题
qjj1120 共回答了24个问题 |采纳率87.5%B1年前查看全部
- 热力学第二定律真实表述是怎样的?
 曾经de_1年前1
曾经de_1年前1 -
 天山雪糕 共回答了21个问题
天山雪糕 共回答了21个问题 |采纳率90.5%概述 ①热不可能自发地、不付代价地从低温物体传到高温物体.(不可能使热量由低温物体传递到高温物体,而不引起其他变化,这是按照热传导的方向来表述的) ②不可能从单一热源取热,把它全部变为功而不产生其他任何影响 在孤立系统内对可逆过程,系统的熵总保持不变;对不可逆过程,系统的熵总是增加的.这个规律叫做熵增加原理.这也是热力学第二定律的又一种表述1年前查看全部
- 气体等温膨胀时,从外界(单一热源)吸收的热量完全对外做功,违背热力学第二定律吗
 狂人日ll1年前2
狂人日ll1年前2 -
 小傻瓜_716 共回答了13个问题
小傻瓜_716 共回答了13个问题 |采纳率100%不违背
从外界吸收的热量不等于外界释放的热量
这个问题你只看到了气体本身,并没有考虑到外力做功时产生的熵
热力学第二定律:必须有温差才能传导热量,冷源不可能向热源传导热量
实际上可以把这个定律进行一下拓展
可以理解为能量的效率不可能等于100%,也就是说,能量在做功的时候肯定会有能量做无用功
从外界(单一热源)吸收的热量完全对外做功,完全对外做功,并不等于完全的有用功
活塞肯定是有阻力的,所以气体对活塞的力肯定要大于活塞对外部的力1年前查看全部
- 急求答案:宇宙中根本没有热力学第二定律?
 poisons271年前2
poisons271年前2 -
 zhonghua20 共回答了24个问题
zhonghua20 共回答了24个问题 |采纳率87.5%热力学第二定律是建立在对实验结果的观测和总结的基础上的定律.虽然在过去的一百多年间未发现与第二定律相悖的实验现象,但始终无法从理论上严谨地证明第二定律的正确性.自1993年以来,Denis J.Evans等学者在理论上对热力学第二定律产生了质疑,从统计热力学的角度发表了一些关于“熵的涨落“的理论,比如其中比较重要的FT理论[2].而后G.M.Wang等人于2002在Physical Review Letters上发表了题为《小系统短时间内有悖热力学第二定律的实验证明》[3]. 从实验观测的角度证明了在一定条件下热,孤立系统的自发熵减反应是有可能发生的.虽然这些新的发现不至于影响到现存热力学的应用,但必然将对未来热力学的研究产生一定的影响. 热力学第二定律是宏观定律,不是微观定律,因此这里所说的“质疑”,并不是对热力学第二定律的质疑,只是一种就像量子力学对牛顿力学一样的补充.1年前查看全部
- 热力学第二定律在凉水里吸热反应然后把化合物转移到热水中进行放热化学反应,就把热由低温传到高温,放热反应完再吸热,循环利用
热力学第二定律
在凉水里吸热反应然后把化合物转移到热水中进行放热化学反应,就把热由低温传到高温,放热反应完再吸热,循环利用.似乎违反热力学定律 飘在云朵上的小白1年前1
飘在云朵上的小白1年前1 -
 cathyhappy123 共回答了17个问题
cathyhappy123 共回答了17个问题 |采纳率94.1%这个问题可能比你想象的要复杂得多,关键是热力学第二定律确实不是很容易透彻理解.
你这里利用的第二定律是一种对它的常见表述,克劳修斯表述.其原文是这样:“不可能将热从低温物体传到高温物体,而不发生其他变化”.
你这里首先如何实现一个循环(一个循环必须是连续的,不可间断),另外你怎么保证这个过程不发生其他变化?这个过程中你不是要把化合物转移到热水中吗?你要不要做功呢?除非它自己长了腿.你一做功就引起了其它变化了,功总是要变热的啊.而这样的变化和表述不符,因此不能说明表述错了.
这个表述并没有说,有其它变化时,不可能将热从低温物体传到高温物体.我们常用的空调不是可以吗,问题是我们要对空调做电功,这就不可避免地发生了其它变化.1年前查看全部
- 节约用能于热力学第二定律有什么关系?
 gy_19781年前2
gy_19781年前2 -
 7145335e97061315 共回答了16个问题
7145335e97061315 共回答了16个问题 |采纳率81.3%热力学第二定理告诉我们,能量的流动是单向的,能量一旦被用过,就不可能在被利用,因此必修节约用能.1年前查看全部
- 热力学第二定律的数学表达式及意义?谁知到的帮忙回答下
 娃哈哈m191年前1
娃哈哈m191年前1 -
 xxzwx118 共回答了15个问题
xxzwx118 共回答了15个问题 |采纳率73.3%孤立系熵增原理的数学表达式吧1年前查看全部
- 热力学第二定律的发现与发展在科学思想与科研方法上有什么特点
 轻机枪1年前1
轻机枪1年前1 -
 fgfghfd 共回答了21个问题
fgfghfd 共回答了21个问题 |采纳率90.5%热力学第一定律又叫第一类永动机造不成,这类永动机是不需要输入能量就能做功的机器.热力学第二定律又叫第二类永动机造不成,这类永动机是利用热能的效率达到100%的热机.
永动机造不成是人们在大量实践中总结出的规律.
热力学第二定律还有另一种说法,就是热量不会自动从低温热源流向高温热源,这也是实验总结,与前一种说法是等价的.
有两种等价表述是热力学第二定律的特点,反映了自然界所有不可逆过程都是等价的.1年前查看全部
- 热力学第二定律的数学表达式是神马?
 戾公子1年前4
戾公子1年前4 -
 亲斤广由 共回答了17个问题
亲斤广由 共回答了17个问题 |采纳率82.4%他没有明确的数学表达式哈 就只是概念性的文字1年前查看全部
- 请用热力学第二定律证明:冬天,热量不可能自发地从低温的户外向房间内进行供暖.
 酸菜土豆丝1年前1
酸菜土豆丝1年前1 -
 garyz 共回答了22个问题
garyz 共回答了22个问题 |采纳率86.4%否则,我们可以制造一个热机,热机连接室内,室外.因为室内温度比室外高,那么通过室内,室外温度差进行做功.
这样,热量自发的进入室内,并且热机利用温度差进行做功.总体上,我们自发的把热量转化成做功,这是违反热力学第二定律的.1年前查看全部
- 热力学第二定律有几种表述,具体内容是什么?
 mljojo1年前1
mljojo1年前1 -
 冰水绿薄荷 共回答了16个问题
冰水绿薄荷 共回答了16个问题 |采纳率81.3%热力学第二定律有无数种表述方式,实质是一切热力学过程都是不可逆的1年前查看全部
- 论证热力学第二定律的两种表述的等效性
论证热力学第二定律的两种表述的等效性
尽量用反证发证明 我真是老狼1年前1
我真是老狼1年前1 -
 ihxieh 共回答了22个问题
ihxieh 共回答了22个问题 |采纳率95.5%证明:假设开尔文(以下简称开氏)说法成立,而克劳修斯(以下简称克氏)不成立.(1)按照开氏说法,一热机有两个热源工作在温度为T1、T2两个热源之间,并从高温热源T1吸热Q1,对外做功W并向冷源T2放热Q2,显然Q1=W+Q2.(2)若克氏说法不成立,即可从低温热源T2自发向高温热源T1传热,并假定传热量为Q2.(3)现在,将上述二者合在一起,形成一个新的热机,并考察综合效果,得出的结论是:新热机从单一热源T1吸收热量(Q1-Q2),并对外做功W,外界与新热机均无变化.这显然违背了开氏说法.所以,若克氏说法不成立,必然导致开氏说法也不成立.同理也可以证明,若克氏说法成立,而开氏说法不成立,同样也导致克氏说法也不成立.
由此可知,假定某一说法不成立是错误的.因此,开氏说法成立,克氏说法也成立,二者等效.
证毕.1年前查看全部
- 有没有符合热力学第二定律 但不符合第一定律的循环过程
 3969839391年前1
3969839391年前1 -
 猪dd大不大 共回答了19个问题
猪dd大不大 共回答了19个问题 |采纳率89.5%没有,热力学第一定律就是能量守恒定律的体现.1年前查看全部
- 水的熵大于冰的熵,那当水结冰的过程是否违反了热力学第二定律,
 遥远的梦想1年前4
遥远的梦想1年前4 -
 haihua88 共回答了16个问题
haihua88 共回答了16个问题 |采纳率100%按照经典理论说吧,
熵的增加是对于孤立体系来说,
水结冰的过程大体分为三类,
1,你给水制冷了……有外加能量……不是孤立体系,熵完全可以减小
2,水在一个孤立体系中,这个体系还有其它物质,水的熵减小了,但伴随着水的结冰放热,其它物质的熵增大了,体系是熵增的
3,水在孤立体系,这个体系只有水——哈哈哈哈,你把水放在真空,与任何其它物质不发生相互作用,它多冷都不会结冰,反而会扩散~
就事论事的话,就是这样.
如果你已经通过了高考,并对自然充满兴趣,不满足于实用主义,我可以告诉你一个好消息,热力学第二定律,其实是不对的!就好比,牛顿力学并不是真理,但是在工程上很好用一样.1年前查看全部
- 谁能严格的证明热力学第二定律我认为该定律错误.人们对热力学第二定律有误解.应改为能量只能从高能量扩散到低能量的地方,不受
谁能严格的证明热力学第二定律
我认为该定律错误.人们对热力学第二定律有误解.应改为能量只能从高能量扩散到低能量的地方,不受外界影响
你们举一个例子来证明,我是没发现,你能否找一个符合的例子.
我举个例子,电冰箱,有人说这符合,电冰箱内能量改变,由于电力做功.让我来说:空气压缩机将冰箱内空气抽出,压缩,温度升高,向外散热,再膨胀吸收冰箱内热量.每个细节都是由高向底流动.看初末状态,很像所说的能量逆向流动引起外界变化,其实不对 .能量只是顺向流动了. zmyy10001年前1
zmyy10001年前1 -
 夕阳下的蚂蚁 共回答了19个问题
夕阳下的蚂蚁 共回答了19个问题 |采纳率94.7%1850年,克劳修斯在卡诺的基础上统一了能量守恒和转化定律与卡诺原理,指出:一个自动运作的机器,不可能把热从低温物体移到高温物体而不发生任何变化,这就是热力学第二定律.不久,开尔文又提出:不可能从单一热源取热,使之完全变为有用功而不产生其他影响;或不可能用无生命的机器把物质的任何部分冷至比周围最低温度还低,从而获得机械功.这就是热力学第二定律的“开尔文表述”.奥斯特瓦尔德则表述为:第二类永动机不可能制造成功.在提出第二定律的同时,克劳修斯还提出了熵的概念S=Q/T,并将热力学第二定律表述为:在孤立系统中,实际发生的过程总是使整个系统的熵增加.1859年克拉克.麦克斯韦用统计方法导出了处于热平衡态中的气体分子的“麦克斯韦速率分布律”.1877年,奥地利物理学家玻尔兹曼发现了宏观的熵与体系的热力学几率的关系.他在使科学界接受热力学理论、尤其是热力学第二定律方面立下了汗马功劳.
具体计算过繁琐,不再详细举列.
你说的冰箱是冷却剂吸热气化.压缩机加压使气化的冷却剂液化,此过程是外界做功使熵值减小.1年前查看全部
- 等温膨胀时,理想气体所吸收的热量全部用来做功,这和热力学第二定律是否矛盾?为什么?
 L_YONG勇1年前1
L_YONG勇1年前1 -
 a85766375 共回答了18个问题
a85766375 共回答了18个问题 |采纳率94.4%热力学第二定律还有一个条件,就是不引起其它变化.
而温膨胀时,理想气体所吸收的热量全部用来做功,气体的体积增大了.气体的体积增大属于“其它变化”,所以不矛盾.1年前查看全部
- 高中物理、热力学第二定律是啥?
 saiveliu1年前4
saiveliu1年前4 -
 新好望角 共回答了25个问题
新好望角 共回答了25个问题 |采纳率100%不可能把热从低温物体传到高温物体而不产生其他影响;不可能从单一热源取热使之完全转换为有用的功而不产生其他影响;不可逆热力过程中熵的微增量总是大于零.1年前查看全部
- 关于熵、热力学第二定律的疑问热力学第二定律说在隔离系统中只能发生熵增大的反应.熵不变能自发吗?根据吉布斯自由能方程式,只
关于熵、热力学第二定律的疑问
热力学第二定律说在隔离系统中只能发生熵增大的反应.
熵不变能自发吗?
根据吉布斯自由能方程式,只要反应放热放出足够热量,即使熵减不是也可以自发进行吗? 太保空间11年前1
太保空间11年前1 -
 冬天的那枝独秀 共回答了21个问题
冬天的那枝独秀 共回答了21个问题 |采纳率85.7%1、对隔离系统,(ΔS)iso ≥ 0,其中取等号,就是熵不变时过程可逆;只有取大于号,即熵变大于零时过程才自发.2、是的.在等温等压下,只要过程放出足够的热量,从而保证ΔG≤0,则即使熵减也可以自发进行.这种情况很常见,...1年前查看全部
- 热力学第二定律的数学表达式
 sailuya1年前1
sailuya1年前1 -
 loveing118 共回答了17个问题
loveing118 共回答了17个问题 |采纳率100%熵增
△S≥01年前查看全部
- 怎样证明热力学第二定律
 ww说我是vv1年前1
ww说我是vv1年前1 -
 xoi4m 共回答了17个问题
xoi4m 共回答了17个问题 |采纳率88.2%热力学第二定律为不可能把热从低温物体传到高温物体而不产生其他影响;不可能从单一热源取热使之完全转换为有用的功而不产生其他影响;当时老师讲的时候没说怎么证明,不过只举过简单的例子.人其实可以把热量从低温传到高温的,冰箱的原理就是如此,不过它并不违背热力学第二定律,因为冰箱消耗了电能,就是说冰箱利用电能把热量传到外面的高温环境.当然,热力学第二定律并不是非常完美的,有人也提出过质疑.但是,我们现在只要会利用就好了.1年前查看全部
- 进化论违反了热力学第二定律是什么意思?说得通俗易懂点好吗...我在网上查了下全是T.M..D..术语...搞不懂呀.最好
进化论违反了热力学第二定律是什么意思?说得通俗易懂点好吗...我在网上查了下全是T.M..D..术语...搞不懂呀.最好是说得老太太都可以懂..说下原理吧...
 keven_ch1年前1
keven_ch1年前1 -
 marswangzi 共回答了27个问题
marswangzi 共回答了27个问题 |采纳率92.6%热力学第二定律意思是热力学过程是有方向性的,除非有外加影响,否则是不会自发地发生相反的过程.而可自发进行的方向总是由各部分差异大的变化到各部分均匀(用术语讲是朝着熵增大的方向),比如说红墨水和清水混合,会自发地扩散,最终各部分变成淡红色的均匀液体.但是淡红色的均匀液体不会自动发过来分离成清水和红墨水这种不均匀的系统.
低等生物无明显的器官划分(类似于均匀淡红色液体),高等生物有明显的器官划分,各种器官之间有明显的差异(类似于红墨水和清水放在一起).这样生物进化就有点像均匀液体的各种成分自发地分离开来,违背了热力学第二定律.
但是,生物过程受到的外界作用很复杂,用简单的热力学系统来类比是不严密的,光从表象上说违背热力学定律是不科学的.1年前查看全部
- 热力学第二定律怎样理解?
 等待天蝎座1年前4
等待天蝎座1年前4 -
 cnnasone 共回答了13个问题
cnnasone 共回答了13个问题 |采纳率92.3%第一,热力学第二定律的表述(说法)虽然繁多,但都反映了客观事物的一个共同本质,即自然界的一切自发过程都有“方向性”,并且一切自发过程都是不可逆的.
第二,热力过程的方向性,是可以用“熵”来衡量的,也即孤立系的一切实际过程,其总熵是增加的,理想条件下(即可逆),总熵不变.
现以最常见的热力学二种说法进行理解.
1、克劳修斯说法(1850年):热不可能自发地、不付代价地从低温物体传到高温物体.
解释:
(1)这里需要强调的是“自发地、不付代价地”.我们通过热泵装置是可以实现“将热从低温物体传向高温物体的”,但这里是付出代价的,即以驱动热泵消耗功为代价,是“人为”的,是“强制”的,不是“自发”的.所以,非自发过程,如热从低温物体传向高温物体,必须同时要有一个自发过程为代价(这里是机械能转化为热能)为补偿,这个过程叫“补偿过程”.
(2)非自发过程(如热从低温物体传向高温物体)能否进行,还要看花的“代价”是否够,就是总系统(孤立系)的熵必须是增加的,或可逆下总熵不变.也就是说,如果投入的“代价”不够的话,非自发过程是不能进行的,或是进行得不够彻底(不能达到预计的状态).孤立系总熵变不小于零,非自发过程才有可能进行.
2、开尔文-普朗特说法(1851年):不可能制造出从单一热源吸热,使之全部转化为功而不留下其他任何变化的热力发电机.
解释:
(1)这里强调的是“不留下其他任何变化”,是指对热机内部、外界环境及其他所有(一切)物体都没有任何变化.
开尔文-普朗特说法说明了热转化为功,必须要将一部分热量转给低温物体(注意,这可是一个自发过程,高温向低温传热哦),也即必须要有一个“补偿过程”为代价.
(2)热全部转化为功,是可以的,但必须要“留下其他变化”.如等温过程中,热可以全部转变成功,但这时热机内部工质的“状态”变了(即工质不能回到初始状态.其实,这样的热机实际上是不存在的),是留下了变化的.
总之,要正确理解热力学第二定律,以下几点是需要把握的:
1、上述热力学第二定律的两种表述及其等效性;
2、卡诺循环与卡诺定理、卡诺效率,且 ηT≤ ηC;
3、克劳修斯积分等式和不等式;
4、熵的过程方程式:dS≥dQ/Tr;
5、孤立系统熵增原理:△Siso=∑△Si=Sg≥0;
6、闭口系(控制质量)熵方程:dS=dSg+dQ/Tr;(开口系也要掌握好)
7、能量贬值原理:dEx,iso≤0;
8、熵产与机械能(火用)的损失关系:I=To×Sg .1年前查看全部
- 热力学第二定律急求:一制冷剂工作在t2=-10°C和t1=11°C之间,若其循环可看做是卡诺可逆循环的逆循环,则每消耗1
热力学第二定律
急求:一制冷剂工作在t2=-10°C和t1=11°C之间,若其循环可看做是卡诺可逆循环的逆循环,则每消耗1.00kj的功可从冷库中取出多少热量??
 xiaoheihei77581年前1
xiaoheihei77581年前1 -
 杀鬼者 共回答了21个问题
杀鬼者 共回答了21个问题 |采纳率85.7%我之前也有过类似你这样的疑惑。仔细想想,其实不然。
首先有一点要纠正,就是如果只是纯概率角度,纯从有序无序角度看,黑洞的熵不是增大到无穷,而是不断减小,趋近于0。因为它使系统趋向无限有序,这个是熵减的过程。因此貌似与热力学第二定律相违背。但也并非如此简单。
如果你感兴趣的话,可以读下霍金的书(我也没读过,这里纯引用)。他提出过黑洞熵值正比于其视界表面积的理论。根据他的理论,物质落入...1年前查看全部
- 孤立系统熵值可以不变吗?热力学第二定律指出一个热力学系统的伤值不会减小,那么可以不变吗?
 xyl_xp1年前2
xyl_xp1年前2 -
 爱众生 共回答了23个问题
爱众生 共回答了23个问题 |采纳率82.6%热力学第二定律明确的说明了,只是不会减少.
可以增加的,可逆则熵值不变,不可逆则熵值增加.
例如:绝热不可逆的化学反应熵就是增加.1年前查看全部
- 热力学第二定律中,我们学习过许多判据中,哪些只是过程性质(可逆,不可逆),而不是自自发过程方向的判据
热力学第二定律中,我们学习过许多判据中,哪些只是过程性质(可逆,不可逆),而不是自自发过程方向的判据
谢谢啦
 我好爱你哟1年前1
我好爱你哟1年前1 -
 断奶的孩子 共回答了18个问题
断奶的孩子 共回答了18个问题 |采纳率100%判据常用的就是三种,既可用于判断过程是否可逆,也可判断过程的自发方向.因此问题本身是不够恰当的.
1 熵判据,任何条件适用.系统与外界的总熵变大于零过程不可逆,可以自发发生;等于零过程可逆,不可自发发生,小于零过程不可能,其逆向过程自发.
2 亥姆赫兹自由能判据,适用于等温等容过程.判断方法与上面类似不再赘述,只是大于和小于互换.
3 吉布斯自由能判据,适用于等温等压过程.类上.
如有不明欢迎追问.1年前查看全部
- 为什么热力学第二定律要加上单一热源这个限制条件?
为什么热力学第二定律要加上单一热源这个限制条件?
那意味着 有可能从非单一热源吸收热量用来全部做功而不引起其它变化,这句话是对的? colehe1年前1
colehe1年前1 -
 我老实所以笨 共回答了17个问题
我老实所以笨 共回答了17个问题 |采纳率88.2%我觉得,这应该意味着仅从单一热源吸收热量用来全部做功是不可能呢,要像做功需要有两个热源,从高温热源吸热,向低温热源放热,吸热量与放热量之差就是做功量1年前查看全部
- 混沌摆没有违反热力学第二定律嘛
 meipp1年前1
meipp1年前1 -
 cgb_1222 共回答了18个问题
cgb_1222 共回答了18个问题 |采纳率77.8%没有啊!热力学第二定律针对的是孤立系统,同外界既没有质量的交换也无能量的交换,首先看你所说的混沌摆有无外界做功?另外混沌也不一定是有序也不一定是无序吧,只是对扰动比较敏感而已,就算有序也肯定是耗散结构的系统.1年前查看全部
- 热力学第二定律的古典或诗意表述.
 saks1年前1
saks1年前1 -
 janjan1551 共回答了18个问题
janjan1551 共回答了18个问题 |采纳率83.3%君不见,黄河之水天上来,奔流到海不复回.
君不见,高堂明镜悲白发,朝如青丝暮成雪.
子在川上曰:逝者如斯夫,不舍昼夜.
体现的都是第二定律的本质:方向性1年前查看全部
- 一个人从出生到老死,熵如何变化?人为什么需要锻炼身体?根据热力学第二定律作出
一个人从出生到老死,熵如何变化?人为什么需要锻炼身体?根据热力学第二定律作出
RT
 酸甜aa1年前1
酸甜aa1年前1 -
 一剑封喉后 共回答了19个问题
一剑封喉后 共回答了19个问题 |采纳率78.9%出生开始,熵增加,趋于有序.死后熵减小(没有摄取能量来维持有序)1年前查看全部
- benard单体,热力学第二定律和熵.
benard单体,热力学第二定律和熵.
近年来,根据热力学第二定律的拓展,它可以被描述成以下:
“当系统远离平衡态,它会用尽一切办法抵抗这种远离,当致使不平衡的因素的量增加时,系统的反对这种因素的量的增加的能力也将提高.”
benard 单体解释了这一说法,当容器内上下温差达到一定梯度时,benard单体形成了更复杂的结构去反抗梯度的增加.
但是我不理解一句话,这句话是这样的:the more pressure that is applied,the harder it will resist.这句话的意思是说更大的压力导致这个系统反抗得更厉害吗?还是说越大的压力导致这个系统更难反抗?
这句话在以下这篇文章中,“the new entropy law and the economic process”,第357页倒数第二段.前面的话是描述熵定律拓展的:“the thermodynamic principle governs the behaviour of systems is that,as they are moved away from equilibrium,they will utilize all avenues to counter the applied gradients.As the applied gradients increase,so does the system's ability to oppose further degradation."
有任何疑问,欢迎登陆百度在线和我联系, Syria19821年前1
Syria19821年前1 -
 cleopatra 共回答了15个问题
cleopatra 共回答了15个问题 |采纳率93.3%你的第一理解是对的.
孤立系统熵增表明,任何不平衡的孤立系统,都会朝着平衡方向变化,最终达到平衡.
这说明,若某一子系统偏离平衡越大,其他子系统就会反抗这样的偏离.比如,一杯热水,它就偏离了平衡(与环境相比),因此,无论如何保温,这杯水最终还是会凉的.反之,若要将环境温度下的水加热成高的温度(即让其远离平衡),温度越高(远离平衡更加厉害),就越难达到(反抗势力的作用),就是这个道理.1年前查看全部
- 热力学第二定律的疑问这个定律是怎推出来得```````?
 667874611年前2
667874611年前2 -
 chejinglin22 共回答了17个问题
chejinglin22 共回答了17个问题 |采纳率94.1%这个问题,傅献彩的《物理化学》中说的很清楚也很有意思,热力学第一定律和第二定律都是从大量实验事实中总结出来的,不能从更基本的定律推出,实践是检验真理的唯一标准.1年前查看全部
- 用熵增加原理证明热力学第二定律的克劳休斯表述
 托塔天王A1年前0
托塔天王A1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 为什么热力学第二定律的地位高于热力学第一定律
 晓寒深深处1年前3
晓寒深深处1年前3 -
 xingang13141314 共回答了17个问题
xingang13141314 共回答了17个问题 |采纳率94.1%我也想知道为什么,
19世纪自然科学三大发现
1.细胞学说
2 达尔文进化论
3.能量守恒与转化定律(热一定律)
我的意思是在说,热一定律并不比热二定律地位低.1年前查看全部
- 可逆过程是否违反热力学第二定律?
可逆过程是否违反热力学第二定律?
热二律说:一切与热现象有关的实际宏观过程都是不可逆的.对于可逆过程,当功全部转化为热后,逆过程热又全转化为功,这是不是与热二律矛盾?可逆过程是在否定热二律的基础上假想的吗?
 zl6906221年前1
zl6906221年前1 -
 treeme003 共回答了17个问题
treeme003 共回答了17个问题 |采纳率88.2%不违背.
1.请区分一下概念.
你所谓的“实际宏观过程”应该是指的“自然界自发过程”.自发过程本身就是不可逆的.
2.热二律的表述中,以开尔文普朗克表述为例,强调“单一热源”,“不引起其他变化”.可逆过程探讨的是可逆性的可能性,而非必须.而且如若回复到初始状态必定经历逆过程,引起其他变化.
3.你说的可逆“可逆过程,当功全部转化为热后,逆过程热又全转化为功”是错误的,错在“全”.热二律中开尔文表述是不可能从单一热源吸热并使之完全变为有用功,你的‘全’本身违反了热二律,相当于构造了第二类永动机.
以上~1年前查看全部
- 热力学第二定律习题A system absorbs 473 J of heat reversibly from a ho
热力学第二定律习题
A system absorbs 473 J of heat reversibly from a hot reservoir at 529 K and gives off 182.1 J of heat to a cold reservoir at 213 K.During this process,124.6 J of work is done by the system
从热源中吸收473J热量可逆,温度为529K,释放了182.1J的热量给冷物体,温度为213K,在这个过程中,做了124.6J的功.
求这个过程中1.内能变化J 2.熵的变化J/K 3.宇宙熵的变化 xujin8551年前1
xujin8551年前1 -
 暗裏着迷 共回答了25个问题
暗裏着迷 共回答了25个问题 |采纳率84%内能的变化是:
473-182.1-124.6
这里,系统熵的变化:529K的热源放热Q1=473,熵变是-473/529,213K的热源的熵变是正的,182.1/213,两者的和就是总熵变.
然后宇宙熵变是0.因为这是可逆过程.1年前查看全部
- 对热力学第二定律理解正确的是( )
对热力学第二定律理解正确的是( )
A.有可能制成第二类永动机
B.热效率为100%的热机是不可能制成的
C.热传导、摩擦生热等热现象是不可逆的
D.内能可以全部转化为机械能,同时不引起其他变化 我是xiaoli1年前1
我是xiaoli1年前1 -
 亲密拥抱 共回答了21个问题
亲密拥抱 共回答了21个问题 |采纳率95.2%解题思路:热力学第二定律:不可能从单一热源吸取热量,使之完全变为有用功而不产生其他影响.不可能使热量由低温物体传递到高温物体,而不引起其他变化.第二定律说明热的传导具有方向性.A、B、第二类永动机是指从单一热源吸取热量,使之完全变为有用功而不产生其他影响的热机,即机械效率达到100%的机器,没有违背能量的守恒定律,违背了热力学第二定律,因此不可能制成,故A错误,B正确;
C、热力学第二定律说明自然界进行的涉及热现象的宏观过程比如:热传导、摩擦生热都具有方向性,是不可逆的,故C正确;
D、根据热力学第二定律可知:内能可以全部转化为机械能,但要引起其他变化,故D错误.
故选:BC.点评:
本题考点: 热力学第二定律.
考点点评: 只有熟练掌握热力学第二定律的内容才能顺利解决本题,故一定要注意基本知识的积累.1年前查看全部
- 热力学第二定律说明,一切能量转化过程都是不可逆的.这句话为什么错?
 susanla1年前1
susanla1年前1 -
 我好好忧伤 共回答了17个问题
我好好忧伤 共回答了17个问题 |采纳率88.2%前提是在自然状态下 有其他物体在做功时是可逆的1年前查看全部
- 热力学第二定律的微观解释怎么解释热传递的方向性呢?
热力学第二定律的微观解释怎么解释热传递的方向性呢?
热传递的话、从高温物体传递到低温物体、那么低温物体变得更加无序、而高温物体不是变得更加有序了么、这该怎么解释呢?
而且觉得热力学第二定律的微观解释与热力学第二定律联系不起来、求高手解释、
如果讲得很好、我会加分滴、
为什么速度平均正是 微观状态数目多的状态 bobkingtiger1年前2
bobkingtiger1年前2 -
 julyfox 共回答了19个问题
julyfox 共回答了19个问题 |采纳率100%这个问题不能把它分割开了看
应该整体看,如:
高温物体传递能量时,和低温物体一起 构成一个系统.因为能量的交换涉及到两个物体.
这个系统,传递前,是有速度大小差别很大
传递后,温度平均了,那么运动的速度也相对平均了.
再者,在一个封闭的系统里,相对高速的物体势必会带动低速物体一起运动,速度分配服从动量定理.
所以,从宏观上看,整体一个系统满足有序向无序发展
热力学第二定律的统计意义是:一个不受外界影响的“孤立系统”,其内部发生的过程,总是由几率小的状态向几率大的状态进行,由包含微观状态数目少的宏观状态向包含微观状态数目多的宏观状态进行.
而速度平均正是 微观状态数目多的状态.所以用热二率好解释了1年前查看全部
- 被冷却水在冷却塔中能冷到比大气温度还低,这是否违背热力学第二定律?为什么?
 rickybill1年前1
rickybill1年前1 -
 ncxall 共回答了20个问题
ncxall 共回答了20个问题 |采纳率90%你所说的大气温度应该是指环境温度,而冷却塔降温的温度极限却是湿球温度.比如,贵州贵阳,夏天温度最高时一般都到40度.但最高湿球温度只有二十多度,冷却水就可以降到二十多度..这个当然不违背热力学第二定律.只是你把环境温度和湿球温度混淆了,你弄清楚湿球温度这个问题就好理解了.1年前查看全部
- 热力学第二定律常见的表述有两种.
热力学第二定律常见的表述有两种.
第一种表述:不可能使热量由低温物体传递到高温物体,而不引起其他变化;
第二种表述:不可能从单一热源吸收热量并把它全部用来做功,而不引起其他变化.
图(a)是根据热力学第二定律的第一种表述画出的示意图:外界对制冷机做功,使热量从低温物体传递到高温物体.请你根据第二种表述在答题卷上完成示意图(b).根据你的理解,热力学第二定律的实质是______.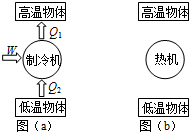
 199587861年前1
199587861年前1 -
 yangmenghua 共回答了19个问题
yangmenghua 共回答了19个问题 |采纳率89.5%1年前查看全部
- (2012•平遥县模拟)下列关于热力学第二定律的表述中正确的是( )
(2012•平遥县模拟)下列关于热力学第二定律的表述中正确的是( )
A.热力学零度不可达到
B.不可能使热量由低温物体传递到高温物体,而不引起其他变化
C.其数学表达式是△U=Q+W
D.能量在转化或转移的过程中总量保持不变 jae661年前1
jae661年前1 -
 天人知我心 共回答了23个问题
天人知我心 共回答了23个问题 |采纳率78.3%解题思路:热力学第三定律:热力学零度不可达到;热力学第二定律的内容:①不可能自发把热量从低温物体传到高温物体而不产生其他影响;②不可能从单一热源取热使之完全转换为有用的功而不产生其它影响.热力学第一定律的表达式为△U=Q+W.能量在转化或转移的过程中总量保持不变.A、根据热力学第三定律知热力学零度不可达到,故A错误.
B、根据热力学第二定律可知:不可能自发把热量从低温物体传到高温物体而不产生其他影响,故B正确.
C、△U=Q+W是热力学第一定律的公式.故C错误.
D、能量在转化或转移的过程中总量保持不变,这个规律是能量转化和守恒定律,而不是热力学第二定律,故D错误.
故选:B点评:
本题考点: 热力学第二定律.
考点点评: 此题要求知道热力学第二定律的内容,明确该定律与热力学第一定律、第三定律和能量守恒定律的区别.1年前查看全部
- 根据热力学第二定律,下列说法正确的是( )
根据热力学第二定律,下列说法正确的是( )
A.热量可以从高温物体传到低温物体,但不能从低温物体传到高温物体
B.热量可以从高温物体传到低温物体,也可能从低温物体传到高温物体
C.机械能可以全部转化为内能,但内能不可能全部转化为机械能
D.机械能可以全部转化为内能,内能也可能全部转化为机械能 bianxuewu1年前1
bianxuewu1年前1 -
 天崖守夜人 共回答了23个问题
天崖守夜人 共回答了23个问题 |采纳率95.7%解题思路:热力学第二定律有不同的表述:不可能把热从低温物体传到高温物体而不产生其他影响;不可能从单一热源取热使之完全转换为有用的功而不产生其他影响;A、B、根据热力学第二定律的表述:热量不可能自发的从高温物体传向低温物体.但是在外界影响的情况下热量也可以从低温传向高温,比如空调,故A错误,B正确.
C、D、热力学第二定律的一种表述为:不可能从单一热源取热使之完全转换为有用的功而不产生其他影响,机械能可以全部转化为内能,但内能不可能全部转化为机械能;故C正确,D错误.
故选:BC.点评:
本题考点: 热力学第二定律.
考点点评: 本题关键熟悉热力学第二定律的各种表述,能够明确热力学第二定律的本质.1年前查看全部
大家在问
- 1(x的平方-mx+2)(x-2)的积中x的二次项系数为零,则m的值是
- 2初一期末数学24题分数如何分配24..(1)①.(直接回答)②.(分类讨论)(2).x=_____,y=____(填空)
- 3I'm going to buy a magazine.(用what改写)_______________
- 4猜字谜 作文
- 5数学无理数问题,知道的告诉我,谢谢,很急的
- 6从一个长80厘米,宽70厘米的长方形纸板剪下一个最大的正方形后,剩下的长方形的周长为多少厘米,面积为多
- 7材料作文 上帝给了你一张脸,笑容必须由你自己完成。生活给你许多路,必须由你自己来决定。力
- 8粗盐提纯的步骤、仪器、注意事项
- 9有没有其他像苏轼的《江城子》那种感觉的诗
- 10六个一样大小的长方形拼成的图形如图所示,如果大长方形的周长为32cm,阴影部分的周长为8cm那么小
- 11辨析:经济规律是客观的,所以人们在经济规律面前是无能为力的.
- 12假如a等于3,那么a的负三次方等于多少?
- 13猴子吃桃子问题 数据结构课程设计
- 14下面这段话中有三处表述不当的地方,请挑出来并加以改正。
- 15(2013•黄冈模拟)有一种电热写字板,上面是一块透明玻璃,下面是一块小电热毯.关于这种电热写字板的说法错误的是( )

