酸、碱、盐在工农业生产和日常生活中的广泛应用,促进了人类文明的进步和社会的可持续发展。下列有关酸、碱、盐的生产或应用的说
 younashi2022-10-04 11:39:541条回答
younashi2022-10-04 11:39:541条回答| 酸、碱、盐在工农业生产和日常生活中的广泛应用,促进了人类文明的进步和社会的可持续发展。下列有关酸、碱、盐的生产或应用的说法不合理的是 |
| [ ] |
| A.将草木灰(含K 2 CO 3 )与氯化铵混合施用 B.纯碱既可从内陆盐湖提取,又可用“侯氏联合制碱法”生产 C.用石灰乳与硫酸铜溶液混合配制防治植物病害的波尔多液 D.汽车或电动车的蓄电池中用到的硫酸溶液是由浓硫酸稀释而成 |

已提交,审核后显示!提交回复
共1条回复
 眷林潴 共回答了16个问题
眷林潴 共回答了16个问题 |采纳率93.8%- A
- 1年前
相关推荐
- 世界人口正在急剧的增,这使得工农业迅速发展很有必要 用英语怎么翻译啊?
 malaxiaoyuan1年前4
malaxiaoyuan1年前4 -
 hhh933 共回答了17个问题
hhh933 共回答了17个问题 |采纳率100%The rapid growth of the world population makes it necessary to develop industry and agriculture fast.
VS天才翻译家团队1年前查看全部
- 世界人口正在急剧的增,这使得工农业迅速发展很有必要 用英语说
 ek172361年前2
ek172361年前2 -
 yemok 共回答了18个问题
yemok 共回答了18个问题 |采纳率77.8%the booming of the world's population makes the rapid development of industry and agriculture essential1年前查看全部
- 什么是酶?酶的生物学特点?酶在生命过程和工农业生产中的作用
 lonely水1年前1
lonely水1年前1 -
 feihan1229 共回答了17个问题
feihan1229 共回答了17个问题 |采纳率88.2%酶的定义:催化特定化学反应的蛋白质、RNA或其复合体.是生物催化剂,能通过降低反应的活化能加快反应速度,但不改变反应的平衡点.绝大多数酶的化学本质是蛋白质.
特点:具有催化效率高、专一性强、作用条件温和等特点.
在生物体内的酶是具有生物活性的蛋白质,存在于生物体内的细胞和组织中,作为生物体内化学反应的催化剂,不断地进行自我更新,使生物体内及其复杂的代谢活动不断地、有条不紊地进行. 酶的催化效率特别高(即高效性),比一般的化学催化剂的效率高10^7~10^18倍,这就是生物体内许多化学反应很容易进行的原因之一. 酶的催化具有高度的化学选择性和专一性.一种酶往往只能对某一种或某一类反应起催化作用,且酶和被催化的反应物在结构上往往有相似性. 一般在37℃左右,接近中性的环境下,酶的催化效率就非常高,虽然它与一般催化剂一样,随着温度升高,活性也提高,但由于酶是蛋白质,因此温度过高,会失去活性(变性),因此酶的催化温度一般不能高于60℃,否则,酶的催化效率就会降低,甚至会失去催化作用.强酸、强碱、重金属离子、紫外线等的存在,也都会影响酶的催化作用. 人体内存在大量酶,结构复杂,种类繁多,到目前为止,已发现3000种以上(即多样性).如米饭在口腔内咀嚼时,咀嚼时间越长,甜味越明显,是由于米饭中的淀粉在口腔分泌出的唾液淀粉酶的作用下,水解成麦芽糖的缘故.因此,吃饭时多咀嚼可以让食物与唾液充分混合,有利于消化.此外人体内还有胃蛋白酶,胰蛋白酶等多种水解酶.人体从食物中摄取的蛋白质,必须在胃蛋白酶等作用下,水解成氨基酸,然后再在其它酶的作用下,选择人体所需的20多种氨基酸,按照一定的顺序重新结合成人体所需的各种蛋白质,这其中发生了许多复杂的化学反应.可以这样说,没有酶就没有生物的新陈代谢,也就没有自然界中形形色色、丰富多彩的生物界.
在工农业中也起到了很大的作用:如啤酒的发酵,乙醇汽油等生产都离不开,1年前查看全部
- 下列对撒哈拉以南非洲经济描述正确的是 A.以出口初级产品为主 B.以出口工业产品为主 C.工农业发达
下列对撒哈拉以南非洲经济描述正确的是 A.以出口初级产品为主 B.以出口工业产品为主 C.工农业发达
D.不受外国资本控制
19号晚上8点选择满意答案. cici_20051年前1
cici_20051年前1 -
 哈萨尼 共回答了15个问题
哈萨尼 共回答了15个问题 |采纳率93.3%A1年前查看全部
- 前年工农业收入共计47.5万元,去年工农收入共计64万元,其中农业收入比前年增加48%,工业收入比前年增...
前年工农业收入共计47.5万元,去年工农收入共计64万元,其中农业收入比前年增加48%,工业收入比前年增...
前年工农业收入共计47.5万元,去年工农收入共计64万元,其中农业收入比前年增加48%,工业收入比前年增加二成,前年工农业收入多少万元? 49dc1年前1
49dc1年前1 -
 须彩 共回答了17个问题
须彩 共回答了17个问题 |采纳率82.4%假设前年工业收入为X
(1+20%)*X+(47.5-X)*(1+48%)=64
前年工业收入X=22.5
前年农业收入=47.5-22.5=251年前查看全部
- 一个乡村前年工农业收入总计47.5元,去年工农业收入总计64万元,其中农业收入比前年增加48% ,工业收入...
一个乡村前年工农业收入总计47.5元,去年工农业收入总计64万元,其中农业收入比前年增加48% ,工业收入...
一个乡村前年工农业收入总计47.5元,去年工农业收入总计64万元,其中农业收入比前年增加48% ,工业收入比前年增加二成,前年农业收入多少万元? golddays1年前1
golddays1年前1 -
 ss到ss 共回答了18个问题
ss到ss 共回答了18个问题 |采纳率100%设前年农业收入为x,设前年工业收入为y,依题意可列方程:
x+y=47.5①,(1+48%)*x+(1+20%)*y=64②
由①得y=47.5-x③
将③代入②得1.48*x+1.2*(47.5-x)=64,0.28x=64-1.2*47.5,x=25(万)
答:前年农业收入25万元1年前查看全部
- 化学与工农业生产、与人类生活都有密切相关,下列说法中正确的是( )
化学与工农业生产、与人类生活都有密切相关,下列说法中正确的是( )
A.14C可用于文物年代的鉴定,14C与12C互为同素异形体
B.葡萄糖注射液不能产生丁达尔效应现象,不属于胶体
C.汽油、柴油和植物油都是碳氢化合物
D.“春蚕到死丝方尽,蜡烛成灰泪始干”中的“丝”和“泪”分别是指纤维素和油脂 aa比尔21年前1
aa比尔21年前1 -
 mmbimae 共回答了18个问题
mmbimae 共回答了18个问题 |采纳率88.9%解题思路:A.有相同质子数,不同中子数的原子互为同位素;
B.根据胶体的性质进行判断;
C.植物油是高级脂肪酸的甘油酯,不是碳氢化合物;
D.诗句中的“丝”含有的物质是蛋白质,诗句中的“泪”指的是液态石蜡.A.测定14C含量法常用来鉴定古文物年代,14C与12C质子数相同,中子数不同,互为同位素,故A错误;B.葡萄糖注射液是溶液,不是胶体,无丁达尔效应,故B正确;C.汽油和柴油都是碳氢化合物,植物油是高级脂肪酸的甘油...
点评:
本题考点: 核素;胶体的重要性质;石油的分馏产品和用途;油脂的性质、组成与结构;纤维素的性质和用途.
考点点评: 本题考查同位素的概念、胶体的性质、有机物的组成等,难度不大.要注意基础知识的积累.1年前查看全部
- 钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛.
钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛.
Ⅰ铁的应用
(1)下列铁制品的利用与金属导热性有关的是______. 悲伤的森林1年前1
悲伤的森林1年前1 -
 alalei2005 共回答了16个问题
alalei2005 共回答了16个问题 |采纳率87.5%解题思路:I.铁的应用
(1)物质的性质决定了物质的用途,所以可以根据铁的用途,分析利用了铁的什么性质.
(2)根据铁锈蚀的条件分析.
II铁的冶炼
(1)冶炼铁的主要原料是铁矿石、焦炭、空气等物质,通过反应生成的一氧化碳可以把铁矿石中的铁还原出来.
(2)根据高炉炼铁的原料及各原料的作用分析即可;
Ⅲ实验探究炼铁原理
(1)根据反应条件和反应物状态选择发生装置;
(2)用氢氧化钙溶液验证二氧化碳气体,浓硫酸具有吸水性,常用来干燥气体;
(3)用氢氧化钙溶液验证二氧化碳气体;
(4)一氧化碳有毒,可据其可燃性进行处理后变成无害物质再排放.
(5)根据反应现象分析.
(6)纯净的Fe2O3固体质量=玻璃管及其中固体的质量-玻璃管质量,根据玻璃管及其中固体的质量的变化推算反应后黑色固体的成分.
(7)根据反应物、生成物和条件书写方程式.I.铁的应用
(1)分析所给三种金属制品可以知道,铁锅是利用了金属的导热性.
(2)铁吸收水与氧气后会变成铁锈,所以“双吸剂”它能够吸收空气中的水分和氧气.
II铁的冶炼
(1)赤铁矿的主要成分是氧化铁,氧化铁和一氧化碳反应能生成铁和二氧化碳,反应的化学方程式为:Fe2O3+3CO
高温
.
2Fe+3CO2 .
(2)炼铁时要用到焦炭,它有两个作用.炼铁时需要高温,焦炭与氧气反应生成二氧化碳,同时放出大量热,可供给炼铁使用;炼铁时还需一氧化碳作还原剂,二氧化碳与过量焦炭反应可以生成一氧化碳;
Ⅲ实验探究炼铁原理
(1)草酸(H2C2O4)与浓硫酸混合加热会产生一氧化碳,反应物均为液体,且需要加热,所以选择发生装置丁;
(2)装置C证明CO2是否已经除尽;浓硫酸具有吸水性,常用来干燥气体;
(3)澄清的石灰水可以用来验证二氧化碳气体;方程式为:CO2+Ca(OH)2═CaCO3↓+H2O;
(4)一氧化碳有毒,不能直接排放.缺少尾气处理装置;
(5)加入足量的稀盐酸,发现固体全部溶解,但无气泡产生,说明没有铁生成,这样就是Fe3O4和FeO的组合了,黑色粉末可能是:①Fe3O4;②FeO③Fe3O4和FeO.
(6)纯净的Fe2O3固体质量为:33.00g-28.20g=4.80g,其中铁元素的质量为4.80g×[112/160]=3.36g,氧元素的质量为4.80g-3.36g=1.44g;反应后损失的氧元素的质量为33.00g-32.84g=0.16g,所以设反应后黑色固体FexOy,则铁元素:氧元素=56x:16y=3.36g:(1.44g-0.16g);解得x:y=3:4
故反应后黑色固体是Fe3O4
(7)Fe2O3与CO反应生成Fe3O4和CO,方程式为:CO+3Fe2O3
400℃~500℃
.
2Fe3O4+CO2
故答案为:I.铁的应用
(1)B(2)氧气和水(或O2和H2O)
II铁的冶炼
(1)Fe2O3+3CO
高温
.
2Fe+3CO2 ;(2)提供热源,维持炉温
Ⅲ实验探究炼铁原理
(1)丁;(2)证明CO2是否已经除尽;吸收水分(或干燥CO)
(3)澄清的石灰水(或氢氧化钙溶液);CO2+Ca(OH)2═CaCO3↓+H2O;
(4)缺少尾气处理装置
(5)FeOFe3O4和FeO
(6)4.80;Fe3O4; CO+3Fe2O3
400℃~500℃
.
2Fe3O4+CO2点评:
本题考点: 金属的物理性质及用途;气体的净化(除杂);铁的冶炼;金属锈蚀的条件及其防护;书写化学方程式、文字表达式、电离方程式;根据化学反应方程式的计算.
考点点评: 此题是对炼铁知识的考查,解决的关键是知道炼铁的原理、原料及过程,题目综合性较强.1年前查看全部
- 水是生命之源,人类的日常生活与工农业生产都离不开水.自然界中的水含有许多可溶性和不溶性杂质,通过多种途径可以使水得到不同
水是生命之源,人类的日常生活与工农业生产都离不开水.自然界中的水含有许多可溶性和不溶性杂质,通过多种途径可以使水得到不同程度的净化.

(1)自然界的水是______(填“混合物”或“纯净物”)
(2)图1是自来水厂净水过程示意图.在此过程中,净化水的方法主要有______(至少写三种).
(3)硬水中含有较多可溶性钙、镁化合物,长期饮用硬水可能会引起体内结石.生活中常用______来区分软水与硬水.
(4)水中若含过量的氮、磷元素,会使藻类生长繁殖过快,导致水质恶化,发生“水华”现象.已知藻类主要含有C106H263O110N16P等物质,下列物质大量使用会导致“水华”现象的是______(填字母序号).
A.向水中加入活性炭来净水B.大量使用含Na5P3O10的洗衣粉
C.过量使用尿素[CO(NH2)2]等化学肥料
(5)某课外小组收集了一些浑浊的河水,利用如图2所示的简易净水装置进行净化.该装置中的小卵石、石英沙的作用是______.
(6)小明同学将浑浊的湖水样品倒入烧杯中,先采用如图3所示装置进行过滤.请问:图中还缺少的一种仪器是______,其作用是______;漏斗下端紧靠烧杯内壁是为了______. uiuiif341年前1
uiuiif341年前1 -
 t34w67457 共回答了20个问题
t34w67457 共回答了20个问题 |采纳率95%解题思路:(1)观察自来水厂净化处理的过程,分析过程中所使用的净化水的方法;
(2)根据硬水、软水与肥皂水混合所出现现象的明显不同,确定使用肥皂水区分硬水与软水;
(3)分析蒸馏水的获得过程,根据变化前后是否产生新物质,判断过程中所发生变化的类型;
(4)水中氮、磷含量过高,会引起赤潮,因此致使水中含氮、磷量增加的做法会引发赤潮;
(5)根据简易净水器的示意图,判断图示中小卵石、石英沙、活性炭的净化作用;
(6)过根据过滤时注意事项和各仪器的用途分析解答:漏斗下端紧靠烧杯内壁是为了防止滤液溅出;(1)自来水厂净化处理中经过沉淀池的沉淀、过滤池的过滤、活性炭吸附池的吸附、投药消毒的消毒杀菌,故该过程中净化水的方法主要有沉淀、过滤、吸附、消毒;
(2)使用肥皂水可区分硬水和软水,倒入肥皂水泡沫少者为硬水,泡沫丰富者为软水;
(3)制取蒸馏水的过程是加热蒸发与冷凝两种单元操作的联合,蒸发、冷凝过程中都没有新的物质形成,因此蒸馏过程属于物理变化过程;
(4)大量使用含Na5P3O10的洗衣粉和过量使用尿素[CO(NH2)2]都会造成水所氮、磷含量的增加,因此②③两种做法可能引发赤潮;
(5)简易净水器,其中小卵石、石英沙的可除去水中不溶性固体杂质,其主要作用是过滤;
(6)图中无玻璃棒引流,如不使用玻璃棒引流,会造成过滤时液体溅出,甚至会损坏滤纸;漏斗下端管口未紧靠烧杯内壁,会使液体溅出;
答案:
(1)混合物,
(2)沉淀、过滤、吸附、消毒,
(3)肥皂水,
(4)BC,
(5)过滤
(6)玻璃棒,引流,防止液体飞溅点评:
本题考点: 自来水的生产过程与净化方法;过滤的原理、方法及其应用;硬水与软水;纯净物和混合物的判别;富营养化污染与含磷洗衣粉的禁用.
考点点评: 本题为涉及较多的化学基础知识,题目难点不大但涉及面较广,耐心审题、沉着作答对于解答类似问题会有较大帮助.1年前查看全部
- (2013•柳州模拟)碱在工农业的生产中有广泛用途.下列物质中属于碱的是( )
(2013•柳州模拟)碱在工农业的生产中有广泛用途.下列物质中属于碱的是( )
A.KCl
B.H2CO3
C.Ca(OH)2
D.C2H5OH 笑看风云_19791年前1
笑看风云_19791年前1 -
 草木野空 共回答了25个问题
草木野空 共回答了25个问题 |采纳率88%解题思路:碱是电离产生的阴离子全部为氢氧根离子的化合物,据此进行分析判断即可.A、KCl是由钾离子和氯离子组成的化合物,属于盐,故选项错误.
B、H2CO3是由氢离子和碳酸根离子组成的化合物,属于酸,故选项错误.
C、Ca(OH)2是由钙离子和氢氧根离子组成的化合物,属于碱,故选项正确.
D、C2H5OH是含碳元素的化合物,属于有机物,故选项错误.
故选C.点评:
本题考点: 常见的氧化物、酸、碱和盐的判别.
考点点评: 本题难度不大,考查物质类别的判别,抓住酸、碱、盐的特征、熟悉常见的物质的组成是正确解答本题的关键.1年前查看全部
- 化学与工农业生产、环境保护、日常生活等方面有广泛联系,下列叙述正确的是 A.纯净水几乎不含任何杂质,喝纯净水比喝矿泉水对
化学与工农业生产、环境保护、日常生活等方面有广泛联系,下列叙述正确的是
A.纯净水几乎不含任何杂质,喝纯净水比喝矿泉水对人体更有营养 B.光缆在信息产业中有广泛应用,制造光缆的主要材料是二氧化硅 C.雨水样品一段时间后,pH由4.68变为4.28,是因为雨水中溶解了较多的氮氧化物和CO 2 D.二氧化硫的大量排放是造成酸雨和光化学烟雾的主要原因  aaYOYO1年前1
aaYOYO1年前1 -
 lover1852 共回答了21个问题
lover1852 共回答了21个问题 |采纳率81%B
分析:A、纯净水加工时,在去除水中的污染物的同时也去除了水中人体必需的微量元素和宏量元素.水是人体获取矿物质的重要途径,在特殊情况条件下还是主要来源.经常和纯净水会导致人体缺乏人体需要的无机盐以及一些微量元素;
B、二氧化硅常用作光导纤维;
C、酸雨中亚硫酸为弱电解质,具有还原性,能被氧化成强电解质硫酸,溶液的PH减小;
D、光化学烟雾由碳氢化合物和氮氧化合物在阳光的作用下起化学反应所产生.
A、纯净水不含人体所需的无机盐,应多喝矿泉水或自来水来补充,故A错误;
B、光纤实际是指由透明材料做成的纤芯和在它周围采用 比纤芯的折射率稍低的材料做成的包层,并将射入纤芯的光纤的光信号,经包层界面反射,使光信号在纤芯中传播前进的媒体.这种透明材料主要成分就是SiO 2 ,故B正确;
C、饱和CO 2 溶液的PH等于5.6,而雨水的pH由4.68变为4.28,是因为2H 2 SO 3 +O 2 ═2H 2 SO 4 ,故C错误;
D、大气中碳氢化合物和氮氧化合物在阳光的作用下起化学反应所产生的化学污染物,故D错误;
故选B.1年前查看全部
- 下列关于金属和金属材料的说法,正确的是( ) A.金属都以化合物的形式存在于自然界中 B.在日常生活、工农业生产中,金
下列关于金属和金属材料的说法,正确的是( ) A.金属都以化合物的形式存在于自然界中 B.在日常生活、工农业生产中,金属材料具有广泛的用途 C.铝是活泼金属,所以铝制品在空气中易腐蚀 D.金属材料严重锈蚀后不值得回收  四十五度微笑1年前1
四十五度微笑1年前1 -
 sfjz 共回答了13个问题
sfjz 共回答了13个问题 |采纳率92.3%A、多数金属化学性质活泼,所以多数金属以化合物的形式存在于自然界中,但也有少数金属如金、银等化学性质不活泼在自然界中以单质形式存在.
B、金属材料在生产和生活中被广泛应用.
C、铝易于空气中的氧气反应表面形成一层致密的氧化铝保护膜所以铝制品经久耐用.
D、回收再利用金属可大大节省能源降低金属冶炼的成本.
故答案选B.1年前查看全部
- (2012•卢湾区一模)水是宝贵的自然资源,对于人类生活、工农业生产都具有重要意义.
(2012•卢湾区一模)水是宝贵的自然资源,对于人类生活、工农业生产都具有重要意义.
①保持水的化学性质的微粒是水分子水分子(填名称);②90克水中含有6.02×10246.02×1024个氢原子;
③能够证明水由氢元素和氧元素组成的实验是2H2O
2H2↑+O2↑2H2O通电 .
2H2↑+O2↑(用化学方程式表示);通电 .
④向盛有紫色石蕊试液的试管里通入二氧化碳,石蕊变成红红色,发生的化学反应方程式是CO2+H2O═H2CO3CO2+H2O═H2CO3;
⑤实验室要配制50克20%的硝酸钾溶液,需要1010克硝酸钾,4040 毫升水.实验中除了电子天平外还必须使用的仪器有量筒、滴管、烧杯、玻璃棒量筒、滴管、烧杯、玻璃棒. 纷飞长发1年前1
纷飞长发1年前1 -
 俺能数到5 共回答了17个问题
俺能数到5 共回答了17个问题 |采纳率88.2%①分子是保持物质化学性质的最小粒子,水是由水分子构成的,所以能保持水的化学性质的最小粒子是水分子.18g水中含有6.02×1023个水分子,90g水中水分子的个数约为:6.02×1023×5=3.01×1024个水分子.含有6.02×1024个氢原子
故答案为:水分子;6.02×1024.
③水电解后生成氢气和氧气,氢气由氢元素组成,氧气有氧元素组成,在化学反应前后,元素的种类不变,所以可推出水是由氢元素和氧元素组成的.
故答案为:2H2O
通电
.
2H2↑+O2↑.
④二氧化碳溶于水生成碳酸,发生化学反应的方程式是:CO2+H2O═H2CO3;碳酸可使石蕊变红.所以向盛有紫色石蕊试液的试管里通入二氧化碳,石蕊变成红色.
故答案为:红;CO2+H2O═H2CO3.
⑤因为溶质的质量分数=
溶质的质量
溶液的质量×100%,所以:20%=
溶质质量
50×100%,溶质质量是10g,加水40mL.
配制溶液需要用到的仪器有:烧杯、量筒、玻璃棒、胶头滴管.
故答案为:10;40;量筒、滴管、烧杯、玻璃棒.1年前查看全部
- 化学与日常生活和工农业生产息息相关.
化学与日常生活和工农业生产息息相关.
(1)家庭中,鉴别硬水和软水通常可使用的方法是______(一种即可).
(2)铵态氮肥不能与碱性物质混用,其原因是______. 神仙阿牛1年前1
神仙阿牛1年前1 -
 sita2002 共回答了13个问题
sita2002 共回答了13个问题 |采纳率100%(1)由于向硬水中倒入肥皂水时,泡沫很少,而倒入软水中的肥皂水则会产生大量的泡沫,因此通过采取加肥皂水的方法鉴别硬水与软水;(2)含铵根的铵态氮肥遇到碱性物质时,两种物质发生反应而放出氨气,使铵态氮...1年前查看全部
- 请列举密度在工农业生产以及日常生活中的应用实例(不少于6个例子).
 340522481年前1
340522481年前1 -
 菲雪一族 共回答了15个问题
菲雪一族 共回答了15个问题 |采纳率86.7%密度的实际应用举例:
a. 地质勘探队员,根据样品的密度,确定矿藏的种类及其经济价值;
b. 农民利用风力扬场,对饱满麦粒、瘪粒、草屑分拣;
c. 农业上,利用盐水漂浮选种;
d. 商业中,鉴别牛奶、酒的浓度(注:一般用液体密度计);
e. 交通工具、航天器材中,选用高强度、低密度的合金材料、玻璃钢等复合材料;
f. 产品包装中,采用密度小的泡沫塑料作填充物,达到防震、便于运输、价格低廉等目的;
g. 化学实验中,萃取实验将不同的两种物质分离开来,也是利用了密度不同分离的实例.
希望帮助到你,若有疑问,可以追问~~~
祝你学习进步,更上一层楼!(*^__^*)1年前查看全部
- 乙湖周边地区人口稠密,工农业发达,应特别注意防止湖水
乙湖周边地区人口稠密,工农业发达,应特别注意防止湖水
A.富营养化
B.水体枯竭
C.酸度增大
D.碱度增大
乙湖在钱塘江旁边 angelnana19821年前2
angelnana19821年前2 -
 一切变得简单 共回答了27个问题
一切变得简单 共回答了27个问题 |采纳率88.9%A,如果只是单选的话,由于工农业发达,人口密集,生活和工农业污水大量排放到水体中,这些污水中含氮磷的有机物含量丰富,有利于水中藻类的生长,造成富营养化.
由于在钱塘江旁边,有水源补给,不会造成水体枯竭
而在有流动水的地区酸碱度的变化也不大,况且在污水处理的时候有害的酸碱离子很多被处理掉了1年前查看全部
- "工农业总产值"和"中小学教师"英文如何翻译
 caixiao66881年前3
caixiao66881年前3 -
 我的爱还在不在 共回答了19个问题
我的爱还在不在 共回答了19个问题 |采纳率89.5%工农业总产值 一般翻译成 Gross industrial and agricultural output value
在句子中也有这样的翻译
在本世纪末实现工农业总产值翻两番的目标是完全可能的.
译:It is entirely possible to achieve the goal of quadrupling the gross annual value of industrial and agricultural production by the end of the century.
中小学教师
Teachers of primary and middle schools1年前查看全部
- 人类的生活和工农业生产都离不开水.下图是自来水厂净水过程示意图.
人类的生活和工农业生产都离不开水.下图是自来水厂净水过程示意图.
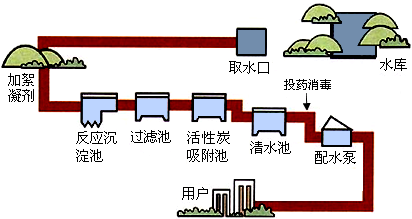
请根据图示回答下列问题:
(1)自来水厂生产自来水时,使用的净水方法有______;
A、沉淀B、过滤C、煮沸D、蒸馏E、吸附
(2)取水后加入絮凝剂(明矾)的作用是______;
(3)自来水厂常用二氧化氯进行投药消毒,二氧化氯的化学式为______;
(4)漂白粉(有效成分为次氯酸钙)也可用为饮水消毒剂,次氯酸钙[Ca(ClO)2]中氯元素的化合价为______. 点点3651年前1
点点3651年前1 -
 88516592 共回答了12个问题
88516592 共回答了12个问题 |采纳率91.7%解题思路:可以根据净化水的方法方面进行分析、考虑,从而得出正确的结论;根据化学式的书写规则来书写化学式;根据化合物中正负化合价的代数和为零计算元素的化合价.(1)自来水厂生产自来水时,使用的净水方法有沉淀、过滤、吸附.故填:ABE.
(2)加入絮凝剂(明矾)的作用是吸附水中的杂质,使其沉降.故填:吸附水中的杂质,使其沉降.
(3)二氧化氯的化学式为:ClO2
(4)根据化合物中元素的化合价代数和为零可以求出氯元素的化合价是+1价.故填:+1.点评:
本题考点: 水的净化.
考点点评: 解答本题要充分理解化学式的含义及其化合价的求法,能够把图中信息和化学知识有机的结合起来.1年前查看全部
- 水是一种重要的自然资源,与人类和生物的生存、工农业生产息息相关,对以下有关水的认识或观点,你认为正确的是______.
水是一种重要的自然资源,与人类和生物的生存、工农业生产息息相关,对以下有关水的认识或观点,你认为正确的是______.
A、比热比砂石、干泥土大得多,这是沿海地区温差比内陆地区小的主要原因.
B、水能灭火,但把少量水撒到烧旺的煤炉里面,火焰反而更猛烈,此时水起到催化剂的作用.
C、往自来水中滴入硝酸银溶液,有白色沉淀产生;盛开水的热水瓶底常沉积一层水垢,这些都说明地表水不是纯净物.
D、“水能载舟”是因为水有浮力,物体浸没在水中越深,受到的浮力越大. MISS6661年前1
MISS6661年前1 -
 qiuqinqun 共回答了17个问题
qiuqinqun 共回答了17个问题 |采纳率100%解题思路:水是一种重要的自然资源,与人类和生物的生存、工农业生产息息相关.我们要会解释与水有关的现象.如水的比热比砂石、干泥土大得多,因此沿海地区温差比内陆地区小.A、水的比热比砂石、干泥土大得多,因此沿海地区温差比内陆地区小.故A正确;
B、水能灭火,但把少量水撒到烧旺的煤炉里面,火焰反而更猛烈,因为水与碳反应生成了水煤气.故B错误;
C、往自来水中滴入硝酸银溶液,有白色沉淀产生;盛开水的热水瓶底常沉积一层水垢,这些都说明地表水不是纯净物.故C正确;
D、水能载舟”是因为水有浮力,物体浸没在水中越深,受到的浮力越大.故D正确;
故选ACD.点评:
本题考点: 水资源状况;水的性质和应用;纯净物和混合物的判别.
考点点评: 本题考查水资源的状况及对水的有关认识.水能载舟”是因为水有浮力,物体浸没在水中越深,受到的浮力越大.1年前查看全部
- 有关土壤与人类活动的关系的叙述,正确的是 [ ] A、土壤与工农业生产关
有关土壤与人类活动的关系的叙述,正确的是 [ ]A、土壤与工农业生产关系都很密切
B、土壤退化与人类不合理的耕作经营活动无关
C、南方水稻土的形成与人类长期的耕作和培育有关
D、土壤是一种永续性的可更新的资源,无论如何利用都不会损耗其肥力 fghjk43211年前1
fghjk43211年前1 -
 祝英台与朱丽叶 共回答了21个问题
祝英台与朱丽叶 共回答了21个问题 |采纳率85.7%C1年前查看全部
- 水是生命之源,我们应该了解水、爱护水资源.人类的生活和工农业生产都离不开水.
水是生命之源,我们应该了解水、爱护水资源.人类的生活和工农业生产都离不开水.
资料一:图I是自来水厂净水过程示意图.
资料二:图II是自来水消毒过程中发生化学反应的微观过程.
请根据图示回答下列问题:
(1)根据图I表示的生产自来水过程,判断其使用的净水方法有_______.(填字母)
A.沉淀B.过滤C.煮沸D.蒸馏E.吸附
(2)根据图II b写出反应的基本反应类型为______.
(3)水的硬度是一项重要的化学指标.日常生活中如何区分硬水与软水?请简述实验步骤与现象:______.
(4)某同学制作的简易净水器如图所示,活性炭的作用是______,小卵石、石英砂和蓬松棉的作用是______,
在实验室进行该操作,不需要用到下列仪器中的(填名称)______、______.
 woaixiaolizi1年前1
woaixiaolizi1年前1 -
 冷鋒 共回答了14个问题
冷鋒 共回答了14个问题 |采纳率100%(1)从自来水厂的净化过程可以得出净水的方法有:沉淀、过滤和吸附,故选ABE;
(2)从图b中可以看出反应物为一种,而生成物为两种,所以该反应属于分解反应;
(3)硬水中含有较多的钙镁离子,而软水中不含或含有较少的钙镁离子,所以可以用肥皂水来区分,产生泡沫多的是软水,产生泡沫少的是硬水;
(4)活性炭具有吸附性,所以其作用为吸附作用,而石英砂、蓬松棉所起的作用为过滤出不溶性的杂质;在实验室净水的过程中用不到酒精灯和量筒;
故答案为:(1)A B E;
(2)分解反应;
(3)向样品中加入肥皂水,产生泡沫较多浮渣较少的为软水,反之则为硬水;
(4)吸附; 过滤;酒精灯; 量筒.1年前查看全部
- (2004•绵阳)传送带在工农业生产中有广泛的应用,四川长虹电器股份公司的彩电生产线主要靠传送带连接.在生产过程中水平的
(2004•绵阳)传送带在工农业生产中有广泛的应用,四川长虹电器股份公司的彩电生产线主要靠传送带连接.在生产过程中水平的传送带匀速运动,将半成品或下一步需要的元器件传递下去,若不考虑空气的作用,则长方体形的遥控器塑料外壳在传送带上随传送带运动的过程中除受重力和支持力外( )
A.还受摩擦力作用
B.还受摩擦力和拉力作用
C.还受拉力作用
D.不受其它力作用 郁闷狂人1年前1
郁闷狂人1年前1 -
 wqfsa3ewqf 共回答了23个问题
wqfsa3ewqf 共回答了23个问题 |采纳率95.7%解题思路:物体处于静止或者匀速直线运动状态时,不受力或者受平衡力的作用.在传送带上的物体做匀速直线运动,在竖直方向上受重力和支持力的作用,二者是一对平衡力;而在水平方向上,不受任何力的作用.
故选D.点评:
本题考点: 力与运动的关系.
考点点评: 解答本题的关键是抓住物体的运动状态,结合运动状态进行受力分析.1年前查看全部
- 你能根据本课题所学和已有知识归纳水的性质吗?水在生活和工农业生产上有哪些用途
你能根据本课题所学和已有知识归纳水的性质吗?水在生活和工农业生产上有哪些用途
水对人类来说,真是太重要了。因为水在人体的各部组织中占了主要的成分。譬如一个看起来很强壮很结实的青年人,其实他体重的65%左右是水分,婴儿体内的含水量更多,约占他体重的75%。至于人体血液中所含的水量竟占到96%之多。因此人体如果缺少了大量水分,那么血液就流动不畅,就不能顺利地把氧气输送到各部组织里去。根据实验的结果:人体中如果一下子失去10%的水分,那就要生病;如果失去20%就会死亡。所以人不能离开水,没有水就没有生命。
你能根据本课题(水的组成)所学知识和已有知识归纳水的性质吗?水在生活和工农业生产上有哪些用途? (至少举三例)
 niaoniaoceo1年前1
niaoniaoceo1年前1 -
 shhtas168 共回答了14个问题
shhtas168 共回答了14个问题 |采纳率92.9%水的性质:
物理性质:水常温下液体,标准大气压下沸点100摄氏度,凝固点0摄氏度,密度为1G/CM3,无色透明状,无味,可以作为很多物质的溶剂。
化学性质:分子式H2O,具有一定的氧化性。
生产:
1.灌溉植物
2。溶解血液输送人体所需各种物质。
3.H2O作为溶剂,可以作为工业原料,更有望为清洁能源H2做原料1年前查看全部
- 2003年7-8月间,我国南方一些地区出现了历史上罕见的高温天气,对这些地区的工农业生产及居民生活都产生了严重的影响.回
2003年7-8月间,我国南方一些地区出现了历史上罕见的高温天气,对这些地区的工农业生产及居民生活都产生了严重的影响.回答5~7题.
在南方受高温煎熬的时段,我国北方很可能出现( )
A.寒冷干燥天气
B.高温多雨天气
C.干热风天气
D.晴朗温暖天气 红苹果子1年前1
红苹果子1年前1 -
 uu轻 共回答了23个问题
uu轻 共回答了23个问题 |采纳率95.7%解题思路:主要考查了副热带高压与我国东部的天气,如果副高提前北进,北方回出现洪涝,南方会出现干旱.2003年7-8月间,我国南方一些地区出现了历史上罕见的高温天气,如果副高提前北进,北方回出现洪涝,南方会出现干旱,在南方受高温煎熬的时段,我国北方很可能出现高温多雨天气.
故选:B.点评:
本题考点: 气压系统与天气.
考点点评: 本题难度适中,属于知识性试题,要求学生熟练掌握副高与我国东部的天气.1年前查看全部
- 中和反应在日常生活和工农业生产中有广泛的饮用.下列做法中,利用中和反应的是( )A.用熟石灰处理
中和反应在日常生活和工农业生产中有广泛的饮用.下列做法中,利用中和反应的是( )A.用熟石灰处理
中和反应在日常生活和工农业生产中有广泛的饮用.下列做法中,利用中和反应的是( )
A.用熟石灰处理硫酸厂废水含有的硫酸
B.用主要成分为碳酸氢钠的药物治疗胃酸过多
C.用熟石灰与硫酸铜溶液来配置农药波尔多液
D.用稀盐酸除去铁制品表面的铁锈
 皮皮鲁6661年前1
皮皮鲁6661年前1 -
 wangrui9825106 共回答了25个问题
wangrui9825106 共回答了25个问题 |采纳率88%A、熟石灰与硫酸反应生成硫酸钙和水,该反应是酸与碱反应生成盐和水的反应,属于中和反应,故选项正确.
B、碳酸氢钠与胃酸中的盐酸反应生成氯化钠、水和二氧化碳,该反应的反应物是盐和酸,生成物是盐、水和二氧化碳,不属于中和反应,故选项错误.
C、熟石灰与硫酸铜溶液反应生成氢氧化铜沉淀和硫酸钙,该反应的反应物是碱和盐,不属于中和反应,故选项错误.
D、铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,该反应的反应物是金属氧化物和酸,不属于中和反应,故选项错误.
故选:A.1年前查看全部
- 生命的孕育和维系需要水,日常生活和工农业生产离不开水,学习和认识水很重要.
生命的孕育和维系需要水,日常生活和工农业生产离不开水,学习和认识水很重要.
(1)请列举水在实验室中的一种用途:配制溶液等配制溶液等
(2)无论是自来水还是纯净水,你认为保持水的化学性质的最小粒子是水分子水分子
(3)下列选项中能确认水是由氧元素和氢元素组成的实验是:CC(填序号)
A.水的蒸馏B.水的蒸发C.水的电解D.水的净化
(4)去年冬天至今年春天,我国西南地区遭遇大范围持续干旱.有些村庄打深井取用地下水.检验地下水是硬水还是软水,可用的物质是肥皂水肥皂水
(5)农业和园林浇灌植物时,将大水漫灌改为喷灌或滴灌的目的是节约用水节约用水
(6)世博园区内有许多饮水台,可取水直接饮用.其中的饮用水处理过程中使用了炭罐(内含颗粒活性炭),炭罐的作用是:吸附杂质吸附杂质. zhzyhahazhzy1年前1
zhzyhahazhzy1年前1 -
 打天打鸭 共回答了14个问题
打天打鸭 共回答了14个问题 |采纳率85.7%(1)水在实验室中有很多用途,可以作溶剂配制溶液、洗涤仪器等.
(2)分子是保持物质化学性质的最小粒子,水是由水分子构成的,所以保持水的化学性质的最小粒子是水分子.
(3)能确认水是由氧元素和氢元素组成的实验可根据质量守恒定律,反应前后元素种类不变,水的电解实验生成了氢气和氧气,说明水是由氢元素和氧元素组成的.
(4)硬水、软水可用肥皂水鉴别,产生泡沫较多的是软水,产生泡沫较少的是硬水.
(5)农业和园林浇灌植物时,将大水漫灌改为喷灌、滴灌,可减小农业用水量,主要是为了节约用水.
(6)活性炭具有吸附性,能吸附色素、异味等.
故答案为:(1)配制溶液(或洗涤,只要合理均给分);(2)水分子;(3)C;(4)肥皂水;(5)节约用水;(6)吸附杂质.1年前查看全部
- 氢氧化钙在工农业生产上应用很广,下列关于氢氧化钙的描述错误的是( ) A.其水溶液能使紫色石蕊试液变红 B.俗称熟石灰
氢氧化钙在工农业生产上应用很广,下列关于氢氧化钙的描述错误的是( ) A.其水溶液能使紫色石蕊试液变红 B.俗称熟石灰或消石灰 C.可用于改良酸性土壤 D.对皮肤、衣服等有腐蚀作用  benmaogao1年前1
benmaogao1年前1 -
 xq279 共回答了18个问题
xq279 共回答了18个问题 |采纳率83.3%A、氢氧化钙为碱,其水溶液可以使紫色石蕊变蓝,故A描述错误;
B、氢氧化钙俗称熟石灰或消石灰,故B描述正确;
C、氢氧化钙为碱性物质,常用来改良酸性土壤,故C描述正确;
D、氢氧化钙为碱性物质,对皮肤或衣服有一定的腐蚀能力,故D描述正确.
故选A.1年前查看全部
- 随着科技和工农业生产的发展,环境污染日趋严重,已严重威胁到人类的生存.为保护环境,减少对树木的砍伐,一种新型的“石头纸”
随着科技和工农业生产的发展,环境污染日趋严重,已严重威胁到人类的生存.为保护环境,减少对树木的砍伐,一种新型的“石头纸”应运而生.这种纸的主要成分是碳酸钙,外观与普通纸相似.鉴别“石头纸”与普通纸的方法有多种,若分别点燃两种纸,则______是“石头纸”;若要证明石头纸的成分是碳酸盐,则必需的实验操作是______.实验过程中所发生反应的化学方程式为:______;______.
 putong1年前1
putong1年前1 -
 fuying2000 共回答了17个问题
fuying2000 共回答了17个问题 |采纳率100%解题思路:普通纸能燃烧,而“石头纸”不能燃烧;但碳酸盐能与酸反应生成二氧化碳;根据反应原理正确书写化学方程式;普通纸能燃烧,而含碳酸钙的纸不能燃烧;但是“石头纸”是碳酸盐能与酸反应生成使澄清石灰水变浑浊的二氧化碳;
故答案为:不能燃烧的; 取适量石头纸于试管中滴加稀盐酸,将生成气体通入澄清石灰水;CaCO3+2HCl═CaCl2+H2O+CO2↑,
Ca(OH)2+CO2=CaCO3↓+H2O.点评:
本题考点: 证明碳酸盐;书写化学方程式、文字表达式、电离方程式.
考点点评: 了解物质的性质是解答此题的关键,此类题形式新颖,起点高,落脚点低,认真分析题目信息,并结合相关知识分析解答即可.1年前查看全部
- 已知:A为常见的短周期轻金属,含A的合金材料常用于火箭、飞机等制造业;B是一种盐,在工农业生产中用途较广;C、F、H为常
已知:A为常见的短周期轻金属,含A的合金材料常用于火箭、飞机等制造业;B是一种盐,在工农业生产中用途较广;C、F、H为常见非金属单质;常温下C、F、I、E、J和K为气体;E对空气的相对密度为0.586;常温常压下G为液体.有关物质间的转化关系如下(图中部分反应物或产物已省略):

请填空:
(1)B的化学式为______.
(2)操作a必须在HCl气流中加热得无水物而不能直接加热浓缩,其原因是______;操作b为______.
(3)反应①的离子反应方程式为______.反应③的化学反应方程式为4NH3+5O2
4NO+6H2O催化剂 .△ 4NH3+5O2.
4NO+6H2O催化剂 .△  绿瘦红肥1年前1
绿瘦红肥1年前1 -
 岸暖风晴 共回答了19个问题
岸暖风晴 共回答了19个问题 |采纳率94.7%解题思路:E对空气的相对密度为0.586,其相对分子质量=0.586×29=17,且E为气体,可推知E为NH3,E与F连续反应得到K,且F、J、K均为气体,可推知F为O2、J为NO、K为NO2,常温常压下G为液体,与K反应得到L浓溶液,则G为H2O、L为HNO3,D系列转化得到黄绿色气体为Cl2,结合转化关系及元素守恒可推知B为NH4Cl,气体C与F反应得到G,可推知C为H2,非金属单质H与浓硝酸反应得到G、I、K,且金属A可以在I中燃烧得到H,可推知H为碳、I为CO2,A为Mg,结合转化关系可知D为MgCl2,据此解答.E对空气的相对密度为0.586,其相对分子质量=0.586×29=17,且E为气体,可推知E为NH3,E与F连续反应得到K,且F、J、K均为气体,可推知F为O2、J为NO、K为NO2,常温常压下G为液体,与K反应得到L浓溶液,则G为H2O、L为HNO3,D系列转化得到黄绿色气体为Cl2,结合转化关系及元素守恒可推知B为NH4Cl,气体C与F反应得到G,可推知C为H2,非金属单质H与浓硝酸反应得到G、I、K,且金属A可以在I中燃烧得到H,可推知H为碳、I为CO2,A为Mg,结合转化关系可知D为MgCl2,
(1)由上述分析可知,B的化学式为NH4Cl,故答案为:NH4Cl;
(2)操作a是由氯化镁溶液得到氯化镁晶体,应用溶液中镁离子水解得到氢氧化镁与HCl,必须在HCl气流中加热得无水物而不能直接加热浓缩,其原因是抑制Mg2+的水解;操作b是电解熔融的氯化镁得到Mg与氯气,
故答案为:抑制Mg2+的水解;熔融状态下电解;
(3)反应①的离子反应方程式为为:Mg+2NH4+═Mg2++H2↑+2NH3↑,反应③的化学反应方程式为:4NH3+5O2
催化剂
.
△4NO+6H2O,
故答案为:Mg+2NH4+═Mg2++H2↑+2NH3↑;4NH3+5O2
催化剂
.
△4NO+6H2O.点评:
本题考点: 无机物的推断.
考点点评: 本题考查无机物推断,E的相对密度及可以连续反应是推断突破口,再结合转化关系推断,需要学生熟练掌握Mg与二氧化碳的反应,在无机推断中经常涉及,反应①在中学没有涉及,是推断障碍,利用推断的产物判断发生的反应,难度较大.1年前查看全部
- 氧气在日常生活、工农业生产以及科技上都有着非常重要的用途。下列有关氧气的说法正确的是 A.鱼、虾能在水中生存说明氧气易溶
氧气在日常生活、工农业生产以及科技上都有着非常重要的用途。下列有关氧气的说法正确的是
A.鱼、虾能在水中生存说明氧气易溶于水 B.物质与氧气发生的反应都是氧化反应 C.氧气的化学性质比较活泼,是可燃物 D.工业上用分离液态空气法得到氧气是分解反应  ILOVYOU1年前1
ILOVYOU1年前1 -
 谁家小娘子 共回答了17个问题
谁家小娘子 共回答了17个问题 |采纳率88.2%B
1年前查看全部
- 水是生命之源,人类的日常生活与工农业生产都离不开水.
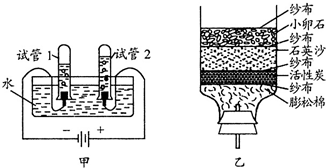 水是生命之源,人类的日常生活与工农业生产都离不开水.
水是生命之源,人类的日常生活与工农业生产都离不开水.
(1)小明利用图甲所 示的装置探究水的组成,通电一段时间后,试管1中所收集的气体为______,试管2中所收集的气体为______,前者与后者的体积比约为______,该实验说明水是由______组成的.
(2)小明为了净化收集到的雨水,自制了一个如图乙所示的简易净水器,其中小卵石、石英沙和膨松棉的作用是______,活性炭的作用是______.
(3)要判断净化后的水是硬水还是软水,你认为可用______来检验.长期饮用硬水对人体健康不利,要降低水的硬度,可采取______的方法. 天边的那棵树1年前1
天边的那棵树1年前1 -
 炽虎 共回答了25个问题
炽虎 共回答了25个问题 |采纳率96%解题思路:(1)依据电解水实验的现象、结论进行解答;
(2)根据小卵石、石英沙和膨松棉的作用是过滤,活性炭的作用是吸附作用进行解答;
(3)根据用肥皂水鉴别净化后的水是硬水还是软水,降低水的硬度,可采取煮沸的方法进行解答.(1)利用图甲所示的装置探究水的组成,通电一段时间后,试管1中所收集的气体体积较多是氢气,试管2中所收集的气体体积较少为氧气,前者与后者的体积比约为2:1,该实验说明水是由氢、氧元素组成的;
(2)小明为了净化收集到的雨水,自制了一个如图乙所示的简易净水器,其中小卵石、石英沙和膨松棉的作用是过滤雨水中的固体(或不溶性)杂质,活性炭的作用是吸附异味,色素;
(3)要判断净化后的水是硬水还是软水,可用肥皂水来检验,其中产生泡沫较少的是硬水,泡沫较多的是软水.长期饮用硬水对人体健康不利,要降低水的硬度,可采取煮沸的方法.
故答案为:(1)氢气;氧气;2﹕1;氢元素和氧元素;
(2)过滤雨水中的固体(或不溶性)杂质;吸附异味,色素;
(3)肥皂水;煮沸.点评:
本题考点: 电解水实验;水的净化;硬水与软水.
考点点评: 熟记电解水的实验现象、结论,以及净水的知识即可轻松解题.1年前查看全部
- 化学与工农业生产、环境保护、日常生活等方面有广泛联系,下列叙述正确的是( ) A.棉花和木材的主要成分都是纤维素、蚕丝
化学与工农业生产、环境保护、日常生活等方面有广泛联系,下列叙述正确的是()
A.棉花和木材的主要成分都是纤维素、蚕丝和人造丝的主要成分都是蛋白质 B.腌制熟食品时,添加少量亚硝酸钠,是为了使其味道更加美味可口 C.为了防止月饼等富脂食品氧化变质,延长食品的保质期,常在包装袋中放入生石灰 D.“神七”宇航员所穿出舱航天服是由我国自行研制的新型“连续纤维增韧”航空材料做成的,其主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型无机非金属材料  哈拉1年前1
哈拉1年前1 -
 boxxp 共回答了18个问题
boxxp 共回答了18个问题 |采纳率94.4%D
A:人造丝为人造纤维,不正确
B:亚硝酸钠有毒,不正确
C:生石灰可吸水,但并不能防止仪器氧化,不正确
D:正确1年前查看全部
- 中和反应在工农业生产和日常生活中有广泛的用途.下列应用与中和反应原理无关的是( )
中和反应在工农业生产和日常生活中有广泛的用途.下列应用与中和反应原理无关的是( )
A.蚊虫丁咬后可涂稀氨水减轻痛痒
B.服用含Al(OH)3的药物治疗胃酸过多
C.用熟石灰和硫酸铜配制波尔多液
D.用NaOH溶液洗涤石油产品中的残余硫酸 第五天堂1年前1
第五天堂1年前1 -
 李骥 共回答了25个问题
李骥 共回答了25个问题 |采纳率88%解题思路:中和反应是酸与碱作用生成盐和水的反应,反应物是酸和碱,生成物是盐和水,据此进行分析判断.A、稀氨水属于碱,能与蚊虫丁咬后产生的蚁酸反应生成盐和水,属于中和反应.
B、Al(OH)3与胃液中的盐酸反应生成氯化铝和水,是酸与碱的反应,属于中和反应.
C、熟石灰与硫酸铜溶液反应生成氢氧化铜沉淀和硫酸钙,不是酸与碱的反应,不属于中和反应.
D、NaOH溶液与硫酸反应生成硫酸钠和水,是酸与碱的反应,属于中和反应.
故选:C.点评:
本题考点: 中和反应及其应用.
考点点评: 本题难度不大,掌握中和反应的特征(反应物是酸和碱,生成物是盐和水)是正确解答此类题的关键.1年前查看全部
- 超声波在科学技术、工农业生产、医疗卫生等方面有着广泛的应用,利用回声定位的原理可探测海洋深度、绘制水下数千米的地形图,科
超声波在科学技术、工农业生产、医疗卫生等方面有着广泛的应用,利用回声定位的原理可探测海洋深度、绘制水下数千米的地形图,科学家利用这一原理发明了 装置,而B超利用的是它 的特点.次声波在自然界 、 等现象中都会产生。  cbouamyd1年前1
cbouamyd1年前1 -
 恩EN123 共回答了22个问题
恩EN123 共回答了22个问题 |采纳率81.8%声呐,穿透能力强,台风,海啸。1年前查看全部
- 工农业及城市生活污水中含磷.家用洗涤剂是污水中磷的一个重要来源(洗涤剂含有磷酸钠).关于处理污水时要不要除去磷的说法正确
工农业及城市生活污水中含磷.家用洗涤剂是污水中磷的一个重要来源(洗涤剂含有磷酸钠).关于处理污水时要不要除去磷的说法正确的是( )
A. 磷是生物所需的营养元素,不必除去
B. 含磷的污水是很好的肥料,不必除去
C. 含磷污水排到自然水中引起藻类增殖,使水变质,必须除去
D. 磷对人无毒,除去与否都无关紧要 edisonrei71年前1
edisonrei71年前1 -
 wjpea1 共回答了17个问题
wjpea1 共回答了17个问题 |采纳率76.5%解题思路:磷是植物生长的营养元素,大量排放到河流中,会导致藻类增殖,使水变质,水中鱼类物质死亡,以此解答.磷虽然是生物的营养元素,但摄入过多有害,且水中含量过高时会造成水体富营养化,致使水生藻类大量繁殖,由于水中缺氧造成水中生物大量死亡,遗体腐败,水质恶化,所以应杜绝含磷废水的排放,
故选C.点评:
本题考点: 常见的生活环境的污染及治理.
考点点评: 本题考查环境污染知识,为高频考点,注意水是人类宝贵的自然资源,与水相关的化学知识是化学考查热点之一,在水资源日益匮乏的今天,节约水资源、水污染及防治等内容,题目难度不大.1年前查看全部
- (2014•青岛二模)碳、氮、硫是中学化学重要的非金属元素,在工农业生产中有广泛的应用.
(2014•青岛二模)碳、氮、硫是中学化学重要的非金属元素,在工农业生产中有广泛的应用.
(1)用于发射“天宫一号”的长征二号F火箭的燃料是液态偏二甲肼(CH3-NH-NH-CH3),氧化剂是液态四氧化二氮.二者在反应过程中放出大量能量,同时生成无毒、无污染的气体.已知室温下,1g燃料完全燃烧释放出的能量为42.5kJ,请写出该反应的热化学方程式______.
(2)298K时,在2L的密闭容器中,发生可逆反应:2NO2(g)⇌N2O4(g)△H=-a kJ•mol-1(a>0).N2O4的物质的量浓度随时间变化如图1.达平衡时,N2O4的浓度为NO2的2倍,回答下列问题.
①298k时,该反应的平衡常数为______ L•mol-1.
②下列事实能判断该反应处于平衡状态的是______.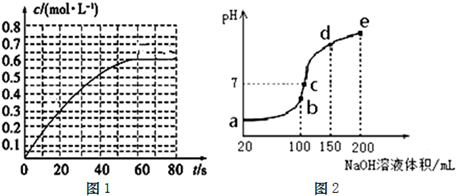
a.混合气体的密度保持不变
b.混合气体的颜色不再变化
c.V(N2O4)正=2V(NO2)逆
③若反应在398K进行,某时刻测得n(NO2)=0.6mol,n(N2O4)=1.2mol,则此时V(正)______V(逆)(填“>”“<”或“=”).
(3)NH4HSO4在分析试剂、医药、电子工业中用途广泛.现向100mL 0.1mol•L-1 NH4HSO4溶液中滴加0.1mol•L-1 NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图2.试分析图2中a、b、c、d、e五个点,
①水的电离程度最大的是______;
②其溶液中c(OH-)的数值最接近NH3•H2O的电离常数K数值的是______;
③在c点,溶液中各离子浓度由大到小的排列顺序是______. nuoqi1年前1
nuoqi1年前1 -
 我是河南人2006 共回答了12个问题
我是河南人2006 共回答了12个问题 |采纳率100%解题思路:(1)先求出偏二甲肼的物质的量,再根据物质的量之比等于热量比求出反应热,然后写出热化学方程式;
(2)①有图可知N2O4的平衡浓度为0.6mol/L,达到平衡时,N2O4的浓度为NO2的2倍,则NO2的平衡浓度为0.3mol/L,带入平衡常数表达式计算;
②a、气体的质量不变,容积恒定,因此气体的密度为一定值;
b、混合气体的颜色不变说明NO2的浓度保持恒定;
c、当2V(N2O4)正=V(NO2)逆时,正、逆反应速率相等;
③反应为放热反应,升高温度,K值减小,计算可知此时的浓度商Q=K(298K)>K(398K),反应向逆反应方向移动,因此V(正)<V(逆);
(3)①a、b、c、d、e五个点,根据反应量的关系,b点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4;c、d、e三点溶液均含有NH3•H2O,(NH4)2SO4可以促进水的电离,而NH3•H2O抑制水的电离.
②溶液中铵根离子浓度与一水合氨浓度最接近时,溶液中c(OH-)的数值最接近NH3•H2O的电离常数K数值;
③c点溶液呈中性,则溶液含有(NH4)2SO4、Na2SO4、NH3•H2O三种成分.(1)1g燃料完全燃烧释放出的能量为42.5kJ,则1mol偏二甲肼完全燃烧释放出的能量为42.5kJ×60=2550kJ,其热化学方程式为:C2H8N2(l)+2N2O4(l)═2CO2(g)+3N2(g)+4H2O(l)△H=-2550 kJ/mol;
故答案为:C2H8N2(l)+2N2O4(l)═2CO2(g)+3N2(g)+4H2O(l)△H=-2550 kJ/mol;
(2)①有图可知N2O4的平衡浓度为0.6mol/L,达到平衡时,N2O4的浓度为NO2的2倍,则NO2的平衡浓度为0.3mol/L,
则K=
c(N2O4)
c2(NO2)=[0.6mol/L
(0.3mol/L)2=6.67L/mol,
故答案为:6.67;
②a、反应物和生成物全是气态物质,气体的质量不变,容积为2L保持恒定,由ρ=
m/V]可知气体的密度为一定值,因此气体的密度保持不变不一定处于平衡状态,故a错误;
b、混合气体的颜色不变说明NO2的浓度不变,说明反应处于化学平衡状态,故b正确;
c、当2V(N2O4)正=V(NO2)逆时,正、逆反应速率相等,说明反应处于化学平衡状态,故c错误;
故答案为:b;
③反应为放热反应,升高温度,K值减小,密闭容器的体积为2L,因此的N2O4的浓度为0.6mol/L,N2O4的浓度为0.3mol/L,浓度商Q=
c(N2O4)
c2(NO2)=
0.6mol/L
(0.3mol/L)2=6.67L/mol=K(298K)>K(398K),反应向逆反应方向移动,因此V(正)<V(逆);
故答案为:<;
(3)①a、b、c、d、e五个点,根据反应量的关系,b点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4;c、d、e三点溶液均含有NH3•H2O,(NH4)2SO4可以促进水的电离,而NH3•H2O抑制水的电离,因此水的电离程度最大的是b点,溶液中c(OH-)的数值最接近NH3•H2O的电离常数K数值,
故答案为:b;
②氨水为弱碱,溶液呈碱性,c点溶液呈中性,铵根离子浓度过大,e点溶液碱性过强,一水合氨浓度过大,相对而言d点溶液中铵根离子浓度与一水合氨浓度最接近,溶液中c(OH-)的数值最接近NH3•H2O的电离常数K数值,
故答案为:d;
③c点溶液呈中性,即溶液含有(NH4)2SO4、Na2SO4、NH3•H2O三种成分,b点时c(Na+)=c(SO42-),b点时c(Na+)>c(SO42-),根据N元素与S元素的关系,可以得出c(SO42-)>c(NH4+),故c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+),
故答案为:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+).点评:
本题考点: 热化学方程式;用化学平衡常数进行计算;化学平衡状态的判断;物质的量或浓度随时间的变化曲线;弱电解质在水溶液中的电离平衡.
考点点评: 本题考查知识点全面,涉及热化学方程式的书写、平衡常数的计算、平衡的移动、离子浓度大小比较、盐类水解等知识点,离子浓度大小比较常与盐类水解、弱电解质的电离联合考查,确定离子浓度大小时要结合电荷守恒、物料守恒来分析解答.1年前查看全部
- 空气、水、天然气、石油和煤等自然资源对人类的生存、日常生活和工农业生产都有着极其广泛和重要的用途.请将与下列用途相对应的
空气、水、天然气、石油和煤等自然资源对人类的生存、日常生活和工农业生产都有着极其广泛和重要的用途.请将与下列用途相对应的物质名称填在空白处:
(1)常用作溶剂的是______;
(2)可用作生活燃料、并能通过管道长途输送的是______;
(3)直接供给人和动物呼吸的是______;
(4)可用于生产城市居***活用管道煤气的是______;
(5)是重要的化工原料而被称为“工业血液”的是______;
(6)可用于获取充置霓虹灯的气体的是______. fatxfat1年前1
fatxfat1年前1 -
 dy_yaili 共回答了26个问题
dy_yaili 共回答了26个问题 |采纳率92.3%解题思路:可以从物质的性质和用途方面进行分析、考虑,从而得出正确的结论.(1)水是常用的溶剂,故填:水.
(2)天然气是人们利用率高并且通过管道输送的燃料,故填:天然气.
(3)氧气能供给呼吸,故填:氧气.
(4)煤常用来生产煤气,故填:煤.
(5)石油被称为工业的血液,故填:石油.
(6)空气中含有的稀有气体常常用作填充霓虹灯,故填:空气.点评:
本题考点: 化石燃料及其综合利用;氧气的用途;常见的溶剂.
考点点评: 本题主要考查了如何根据物质的性质确定物质的用途方面的问题.1年前查看全部
- 碳酸钠与工农业生产、日常生活紧密相关.工业碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品中往往含有少量NaCl,现欲测定样
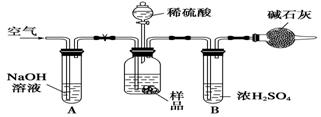
碳酸钠与工农业生产、日常生活紧密相关.工业碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品中往往含有少量NaCl,现欲测定样品中Na2CO3的质量分数,某探究性学习小组分别设计了如下实验方案.请回答下列有关问题:
方案三:质量差分析法
(3)把一定质量的样品和足量的稀硫酸反应,采用上右图所示装置,通过称量反应前后盛有碱石灰的干燥管的质量,利用其质量差求算样品的纯度.
该实验的操作步骤有:①在干燥管内填满碱石灰,质量为m g;②取n g样品装入广口瓶中;③检验装置的气密性;④缓慢鼓入空气数分钟,再称量干燥管质量为w g;⑤关闭止水夹;⑥打开止水夹;⑦缓慢加入稀硫酸至不再产生气体为止;⑧缓慢鼓入空气数分钟.
Ⅰ.正确的操作顺序是(填序号):
③―→__________―→⑥―→________―→⑤―→________―→⑦―→________―→④.
Ⅱ.若去掉装置A,测定结果________;若去掉装置B,测定结果________(填“偏大”、“偏小”或“无影响”).
求详解 舍予尔芬1年前1
舍予尔芬1年前1 -
 woainipt 共回答了25个问题
woainipt 共回答了25个问题 |采纳率88%正确的操作顺序是3,2,6,8,5,1,7,6,4检验装置的气密性后装样品没什么好说的.然后打开止水夹缓慢鼓入空气数分钟,使内部的气体组成相同.再关闭止水夹装干燥管.开启反应,反应完后打开止水夹,鼓入空气数分钟将装置里的CO2...1年前查看全部
- 金属材料是工农业生产和人们生活离不开的材料之一,人类每年要从自然界获取大量的金属,根据你对金属的认识,回答下列问题.
金属材料是工农业生产和人们生活离不开的材料之一,人类每年要从自然界获取大量的金属,根据你对金属的认识,回答下列问题.
(1)炼铁厂以赤铁矿石为原料炼制生铁的原理为 (用化学方程式表示).
(2)在农业上用硫酸铜溶液和石灰乳配制农药波尔多液,不能使用铁制容器的原因是 (用化学方程式表示),该反应所属的基本反应类型为 .
(3)为了防止自行车锈蚀,人们常采用在支架时尚喷漆,链条上涂油,车圈上镀其他金属等覆盖保护膜的方法.这些方法都能防止铁锈蚀的共同原理是 . 白龙马脖铃儿急1年前0
白龙马脖铃儿急1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 化学与工农业生产和人类生活密切相关。下列说法中正确的是 A.铜矿石在细菌作用下可直接转化为单质铜,这个过程叫生物炼铜 B
化学与工农业生产和人类生活密切相关。下列说法中正确的是
A.铜矿石在细菌作用下可直接转化为单质铜,这个过程叫生物炼铜 B.用纯碱制玻璃、用铁矿石炼铁、用氨制碳酸铵都会产生温室气体 C.海轮外壳上镶入锌块,可减缓船体的腐蚀,该方法叫牺牲阳极的阴极保护法 D.酸雨就是pH <7的雨水,主要是由大气中的SO 2 、NO 2 等造成的  adidass1年前1
adidass1年前1 -
 ccyy7923 共回答了20个问题
ccyy7923 共回答了20个问题 |采纳率90%C
A.生物炼铜利用某些具有特殊本领的细菌帮助我们解决这个问题。这些被称为“吃岩石的细菌”能耐受铜盐的毒性,并能用空气中的氧气氧化硫化铜矿石,把不溶性的硫化铜转化为可溶性的铜盐,使铜的冶炼变得非常简单。铜矿石在细菌作用下可直接转化为单质铜这种说法错误;
B.用纯碱制玻璃、用铁矿石炼铁、都会产生温室气体CO 2 ,用氨制碳酸铵,是氨吸收CO 2 ,不产生温室气体,B错误;
C.海轮外壳上镶入锌块,可减缓船体的腐蚀,该方法叫牺牲阳极的阴极保护法。正确;
D.酸雨就是pH <5.6的雨水,主要是由大气中的SO 2 、NO 2 等造成的,通常由于雨水中溶解了CO 2 ,都显酸性pH <7,所以并不是所有pH <7的都是酸雨。D错误。1年前查看全部
- (2011•济南)在现代生活和工农业生产中,经常会见到各种各样的测量工具或仪表.许多测量工具或仪表的刻度盘上都标有一个或
 (2011•济南)在现代生活和工农业生产中,经常会见到各种各样的测量工具或仪表.许多测量工具或仪表的刻度盘上都标有一个或几个字母,通过这些字母我们可以判断出该测量工具或仪表所测量的物理量及其单位.我们使用过的刻度尺和电流表、电压表都是如此.如图所示是小明同学在实验室见到的某种仪表的刻度盘,据此我们可以判断出:这种仪表是用来测量______(填写物理量名称)的,测量结果的单位名称是______.
(2011•济南)在现代生活和工农业生产中,经常会见到各种各样的测量工具或仪表.许多测量工具或仪表的刻度盘上都标有一个或几个字母,通过这些字母我们可以判断出该测量工具或仪表所测量的物理量及其单位.我们使用过的刻度尺和电流表、电压表都是如此.如图所示是小明同学在实验室见到的某种仪表的刻度盘,据此我们可以判断出:这种仪表是用来测量______(填写物理量名称)的,测量结果的单位名称是______.  声色犬马1年前1
声色犬马1年前1 -
 amei135 共回答了20个问题
amei135 共回答了20个问题 |采纳率95%由图示可知:这种仪表测量结果的单位符号是Ω,它是电阻的单位:欧姆,因此该仪器是用来测量电阻的.
故答案为:电阻;欧姆.1年前查看全部
- 水是一种重要的自然资源,与人类和生物生存、工农业生产等息息相关,下列有关水的说法中正确的是( )
水是一种重要的自然资源,与人类和生物生存、工农业生产等息息相关,下列有关水的说法中正确的是( )
A. 在淡水资源缺乏的海岛上,可考虑用蒸馏法从海水中提取淡水
B. 白天,植物吸收大量的水,主要用来满足蒸腾作用的需要
C. 防治水污染是保护水资源的重要措施
D. 地球上有的是水,根本不会缺水 tonylx1年前1
tonylx1年前1 -
 sgzjj1600 共回答了29个问题
sgzjj1600 共回答了29个问题 |采纳率93.1%解题思路:水资源是经人类控制并可直接利用的地表水和地下水的总称,是发展国民经济不可缺少的重要自然资源.地球上水的总量不会减少,但这些水能否被人类控制和利用才是它是否能称之为水资源的标准.A、蒸馏法可以从海水中提取淡水,是可行的,符合题意;
B、植物吸收大量的水,来满足蒸腾作用的需要,是符合植物生长特点的,符合题意;
C、水资源如果遭到污染将无法被人类利用,因此要防止水的污染,符合题意;
D、水资源并非指水的总量,而是指能被人类所利用的水,因此,不合题意.
故选ABC.点评:
本题考点: 能源的利用和对环境的危害.
考点点评: 水资源和水是两个不同的概念,我们应该从本质上去理解它,并了解一些如何保护和合理利用水资源的方法.1年前查看全部
- 下列有关美国工农业生产的叙述正确的是( )
下列有关美国工农业生产的叙述正确的是( )
A.美国的传统工业近年来发展较快
B.美国许多农产品的生产量和出口量居世界前列
C.棉花带主要分布在西部山区
D.美国大量出口咖啡、可可等热带经济作物 fangqisp1年前1
fangqisp1年前1 -
 lws6505 共回答了12个问题
lws6505 共回答了12个问题 |采纳率91.7%解题思路:美国农业十分依赖于国际市场,经常面临农产品过剩的问题.过去由于大量使用化肥、农药以及滥垦土地,造成环境污染和生态破坏,美国曾多次发生“黑色风暴”灾难.目前,许多农场实行轮作制度和免耕法,以保护耕地.美国是高度发达的资本主义国家.第二次世界大战以后,它的工农业总产值一直居世界首位.20世纪80年代以来,美国传统工业面临新兴工业国家的激烈竞争,呈衰落状态,被称为“夕阳工业”;自20世纪90年代以来,美国以高新技术为核心的新兴工业则呈现蓬勃向上的发展趋势;美国是世界上的农业大国.它生产的小麦、大豆、玉米、乳肉等都居世界前列,美国是世界上出口粮食最多的国家,但咖啡、可可、天然橡胶等热带农产品需要大量进口;美国的农业地区专门化是指每个地区根据自然条件和经济条件,重点发展一种或几种农产品的专门化生产,棉花带分布在美国的东南部.
故选:B.点评:
本题考点: 美国的工农业生产及分布.
考点点评: 考查美国农业的特点.1年前查看全部
- 人类的日常生活和工农业生产都离不开水.请回答下列与水有关的问题:
人类的日常生活和工农业生产都离不开水.请回答下列与水有关的问题:
(1)硬水会给生产和生活带来许多不便,检验生活用水是否为硬水的物质是______,生活中有些硬水可用______的方法降低它的硬度;
(2)农业和园林浇灌植物时,将大水漫灌改为喷灌、滴灌的目的是______. xu_39800331年前1
xu_39800331年前1 -
 飞天猪娃 共回答了18个问题
飞天猪娃 共回答了18个问题 |采纳率83.3%解题思路:根据已有的知识进行分析,硬水就是含有较多的可溶性钙镁化合物的水,检验是否为硬水可以使用肥皂水,硬水软化就是减少水中的钙镁离子的含量,大水漫灌改为喷灌、滴灌能起到节约用水的作用.(1)检验生活用水是否为硬水的物质是肥皂水,肥皂水与硬水混合产生大量的浮渣,与软水混合产生泡沫,硬水软化就是减少水中的钙镁离子的含量,可溶性钙镁化合物受热易转化成不溶性钙镁化合物,故可以采用加热煮沸的方法降低水的硬度,故填:肥皂水,加热煮沸;
(2)大水漫灌改为喷灌、滴灌能起到节约用水的作用,故填:节约用水.点评:
本题考点: 硬水与软水;保护水资源和节约用水.
考点点评: 本题考查了硬水的检验和软化以及节约用水的知识,完成此题,可以依据已有的知识进行.1年前查看全部
- (2014•闸北区一模)水是生命之源,人类的日常生活与工农业生产都离不开水.
 (2014•闸北区一模)水是生命之源,人类的日常生活与工农业生产都离不开水.
(2014•闸北区一模)水是生命之源,人类的日常生活与工农业生产都离不开水.
①自然界大部分水不能直接使用,洪涝地区的灾民将河水转化为可饮用水的步骤有:a.用明矾进行化学沉降;b.用漂白粉消毒杀菌;c.过滤;d.加热煮沸.上述处理过程中有关步骤合理的顺序是______.
②用如图所示的简易电解水装置,进行电解水实验(注:该装置气密性良好,且反应一段时间后停止通电,A、B管内液面均高于图中D线).请根据要求回答问题:闭合开关后观察到A、B管内的气体的体积比是______,若检验A管内生成的气体应该用______;C管中的现象是______,电解水实验证明了水是由______组成. woyaoayan1年前1
woyaoayan1年前1 -
 风土不人情 共回答了26个问题
风土不人情 共回答了26个问题 |采纳率88.5%解题思路:①净化水时,根据净化的原理按照净水程度由低到高的顺序进行;
②根据电解水实验的现象、结论分析回答.①净化水时按照净水程度由低到高的顺序进行,故其合理的顺序为acbd.
②由电解水的装置可知,A试管收集的气体是电源的正极产生的气体较少是氧气,B试管收集的气体是电源的负极产生的气体较多是氢气,二者的体积比是1:2;由于A试管产生的氧气能支持燃烧.所以,若检验A管内生成的气体应该用带火星的木条;在电解水的过程中,不打开管AB的弹簧夹时,产生的气体会将管AB中的液面下压,导致管C中的液面上升.电解水实验证明了水是由氢元素和氧元素组成.
故答为:①acbd;②1:2,带火星的木条,液面上升,氢元素和氧元素.点评:
本题考点: 水的净化;常见气体的检验与除杂方法;电解水实验;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查了净化水以及电解水的知识,难度不大,属于基础的知识.完成此题,可以依据已有的知识进行.1年前查看全部
- 人类的生活和工农业生产都离不开水.下图是自来水厂净水过程示意图.
人类的生活和工农业生产都离不开水.下图是自来水厂净水过程示意图.

请根据图示回答下列问题:
(1)上图吸附池内的活性炭起______作用,在乡村没有活性炭,常加入______来净水;
(2)家庭生活中可以用______检验某水样是硬水还是软水;
(3)若该地区源水中含有较多的MgCl2,请写出在源水处理流程中加入CaO时有关化学方程式①______;
②______. 微笑的太阳风1年前1
微笑的太阳风1年前1 -
 joechiu 共回答了12个问题
joechiu 共回答了12个问题 |采纳率83.3%解题思路:本题结合自来水生产的图示来综合考查学生对净水方法的应用,要求学生理解净水的各方法异同,同时还涉及硬水软化及化学方程式的书写.(1)活性炭具有很强的吸附能力,因此在吸附池内的活性炭主要是起到吸附作用,在农村没有活性炭,也可以用木炭或明矾代替,它们也具有吸附性;
(2)鉴别硬水和软水,最简便的方法是用肥皂水,有大量浮渣的是硬水,没有或很少的是软水;
(3)生石灰是氧化钙,与水反应生成氢氧化钙,氢氧化钙与水中的氯化镁反应生成氯化钙和氢氧化镁,化学方程式为CaO+H2O═Ca(OH)2、Ca(OH)2+MgCl2=CaCl2+Mg(OH)2↓.
故答案为:(1)吸附、明矾或木炭;
(2)肥皂水;
(3)CaO+H2O═Ca(OH)2、Ca(OH)2+MgCl2=CaCl2+Mg(OH)2↓.点评:
本题考点: 水的净化;水的性质和应用;硬水与软水;碱的化学性质;盐的化学性质;碳单质的物理性质及用途;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题较为简单,但书写化学方程式具有一定难度,要注意配平和沉淀符号.1年前查看全部
- (18分)铵盐在工农业生产中有着重要的用途,请根据要求完成下列各题。
(18分)铵盐在工农业生产中有着重要的用途,请根据要求完成下列各题。
Ⅰ.某化学兴趣小组欲从下列装置中选取必要的装置制取(NH 4 ) 2 SO 4 溶液。
(1)仪器连接的顺序(用接口序号字母表示)是:a
(2)试从电离平衡角度分析该实验装置A中能产生氨气的原因:
。
(3)将装置C中两种液体分离开的操作名称是 。
(4)(NH 4 ) 2 SO 4 “低毒,有刺激性,有吸湿性、吸湿后固结成块”。储存应注意 。
Ⅱ.为提高氯化铵的经济价值,我国化学家设计了利用氢氧化镁热分解氯化铵制氨气并得到碱式氯化镁[Mg(OH)Cl]的工艺。某同学根据该原理设计的实验装置如图: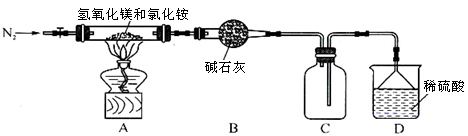
请回答下列问题:
(1)装置A中发生反应生成碱式氯化镁的化学方程式为 。
(2)反应过程中持续通入N 2 的作用有两点:一是使反应产生的氨气完全导出并被稀硫酸充分吸收,
二是 。
(3)由MgCl 2 溶液蒸发得到MgCl 2 ·6H 2 O晶体,蒸发的目的是_________。
a.得到热饱和溶液b.析出晶体
(4)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。
①若要验证所得无水MgCl 2 中不含NaCl,最简单的操作方法是:
。
②由MgCl 2 ·6H 2 O制备无水MgCl 2 的操作在 氛围中进行,若在空气中加热,则会生成Mg(OH)Cl。 飞翔在蓝天中1年前1
飞翔在蓝天中1年前1 -
 skywalkye 共回答了25个问题
skywalkye 共回答了25个问题 |采纳率96%1年前查看全部
- 高中化学氨气是一种重要工业原料,在工农业生产中具有重要的应用. (1)已知:N2(g)+O2(g)===2NO(g);Δ
高中化学
氨气是一种重要工业原料,在工农业生产中具有重要的应用. (1)已知:N2(g)+O2(g)===2NO(g);ΔH=+180.5 kJ·mol-1 4NH3(g)+5O2(g)===4NO(g)+6H2O(g);ΔH=-905 kJ·mol-1 bm 2H2(g)+O2(g)===2H2O(g);ΔH=-483.6 kJ·mol-1 则N2(g)+3H2(g)===2NH3(g);ΔH= . (2)工业合成氨气的反应为N2(g)+3H2(g) 2NH3(g).在一定温度下,将一定量的N2和H2通入 到初始体积为1 L的密闭容器中达到平衡后,单独改变下列条件,能使平衡向正反应方向移动且 平衡常数不变的是 . ①增大压强 ②增大反应物的浓度 ③使用催化剂 ④降低温度 (3)①常温下0.1 mol/L氨水中电离出的c(OH- ) 10-1 mol/L(填写“>”、“<”或“=”); ②将相同体积、pH之和为14的氨水和盐酸混合后,溶液中离子浓度由大到小的顺序为 . (4)用氨水和40 mL 0.5 mol/L硫酸铝溶液来制备一定量的氢氧化铝,该反应的离子方程式 为 .某同学改用2 mol/L的氢氧化钠溶液代替氨水来制备,结果只得到了0.78克的沉淀,其加入的氢氧化钠溶液的体积可能为__________求高人详解(4)答案为15ml或75ml不明白75ml谢
 银座1年前1
银座1年前1 -
 大胖子_ss 共回答了23个问题
大胖子_ss 共回答了23个问题 |采纳率87%最后一问两种情况 第一种情况是加入的碱少量 氢氧根直接与铝离子生成沉淀 第二种情况就是碱过量 先全部生成氢氧化铝 再生成偏铝酸钠 剩余少部分未反应的氢氧化铝1年前查看全部
- 人类的生活和工农业生产都离不开水.如图是自来水厂净水过程示意图.自来水厂生产自来水时,使用的净水方法有 A.沉
人类的生活和工农业生产都离不开水.如图是自来水厂净水过程示意图.自来水厂生产自来水时,使用的净水方法有 A.沉淀B.过滤C.煮沸 D.蒸馏 E.吸附 请根据图1示回答下列问题:
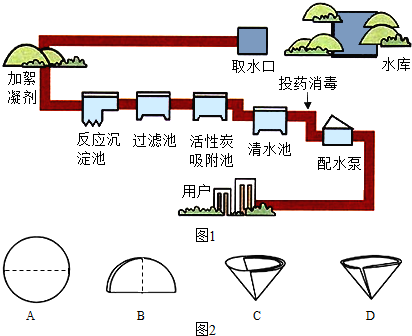
(1)取水后加入絮凝剂(明矾)的作用是______
(2)自来水厂常用二氧化氯进行投药消毒,二氧化氯的化学式为______,其作用是______
(3)实验室进行过滤操作时,玻璃仪器除了烧杯、漏斗外还需要______,其作用是______操作中需要将圆形滤纸折叠处理,如图2所示中不该出现的情形是______(填序号)
(4)进入用户的水______(填“是”或“不是”)纯水,理由是______
(5)生活中采用______的方法将硬水软化.
(6)生活中节约用水的方法①______②______. nbdbg1年前1
nbdbg1年前1 -
 武恒海 共回答了20个问题
武恒海 共回答了20个问题 |采纳率80%解题思路:(1)根据明矾溶入水生成物的性质分析回答;
(2)根据二氧化氯的名称、作用分析回答;
(3)根据过滤的操作、仪器的用途分析回答;
(4)根据进入用户的水的组成分析回答;
(5)根据生活中硬水软化的方法回答;
(6)根据生活中节约用水的方法分析回答.(1)由于明矾溶入水生成物具有吸附性,取水后加入絮凝剂(明矾)的作用是:吸附不溶于水的杂质,加速不溶物的沉降;
(2)自来水厂常用二氧化氯进行投药消毒,二氧化氯的化学式为:ClO2,其作用是:杀菌消毒;
(3)实验室进行过滤操作时,玻璃仪器除了烧杯、漏斗外还需要玻璃棒,其作用是引流,操作中需要将圆形滤纸折叠处理,在D中,接口处出现缝隙,液体会直接的进入下面的烧杯,是不该出现的情形;
(4)进入用户的水不是纯水,理由是含有可溶于水的物质;
(5)生活中采用煮沸的方法将硬水软化.
(6)生活中节约用水的方法由很多,例如:①洗菜水浇花,②及时关闭水龙头.
故答为:(1)吸附不溶于水的杂质,加速不溶物的沉降;(2)ClO2,杀菌消毒;(3)玻璃棒,引流,D;(4)不是,含有可溶于水的物质;(5)煮沸;(6)①洗菜水交换,②及时关闭水龙头.点评:
本题考点: 自来水的生产过程与净化方法;过滤的原理、方法及其应用;硬水与软水;化学式的书写及意义;保护水资源和节约用水.
考点点评: 本题考查了净水的知识,完成此题,可以依据已有的知识进行解答,属于基础知识,难度中等.能够把图中信息和化学知识有机的结合起来.1年前查看全部
大家在问
- 1r(a1,a2...as)=r(a1,a2...as,as+1)=r.且ai1,ai2,air是a1,a2...as的极
- 2英语翻译-1)pei 2)pi:z 3)pen 4)pcul 5)pul 6)pus 7)bei 8)bi:z 9)be
- 3实数列a 0 ,a 1 ,a 2 ,a 3 ,...由下述等式定义:
- 4i'll跟ill一个意思吗?我看电影里有个是这样的 i'll kill you 两个词有区别吗?
- 5一质量为m的质点绕着一固定转轴转动,当其转动半径变小时,它的转动角速度将变(大/小);
- 6两个有理数相除还是有理数吗?
- 7山谷中的谜底 阅读1983年的冬天,大雪纷飞,有两个旅行者来到了这个山谷.他们支起帐篷,望着满天飞舞的大雪,突然惊奇地发
- 8Which sentence below is right?Five kilometres is a long walk
- 9诗人王冕通过“----------,---------"来寄予他鄙视流俗、贞节自守的高尚情操,这种手法
- 10如何理解世界的物质性和人的实践性活动的关系
- 11用图所示的实验装置测滑轮组的机械效率,实验中得到的一组数据列在表中,根据这组数据可计算出:弹簧测力计移动的距离是____
- 12let me try your
- 13弓形弦AB=2cm,高为根号3cm.求AB的度数及弓形弧ACB的面积
- 14四水三氯化铟溶解于强酸和强碱么?什么溶剂可以同时溶解二氧化碲和四水三氯化铟?
- 15对某人来说用英语怎么表达


