氨碱法制备纯碱的工艺流程
 和风一起飞2022-10-04 11:39:542条回答
和风一起飞2022-10-04 11:39:542条回答
已提交,审核后显示!提交回复
共2条回复
 yuanzi5811 共回答了23个问题
yuanzi5811 共回答了23个问题 |采纳率95.7%- 精制盐(NaCl)制成饱和溶液,
通入氨气达到饱和
再通入二氧化碳
继续同时通入NH3和CO2
析出大量沉淀后过滤,得到NaHCO3
灼烧NaHCO3得到Na2CO3 - 1年前
 爱上你我错了 共回答了7个问题
爱上你我错了 共回答了7个问题 |采纳率- 根据题中所给生成物进行分析,要制备饱和氨水肯定是将氨水通入食盐水中,由饱和的氨水食盐溶液制备碳酸氢钠,根据物质的性质和元素守恒知应通入二氧化碳气体;碳酸氢钠受热易分解变为碳酸钠.
故答案为:①NH3 ②CO2 ③加热 - 1年前
相关推荐
- 某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上标明:碳酸钠≥96%.为测定该产品中含碳酸钠的质
某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上标明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验;取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,充分反应后,实验数据记录如下:
请你据此分析计算:所加盐酸的次数 第一次 第二次 第三次 第四次 烧杯及所盛物质的总质量/g 181.2 204.4 228.6 253.6 
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是______g.
(2)该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
(3)根据实验数据,在下边的坐标纸上绘制出所加稀盐酸的质量与生成的二氧化碳的质量关系的曲线.(不要求写出计算过程,只画出曲线即可)
 basgjggy1年前1
basgjggy1年前1 -
 zhouchangda 共回答了14个问题
zhouchangda 共回答了14个问题 |采纳率100%解题思路:(1)根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.故第一次加入稀盐酸充分反应后,生成二氧化碳的质量=反应前烧杯及所盛物质的质量总和-反应后烧杯及所盛物质的质量总和;
(2)由图表数据可知,前二次反应后,每次生成气体的质量都是1.8g,第四次反应没有气体生成,故可判断第三次反应已完全.故生成气体的质量为158g+75g-228.6g=4.4g.根据碳酸钠与稀盐酸反应的化学方程式和生成的气体质量,列出比例式,即可计算出参与反应的Na2CO3的质量,然后根据溶质质量分数=[溶质质量/溶液质量]×100%计算即可;(1)第一次的结果中,二氧化碳的质量为158.0g+100g÷4-181.2g=1.8g;故答案为:1.8g.
(2)前二次反应后,每次生成气体的质量都是1.8g,第四次反应没有气体生成,故可判断第三次反应已完全.故生成气体的质量为158g+75g-228.6g=4.4g
设参与反应的Na2CO3的质量为x,
Na2CO3+2HCl=2NaCl+CO2↑+H2O
106 44
x 4.4g
∴[106/44=
x
4.4g],
解之得:x=10.6g,
产品中碳酸钠的质量分数为:[10.6g/11g]×100%≈96.4%≥96%;
故该产品中碳酸钠的质量分数合格.
(3)根据前两步可以计算出当碳酸钠存在的情况下,每25g盐酸对应的二氧化碳质量为1.8g,当生成4.4g二氧化碳时,消耗的盐酸溶液的质量为61g.之后再加盐酸无气体生成.而开始时,盐酸为零,二氧化碳也为零.所以得图: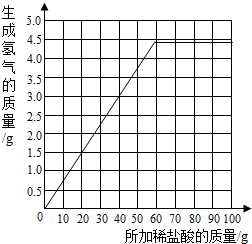
点评:
本题考点: 根据化学反应方程式的计算;实验数据处理或者误差分析的探究;质量守恒定律及其应用.
考点点评: 本题主要考查学生运用化学方程式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.1年前查看全部
- 某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%。为了测定该产品中含碳酸钠的
某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%。为了测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.0克纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0克,再把100克稀盐酸平均分成四份依次加入样品中,每次均充分反应。实验数据记录如下: 
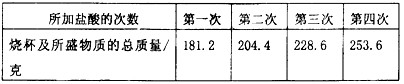
请你据此分析计算:
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是____________克。
(2)该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
(3)根据实验数据,在下边的坐标纸上绘制出所加稀盐酸质量与生成气体质量关系的曲线。(不要求写出计算过程,只画出曲线即可)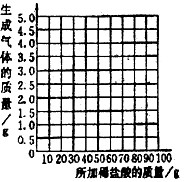
 jjc4111年前1
jjc4111年前1 -
 支离破碎YOO 共回答了18个问题
支离破碎YOO 共回答了18个问题 |采纳率94.4%(1)1.8g
(2)合格 (步骤略)
(3)“略”1年前查看全部
- (2014•南昌模拟)纯碱是一种重要的化工原料.制碱工业主要有“氨碱法”(索尔维法)和“联合制碱法”(侯氏制碱法)两种工
(2014•南昌模拟)纯碱是一种重要的化工原料.制碱工业主要有“氨碱法”(索尔维法)和“联合制碱法”(侯氏制碱法)两种工艺.请按要求回答问题:
(1)CO2是制碱工业的重要原料,“联合制碱法”中CO2的来源于______,“氨碱法”中CO2来源于______.
(2)氨碱法的原子利用率(原子利用率=期望产物的总质量与生成物的总质量之比)[106/275][106/275].
(3)写出“联合制碱法”有关反应的化学方程式:NH3+H2O+CO2+NaCl(饱和)=NaHCO3↓+NH4Cl、2NaHCO3
Na2CO3+CO2↑+H2O△ .NH3+H2O+CO2+NaCl(饱和)=NaHCO3↓+NH4Cl、2NaHCO3.
Na2CO3+CO2↑+H2O△ . fjxmwxh1年前1
fjxmwxh1年前1 -
 sharonliu99 共回答了15个问题
sharonliu99 共回答了15个问题 |采纳率93.3%(1)CO2是制碱工业的重要原料,氨碱法中CO2的来源于合成氨厂用水煤气制取氢气时的废气,联合制碱法中CO2来源于高温煅烧石灰石的产物,
故答案为:合成氨厂;煅烧石灰石;
(2)氨碱法的原理为:NH3+CO2+H2O+NaCl(饱和)=NaHCO3↓+NH4Cl,2NaHCO3
△
.
Na2CO3+CO2↑+H2O,原子利用率=
m(Na2CO3)
m(Na2CO3)+2m(NH4Cl)+m(CO2)+m(H2O)=[106/275],
故答案为:[106/275];
(3)联合制碱法是在氨的饱和NaCl溶液中二氧化碳气体,反应生成碳酸氢钠,解热碳酸氢钠即可制备碳酸钠,反应的有关方程式为NH3+CO2+H2O+NaCl(饱和)=NaHCO3↓+NH4Cl、2NaHCO3
△
.
Na2CO3+CO2↑+H2O,
故答案为:NH3+CO2+H2O+NaCl(饱和)=NaHCO3↓+NH4Cl、2NaHCO3
△
.
Na2CO3+CO2↑+H2O.1年前查看全部
- [选修一化学与技术]联碱法(候氏制碱法)和氨碱法的生产流程简要表示如下图:
[选修一化学与技术]联碱法(候氏制碱法)和氨碱法的生产流程简要表示如下图:

(1)沉淀池中发生反应的化学方程式为______;
(2)X是______,Y是______ (填化学式);
(3)Z中除了溶解的氨气、食盐外,其它溶质还有______;排出液中的溶质除了氢氧化钙外,还有______;
(4)从理论上分析,在氨碱法生产过程中______ (填“需要”、“不需要”)补充氨气,从原料到产品,氨碱法总反应过程用化学方程式表示,可写为______;
(5)根据联碱法中从母液中提取氯化铵晶体的过程推测,所得结论正确是______;
a.常温时氯化铵的溶解度比氯化钠小
b.通入氨气目的是使氯化铵更多析出
c.加入食盐细粉目的是提高Na+的浓度,促进碳酸氢钠结晶析出
(6)联碱法中,每当通入NH3 44.8L(已折合成标准状况下)时可以得到纯碱100.0g则NH3的利用率为______.相比于氨碱法,指出联碱法的一项优点______• zzm09081年前1
zzm09081年前1 -
 熊熊狗 共回答了20个问题
熊熊狗 共回答了20个问题 |采纳率100%解题思路:(1)依据生产流程联碱法和氨碱法生产流程中沉淀池中发生的反应是氨气、二氧化碳、水、氯化钠反应生成碳酸氢钠晶体和氯化铵;
(2)联碱法生产流程图中分析循环Ⅱ中是碳酸氢钠分解生成的二氧化碳气体;氨碱法的生产流程中循环Ⅰ是氧化钙和水反应生成氢氧化钙与铵盐反应生成的氨气;
(3)联碱法母液主要是氯化铵、碳酸钠、碳酸氢钠、氯化钠;Z中除了溶解的氨气、食盐外,其它溶质还有氯化铵、碳酸钠;氨碱法排出液中的溶质除了氢氧化钙外,还有氢氧化钙和氯化铵反应生成的氯化钙,氯化钠;
(4)氨碱法生产过程中,母液中加入氧化钙反应生成氢氧化钙会和铵盐生成氨气,反应过程中氨气转化为铵盐,铵盐转化为氨气,氨气循环使用,不需要补充氨气;
NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl;CaCO3═CaO+CO2↑;CaO+H2O═Ca(OH)2;Ca(OH)2+2NH4Cl═CaCl2+2NH3↑+2H2O;2NaHCO3═Na2CO3+H2O+CO2↑;
合并得到总化学方程式为:CaCO3+2NaCl═Na2CO3+CaCl2;
(5)向母液中通氨气作用有增大NH4+的浓度,使NH4Cl更多地析出和使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度;加入食盐细粉目的是提高Cl-的浓度,使氯化氨析出;
(6)依据联碱法反应的化学方程式计算,根据反应生成碳酸钠的质量计算实际消耗氨气的物质的量,得到氨气的利用率;综合分析两个过程的流程图和生成产物,及过程中循环利用的特征分析判断.(1)依据流程图分析可知,生产流程联碱法和氨碱法生产流程中沉淀池中发生的反应是氨气、二氧化碳、水、氯化钠反应生成碳酸氢钠晶体和氯化铵,所以反应的化学方程式为:NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl,故答案为:NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl;
(2)联碱法生产流程图中分析循环Ⅱ中是碳酸氢钠分解生成的二氧化碳气体;氨碱法的生产流程中循环Ⅰ是氧化钙和水反应生成氢氧化钙,氢氧化钙与铵盐反应生成的氨气可以循环使用,故答案为:CO2;NH3;
(3)依据两个过程中的物质发生的反应分析,联碱法母液主要是氯化铵、碳酸钠、碳酸氢钠、氯化钠;Z中除了溶解的氨气、食盐外,其它溶质还有氯化铵、碳酸钠;氨碱法排出液中的溶质除了氢氧化钙外,还有氢氧化钙和氯化铵反应生成的氯化钙,氯化钠,故答案为:Na2CO3、NH4Cl;CaCl2、NaCl;
(4)从理论上分析,氨碱法生产过程中,母液中加入氧化钙反应生成氢氧化钙会和铵盐生成氨气,反应过程中氨气转化为铵盐,铵盐转化为氨气,氨气循环使用,不需要补充氨气;
NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl;CaCO3═CaO+CO2↑;CaO+H2O═Ca(OH)2;Ca(OH)2+2NH4Cl═CaCl2+2NH3↑+2H2O;2NaHCO3═Na2CO3+H2O+CO2↑合并得到总化学方程式为:CaCO3+2NaCl═Na2CO3+CaCl2,故答案为:不需要;CaCO3+2NaCl═Na2CO3+CaCl2;
(5)联碱法中从母液中提取氯化铵晶体的过程中;
a、温时氯化铵的溶解度比氯化钠大,故a错误;
b、通氨气作用有增大NH4+的浓度,使NH4Cl更多地析出和使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度,故b正确;
c、加入食盐细粉目的是提高Cl-的浓度,促进氯化铵结晶析出,故c错误;
故答案为:b;
(6)联碱法中发生的反应为:NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl;2NaHCO3═Na2CO3+H2O+CO2↑;每当通入NH3 44.8L(已折合成标准状况下)物质的量为2mol;生产过程中得到纯碱100.0g,物质的量为[100g/106g/mol]=[50/53]mol;需要氨气的物质的量为[50/53×2=
100
53]mol;则NH3的利用率=
100
53mol
2mol×100%=94.3%;
联合制碱法与氨碱法比较,其最大的优点是使食盐的利用率提高到96%以上,应用同量的食盐比氨碱法生产更多的纯碱.另外它综合利用了氨厂的二氧化碳和碱厂的氯离子,同时,生产出两种可贵的产品--纯碱和氯化铵.将氨厂的废气二氧化碳,转变为碱厂的主要原料来制取纯碱,这样就节省了碱厂里用于制取二氧化碳的庞大的石灰窑;将碱厂的无用的成分氯离子(Cl-)来代替价格较高的硫酸固定氨厂里的氨,制取氮肥氯化铵.从而不再生成没有多大用处,又难于处理的氯化钙,减少了对环境的污染,并且大大降低了纯碱和氮肥的成本,充分体现了大规模联合生产的优越性,
故答案为:94.3%;不产生无用的CaCl2,提高了食盐的转化率.点评:
本题考点: 纯碱工业(侯氏制碱法);工业合成氨.
考点点评: 本题考查了联碱法和氨碱法生产流程的原理比较和物质分析判断,纯碱制备的条件应用和服产物的提纯析出,反应过程中反应的原理分析和物质来源是解题的关键,题目难度中等.1年前查看全部
- 某化工厂用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.
某化工厂用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.
为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:第一次加入稀盐酸充分反应后,生成二氧化碳的质量是______g.要说明理由,或写出过程. 呐呐大人1年前1
呐呐大人1年前1 -
 像小狗一样爱你 共回答了13个问题
像小狗一样爱你 共回答了13个问题 |采纳率84.6%分析:(1)根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.故第一次加入稀盐酸充分反应后,生成二氧化碳的质量=反应前烧杯及所盛物质的质量总和-反应后烧杯及所盛物质的质量总和;
158.0g+100g÷4-181.2g=1.8g;故答案为:1.8g.
如果满意,请采纳!
您的采纳使我继续努力的动力!1年前查看全部
- 某化工集团用氨碱法生产的纯碱中含有少量氯化钠杂质,为了测定该产品中碳酸钠的纯度,某化学研究性学习小组设计有关方案进行如图
 某化工集团用氨碱法生产的纯碱中含有少量氯化钠杂质,为了测定该产品中碳酸钠的纯度,某化学研究性学习小组设计有关方案进行如图实验:
某化工集团用氨碱法生产的纯碱中含有少量氯化钠杂质,为了测定该产品中碳酸钠的纯度,某化学研究性学习小组设计有关方案进行如图实验:
(1)其中一个小组设计如图甲所示实验装置,Y型管中一侧管中加入碳酸钠样品,另一侧加入过量稀硫酸,将稀硫酸加入到纯碱样品使之反应的操作为______.此时反应的离子方程式______.待反应结束后,冷却,再次调节量气管和水准管中液面相平,读取气体体积为aL(已换算成标准状况),则所取样品中含碳酸钠的质量为[106a/22.4][106a/22.4]g.
(2)另一个小组设计如图乙所示装置,测的反应前后的有关质量如表,取16.50g纯碱样品放入烧杯中,将烧杯放在电子天平上,再把150.00g稀硫酸(足量)加入样品中(假设装置中CO2无残留).观察读数变化如表所示:
请你据此分析计算:时间/s 0 5 10 15 读数/g 215.20 211.40 208.60 208.60
①实验中产生的CO2气体质量为______;
②该产品中碳酸钠的质量分数(结果精确到小数点后一位)______.小组中有一个成员提出图乙装置中有一个缺陷,不管操作如何精确,碳酸钠的含量总是偏大,原因是______.
③第三小组设计的不同前两种的方法测定碳酸钠的质量分数,可能的方法是______(只要出试剂和方法即可)例如第一种方法可以写成:取一定量的样品,加入足量的稀硫酸,测量产生气体的体积. 三宅又一生1年前1
三宅又一生1年前1 -
 xieandyang 共回答了19个问题
xieandyang 共回答了19个问题 |采纳率78.9%解题思路:(1)Y型管倾斜,使液体倒入碳酸钠样品中;碳酸钠和盐酸反应生成氯化钠、二氧化碳和水;收集的aL气体为二氧化碳的体积,根据反应方程式计算碳酸钠的质量;
(2)①依据装置图分析反应前后质量减小为二氧化碳的质量;
②依据化学方程式可知生成二氧化碳物质的量和碳酸钠物质的量相同,计算得到碳酸钠的质量分数;二氧化碳携带水蒸气逸出使质量减小的多;
③前两种方案是通过测定生成气体的体积或质量来计算碳酸钠的质量分数,也可通过生成碳酸盐沉淀或氯化银沉淀来测定.(1)甲所示装置,碳酸钠和稀硫酸分装在Y型玻璃管中,使碳酸钠样品与稀硫酸反应的操作为液体倒入固体中反应,将Y型管倾斜,使硫酸溶液流入到碳酸钠样品中,发生反应的化学方程式为:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑,离子方程式为:CO32-+2H+=H2O+CO2 ↑;
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑,
106g 22.4L
m aL
m=[106g×aL/22.4L]=[106a/22.4]g;
故答案为:将Y型管倾斜,使硫酸溶液流入到碳酸钠样品中;CO32-+2H+=H2O+CO2 ↑;[106a/22.4];
(2)①反应前后质量减小为二氧化碳的质量,215.20-208.60=6.60g;
②二氧化碳物质的量=碳酸钠物质的量=[6.60g/44g/mol]=0.15mol,碳酸钠的质量=0.15mol×106g/mol=15.9g,碳酸钠的质量分数为:[15.9g/16.5g]×100%=96.4%;
二氧化碳携带水蒸气逸出使质量减小的多,二氧化碳的质量增大,碳酸钠质量分数偏大,
③前两种方案是通过测定生成气体的体积或质量来计算碳酸钠的质量分数,也可通过生成碳酸盐沉淀或氯化银沉淀来测定,可设计为:取一定量的样品,加入足量的氯化钙溶液,过滤、洗涤、干燥,测量产生沉淀的质量.或者取一定量的样品,加入足量的硝酸银溶液,再加稀硝酸,过滤、洗涤、干燥,测得产生沉淀的质量,根据沉淀的质量计算碳酸钠或氯化钠的质量,进而计算碳酸钠的质量分数;
故答案为:6.6g;96.4%;逸出的二氧化碳中含有水蒸气;取一定量的样品,加入足量的氯化钙溶液,过滤、洗涤、干燥,测量产生沉淀的质量或者取一定量的样品,加入足量的硝酸银溶液,再加稀硝酸,过滤、洗涤、干燥,测得产生沉淀的质量.点评:
本题考点: 探究物质的组成或测量物质的含量.
考点点评: 本题考查了物质性质的实验探究分析判断,实验过程的数据处理方法,物质性质的分析应用是解题关键,题目难度中等.1年前查看全部
- 某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上标明:碳酸钠≥96%.为测定该
 jiangmyli1年前1
jiangmyli1年前1 -
 xrh8509 共回答了20个问题
xrh8509 共回答了20个问题 |采纳率80%由表格数据可知,第一次生成二氧化碳的质量为:158.0g+100g÷4-181.2g=1.8g充分反应后生成二氧化碳的质量为:158.0g+100g-253.6g=4.4g设样品中含有的碳酸钠的质量为XNa2CO3+2HCl=2NaCl+H2O+CO2↑106 ...1年前查看全部
- (2010•高淳县二模)某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上标明:碳酸钠≥96%.为
(2010•高淳县二模)某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上标明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验;取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,充分反应后,实验数据记录如下:
请你据此分析计算:所加盐酸的次数 第一次 第二次 第三次 第四次 烧杯及所盛物质的总质量/g 181.2 204.4 228.6 253.6
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是______g.
(2)该产品中碳酸钠的质量分数是______.(结果精确到0.1%) hjj991年前1
hjj991年前1 -
 rex_蔸蔸 共回答了17个问题
rex_蔸蔸 共回答了17个问题 |采纳率76.5%解题思路:分析表格中所给的实验数据,可知在反应的过程中,烧杯内的物质的总质量不断减少,所减少的质量为二氧化碳的质量.由二氧化碳的质量可以求出碳酸钠的质量分数.由表格数据可知,第一次生成二氧化碳的质量为:158.0g+100g÷4-181.2g=1.8g
充分反应后生成二氧化碳的质量为:158.0g+100g-253.6g=4.4g
设样品中含有的碳酸钠的质量为X
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
X 4.4g
[106/X=
44
4.4g]
X=10.6g
碳酸钠的质量分数为:[10.6g/11.0g]×100%=96.4%
故答案为:
(1)1.8
(2)96.4%点评:
本题考点: 实验探究物质的组成成分以及含量;质量守恒定律及其应用;根据化学反应方程式的计算.
考点点评: 在有表格的计算中,我们要根据表格中所给的数据来分析并得出我们所需要的物质的质量,然后再利用化学方程式进行计算.1年前查看全部
- 某化工厂用氨碱法生产的纯碱碳酸钠质量分数是多少
 爱在爱中CC1年前1
爱在爱中CC1年前1 -
 jannast 共回答了22个问题
jannast 共回答了22个问题 |采纳率90.9%其化学反应原理是:NaCl+NH3+H2O+CO2=NaHCO3↓+NH4Cl
将经过滤、洗涤得到的NaHCO3微小晶体,再加热煅烧制得纯碱产品.2NaHCO3=Na2CO3+H2O+CO2↑放出的二氧化碳气体可回收循环使用.1年前查看全部
- 根据氨碱法用食盐制纯碱的反应原理是:
根据氨碱法用食盐制纯碱的反应原理是:
(1)NaCl+NH 3 +CO 2 +H 2 O=NaHCO 3 +NH 4 Cl
(2)2NaHCO 3 Na 2 CO 3 +CO 2 ↑+H 2 O
Na 2 CO 3 +CO 2 ↑+H 2 O
下列对上述信息的有关理解中,错误的是( )A.用食盐制纯碱需要含碳、氧元素的物质 B.纯碱属于盐类物质 C.因生成气体,反应不遵循质量守恒定律 D.副产品氯化铵是一种氮肥  害虫吃猪肉1年前1
害虫吃猪肉1年前1 -
 liuzhen27 共回答了6个问题
liuzhen27 共回答了6个问题 |采纳率100%C
化学反应都遵循质量守恒定律,不受产物状态的影响。1年前查看全部
- 纯碱(Na2CO3)是一种重要的盐类物质,在化学工业中用途极广.工业上通常用氨碱法来生产.
纯碱(Na2CO3)是一种重要的盐类物质,在化学工业中用途极广.工业上通常用氨碱法来生产.
纯碱(Na2CO3)是一种重要的盐类物质,在化学工业中用途极广.工业上通常用氨碱法来生产.小红同学为探究纯碱的化学性质进行了猜想,并设计实验进行验证.请你帮助她将下列实验报告填写完整.
猜想x05实验操作x05实验现象x05结论(或化学方程式)
猜想一:Na2CO3溶液显碱性x05取少量Na2CO3溶液于试管中,滴入2-3滴酚酞试液,振荡x05
x05溶液显碱性
猜想二:能与酸反应x05取少量溶液于试管中,然后滴加稀盐酸x05有大量气泡产生x05化学方程式
猜想三:能与Ca(OH)2反应x05向盛有少量Na2CO3溶液于试管中,滴加澄清石灰水x05产生白色沉淀x05化学方程式
猜想四:能与BaCl2反应x05
x05产生白色沉淀x05Na2CO3+BaCl2=BaCO3↓+2NaCl 郁闷过后1年前1
郁闷过后1年前1 -
 soso59 共回答了19个问题
soso59 共回答了19个问题 |采纳率84.2%猜想1: 溶液呈红色
猜想2:Na2CO3 + 2HCl ====2NaCl + H2O + CO2(气体)
猜想3:Na2CO3 + Ca(OH)2 ====CaCO3(沉淀) + 2NaOH
猜想4: 向盛有少量Na2CO3溶液于试管中,滴加BaCl2溶液,结果产生白色沉淀
回答满意请采纳1年前查看全部
- (2012•宝坻区一模)纯碱在化学工业中用途极广.工业上通常用氨碱法来生产.小红同学为探究纯碱的化学性质进行了猜想,并设
(2012•宝坻区一模)纯碱在化学工业中用途极广.工业上通常用氨碱法来生产.小红同学为探究纯碱的化学性质进行了猜想,并设计实验进行验证.请你帮助她将下列实验报告填写完整.
猜想 实验操作 实验现象 结论(或化学方程式) 猜想一:Na2CO3溶液显碱性 取少量Na2CO3溶液于试管中,滴入2-3滴酚酞溶液,振荡 溶液变为红色 溶液显______性 猜想二:能与酸反应 取少量Na2CO3溶液于试管中,然后滴加稀盐酸 ______ 化学方程式
______猜想三:能与Ca(OH)2反应 取少量Na2CO3溶液于试管中,滴加澄清石灰水 产生
______化学方程式
______猜想四:能与BaCl2反应 取少量Na2CO3溶液于试管中,滴入BaCl2溶液 产生
______反应的基本类型
为______ 会哭却不流泪的鱼1年前1
会哭却不流泪的鱼1年前1 -
 此语111111 共回答了17个问题
此语111111 共回答了17个问题 |采纳率82.4%解题思路:根据碳酸钠的化学性质分析解答:水溶液呈碱性,能使酚酞变红,能与酸、某些碱、某些盐发生复分解反应,并根据反应写出有关反应的化学方程式.能使酚酞试液变红的溶液说明溶液呈碱性;碳酸钠与盐酸反应生成氯化钠、二氧化碳和水;碳酸钠与氢氧化钙发生反应生成碳酸钙白色沉淀,同时生成氢氧化钠;碳酸钠溶液与氯化钡溶液反应,生成碳酸钡沉淀和氯化钠,该反应由两种化合物相互交换成分生成另外两种化合物,属于复分解反应;
故答案为:
猜想 实验操作 实验现象 结论(或化学方程式)
猜想一:Na2CO3溶液显碱性 取少量Na2CO3溶液于试管中,滴入2-3滴酚酞溶液,振荡 溶液变为红色 溶液显 碱性
猜想二:能与酸反应 取少量Na2CO3溶液于试管中,然后滴加稀盐酸 有大量气泡产生 化学方程式
Na2CO3+2HCl=2NaCl+H2O+CO2↑
猜想三:能与Ca(OH)2反应 取少量Na2CO3溶液于试管中,滴加澄清石灰水 产生
有白色沉淀产生 化学方程式
Na2CO3+Ca(OH)2=2NaOH+CaCO3↓
猜想四:能与BaCl2反应 取少量Na2CO3溶液于试管中,滴入BaCl2溶液 产生
有白色沉淀产生 反应的基本类型
为 复分解反应点评:
本题考点: 碳酸钠、碳酸氢钠与碳酸钙;酸碱指示剂及其性质;反应类型的判定;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题重点考查了碳酸钠的化学性质,完成此题,要根据已有知识进行实验报告内容的补充,尤其是方程式的书写,因此同学们要注意平时对知识的积累,加强常见物质性质的记忆,尤其是物质的化学性质.1年前查看全部
- (2010•朝阳区一模)某化工厂用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该
(2010•朝阳区一模)某化工厂用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取12g纯碱样品放入烧杯中,称得烧杯及纯碱样品的总质量为158g,再把100g稀盐酸平均分成四份,依次加入到样品中,每次均充分反应.实验数据记录如下:
请计算:(要求计算过程)所加盐酸的次数 第一次 第二次 第三次 第四次 盐酸的质量/g 25 25 25 25 烧杯及所盛物质总质量/g 181.2 204.4 228.6 253.6
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量.
(2)该产品中碳酸钠的质量分数是否合格? 为爱守侯的天使1年前1
为爱守侯的天使1年前1 -
 冰冰红雪儿 共回答了9个问题
冰冰红雪儿 共回答了9个问题 |采纳率88.9%解题思路:(1)分析表中数据可知,每加入25g稀盐酸完全反应,产生气体二氧化碳的质量为158+25-181.2g=1.8g;
(2)第四次加入25g稀盐酸放出二氧化碳的质量228.6g+25g-253.6g=0,可判断样品中碳酸钠已完全反应,根据完全反应放出二氧化碳的质量计算样品中碳酸钠的质量,并由此判断该产品中碳酸钠的质量分数是否合格.(1)根据表中数据可得,第一次加入稀盐酸充分反应后,生成二氧化碳的质量=158+25-181.2g=1.8g
(2)样品完全反应时,产生CO2的质量为=158g+100g-253.6g=4.4g
设生成4.4gCO2,需碳酸钠的质量为x
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 44
x 4.4g
[106/x]=[44/4.4g] x=10.6g
该产品中碳酸钠的质量分数=[10.6g/12g]×100%=88.3%
∵96%>88.3%
∴该产品中Na2CO3的质量分数不合格
答:(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量1.8g;(2)该产品中碳酸钠的质量分数不合格.点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 根据每次加入稀盐酸充分反应前后物质的总质量可得到充分反应所产生二氧化碳的质量,由此质量对反应进行情况做出判断,此为解答本题的基本思路.1年前查看全部
- 【化学--选修化学与技术】(1)纯碱是一种重要的化工原料.目前制碱工业主要有“氨碱法”和“联合制碱法”两种工艺.①“氨碱
【化学--选修化学与技术】
(1)纯碱是一种重要的化工原料.目前制碱工业主要有“氨碱法”和“联合制碱法”两种工艺.
①“氨碱法”产生大量CaCl2废弃物,写出该工艺中产生CaCl2的化学方程式:______;
②写出“联合制碱法”有关反应的化学方程式:______;
③CO2是制碱工业的重要原料,“联合制碱法”与“氨碱法”中CO2的来源有何不同?______;
(2)钢铁工业对促进经济和社会发展起了重要作用.
①炼钢时,加入硅、锰和铝的目的是______.
②不锈钢含有的Cr元素是在炼钢过程的氧吹______(填“前”或“后”)加入,原因是______.
③炼铁和炼钢生产中,尾气均含有的主要污染物是______.从环保和经济角度考虑,上述尾气经处理可用作______. 小猪大人1年前1
小猪大人1年前1 -
 9又二分之一 共回答了19个问题
9又二分之一 共回答了19个问题 |采纳率78.9%解题思路:纯碱是一种重要的化工原料,目前制碱工业主要有两种工艺:①氨碱法 2NH4Cl+Ca(OH)2 2NH3↑+CaCl2+2H2O;②联合制碱法 NH3+CO2+H2O+NaCl(饱和)=NaHCO3↓+NH4Cl; 2NaHCO3
2NH3↑+CaCl2+2H2O;②联合制碱法 NH3+CO2+H2O+NaCl(饱和)=NaHCO3↓+NH4Cl; 2NaHCO3 Na2CO3+CO2↑+H2O.炼钢时,加入硅、锰和铝主要是可以脱氧和调整钢的成分. 因为Cr易被氧化,为防止Cr被氧化,不锈钢含有的Cr元素是在炼钢过程的氧吹后,若氧吹前加入Cr会形成炉渣被除去.炼铁和炼钢生产中,CO是主要的还原剂,故尾气均含有的主要污染物是CO,一氧化碳会引起中毒,故需对其进行处理等来解题.
Na2CO3+CO2↑+H2O.炼钢时,加入硅、锰和铝主要是可以脱氧和调整钢的成分. 因为Cr易被氧化,为防止Cr被氧化,不锈钢含有的Cr元素是在炼钢过程的氧吹后,若氧吹前加入Cr会形成炉渣被除去.炼铁和炼钢生产中,CO是主要的还原剂,故尾气均含有的主要污染物是CO,一氧化碳会引起中毒,故需对其进行处理等来解题.
(1)①氨碱法是由氯化铵和消石灰在加热条件下反应后生成氨气和氯化钙的反应,反应的化学方程式为:
2NH4Cl+Ca(OH)2 2NH3↑+CaCl2+2H2O,
2NH3↑+CaCl2+2H2O,
故答案为:2NH4Cl+Ca(OH)2 2NH3↑+CaCl2+2H2O;
2NH3↑+CaCl2+2H2O;
②联合制碱法是在氨的饱和NaCl溶液中二氧化碳气体,反应生成碳酸氢钠,解热碳酸氢钠即可制备碳酸钠,反应的有关方程式为,NH3+CO2+H2O+NaCl(饱和)=NaHCO3↓+NH4Cl; 2NaHCO3 Na2CO3+CO2↑+H2O,
Na2CO3+CO2↑+H2O,
故答案为:NH3+CO2+H2O+NaCl(饱和)=NaHCO3↓+NH4Cl;2NaHCO3 Na2CO3+CO2↑+H2O;
Na2CO3+CO2↑+H2O;
③CO2是制碱工业的重要原料,氨碱法中CO2来源于石灰石煅烧,联合制碱法中CO2的来源于合成氨工业的废气,
故答案为:“氨碱法”CO2来源于石灰石煅烧,“联合制碱法”CO2来源于合成氨工业的废气;
(2)①炼钢时,加入硅、锰和铝主要是为了脱氧和调整钢的成分.
故答案为:脱氧和调整钢的成分;
②因为Cr易被氧化,为Cr被氧化,不锈钢含有的Cr元素是在炼钢过程的氧吹后,若氧吹前加入Cr会形成炉渣被除去.
故答案为:后; 避免Cr被氧化;
③炼铁和炼钢生产中,CO是主要的还原剂,故尾气均含有的主要污染物是CO,一氧化碳会引起中毒,故需对其进行尾气处理.一氧化碳是一种很好的还原剂还是一种燃料.
故答案为:CO;燃料.点评:
本题考点: 纯碱工业(侯氏制碱法);高炉炼铁;生活中常见合金的组成.
考点点评: 本题考查目前制碱工业主要有“氨碱法”和“联合制碱法”两种工艺的实验设计,题目难度较大,易出错点为化学方程式的书写,注意把握反应的原理,注重相关基础知识的积累.1年前查看全部
- (2011•高青县一模)纯碱是一种重要的盐类物质,在化学工业中用途极广.工业上通常用氨碱法来生产.小红同学为探究纯碱的化
(2011•高青县一模)纯碱是一种重要的盐类物质,在化学工业中用途极广.工业上通常用氨碱法来生产.小红同学为探究纯碱的化学性质进行了猜想,并设计实验进行验证.请你帮助她将下列实验报告填写完整.
______若用稀硫酸代替稀盐酸进行实验,与猜想二相同,原因是______.猜想 实验操作 实验现象 结论(或化学方程式) 猜想一:纯碱溶液显碱性 ______
____________ 溶液显碱性 猜想二:能与酸反应 取少量纯碱溶液于试管中,滴加稀盐酸 ______ 猜想三:能与石灰水反应 取少量纯碱溶液于试管中,滴加澄清石灰水 产生白色沉淀 化学方程式:
______猜想四:能与氯化钡溶液反应 取少量纯碱溶液于试管中,滴加氯化钡溶液 产生白色沉淀 化学方程式:
______ 倒着走一回1年前1
倒着走一回1年前1 -
 蒜蓉空心菜 共回答了19个问题
蒜蓉空心菜 共回答了19个问题 |采纳率89.5%解题思路:本题通过实验的方式探究了碳酸钠的化学性质,水溶液呈碱性,能使酚酞变红,能与酸、某些碱、某些盐发生复分解反应,并要求写出有关反应的化学方程式.碳酸盐的检验是通过碳酸根与酸中的氢离子反应所放出的气体确定的,所以换成稀硫酸会出现同样的现象.碳酸钠的水溶液呈碱性,能使酚酞试液变红,碳酸钠与盐酸反应生成氯化钠、二氧化碳和水,碳酸钠与氢氧化钙发生复分解反应生成碳酸钙白色沉淀,同时生成氢氧化钠.取少量碳酸钠溶液于试管中,滴入氯化钡溶液,此时发生复分解反应,生成碳酸钡沉淀和氯化钠,所以本题答案为:
猜想一:取少量纯碱溶液于试管中,滴入2-3滴酚酞试液,振荡; 酚酞试液变红(或溶液变红);
猜想二:有气泡冒出;
猜想三:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
猜想四:Na2CO3+BaCl2=BaCO3↓+2NaCl;
交流与反思:稀硫酸和稀盐酸溶液中都含有氢离子.点评:
本题考点: 碳酸钠、碳酸氢钠与碳酸钙.
考点点评: 本题考查了碳酸钠的化学性质,完成此类题目,要根据已有的知识进行实验报告内容的补充,所以同学们要注意知识的储备,加强常见物质性质的记忆.1年前查看全部
- 2010上海卷27题)工业生产纯碱的工艺流程示意图如下: 氨碱法流程中氨是循环使用的,为此,滤液D加入
2010上海卷27题)工业生产纯碱的工艺流程示意图如下: 氨碱法流程中氨是循环使用的,为此,滤液D加入
2010上海卷27题)工业生产纯碱的工艺流程示意图如下:
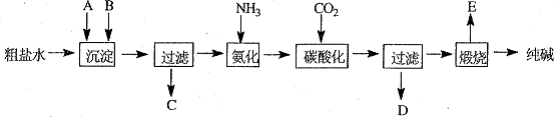
氨碱法流程中氨是循环使用的,为此,滤液D加入石灰水产生氨.加石灰水后所发生的反应的离子方程式为: 滤液D加石灰水前先要加热,原因回答第二问就可以了.我知道含有碳酸氢钠,但这步主要是制氨气,有没有含碳酸氢钠没有影响啊
答案是为了防止生成碳酸钙沉淀,
我不理解,这步不是主要制氨气吗,即使生成碳酸钙,也不影响生成的氨啊 myjsj1年前1
myjsj1年前1 -
 wangweijia01 共回答了21个问题
wangweijia01 共回答了21个问题 |采纳率95.2%是电离平衡方向移动,促使氨从氨水中一处,提高生产速率.1年前查看全部
- (2011•淮阴区一模)某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上标明:碳酸钠≥96%.为
(2011•淮阴区一模)某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上标明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验;取11.0g纯碱样品放入烧杯中,再把100g稀盐酸平均分成四份依次加入样品中,充分反应后,实验数据记录如下:
请你据此分析计算所加盐酸的次数 第一次 第二次 第三次 第四次 所加盐酸的质量/g 25 25 25 25 烧杯中所盛物质的总质量/g 34.2 57.4 81.6 106.6
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是______ g.
(2)该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%) 紫砚斋1051年前1
紫砚斋1051年前1 -
 slody 共回答了26个问题
slody 共回答了26个问题 |采纳率76.9%解题思路:根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和,故生成二氧化碳的质量=反应所盛物质的质量总和-反应后所盛物质的质量总和,分析表格中所给的实验数据,可知在反应过程中,烧杯内的物质的总质量不断减少,所减少的质量即为二氧化碳的质量.由二氧化碳的质量可以求出碳酸钠的质量分数.(1)由表格数据可知,第一次生成二氧化碳的质量为:11.0g+25g-34.2g=1.8g;
(2)分析可知,第二次生成二氧化碳的质量是3.6g,第三次生成二氧化碳的质量是4.4g,第四次仍然是4.4g,说明产品中碳酸钠在第三次就已经完全反应且恰好完全反应,最多生成二氧化碳的质量为:25g×3+11.0g-81.6g=4.4g.
设样品中含有的碳酸钠的质量为X
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
X 4.4g
[106/X=
44
4.4g]
产品中碳酸钠的质量分数为:[10.6g/11g]×100%≈96.4%≥96%;
故该产品中碳酸钠的质量分数合格.
故答案为:
(1)1.8
(2)设样品中含有的碳酸钠的质量为X
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
X 4.4g
[106/X=
44
4.4g]
产品中碳酸钠的质量分数为:[10.6g/11g]×100%≈96.4%≥96%;
故该产品中碳酸钠的质量分数合格.点评:
本题考点: 实验探究物质的组成成分以及含量;根据化学反应方程式的计算.
考点点评: 本题主要考查学生运用化学方程式计算和分析表格数据解决问题的能力,在有表格的计算中,我们通常要用到质量守恒定律分析表格中所给的数据,得出我们所需要的物质的质量,然后再利用化学方程式进行计算.1年前查看全部
- 侯氏制碱法和氨碱法有什么不一样之处?
 hero_gjh1年前1
hero_gjh1年前1 -
 cjhandm 共回答了20个问题
cjhandm 共回答了20个问题 |采纳率85%没有不一样之处.
侯氏制碱法又叫做氨碱法.1年前查看全部
- (2013•长宁区一模)氨碱法(索氏)和联合制碱法(侯氏)是两大重要的工业制碱法,
(2013•长宁区一模)氨碱法(索氏)和联合制碱法(侯氏)是两大重要的工业制碱法,
下列表达不正确的是( )氨碱法 联合制碱法 A 原料 食盐、氨气、生石灰 食盐、氨气、二氧化碳 B 可能的副产物 氯化钙 氯化铵 C 循环物质 氨气、二氧化碳 氯化钠 D 评价 原料易得;设备复杂;能耗高 原料利用率高;废弃物少
A.A
B.B
C.C
D.D joyrock1年前1
joyrock1年前1 -
 耗儿爱上猫 共回答了19个问题
耗儿爱上猫 共回答了19个问题 |采纳率78.9%解题思路:氨碱法:以食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气为原料来制取纯碱.先使氨气通入饱和食盐水中而成氨盐水,再通入二氧化碳生成溶解度较小的碳酸氢钠沉淀和氯化铵溶液.其化学反应原理是:NH3+CO2+H2O+NaCl(饱和)=NaHCO3↓+NH4Cl,将经过滤、洗涤得到的NaHCO3微小晶体,再加热煅烧制得纯碱产品:2NaHCO3
Na2CO3+CO2↑+H2O,放出的二氧化碳气体可回收循环使用.△ .
含有氯化铵的滤液与石灰乳(Ca(OH)2)混合加热,所放出的氨气可回收循环使用,CaO+H2O=Ca(OH)2,2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2H2O;
联合制碱法:以食盐、氨和二氧化碳(其中二氧化碳来自合成氨厂用水煤气制取氢气时的废气)为原料来制取纯碱,联合制碱法包括两个过程:第一个过程与氨碱法相同,将氨通入饱和食盐水而成氨盐水,再通入二氧化碳生成碳酸氢钠沉淀,经过滤、洗涤得NaHCO3微小晶体,再煅烧制得纯碱产品,其滤液是含有氯化铵和氯化钠的溶液.
第二个过程是从含有氯化铵和氯化钠的滤液中结晶沉淀出氯化铵晶体.由于氯化铵在常温下的溶解度比氯化钠要大,低温时的溶解度则比氯化钠小,而且氯化铵在氯化钠的浓溶液里的溶解度要比在水里的溶解度小得多,所以在低温条件下,向滤液中加入细粉状的氯化钠,并通入氨气,可以使氯化铵单独结晶沉淀析出,经过滤、洗涤和干燥即得氯化铵产品.此时滤出氯化铵沉淀后所得的滤液,已基本上被氯化钠饱和,可回收循环使用.
联合制碱法与氨碱法比较,其最大的优点是使食盐的利用率提高到96%以上,应用同量的食盐比氨碱法生产更多的纯碱.A、氨碱法原料有:食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气,联合制碱法原料有:食盐、氨气、二氧化碳,故A错误;
B、氨碱法可能的副产物为氯化钙,联合制碱法可能的副产物氯化铵,故B正确;
C、氨碱法循环物质:氨气、二氧化碳,联合制碱法循环物质:氯化钠,二氧化碳,故C错误;
D、氨碱法原料(食盐和石灰石)便宜,产品纯碱的纯度高,副产品氨和二氧化碳都可以回收循环使用,制造步骤简单,适合于大规模生产,但设备复杂;能耗高,氨碱法的最大缺点还在于原料食盐的利用率只有72%~74%;联合制碱法最大的优点是使食盐的利用率提高到96%以上,废弃物少,故D正确;
故选AC.点评:
本题考点: 纯碱工业(侯氏制碱法).
考点点评: 本题主要考查了氨碱法(索氏)和联合制碱法(侯氏)的原理,掌握原理是解题的关键,难度中等以上.1年前查看全部
- (2013•上海)碳酸氢纳俗称“小苏打”,是氨碱法和联合制碱法制纯碱的中间产物,可用作膨松剂,制酸剂,灭火剂等.工业上用
(2013•上海)碳酸氢纳俗称“小苏打”,是氨碱法和联合制碱法制纯碱的中间产物,可用作膨松剂,制酸剂,灭火剂等.工业上用纯碱溶液碳酸化制取碳酸氢钠.
(1)某碳酸氢钠样品中含有少量氯化钠.称取该样品,用0.1000mol/L盐酸滴定,耗用盐酸20.00mL.若改用0.05618mol/L硫酸滴定,需用硫酸______mL(保留两位小数).
(2)某溶液组成如表一:
表一
向该溶液通入二氧化碳,析出碳酸氢钠晶体.取出晶体后溶液组成如表二:化合物 Na2CO3 NaHCO3 NaCl 质量(kg) 814.8 400.3 97.3
表二
计算析出的碳酸氢纳晶体的质量(保留1位小数).化合物 Na2CO3 NaHCO3 NaCl 质量(kg) 137.7 428.8 97.3
(3)将组成如表二的溶液加热,使碳酸氢纳部分分解,溶液中NaHCO3的质量由428.8kg降为400.3kg,补加适量碳酸纳,使溶液组成回到表一状态.计算补加的碳酸纳质量(保留1位小数).
(4)某种由碳酸钠和碳酸氢钠组成的晶体452kg溶于水,然后通入二氧化碳,吸收二氧化碳44.8×103 L(标准状况),获得纯的碳酸氢钠溶液,测得溶液中含碳酸氢钠504kg.通过计算确定该晶体的化学式. wangweidong1231年前1
wangweidong1231年前1 -
 乡村的云 共回答了20个问题
乡村的云 共回答了20个问题 |采纳率95%解题思路:(1)根据碳酸氢钠样品消耗的氢离子物质的量相等,计算出消耗硫酸的体积;
(2)先求出通入二氧化碳消耗的碳酸钠的质量,然后根据反应计算出生成的碳酸氢钠的质量,再计算析出的碳酸氢钠的质量;
(3)根据碳酸氢钠减少的质量,计算出生成的碳酸钠的质量,再用814.8kg减掉现有的碳酸钠质量,就是需要添加的碳酸钠质量;
(4)先根据二氧化碳的体积计算出生成的碳酸氢钠和反应的碳酸钠质量,反应后溶液中含碳酸氢钠504kg,减掉生成的碳酸氢钠,得到原晶体中的碳酸氢钠质量,最后计算出水的质量,就可以求出晶体的化学式.(1)样品消耗盐酸中的氢离子的物质的量是:n(H+)=0.1000mol/L×0.020L=0.002mol,需要0.05618mol/L的硫酸的体积为:[0.002mol
2×0.05618mol•L−1≈17.80mL,
故答案是:17.80;
(2)设生成的碳酸氢钠质量为m,向溶液中通入二氧化碳,发生了反应:Na2CO3+CO2+H2O=2NaHCO3,反应消耗的碳酸钠的质量是:814.8kg-137.7kg=677.1kg
Na2CO3+CO2+H2O=2NaHCO3
106 168
677.1kg m
m=
677.1kg×168/106]≈1073.1kg
则析出的碳酸氢钠晶体的质量:1073.1+400.3-428.8=1044.6 kg
答:析出的碳酸氢纳晶体的质量是1044.6kg;
(3)设碳酸氢钠分解生成了xkg碳酸钠,碳酸氢钠分解反应为:2NaHCO3=Na2CO3+CO2+H2O,被分解的碳酸氢钠质量是:428.8kg-400.3kg=28.5kg,
2NaHCO3=Na2CO3+CO2+H2O
168106
28.5kg x
x=[28.5kg×106/168]=17.98 kg,
则补加的碳酸钠质量814.8-137.7-17.98=659.1 kg,
答:需要补加的碳酸钠的质量是:659.1 kg;
(4)设晶体中含有碳酸钠mkg,通入二氧化碳生成了m1kg碳酸氢钠,
Na2CO3 +CO2 +H2O=2NaHCO3
106 22.4×103 168
m 44.8×103 m1
m=
106×44.8×103
22.4×103=212kg,m1=
168×44.8×103
22.4×103=336kg,
则452kg晶体中含Na2CO3 212 kg,NaHCO3:504kg-336kg=168kg,水:452kg-212kg-168kg=72 kg,
所以n(Na2CO3):n(NaHCO3):n(H2O )=[212/106]:[168/84]:[72/18]=1:1:2
该晶体的化学式为NaHCO3•Na2CO3•2H2O,
答:该晶体的化学式为NaHCO3•Na2CO3•2H2O.点评:
本题考点: 探究物质的组成或测量物质的含量;钠的重要化合物.
考点点评: 本题考查了测定碳酸钠、碳酸氢钠的含量测定,本题计算量比较大,难度中等.1年前查看全部
- (2012•淄博一模)工业上采用氨碱法生产纯碱,是先向______中通入氨气,制成饱和氨盐水;在加压的条件下不断通入__
(2012•淄博一模)工业上采用氨碱法生产纯碱,是先向______中通入氨气,制成饱和氨盐水;在加压的条件下不断通入______,而使______结晶析出;将______加热分解即得纯碱.发生反应的化学原理是(填化学方程式):(1)______;(2)2NaHCO3
Na2CO3+CO2↑+H2O△ .2NaHCO3.
Na2CO3+CO2↑+H2O△ . qd_yaya1年前1
qd_yaya1年前1 -
 xuehuiwuying 共回答了22个问题
xuehuiwuying 共回答了22个问题 |采纳率95.5%解题思路:根据氨碱法生产纯碱的反应原理书写化学方程式,注意条件和配平;氨气溶于水呈碱性,更容易吸收酸性氧化物二氧化碳,在一定温度下,碳酸氢铵的溶解度比氯化铵小的多,会先从溶液中析出.在受热的条件下,碳酸氢钠分解生成了碳酸钠、水和二氧化碳.氨碱法生产纯碱的化学反应原理是用氨气和二氧化碳与氯化钠饱和溶液反应生成碳酸氢钠,然后加热碳酸氢钠制取碳酸钠;氨气溶于水所得氨水呈碱性,比水更易吸收二氧化碳;在一定温度下,碳酸氢铵的溶解度比氯化铵的溶解度小,故碳酸氢铵能首先从溶液中析出.在受热的条件下,碳酸氢钠分解生成了碳酸钠、水和二氧化碳.发生反应的化学原理是:(1)NH3+CO2+H2O+NaCl═NaHCO3+NH4Cl;(2)2NaHCO3
△
.
Na2CO3+CO2↑+H2O.
故答为:饱和食盐水,CO2,NaHCO3,NaHCO3,(1)NH3+CO2+H2O+NaCl═NaHCO3+NH4Cl;(2)2NaHCO3
△
.
Na2CO3+CO2↑+H2O.点评:
本题考点: 纯碱的制取.
考点点评: 了解工业上采用氨碱法生产纯碱的方法是解答本题的关键.应提高书写化学用语的能力.1年前查看全部
- 联合制碱法与氨碱法中的CO2的来源有何不同
 sailor0281年前2
sailor0281年前2 -
 超级老鼠 共回答了22个问题
超级老鼠 共回答了22个问题 |采纳率86.4%(联合制碱法)
(1)NH3+H2O+CO2=NH4HCO3
(2) NH4HCO3+NaCl=NH4Cl+NaHCO3↓
(3)2NaHCO3=加热=Na2CO3+H2O+CO2↑
即:①NaCl(饱和)+NH3+H2O+CO2=NH4Cl+NaHCO3↓
②2NaHCO3=加热=Na2CO3+H2O+CO2↑
氨气与水和二氧化碳反应生成一分子的碳酸氢铵,这是第一步.第二步是:碳酸氢铵与氯化钠反应生成一分子的氯化铵和碳酸氢钠沉淀,碳酸氢钠之所以沉淀是因为他的溶解度较小.
根据 NH4Cl 在常温时的溶解度比 NaCl 大,而在低温下却比 NaCl 溶解度小的原理,在 278K ~ 283K(5 ℃~ 10 ℃ ) 时,向母液中加入食盐细粉,而使 NH4Cl 单独结晶析出供做氮肥.
此法优点:保留了氨碱法的优点,消除了它的缺点,使食盐的利用率提高到 96 %; NH4Cl 可做氮肥;可与合成氨厂联合,使合成氨的原料气 CO 转化成 CO2 ,革除了 CaCO3 制 CO2 这一工序.
氨减法 CaCO3=CaO+CO2
NH3+CO2+H2O===NH4HCO3
NH4HCO3+NaCl===NaHCO3+NH4Cl
2NaHCO3===Na2CO3+CO2 +H2O
反应生成的CO2可以回收再用,而NH4Cl又可以与生石灰反应,产生NH3,重新作为原料使用:2NH4Cl+CaO===2NH3+CaCl2+H2O1年前查看全部
- 某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该
某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该
所加盐酸的次数 烧杯及所盛物质总质量/g
第一次 176.9
第二次 195.8
第三次 214.7
第四次 233.6
第五次 253.6
请你据此分析计算:
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是 g.
(2)该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
(3)根据实验数据,在右边的坐标纸上绘制出所加稀盐酸质量与生成气体质量关系的曲线.(不要求写出计算过程,只画出曲线即可) figo11年前0
figo11年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 侯氏制碱法与氨碱法的区别是什么百度百科上搜索词条,它们的过程是一样的啊,怎么回事,不是说有区别么?
 番茄炒皮蛋1年前2
番茄炒皮蛋1年前2 -
 xuyunfeng85 共回答了17个问题
xuyunfeng85 共回答了17个问题 |采纳率100%索尔维制碱法与侯氏制碱法(也叫做氨碱法与联碱法)
guoyongbin 发表于 2006-8-10 19:15:28
无水碳酸钠,俗名纯碱、苏打.它是玻璃、造纸、肥皂、洗涤剂、纺织、制革等工业的重要原料,还常用作硬水的软化剂,也用于制造钠的化合物.它的工业制法主要有氨碱法和联合制碱法两种.
一、氨碱法(又称索尔维法)
它是比利时工程师苏尔维(1838~1922)于1892年发明的纯碱制法.他以食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气为原料来制取纯碱.先使氨气通入饱和食盐水中而成氨盐水,再通入二氧化碳生成溶解度较小的碳酸氢钠沉淀和氯化铵溶液.其化学反应原理是:NaCl+NH3+H2O+CO2=NaHCO3↓+NH4Cl
将经过滤、洗涤得到的NaHCO3微小晶体,再加热煅烧制得纯碱产品.2NaHCO3=Na2CO3+H2O+CO2↑放出的二氧化碳气体可回收循环使用.含有氯化铵的滤液与石灰乳[Ca(OH)2]混合加热,所放出的氨气可回收循环使用.CaO+H2O=Ca(OH)2,2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2H2O其工业生产的简单流程如图所示.
氨碱法的优点是:原料(食盐和石灰石)便宜;产品纯碱的纯度高;副产品氨和二氧化碳都可以回收循环使用;制造步骤简单,适合于大规模生产.但氨碱法也有许多缺点:首先是两种原料的成分里都只利用了一半——食盐成分里的钠离子(Na+)和石灰石成分里的碳酸根离子(CO32-)结合成了碳酸钠,可是食盐的另一成分氯离子(Cl-)和石灰石的另一成分钙离子(Ca2+)却结合成了没有多大用途的氯化钙(CaCl2),因此如何处理氯化钙成为一个很大的负担.氨碱法的最大缺点还在于原料食盐的利用率只有72%~74%,其余的食盐都随着氯化钙溶液作为废液被抛弃了,这是一个很大的损失.
二、联合制碱法(又称侯氏制碱法)
它是我国化学工程专家侯德榜(1890~1974)于1943年创立的.是将氨碱法和合成氨法两种工艺联合起来,同时生产纯碱和氯化铵两种产品的方法.原料是食盐、氨和二氧化碳——合成氨厂用水煤气制取氢气时的废气.其化学反应原理是:C+H2O=CO+H2 CO+H2O=CO2+H2
联合制碱法包括两个过程:第一个过程与氨碱法相同,将氨通入饱和食盐水而成氨盐水,再通入二氧化碳生成碳酸氢钠沉淀,经过滤、洗涤得NaHCO3微小晶体,再煅烧制得纯碱产品,其滤液是含有氯化铵和氯化钠的溶液.第二个过程是从含有氯化铵和氯化钠的滤液中结晶沉淀出氯化铵晶体.由于氯化铵在常温下的溶解度比氯化钠要大,低温时的溶解度则比氯化钠小,而且氯化铵在氯化钠的浓溶液里的溶解度要比在水里的溶解度小得多.所以在低温条件下,向滤液中加入细粉状的氯化钠,并通入氨气,可以使氯化铵单独结晶沉淀析出,经过滤、洗涤和干燥即得氯化铵产品.此时滤出氯化铵沉淀后所得的滤液,已基本上被氯化钠饱和,可回收循环使用.其工业生产的简单流程如图所示.
联合制碱法与氨碱法比较,其最大的优点是使食盐的利用率提高到96%以上,应用同量的食盐比氨碱法生产更多的纯碱.另外它综合利用了氨厂的二氧化碳和碱厂的氯离子,同时,生产出两种可贵的产品——纯碱和氯化铵.将氨厂的废气二氧化碳,转变为碱厂的主要原料来制取纯碱,这样就节省了碱厂里用于制取二氧化碳的庞大的石灰窑;将碱厂的无用的成分氯离子(Cl-)来代替价格较高的硫酸固定氨厂里的氨,制取氮肥氯化铵.从而不再生成没有多大用处,又难于处理的氯化钙,减少了对环境的污染,并且大大降低了纯碱和氮肥的成本,充分体现了大规模联合生产的优越性.1年前查看全部
- 某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上标明:碳酸钠≥96%.为测定该产品中含碳酸钠的质
某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上标明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分了以下实验:取34.6g纯碱样品放入盛有130g稀盐酸的烧杯中,恰好完全反应,反应后溶液的质量为151.4g,请计算:
(1)充分反应后,生成二氧化碳的质量是______g
(2)该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%) baker20071年前1
baker20071年前1 -
 JZY风铃JZY 共回答了22个问题
JZY风铃JZY 共回答了22个问题 |采纳率95.5%解题思路:(1)根据盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,所以反应前后烧杯内减少的质量就是生成二氧化碳的质量进行解答;
(2)根据二氧化碳的质量求出碳酸钠的质量,从而进一步求出产品中碳酸钠的质量分数进行解答.(1)盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,所以反应前后烧杯内减少的质量就是生成二氧化碳的质量,生成二氧化碳的质量=34.6g+130g-151.4g=13.2g;故填:13.2;
(2)设该产品中碳酸钠的质量为x.
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
x 13.2g
[106/x=
44
13.2g]
x=31.8g
该产品中碳酸钠的质量分数=
31.8g
34.6g×100%=91.9%<96%
所以该产品中碳酸钠的质量分数不合格
答:该产品中碳酸钠的质量分数不合格.点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 本题考查有关化学计算,难度不大,确定二氧化碳的质量是关键,注意理解质量分数.1年前查看全部
- 氨碱法和侯氏制碱法的生产流程图可用如图表示,试回答下列问题。 (1)请把图中的数字用具体的化学式表示:①___、②___
氨碱法和侯氏制碱法的生产流程图可用如图表示,试回答下列问题。 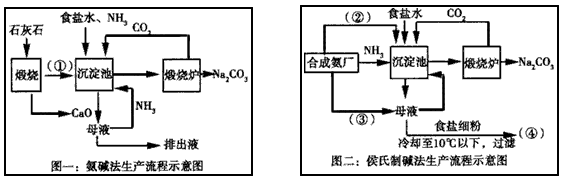
(1)请把图中的数字用具体的化学式表示:①___、②___、③___、④___。
(2)“氨碱法”产生大量的CaCl 2 废弃物,请写出该工艺中产生CaCl 2 的化学方程式:____;“侯氏制碱法”中,在母液中通入③的目的是________。
(3)CO 2 是制碱工业的重要原料,“侯氏制碱法”与“氨碱法”中CO 2 的来源有何不同:____。
(4)取“侯氏制碱法”生产的纯碱样品(设其中的杂质不与盐酸反应)11.0 g配成250.00 mL溶液,取25.00 mL溶液用1.00 mol.L -1 的标准盐酸滴定,用酚酞作指示剂,三次滴定消耗盐酸的平均量为10.00 mL。请计算纯碱样品的纯度______。 洒的奇奥看1年前1
洒的奇奥看1年前1 -
 搁浅的帆 共回答了24个问题
搁浅的帆 共回答了24个问题 |采纳率87.5%1年前查看全部
- 氨碱法用食盐制纯碱的反应原理是:
氨碱法用食盐制纯碱的反应原理是:
(1)NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl(2)2NaHCO3
Na2CO3+H2O+CO2↑△ .
下列对上述信息的有关理解中,错误的是( )
A.用食盐制纯碱需要含碳、氧元素的物质
B.在该条件下,NaHCO3的溶解度比NH4Cl小
C.在反应(1)中析出固体后的溶液是NaHCO3 的不饱和溶液
D.副产品氯化铵是一种盐 xiaoyue0001年前1
xiaoyue0001年前1 -
 peiyu0457 共回答了18个问题
peiyu0457 共回答了18个问题 |采纳率88.9%解题思路:A、根据质量守恒定律判断.
B、由于反应时生成的碳酸氢钠多,而NH4Cl少,所以在溶剂质量相等的情况下,只能说碳酸氢钠更容易形成饱和溶液,不能说明溶解度就一定是碳酸氢钠的小.
C、判断溶液是否饱和,可以采用两种方式:判断溶液底部是否存在晶体或加入晶体看是否能溶解.
D、盐的组成特点是它是由金属元素和酸根组成的.A、根据质量守恒定律,化学反应前后元素的种类不变,氯化钠中无碳、氢元素,而碳酸氢钠中含碳、氢两种元素,因此用食盐制纯碱,还需要含碳、氧元素的物质,故A不符合要求.
B、由于反应时生成的碳酸氢钠多,而NH4Cl少,所以在溶剂质量相等的情况下,只能说碳酸氢钠更容易形成饱和溶液,不能说明溶解度就一定是碳酸氢钠的小,故B符合题意;
C、析出固体后的溶液一定是饱和溶液,所以是NaHCO3的饱和溶液,故C不符合题意;
D、氯化铵是由铵根离子和氯酸根离子构成的,属于盐类,故D不符合题意.
故选:B.点评:
本题考点: 纯碱的制取;饱和溶液和不饱和溶液;常见的氧化物、酸、碱和盐的判别.
考点点评: 信息的分析、处理是考查学生素质的重要手段之一,本题以方程式为信息源,考查化学方程式的含义及提供的诸多信息,透彻掌握化学方程式的含义是解题的关键.1年前查看全部
- [选修一化学与技术]联碱法(候氏制碱法)和氨碱法的生产流程简要表示如下图:
[选修一化学与技术]联碱法(候氏制碱法)和氨碱法的生产流程简要表示如下图: 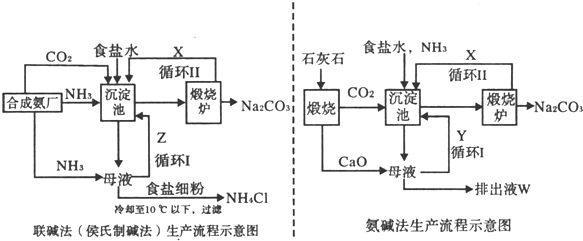
(1)沉淀池中发生反应的化学方程式为______;
(2)X是______,Y是______ (填化学式);
(3)Z中除了溶解的氨气、食盐外,其它溶质还有______;排出液中的溶质除了氢氧化钙外,还有______;
(4)从理论上分析,在氨碱法生产过程中______ (填“需要”、“不需要”)补充氨气,从原料到产品,氨碱法总反应过程用化学方程式表示,可写为______;
(5)根据联碱法中从母液中提取氯化铵晶体的过程推测,所得结论正确是______;
a.常温时氯化铵的溶解度比氯化钠小
b.通入氨气目的是使氯化铵更多析出
c.加入食盐细粉目的是提高Na + 的浓度,促进碳酸氢钠结晶析出
(6)联碱法中,每当通入NH 3 44.8L(巳折合成标准状况下)时可以得到纯碱100.0g则NH 3 的利用率为______.相比于氨碱法,指出联碱法的一项优点______• zhong8888801年前1
zhong8888801年前1 -
 蹒跚学步 共回答了18个问题
蹒跚学步 共回答了18个问题 |采纳率94.4%(1)依据流程图分析可知,生产流程联碱法和氨碱法生产流程中沉淀池中发生的反应是氨气、二氧化碳、水、氯化钠反应生成碳酸氢钠晶体和氯化铵,所以反应的化学方程式为:NaCl+NH 3 +CO 2 +H 2 O═NaHCO 3 ↓+NH 4 Cl,故答案为:NaCl+NH 3 +CO 2 +H 2 O═NaHCO 3 ↓+NH 4 Cl;
(2)联碱法生产流程图中分析循环Ⅱ中是碳酸氢钠分解生成的二氧化碳气体;氨碱法的生产流程中循环Ⅰ是氧化钙和水反应生成氢氧化钙,氢氧化钙与铵盐反应生成的氨气可以循环使用,故答案为:CO 2 ;NH 3 ;
(3)依据两个过程中的物质发生的反应分析,联碱法母液主要是氯化铵、碳酸钠、碳酸氢钠、氯化钠;Z中除了溶解的氨气、食盐外,其它溶质还有氯化铵、碳酸钠;氨碱法排出液中的溶质除了氢氧化钙外,还有氢氧化钙和氯化铵反应生成的氯化钙,氯化钠,故答案为:Na 2 CO 3 、NH 4 Cl;CaCl 2 、NaCl;
(4)从理论上分析,氨碱法生产过程中,母液中加入氧化钙反应生成氢氧化钙会和铵盐生成氨气,反应过程中氨气转化为铵盐,铵盐转化为氨气,氨气循环使用,不需要补充氨气;
NaCl+NH 3 +CO 2 +H 2 O═NaHCO 3 ↓+NH 4 Cl;CaCO 3 ═CaO+CO 2 ↑;CaO+H 2 O═Ca(OH) 2 ;Ca(OH) 2 +2NH 4 Cl═CaCl 2 +2NH 3 ↑+2H 2 O;2NaHCO 3 ═Na 2 CO 3 +H 2 O+CO 2 ↑合并得到总化学方程式为:CaCO 3 +2NaCl═Na 2 CO 3 +CaCl 2 ,故答案为:不需要;CaCO 3 +2NaCl═Na 2 CO 3 +CaCl 2 ;
(5)联碱法中从母液中提取氯化铵晶体的过程中;
a、温时氯化铵的溶解度比氯化钠大,故a错误;
b、通氨气作用有增大NH 4 + 的浓度,使NH 4 Cl更多地析出和使NaHCO 3 转化为Na 2 CO 3 ,提高析出的NH 4 Cl纯度,故b正确;
c、加入食盐细粉目的是提高Cl - 的浓度,促进氯化铵结晶析出,故c错误;
故答案为:b;
(6)联碱法中发生的反应为:NaCl+NH 3 +CO 2 +H 2 O═NaHCO 3 ↓+NH 4 Cl;2NaHCO 3 ═Na 2 CO 3 +H 2 O+CO 2 ↑;每当通入NH 3 44.8L(巳折合成标准状况下)物质的量为2mol;生产过程中得到纯碱100.0g,物质的量为
100g
106g/mol =
50
53 mol;需要氨气的物质的量为
50
53 ×2 =
100
53 mol;则NH 3 的利用率=
100
53 mol
2mol ×100%=94.3%;
联合制碱法与氨碱法比较,其最大的优点是使食盐的利用率提高到96%以上,应用同量的食盐比氨碱法生产更多的纯碱.另外它综合利用了氨厂的二氧化碳和碱厂的氯离子,同时,生产出两种可贵的产品--纯碱和氯化铵.将氨厂的废气二氧化碳,转变为碱厂的主要原料来制取纯碱,这样就节省了碱厂里用于制取二氧化碳的庞大的石灰窑;将碱厂的无用的成分氯离子(Cl - )来代替价格较高的硫酸固定氨厂里的氨,制取氮肥氯化铵.从而不再生成没有多大用处,又难于处理的氯化钙,减少了对环境的污染,并且大大降低了纯碱和氮肥的成本,充分体现了大规模联合生产的优越性,
故答案为:94.3%;不产生无用的CaCl 2 ,提高了食盐的转化率.1年前查看全部
- (1)纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制碱法”(侯氏制碱法)两种工艺。
(1)纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制碱法”(侯氏制碱法)两种工艺。
①“氨碱法”产生大量CaCl 2 废弃物,写出该工艺中产生CaCl 2 的化学方程式:_________________________________________________;
②写出“联合制碱法”有关反应的化学方程式_________________ _; 。
③CO 2 是制碱工业的重要原料,“联合制碱法”与“氨碱法”中CO 2 的来源有何不同?________________________________________;
(2)钢铁工业对促进经济和社会发展起了重要作用。
①炼钢时,加入硅、锰和铝的目的是_______________________________。
②不锈钢含有的Cr元素是在炼钢过程的氧吹__ __(填“前”或“后”)加入。
③炼铁和炼钢生产中,尾气均含有的主要污染物是________。从环保和经济角度考虑,上述尾气经处理可用作_________。 huamingxu12081年前0
huamingxu12081年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 根据氨碱法用食盐制纯碱的反应原理是:(1)NaCl+NH 3 +CO 2 +H 2 O=NaHCO 3 +NH 4 Cl
根据氨碱法用食盐制纯碱的反应原理是:(1)NaCl+NH 3 +CO 2 +H 2 O=NaHCO 3 +NH 4 Cl,(2)2NaHCO 3
Na 2 CO 3 +CO 2 ↑+H 2 O下列对上述信息的有关理解中,错误的是( )△ . A.用食盐制纯碱需要含碳、氧元素的物质 B.纯碱属于盐类物质 C.因生成气体,反应不遵循质量守恒定律 D.副产品氯化铵是一种氮肥  落花飘雨1年前1
落花飘雨1年前1 -
 wubinbuaa 共回答了29个问题
wubinbuaa 共回答了29个问题 |采纳率86.2%A、根据质量守恒定律,化学反应前后元素的种类不变,氯化钠中无碳、氢元素,而碳酸氢钠中含碳、氢两种元素,因此用食盐制纯碱,还需要含碳、氧元素的物质,所以正确.
B、纯碱是碳酸钠,是由钠离子和碳酸根离子构成的,符合盐的定义,属于盐类物质,所以正确.
C、质量守恒定律的内容是参加化学反应的各物质质量总和等于反应后生成的各物质质量总和,与反应物或生成物的状态无关,所以错误.
D、氯化铵中含有氮元素,为氮肥,所以正确.
故选C.1年前查看全部
- (2005•青岛)某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上标明:碳酸钠≥96%.为测定该
(2005•青岛)某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上标明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验;取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,充分反应后,实验数据记录如下:
请你据此分析计算:所加盐酸的次数 第一次 第二次 第三次 第四次 烧杯及所盛物质的总质量/g 181.2 204.4 228.6 253.6
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是______g.
(2)该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
(3)根据实验数据,在下边的坐标纸上绘制出所加稀盐酸的质量与生成的二氧化碳的质量关系的曲线.(不要求写出计算过程,只画出曲线即可)
 无用1231年前1
无用1231年前1 -
 娃哈哈d582 共回答了14个问题
娃哈哈d582 共回答了14个问题 |采纳率92.9%解题思路:(1)根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.故第一次加入稀盐酸充分反应后,生成二氧化碳的质量=反应前烧杯及所盛物质的质量总和-反应后烧杯及所盛物质的质量总和;
(2)由图表数据可知,前二次反应后,每次生成气体的质量都是1.8g,第四次反应没有气体生成,故可判断第三次反应已完全.故生成气体的质量为158g+75g-228.6g=4.4g.根据碳酸钠与稀盐酸反应的化学方程式和生成的气体质量,列出比例式,即可计算出参与反应的Na2CO3的质量,然后根据溶质质量分数=[溶质质量/溶液质量]×100%计算即可;(1)第一次的结果中,二氧化碳的质量为158.0g+100g÷4-181.2g=1.8g;故答案为:1.8g.
(2)前二次反应后,每次生成气体的质量都是1.8g,第四次反应没有气体生成,故可判断第三次反应已完全.故生成气体的质量为158g+75g-228.6g=4.4g
设参与反应的Na2CO3的质量为x,
Na2CO3+2HCl=2NaCl+CO2↑+H2O
106 44
x 4.4g
∴[106/44=
x
4.4g],
解之得:x=10.6g,
产品中碳酸钠的质量分数为:[10.6g/11g]×100%≈96.4%≥96%;
故该产品中碳酸钠的质量分数合格.
(3)根据前两步可以计算出当碳酸钠存在的情况下,每25g盐酸对应的二氧化碳质量为1.8g,当生成4.4g二氧化碳时,消耗的盐酸溶液的质量为61g.之后再加盐酸无气体生成.而开始时,盐酸为零,二氧化碳也为零.所以得图:
点评:
本题考点: 根据化学反应方程式的计算;实验数据处理或者误差分析的探究;质量守恒定律及其应用.
考点点评: 本题主要考查学生运用化学方程式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.1年前查看全部
- 工业上采用氨碱法生产纯碱,其反应的化学反应原理为NH3+CO2+H2O+NaCl═NaHCO3+NH4ClNH3+CO2
工业上采用氨碱法生产纯碱,其反应的化学反应原理为NH3+CO2+H2O+NaCl═NaHCO3+NH4ClNH3+CO2+H2O+NaCl═NaHCO3+NH4Cl;2NaHCO3
Na2CO3+CO2↑+H2O2NaHCO3△ .
Na2CO3+CO2↑+H2O.氨盐水比食盐水更容易吸收二氧化碳的原因是氨气溶于水后显碱性,二氧化碳的水溶液显酸性,酸碱易中和氨气溶于水后显碱性,二氧化碳的水溶液显酸性,酸碱易中和,氨盐水吸收二氧化碳后,首先结晶析出的是碳酸氢钠碳酸氢钠,该现象说明了该温度下,碳酸氢钠的溶解度比NH4Cl少的多该温度下,碳酸氢钠的溶解度比NH4Cl少的多.△ .  你是我的女神1年前1
你是我的女神1年前1 -
 无力揽狂澜 共回答了18个问题
无力揽狂澜 共回答了18个问题 |采纳率88.9%解题思路:根据氨碱法生产纯碱的反应原理书写化学方程式,注意条件和配平;氨气溶于水呈碱性,更容易吸收酸性氧化物二氧化碳,在一定温度下,碳酸氢铵的溶解度比氯化铵小的多,会先从溶液中析出.氨碱法生产纯碱的化学反应原理是用氨气和二氧化碳与氯化钠和水反应生成碳酸氢钠,然后加热碳酸氢钠制取碳酸钠;氨气溶于水所得氨水呈碱性,比水更易吸收二氧化碳;在一定温度下,碳酸氢铵的溶解度比氯化铵的溶解度小,故碳酸氢铵能首先从溶液中析出.
故答案为:NH3+CO2+H2O+NaCl═NaHCO3+NH4Cl; 2NaHCO3
△
.
Na2CO3+CO2↑+H2O.氨气溶于水后显碱性,二氧化碳的水溶液显酸性,酸碱易中和,碳酸氢钠,该温度下,碳酸氢钠的溶解度比NH4Cl少的多.点评:
本题考点: 书写化学方程式、文字表达式、电离方程式;固体溶解度的影响因素;物质的相互转化和制备.1年前查看全部
- 联合制碱法和氨碱法的区别
 快乐12451年前1
快乐12451年前1 -
 机秘行动 共回答了25个问题
机秘行动 共回答了25个问题 |采纳率80%1.把氨厂和碱厂建在一起,联合生产.由氨厂提供碱厂需要的氨和二氧化碳.
2.使食盐的利用率提高到 96 %
3.与合成氨厂联合,使合成氨的原料气CO 转化成 CO2 ,革除了 CaCO3 制 CO2 这一工序.
低调の小鑫 | 2011-06-12
3
01年前查看全部
- 纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制 碱法”两种工艺。请按要求回答问题:
纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制 碱法”两种工艺。请按要求回答问题:
(1)“氨碱法”产生大量CaCl 2 废弃物,请写出该工艺中产生CaCl 2 的化学方程式:_______________________________________________________;
(2)写出“联合制碱法”有关反应的化学方程式:____________________________________________;
(3) CO 2 是制碱工业的重要原料,“联合制碱法”与“氨碱法”中CO 2 的来源有何不同?__________________________________________________________;
(4)绿色化学的重要原则之一是提高反应的原子利用率。根据“联合制碱法”总反应,列出计算原子利用率的表达式:
原子利用率(%) =________________________________。 mmy361年前0
mmy361年前0 -
 共回答了个问题
共回答了个问题 |采纳率
大家在问
- 1能直接说“原电池中的负极就是阳极”吗?
- 2英语翻译请会的人来答,不要复制再用网上的那个翻译,我试了直接不准
- 3请领导阅示与呈领导阅示的区别
- 4you don't bother me!能帮我翻译成中文吗谢谢
- 5高二立体几何5)如图,已知ABCD-A1B1C1D1是棱长为a的正方体,① 棱锥A1-ABCD的体积为 ;② 棱锥C1-
- 6The greatest happiness in life is to make progress everyday!
- 7he had got on the bus.the bus began to move.(用no sooner .tha
- 8用换元法求不定积分 ∫e^根号x的三次方/根号x
- 9载歌载舞的载读音是第3声还是第4声?
- 101-5分之4x=8分之7
- 11竖式计算.[(1)、(4)两题请写出验算过程]
- 12一个圆锥形沙堆的体积180立方米,高是12米,这个沙堆的占地面积是多少?一个粮仓的上部份时圆锥体,下部分时圆柱体.已知粮
- 13the following
- 14阅读下面两段文字,完成下面问题。
- 15若√-x²-2x-1有意义,求x范围

