核内中子数为N的R3+离子,其质量数为A,它的m g氧化物中 所含电子的物质的量是( )
 香草qq2022-10-04 11:39:541条回答
香草qq2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 说过的故事 共回答了28个问题
说过的故事 共回答了28个问题 |采纳率92.9%- 一个R2O3分子中含有电子数=2(A-N)+3*8=(2A -2N + 24)个
m g氧化物的物质的量=m/(2A +48) mol
所含电子的物质的量是=(2A -2N + 24)*m/(2A +48) mol - 1年前
相关推荐
- 电子数变了中子数会变吗拜托了各位 谢谢
 kuangkaizhi1年前1
kuangkaizhi1年前1 -
 头发是乱了 共回答了12个问题
头发是乱了 共回答了12个问题 |采纳率83.3%一般不会. 中子数变了就成同位素了. 电子数只与原子核中质子数有关. 得失电子与外界条件(物理 如老式电视屏 化学方面氧化还原 )有关.1年前查看全部
- 质子数和中子数为8,电子数为10是带正电的离子吗
 南昌的叶子1年前4
南昌的叶子1年前4 -
 晒太阳的树袋熊 共回答了16个问题
晒太阳的树袋熊 共回答了16个问题 |采纳率93.8%不是,是O^2-1年前查看全部
- 元素周期表元素排列的根据是什么是根据质子数还是中子数、还是电子数?
 zcvvv1年前4
zcvvv1年前4 -
 潇湘涵子 共回答了18个问题
潇湘涵子 共回答了18个问题 |采纳率94.4%是根据元素的最外层电子数、电子层数等性质排列1年前查看全部
- 不同元素的原子,质子数是否相等,中子数是否相等,质量数是否相等,核外电子数是否不等,请分别举例,谢
不同元素的原子,质子数是否相等,中子数是否相等,质量数是否相等,核外电子数是否不等,请分别举例,谢
举例包括元素种类及具体的数字 四川张7181年前2
四川张7181年前2 -
 ww773600 共回答了10个问题
ww773600 共回答了10个问题 |采纳率100%不同元素的原子,质子数肯定不相等.
比如 Na、K,质子数分别是11、19.
不同元素的原子,中子数不一定相等.
比如 23Na、24Mg,中子数都是12.23Na和27Al,中子数分别是12、14.
不同元素的原子,质量数不一定相等.
比如 32P和32S,质量数都是32.23Na、24Mg,质量数分别是23、24.
(31P、32P互为同位素)
这些问题,只要了解同位素的概念,是很容易的1年前查看全部
- 已知某元素的阳离子Rn+,其原子质量数为A,中子数为A-x+n,则m克Rn+核外电子的物质的量为______
 engsn0yugfdgng1年前2
engsn0yugfdgng1年前2 -
 abc3326 共回答了20个问题
abc3326 共回答了20个问题 |采纳率90%质量数 = 中子数 + 质子数
阳离子的电子数 = 质子数 - 电荷数
质子数 = A - (A-x+n)=x-n
阳离子的电子数 = x - 2n
Rn+核外电子的物质的量= m/A × ( x - 2n)=m( x - 2n)/A1年前查看全部
- 挑老师的刺:老师出作业题让同学们算:.求出R为何种元素后 已知R有一种同位素 中子数与质子数相等.我的问题是:说R元素有
挑老师的刺:
老师出作业题让同学们算:.求出R为何种元素后 已知R有一种同位素 中子数与质子数相等.
我的问题是:说R元素有一种同位素这种说法对不对 问周围人他们都说是对的 我感觉不对 火龙哥1年前1
火龙哥1年前1 -
 知识人智 共回答了26个问题
知识人智 共回答了26个问题 |采纳率100%这种说法本身就有问题,同位素是相对的,不能孤立起来说.我们可以说R有两种核素,他们互为同位素,但不可以说R有两种同位素.同位素是一个相对的概念.
不过你说的这个地方是不会命题的,同位素作为高中的四同之一,主要考察你是否了解其概念,相应的作出判断.1年前查看全部
- x元素原子核内质子数35,它有中子数为46和44同位素,x相对原子质量79.9,中子数为44的原子在x个数百分比为
 三月的天真1年前1
三月的天真1年前1 -
 我没名字123 共回答了17个问题
我没名字123 共回答了17个问题 |采纳率100%同位素质量数分别为35+46=81,35+44=79,x+y=1,81x+79y=79.9.自己算x,y,44对应y1年前查看全部
- 为什么有的元素质子数相同而中子数却不同呢?
为什么有的元素质子数相同而中子数却不同呢?
例如:碳14 氚 ljlj20001年前1
ljlj20001年前1 -
 uu人罗新 共回答了31个问题
uu人罗新 共回答了31个问题 |采纳率90.3%具有相同质子数,不同中子数(或不同质量数)的原子互称为同位素.
这里的原子是广义的概念,指微观粒子.
例如氕(11H)、氘(21H)和氚(31H),它们原子核中都有1个质子,但是它们的原子核中分别有0个中子,1个中子及2个中子,所以它们互为同位素.
同位素是具有相同原子序数的同一化学元素的两种或多种原子之一,在元素周期表上占有同一位置,化学行为几乎相同,但原子质量或质量数不同,从而其质谱行为、放射性转变和物理性质(例如在气态下的扩散本领)有所差异.同位素的表示是在该元素符号的左上角注明质量数,例如碳14,一般用14C而不用C14.
自然界中与多元素都有同位素.同位素有的是天然存在的,有的是人工制造的,有的有放射性,有的没有反射性.
同一元素的同位素虽然质量数不同,但他们的化学性质基本相同,物理性质有差异(主要表现在质量上).自然界中,各种同位素的原子个数百分比一定.1年前查看全部
- 计算推理题某元素R的核外电子书等于核内中子数,2.8g该元素单质与氧气完全反应,可得到6g化合物RO2(1)该元素的原子
计算推理题
某元素R的核外电子书等于核内中子数,2.8g该元素单质与氧气完全反应,可得到6g化合物RO2
(1)该元素的原子的质量数为多少,是什么元素?
如果把2.8g该元素单质投入到足量的氢氧化钠溶液中,生成的气体在标况下的体积是多少 w37012319721年前3
w37012319721年前3 -
 灰鸽子2007 共回答了16个问题
灰鸽子2007 共回答了16个问题 |采纳率93.8%设该元素的原子的质量数为x
2.8/x=6/(x+16*2)
x=28
此元素为Si(硅)
2.
Si+2NaOH+H2O=Na2SiO3+2H2
(2.8/28)*2*22.4=4.481年前查看全部
- 1到20号元素的质子数中子数质子数是多少,中子数是多少。
 oo的蜗牛_791年前3
oo的蜗牛_791年前3 -
 buttygu 共回答了16个问题
buttygu 共回答了16个问题 |采纳率87.5%22每种元素都可以有中子数不同的同位素isotopes
如,中子数分别为1,2,3的氢的同位素氕氘氚.
假定你问的是元素最常见(丰度最高的稳定同位素)的中子数,那么
氢:0 (>99.9%)
氦:2 (>99.9%)
锂:4 (92.5%)
铍:5 100%)
硼:6 (80.1%),5 (19.9%)
碳:6 (99%)
氮:7 (99.6%)
氧:8 (99.8%)
氟:10 100%)
氖:10 (90.5%),12(9.3%)
钠:12 100%)
镁:12 (79%),13(10%),14(11%)
铝:14 100%)
硅:14 (92.2%),15(4.7%),16(3.1%)
磷:16 (100%)
硫:16 (95%),18 (4.2%)
氯:18(75.8%),20(24.2%)
氩:20 (99.6%)
钾:20 (93.3),22(6.7%)
钙:20 (96.9%),24 (2.1%)1年前查看全部
- 1.已知一种碳原子(质子数,中子数均为6)的一个原子的质量为mg.铁原子的相对原子质量为n,则一个铁原子的质量为多少?
 白色小窗1年前1
白色小窗1年前1 -
 m3m3m 共回答了19个问题
m3m3m 共回答了19个问题 |采纳率84.2%根据公式n=m/M,由题意,该碳原子的相对原子质量为12,则一个该原子的物质的量为n=m/12,一个铁原子的物质的量大小等于一个碳原子的物质的量,则一个铁原子的质量应为,m'=n*M'=mn/121年前查看全部
- 据报道,科学家发现一种新元素,它的原子核质子数为111个,中子数为161个,则该元素的原子核外电子数是( )
据报道,科学家发现一种新元素,它的原子核质子数为111个,中子数为161个,则该元素的原子核外电子数是( )
A. 111
B. 161
C. 272
D. 50 星子逍遥1年前1
星子逍遥1年前1 -
 记忆深处_1013 共回答了18个问题
记忆深处_1013 共回答了18个问题 |采纳率94.4%解题思路:根据“核内质子数=核外电子数”,由题意“某元素原子核内有质子111个,中子161个”.则可推测该元素原子的核外电子数.由题意“某元素原子核内有质子111个,中子161个”.根据核内质子数=核外电子数=111,则可推测该元素原子的核外电子数为111.
故选A.点评:
本题考点: 原子的有关数量计算.
考点点评: 了解原子的定义和构成:原子由原子核和核外电子构成,其中原子核由质子和中子构成的1年前查看全部
- 质量相同的H2O与D2O所含质子数之比____,中子数之比____,分别与足量的Na反应生成的气体在同温同压下的体积之比
质量相同的H2O与D2O所含质子数之比____,中子数之比____,分别与足量的Na反应生成的气体在同温同压下的体积之比____.
 清瞳11191年前1
清瞳11191年前1 -
 refregr 共回答了15个问题
refregr 共回答了15个问题 |采纳率93.3%假设都是20g
H2O为10/9mol D2O为1mol 质子数都是10 中子数H2O 8个 D2O 10个
质量相同的H2O与D2O所含质子数之比 10:9
中子数之比8:9
分别与足量的Na反应生成的气体在同温同压下的体积之比10:9
H2O--0.5H2 D2O---0.5D2
10/18 0.51年前查看全部
- 质子数和中子数还有电子数怎么看?
 梦幻依度1年前1
梦幻依度1年前1 -
 因为我漂亮呗 共回答了20个问题
因为我漂亮呗 共回答了20个问题 |采纳率90%同一元素质子数=电子数=原子系数(查元素周期表)
中子数大于等于质子数,且不唯一,具体上网查1年前查看全部
- 已知,n个银原子的质量为mkg,质子数为6,中子数为6的a个碳原子的质量为bkg,则银原子的相对原子质量为:
已知,n个银原子的质量为mkg,质子数为6,中子数为6的a个碳原子的质量为bkg,则银原子的相对原子质量为:
A.12am/bn B.am/12bm C.12bm/am D.bn/12am 尼小采1年前2
尼小采1年前2 -
 lio0jyc 共回答了11个问题
lio0jyc 共回答了11个问题 |采纳率81.8%答案C打错了吧,应该是12mb/na
理由:相对原子质量为一个原子的质量与质子数为6,中子数为6的碳原子质量的1/12之比
一个银原子的质量为m/n 一个质子数为6,中子数为6的碳原子的质量的1/12为b/12a
则银原子的相对原子质量为m/n:b/12a
最后推出得12mb/na1年前查看全部
- 某原子的质子数为26,中子数比质子数多4,则该原子中粒子总数为______.
 颠机1年前3
颠机1年前3 -
 我是你的圈圈 共回答了19个问题
我是你的圈圈 共回答了19个问题 |采纳率100%解题思路:依据原子中质子数等于电子数结合原子的内部结构分析解答即可;由于原子中质子数等于电子数,所以该原子核外的电子数为26,而中子数比质子数多4,所以中子数为26+4=30,则该原子中粒子总数为质子数+中子数+电子数=26+30+26=82;
故答案为:82点评:
本题考点: 原子的有关数量计算.
考点点评: 主要考查了原子的结构中质子,中子,电子之间的关系.掌握原子的核内质子数和核外电子数相等是解题的关键.1年前查看全部
- 高一化学. 核内中子数为N的R2+,质量数位A,则ng它的同价态氧化物中所含电子物质的量是多少?求详解
 到成真1年前3
到成真1年前3 -
 冰封王子 共回答了17个问题
冰封王子 共回答了17个问题 |采纳率88.2%中子数为N,质量数位A,则质子数 = A-N
因为R2+带两个单位正电荷,所以R2+的电子数 = A-N-2
氧化物是RO,1mol氧化物含有电子 = A-N+8 mol,RO相对分子质量 = A+16
所以ng它的同价态氧化物中所含电子物质的量 = n/(A+16) * (A-N+8) = n*(A-N+8)/(A+16)1年前查看全部
- 某元素R的一种单质分子中含有四个原子,该单质的气体的密度折算到标准状况下为5.71克每升,已知R原子中质子数等于中子数.
某元素R的一种单质分子中含有四个原子,该单质的气体的密度折算到标准状况下为5.71克每升,已知R原子中质子数等于中子数.
1.求R的质子数和相对原子质量 2.求R的气态氢化物与最高价氧化物在同温同压下的相对密度 3.求R的最高价氧化物对应水化物的浓溶液与R的气态氢化物之间发生氧化还原反应时,被氧化与被还原的元素的质量比 那年的雨夜1年前2
那年的雨夜1年前2 -
 fanyunxiaoyuer 共回答了16个问题
fanyunxiaoyuer 共回答了16个问题 |采纳率100%标况密度为 5.71*22.4=128
相对原子量为128/4=32
质子数16
即为S
浓硫酸与硫化氢反应 H2S+H2SO4=S↓+SO2↑+2H20
被氧化:被还原=1:11年前查看全部
- 核内中子数为N的R2+,质量数为A,则ng它的氧化物中所含质子的物质的量是( )
核内中子数为N的R2+,质量数为A,则ng它的氧化物中所含质子的物质的量是( )
A.
mol(A-N+8)n (A+16)
B.
mol(A-N+10)n (A+16)
C.
mol(A-N+8)n A
D. (A-N+2)mol 长白云1年前3
长白云1年前3 -
 彼岸小乔 共回答了16个问题
彼岸小乔 共回答了16个问题 |采纳率93.8%解题思路:该离子的质子数=A-N,根据化合物中化合价的代数和为0知,该氧化物的化学式为RO,一个RO中质子数是A-N+8,先计算氧化物的物质的量,再根据质子的物质的量.该离子的质子数=A-N,一个RO中质子数是A-N+8,该氧化物的物质的量=[n/A+16mol,
则ng它的氧化物中所含质子的物质的量=
n
A+16mol×(A-N+8)=
(A-N+8)n
A+16]mol,
故选A.点评:
本题考点: 质量数与质子数、中子数之间的相互关系.
考点点评: 本题考查了物质的量的有关计算,明确“数值上,原子的相对原子质量等于其质量数“是解本题的关键,难度不大.1年前查看全部
- x元素原子核内质子数35,它有中子数为46和44同位素,x相对原子质量79.9,中子数为44的原子在x元素中所占的物质的
x元素原子核内质子数35,它有中子数为46和44同位素,x相对原子质量79.9,中子数为44的原子在x元素中所占的物质的量分数为
 yaya_0551年前1
yaya_0551年前1 -
 niliwei 共回答了23个问题
niliwei 共回答了23个问题 |采纳率100%X元素的两种同位素的相对原子质量分别为81和79
设中子数为44的原子在x元素中所占的物质的量分数为a,那么中子数为46的原子在x元素中所占的物质的量分数为1-a
81a+79(1-a)=79.9
解得a=45%1年前查看全部
- 原子中质子数一定等于( )核电核数 B:最小层电子数 C:中子数 D:中子数与电子数之和
 xtwzljz1年前3
xtwzljz1年前3 -
 好慧儿 共回答了20个问题
好慧儿 共回答了20个问题 |采纳率90%A:核电核数1年前查看全部
- 质子数 中子数 电子数 离子数 电荷数 之间的关系
 走夜路不怕鬼3号1年前1
走夜路不怕鬼3号1年前1 -
 diy120110 共回答了17个问题
diy120110 共回答了17个问题 |采纳率94.1%质子数=电子数=电荷数 中子数与质子数,电子数,电荷数没有必然联系 离子数指的是离子的数目
化学键与元素的性质有关,即与最外层电子数有关1年前查看全部
- 已知n(H2O)=2mol,求质子数,中子数
 flylok1年前2
flylok1年前2 -
 舞动泪珠 共回答了17个问题
舞动泪珠 共回答了17个问题 |采纳率94.1%质子数就是几号元素相加.H 1号元素,1个质子,O 8号元素,8个质子.
所以1个H2O中有1*2+8=10个质子.则2molH2O中就有2*10=20mol 个数为20NA(20*6.02*10^23)
高一刚学,中子数一般是相对分子质量减去质子数就是中子数了.
H2O的分子量18,质子数10,所以中子数8个(注意以后会不一样)
所以2molH2O中有16mol中子,个数16NA1年前查看全部
- 核内中子数为N的R+2,质量数为A,则ng它的同价态氧化物中的电子物质的量是多少
 kissxiaoxue1年前2
kissxiaoxue1年前2 -
 quickn 共回答了19个问题
quickn 共回答了19个问题 |采纳率100%(R)2+质量数为A,电子质量相对于质子和中子可以忽略,所以R质量数也为A
所以R的质子数Z(R)= A - N = R原子核外电子数
(R)2+为+2价,所以氧化物为RO(氧原子核外有8个电子,电子数= A - N + 8)
RO的质量数 = A + 16 (数值上等于它的摩尔质量数)
即1摩尔RO中电子物质的量 =(A - N + 8)mol
所以ngRO(物质的量为n/(A + 16))中电子物质的量 =(A - N + 8)*n/(A + 16)mol1年前查看全部
- 相对原子质量=质子数+中子数,为什么不是核外电子数+中子数,好像和什么离子有关吧,
 御剑流1年前1
御剑流1年前1 -
 我的阴暗无可救药 共回答了14个问题
我的阴暗无可救药 共回答了14个问题 |采纳率92.9%原子的核外电子数=质子数
但原子变成离子时会失去或得到电子,此时核外电子数≠质子数
即此时相对原子质量=质子数+中子数,不是核外电子数+中子数1年前查看全部
- 下列说法中正确的是( )A.所有的原子核内质子数都比中子数多B.氢离子(H+)实质上是一个裸露的质子C.核外电子排布相
下列说法中正确的是( )
A.所有的原子核内质子数都比中子数多
B.氢离子(H+)实质上是一个裸露的质子
C.核外电子排布相同的微粒,其化学性质也相同
D.非金属元素原子最外层电子数都大于4 17泡妞王1年前1
17泡妞王1年前1 -
 司马夏草 共回答了16个问题
司马夏草 共回答了16个问题 |采纳率93.8%解题思路:A.质子数与中子数无关;
B.氢原子失去一个电子形成氢离子;
C.核外电子排布相同的粒子,化学性质不一定相同;
D.氢原子最外层电子数为1.A.D中质子数=中子数,T中质子数小于中子数,故A错误;
B.氢原子失去一个电子剩余一个质子形成氢离子,故B正确;
C.核外电子排布相同的粒子,化学性质不一定相同,如Na+和OH-,故C错误;
D.氢原子最外层电子数为1,小于4,故D错误.
故选B.点评:
本题考点: 质子数、中子数、核外电子数及其相互联系;原子核外电子排布.
考点点评: 本题考查原子结构、质子数、中子数、核外电子数及其相互联系,题目难度不大,学习中注意相关基础知识的积累.1年前查看全部
- ★先看大题图:1)质子数与中子数不相等的核素有__________________;互称同位素的核素有_________
★先看大题图:

1)质子数与中子数不相等的核素有__________________;互称同位素的核素有___________________.
中子数相等的不同元素的原子是_________________.
2)现有10.0g由
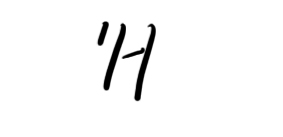
和

组成的水分子的物质的量为________;其中含质子数为________NA;中子数为_______________个.
3)由

和

构成的CO2摩尔质量为______________.标准状况下9.2g这种CO2所占有的体积约为_______________. 雪花美人1年前1
雪花美人1年前1 -
 Shabl 共回答了19个问题
Shabl 共回答了19个问题 |采纳率84.2%h1 c14 o18;hi&h2;o16&o18
0.2,2,2na
50,0.184*22.41年前查看全部
- 紫薯中含有被誉为“抗癌大王”的硒元素.已知硒元素的电荷数为34,中子数为45,则硒原子的核外电子数为( )
紫薯中含有被誉为“抗癌大王”的硒元素.已知硒元素的电荷数为34,中子数为45,则硒原子的核外电子数为( )
A.10
B.34
C.44
D.78 莲花手1年前1
莲花手1年前1 -
 007wxh 共回答了18个问题
007wxh 共回答了18个问题 |采纳率94.4%解题思路:根据原子中:核电荷数=核内质子数=核外电子数,结合题意进行分析解答.因为原子中:核电荷数=核内质子数=核外电子数,由题意已知硒元素的电荷数为34,故其核外电子数为34.
故选:B.点评:
本题考点: 原子的有关数量计算.
考点点评: 本题难度不大,解题的关键是掌握并灵活运用原子中核电荷数=核内质子数=核外电子数.1年前查看全部
- 下列叙述正确的是① 7 Li + 中含有的中子数与电子数之比为2︰1② 在C 2 H 6 分子中极性共价键与非极性共价键
下列叙述正确的是
① 7 Li + 中含有的中子数与电子数之比为2︰1
② 在C 2 H 6 分子中极性共价键与非极性共价键数之比为3︰1
③ 常温下,11.2 L的甲烷气体中含有的氢、碳原子数之比为4︰1
④5.6 g铁与足量的氯气反应失去的电子与参与反应的铁的物质的量之比为2︰1A.①② B.②③ C.①③ D.③④  baijianqianbei1年前1
baijianqianbei1年前1 -
 ening472 共回答了22个问题
ening472 共回答了22个问题 |采纳率68.2%C
1年前查看全部
- 某元素原子的质量数为A,它的阴离子Xn-核外有x个电子,w克这种元素的原子核内中子数为( )
某元素原子的质量数为A,它的阴离子Xn-核外有x个电子,w克这种元素的原子核内中子数为( )
A.
molw(A−x+n) A
B.
molw(A+x−n) A
C.
molA(A−x+n) W
D.
molA(A−x−n) A  天之恋1年前1
天之恋1年前1 -
 琦琪哈鱼 共回答了15个问题
琦琪哈鱼 共回答了15个问题 |采纳率93.3%解题思路:先利用n=[m/M]计算原子的物质的量,再由阴离子中质子数=核外电子数-电荷数求出质子数,最后利用质子数与中子数之和等于质量数来计算中子数;w克这种元素的原子的物质的量为[w/A]mol,阴离子Xn-核外有x个电子,则质子数为x-n,中子数为A-(x-n)=A-x+n,则w克这种元素的原子核内中子数为[w/A]mol×(A-x+n)=
w(A−x+n)
A;
故选:A.点评:
本题考点: 质量数与质子数、中子数之间的相互关系.
考点点评: 本题考查学生利用原子构成的简单计算,明确原子的物质的量的计算是解答本题的关键,注意质量数在数值上等于摩尔质量.1年前查看全部
- 有四种元素,其核电荷数均小于20,A能形成氧化物AO,AO中A元素占60%,且A中质子数等于中子数;B元素原子核内没有中
有四种元素,其核电荷数均小于20,A能形成氧化物AO,AO中A元素占60%,且A中质子数等于中子数;B元素原子核内没有中子;C原子和D - 都比B原子多17个电子.
(1)写出各元素的符号:A______、B______、C______、D______.
(2)A、D两元素形成的化合物的化学式为______,B、D两元素形成的化合物的化学式为______. fhazi_O1年前1
fhazi_O1年前1 -
 bobomwl 共回答了15个问题
bobomwl 共回答了15个问题 |采纳率93.3%(1):已知“A能形成氧化物AO,则A的化合价为+2价目,A原子最外层有两个电子,A的核电荷数小于20,A的质量分数为60%,则60%=
Ar(A)
Ar(A)+16 ×100%,Ar(A)=24,A元素原子核内质子数等于中子数”,因为相对原子质量=质子数+中子数,故质子数为12,A为镁元素,由“B元素原子内无中子”则B为氢元素,由“C原子和D - 都比B原子多17个电子”则C为氩元素,D为氯元素;
(2)四种元素两两组合,形成的化合物为MgCl 2 ,HCl
故答案为:(1)Mg、H、Ar、Cl (2)MgCl 2 、HCl1年前查看全部
- A,B分别为3周期和4周期的同一主族的不同元素的原子,原子核内质子数等于中子数.(1)若A为二主族元素原子
 秀哉1年前2
秀哉1年前2 -
 泉州之水 共回答了17个问题
泉州之水 共回答了17个问题 |采纳率88.2%1.A是镁,x=24,B是钙,y=20 2.A是硅,m=14,B是锗(Ge),n=64选C 1个氘原子(D)中子数有1个,1个He原子种子数有2个 等物质的量时,1个D2分子有2个,1个He有2个 所以D2中子数>4He中子数 选B Na2O2 阳离子2个Na+,阴离子有1个...1年前查看全部
- A原子的质量是5.146*负26次方kg,若A原子核内质子数比中子数少一个求A原子的相对原子质量和他的核外电子数
 如何能将一切归零1年前2
如何能将一切归零1年前2 -
 a020911 共回答了23个问题
a020911 共回答了23个问题 |采纳率91.3%相对原子质量=原子质量/(1.6606×10-27)
=5.146*10-26/(1.6606×10-27)
约等于31
P的相对原子质量也是31,所以核外电子数为15
或者设质子数为X
得2X+1=31 得X=15
祝愿您学业进步.1年前查看全部
- 完成下列表格,并根据表格填空:原子种类质子数中子数核外电子数相对原子质量氢10____________碳______66
完成下列表格,并根据表格填空:
通过表格,你可以获得哪些信息:(至少写三点)原子种类 质子数 中子数 核外电子数 相对原子质量 氢 1 0 ______ ______ 碳 ______ 6 6 ______ 氯 ______ ______ 17 35
(1)______;
(2)______;
(3)______. mimosa211年前1
mimosa211年前1 -
 风露1清愁 共回答了17个问题
风露1清愁 共回答了17个问题 |采纳率94.1%解题思路:根据:质子数=电子数、相对原子质量=质子数+中子数,将表格所缺内容填好,再通过观察数据找出规律性的东西,并能灵活运用.填好表格内容后,通过观察表格中的数据,得到了以下启示:在原子中质子数=电子数=核电荷数,相对原子质量=质子数+中子数,不同元素质子数不同,原子内质子数不一定等于中子数,有的原子的原子核中没有中子,但一定有质子.
故答案为:
原子种类质子数中子数核外电子数相对原子质量
氢1011
碳66612
氯17181735(1)在原子中质子数等于电子数;
(2)质子数和中子数可能相同,也可能不相同;
(3)相对原子质量=质子数+中子数;(不同种类的原子,质子数不同等).点评:
本题考点: 原子的定义与构成.
考点点评: 通过回答本题知道了在原子里:质子数=电子数=核电荷数;不同种类的原子,质子数不同;相对原子质量=质子数+中子数.1年前查看全部
- 铜有两种天然同位素:质量数为63,中子数为29的铜和质量数为65,中子数为29的铜.则质量数为65的铜的质量分数约为?
 Rochawi剑1年前1
Rochawi剑1年前1 -
 清青123456 共回答了16个问题
清青123456 共回答了16个问题 |采纳率93.8%设63的铜x,65铜为1-x
63*x+65(1-x)=铜相对原子质量
求x
您的题目不完整
欢迎追问~1年前查看全部
- 原子中,质子数=中子数+电子数吗?
 jiangshanru1年前2
jiangshanru1年前2 -
 zhzejun2007 共回答了22个问题
zhzejun2007 共回答了22个问题 |采纳率81.8%质子数 = 电子数
因为每个质子带一个单位的正电荷,而每个电子带一个单位的负电荷
对于原子来说,原子是中性的,所以正电荷 和负电荷的数目应该相等才对
中子是不带电的,所以跟它没关系
离子跟原子不同,离子是整体显电性的,所以对于离子来说,质子和电子不相等
当然.你这里说的是原子,所以:质子数=电子数1年前查看全部
- 氯化钠是由钠离子和氯离子构成的已知钠离子的原子核中质子数11,中子数为12下列有关钠离子的说法正确的是( )
氯化钠是由钠离子和氯离子构成的已知钠离子的原子核中质子数11,中子数为12下列有关钠离子的说法正确的是( )
A. 原子核外电子数为11
B. 它的相对原子质量和钠原子的相同
C. 原子核内的正电荷数为+10
D. 原子核外电子数为12 linagca1年前3
linagca1年前3 -
 wuway 共回答了27个问题
wuway 共回答了27个问题 |采纳率92.6%解题思路:A、根据钠离子是钠原子失去1个电子后形成的进行解答;
B、根据相对原子质量=质子数+中子数进行解答;
C、根据原子核内的正电荷数与质子数相同进行解答;
D、根据钠离子是钠原子失去1个电子后形成的进行解答.A、钠离子是钠原子失去1个电子后形成的,钠原子的核外电子数为11,所以钠离子核外电子数为10,故A错误;
B、相对原子质量=质子数+中子数,钠原子和钠离子中质子数和中子数相同,所以钠离子的相对原子质量和钠原子的相同,故B正确;
C、原子核内的正电荷数与质子数相同,所以钠离子中原子核内的正电荷数为+11,故C错误;
D、钠离子是钠原子失去1个电子后形成的,钠原子的核外电子数为11,所以钠离子核外电子数为10,故D错误.
故选:B.点评:
本题考点: 原子和离子的相互转化.
考点点评: 本题难度不大,解题的关键是掌握原子中核电荷数=质子数=电子数、相对原子质量=质子数+中子数.1年前查看全部
- 钠离子Na+原子核中质子数11,中子数12,那下面那个是对的 A原子核外电子数为11 B它的相对原
钠离子Na+原子核中质子数11,中子数12,那下面那个是对的 A原子核外电子数为11 B它的相对原
钠离子Na+原子核中质子数11,中子数12,那下面那个是对的
A原子核外电子数为11
B它的相对原子质量与钠原子相同
C原子核内正电荷数为+10
D原子核外电子数为12
说出原因, KingKong01年前2
KingKong01年前2 -
 01016 共回答了22个问题
01016 共回答了22个问题 |采纳率86.4%选B
对于原子质子数=核电荷数=核外电子数,对于Na+离子核外电子数比钠原子少一即为10个,AD不对;对于原子核的正电荷数不变还是11,C不对;B项相对原子质量都是11+12=231年前查看全部
- A、B、C三种元素的原子核里都有几个质子,中子数分别为n-1,n,n+1,下列说法正确的是( )(说理由)
A、B、C三种元素的原子核里都有几个质子,中子数分别为n-1,n,n+1,下列说法正确的是( )(说理由)
A、它们属于同种元素
B、它们是同一种原子
C、它们是不同元素的微粒
D、它们是不同种分子 joogger1年前1
joogger1年前1 -
 sevening 共回答了15个问题
sevening 共回答了15个问题 |采纳率100%应该是都有一样的质子数吧?
首先质子数相同就表示他们是同一种元素的原子,元素的分类就是按原子核里的质子数分,A是对的
B不对,同一种原子必须质子数和中子数一样
C,不对,他们是同一元素的微粒
D,这个,错的啦……
所以选A1年前查看全部
- 下列化学用语正确的是( )A.铝离子的结构示意图:B.CH3CH2Br中的官能团:Br-C.中子数为20的氯原子:17
下列化学用语正确的是( )
A.铝离子的结构示意图: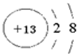
B.CH3CH2Br中的官能团:Br-
C.中子数为20的氯原子:1720Cl
D.CO2的比例模型:
 ww的鱼1年前1
ww的鱼1年前1 -
 月蓝宫人 共回答了24个问题
月蓝宫人 共回答了24个问题 |采纳率91.7%解题思路:A、铝离子的核电荷数为13,核外电子数为10;B、溴乙烷的官能团为溴原子,表示溴离子,其官能团正确表示应该为-Br;C、原子的左上角表示的是质量数,中子数为20的氯原子的质量数为37;D、二氧化碳分子中碳原子的原子半径应该大于氧原子的原子半径.A、铝离子核外电子数为10,铝离子的结构示意图为:
 ,故A正确;
,故A正确;
B、CH3CH2Br中的官能团为溴原子,其官能团表示为:-Br,故B错误;
C、中子数为20的氯原子,其质量数为37,该氯原子的正确表示为:1737Cl,故C错误;
D、二氧化碳分子中,碳原子原子比较大于氧原子的原子半径,则 ,故D错误;
,故D错误;
故选A.点评:
本题考点: 原子结构示意图;球棍模型与比例模型;烃的衍生物官能团.
考点点评: 本题考查了常见化学用语的正误判断,题目难度中等,该题是高考中的常见题型与重要的考点,该题基础性强,难易适中,主要是考查学生对常见化学用语的熟悉掌握程度,该类试题需要明确的是常见的化学用语主要包括元素符号、化学式、化合价、电子式、原子结构示意图、结构式、结构简式以及方程式和各种模型等,需要学生熟练记住.1年前查看全部
- 有关物质的量计算的问题已知Mg元素的核内中子数为12,求47.5克的MgCl2中所含质子的物质的量是多少?就是不知道“所
有关物质的量计算的问题
已知Mg元素的核内中子数为12,求47.5克的MgCl2中所含质子的物质的量是多少?
就是不知道“所含质子的物质的量”是什么意思,然后就无从下手了.
请附上分析、计算过程, 疯了20081年前3
疯了20081年前3 -
 SnowChen11 共回答了24个问题
SnowChen11 共回答了24个问题 |采纳率87.5%Cl的质子数为17
Mg的质子数为12
Cl的相对原子质量为35.5
Mg的相对原子质量为12+12=24
47.5克的MgCl2的物质的量为47.5/(24+35.5+35.5)
47.5克的MgCl2中所含质子的物质的量=47.5克的MgCl2的物质的量*(12+17+17)
只有分析,没有答案.嘿嘿1年前查看全部
- 氦原子核内的质子数为2,中子数为1,而相对原子质量为4?
氦原子核内的质子数为2,中子数为1,而相对原子质量为4?
周期表上为4,但相对原子质量=质子数+中子数, wang_1978狼1年前2
wang_1978狼1年前2 -
 wjdb0222 共回答了21个问题
wjdb0222 共回答了21个问题 |采纳率76.2%氦在自然界中存在两种同位素,氦3和氦4,氦3如你所说,相对原子质量为3,氦4质子2中子2相对原子质量为4.
周期表上的相对原子质量数为自然界各种同位素按含量求平均数.而自然界氦4含量远高于氦3,所以为4.
你看到的原子核内的质子数为2,中子数为1,应该是氦31年前查看全部
- 铀元素的平均相对原子质量为238.0289 它有三种同位素 238-92U 235-92U 234-92U,其中中子数为
铀元素的平均相对原子质量为238.0289 它有三种同位素 238-92U 235-92U 234-92U,其中中子数为146的同位素所占原子百分数应最接近于
A 99% B 50% C 10% D无法确定 转瞬即逝anni1年前1
转瞬即逝anni1年前1 -
 老--屋 共回答了16个问题
老--屋 共回答了16个问题 |采纳率81.3%铀的质子数为92,中子数为146,则质量数为238.三个同位素中的第一种.
平均相对原子质量=质量数1×原子百分数+质量数2×原子百分数+质量数3×原子百分数+……
这个只有三个,用三个就可以了.
238.0289=238×原子百分数+235×原子百分数+234×原子百分数
其实不用算,就可以看出来,为A.1年前查看全部
- 核电荷数是6 ,原子质量数是14 ,核内中子数是多少?
核电荷数是6 ,原子质量数是14 ,核内中子数是多少?
如题 wcxz1年前1
wcxz1年前1 -
 tokacyu1984 共回答了22个问题
tokacyu1984 共回答了22个问题 |采纳率100%14-6=81年前查看全部
- 在原子里,核电荷数等于A、核外电子总数B、中子数C、质子数D、相对原子质量
 哈哈kgl哈1年前2
哈哈kgl哈1年前2 -
 听风雨轩 共回答了12个问题
听风雨轩 共回答了12个问题 |采纳率100%相对原子质量是=质子数+中子数=B+C1年前查看全部
- 核内中子数为N的R2+,质量数为A责该离子的核外电子数为?(R2+指 R带有2个单位的正电荷)
核内中子数为N的R2+,质量数为A责该离子的核外电子数为?(R2+指 R带有2个单位的正电荷)
求具体过程 庆祝新楼1年前1
庆祝新楼1年前1 -
 gymm 共回答了17个问题
gymm 共回答了17个问题 |采纳率94.1%中子数为N 质量数为A 质子数为A-N 对于原子,质子数等于核外电子数,现在变成+2价离子,是失去了两个电子,所以,电子数为A-N-21年前查看全部
- 原子质量定义为质子数加上中子数岂不是更容易理解,为什么非要用碳来作为标准?
 含笑幽灵1年前1
含笑幽灵1年前1 -
 30岁东北女不怕烂 共回答了23个问题
30岁东北女不怕烂 共回答了23个问题 |采纳率78.3%质子和中子质量是不一定的,会有点小小的差别,这就是核反应(聚变和裂变)会放出能量的原因.距离来说,氘核1中子1质子,2个氘核聚变成一个氦核,2中子2质子,但质量会有微小损失,变成巨大能量放出了.1年前查看全部
- 同位素就是质子数相同中子数不同的原子 这话哪错了?
 chenyuanchi1101年前3
chenyuanchi1101年前3 -
 若是偶然 共回答了19个问题
若是偶然 共回答了19个问题 |采纳率89.5%科技名词定义
中文名称:同位素 英文名称:isotope 定义1:具有相同原子序数(即质子数相同,因而在元素周期表中的位置相同),但质量数不同,亦即中子数不同的一组核素.所属学科:电力(一级学科);核电(二级学科) 定义2:中子数不同的同一种元素的一种原子形式,包括稳定同位素和放射性同位素.所属学科:生态学(一级学科);全球生态学(二级学科)1年前查看全部
- 磷元素在空气中自燃,其原子核中的质子数和中子数怎么变化
 zhou_3ss1年前3
zhou_3ss1年前3 -
 我也来一泡 共回答了22个问题
我也来一泡 共回答了22个问题 |采纳率86.4%化学变化中,是分子分成了原子,原子没有再分,而是重新组合形成新的分子,所以在化学变化中,原子没有变化,所以原子核里的中子和质子也不可能发生变化.磷在空气中燃烧时与空气中的氧气发生反应,磷原子与氧原子通过公用电子对,重新组合成五氧化二磷分子,原子核里的质子和中子都没有变化.
4P +5O2 点燃 2P2O51年前查看全部
大家在问
- 1有谁知道英语单词"古筝"英语单词怎么拼?
- 2Time怎么用?good times 为什么要加s呢 不是表示时间不可数吗?
- 3设U=R,A={x∣x小于等于1},B=[X∣X大于a+1},且CuA是B的子集,求a的范围
- 4詹姆斯卡梅隆的名言英文原文如果你设定了一个几乎无法企及的目标但最终失败了你的失败依然比他人的成功高明
- 5(语文问题)形容一句话放在文章里很不合适,就是说显得很唐突,很怪,这应该用什么词语
- 623点之前
- 7生活中的透镜 知识结构
- 8巴金、沈从文、老舍、钱钟书文笔比较
- 9一定量的氢气在氯气中燃烧,所得混合物冷却后用500mL 0.6mol•L-1的NaOH溶液恰好完全吸收,测得溶液中含有N
- 10给加线字注音,根据拼音写汉字。
- 11急.如图一个重为G的小环套在坚直放置的半径为R 的光滑大圆环上
- 12请问1+1=?感谢昨晚给我发东西的朋友~
- 13画出函数y=2x+6的图像,利用图像(1)求方程2X+6=0的解(2)求直线y=2x+6在x轴上方所对应x的取值(3)若
- 14一件衣服现价136元,比原来降低了15%.原来售价多少元?
- 15在一定温度和压强下,5体积A2与15体积B2化合生成10体积C(都是气体).则C的化学式为?
