超细玻璃纤维 密度求超细玻璃纤维密度~知道的大侠给个答案~thanks
 frankzhang932022-10-04 11:39:542条回答
frankzhang932022-10-04 11:39:542条回答
已提交,审核后显示!提交回复
共2条回复
 ltiande 共回答了24个问题
ltiande 共回答了24个问题 |采纳率91.7%- 3.1415926
- 1年前
 hnyxwxj 共回答了2个问题
hnyxwxj 共回答了2个问题 |采纳率- 这能信吗?这不是圆周率吗?有点疑惑
- 1年前
相关推荐
- (2013•周口一模)超细的铁微粒是一种纳米颗粒型材料,可在低温下将CO2分解为炭.下列推测不合理的( )
(2013•周口一模)超细的铁微粒是一种纳米颗粒型材料,可在低温下将CO2分解为炭.下列推测不合理的( )
A.超细铁微粒在反应中可能做催化剂
B.该反应有助于减少温室气体排放
C.该反应的另一产物可能是O2
D.该反应属于化合反应 yangliangel1年前1
yangliangel1年前1 -
 weisb_2002 共回答了28个问题
weisb_2002 共回答了28个问题 |采纳率89.3%解题思路:根据题干提供的信息进行分析,二氧化碳在超细铁微粒的作用下能在低温下分解生成碳,根据质量守恒定律,化学反应前后元素的种类不变,故另一种物质可能是氧气,该反应是一个分解反应,能减少二氧化碳的排放,超细铁微粒可能是催化剂.A、二氧化碳在超细铁微粒的作用下能在低温下分解生成碳,超细铁微粒可能是催化剂,故A正确;
B、该反应时二氧化碳分解生成了碳,能减少空气中二氧化碳的排放,故B正确;
C、根据质量守恒定律,化学反应前后元素的种类不变,故另一种物质可能是氧气,故C正确;
D、该反应是一种物质参加反应,不可能是化合反应,故D错误;
故选D.点评:
本题考点: 二氧化碳对环境的影响;反应类型的判定;质量守恒定律及其应用.
考点点评: 本题考查了二氧化碳的转化,完成此题,可以依据题干提供的信息进行.1年前查看全部
- 超细铜粉主要应用于导电材料、催化剂等领域中.超细铜粉的某制备方法如下:
超细铜粉主要应用于导电材料、催化剂等领域中.超细铜粉的某制备方法如下: 
试回答下列问题:
(1)下列关于[Cu(NH 3 ) 4 ]SO 4 的说法中,正确的有______.(填字母序号)
A.[Cu(NH 3 ) 4 ]SO 4 中所含的化学键有离子键、极性键和配位键
B.[Cu(NH 3 ) 4 ]SO 4 含有NH 3 分子,其水溶液中也含有NH 3 分子
C.[Cu(NH 3 ) 4 ]SO 4 的组成元素中第一电离能最大的是氧元素
D.[Cu(NH 3 ) 4 ]SO 4 的外界离子的空间构型为正四面体
(2)NH 4 CuSO 3 中的金属阳离子的核外电子排布式为:______.
(3)SO
离子中S硫原子的杂化方式为______,与其互为等电子体的一种分子的分子式是______.2-3
(4)NH 3 易液化的原因是______.
(5)如图是铜的某种氧化物的晶胞结构示意图,由此可确定该氧化物的化学式为______.
(6)NH 4 CuSO 3 与硫酸微热时除得到超细铜粉外,还可看到溶液变蓝,同时有使品红褪色的气体.则该反应的离子方程式为______.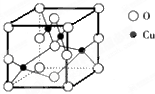
 呵呵15号1年前1
呵呵15号1年前1 -
 岩冰 共回答了15个问题
岩冰 共回答了15个问题 |采纳率93.3%(1)A.[Cu(NH 3 ) 4 ]SO 4 中硫酸根离子和[Cu(NH 3 ) 4 ] 2+ 存在离子键,N原子和铜原子之间存在配位键,NH 3 中H和N之间存在共价键,所以[Cu(NH 3 ) 4 ]SO 4 中所含的化学键有共价键、离子键、配位键,故A正确;
B.NH 3 为配体分子,溶液中不存在NH 3 ,故B错误;
C..元素周期律中,同一周期元素的第一电离能随着原子序数的增大而增大,但N原子最外层达到半饱和的稳定结构,难以失去电子,所以其第一电离能大小为N>O,故C错误
D.SO 4 2- 离子中价层电子对数为4+
1
2 ×(6+2-4×2)=4,孤电子对数为0,所以是正四面体体型,故D正确.
故答案为:AD.
(2)Cu原子的核外电子排布式为[Ar]3d 10 4s 1 ,NH 4 CuSO 3 中Cu的化合价为+1价,则金属阳离子的核外电子排布式为
[Ar]3d 10 ,故答案为[Ar]3d 10 :
(3)SO 3 2- 中含有3个δ键和1个孤电子对,故为sp 3 杂化,离子含有4的原子,价电子总数为26,对应的等电子体有NF 3 (或PF 3 、NCl 3 、PCl 3 等),故答案为:sp 3 ;NF 3 (或PF 3 、NCl 3 、PCl 3 等);
(4)N元素的非金属性较强,对应的氢化物中含有氢键,沸点较高,易液化,故答案为:NH 3 分子间可形成氢键,
(5)晶胞中4个Cu位于晶胞内部,O位于晶胞的顶点和面心,共有8×
1
8 +6
1
2 =4,则该氧化物的化学式为CuO,
故答案为:CuO;
(6)除得到超细铜粉外,还可看到溶液变蓝,同时有使品红褪色的气体,说明生成Cu、Cu 2+ 和SO 2 ,反应的离子方程式为2NH 4 CuSO 3 +4H +
微热
.
2NH 4 + +Cu 2+ +Cu+2SO 2 ↑+2H 2 O,
故答案为:2NH 4 CuSO 3 +4H +
微热
.
2NH 4 + +Cu 2+ +Cu+2SO 2 ↑+2H 2 O.1年前查看全部
- 用特殊的方法把固体物质加工到纳米级的超细粉末粒子,然后制得纳米材料.下列分散系中分散质的微粒直径和这种粒子具有相同数量级
用特殊的方法把固体物质加工到纳米级的超细粉末粒子,然后制得纳米材料.下列分散系中分散质的微粒直径和这种粒子具有相同数量级的是( )
A. 溶液
B. 悬浊液
C. 胶体
D. 乳浊液 紫色精灵2FSW1年前1
紫色精灵2FSW1年前1 -
 擦网而过 共回答了24个问题
擦网而过 共回答了24个问题 |采纳率87.5%解题思路:根据溶液、胶体、浊液微粒的直径判断,胶体微粒的直径为1-100nm之间.溶液的微粒直径为小于1nm,浊液的微粒直径大于100nm,胶体微粒的直径为1-100nm之间,把固体物质加工到纳米级的超细粉末粒子,与胶体的微粒直径相当,
故选C.点评:
本题考点: 分散系、胶体与溶液的概念及关系.
考点点评: 本题以纳米材料为载体考查了胶体微粒的本质特征,注意把握分散系分类的依据,题目难度不大,注意把握微粒直径大小的不同.1年前查看全部
- 纳米材料是21世纪最有前途的新型材料之一,世界各国对这一新材料给予了极大的关注。纳米粒子是指直径为1~100 nm的超细
纳米材料是21世纪最有前途的新型材料之一,世界各国对这一新材料给予了极大的关注。纳米粒子是指直径为1~100 nm的超细粒子(1 nm=10 -9 m)。由于表面效应和体积效应,其常有奇特的光、电、磁、热等性能,可开发为新型功能材料,有关纳米粒子的叙述不正确的是()。
A.因纳米粒子半径太小,故不能将其制成胶体 B.一定条件下纳米粒子可催化水的分解 C.一定条件下,纳米陶瓷可发生任意弯曲,可塑性好 D.纳米粒子半径小,表面活性高  silencegreen1年前1
silencegreen1年前1 -
 江伯牙 共回答了16个问题
江伯牙 共回答了16个问题 |采纳率93.8%A
题中涉及纳米材料这一新型材料,根据纳米粒子微粒大小,判断出其分散质粒子大小刚好处在胶体分散质大小的范围内,因此我们要结合胶体知识,并紧密联系题干中的有关知识分析、讨论。1年前查看全部
- 我以前没用过硫酸钡,现在有需要这个硫酸钡,不知是沉淀的好还是超细的好,还有外墙可不不以用,请指教
我以前没用过硫酸钡,现在有需要这个硫酸钡,不知是沉淀的好还是超细的好,还有外墙可不不以用,请指教
还有还有它的稳定性,比如说贮存中结块,分层等之类问题。 朝下游泳的鱼1年前1
朝下游泳的鱼1年前1 -
 爱已触礁 共回答了15个问题
爱已触礁 共回答了15个问题 |采纳率80%沉淀是悬浮物,是会溶于水的超细小颗粒,要是水的溶解性好的话是可以溶解的1年前查看全部
- 定性滤纸的最小孔径是多少?最近,做矿物的湿法超细实验,用到滤纸来分离和干燥样品,磨到几个微米不知道还能用滤纸分离不
 lf56861年前1
lf56861年前1 -
 wzr1001 共回答了21个问题
wzr1001 共回答了21个问题 |采纳率85.7%定性滤纸的孔径是不规律的,通常定性滤纸的孔隙大,定量的小.你可以试一下用定量滤纸,滤过速度的不同,孔径也不同.一般定性滤纸孔径大而且也没有很严格的规定.定量滤纸分为快速、中速和慢速三种,其孔径分别大约是80~120微米、30~50微米、和1~3微米.1年前查看全部
- 超细的铁微粒是一种纳米颗粒材料,可在低温下将二氧化碳分解为碳.推理不合理的说法是?
 就范1年前3
就范1年前3 -
 高山滚鼓 共回答了17个问题
高山滚鼓 共回答了17个问题 |采纳率100%没有选项,我们怎么来推理呢?请补充1年前查看全部
- 求这几个字体,答案全面者,方正小篆体方正宋刻本秀楷繁体方正平黑繁体方正兰亭超细黑方正字迹-邱氏粗瘦金书方正字迹-潇洒隶书
求这几个字体,答案全面者,
方正小篆体
方正宋刻本秀楷繁体
方正平黑繁体
方正兰亭超细黑
方正字迹-邱氏粗瘦金书
方正字迹-潇洒隶书繁体
方正宋刻本秀楷简体
方正品尚细黑简体
——————————————————————
我想要以上的八个字体,因为知道不好找,所以也不要求你都有.麻烦有里面字体的发送一下.谁发送得全面者采纳谁.发送一个也可采纳. 大良满屋浪漫1年前1
大良满屋浪漫1年前1 -
 fescen 共回答了24个问题
fescen 共回答了24个问题 |采纳率100%方正平黑繁体.ttf
方正字迹-邱氏粗瘦金书体.ttf
方正宋刻本秀楷简.TTF
方正兰亭超细黑简体.TTF
方正小篆体.ttf这5个现在上传!希望帮到你! 其他的如果有我也很高兴1年前查看全部
- 把固体物质加工到纳米级的超细粉末,即可得到纳米材料,这一过程是物理变化还是化学变化?
 490282811年前1
490282811年前1 -
 zq1977 共回答了14个问题
zq1977 共回答了14个问题 |采纳率100%物理变化,没生成新物质,分子没改变1年前查看全部
- 铁能在什么情况下做催化剂?超细的铁微粒可在低温下将CO2分解为炭.这个化学方程式怎么写?铁在反应中作
铁能在什么情况下做催化剂?超细的铁微粒可在低温下将CO2分解为炭.这个化学方程式怎么写?铁在反应中作
为什么 林尚沃821年前1
林尚沃821年前1 -
 maodan77 共回答了28个问题
maodan77 共回答了28个问题 |采纳率89.3%在苯与液态的卤素元素(氟除外)反应时,需要铁催化(FeX3也可以催化).8Fe+3CO2=3C+Fe4O31年前查看全部
- 超细玻璃纤维纸的特点是
 kk_20041年前1
kk_20041年前1 -
 秦先其 共回答了22个问题
秦先其 共回答了22个问题 |采纳率95.5%超细玻璃纤维纸除了纤维直径小、含有约(2-5)%的粗料和渣球外,并无其他杂质.不需要用水洗涤.超细玻璃纤维纸的碎裂性较大,在水中容易下沉.而且交织力较差.超细玻璃纤维纸的过滤效率是非常突出的,过滤效率为99.99995%.透过率是0.00005%.
希望能帮助到你^_^1年前查看全部
- 超细铜粉主要应用于导电材料、催化剂等领域中.超细铜粉的某制备方法如下:
超细铜粉主要应用于导电材料、催化剂等领域中.超细铜粉的某制备方法如下:

试回答下列问题:
(1)下列关于[Cu(NH3)4]SO4的说法中,正确的有______.(填字母序号)
A.[Cu(NH3)4]SO4中所含的化学键有离子键、极性键和配位键
B.[Cu(NH3)4]SO4含有NH3分子,其水溶液中也含有NH3分子
C.[Cu(NH3)4]SO4的组成元素中配体是NH3,N原子提供空轨道
D.[Cu(NH3)4]SO4的外界离子的空间构型为正四面体
(2)NH4CuSO3中的金属阳离子的简化核外电子排布式为______.
(3)向硫酸铜的溶液中逐滴滴入氨水溶液至过量可得到[Cu(NH3)4]SO4溶液,出现的现象是______,用反应的离子方程式为:______;______. 宴山亭061年前1
宴山亭061年前1 -
 xun3 共回答了23个问题
xun3 共回答了23个问题 |采纳率87%解题思路:(1)A.阴阳离子存在离子键,非金属元素间易形成共价键,配合物中存在配位键;
B.NH3为配体分子,溶液中不存在NH3;
C.根据配合物的组成及其概念来判断;
D.根据价层电子对互斥理论判断离子构型.
(2)NH4CuSO3中Cu的化合价为+1价,基态Cu+核外有28个电子,根据构造原理书写其核外电子排布式;
(3)先生成蓝色沉淀,后氢氧化铜溶解在氨水中生成络离子,得到深蓝色溶液.(1)A.[Cu(NH3)4]SO4中硫酸根离子和[Cu(NH3)4]2+存在离子键,N原子和铜原子之间存在配位键,NH3中H和N之间存在共价键,所以[Cu(NH3)4]SO4中所含的化学键有共价键、离子键、配位键,故A正确;
B.NH3为配体分子,溶液中不存在NH3,故B错误;
C.根据配合物的组成可以判断配体是NH3,但N原子是提高孤对电子,中心原子是提供空轨道,故C错误;
D.SO42-离子中价层电子对数为4+[1/2]×(6+2-4×2)=4,孤电子对数为0,所以是正四面体体型,故D正确.
故答案为:AD;
(2)Cu原子的核外电子排布式为[Ar]3d104s1,NH4CuSO3中Cu的化合价为+1价,基态Cu+核外有28个电子,根据构造原理金属阳离子的核外电子排布式为[Ar]3d10,
故答案为:[Ar]3d10;
(3)先生成蓝色沉淀,后氢氧化铜溶解在氨水中生成络离子,得到深蓝色溶液,发生Cu2++2NH3•H2O=Cu(OH)2↓+2NH4+,Cu(OH)2+4NH3•H2O=[Cu(NH3)4]2++2OH-+4H2O,
故答案为:形成蓝色沉淀,继续滴加氨水蓝色沉淀溶解,得到深蓝色溶液;Cu2++2NH3•H2O=Cu(OH)2↓+2NH4+;Cu(OH)2+4NH3•H2O=[Cu(NH3)4]2++2OH-+4H2O.点评:
本题考点: 铜金属及其重要化合物的主要性质;配合物的成键情况.
考点点评: 本题较为综合,突出考查配合物知识、核外电子排布、杂化类型、化学键、物质性质、配合物成键状况的了解,综合性较强,全面考查物质的结构和性质,题目难度较大.1年前查看全部
- 用特殊方法把固体物质加工到纳米级(1nm~100nm,1nm=10 —9m) 的超细粉末粒子,然后制得纳米材料。下列分散
用特殊方法把固体物质加工到纳米级(1nm~100nm,1nm=10 —9m) 的超细粉末粒子,然后制得纳米材料。下列分散系中的分散质的微粒直径和这种粒子具有相同数量级的是
A.溶液 B.胶体 C.悬浊液 D.乳浊液  涅确呢嘎1年前1
涅确呢嘎1年前1 -
 IA245731776 共回答了21个问题
IA245731776 共回答了21个问题 |采纳率90.5%B
1年前查看全部
- 雾霾天气,警惕PM2.5 污染①最近一段时间,随着媒体的关注,以PM2.5为代表的“超细灰尘”污染引起了人们的广泛关注。
雾霾天气,警惕pm2.5 污染
①最近一段时间,随着媒体的关注,以pm2.5为代表的“超细灰尘”污染引起了人们的广泛关注。那么,pm2.5是什么?它对人体健康有哪些危害?面对雾霾天气,我们应如何抵御pm2.5污染呢?
②pm2.5是指大气中直径小于或等于2.5微米的颗粒物,也称为可入肺颗粒物。 它的直径还不到人的头发丝粗细的1/20。 虽然pm2.5只是地球大气成分中含量很少的组成部分,但pm2.5粒径小,富含大量的有毒、有害物质,同时pm2.5在大气中的停留时间长、输送距离远,因而对人体健康和大气环境质量的影响更大。
④pm2.5“超细灰尘”主要来自机动车尾气尘、燃油尘、硫酸盐、餐饮油烟尘、建筑水泥尘、煤烟尘和硝酸盐等,它是雾霾有害细颗粒的重要组成部分。
⑤气象专家和医学专家认为,由细颗粒物造成的灰霾天气对人体健康的危害甚至要比沙尘暴更大。粒径10微米以上的颗粒物,会被挡在人的鼻子外面;粒径在2.5微米至10微米之间的颗粒物,能够进入上呼吸道,但部分可通过痰液等排出体外,也会被鼻腔内部的绒毛阻挡,对人体健康危害相对较小;而粒径在2.5微米以下的细颗粒物不易被阻挡,被吸入人体后会直接进入支气管,干扰肺部的气体交换,引发包括哮喘、支气管炎和心血管病等方面的疾病。
⑥人体的生理结构决定了对pm2.5没有任何过滤、阻拦能力。进入肺泡的微尘可迅速被吸收、不经过肝脏解毒直接进入血液循环,其中的有害气体、重金属等溶解在血液中,分布到全身,损害血红蛋白输送氧的能力。对贫血和血液循环障碍的病人来说,可能产生严重后果。例如可以加重呼吸系统疾病,甚至引起充血性心力衰竭等心脏疾病。
⑦pm2.5还可成为病毒和细菌的载体,为呼吸道传染病的传播推波助澜。
⑧近30年来,***公众吸烟率不断下降,但肺癌患病率却上升了4倍多。目前普遍认为这可能与雾霾天增加有一定的关系,很多人已经把雾霾天气比喻成为大自然的“吸烟室”。不但浓雾缠绕、能见度非常低的天气会对人体健康产生影响,时而有雾时而多云的天气也会有同样的问题。雾霾天对人体心脑血管疾病的影响也很严重,会阻碍正常的血液循环,导致心血管病、高血压、冠心病、脑溢血,可能诱发心绞痛、心肌梗塞、心力衰竭等,使慢性支气管炎出现肺源性心脏病等。
⑨人体每天需要呼吸大约10立方米的空气,生活在城市里的人就相当于一个移动的“空气过滤器”。 面对雾霾天气,我们应该如何抵御pm2.5污染呢?1.少开车,堵车就熄火。汽车尾气不仅危害长时间在道路周边的人,也危害司机本身,特别是长时间堵车、汽油得不到完全燃烧时产生的尾气危害更大。所以长时间堵车时最好熄火,尽量少开窗。2.严禁近郊私***烧垃圾和枯草败叶。私***烧所产生的***、烟尘颗粒等有毒物质,会使周边的城市在不知不觉中陷入“毒雾”。3.减少外出。专家认为,对于雾霾天气最直接的办法就是尽量减少外出。戴口罩可以防止一些灰尘进入鼻腔,能起到一定的防护作用。但对于最近引发热议的pm2.5,专家认为即便是专业的医用口罩,主要针对pm3以上的可吸入颗粒物,对于pm2.5以下的可吸入颗粒物抵御能力不强。4.室内不吸烟,远离二手烟;灰霾天气少开窗,可以养点花花草草;使用空气净化器,市面上80%的空气净化器都以净化空气中的细微颗粒物为主,对pm2.5有很好的吸附效果,但在使用时要注意勤换过滤芯。
小题1:本文向我们介绍了关于pm2.5哪些方面的知识?(4分)
答:
小题2:第②段中画横线的句子“它的直径还不到人的头发丝粗细的1/20”能否换成“它的直径很小”,为什么?(3分)
答:
小题3:阅读⑤⑥⑦三个段落,分点概括pm2.5对人体的危害。(3分)
答:
小题4:结合文章内容,简要分析下列案例中李强的做法有哪些地方不恰当。(3分)
【案例】李强患有贫血,为增强体质,他加强锻炼身体,一年四季从不间断。遇到多雾天气,也会驾车到城郊去爬山。有时遇到拥堵,他也从不熄火。他认为雾再厚,街上买个普通的口罩戴着爬山就没事了。
答: &nb可能相似的问题-
雾霾天气警惕pm2.5污染举例说一说这篇说明文运用了哪些说明方法
1年前1个回答
-
1年前1个回答
-
1年前1个回答
-
1年前1个回答
你能帮帮他们吗
Copyright © 2022 YULUCN.COM - 雨露学习互助 - 17 q. 0.121 s. - webmaster@yulucn.com zhugen19851年前1
zhugen19851年前1 -
-
 泪有痕 共回答了19个问题
泪有痕 共回答了19个问题 |采纳率94.7%小题1:PM2.5的性质(特点)、来源、危害、抵御的方法。(4分)
小题2:不能。(1分)因为原句用作比较的说明方法,以具体的数字,准确地说明了PM2.5的大小,比改句更具体、形象。(2分)
小题3:(1)干扰肺部的气体交换;(2)损害血红蛋白输送氧的能力;(3)成为病毒和细菌的载体,为呼吸道传染病的传播推波助澜。(3分)
小题4:①多雾天气时,空气污染严重,锻炼会加重贫血病情;②遇到拥堵,应该熄火,避免汽车尾气污染;③戴口罩并不能有效抵御PM2.5以下颗粒物的污染。(3分)
1年前查看全部
- (2011•朝阳区一模)KClO3在农业上用作除草剂,超细CaCO3 广泛用于消光纸、无炭复写纸等.某同学在实
(2011•朝阳区一模)KClO3在农业上用作除草剂,超细CaCO3 广泛用于消光纸、无炭复写纸等.某同学在实验室模拟工业过程,利用制乙炔产生的残渣制备上述两种物质,过程如下:
Ⅰ.电石
灰浆水
残渣自然风干
①电石与水反应的化学方程式是______.
②残渣中主要成分是Ca(OH)2和______.
Ⅱ.将Ⅰ中的部分灰浆配成浊液,通入Cl2,得到Ca(ClO3)2与CaCl2物质的量之比为1:5的溶液,反应的化学方程式是______.
Ⅲ.向Ⅱ所得溶液中加入KCl,发生复分解反应,经蒸发浓缩,冷却结晶,过滤得KClO3 晶体.你认为能得到KClO3 晶体的原因是______.
Ⅳ.将Ⅰ中的残渣溶于NH4Cl溶液,加热,收集挥发出的气体再利用.向所得CaCl2溶液中依次通入NH3、CO2,便可获得超细CaCO3,过程如下: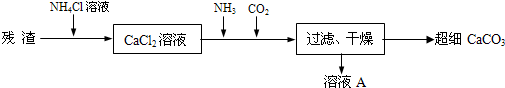
①根据沉淀溶解平衡原理,解释残渣中难溶盐的溶解原因______.
②CaCl2溶液中通入两种气体后,生成超细CaCO3的化学方程式是______.
③图示的溶液A可循环使用,其主要成分的化学式是______. BCVJPK1年前1
BCVJPK1年前1 -
 hakuna0714 共回答了19个问题
hakuna0714 共回答了19个问题 |采纳率89.5%解题思路:Ⅰ.①实验室常用碳化钙固体(俗称电石,化学式为CaC2)与水反应制备乙炔;
②氢氧化钙能与二氧化碳反应生成碳酸钙和水;
Ⅱ.根据反应物和生成物结合得失电子守恒,即可正确书写出化学方程式;
Ⅲ.根据 复分解反应的条件可知能发生与Ca(ClO3)2、KClO3的溶解度有关;
Ⅳ.①氯化铵为强酸弱碱盐,水解呈酸性,加入NH4Cl溶液的目的是溶解残渣中的难溶盐CaCO3;
②由流程图找出反应物和生成物,正确书写化学方程式;
③由CaCl2+2NH3+CO2+H2O═CaCO3↓+2NH4Cl可知A溶液的化学式为:NH4Cl.Ⅰ.①实验室常用碳化钙固体(俗称电石,化学式为CaC2)与水反应制备乙炔,同时生成氢氧化钙,该反应的化学方程式为CaC2+2H2O═Ca(OH)2+C2H2↑,
故答案为:CaC2+2H2O→Ca(OH)2+C2H2↑;
②氢氧化钙能够和空气中的二氧化碳发生反应生成碳酸钙和水,CO2+Ca(OH)2═CaCO3↓+H2O,所以残渣中主要成分是Ca(OH)2和CaCO3,故答案为:CaCO3;
Ⅱ.由题意可知反应物为氯气和氢氧化钙,生成物为Ca(ClO3)2、CaCl2和H2O,氯元素从0价变为Ca(ClO3)2中+5价,两个氯原子失10个电子,氯元素从0价变为CaCl2中-1价,两个氯原子得到2个电子,所以氯化钙前得系数为5,氯酸钙前的系数为1,再根据原子守恒就可得到反应的化学方程式为:6Cl2+6Ca(OH)2=Ca(ClO3)2+5CaCl2+6H2O,
故答案为:6Cl2+6Ca(OH)2═5CaCl2+Ca(ClO3)2+6H2O;
Ⅲ.根据复分解反应的定义,两种化合物相互交换成分,KCl与Ca(ClO3)2能发生复分解反应,说明KClO3在常温下溶解度较小,故可结晶析出,得到其固体,
故答案为:KClO3的溶解度小;
Ⅳ.①氯化铵为强酸弱碱盐,水解呈酸性,碳酸钙虽难溶,但在水中存在电离,CaCO3(s)═Ca2++CO32-,加入NH4Cl溶液,NH4Cl溶液显酸性,使CO32-浓度减小,平衡向右移动,CaCO3溶解,
故答案为:CaCO3(s)═Ca2++CO32-,NH4Cl溶液显酸性,使CO32-浓度减小,平衡向右移动,CaCO3溶解;
②由流程图可以看出,反应物为氨气和二氧化碳和氯化钙和水,生成物为碳酸钙和氯化铵,用观察法配平,碳酸钙后面标上沉淀符号,其反应的化学方程式为:CaCl2+2NH3+CO2+H2O=CaCO3↓+2NH4Cl,
故答案为:CaCl2+2NH3+CO2+H2O═CaCO3↓+2NH4Cl;
③加入NH4Cl溶液的目的是溶解残渣中的难溶盐,根据②CaCl2+2NH3+CO2+H2O═CaCO3↓+2NH4Cl可知A溶液的化学式为:NH4Cl,故答案为:NH4Cl.点评:
本题考点: 制备实验方案的设计;物质分离和提纯的方法和基本操作综合应用.
考点点评: 本题主要考查了化学工艺制KClO3、超细CaCO3,掌握沉淀溶解平衡的影响因素,掌握化学方程式的书写是解答的关键,题目难度中等.1年前查看全部
- 普通胶粉与塑化胶粉的区别多少目以上属于超细胶粉
 gaoooyan1年前1
gaoooyan1年前1 -
 燕子的家 共回答了12个问题
燕子的家 共回答了12个问题 |采纳率91.7%塑化胶粉是在比普通胶粉还要细的基础上塑炼制成的!属于超细胶粉,能提高撕裂、疲劳等性能.而普通胶粉性能要差一些!
100目以上就属于超细胶粉1年前查看全部
- 英语翻译超细AL(OH)3阻燃剂的制备及阻燃性能研究
 势啊1年前4
势啊1年前4 -
 蝶舞寒池 共回答了23个问题
蝶舞寒池 共回答了23个问题 |采纳率82.6%the study of Superfine AL (OH) 3 and flame retardant properties of the preparation
Preparation of superfine powder of Al(OH)3 and research as fire retardant
以上请参考1年前查看全部
- (2014•南京模拟)超细氧化镍(NiO)是一种功能材料,已被广泛用于电池电极、催化剂、半导体、玻璃染色剂等方面.工业上
(2014•南京模拟)超细氧化镍(NiO)是一种功能材料,已被广泛用于电池电极、催化剂、半导体、玻璃染色剂等方面.工业上常以Ni(NO3)2•6H2O和尿素[CO(NH2)2]为原料制备.

(1)Ni2+的基态核外电子排布式为______.
(2)与NO3-离子互为等电子体的一种分子的分子式为______.
(3)尿素分子中碳原子的杂化方式为______,1mol尿素分子中含有的σ键数为______.
(4)NiO晶胞结构如图1所示,Ni的配位数为______.天然的和绝大部分人工制备的晶体都存在各种缺陷.某种NiO晶体中就存在如图2所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代.其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化.经测定某氧化镍样品中Ni3+与Ni2+的离子数之比为6:91.若该晶体的化学式为NixO,则x=______. 觅雪_晴韵1年前1
觅雪_晴韵1年前1 -
 litiandi 共回答了20个问题
litiandi 共回答了20个问题 |采纳率85%解题思路:(1)Ni是28号元素,根据原子核外电子排布规律可知,Ni2+的基态核外电子排布式为1s22s22p63s23p63d8,据此答题;
(2)根据等电子体概念可知,原子数和价电子数都相等 的微粒互为等电子体,NO3-离子中有四个原子,价电子数为24,所以与NO3-离子互为等电子体的一种分子为BF3、SO3、COCl2等,据此答题;
(3)尿素分子的结构简式为: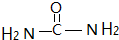 ,所以尿素分子中碳原子的杂化方式为sp2杂化,每个分子中含有7个σ键,据此答题;
,所以尿素分子中碳原子的杂化方式为sp2杂化,每个分子中含有7个σ键,据此答题;
(4)根据NiO晶胞结构可知,每个镍有6个氧,所以配位数为6,根据化合物化合价代数各为零,可以算出NixO中x的值;(1)Ni是28号元素,根据原子核外电子排布规律可知,Ni2+的基态核外电子排布式为1s22s22p63s23p63d8,故答案为:1s22s22p63s23p63d8;
(2)根据等电子体概念可知,原子数和价电子数都相等 的微粒互为等电子体,NO3-离子中有四个原子,价电子数为24,所以与NO3-离子互为等电子体的一种分子为BF3、SO3、COCl2等,故答案为:BF3、SO3、COCl2等;
(3)尿素分子的结构简式为: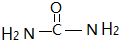 ,所以尿素分子中碳原子的杂化方式为sp2杂化,每个分子中含有7个σ键,所以1mol尿素中含有7moσ键,故答案为:sp2、7mol或7×6.02×1023个;
,所以尿素分子中碳原子的杂化方式为sp2杂化,每个分子中含有7个σ键,所以1mol尿素中含有7moσ键,故答案为:sp2、7mol或7×6.02×1023个;
(4)根据NiO晶胞结构可知,每个镍有6个氧,所以配位数为6;因为氧化镍样品中Ni3+与Ni2+的离子数之比为6:91,所以镍元素的平均价为[6×3+91×2/6+91]=[200/97]根据化合物化合价代数各为零,得[200/97]x=2,则x=0.97,故答案为:6、0.97;点评:
本题考点: 晶胞的计算;配合物的成键情况.
考点点评: 本题主要考查了核外电子的排布、等电子体、原子杂化、化学键、晶胞的计算等知识,中等难度,注重基础知识的考查.1年前查看全部
- 粒径大约0.5微米的超细铜粉,里面含有约总质量5%左右的氧化亚铜,如果不能用酸洗,怎么才能去掉这一部分
粒径大约0.5微米的超细铜粉,里面含有约总质量5%左右的氧化亚铜,如果不能用酸洗,怎么才能去掉这一部分
可不可以用纯水洗掉?氧化亚铜在水中形成什么样的体系,是类似悬浊液,乳浊液之类的么? 春风之章1年前1
春风之章1年前1 -
 wanglifang7210 共回答了20个问题
wanglifang7210 共回答了20个问题 |采纳率100%用水是不可能的
氧化铜比重是6 而且不溶于水,不会形成分散系.
可以考虑浓氨水 Cu不溶于浓氨水 而CuO溶于浓氨水,
而且氨水易挥发,没有残留.1年前查看全部
- 超细颗粒、胶体颗粒的颗粒是多大?
超细颗粒、胶体颗粒的颗粒是多大?
请问颗粒大小达到了多少,才能称的上是超细颗粒、胶体颗粒? 断肠人25531年前1
断肠人25531年前1 -
 49398773 共回答了17个问题
49398773 共回答了17个问题 |采纳率100%胶体颗粒应该是1纳米到100纳米之间
超细颗粒,不好意思,我不太清楚...可能是小于1纳米吧...1年前查看全部
大家在问
- 1介词后面不是只可以是名词性质的宾语吗,例如:of value 但是我今天看到伴随的with 用法wi
- 2从功能来划分,深圳东门属于什么社区?南山高科技园区属于什么区?和广州大学属于什么区?
- 3英语的句型转化题 是人教版七年级下册英语书的第五单元的知识.
- 4下图是人体的心脏的结构模式图,请据图回答下列问题: (1)标出下列各部分的名称:[6]
- 5化简比 0.6公顷:2平方千米
- 6英语作文“My vocation”
- 7记梦别三首 作文
- 8某人骑自行车以10m/s的速度在大风中向东行使,他感觉到风正以相当于车的速度从北方吹来,实际上风的速度是( )
- 91.2.3.4.5.7.8.9.12.20.21.100的英语怎么写
- 10负四的二次方乘以中括号小括号一减七小括号除以六中括号三次方加括号小括号负五括号的3次方]÷(负二的三次方)乘小括号负1/
- 11C:\Documents and Settings\Administrator\
- 12体育室有排球25只,篮球的只数是排球的2倍,小皮球的只数比篮球的3倍多20只.小皮球有多少只?
- 136+6比9加( )少2,这是小学一年级的题目希望大神们解答?
- 14阅读理解. He's an old cobbler (修鞋匠) wit
- 15业精于勤荒于喜,行成于思毁于随.这句诗源自谁之口



