脱硫吸收塔设计脱硫效率最好的形式有哪些类型
 昔日好友2022-10-04 11:39:543条回答
昔日好友2022-10-04 11:39:543条回答
已提交,审核后显示!提交回复
共3条回复
 weik 共回答了14个问题
weik 共回答了14个问题 |采纳率85.7%- 在合成氨生产中要进行变换气脱硫,其中脱硫效率最高的是带气液分布装置的无填料塔,入口H2S含量小于300PPM,出口含量小于10PPM,碱液循环量小,节电30%以上.
- 1年前
 冰河飞花 共回答了1个问题
冰河飞花 共回答了1个问题 |采纳率- 如是空喷塔的话,除喷淋层布置合理外,加气体分布器和塔壁分液板,脱硫效果最佳
- 1年前
 xianzu4235 共回答了3个问题
xianzu4235 共回答了3个问题 |采纳率- 喷淋塔效果较好,应用也比较多
- 1年前
相关推荐
- (2014•肇庆二模)某热电厂用脱硫得到的石膏(CaSO4•2H2O)生产K2SO4肥料的流程如图1.
(2014•肇庆二模)某热电厂用脱硫得到的石膏(CaSO4•2H2O)生产K2SO4肥料的流程如图1.
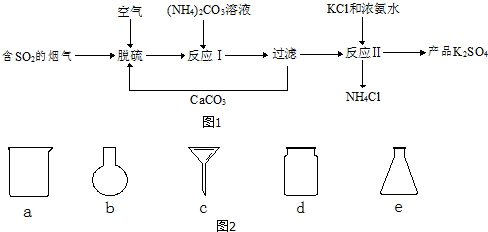
请回答下列问题:
(1)脱硫过程的化学方程式为2CaCO3+2SO2+O2+4H2O=2CaSO4•2H2O+2______.
(2)石膏与饱和(NH4)2CO3溶液相混合,发生反应Ⅰ时需不断搅拌,其目的是______.
(3)实验室完成过滤操作所需要的仪器(如图2)有铁架台、玻璃棒以及______(填字母序号).
(4)该工艺可以循环利用的物质有______(写一种),副产品NH4Cl与NaOH溶液混合微热,产生的气体能使湿润的红色石蕊试纸变______色. zhiked1年前1
zhiked1年前1 -
 yzztx 共回答了22个问题
yzztx 共回答了22个问题 |采纳率90.9%解题思路:(1)根据质量守恒定律进行分析;
(2)根据玻璃棒的作用进行分析;
(3)根据过滤的操作中需要的仪器进行分析;
(4)根据反应过程中的反应物、生成物,找出能循环利用的物质,根据氨气的性质能使湿润的红色石蕊试纸变色进行分析.(1)由质量守恒定律可知,反应前后原子的种类及数目不变可知,所以生成物中应填入的物质是:CO2;
(2)石膏与饱和(NH4)2CO3溶液相混合,发生反应Ⅰ时需不断搅拌,其目的是:使原料充分反应,提高原料利用率;
(3)实验室完成过滤操作所需要的仪器有铁架台、玻璃棒以及烧杯和漏斗;
(4)通过分析反应的流程可知,该工艺可以循环利用的物质是碳酸钙,由于NH4Cl与NaOH溶液混合微热,产生了氨气,氨气的水溶液显碱性,能使湿润的红色石蕊试纸变蓝色.
故答案为:(1)CO2;
(2)使原料充分反应,提高原料利用率;
(3)a c;
(4)碳酸钙,蓝.点评:
本题考点: 物质的相互转化和制备;过滤的原理、方法及其应用;盐的化学性质;质量守恒定律及其应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题通过物质的转化和制备,考查的知识点较多,只有全面地掌握有关的知识,才能解决好本题.1年前查看全部
- 为了减少二氧化硫的排放,现普遍应用湿净化器对煤燃烧后产生的烟气进行脱硫的方法,主要反应原理为:
为了减少二氧化硫的排放,现普遍应用湿净化器对煤燃烧后产生的烟气进行脱硫的方法,主要反应原理为:
2SO 2 +2CaCO 3 +4H 2 O+O 2 =2CO 2 +2CaSO 4 -2H 2 O(石膏).现有l25t含杂质20%的石灰石,若运用上述反应原理吸收SO 2 气体.则最多可以吸收S0 2 气体多少吨?(杂质不参加反应) 爱无悔211年前1
爱无悔211年前1 -
 緤妩苼 共回答了17个问题
緤妩苼 共回答了17个问题 |采纳率88.2%最多可以吸收S0 2 气体的质量为x,2SO 2 +2CaCO 3 +4H 2 O+O 2 =2CO 2 +2CaSO 4 ?2H 2 O128 200x 125t×(1-20%) 128 200 = x 125t×(1-20%) &...1年前查看全部
- 对煤燃烧产生的废气用CaCO3进行脱硫处理过程中发生的两个主要反应的化学方程式
 人外仁1年前1
人外仁1年前1 -
 闲听花落lily 共回答了21个问题
闲听花落lily 共回答了21个问题 |采纳率100%caco3+so2=caso3+co2气体符号升2caso3+o2=2caso41年前查看全部
- (2012•四川)直接排放煤燃烧产生的烟气会引起严重的环境问题,将烟气通过装有石灰石浆液的脱硫装置可以除去其中的二氧化硫
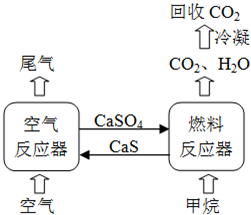 (2012•四川)直接排放煤燃烧产生的烟气会引起严重的环境问题,将烟气通过装有石灰石浆液的脱硫装置可以除去其中的二氧化硫,最终生成硫酸钙.硫酸钙可在有图所示的循环燃烧装置的燃料反应器重与甲烷反应,气体产物分离出水后得到几乎不含杂质的二氧化碳,从而有利于二氧化碳的回收利用,达到减少碳排放的目的.
(2012•四川)直接排放煤燃烧产生的烟气会引起严重的环境问题,将烟气通过装有石灰石浆液的脱硫装置可以除去其中的二氧化硫,最终生成硫酸钙.硫酸钙可在有图所示的循环燃烧装置的燃料反应器重与甲烷反应,气体产物分离出水后得到几乎不含杂质的二氧化碳,从而有利于二氧化碳的回收利用,达到减少碳排放的目的.
请回答下列问题:
(1)煤燃烧产生的烟气直接排放到空气中,引发的主要环境问题有______.(填写字母编号)
A.温室效应B.酸雨C.粉尘污染D.水体富营养化
(2)在烟气脱硫的过程中,所用的石灰石浆液在进入脱硫装置前,需通一段时间的二氧化碳,以增加其脱硫效率;脱硫时控制浆液的PH值,此时浆液含有的亚硫酸氢钙可以被氧气快速氧化生成硫酸钙.
①二氧化碳与石灰石浆液反应得到的产物为______.
②亚硫酸氢钙被足量氧气氧化生成硫酸钙的化学方程式:______.
(3)已知1molCH4在燃料反应器中完全反应生成气态水时吸热160.1kJ,1mol CH4在氧气中完全燃烧生成气态水时放热802.3kJ.写出空气反应器重发生反应的热化学方程式:______.
(4)回收的CO2与苯酚钠在一定条件下反应生成有机物M,其化学为C7H5O3Na,M经稀硫酸化得到一种药物中间N,N的结构简式为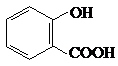 .
.
①M的结构简式为______.
②分子中无-O-O-,醛基与苯环直接相连的N的同分异构体共有______种. 阿富汉1年前1
阿富汉1年前1 -
 我就是阿色 共回答了20个问题
我就是阿色 共回答了20个问题 |采纳率90%解题思路:(1)煤燃烧产生的烟气中含有二氧化硫、二氧化碳以及粉尘等,都可导致环境污染;
(2)CO2与CaCO3反应生成易溶的Ca(HCO3)2,亚硫酸氢钙具有还原性,可被氧化为硫酸钙;
(3)利用盖斯定律计算反应热并以此书写反应的热化学方程式;
(4)因为酸性羧酸>碳酸>苯酚,碳酸不与-COONa反应,则M为,N对应的同分异构体中含有2个-OH和1个-CHO,根据位置异构判断.(1)煤燃烧的产物中有CO2、烟尘以及SO2,分别导致温室效应、粉尘污染和酸雨,没有营养元素排入水中,不会引起水体富营养化,故答案为:A、B、C;
(2)①CO2与CaCO3反应生成易溶的Ca(HCO3)2,故答案为:Ca( HCO3)2;
②亚硫酸氢钙具有还原性,可被氧化为硫酸钙,反应的方程式为Ca( HSO3)2+O2=CaSO4+H2SO4,故答案为:Ca( HSO3)2+O2=CaSO4+H2SO4;
(3)根据右图以及硫酸钙与甲烷反应的气体产物只有水可知,燃料反应器中发生的热化学方程式为:CH4(g)+CaSO4(s)=CO2(g)+2H2O(g)+CaS(s)△H=160.1 kJ•mol-1 ①,再写出甲烷在氧气中燃烧的热化学方程式:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-802.3 kJ•mol-1②,
②-①可得热化学方程式:CaS(s)+2O2(g)=CaSO4(s)△H=-962.4 kJ/mol,
故答案为:CaS(s)+2O2(g)=CaSO4(s)△H=-962.4 kJ/mol;
(4)①因为酸性羧酸>碳酸>苯酚,碳酸不与-COONa反应,则M为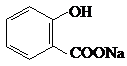 ,故答案为:
,故答案为: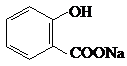 ;
;
②N对应的同分异构体中含有2个-OH和1个-CHO,-CHO可在如图中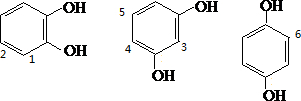 6种位置,故答案为:6.
6种位置,故答案为:6.点评:
本题考点: 有机物的推断;热化学方程式;二氧化硫的污染及治理;常见的生活环境的污染及治理.
考点点评: 本题考查了燃料脱硫的原理、热化学方程式的书写、有机物的推断以及同分异构体的性质等,题中难度中等,注意同分异构体的判断,为该题的易错点和难点.1年前查看全部
- 1.还原剂的生成———————— ————————2.铁的还原————————3.将生铁脱硫去P降低含C量得钢—————
1.还原剂的生成
———————— ————————
2.铁的还原
————————
3.将生铁脱硫去P降低含C量得钢
————————
横线是方程式, 墨______池1年前1
墨______池1年前1 -
 贱精男人 共回答了17个问题
贱精男人 共回答了17个问题 |采纳率88.2%1 C+O2--CO2
CO2+C--CO
2 Fe2O3+CO--Fe+CO2
3 X+O2---***1年前查看全部
- 请比较铁水预处理过程脱硫与转炉炼钢过程的原理有什么不同?
 静oo静1年前1
静oo静1年前1 -
 tianxin0508 共回答了17个问题
tianxin0508 共回答了17个问题 |采纳率88.2%两者脱硫的原理应该有所不同吧.
铁水脱硫由于在还原条件下脱硫所以效果更好,铁水脱硫可以用到纯镁,石灰、电石.而转炉内只能通过石灰脱硫:
铁水预脱硫:FeS+CaO+C=Fe+CaS+CO
CaC2+FeS=CaS+Fe+2C
转炉内氧化性条件脱硫效果较差
FeS+CaO=CaS+FeO.1年前查看全部
- 某种煤含硫量%1进行脱硫,一吨煤应加入多少石灰石?可得硫酸钙多少千克
 话话偶1年前1
话话偶1年前1 -
 香水我只用六神 共回答了15个问题
香水我只用六神 共回答了15个问题 |采纳率93.3%二氧化硫脱除量=燃煤量×硫分(1%)×1.6×脱硫效率
石灰石耗量=二氧化硫脱除量÷64×100×Ca/S比(1.03)÷石灰石纯度
石膏产量=二氧化硫脱除量÷64(二氧化硫分子量)×172(石膏的分子量)1年前查看全部
- 已知,某燃煤型锅炉燃烧能力为:10t/h,燃烧用煤的含硫量为0.9%,燃烧前经水洗脱硫20%,燃烧后的烟尘经除尘设备脱硫
已知,某燃煤型锅炉燃烧能力为:10t/h,燃烧用煤的含硫量为0.9%,燃烧前经水洗脱硫20%,燃烧后的烟尘经除尘设备脱硫95%.请计算该锅炉SO2的产生量和排放量
 kmxv1年前1
kmxv1年前1 -
 chunjian82 共回答了15个问题
chunjian82 共回答了15个问题 |采纳率86.7%SO2产生量计算公式是:G=1.6×B×S
其中:B—耗煤量
S—硫份
所以你的问题就好计算了.
SO2 产生量: G = 1.6×B×S = 1.6×10×0.9% = 0.144t/h
因为脱硫效率为95%.
所以SO2排放量:
G = 1.6×B×S×(1-95%)= 1.6×10×0.9% ×5% = 0.0072t/h1年前查看全部
- 脱硫生成的结晶物是什么?请问采用石灰法工艺脱硫,在设备内部附着的白色结晶物是什么?好像不溶于水,请问怎么消除?
 PisenLiu1年前2
PisenLiu1年前2 -
 海不悔 共回答了19个问题
海不悔 共回答了19个问题 |采纳率94.7%软垢.CaSO3·1/2H2O,溶于酸1年前查看全部
- 在1200℃时,天然气脱硫工艺中会发生下列反应 H2S(g)+[3/2]O2(g)=SO2(g)+
在1200℃时,天然气脱硫工艺中会发生下列反应H2S(g)+[3/2]O2(g)=SO2(g)+H2O(g)△H1 2H2S(g)+SO2(g)=[3/2]S2(g)+2H2O(g)△H2 H2S(g)+[1/2]O2(g)=S(g)+H2O(g)△H3 2S(g)=S2(g)△H4则△H4的正确表达式为( )
A.△H4=[2/3](3△H3-△H2-△H1)
B.△H4=[2/3](△H1-3△H3+△H2)
C.△H4=[3/2](△H1-3△H3+△H2)
D.△H4=[3/2](△H1-△H2-3△H3) 春困秋乏1年前1
春困秋乏1年前1 -
 土工干士 共回答了18个问题
土工干士 共回答了18个问题 |采纳率83.3%解题思路:利用盖斯定律分析,不管化学反应是一步或分几步完成,其反应热是不变的;根据目标方程改写分方程,然后求出反应热.根据目标方程,把方程3反写,计量数乘以2;把方程2乘以[2/3];把方程1乘以[2/3];然后三者相加;即△H4=-△H3×2+△H2×[2/3]+△H1×[2/3]=[2/3](△H1+△H2-3△H3),
故选B.点评:
本题考点: 用盖斯定律进行有关反应热的计算.
考点点评: 本题考查了盖斯定律的应用,要注意方程式计量数的变化,及△H的符号的变化.1年前查看全部
- 简述脱硫,脱磷的热力学条件简述脱硫热力学条件,简述脱磷的热力学条件?这两个··请知道的赐教 很急啊···
 rr客新1年前1
rr客新1年前1 -
 xiagu1983 共回答了13个问题
xiagu1983 共回答了13个问题 |采纳率84.6%找本冶金物理化学看看,上面有的
脱硫是吸热反应
1.高温有利于脱硫
2.低FeO有利于脱硫
脱磷是放热反应
1.低熔池温度有利其
2.FeO创造的氧化性条件
3.高碱度,二元碱度在2.5以上1年前查看全部
- 为了减少煤燃烧带来的大气污染,提高煤的燃烧效率,一些城市使用焦炉煤气(焦炉煤气是脱硫煤隔绝空气强热的部分产物)作为洁净的
为了减少煤燃烧带来的大气污染,提高煤的燃烧效率,一些城市使用焦炉煤气(焦炉煤气是脱硫煤隔绝空气强热的部分产物)作为洁净的生活燃料,其成分是初中化学中常见的气体.现通过下图实验流程对焦炉煤气的成分进行部分探究.
(1)从探究过程可得出焦炉煤气中一定含有______气体;
(2)焦炉煤气成分的可能组合是______;______;______;______.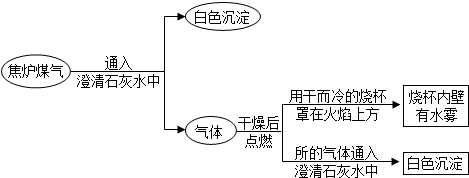
 ambabyzhang1年前1
ambabyzhang1年前1 -
 y022311 共回答了18个问题
y022311 共回答了18个问题 |采纳率94.4%(1)由气体通入澄清石灰水中,澄清石灰水变浑浊,说明气体中一定含有二氧化碳.
(2)将剩余气体点燃,烧杯内壁有水珠,说明气体中含有氢元素;将生成的气体通入澄清石灰水中,澄清石灰水变浑浊,说明气体中含有碳元素.
故答案为:
(1)CO 2
(2)CO 2 、CH 4 ;
CO 2 、CO、H 2 ;
CO 2 、CH 4 、CO;
CO 2 、CH 4 、CO、H 2 ;1年前查看全部
- 高中化学能减少酸雨的形成对燃煤进行脱硫B人工收集雷电作用产生的氮的氧化物
高中化学能减少酸雨的形成对燃煤进行脱硫B人工收集雷电作用产生的氮的氧化物
3.下列有关防止或减少酸雨的措施中不可行的是 A.对燃煤及燃煤烟气进行脱硫 ...C.人工收集大气雷电产生的氮的氧化物 D.推广天然气、甲醇等作为汽车的燃料 A ①②③④ B ①②③ C ①②④ D ①③④ A-ha1年前1
A-ha1年前1 -
 1314520zl 共回答了16个问题
1314520zl 共回答了16个问题 |采纳率87.5%大气雷电产生的氮氧化物被豆科植物直接吸收,人工不可以1年前查看全部
- (1/3)在脱硫过程中废气的污染物数量P mg/L与时间t的关系为P=Po乘e^(-kt) 如果在前两个小时消除了10%
(1/3)在脱硫过程中废气的污染物数量P mg/L与时间t的关系为P=Po乘e^(-kt) 如果在前两个小时消除了10%...
(1/3)在脱硫过程中废气的污染物数量P mg/L与时间t的关系为P=Po乘e^(-kt) 如果在前两个小时消除了10%的污染物,请回答? 勒涩1年前3
勒涩1年前3 -
 小少爷来了 共回答了12个问题
小少爷来了 共回答了12个问题 |采纳率83.3%P5/P0=e^-5k=0.9
-k=1/5ln0.9
P=P0e^(1/5ln0.9*t)
P10/P0=e^(1/5ln0.9*10)=e^(2ln0.9)=e^ln0.81=0.81=81%
P/Po=e^(1/5ln0.9*t)=1/2
1/5ln0.9*t=ln0.5
t=5ln0.5/ln0.9=5*0.6931/0.1053=32.89
33小时1年前查看全部
- 归纳海水法 脱硫 的优势和局限?
 shimei06091年前1
shimei06091年前1 -
 大小风 共回答了17个问题
大小风 共回答了17个问题 |采纳率94.1%海水脱硫工艺是利用海水的碱度达到脱除烟气中二氧化硫的一种脱硫方法.在脱硫吸收塔内,大量海水喷淋洗涤进入吸收塔内的燃煤烟气,烟气中的二氧化硫被海水吸收而除去,净化后的烟气经除雾器除雾、经烟气换热器加热后排放.吸收二氧化硫后的海水与大量未脱硫的海水混合后,经曝气池曝气处理,使其中的SO32-被氧化成为稳定的SO42-,并使海水的PH值与COD调整达到排放标准后排放大海.海水脱硫工艺一般适用于靠海边、扩散条件较好、用海水作为冷却水、燃用低硫煤的电厂.海水脱硫工艺在挪威比较广泛用于炼铝厂、炼油厂等工业炉窑的烟气脱硫,先后有20多套脱硫装置投入运行.近几年,海水脱硫工艺在电厂的应用取得了较快的进展.此种工艺最大问题是烟气脱硫后可能产生的重金属沉积和对海洋环境的影响需要长时间的观察才能得出结论,因此在环境质量比较敏感和环保要求较高的区域需慎重考虑.1年前查看全部
- (2014•四川模拟)某火电厂的脱硫尾气通入饱和K2CO3溶液吸收池后,经分解池制得纯净的CO2,再在合成塔与H2反应生
(2014•四川模拟)某火电厂的脱硫尾气通入饱和K2CO3溶液吸收池后,经分解池制得纯净的CO2,再在合成塔与H2反应生成甲醇.其工艺艺流程示意图如下:
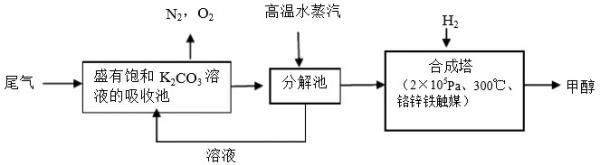
(1)吸收池中饱和K2CO3溶液吸收CO2的离子方程式是______.
(2)流程示意图中循环使用的物质是______.
(3)300℃时,合成塔中的反应为CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),在密闭条件下,下列示意图能说明反应进行到t1时刻时达到平衡状态的是______(填字母序号)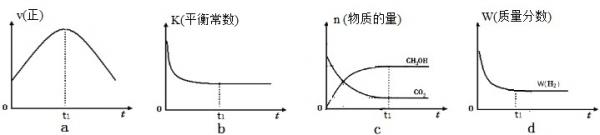
(4)利用合成塔中失活后的铬锌触媒可制得含有Cl-和CrO42-的溶液,其浓度均为0.01mol/L,向该溶液中逐滴加入0.01mol/L的AgNO3溶液时,首先产生沉淀的阴离子是______(已知:Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=9.0×10-12)
(5)合成塔中失活的铬锌触媒可用于制备锌锰电池.在碱性条件下,该电池的总反应为:
Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s),该电池正极的电极反应式是______.若用电池电解(惰性电极)足量的Mg(NO3)2和NaCl的混合溶液,电解过程中阴极的现象是______. 新月婉清1年前1
新月婉清1年前1 -
 云落风起 共回答了17个问题
云落风起 共回答了17个问题 |采纳率100%解题思路:由流程图可知,火电厂的脱硫尾气的主要成份是二氧化碳,在吸收池中充分反应生成碳酸氢钾,生成的碳酸氢钾由分解池分解后所得溶液是碳酸钾可通入吸收池再利用,合成塔内反应是氢气与二氧化碳反应生成甲醇和水,由此分析解题.(1)二氧化碳和碳酸钾反应生成碳酸氢钾,离子方程式为CO2+CO32-+H2O=2HCO3-,故答案为:CO2+CO32-+H2O=2HCO3-.
(2)碳酸氢钾在分解池中分解产生碳酸钾在吸收池中可重复利用,故答案为:碳酸钾;
(3)平衡状态是指外界一定各组份的浓度、物质的量、质量分数、速率不再随时间的改变而改变的动态平衡状态,
a、t1时刻正反应速率最大,不是变,故a不选;
b、温度不变,平衡常数不变,故b不选;
c、t1时刻,各物质的量不再随时间的变化而变化,故选c;
d、t1时刻,氢气的体积分数不再随时间的改而改变,故选d;
故答案为:c、d;
(4)析出沉淀时,AgCl溶液中c(Ag+)=
Ksp(AgCl)
c(Cl−)=
1.56×10−10
0.01=1.56×10-8mol/L,Ag2CrO4溶液中c2(Ag+)=Ksp(Ag2CrO4)/c(CrO42-)=
9.0×10−12
0.01,则c(Ag+)为3×10-5mol/L,c(Ag+)越小,则越先生成沉淀,故答案为:Cl-;
(5)正极发生还原反应,得电子化合价降低,二氧化锰中的锰元素由+4价变成+3价,故正极是二氧化锰发生还原反应,电极反应式为:2MnO2+2e-+H2O=2OH-+Mn2O3,若用电池电解(惰性电极)足量的Mg(NO3)2和NaCl的混合溶液,阴极是氢离子放电,电极反应方程式为2H2O+2e-=H2↑+2OH-,氢氧根离子与镁离子结合在难溶氢氧化镁沉淀,故答案为:2MnO2+2e-+H2O=2OH-+Mn2O3;有无色气体和白色沉淀产生.点评:
本题考点: 离子方程式的书写;常见化学电源的种类及其工作原理;化学平衡状态的判断;难溶电解质的溶解平衡及沉淀转化的本质.
考点点评: 此题通过研究二氧化碳对环境的影响考察对二氧化碳的了解.根据题中的条件对化学方程式的推理及应用,根据化学方程式进行数据的求解都是考查的重点.溶解平衡问题,题目难度中等,注意根据溶解度判断生成沉淀的先后顺序,对于组成不相似的物质,不能直接根据溶度积判断.1年前查看全部
- 工业上燃烧煤常用CaO进行脱硫处理.脱硫处理?
工业上燃烧煤常用CaO进行脱硫处理.脱硫处理?
脱硫处理是? 29h21年前1
29h21年前1 -
 bullstar 共回答了11个问题
bullstar 共回答了11个问题 |采纳率90.9%媒中含有硫元素,燃烧后生成SO2,SO3会污染空气,用CaO与SO2,SO3反应生成CaSO4,可以消除污染,同时生成了石膏1年前查看全部
- (2010•南京二模)烟气脱硫电控制二氧化硫污染的主要技术手段.
(2010•南京二模)烟气脱硫电控制二氧化硫污染的主要技术手段.
(1)利用海水脱硫是一种有效的方法,其工艺流程如下图所示: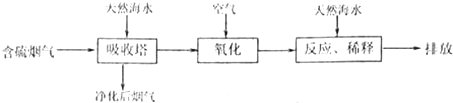
某研究小组为探究提高含硫烟气中SO2的吸收效率的措施,进行了天然海水吸收含硫烟气的模拟实验,实验结果如图1所示.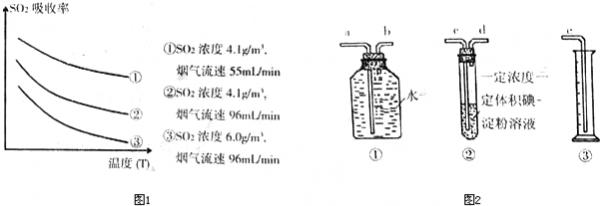
①根据图示实验结果,为了提高一定浓度含硫烟气中SO2的吸收效率,下列措施正确的是______.
A.降低通入含硫烟气的温度;B.减小通入含硫烟气的流速
C.减少天然海水的进入量;D.在天然海水中加入生石灰
②天然海水吸收了含硫烟气后会溶有H2SO3,使用空气中的氧气将其氧化,写出该反应的离子方程式______.
③该小组采用图2装置在实验室测定烟气中SO2的体积分数(假设实验在标准状况下进行):上述装置组装连接的顺序是:原料气→______(填a、b、c、d、e).下列试剂中(浓度、体积一定),可以用来代替试管中的碘-淀粉溶液的是______(填编号).
A.酸性KMnO4溶液;B.NaOH溶液;C.溴水;D.氨水
(2)石灰石-石膏湿法烟气脱硫工艺技术的工作原理是烟气中的二氧化硫与浆液中的碳酸钙以及鼓入的空气反应生成石膏(CaSO4•2H2O).写出该反应的化学方程式:______.某电厂用煤300吨(煤中含硫质量分数为2.5%),若燃烧时煤中的硫全部转化成二氧化硫,用石膏湿法烟气脱硫中有96%的硫转化为石膏,则可生产石膏______吨. ab6081年前1
ab6081年前1 -
 欧米嘎 共回答了25个问题
欧米嘎 共回答了25个问题 |采纳率88%解题思路:(1)①总体来看,SO2的吸收效率随温度的升高而降低,当温度和浓度相同时,SO2的吸收效率随烟气流速的增大而降低,当温度和烟气流速相同时,SO2的吸收效率随SO2浓度的增大而降低,同时根据生石灰能与水反应生成碱,碱能与SO2反应;
②根据使用空气中的氧气将H2SO3氧化;
③根据实验的原理来分析;测定模拟烟气中SO2的体积分数,可根据二氧化硫气体的还原性,与具有氧化性的酸性高锰酸钾或溴水反应,通过颜色的变化判断;
(2)二氧化硫与碳酸钙反应生成亚硫酸钙与二氧化碳,亚硫酸钙在水存在的条件下被氧气氧化生成CaSO4•2H2O;根据关系式S~SO2~CaSO4•2H2O来计算;(1)①总体来看,SO2的吸收效率随温度的升高而降低,当温度和浓度相同时,SO2的吸收效率随烟气流速的增大而降低,当温度和烟气流速相同时,SO2的吸收效率随SO2浓度的增大而降低,同时根据生石灰能与水反应生成碱,碱能与SO2反应;所以为了提高一定浓度含硫烟气中SO2的吸收效率,可通过降低通入含硫烟气的温度,减小通入含硫烟气的流速以及在天然海水中加入生石灰;故答案为:ABD;
②由空气中的氧气将H2SO3氧化为硫酸,该反应为2H2SO3+O2=2H2SO4,
故答案为:2H2SO3+O2=4H++2SO4 2-;
③该实验的测定原理为:烟气通过一定浓度一定体积的碘-淀粉溶液,其中的SO2与碘反应,当恰好反应时,溶液的蓝色消失,根据碘的物质的量可以求出SO2的物质的量,余下的气体排入广口瓶,将水压入量筒,由量筒中的水的体积可以确定剩余气体的体积,最后求出SO2体积分数;测定模拟烟气中SO2的体积分数,可根据二氧化硫气体的还原性,与具有氧化性的酸性高锰酸钾或溴水反应,通过颜色的变化判断,选项中AC符合,都有颜色,且都具有氧化性,能与二氧化硫反应,故选:cdbae;AC;
(2)二氧化硫与碳酸钙反应生成亚硫酸钙与二氧化碳,反应方程式为:SO2+CaCO3=CaSO3+CO2,亚硫酸钙在水存在的条件下被氧气氧化生成CaSO4•2H2O,反应方程式为:2CaSO3+O2+4H2O=2(CaSO4•2H2O),总反应为:2CaCO3+2SO2+O2+4H2O═2(CaSO4•2H2O)+2CO2;
故答案为:SO2+CaCO3=CaSO3+CO2;2CaSO3+O2+4H2O=2(CaSO4•2H2O);
S~SO2 ~CaSO4•2H2O
32172
300t×2.5%×96% m
[ 32/300t×2.5%×96%=
172
m],解得m=38.7t,
故答案为:38.7;点评:
本题考点: 二氧化硫的污染及治理.
考点点评: 本题考查污染的处理,利用所学知识结合习题中的信息即可解答,习题中图象及数据是解答本题的关键,较好的考查学生分析问题、解决问题的能力.1年前查看全部
- 火力发电厂释放出大量的氮氧化物(NO x )、二氧化硫和二氧化碳等气体会造成环境污染.对燃煤废气进行脱硝、脱硫和脱碳等处
火力发电厂释放出大量的氮氧化物(NO x )、二氧化硫和二氧化碳等气体会造成环境污染.对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的.
(1)脱硝.利用甲烷催化还原NO x :
CH 4 (g)+4NO 2 (g)=4NO(g)+CO 2 (g)+2H 2 O(g)△H 1 =-574kJ•mol -1
CH 4 (g)+4NO(g)=2N 2 (g)+CO 2 (g)+2H 2 O(g)△H 2 =-1160kJ•mol -1
甲烷直接将NO 2 还原为N 2 的热化学方程式为______.
(2)脱碳.将CO 2 转化为甲醇的热化学方程式为:CO 2 (g)+3H 2 (g)═CH 3 OH(g)+H 2 O(g)△H 3
①取五份等体积的CO 2 和H 2 的混合气体(物质的量之比均为1:3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH 3 OH) 与反应温度T的关系曲线如图1所示,则上述CO 2 转化为甲醇的反应的△H 3 ______0(填“>”、“<”或“=”).
②在一恒温恒容密闭容器中充入1mol CO 2 和3mol H 2 ,进行上述反应.测得CO 2 和CH 3 OH(g)的浓度随时间变化如图2所示.试回答:0~10min内,氢气的平均反应速率为______mol/(L•min);该温度下,反应的平衡常数的值为______;第10min后,向该容器中再充入1mol CO 2 和3mol H 2 ,则再次达到平衡时CH 3 OH(g)的体积分数______(填变大、减少、不变).
(3)脱硫.某种脱硫工艺中将废气经处理后,与一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物作为副产品化肥.硫酸铵和硝酸铵的水溶液的pH<7,其原因用离子方程式表示为______;在一定物质的量浓度的硝酸铵溶液中滴加适量的NaOH溶液,使溶液的pH=7,则溶液中c(Na + )+c(H + )______c(NO 3 - )+c(OH - )(填写“>”“=”或“<”) 刺鸟腹语录1年前1
刺鸟腹语录1年前1 -
 天天6170 共回答了23个问题
天天6170 共回答了23个问题 |采纳率95.7%(1)已知:①CH 4 (g)+4NO 2 (g)=4NO(g)+CO 2 (g)+2H 2 O(g)△H 1 =-574kJ•mol -1 ②CH 4 (g)+4NO(g)=2N 2 (g)+CO 2 (g)+2H 2 O(g)△H 2 =-1160kJ•mol -1 则CH 4 (g)+2NO 2 (g)=N 2 ...1年前查看全部
- 火力发电厂释放出的大量氮氧化物(NOx)、二氧化硫和二氧化碳等气体会造成环境污染.对燃烧废气进行脱硝、脱碳和脱硫等处理,
火力发电厂释放出的大量氮氧化物(NOx)、二氧化硫和二氧化碳等气体会造成环境污染.对燃烧废气进行脱硝、脱碳和脱硫等处理,可实验绿色环保、节能减排、废物利用.
(1)脱硝:利用甲烷催化还原NOx;
CH4(g)+4NO2(g)=CO2(g)+2H2O(g)△H1=-574kJ•mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2=-1160kJ•mol-1
甲烷直接将NO2还原为N2的热化学方程式为______.
(2)脱碳:将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H<0
CH3OH(g)+H2O(g)△H<0
T℃时,取2mol CO2和4mol H2混合,加入到1L恒容密闭容器中,发生上述反应,10分钟后达到平衡时测得甲醇的体积分数为25%,计算氢气的转化率______.T℃时该反应的化学平衡常数K=______;升高温度,K______.(选填“增大”“减小”“不变”)
(3)脱硫:某种脱硫工艺中将废气处理后,与一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物.设烟气中SO2、NO2的物质的量为1:1,写出该反应的化学方程式(不要求配平)______.将生成的硫酸铵和硝酸铵的混合物溶解于水,室温下测得溶液的pH小于7,其原因是______. 过年去媳妇1年前1
过年去媳妇1年前1 -
 XIAYE1994 共回答了15个问题
XIAYE1994 共回答了15个问题 |采纳率93.3%解题思路:(1)根据盖斯定律,不管化学反应是一步完成还是分几步完成,其反应热是相同的,化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关.
(2)根据化学平衡计算三步曲,求出参加反应氢气的物质的量,计算氢气的转化率;根据化学平衡常数概念,代入数据,求出常数;根据温度对对化学平衡的影响.
(3)根据题目信息,抓住质量守恒,写出化学方程式;考虑盐类的水解.(1)因盖斯定律,不管化学反应是一步完成还是分几步完成,其反应热是相同的.两式相加,可得
2CH4(g)+4NO2(g)=2N2(g)+2CO2(g)+4H2O(g)△H=-1734 kJ/mol
故答案为:2CH4(g)+4NO2(g)=2N2(g)+2CO2(g)+4H2O(g)△H=-1734 kJ/mol
(2)CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H<0
CH3OH(g)+H2O(g)△H<0
起始(mol) 2 4 0 0
反应(mol) X3X XX
10分钟后(mol) 2-X 4-3X X X
甲醇的体积分数为[X/2-X+4-3X+X+X]×100%=25%可得:X=1
所以氢气的转化率为:[3/4]×100%=75%,
平衡常数K=
C(CH3OH)C(H2O)
C(CO2)C3( H2) =[1×1/1×1]=1
升高温度,平衡向吸热的方向移动,即逆向移动,K减小.
故答案为:75%;1;减小;
(3)由题目信息可知反应为NH3、O2、SO2、NO2、H2O,生成物为(NH4)2SO4、NH4NO3,
由此可写出方程式为NH3+O2+SO2+NO2+H2O→(NH4)2SO4+NH4NO3,
故答案为:NH3+O2+SO2+NO2+H2O→(NH4)2SO4+NH4NO3
(4)因铵盐要发生水NH4++H2O NH3•H2O+H+,故答案为:NH4++H2O
NH3•H2O+H+,故答案为:NH4++H2O NH3•H2O+H+
NH3•H2O+H+
点评:
本题考点: 二氧化硫的污染及治理;热化学方程式;化学平衡的计算;氮的氧化物的性质及其对环境的影响.
考点点评: 本题从多个角度对化石燃料进行了全面的考查,培养了学生分析问题的能力.1年前查看全部
- 某研究人员按如图所示流程进行“燃煤烟气的脱硫研究”.实验中,SO 2 和O 2 的混合气体连续通入,水和铁在起始时一次性
某研究人员按如图所示流程进行“燃煤烟气的脱硫研究”.实验中,so 2 和o 2 的混合气体连续通入,水和铁在起始时一次性加入,反应液多次循环. 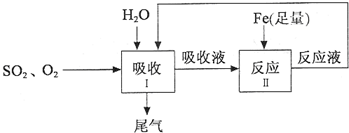
(1)Ⅰ中发生反应的化学方程式是2so 2 +2h 2 o+o 2 ═2x,则x的化学式是______.
(2)Ⅱ中发生反应的化学方程式是______.
(3)随着反应液流入Ⅰ中,吸收液中x的生成速率明显加快,其原因可能是______.
(4)经过多次循环后,反应液可以用来制备feso 4 •7h 2 o,它在医疗上常用于治疗______(选填字母).
a.甲状腺肿***.佝偻病c.龋齿d.贫血症. hw20051年前1
hw20051年前1 -
 jasowood 共回答了19个问题
jasowood 共回答了19个问题 |采纳率89.5%(1)反应前S:2,O:8,H:4,反应后一个X分子的组成为2个氢原子、1个硫原子、4个氧原子,故化学式为:H 2 SO 4 ;
(2)铁与硫酸反应生成硫酸亚铁和氢气的写出化学方程式为:Fe+H 2 SO 4 =FeSO 4 +H 2 ↑;
(3)吸收液中X的生成速率明显加快,其原因可能是生成的Fe 2+ 对Ⅰ中发生的反应起催化作用;
(4)贫血可能缺少铁元素,故选D.
答案:
(1)H 2 SO 4
(2)Fe+H 2 SO 4 =FeSO 4 +H 2 ↑
(3)反应液中的Fe 2+ 对Ⅰ中发生的反应起催化作用
(4)D1年前查看全部
- 石灰石脱硫过程的方程式
 小荷诗魔1年前1
小荷诗魔1年前1 -
 雨后金荷 共回答了23个问题
雨后金荷 共回答了23个问题 |采纳率87%CaCO3=高温=CaO+CO2↑
CaO+SO2=CaSO3
2CaSO3+O2=2CaSO41年前查看全部
- 煤炭燃烧过程中会释放出大量的SO2,严重破坏生态环境.采用一定的脱硫技术可以把硫元素以CaSO4的形式固定,从而降低SO
煤炭燃烧过程中会释放出大量的SO2,严重破坏生态环境.采用一定的脱硫技术可以把硫元素以CaSO4的形式固定,从而降低SO2的排放.但是煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低脱硫效率.相关反应的热化学方程式如下:CaSO4(s)+CO(g)═CaO(s)+SO2(g)+CO2(g)△H1=+218.4kJ•mol-1(反应Ⅰ)CaSO4(s)+4CO(g)═CaS(s)+4CO2(g)△H2=-175.6kJ•mol-1(反应Ⅱ)假设某温度下,反应Ⅰ的速率(v1)大于反应Ⅱ的速率(v2),则下列反应过程能量变化示意图正确的( )
A.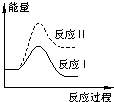
B.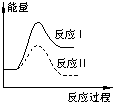
C.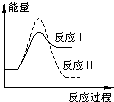
D.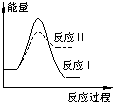
 脉脉01年前1
脉脉01年前1 -
 totofly 共回答了17个问题
totofly 共回答了17个问题 |采纳率100%解题思路:反应Ⅰ为吸热反应,反应Ⅱ为放热反应,结合反应物与生成物总能量大小之间的关系判断.反应Ⅰ为吸热反应,反应Ⅱ为放热反应,则A、D错误;反应Ⅰ的速率(v1)大于反应Ⅱ的速率(v2),则反应Ⅱ的活化能较大,则B错误、C正确,
故选C.点评:
本题考点: 反应热和焓变.
考点点评: 本题为2014浙江高考题的一部分,涉及化学平衡以及反应热与焓变的考查,题目难度中等.1年前查看全部
- (2006•佛山)为减少煤燃烧带来的大气污染,提高煤的燃烧效率,一些城市使用焦炉煤气(焦炉煤气是脱硫煤隔绝空气强热的部分
(2006•佛山)为减少煤燃烧带来的大气污染,提高煤的燃烧效率,一些城市使用焦炉煤气(焦炉煤气是脱硫煤隔绝空气强热的部分产物)作为洁净的生活燃料,其成分是初中课本中常见的气体.现通过以下实验流程对焦炉煤气的成分进行局部探究.
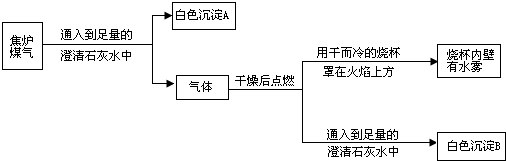
(1)白色沉淀A、B是不是同一种物质?______(填“是”或“不是”);
(2)从探究过程可推出焦炉煤气中一定含有______气体;
(3)焦炉煤气的可能组成为______(只写一种可能的情况). 124171771年前1
124171771年前1 -
 和hh力 共回答了22个问题
和hh力 共回答了22个问题 |采纳率95.5%解题思路:焦炉气是脱硫煤在隔绝空气的条件下进行分解而产生的物质,而煤中含有碳元素、氢元素、氧元素等元素,所以可以据此并结合图中的图表来判断焦炉气的成分,并完成该题的解答.(1)根据焦炉气的成分可以知道在焦炉气中含有碳元素,所以在本实验中能够跟澄清石灰水反应生成白色沉淀的只有二氧化碳,并且白色沉淀也只能是碳酸钙即A和B为同一种物质;
(2)根据图表一开始将焦炉气通入澄清石灰水即产生了白色沉淀说明在焦炉气中一定含有二氧化碳;
(3)对通过澄清石灰水后的气体干燥后点燃,气体可以燃烧,并且产生了水雾,所以在干燥后的气体中含有氢元素,并且含有碳元素,所以根据焦炉气的来源结合质量守恒定律可以判断该气体可能是甲烷、氢气、一氧化碳等气体的混合物,结合(2)的解答可以得出焦炉气可能的组成成分.
故答案为:
(1)是;
(2)CO2(或二氧化碳);
(3)CO2、CH4、H、CO若填CO2、CH4或CO2、H2、CO或CO2、CH4、CO同样对(其余答案不给分)点评:
本题考点: 实验探究物质的组成成分以及含量;常见气体的检验与除杂方法;二氧化碳的化学性质.
考点点评: 在熟练掌握各气体性质的基础上,结合物质的组成元素及质量守恒定律来解答;本题中注重了学生的分析推理能力的考察,所以在平时的学习过程中要注意培养自己的分析推理能力.1年前查看全部
- 烟气的脱硫(除SO2)技术和脱硝(除NOx)技术都是环境科学研究的热点.
烟气的脱硫(除SO2)技术和脱硝(除NOx)技术都是环境科学研究的热点.
(1)烟气脱硫、脱硝的环境意义是______.
(2)选择性催化还原法的脱硝原理为:6NOx+4x NH3
(3+2x)N2+6xH2O催化剂 .
上述反应中每转移3mol电子,生成标准状况下N2的体积为[16.8+11.2x/x][16.8+11.2x/x]L.
(3)目前,科学家正在研究一种以乙烯(C2H4)作为还原剂的脱硝(NO)原理,其脱硝机理示意图如图1,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2所示.
①写出该脱硝原理总反应的化学方程式:6NO+3O2+2C2H4
3N2+4CO2+4H2O催化剂 .6NO+3O2+2C2H4.
3N2+4CO2+4H2O催化剂 .
②为达到最佳脱硝效果,应采取的条件是______. 遇见自已1年前1
遇见自已1年前1 -
 wangquanai5 共回答了16个问题
wangquanai5 共回答了16个问题 |采纳率81.3%解题思路:(1)硫的氧化物、氮的氧化物是形成酸雨的主要成因,烟气脱硫、脱硝可以防止酸雨的发生;
(2)反应中氨气中的N元素由-3价升高为0价,据此计算转移3mol电子参加反应的氨气的物质的量,再根据方程式计算生成的氮气,根据V=nVm计算氮气的体积;
(3)①图1可知,在催化剂的作用下,C2H4与NO、O2反应最终生成N2、CO2、H2O,据此写出反应的总方程式;
②为达到最佳脱硝效果,应满足脱硝率高,负载率低,适宜的温度.(1)烟气脱硫、脱硝可以降低硫的氧化物、氮的氧化物含量,防止酸雨的发生,
故答案为:防止酸雨的发生;
(2))反应中氨气中的N元素由-3价升高为0价,化合价升高3价,泽尔转移3mol电子参加反应的氨气的物质的量为:[3mol/3]=1mol,根据方程式可知生成的氮气的物质的量为:1mol×[3+2x/4x]=[3+2x/4x]mol,
氮气的体积为:[3+2x/4x]mol×22.4L/mol=[16.8+11.2x/x]L,
故答案为:[16.8+11.2x/x];
(3)①根据图1可知,在催化剂的作用下,C2H4与NO、O2反应最终生成N2、CO2、H2O,反应总方程式为:6NO+3O2+2C2H4
催化剂
.
3N2+4CO2+4H2O,
故答案为:6NO+3O2+2C2H4
催化剂
.
3N2+4CO2+4H2O;
②由图可知,b曲线的最高点处,脱硝率高,负载率低,温度温度适宜,适宜适合条件为350℃、负载率3%,
故答案为:350℃、负载率3%.点评:
本题考点: 氧化还原反应的计算;氮的氧化物的性质及其对环境的影响.
考点点评: 本题以烟气的脱硫和脱硝为载体,考查环境保护、氧化还原反应计算、方程式书写等知识,题目难度中等,本题注意把握数据处理和图象分析.1年前查看全部
- 炼钢脱硫的反应是怎样的?又有什么样的条件呢?
 注个一次性ID1年前1
注个一次性ID1年前1 -
 sd2110617 共回答了20个问题
sd2110617 共回答了20个问题 |采纳率100%炼钢脱硫反应:(1)脱S总反应式:[FeS]+(CaO)=(CaS)+ [FeO](2)热力学条件:①高碱度渣有利于脱硫;②氧化铁较高对脱硫有利;③较高的熔池温度有利于脱硫;④增大渣量有利于脱硫.(3)动力学条件:增强反应熔池内流体运动,增大反应界面.化学式:氧化脱磷2[P]+5(FeO)+3(CaO)=3CaO.P2O5+5[Fe]
2[P]+5(FeO)+4(CaO)=4CaO.P2O5+5[Fe]脱硫反应[S]+(CaO)=(CaS)+[O]
[S]+(MnO)=(MnS)+[O]
[S]+(MgO)=(MgS)+[O]炼钢过程中电石脱硫原理
电石的分子式是CaC2,脱硫反应如下
CaC2+S=CaS+2C
这个式子是瞬间反应.即吹入铁水中的电石粉在上浮期间与铁水中的硫反应,生成的硫化钙进入渣中.提高电石的脱硫效率
的要点是一,增加电石粉在铁水中的滞留时间,比如采用斜吹,二,提高铁水温度,脱硫反应是吸热的,提高铁水温度可以
提高脱硫的效率.1年前查看全部
- 钢铁冶炼中是用什么进行脱硫的,其成分是什么.谁可以答我吗,
 月下柳梢人1年前1
月下柳梢人1年前1 -
 孤独ZY 共回答了18个问题
孤独ZY 共回答了18个问题 |采纳率83.3%镁脱硫剂:其中镁粒占88-96%,保护膜占4-12%.采用耐高温的材料如:MgO、MgCl2、CaO、云石、冰晶石等材料组成.
电石脱硫剂:碳化钙、氧化钙、二氧化硅、氧化铁、氧化铝、氧化镁、碳等.
氧化铁脱硫剂1年前查看全部
- 你认为减少酸雨产生可采取的措施是①工厂烟囱造高一些;②将矿石燃料脱硫;③在已酸化的土壤中加石灰;④开发新能源.( )
你认为减少酸雨产生可采取的措施是①工厂烟囱造高一些;②将矿石燃料脱硫;③在已酸化的土壤中加石灰;④开发新能源.( )
A. ②③④
B. ①②④
C. ②④
D. ①③ 梦中小屋1年前1
梦中小屋1年前1 -
 风沙739 共回答了16个问题
风沙739 共回答了16个问题 |采纳率100%解题思路:少用煤作燃料、燃料脱硫、开发新的能源等措施可以减少二氧化硫气体的排放,从而减少酸雨的形成,据此分析解答.①工厂烟囱造高一些不能减少二氧化硫、氮氧化物的产生,所以不能减少酸雨的产生,故错误;
②将矿石燃料脱硫、④开发新能源都能减少二氧化硫、氮氧化物的排放,所以能减少酸雨的形成,故正确;
③在已酸化的土壤中加石灰,可以改良土壤,但不能减缓酸雨污染,故错误;
故选C.点评:
本题考点: 二氧化硫的污染及治理.
考点点评: 本题考查了环境污染及治理,明确环境污染的原因是解本题关键,根据绿色化学从根源上杜绝有毒物质的产生,将部分物质转化为有用物质,充分利用化学知识造福于人类.1年前查看全部
- 下列说法中,错误的是( ) A.用熟石灰处理含酸量超标的工业污水 B.煤气中毒通常是指一氧化碳中毒 C.使用燃煤脱硫技
下列说法中,错误的是( ) A.用熟石灰处理含酸量超标的工业污水 B.煤气中毒通常是指一氧化碳中毒 C.使用燃煤脱硫技术防止二氧化硫污染 D.铵态氮肥可与碱性物质混合使用  whitebirdzr1年前1
whitebirdzr1年前1 -
 烧火凤凰 共回答了20个问题
烧火凤凰 共回答了20个问题 |采纳率95%A、熟石灰显碱性,所以可以处理含酸量超标的工业污水,故A正确;
B、煤气中毒通常是指一氧化碳中毒,故B正确;
C、硫燃烧生成二氧化硫,使用燃煤脱硫技术防止二氧化硫污染,故C正确;
D、铵态氮肥可与碱性物质混合会放出氨气,所以不可混用,故D错误.
故选:D.1年前查看全部
- 石膏脱硫中,石膏水密度是多少?石膏含量为20%,其他为水,请写出具体的换算方法或者公式,
 爱吃果果的猴子1年前1
爱吃果果的猴子1年前1 -
 zxh1106 共回答了15个问题
zxh1106 共回答了15个问题 |采纳率100%吸收塔中石膏浆液过饱和度最大不超过140% 石膏浆液浓度在设计范围内 一般固率在10%-20% 密度在1060-1127 kqm31年前查看全部
- 高中范围内,下列反应方程式侯式制碱法炼钢的脱碳脱硫反应热还原法制镁精制饱和食盐水:钙镁铁硫酸根离子煤的液化泡沫灭火器反应
高中范围内,下列反应方程式
侯式制碱法
炼钢的脱碳脱硫反应
热还原法制镁
精制饱和食盐水:钙镁铁硫酸根离子
煤的液化
泡沫灭火器反应
混凝法净水
钢铁生锈 iom_xd3b_ve688f1年前4
iom_xd3b_ve688f1年前4 -
 进士 共回答了19个问题
进士 共回答了19个问题 |采纳率94.7%1第一步:CO2 + NH3 + NaCl + H2O = NaHCO3 + NH4Cl
第二部:NaHCO3 (加热)=Na2CO3 + CO2↑+ H2O
2炼钢主要是用氧化剂把生铁里过多的碳和其它杂质氧化而除去,常用的氧化剂:空气、氧气或氧化铁,降低碳量:C+FeO==CO+Fe-热量;
脱硫:炉渣脱硫
气化去硫:3(Fe2O3)+CaS=CaO+6(FeO)+SO2↑
3碳热还原:MgO+C=Mg+CO
4加入足量NaCO3,去沉淀,之后加入BaCl2,去沉淀,之后蒸馏使其饱和(这个不一定对)
5直接液化
间接液化:高温液化、低温液化
6、Al2(SO4)3+6NaHCO3==3Na2SO4+2Al(OH)3↓+6CO2↑
7混凝法:在混凝剂的作用下,使废水中的胶体和细微悬浮物凝聚成絮凝体,然后予以分离除去的水处理法.
8在潮湿的空气中:4Fe + 3O2 + XH2O ==== 2Fe2O3·XH2O
铁的缓慢氧化:4Fe+3O2=2Fe2O31年前查看全部
- 石灰浆液脱硫管道怎么冲洗?湿法石灰石脱硫工艺中,浆液管道非常容易堵塞,怎么防范和处理呢?
 hqeyou1年前1
hqeyou1年前1 -
 miller_no_31 共回答了14个问题
miller_no_31 共回答了14个问题 |采纳率78.6%首先管道铺设要有一定的坡度,其次每次停泵以后及时排放冲洗.这是最有效得了,只要有责任心就会没问题.1年前查看全部
- 电厂脱硫为什么要用到氢氧化钙?
 alexiayuna1年前1
alexiayuna1年前1 -
 jfjh 共回答了18个问题
jfjh 共回答了18个问题 |采纳率94.4%双碱法可能会用到,单用的话有用氧化钙的,加水制备成氢氧化钙作为脱硫剂也可行.1年前查看全部
- 喷洒碳酸钙粉末脱硫和石油燃烧的化学方程式
喷洒碳酸钙粉末脱硫和石油燃烧的化学方程式
1.喷洒碳酸钙粉末脱硫的化学方程式
2.石油(CnH2n+2)(2n+2下标)燃烧过程中的化学方程式 piaofushi1年前1
piaofushi1年前1 -
 啊匪 共回答了19个问题
啊匪 共回答了19个问题 |采纳率89.5%(1):CaCO3+SO2=CsSO3+CO2 (其实只要在两边加个水就知道反应原理是中强酸制弱酸)
(2):我记得石油是混合物(不同等级的碳烃繁衍物)好象不能写.如果要写的话2CnH(2n+2)+(3n+1)O2===2nCO2+(2n+2)H2O1年前查看全部
- 尾气脱硫工艺中反应的化学方程式
 泉客1年前1
泉客1年前1 -
 黎明之空1 共回答了18个问题
黎明之空1 共回答了18个问题 |采纳率83.3%就是氨液吸收,生成亚硫酸铵,再分解,提取到更纯的二氧化硫.在送到硫酸.脱硫的气体就排空了.1年前查看全部
- 在煤中掺入熟石灰脱硫写出化学方程式
 欲辩忘言1年前1
欲辩忘言1年前1 -
 stiphine 共回答了17个问题
stiphine 共回答了17个问题 |采纳率94.1%S+O2=SO2
Ca(OH)2+SO2=CaSO3+H2O
二氧化硫被吸收后就不会再污染空气了,而亚硫酸钙又不容易分解1年前查看全部
- 煤中掺入熟石灰脱硫 方程式急!
 那姿1年前1
那姿1年前1 -
 牵手同行 共回答了19个问题
牵手同行 共回答了19个问题 |采纳率100%似乎应该是掺入生石灰
CaO+SO2=(加热)CaSO3
2CaSO3+O2=2CaSO41年前查看全部
- 脱硫中cl离子怎么产生的
 不可告人的心痛1年前1
不可告人的心痛1年前1 -
 kukucoolfish 共回答了18个问题
kukucoolfish 共回答了18个问题 |采纳率88.9%cl离子不是产生,而是说原烟气里带有的,因为煤炭成分复杂.概念上的误区1年前查看全部
- 煤炭燃烧后,产生硫,如何脱硫,求化学式及名称
 狂啸原野1年前1
狂啸原野1年前1 -
 cyy3500183 共回答了17个问题
cyy3500183 共回答了17个问题 |采纳率100%用氧化钙,化学式CaO,反应方程式:CaO+SO2=CaSO31年前查看全部
- 脱硫系统中出来的石灰石粉(250目 90%)的密度是多少?谢谢!
 xd131788287271年前2
xd131788287271年前2 -
 可以跳舞的美人鱼 共回答了19个问题
可以跳舞的美人鱼 共回答了19个问题 |采纳率94.7%堆密度,1400kg/m3 .一般人我不告诉他!1年前查看全部
- 脱硫中2TQ是什么意思,2TQ是什么组成的,
 罚站的种子1年前1
罚站的种子1年前1 -
 tbwrtvqt 共回答了15个问题
tbwrtvqt 共回答了15个问题 |采纳率66.7%这是栲胶脱硫,TQ为醌态栲胶,Na2V4O9+2TQ+2NaOH+H2O — 4NaVO3+2THQ,THQ为酚态栲胶1年前查看全部
- 一道化学的有关碳酸钙的计算已知某种煤的含硫量为1%(质量分数),进行煤的脱硫处理时,1t煤种至少应加入多少千克石灰石?反
一道化学的有关碳酸钙的计算
已知某种煤的含硫量为1%(质量分数),进行煤的脱硫处理时,1t煤种至少应加入多少千克石灰石?反应后可得硫酸钙多少千克? cool头1年前1
cool头1年前1 -
 yyy780120 共回答了27个问题
yyy780120 共回答了27个问题 |采纳率92.6%1吨煤中硫的质量=1000*1%=10kg
解得x=31.25kg,y=42.5kg
所以加入的石灰石为31.25千克,得到硫酸钙42.5千克
注意:方程式的反应过程
CaCO3=CaO+CO2
S+O2=SO2
SO2+1/2O2=SO3
CaO+SO3=CaSO41年前查看全部
- 火力发电厂释放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等气体会造成环境污染.对燃煤废气进行脱硝、脱硫和脱碳等处理,
火力发电厂释放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等气体会造成环境污染.对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的.
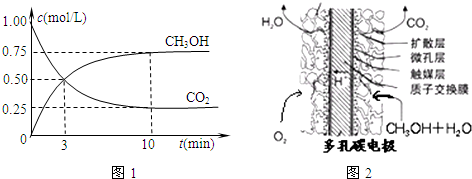
(1)脱硝.利用甲烷催化还原NOx:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ•mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2=-1160kJ•mol-1
甲烷直接将NO2还原为N2的热化学方程式为______.
(2)脱碳.将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g);△H3<0
①在一恒温恒容密闭容器中充入1mol CO2和3mol H2,进行上述反应.测得CO2和CH3OH(g)的浓度随时间变化如图1所示.下列说法正确的是______(填字母代号).
A.第10min后,向该容器中再充入1mol CO2和3mol H2,则再次达到平衡时c(CH3OH)=1.5mol•L-1
B.0~10min内,氢气的平均反应速率为0.075mol/(L•min)
C.达到平衡时,氢气的转化率为75%
D.该温度下,反应的平衡常数的值为[3/16]
E.升高温度将使
减小n(CH3OH) n(CO2)
②甲醇燃料电池结构如图2所示.其工作时正极的电极反应式可表示为:______.
(3)脱硫.某种脱硫工艺中将废气经处理后,与一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物作为副产品化肥.硫酸铵和硝酸铵的水溶液的pH<7,其中原因可用一个离子方程式表为:______;在一定物质的量浓度的硝酸铵溶液中滴加适量的NaOH溶液,使溶液的pH=7,则溶液中:c(Na+)+c(H+)______c(NO3-)+c(OH-)(填写“>”“=”或“<”). 冷月心蓝1年前1
冷月心蓝1年前1 -
 25只蜜蜂 共回答了20个问题
25只蜜蜂 共回答了20个问题 |采纳率95%解题思路:(1)利用盖斯定律分析;
(2)①A、再充入1mol CO2和3mol H2,可等效为开始体积变为原来的2倍,加入2mol CO2和6mol H2,平衡后,再将体积压缩为原来的体积,增大压强平衡向体积减小的方向移动,即向正反应移动,反应物的转化率增大;
B、利用v=[△n/△t]计算v(H2)判断;
C、根据转化率的定义计算判断;
D、该温度下该反应的K=
,代入数据计算;[CH3OH][H2O] [CO2][H2]3
E、该反应为放热反应,升高温度平衡向逆反应进行,n(CH3OH)减小,n(CO2)增大.
②正极上氧化剂得电子发生还原反应;
(3)强酸弱碱盐易水解而使其溶液呈酸性,根据电荷守恒判断.(1)已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ•mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2=-1160kJ•mol-1
不管化学反应是一步完成还是分几步完成,其反应热是相同的.两式相加,可得
2CH4(g)+4NO2(g)=2N2(g)+2CO2(g)+4H2O(g)△H=-1734 kJ/mol
即CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867 kJ•mol-1
故答案为:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867 kJ•mol-1;
(2)①由图2可知,开始二氧化碳的浓度为1.0mol/L,开始容器中充入1mol CO2和3mol H2,所以开始氢气的浓度为3.0mol/L,容器体积为[1.0mol/1.0mol/L]=1L.
平衡时,甲醇的浓度为0.75mol/L
CO2(g)+3H2(g)
一定条件
CH3OH(g)+H2O(g)
开始(mol/L):1 3 0 0
变化(mol/L):0.75 2.250.75 0.75
平衡(mol/L):0.25 0.750.75 0.75
A、通过上述计算可知二氧化碳的转化率为[0.75mol/L/1.0mol/L]×100%=75%,再充入1mol CO2和3mol H2,可等效为开始体积变为原来的2倍,加入2mol CO2和6mol H2,平衡后,再将体积压缩为原来的体积,增大压强平衡向体积减小的方向移动,即向正反应移动,反应物的转化率增大,所以再次达到平衡时c(CH3OH)>1.5mol/L,故A错误;
B、10分钟内,氢气的平均反应速率为v(H2)=[2.25mol/L/10min]=0.225mol/(L•min),故C错误;
C.通过上述计算可知氢气的转化率为[2.25mol/L/3mol/L]×100%=75%,故C正确;
D、该温度下该反应的K=
[CH3OH][H2O]
[CO2][H2]3=[0.75×0.75
0.25×(0.75)3=
16/3],故D错误;
E、该反应为放热反应,升高温度平衡向逆反应进行,n(CH3OH)减小,n(CO2)增大,所以n(CH3OH)/n(CO2)值减小,故E正确.
故选:CE;
②正极上氧气得电子和氢离子反应生成水,所以电极反应式为:O2+4e-+4H+=2H2O,故答案为:O2+4e-+4H+=2H2O;
(3)硫酸铵和硝酸铵都是强酸弱碱盐,铵根离子易水解而使其溶液呈酸性,水解离子方程式为:NH4++H2O⇌NH3•H2O+H+,溶液呈中性,则c(H+)=c(OH-),溶液中存在电荷守恒,则c(Na+)+c(H+)+c(NH4+)=c(NO3-)+c(OH-),所以c(Na+)+c(H+)<c(NO3-)+c(OH-),
故答案为:NH4++H2O⇌NH3•H2O+H+;<.点评:
本题考点: 二氧化硫的污染及治理;热化学方程式;化学电源新型电池;化学平衡建立的过程;氮的氧化物的性质及其对环境的影响.
考点点评: 本题考查了盖斯定律、原电池原理、化学平衡、盐类水解等知识点,难点是化学平衡的有关计算,有关化学平衡的计算是考试热点,难度中等.1年前查看全部
- 电厂化学脱硫化验中,皮带机石膏亚硫酸盐(碘量法)的测定?
电厂化学脱硫化验中,皮带机石膏亚硫酸盐(碘量法)的测定?
实验原理:
亚硫酸盐在酸性条件下与过量的0.05mol/L 的碘溶液反应,被氧化,然后,未反应的碘用0.1mol/L 的硫代硫酸钠标准液反滴定.其终点以电位法或指示剂法测定.
实验方法:
1.5g~2.0g石膏(已在40℃干燥) →放入250ml锥形瓶(或烧杯)→用150mlL除盐水稀释→加10ml 0.05mol/L 的碘溶液+大约10mL HCl(1:1)→摇动滴定瓶5 min,固体应溶解.当液体颜色变淡黄时加1%淀粉指示剂→用0.1mol/L Na2S2O3滴定→溶液蓝色消失时即为滴定终点→计消耗的0.1mol/L Na2S2O3 溶液体积(bmL).最后不加石膏样品按上述步骤作空白实验,记最后0.1mol/L Na2S2O3标准液消耗体积为a mL.
在这个实验中,前后所用的硫代硫酸钠起什么作用呀?
 云之言忍1年前1
云之言忍1年前1 -
 娃哈哈r8 共回答了20个问题
娃哈哈r8 共回答了20个问题 |采纳率90%第一部分的实验中,硫代硫酸钠是用来滴定被亚硫酸根还原后剩余的碘的量.空白实验是为了排除干扰因素,因为硫代硫酸钠易被空气中的氧气氧化.1年前查看全部
- 2.合成氨工业中原料气的脱硫需要如何控制工艺条件?(
 晓风残月28881年前1
晓风残月28881年前1 -
 1230cui 共回答了21个问题
1230cui 共回答了21个问题 |采纳率85.7%脱硫液相的温度,从脱硫塔进气就开始控制了,一般取35度以下.
各塔的液位当然也要控制好,防止跑气.
控制好脱硫液循环量和煤气量的定值范围.
还有就是每天分析脱硫液的成分.包括副盐含量和PH等.1年前查看全部
- (2014•郑州一模)在1200℃时,天然气脱硫工艺中会发生下列反应:
(2014•郑州一模)在1200℃时,天然气脱硫工艺中会发生下列反应:
H2S(g)+[3/2]O2(g)═SO2(g)+H2O(g)△H1
2H2S(g)+SO2(g)═[3/2]S2(g)+2H2O(g)△H2
H2S(g)+[1/2]O2(g)═S(g)+H2O(g)△H3
2S(g)═S2(g)△H4
则△H4的正确表达式为( )
A.△H4=[2/3](△H1+△H2-3△H3)
B.△H4=[2/3](3△H3-△H1-△H2)
C.△H4=[3/2](△H1+△H2-3△H3)
D.△H4=[3/2](△H1-△H2-3△H3) freekick1年前1
freekick1年前1 -
 fzhiming2008 共回答了10个问题
fzhiming2008 共回答了10个问题 |采纳率100%解题思路:利用盖斯定律分析,不管化学反应是一步或分几步完成,其反应热是不变的;根据目标方程改写分方程,然后求出反应热.根据目标方程,把方程3反写,计量数乘以2;把方程2乘以[2/3];把方程1乘以[2/3];然后三者相加;即-△H3×2+△H2×[2/3]+△H1×[2/3]=[2/3](△H1+△H2-3△H3),
故选A.点评:
本题考点: 用盖斯定律进行有关反应热的计算.
考点点评: 本题考查了盖斯定律的应用,要注意方程式计量数的变化,及△H的符号的变化.1年前查看全部
- 炼钢中脱磷和脱硫的顺序可以颠倒么?
 东方不败abc1年前2
东方不败abc1年前2 -
 心蓝780501 共回答了14个问题
心蓝780501 共回答了14个问题 |采纳率85.7%炼钢中脱磷和脱硫的顺序是可以颠倒的.
以目前的转炉炼钢为例,转炉的目的是脱磷,但对钢水的脱硫可以安排在铁水预处理阶段,也可以安排在炉后脱硫阶段.
但有一点,钢水中渣系不可能同时进行脱磷与脱硫(一个需要氧化性,一个需要还原性),所以不管哪一步安排在前,都要进行钢渣分离后再进行下一步.1年前查看全部
- 请问在脱硫工作中加入熟石灰的两个化学方程式是什么?
请问在脱硫工作中加入熟石灰的两个化学方程式是什么?
快啊,是2个化学方程式! 若为_邀月1年前3
若为_邀月1年前3 -
 吴紫东 共回答了19个问题
吴紫东 共回答了19个问题 |采纳率68.4%Ca(OH)2+SO2==CaSO3↓+H2O
2CaSO3+O2==2CaSO4
第二个方程虽然不是起到脱硫的作用,但反应是很有可能发生的,因为亚硫酸盐具有很强的还原性,在煤燃烧的过程中很容易被氧化,在许多参考书中都是这样写的.1年前查看全部
- 3.下列有关防止或减少酸雨的措施中不可行的是 A.对燃煤及燃煤烟气进行脱硫 ...C.人工收集大气雷电产生的氮的氧化物
3.下列有关防止或减少酸雨的措施中不可行的是 A.对燃煤及燃煤烟气进行脱硫 ...C.人工收集大气雷电产生的氮的氧化物 D.推广天然气、甲醇等作为汽车的燃料 A ①②③④ B ①②③ C ①②④ D ①③④
 hezhizhang20001年前1
hezhizhang20001年前1 -
 wh_xb 共回答了24个问题
wh_xb 共回答了24个问题 |采纳率83.3%3、C是错误的.1年前查看全部
大家在问
- 1Lin tao and I live in the same building.But he lives two flo
- 2there are some app|es in the bag.否定疑问句怎写?
- 3如图4.2-3所示,图中直线有____条,线段有____条,射线有____条.
- 4同问一个正方体六个面写着上分别写着ABCDEF ,每个字母对面的字分别是什么
- 5柳永 玉蝴蝶 赏析柳永 《玉蝴蝶》 是处小街斜巷,烂游花馆,连醉瑶卮.选得芳容端丽,冠绝吴姬.绛唇轻、笑歌尽雅,莲步稳、
- 6判断下列说法正确的是( ) A.如果某同学在透明纸上写一个“b”,则在显微镜下的视野看到的是“p” B.观察洋葱磷叶表
- 7溶液中铁离子、铝离子的浓度相同为0.1mol/L,Al(OH)3的Ksp或溶解度远大于
- 8我国的语言文字丰富多彩,其中有许多词语都蕴涵了物理知识,请将下面的表格填写完整.
- 9已知x分之45=18分之27,则x=
- 10------I’ve been told that John ________ from his journ
- 11运一批货,第一天运了这批货的九分之四多300吨,第二天运了这批货物的37.5%少40吨,正好运完,这批货有多
- 12if you don't believe me ,you'd better go to have a look like
- 13求大神围观,为啥这样填,纯手打,
- 14以的作文怎么写
- 15“以前是那样认为的,现在却不这么想了”用文言文怎么说?
