(2010•镇江模拟)安娜同学想利用如图所给实验器材“测定小灯泡的额定功率”,已知电源电压为6V,小灯泡的额定电压2.5
 lfzs12302022-10-04 11:39:541条回答
lfzs12302022-10-04 11:39:541条回答 (2010•镇江模拟)安娜同学想利用如图所给实验器材“测定小灯泡的额定功率”,已知电源电压为6V,小灯泡的额定电压2.5V,电阻约为10Ω.
(2010•镇江模拟)安娜同学想利用如图所给实验器材“测定小灯泡的额定功率”,已知电源电压为6V,小灯泡的额定电压2.5V,电阻约为10Ω.(1)实验的原理是______;
(2)电路连接中有一处明显错误,请你在错误处打“×”,并在原图中画出正确的电路连线.
(3)正确连接电路后,闭合开关,移动滑片P到某一点时,电压表示数为2V;为了测出小灯泡的额定功率,他应继续移动滑片P向______(选填“左”或“右”)端移动,使电压表的示数为______V,然后再读出电流表的示数,从而求出额定功率.
(4)安娜纠正电路中的错误后,移动滑动变阻器,使小灯泡发光,此时电流表和电压表的示数如图甲、乙所示,则通过小灯泡的电流是______A,小灯泡两端的电压是______V.

(5)小明重新移动滑动变阻器多次测量通过小灯泡的电流和小灯泡两端的电压,画出了通过小灯泡的电流随两端电压变化的图象,如图丙所示,则小灯泡的额定功率是______W,此时灯泡的电阻为________Ω.

已提交,审核后显示!提交回复
共1条回复
 小小小小寒 共回答了15个问题
小小小小寒 共回答了15个问题 |采纳率100%- 解题思路:(1)伏安法测功率的原理是P=UI.
(2)灯泡的额定电压是2.5V,电压表量程应选3V,而不是15V,把电压表量程该接为3V.
(3)灯泡两端电压小于额定电压,要使灯泡正常发光,应调节滑动变阻器滑片,减小接入电路的电阻,增大灯泡两端的电压,使电压表示数等于灯泡的额定电压.
(4)确定电压表与电流表的量程与最小分度值.然后根据指针所知刻度读出电压表与电流表的示数.
(5)由图象找出灯泡额定电压对应的电流,由P=UI求出灯泡的额定功率;由R=[U/I]求出此时灯泡的电阻.(1)
 实验的原理是P=UI.
实验的原理是P=UI.
(2)电压表量程接错,改正后的电路图如图所示.
(3)为了测出小灯泡的额定功率,应继续移动滑片P向右端移动,使电压表的示数为2.5V,然后再读出电流表的示数.
(4)电流表的量程是0.6A,最小分度值是0.02A,电流表示数是
0.2A;电压表量程是3V,最小分度值是0.1V,电压表示数是1.5V.
(5)由图知灯泡的额定电压U=2.5V对应的电流I=0.25A,灯泡的额定功率P=UI=2.5V×0.25A=0.625W;此时灯泡的电阻R=[U/I]=[2.5V/0.25A]=10Ω.
故答案为:(1)P=UI;(2)电路图如图所示;(3)右;2.5;(4)0.2;1.5;(5)0.625;10.点评:
本题考点: 探究用电器的电功率实验.
考点点评: 本题考查了测灯泡功率的原理、电压表与滑动变阻器的使用、电压表与电流表的读数、求灯泡功率及灯泡的电阻,本题解题的关键是由图象求出灯泡的额定电压对应的电流. - 1年前
相关推荐
- (2003•镇江)已知抛物线y=-x2+(k+1)+3,当x<1时,y随着x的增大而增大,当x>1时,y随着x的增大而减
 (2003•镇江)已知抛物线y=-x2+(k+1)+3,当x<1时,y随着x的增大而增大,当x>1时,y随着x的增大而减小.
(2003•镇江)已知抛物线y=-x2+(k+1)+3,当x<1时,y随着x的增大而增大,当x>1时,y随着x的增大而减小.
(1)求k的值及抛物线的解析式;
(2)设抛物线与x轴交于A、B两点(A在B的左边),抛物线的顶点为P,试求出A、B、P三点的坐标,并在下面的直角坐标系中画出这条抛物线;
(3)求经过P、A、B三点的圆的圆心O′的坐标;
(4)设点G(0,m)是y轴的一个动点.
①当点G运动到何处时,直线BG是⊙O′的切线并求出此时直线BG的解析式;
②若直线BG与⊙O‘相交,且另一交点为D,当m满足什么条件时,点D在x轴的下方. 谎话精EASYWANG1年前0
谎话精EASYWANG1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2011•镇江一模)已知过点O的直线与函数y=3x的图象交于A、B两点,点A在线段OB上,过A作y轴的平行线交函数y=
(2011•镇江一模)已知过点O的直线与函数y=3x的图象交于A、B两点,点A在线段OB上,过A作y轴的平行线交函数y=9x的图象于C点,当BC∥x轴,点A的横坐标______.
 LADSKFJOWEFDF1年前0
LADSKFJOWEFDF1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 海凌和镇江两地相距210千米.一辆客车和一辆轿车同事从两地出发,相向而行.客车每小时行60千米,经过2小时两车相遇.轿车
海凌和镇江两地相距210千米.一辆客车和一辆轿车同事从两地出发,相向而行.客车每小时行60千米,经过2小时两车相遇.轿车每小时行多少千米?
 归海浪子1年前1
归海浪子1年前1 -
 格格7583 共回答了19个问题
格格7583 共回答了19个问题 |采纳率84.2%451年前查看全部
- 李亮从南京出发 骑自行车旅游,途经镇江,苏州到达上海.南京~镇江85千米.镇江~苏州大约( )千米.苏州到上海110千米
李亮从南京出发 骑自行车旅游,途经镇江,苏州到达上海.南京~镇江85千米.镇江~苏州大约( )千米.苏州到上海110千米.李亮平均每天行45千米,他11天能到上海吗?
 Kitty271年前1
Kitty271年前1 -
 山阳冲印 共回答了20个问题
山阳冲印 共回答了20个问题 |采纳率95%从百度地图上测了距离大约160多到170多千米,所以可认为镇江~苏州大约(170 )千米.
85+170+110=365
45X11=495
3651年前查看全部
- (2009•镇江)芝麻酱具有丰富的营养.右图为某品牌芝麻酱商标的一部分.
 (2009•镇江)芝麻酱具有丰富的营养.右图为某品牌芝麻酱商标的一部分.
(2009•镇江)芝麻酱具有丰富的营养.右图为某品牌芝麻酱商标的一部分.
(1)人们为了维持生命和健康,必须从食物中摄入六大类主要营养物质,右图中没有标出的营养物质是______.
(2)右图中钙、铁、硒是指______(填字母序号).
A.分子;B.原子;C.单质;D.元素
(3)芝麻酱中含铁量比猪肝高出一倍多,因此食用芝麻酱可以预防的疾病是______.
(4)沾有芝麻酱的餐具用加入洗洁精的水更易洗净,这是利用了洗洁精的______作用. 一个人的天1年前1
一个人的天1年前1 -
 1307 共回答了19个问题
1307 共回答了19个问题 |采纳率84.2%解题思路:(1)欲正确解答本题,须知人们为了维持生命和健康,必须从食物中摄入六大类主要营养物质有哪些;
(2)根据分子、原子、单质和元素的概念就可正确选择;
(3)欲正确解答本题,须知铁存在于人体的哪些部位.
(4)欲正确解答本题,须知乳化作用的概念.(1)人们为了维持生命和健康,必须从食物中摄入六大类主要营养物质有蛋白质、糖类、油脂、维生素、无机盐和水.由图可知没有标出的营养物质是水,故答案为:水.
(2)元素又称化学元素,指自然界中一百多种基本的金属和非金属物质,它们由几种有共同特点的原子组成.因此图中钙、铁、硒是指元素.故选D.
(3)铁元素是构成人体的必不可少的元素之一,成人体内约有4-5克铁,其中72%以血红蛋白形式存在,如果缺少了铁元素也会造成贫血.有题意可知,芝麻酱中含铁量比猪肝高出一倍多,故食用芝麻酱可以预防缺铁性贫血.故答案为:缺铁性贫血.
(4)乳化作用是将一种液体分散到第二种不相溶的液体中去的过程.洗洁精可以分散到芝麻酱中,更易洗净.故答案为:乳化.点评:
本题考点: 标签上标示的物质成分及其含量;乳化现象与乳化作用;物质的元素组成;人体的元素组成与元素对人体健康的重要作用;生命活动与六大营养素.
考点点评: 本题主要考查学生对人类主要的营养物质、元素的概念、微量元素的作用以及乳化作用的认识.1年前查看全部
- (2013•镇江)图1、2分别是两种固体熔化时温度随时间变化的图象.
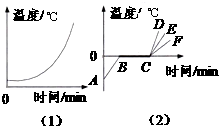 (2013•镇江)图1、2分别是两种固体熔化时温度随时间变化的图象.
(2013•镇江)图1、2分别是两种固体熔化时温度随时间变化的图象.
(1)图1所对应的固体属于______(选填“晶体”或“非晶体”),理由是______;
(2)图2是冰的熔化图象,处于冰水混合状态的是图中______段,在此过程中,混合物需要______热量,总体积______;
(3)已知冰的比热容比水的小.图2中C点对应冰刚好完全熔化,若此后继续加热一会儿,则水温随时间变化的图线是______. meinvlimeng1年前1
meinvlimeng1年前1 -
 kevin516 共回答了19个问题
kevin516 共回答了19个问题 |采纳率89.5%解题思路:(1)晶体和非晶体在熔化过程中的区别:晶体在熔化过程中,温度不变;非晶体在熔化过程中温度不断上升,晶体熔化时的温度为熔点.
(2)晶体从开始熔化到完全熔化完为晶体的熔化过程,在熔化的过程中该物质吸收的热量用来熔化,因此此过程温度保持不变.
(3)由图可知,BC段为冰的熔化过程,在B点开始熔化,到C点结束,若此后继续加热一会儿,温度上升较慢.(1)由图知,该物质在熔化过程中,没有固定的熔点,所以该物质为非晶体.
(2)图2是冰的熔化图象,处于冰水混合状态的是图中BC段在熔化的过程中该物质吸收的热量用来熔化,因此此过程温度保持不变,冰不断熔化成水,因为水的密度比冰的密度大,所以同质量的冰熔化成水后体积减小,故总体积减小.
(3)图2中C点对应冰刚好完全熔化,若此后继续加热一会儿,温度上升较慢,则水温随时间变化的图线CF比较符合实际.
故答案为:(1)非晶体;没有固定的熔点;(2)BC;吸收;减小;(3)CF.点评:
本题考点: 熔化和凝固的温度—时间图象.
考点点评: 对于此类图形题,应明确横、纵坐标轴及各关键点所代表的物理意义,熟练掌握相关知识点是解题的关键所在.1年前查看全部
- (2008•镇江模拟)如图所示,MN、PQ是平行金属板,板长为L两板间距离为d,在PQ板的上方有垂直纸面向里足够大的匀强
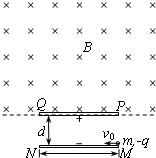 (2008•镇江模拟)如图所示,MN、PQ是平行金属板,板长为L两板间距离为d,在PQ板的上方有垂直纸面向里足够大的匀强磁场.一个电荷量为q,质量为m的带负电粒子以速度V0从MN板边缘且紧贴M点,沿平行于板的方向射入两板间,结果粒子恰好从PQ板左边缘飞进磁场,然后又恰好从PQ板的右边缘飞进电场.不计粒子重力,求:
(2008•镇江模拟)如图所示,MN、PQ是平行金属板,板长为L两板间距离为d,在PQ板的上方有垂直纸面向里足够大的匀强磁场.一个电荷量为q,质量为m的带负电粒子以速度V0从MN板边缘且紧贴M点,沿平行于板的方向射入两板间,结果粒子恰好从PQ板左边缘飞进磁场,然后又恰好从PQ板的右边缘飞进电场.不计粒子重力,求:
(1)两金属板间所加电压U的大小;
(2)匀强磁场的磁感应强度B的大小;
(3)当该粒子再次进入电场并再次从电场中飞出时的速度及方向. KERENYIN1年前1
KERENYIN1年前1 -
 da-bian 共回答了15个问题
da-bian 共回答了15个问题 |采纳率100%解题思路:(1)带电粒子在平行金属板间做的是类平抛运动,对物体受力分析,根据平抛运动的规律可以求得电压的大小;
(2)带电粒子以速度v飞出电场后射入匀强磁场做匀速圆周运动,根据粒子的运动画出运动的轨迹,由几何关系可以求得磁感强度的大小;
(3)根据粒子在磁场及电场中运动的对称性可知,粒子再次进入电场并再次从电场中飞出时的速度为v0,方向水平向左(1)设带电粒子在平行金属板匀强电场中运动的时间为t,
由类平抛运动可知:
L=v0t…①
d=[1/2at2…②
加速度a=
qU
md]…③
由①②③得:电压U=
2mv02d2
qL2④
(2)带电粒子以速度v飞出电场后射入匀强磁场做匀速圆周运动,
由Bqv=m
v2
R…⑤
sinθ=[L/2R]⑥
tanθ=
vy
v…⑦
vy=at…⑧
联立求解①③④⑤⑥⑦⑧可得
B=
4mv0d
qL2
(3)根据粒子在磁场及电场中运动的对称性可知,粒子再次进入电场并再次从电场中飞出时的速度为v0,方向水平向左.
答:(1)两金属板间所加电压U的大小为
2mv02d2
qL2;
(2)匀强磁场的磁感应强度B的大小为
4mv0d
qL2;
(3)当该粒子再次进入电场并再次从电场中飞出时的速度大小为v0,方向水平向左.点评:
本题考点: 带电粒子在匀强磁场中的运动;牛顿第二定律;向心力;带电粒子在匀强电场中的运动.
考点点评: 本题考查带电粒子在匀强磁场中的运动,要掌握住半径公式、周期公式,画出粒子的运动轨迹后,几何关系就比较明显了.1年前查看全部
- 先有一批煤从徐州运往镇江,由铁路运送.如果每节车皮装60吨,还缺3节车皮才能全部运走;
先有一批煤从徐州运往镇江,由铁路运送.如果每节车皮装60吨,还缺3节车皮才能全部运走;
如果每节车皮多装225吨其他物资,问原有煤多少吨?车皮有多少?
请用一元二次方程解决
 vcje1年前1
vcje1年前1 -
 水之月 共回答了13个问题
水之月 共回答了13个问题 |采纳率92.3%这个一元二次方程基本没法列了……1年前查看全部
- (2011•镇江一模)Li-Al/FeS电池是一种正在开发的电动车用电池,该电池反应式为:2Al+6Li++3FeS=2
(2011•镇江一模)Li-Al/FeS电池是一种正在开发的电动车用电池,该电池反应式为:2Al+6Li++3FeS=2Al3++3Li2S+3Fe.有关该电池的下列说法中,正确的是( )
A.作为二次电源,该电池在使用的过程中至少存在3种形式的能量转化
B.Li-Al在电池中作为负极材料,负极的电极反应式为Li-e-=Li+
C.该电池替代现在电动车广泛使用的铅蓄电池可以减少重金属的污染
D.充电时,阴极发生的电极反应式为:Li2S+Fe-2e-=2Li++FeS kuaimen1年前1
kuaimen1年前1 -
 3uh9 共回答了15个问题
3uh9 共回答了15个问题 |采纳率86.7%解题思路:Li和Al都属于金属,合金中Li较Al活泼,根据正极反应式知,原电池的电极材料Li-Al/FeS,判断出负极材料为Al,发生反应为:2Al-6e-=2Al3+,又知该电池中正极的电极反应式为:2Li++FeS+2e-=Li2S+Fe,所以电池反应为:2Al+6Li++3FeS=2Al3++3Li2S+3Fe,充电时为电解池原理,阴极与原电池的负极相连,阴极发生还原反应.A、二次电源在使用的过程中至少存在3种形式的能量转化,即电能、化学能、热能等能量之间的转化,故A正确;
B、根据电极反应式:2Al+6Li++3FeS=2Al3++3Li2S+3Fe,铝元素化合价升高,所以负极反应为2Al-6e-=2Al3+,故B错误;
C、该电池不含有重金属元素,替代现在电动车广泛使用的铅蓄电池可以减少重金属的污染,故C正确;
D、充电时为电解池原理,阴极发生还原反应,即2Al3++6e-=2Al,故D错误.
故选AC.点评:
本题考点: 化学电源新型电池.
考点点评: 本题涵盖电解池和原电池的主体内容,涉及电极判断与电极反应式书写等问题,做题时注意从氧化还原的角度判断原电池的正负极以及电极方程式的书写,本题中难点和易错点为电极方程式的书写.1年前查看全部
- (2003•镇江)在金属、人体、空气及酸、碱、盐的水溶液中,______是绝缘体.将两个吹足了气的气球在手上或衣服上摩擦
(2003•镇江)在金属、人体、空气及酸、碱、盐的水溶液中,______是绝缘体.将两个吹足了气的气球在手上或衣服上摩擦几下,然后将线提起来,看到两气球互相排斥,说明两球带上了______电荷.
 vddersss1年前1
vddersss1年前1 -
 ybdxdd 共回答了14个问题
ybdxdd 共回答了14个问题 |采纳率92.9%(1)在金属、人体、空气及酸、碱、盐的水溶液中,属于导体:金属、人体、酸碱盐的水溶液;属于绝缘体:空气;
(2)每一个气球和手摩擦会出现摩擦起电现象,使两个气球都带有同种电荷,同种电荷相互排斥.
故答案为:空气;同种.1年前查看全部
- (2013•镇江一模)如图表示两细胞间发生某种信息传递的过程,①②分别代表不同的细胞,A表示物质,符合该模型的是( )
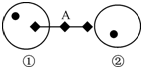 (2013•镇江一模)如图表示两细胞间发生某种信息传递的过程,①②分别代表不同的细胞,A表示物质,符合该模型的是( )
(2013•镇江一模)如图表示两细胞间发生某种信息传递的过程,①②分别代表不同的细胞,A表示物质,符合该模型的是( )
A.①效应T细胞,②被病原体侵染的细胞,A抗体
B.①传入神经元,②神经中枢的神经元,A神经递质
C.①胰岛A细胞,②肝细胞,A胰高血糖素
D.①甲状腺细胞,②下丘脑细胞,A甲状腺激素 qqVV天使1年前1
qqVV天使1年前1 -
 葛格 共回答了17个问题
葛格 共回答了17个问题 |采纳率82.4%解题思路:①和②之间通过信号分子进行信息交流,其化学本质可以是抗体、神经递质或者各种激素,但要正确分析细胞之间的关系.该模型表示的是细胞①产生物质A,分泌到细胞外,并作用在细胞②细胞膜上的特异性受体上.A、效应T细胞和被病原体侵染的细胞都与细胞免疫相关,但抗体却是体液免疫中的物质,是效应B细胞产生的,故A错误;
B、传入神经元与神经中枢的神经元是通过突触相连的,突触前膜可以释放神经递质作用于突触后膜,故B正确;
C、胰岛A细胞能够分泌胰高血糖素,胰高血糖素可以促进肝脏中肝糖原的分解和非糖物质的转化,从而使血糖含量升高,故C正确;
D、甲状腺细胞分泌的甲状腺激素可以抑制下丘脑的分泌细胞,属于负反馈调节,故D正确.
故选BCD.点评:
本题考点: 神经、体液调节在维持稳态中的作用;人体免疫系统在维持稳态中的作用.
考点点评: 本题考查相对综合,考查细胞之间的信息交流的相关知识,考查了考生获取图示信息的能力、审题能力、分析问题能力.1年前查看全部
- (2011•镇江模拟)珠江三角洲与港澳地区合作的独特模式是( )
(2011•镇江模拟)珠江三角洲与港澳地区合作的独特模式是( )
A.“前店后厂”
B.“前厂后店”
C.“厂店联合”
D.“厂厂合作” xudejin1年前1
xudejin1年前1 -
 农妇3拳 共回答了17个问题
农妇3拳 共回答了17个问题 |采纳率100%解题思路:香港特别行政区位于珠江口的东侧,北邻深圳.澳门特别行政区位于珠江口的西侧,北邻珠海.
珠江三角洲位于广东省的东南部,毗邻港澳,与东南亚地区隔海相望,被称为我国的“南大门”.位于本区的经济特区有深圳和珠海.1985年,整个珠江三角洲被辟为沿海经济开放区.该地区依靠优越的地理位置、政策的优惠及人文因素的优势,重点发展了外向型经济.珠江三角洲和港澳的关系非常密切,其合作形式以“前店后厂”为基本模式,港澳为珠江三角洲提供丰富的资金、技术和管理经验,控制产品的质量,进行市场推广和对外营销,扮演“店”的角色.而珠江三角洲为港澳提供土地、自然资源和劳动力,进行产品的加工、制造和装配,扮演“厂”的角色.
故选:A.点评:
本题考点: 珠江三角洲工业基地的位置和特点.
考点点评: 本题考查了珠江三角洲与港澳地区合作的独特模,属基础题,识记.1年前查看全部
- (2014•镇江二模)已知不等式|a-2|≤x2+2y2+3z2对满足x+y+z=1的一切实数x,y,z都成立,求实数a
(2014•镇江二模)已知不等式|a-2|≤x2+2y2+3z2对满足x+y+z=1的一切实数x,y,z都成立,求实数a的取值范围.
 伊婉儿M1年前1
伊婉儿M1年前1 -
 阿弥陀佛55562 共回答了21个问题
阿弥陀佛55562 共回答了21个问题 |采纳率85.7%解题思路:不等式|a-2|≤x2+2y2+3z2恒成立,只要|a-2||≤(x2+2y2+3z2)min,利用柯西不等式求出x2+2y2+3z2的最小值,再解关于a的绝对值不等式即可.因为已知x,y,z是实数,且x+y+z=1,
根据柯西不等式(a2+b2+c2)(x2+y2+z2)≥(ax+by+cz)2
故有(x2+2y2+3z2)(1+[1/2]+[1/3])≥(x+y+z)2
故x2+2y2+3z2≥[6/11],当且仅当x=[6/11],y=[3/11],z=[2/11]时取等号,
∵不等式|a-2|≤x2+2y2+3z2对满足x+y+z=1的一切实数x,y,z都成立,
∴|a-2|≤[6/11],
∴[16/11]≤a≤[28/11].点评:
本题考点: 二维形式的柯西不等式.
考点点评: 本题主要考查了柯西不等式求解最值的应用及函数的恒成立与最值的相互转化关系的应用.1年前查看全部
- (2014•镇江模拟)所有的营养成分都通过小肠绒毛中的毛细血管直接吸收进入血液.______.(判断对错)
 psongmagic1年前1
psongmagic1年前1 -
 秦之梦 共回答了11个问题
秦之梦 共回答了11个问题 |采纳率90.9%解题思路:食物中含有维生素、水和无机盐等小分子的营养物质人体可以直接吸收利用,而蛋白质、糖类、脂肪这些大分子的营养物质是不溶于水的,必须在消化道内变成小分子的能溶于水的物质后,才能被消化道壁吸收.营养物质通过消化道壁进入循环系统的过程叫做吸收;葡萄糖、氨基酸、维生素、无机盐、水等营养物质透过消化道壁进入小肠绒毛内的毛细血管里,而由脂肪分解形成的甘油和脂肪酸等营养物质透过消化道壁进入了小肠绒毛内的毛细淋巴管里.
故答案为:×点评:
本题考点: 食物的消化和营养物质的吸收过程.
考点点评: 消化后营养物质的去路是有所区别的,大部分的脂肪成分先是进入淋巴循环,然后再汇入血液循环.1年前查看全部
- (2012•镇江一模)如图所示,甲、乙两个相邻的工厂向河水中排放的废水中分别含有CuSO4、NaOH、BaCl2、FeC
 (2012•镇江一模)如图所示,甲、乙两个相邻的工厂向河水中排放的废水中分别含有CuSO4、NaOH、BaCl2、FeCl3四种物质中的两种.某中学环保小组对河水取样测试时发现A处河水的pH>7.
(2012•镇江一模)如图所示,甲、乙两个相邻的工厂向河水中排放的废水中分别含有CuSO4、NaOH、BaCl2、FeCl3四种物质中的两种.某中学环保小组对河水取样测试时发现A处河水的pH>7.
试回答:
(1)甲厂排放的废水中,含有的两种物质是______乙厂排放的废水中,含有的两种物质是______(用化学式表示)
(2)请你从环境保护的角度出发,给甲、乙两厂提出合理化建议:______最后得到NaCl溶液.
写出有关的方程式______,______(要求只要写出两个碱和盐的反应) xyz_00001年前1
xyz_00001年前1 -
 我是Btt 共回答了19个问题
我是Btt 共回答了19个问题 |采纳率84.2%解题思路:根据物质的性质进行分析,A处河水的pH>7,则A处河水呈碱性,含有氢氧化钠,氢氧化钠能与硫酸铜和氯化铁反应,故A处不会含有硫酸铜和氯化铁,硫酸铜和氯化铁应该是乙厂排放的废水,氯化钡是甲厂排放的废水;硫酸铜能与氯化钡反应生成硫酸钡沉淀,氢氧化钠与氯化铁、硫酸铜反应分别生成氢氧化铁沉淀、氢氧化铜沉淀,所以两厂的废水混合后能产生沉淀,从而除去有害离子而达到初步净化的目的.(1)A处河水的pH>7,则A处河水呈碱性,含有氢氧化钠,氢氧化钠能与硫酸铜和氯化铁反应,故A处不能含有硫酸铜和氯化铁,硫酸铜和氯化铁应该是乙厂排放的废水,由于每厂排放的废水成分有两种,故氯化钡是甲厂排放的废水;
(2)硫酸铜能与氯化钡反应生成硫酸钡沉淀,氢氧化钠与氯化铁、硫酸铜反应分别生成氢氧化铁沉淀、氢氧化铜沉淀,所以两厂的废水混合后能产生沉淀,然后将沉淀过滤得到得到NaCl溶液,从而除去有害离子而达到初步净化的目的;
故答案为:(1)NaOH、BaCl2;CuSO4、FeCl3;
(2)两厂联合建立废水处理厂,将两厂废水混合、沉淀,过滤;FeCl3+3NaOH═Fe(OH)3↓+3NaCl;2NaOH+CuSO4=Na2SO4+Cu(OH)2↓.点评:
本题考点: 酸、碱性废水的处理;溶液的酸碱性与pH值的关系;离子或物质的共存问题.
考点点评: 本题考查了物质的共存和废水的处理问题,可以依据物质的性质结合题意进行分析解答.1年前查看全部
- (2003•镇江)酸雨是pH<5.6的降水,我国南方某地区所降酸雨主要是由居民和工厂燃烧含硫的煤以及某些化工厂生产过程中
(2003•镇江)酸雨是pH<5.6的降水,我国南方某地区所降酸雨主要是由居民和工厂燃烧含硫的煤以及某些化工厂生产过程中排放的一种无色有刺激性气味的气体经一系列化学反应而形成,有许多植物如广玉兰、夹竹桃等在它们能忍受的浓度下可以吸收这种有害气体.
(1)你认为该有害气体是二氧化硫二氧化硫.
(2)请写出测定地区雨水的pH操作方法用玻璃棒蘸取雨水,滴在PH试纸上,再与标准比色卡对照用玻璃棒蘸取雨水,滴在PH试纸上,再与标准比色卡对照.
(3)为减少酸雨对该地区环境的危害,请你提出两条合理化建议 减少煤的燃烧,化工厂的尾气处理后再排放. lycyb1年前1
lycyb1年前1 -
 wyw8n6jy 共回答了19个问题
wyw8n6jy 共回答了19个问题 |采纳率94.7%(1)煤燃烧生成二氧化硫等气体,二氧化硫是形成酸雨的主要气体.故填:二氧化硫.
(2)用玻璃棒蘸取雨水,滴在pH试纸上,再与标准比色卡对照.
(3)减少煤的燃烧,化工厂的尾气处理后再排放.1年前查看全部
- (2011•镇江一模)下图是某空间站能量转化系统局部示意图,其中水电解系统及燃料电池系统中的溶液均采用KOH溶液.下列有
(2011•镇江一模)下图是某空间站能量转化系统局部示意图,其中水电解系统及燃料电池系统中的溶液均采用KOH溶液.下列有关说法错误的是( )

A.该能量转化系统中的水可以循环使用
B.水电解系统实现由电能到化学能的转化,燃料电池系统实现由化学能到电能的转化
C.水电解系统中的溶液采用KOH溶液,是为了增强水的导电性
D.燃料电池系统产生的能量实际上来自于水 _小新_1年前1
_小新_1年前1 -
 xbox44 共回答了18个问题
xbox44 共回答了18个问题 |采纳率77.8%解题思路:根据空间站能量转化系统局部示意图,利用水的分解反应和燃料电池中的反应来分析反应中的能量变化.A、由转化图可知,该系统中水既可分解也可生成,是循环使用的,说法正确,故A错误;
B、水电解是电能转化为化学能,燃料电池是利用化学反应产生能量,则是化学能转变为电能,说法正确,故B错误;
C、水电解系统中的溶液采用KOH溶液,使离子的浓度变大,导电性增强,说法正确,故C错误;
D、燃料电池系统产生的能量来源于所发生的化学反应,则说法错误,故D正确.
故选D.点评:
本题考点: 物质发生化学变化时的能量变化;电解水实验;溶液的导电性及其原理分析.
考点点评: 本题利用信息来考查化学与能源问题,注重了与生活实际的紧密联系,也体现了利用所学课本知识能够学以致用.1年前查看全部
- (2014•镇江模拟)下列四种溶液,不用其他任何试剂,只需组内两两物质间反应,就能加以鉴别的是( )
(2014•镇江模拟)下列四种溶液,不用其他任何试剂,只需组内两两物质间反应,就能加以鉴别的是( )
A.HNO3、NaOH、Na2CO3、HCl
B.HCl、Na2CO3、CaCl2、NaNO3
C.FeCl3、NaOH、H2SO4、Ba(OH)2
D.K2SO4、CuSO4、NaOH、NaNO3 zoe_yeun1年前1
zoe_yeun1年前1 -
 gyn1228 共回答了15个问题
gyn1228 共回答了15个问题 |采纳率73.3%解题思路:不用其他试剂,就能将组内物质鉴别出来,首先需考虑物质的颜色,然后将鉴别出来的物质与其他物质混合,根据现象的不同加以鉴别,若物质都是没有颜色,则让溶液之间两两混合,根据不同的实验现象加以鉴别.A、碳酸钠和盐酸、硝酸混合都能够产生气泡,无现象的是氢氧化钠,可以鉴别出氢氧化钠,但不能鉴别盐酸和硝酸,故A不可选;
B、碳酸钠能和盐酸反应生成气体、与氯化钙反应生成白色沉淀,所以既有气体又有沉淀生成的为碳酸钠,只有气体生成的为盐酸,只有沉淀生成的为氯化钙,无现象的为硝酸钠,不加任何试剂可以鉴别,故B可选;
C、氯化铁溶液为黄色,根据溶液颜色,首先鉴别出氯化铁,然后将氯化铁与其他三种物质混合,能产生红褐色沉淀的是氢氧化钠和氢氧化钡,无现象的为硫酸,最后将硫酸滴加氢氧化钠和氢氧化钡溶液中,有白色沉淀生成的为氢氧化钡,无现象的为氢氧化钠,不加任何试剂可以鉴别,故C可选.
D、硫酸铜溶液为蓝色,根据溶液颜色,首先鉴别出硫酸铜,然后将硫酸铜与其他三种物质混合,能产生蓝色沉淀的是氢氧化钠,但不能鉴别硫酸钾和硝酸钠,故D不可选;
故选BC.点评:
本题考点: 酸、碱、盐的鉴别.
考点点评: 不加任何试剂的物质的鉴别题时,主要分为两类:一是类选项中的有带色的离子,首先鉴别,然后再区别其他的物质,另一类就是需要鉴别物质都是无色的,就需要互滴进行鉴别,不管哪种,在鉴别时每组出现的现象不能完全相同.1年前查看全部
- (2005•镇江)下列实验操作错误的是( )
(2005•镇江)下列实验操作错误的是( )
A.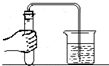 检查装置的气密性
检查装置的气密性
B. 点燃酒精灯
点燃酒精灯
C. 过滤
过滤
D. 加热液体
加热液体  yan02101年前1
yan02101年前1 -
 西狂杨过 共回答了14个问题
西狂杨过 共回答了14个问题 |采纳率85.7%解题思路:A、根据检查装置的气密性的步骤进行解答;
B、根据实验室中应用火柴点燃酒精灯,绝对禁止拿一盏酒精灯去引燃另一盏酒精灯,以免酒精流出着火;
C、根据过滤实验要考虑“一低二贴三靠”的原则进行解答;
D、根据液体加热的注意事项进行解答.A、由检查装置的气密性的步骤可知该实验操作正确,故a正确;
B、实验室中应用火柴点燃酒精灯,绝对禁止拿一盏酒精灯去引燃另一盏酒精灯,以免酒精流出着火,故B错误;
C、过滤实验时,滤纸要紧贴漏斗内壁;滤纸边缘要低于漏斗边缘,漏斗内液体的液面低于滤纸边缘;烧杯嘴紧靠引流的玻璃棒,玻璃棒的末端轻靠在三层滤纸的一边,漏斗下端紧靠接受的烧杯,故C正确;
D、给试管里的液体加热时,为避免液体沸腾而喷出伤人.试管内液体不能超过试管容积的1/3,故D正确.
故选:B.点评:
本题考点: 检查装置的气密性;加热器皿-酒精灯;给试管里的液体加热;过滤的原理、方法及其应用.
考点点评: 本题考查以图示的方法考查化学实验基本操作.图示法形象生动,便于巩固对化学实验基本操作的理解.1年前查看全部
- (2008•镇江)某研究性学习小组对能量转化现象进行了研究,他们利用铁丝、镍铬丝、灵敏电流计等器材组成一个闭合电路,如图
 (2008•镇江)某研究性学习小组对能量转化现象进行了研究,他们利用铁丝、镍铬丝、灵敏电流计等器材组成一个闭合电路,如图所示,A点为铁丝和镍锤绞合在一起组成的加热点.用打火机给A点加热时,观察到灵敏电流计的指针发生了明显偏转,这一实验现象说明了______能可以转化成______能.
(2008•镇江)某研究性学习小组对能量转化现象进行了研究,他们利用铁丝、镍铬丝、灵敏电流计等器材组成一个闭合电路,如图所示,A点为铁丝和镍锤绞合在一起组成的加热点.用打火机给A点加热时,观察到灵敏电流计的指针发生了明显偏转,这一实验现象说明了______能可以转化成______能.  多事之冬1年前1
多事之冬1年前1 -
 李军8888 共回答了24个问题
李军8888 共回答了24个问题 |采纳率91.7%解题思路:不同形式的能之间在适当条件下是可以相互转化的.如图,用打火机给A点加热时,A点的温度升高,内能增加,这时,灵敏电流计的指针发生了明显的偏转,说明电路中有电流产生,也就是说,内能转化成了电能.
故答案为:内;电.点评:
本题考点: 能量的转化.
考点点评: 该题的关键是:由灵敏电流计的指针发生了明显的偏转,可以知道,闭合电路中有微小的电流产生.1年前查看全部
- (2003•镇江)现有初中化学中常见的易溶于水的三种盐组成的混合物,将其溶于水后得到无色溶液A,进行如下实验:
(2003•镇江)现有初中化学中常见的易溶于水的三种盐组成的混合物,将其溶于水后得到无色溶液A,进行如下实验:

试回答下列问题:
(1)该混合物中含有的三种易溶于水的盐分别是(填化学式)Na2CO3Na2CO3、Na2SO4Na2SO4、NaClNaCl;
(2)确定钡盐B溶液中所含阴离子的实验方法是(简述实验操作步骤、现象和结论):取该钡盐溶液少量于试管中,滴入几滴硝酸银溶液,有白色沉淀生成,再滴加稀硝酸,沉淀不溶解,证明该钡盐溶液中所含的阴离子为氯离子.取该钡盐溶液少量于试管中,滴入几滴硝酸银溶液,有白色沉淀生成,再滴加稀硝酸,沉淀不溶解,证明该钡盐溶液中所含的阴离子为氯离子.. gougou05121年前1
gougou05121年前1 -
 smlty 共回答了14个问题
smlty 共回答了14个问题 |采纳率92.9%(1)由框图可知,白色沉淀部分溶于稀硝酸,且有气体产生,说明该沉淀为碳酸钡和硫酸钡的混合物,无色溶液A中含有碳酸根离子和硫酸根离子;无色溶液F蒸发结晶,析出氯化钠晶体,说明无色溶液F中含有钠离子和氯离子;由以上可知无色溶液A和钡盐中有碳酸根离子、硫酸根离子、氯离子、钡离子四种离子,混合物中的三种盐为碳酸钠、硫酸钠、氯化钠,钡盐为氯化钡;
(2)由(1)推断可知钡盐溶液中含有的阴离子为氯离子,取该钡盐溶液少量于试管中,滴入几滴硝酸银溶液,有白色沉淀生成,再滴加稀硝酸,沉淀不溶解,证明该钡盐溶液中所含的阴离子为氯离子.
故答案为:(1)Na2CO3,Na2SO4,NaCl;
(2)取该钡盐溶液少量于试管中,滴入几滴硝酸银溶液,有白色沉淀生成,再滴加稀硝酸,沉淀不溶解,证明该钡盐溶液中所含的阴离子为氯离子.1年前查看全部
- (2012•镇江一模)A、B可发生中和反应,D是生活中最常见的液体.通常情况下,F、G、I为气体,且F是一种清洁能源.x
(2012•镇江一模)A、B可发生中和反应,D是生活中最常见的液体.通常情况下,F、G、I为气体,且F是一种清洁能源.x是目前应用最广泛的金属,y常用作食品干燥剂.各物质间的转化关系如图所示(个别产物略去).
 (1)B俗称______.B溶液可用来检验二氧化碳,其反应的化学方程式为______.
(1)B俗称______.B溶液可用来检验二氧化碳,其反应的化学方程式为______.
(2)反应⑤中,将B的固体粉末与(NH4)2SO4等混合研磨,可区别______肥与钾肥.
(3)反应③发生时放出大量热,化学方程式为______.反应④的实验现象是______ 方程式3Fe+2O2
Fe3O4点燃 .3Fe+2O2
Fe3O4点燃 .
(4)金属x也能与硫酸铜溶液反应,其化学方程式为______.反应②的化学方程式为______. 米781年前1
米781年前1 -
 jolene78 共回答了23个问题
jolene78 共回答了23个问题 |采纳率91.3%解题思路:找准解题突破口,直接得出物质的化学式,F是一种清洁能源,说明F是氢气,x是目前应用最广泛的金属,说明X是铁,y常用作食品干燥剂,说明y是氧化钙,A、B可发生中和反应,说明AB是酸和碱的反应,D是生活中最常见的液体,说明D是水,然后逐步推导得出其他物质的化学式.(1)B能用来检验二氧化碳的存在,说明B是氢氧化钙,俗称熟石灰或消石灰;
故本题答案为:熟石灰或消石灰,CO2+Ca(OH)2=CaCO3↓+H2O;
(2)将B的固体粉末与(NH4)2SO4等混合研磨,则铵态氮肥遇碱能生成有刺激性气味的气体,可区别氮肥和钾肥;
故本题答案为:铵态氮;
(3)是生活中最常见的液体,说明D是水,能通电分解生成氢气和氧气,F是一种清洁能源,说明F是氢气,则G是氧气,y常用作食品干燥剂,能与水反应生成氢氧化钙,说明y是氧化钙,x是目前应用最广泛的金属,说明x是铁,铁和氧气在点燃的条件下生成四氧化三铁,燃烧的现象是:剧烈燃烧,火星四射,放出热量,生成黑色固体;
故本题答案为:CaO+H2O=Ca(OH)2,剧烈燃烧,火星四射,生成黑色固体;3Fe+2O2
点燃
.
Fe3O4
(4)铁能与硫酸铜反应生成硫酸亚铁和铜,A、B可发生中和反应,则A为酸,能与铁反应生成氯化亚铁,说明A是盐酸,与氢氧化钙反应生成了氯化钙,氯化钙能与碳酸钠反应生成碳酸钙沉淀和氯化钠;
故本题答案为:Fe+CuSO4=FeSO4+Cu,CaCl2+Na2CO3═CaCO3↓+2NaCl.点评:
本题考点: 物质的鉴别、推断;铵态氮肥的检验;化学式的书写及意义;书写化学方程式、文字表达式、电离方程式.
考点点评: 此题为框图式物质推断题,完成此类题目,关键是找准解题突破口,直接得出结论,然后利用顺向或逆向或两边向中间推,逐一导出其他结论.1年前查看全部
- (2008•镇江模拟)如图所示为小灯泡的UI图线,若将该小灯泡与一节电动势E=1.5V,内阻r=0.75Ω的干电池组成闭
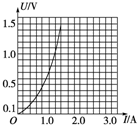 (2008•镇江模拟)如图所示为小灯泡的UI图线,若将该小灯泡与一节电动势E=1.5V,内阻r=0.75Ω的干电池组成闭合电路时,电源的总功率和小灯泡的实际电功率分别接近以下哪一组数据( )
(2008•镇江模拟)如图所示为小灯泡的UI图线,若将该小灯泡与一节电动势E=1.5V,内阻r=0.75Ω的干电池组成闭合电路时,电源的总功率和小灯泡的实际电功率分别接近以下哪一组数据( )
A.1.5 W 1.0 W
B.0.75 W 0.5 W
C.0.75 W 0.75 W
D.1.5 W 0.75 W wangyejun8811年前0
wangyejun8811年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2013•镇江二模)有一包白色固体,可能含有氯化钡、硝酸钾、硫酸铜、氯化钠、碳酸钠、硫酸钠中某几种.(1)取该固体混合
(2013•镇江二模)有一包白色固体,可能含有氯化钡、硝酸钾、硫酸铜、氯化钠、碳酸钠、硫酸钠中某几种.(1)取该固体混合物溶于水,有白色沉淀生成,经过滤,得到无色滤液;(2)在白色沉淀中加稀硝酸,沉淀部分溶解;(3)在滤液中滴入硝酸银溶液,生成不溶于稀硝酸的白色沉淀.由此可见:
①混合物中一定有______、______、______;肯定没有______.(填化学式)
②写出步骤(1)(2)反应中的化学方程式:______;______. sunao19991年前1
sunao19991年前1 -
 sulash 共回答了22个问题
sulash 共回答了22个问题 |采纳率90.9%解题思路:找出突破口:①将混合物溶于水,有白色沉淀生成,经过滤,得到无色滤液,一定不存在蓝色的硫酸铜;在白色沉淀中加稀硝酸,沉淀部分溶解,则白色沉淀为碳酸钡或硫酸钡,一定存在碳酸钠、硫酸钠、氯化钡;②加入硝酸银溶液,生成白色氯化银沉淀,加稀硝酸,沉淀不消失,说明含有氯离子,但是氯化钡中的氯离子也会生成沉淀,对于氯化钠有没有不影响现象;对于硝酸钾题中的现象不能确定;据此得出结论.(1)①将混合物溶于水,有白色沉淀生成,经过滤,得到无色滤液,则白色沉淀可能为碳酸钡或硫酸钡,说明一定有钡离子;一定没有硫酸铜,因为硫酸铜是“蓝色溶液”;
②白色沉淀中加入稀硝酸,沉淀一部分消失,说明白色沉淀为碳酸钡或硫酸钡;因为碳酸钡与硝酸反应生成二氧化碳气体,而硫酸钡不与硝酸反应,说明一定含有碳酸钠和硫酸钠;
③加入硝酸银溶液,生成白色沉淀,加稀硝酸,沉淀不消失:则沉淀为氯化银;而氯离子可能来自氯化钡或氯化钠,因此无法确定是否含有氯化钠.
故答案为:①混合物中一定有 Na2CO3、Na2SO4、BaCl2;肯定没有 CuSO4;
②步骤(1)发生的反应方程式:Na2CO3+BaCl2=BaCO3↓+2NaCl,Na2SO4+BaCl2=BaSO4↓+2NaCl;
(2)反应的方程式:BaCO3+2HNO3=Ba(NO3)2+H2O+CO2↑.点评:
本题考点: 物质的鉴别、推断;化学式的书写及意义;书写化学方程式、文字表达式、电离方程式.
考点点评: 推断题在解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口,导出结论,最后别忘了把结论代入原题中验证;本题主要考查了碳酸根离子,硫酸根离子及氯离子的检验方法,在检验硫酸根离子和氯离子是要注意防止碳酸根离子的干扰.1年前查看全部
- (2013•镇江模拟)如图,已知一次函数y=ax-2的图象与反比例函数y=[k/x]的图象交于A(k,a),B两点.
 (2013•镇江模拟)如图,已知一次函数y=ax-2的图象与反比例函数y=[k/x]的图象交于A(k,a),B两点.
(2013•镇江模拟)如图,已知一次函数y=ax-2的图象与反比例函数y=[k/x]的图象交于A(k,a),B两点.
(1)求a,k的值;
(2)求B点的坐标;
(3)不等式ax-2<[k/x]的解集是______(直接写出答案) 红色04外衣1年前1
红色04外衣1年前1 -
 粉晶百合 共回答了23个问题
粉晶百合 共回答了23个问题 |采纳率78.3%解题思路:(1)先把把A(k,a)代入反比例函数解析式可计算出a=1,然后把A点坐标代入一次函数解析式可计算出k的值;
(2)解由两解析式所组成的方程组可确定B点坐标;
(3)观察函数图象得到当x<-1或0<x<3时,一次函数图象都在反比例函数图象下方,即ax-2<[k/x].(1)把A(k,a)代入y=[k/x]得a=[k/k]=1,
所以A点坐标为(k,1),
把A(k,1)代入y=ax-2得k-2=1,解得k=3,
所以a的值为1,k的值为3;
(2)解方程组
y=x−2
y=
3
x
x=3
y=1或
x=−1
y=−3,
所以B点坐标为(-1,-3);
(3)x<-1或0<x<3.点评:
本题考点: 反比例函数与一次函数的交点问题.
考点点评: 本题考查了反比例函数与一次函数的交点问题:反比例函数与一次函数的交点坐标满足两函数的解析式.也考查了观察函数图象的能力.1年前查看全部
- (2010•镇江一模)根据所给提示,请用化学符号填空:
(2010•镇江一模)根据所给提示,请用化学符号填空:
(1)氩气 ______;(2) 汽水中含有的不稳定的酸 ______;
(3) 某气体在空气中占78%(体积百分含量),表示出它的8个分子 ______;
(4)温度计中填充的金属是 ______;(5)地壳中含量最多的金属元素 ______. buike1年前1
buike1年前1 -
 martinguan1013 共回答了21个问题
martinguan1013 共回答了21个问题 |采纳率100%解题思路:本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目.(1)原子的表示方法就是用元素符号来表示一个原子,
(2)分子的表示方法:正确书写物质的化学式,如碳酸分子是多原子分子,可表示为:H2CO3,表示多个分子,就在其化学式前加上相应的数字,所以3个氮气分子可表示为8N2.
(3)氩是稀有气体元素,由稀有气体元素组成的单质是单原子分子,所以氩气的化学式就是表示氖元素的元素符号Ar,
故答为:(1)Ar(2)H2CO3(3)8N2.(4)Hg,(5)Al点评:
本题考点: 化学符号及其周围数字的意义.
考点点评: 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.1年前查看全部
- (2013•镇江)写一个你喜欢的实数m的值______,使关于x的一元二次方程x2-x+m=0有两个不相等的实数根.
 kusnilac1年前1
kusnilac1年前1 -
 8ag5lz 共回答了19个问题
8ag5lz 共回答了19个问题 |采纳率84.2%根据题意得:△=1-4m>0,
解得:m<[1/4],
则m可以为0,答案不唯一.
故答案为:01年前查看全部
- (2010•镇江)“海宝”是2010年上海世博会的吉祥物,其形象如图所示.在点缀街头的各种“海宝”中,有一座“海宝”(材
 (2010•镇江)“海宝”是2010年上海世博会的吉祥物,其形象如图所示.在点缀街头的各种“海宝”中,有一座“海宝”(材质均匀、实心)的质量为1.0×103kg,体积为2m3,与水平地面的接触面积为1m2(g=10N/kg).则“海宝”的密度是______kg/m3;“海宝”对地面的压强是______Pa.
(2010•镇江)“海宝”是2010年上海世博会的吉祥物,其形象如图所示.在点缀街头的各种“海宝”中,有一座“海宝”(材质均匀、实心)的质量为1.0×103kg,体积为2m3,与水平地面的接触面积为1m2(g=10N/kg).则“海宝”的密度是______kg/m3;“海宝”对地面的压强是______Pa.  rafaelkevin1年前1
rafaelkevin1年前1 -
 临阵租枪 共回答了18个问题
临阵租枪 共回答了18个问题 |采纳率94.4%解题思路:算密度可直接根据密度公式ρ=[m/v]进行计算;先根据G=mg算出“海宝”的重力,然后根据P=[F/S]算出“海宝”对地面的压强.“海宝”的密度:ρ=[m/v]=
1.0×103kg
2m3=0.5×103kg/m3;
“海宝”的重力:G=mg=1.0×103kg×10N/kg=104N;
“海宝”对地面的压强:P=[F/S]=[G/S]=
104N
1m2=104Pa.
故答案为:0.5×103;104.点评:
本题考点: 密度的计算;压强的大小及其计算.
考点点评: 本题考查了密度和压强大小的计算,属于比较简单的计算题,这类计算题多以填空题出现.1年前查看全部
- (2010•镇江模拟)关于x的方程exlnx=1的实根个数是______.
 torchyben1年前1
torchyben1年前1 -
 wens0104 共回答了19个问题
wens0104 共回答了19个问题 |采纳率100%解题思路:已知方程exlnx=1,移项构造形函数f(x)=exlnx-1,然后对其进行求导,求出其值域即可求解.∵方程exlnx=1,
∴令f(x)=exlnx-1,
∴f′(x)=exlnx+
ex
x=ex(lnx+[1/x]),
∴令f′(x)=0,可得ex(lnx+[1/x])=[xlnx+1/x]=0,
∴xlnx+1=0,
令g(x)=xlnx+1,
∴g′(x)=lnx+1=0,
解得x=[1/e],
当x>
1
e时 g(x)为增函数,
当x<[1/e]时,g(x)为减函数,
∴g(x)的极小值也是最小值为g([1/e])=-[1/e]+1>0,
∴f(x)为单调增函数,
f([1/e])=e
1
e×(-1)-1<0,
∴方程exlnx=1的实根个数是1个,
故答案为1.点评:
本题考点: 根的存在性及根的个数判断.
考点点评: 此题考查方程根的存在性及其性质,解题的关键是利用导数来判断函数的单调性,要学会构造函数的思想,此题是一道好题.1年前查看全部
- (2014•镇江模拟)被欧洲西部的人们称为“绿色金子”的是( )
(2014•镇江模拟)被欧洲西部的人们称为“绿色金子”的是( )
A.小麦
B.绿宝石
C.牧草
D.水稻 dicklxh1年前1
dicklxh1年前1 -
 四掌柜 共回答了15个问题
四掌柜 共回答了15个问题 |采纳率86.7%解题思路:被欧洲西部人们称为“绿色金子”的是牧草,当地人们大力发展了畜牧业.欧洲是平均海拔最低的大洲,欧洲西部地形以平原为主,西部沿海地区有北大西洋暖流经过,加上西风的影响,形成温带海洋性气候,冬无严寒,夏无酷暑,一年内降水均匀,牧草生长茂盛,被欧洲西部的人们称为“绿色金子”,畜牧业发达.
故选:C.点评:
本题考点: 欧洲温带海洋性气候和地中海气候的特征.
考点点评: 此题考查的有关欧洲人民的生活概况,点出畜牧业在该区域发展的重要性,结合教材理解记忆.1年前查看全部
- 下列属于天气的说法是( ) A.明天大风降温 B.昆明四季如春 C.镇江夏季高温多雨 D.极地全年严寒
 SUPER50001年前1
SUPER50001年前1 -
 孤单小猪暴走 共回答了13个问题
孤单小猪暴走 共回答了13个问题 |采纳率84.6%天气是指某个地方距离地表较近的大气层在短时间内的具体状态,具有多变性;气候是指一个地方多年的天气平均状况,它具有相对的稳定性.选项A说的是天气;选项B、C、D说的是气候.
故选:A.1年前查看全部
- (2003•镇江)如图,正方形ABCD中,E为CD上一点,F为BC延长线上一点,CE=CF.
 (2003•镇江)如图,正方形ABCD中,E为CD上一点,F为BC延长线上一点,CE=CF.
(2003•镇江)如图,正方形ABCD中,E为CD上一点,F为BC延长线上一点,CE=CF.
(1)求证:△BCE≌△DCF;
(2)若∠BEC=60°,求∠EFD的度数. xjzy5201年前1
xjzy5201年前1 -
 judo_yoga 共回答了18个问题
judo_yoga 共回答了18个问题 |采纳率77.8%解题思路:(1)根据正方形的性质及全等三角形的判定方法即可证明△BCE≌△DCF;
(2)由两个三角形全等的性质得出∠CFD的度数,再用等腰三角形的性质求∠EFD的度数.(1)证明:∵ABCD是正方形,
∴DC=BC,∠DCB=∠FCE,
∵CE=CF,
∴△DCF≌△BCE;
(2)∵△BCE≌△DCF,
∴∠DFC=∠BEC=60°,
∵CE=CF,
∴∠CFE=45°,
∴∠EFD=15°.点评:
本题考点: 正方形的性质;全等三角形的判定与性质.
考点点评: 此题主要考查正方形的特殊性质及全等三角形的判定的综合运用.1年前查看全部
- (2010•镇江)如图所示,通过灯泡L1、L2中的电流分别为0.2A和0.3A,电源电压保持不变,L1的电阻为15Ω,则
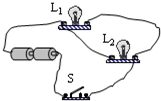 (2010•镇江)如图所示,通过灯泡L1、L2中的电流分别为0.2A和0.3A,电源电压保持不变,L1的电阻为15Ω,则干路电流为______A,电源电压是______V,L2的电阻为______Ω.
(2010•镇江)如图所示,通过灯泡L1、L2中的电流分别为0.2A和0.3A,电源电压保持不变,L1的电阻为15Ω,则干路电流为______A,电源电压是______V,L2的电阻为______Ω.  03111120361年前1
03111120361年前1 -
 寒亭渡鹤影 共回答了14个问题
寒亭渡鹤影 共回答了14个问题 |采纳率85.7%解题思路:(1)分析电路图确认两灯的连接方式为并联,根据并联电路的电流特点求干路电流;
(2)知道L1的电阻和通过的电流,利用欧姆定律可以求灯两端的电压(电源电压);
(3)知道电源电压和通过L2的电流,利用欧姆定律可以求L2的电阻.(1)∵两个电灯并联,
∴I=I1+I2=0.2A+0.3A=0.5A;
(2)U=U2=U1=I1R1=0.2A×15Ω=3V;
(3)R2=
U2
I2=
3V
0.3A=10Ω;
故答案为:0.5,3,10.点评:
本题考点: 欧姆定律的应用.
考点点评: 灵活运用并联电路的特点和欧姆定律及变形公式,使用欧姆定律时注意三量(I、U、R)同体.1年前查看全部
- (2014•海陵区一模)小丽乘坐汽车从泰州到镇江奶奶家,她去时经过启扬高速,全程约84千米,返回时经过泰州大桥,全程约5
(2014•海陵区一模)小丽乘坐汽车从泰州到镇江奶奶家,她去时经过启扬高速,全程约84千米,返回时经过泰州大桥,全程约55千米,小丽去时所乘汽车的平均速度是返回时的1.2倍,所用时间却比返回多20分钟.求小丽所乘汽车返回时的平均速度.
 xiaonizi00741年前1
xiaonizi00741年前1 -
 dsk118 共回答了18个问题
dsk118 共回答了18个问题 |采纳率94.4%解题思路:设小丽所乘汽车返回时的平均速度为x千米/小时,则去时所乘汽车的平均速度为1.2x千米/小时,根据去时比返回用时多20分钟,列方程求解.设小丽所乘汽车返回时的平均速度为x千米/小时,则去时所乘汽车的平均速度为1.2x千米/小时,
由题意得,[84/1.2x]-[55/x]=[1/3],
解得:x=45,
经检验:x=45是原方程的解,且符合题意.
答:小丽所乘汽车返回时的平均速度45千米/小时.点评:
本题考点: 分式方程的应用.
考点点评: 本题考查了分式方程的应用,解答本题的关键是读懂题意,设出未知数,找出合适的等量关系,列方程求解.1年前查看全部
- (2005•镇江)葡萄糖是一种有甜味、易溶于水的白色粉状固体,化学式是C6H12O6.葡萄糖在人体内发生缓慢氧化转化为二
(2005•镇江)葡萄糖是一种有甜味、易溶于水的白色粉状固体,化学式是C6H12O6.葡萄糖在人体内发生缓慢氧化转化为二氧化碳和水并释放出热量.试回答:
(1)每个葡萄糖分子共有______个原子;
(2)葡萄糖分子的相对分子质量______;
(3)葡萄糖中各元素的质量比C:H:O=______;
(4)列式计算葡萄糖中碳元素的质量分数. rr人都是大SB1年前1
rr人都是大SB1年前1 -
 wzy0515 共回答了21个问题
wzy0515 共回答了21个问题 |采纳率95.2%解题思路:(1)根据葡萄糖的化学式计算.
(2)根据葡萄糖的化学式和相对分子质量的定义计算.
(3)根据葡萄糖的化学式和元素质量比为相对原子质量总和的比计算.
(4)根据元素质量分数的计算公式和葡萄糖的化学式计算.葡萄糖的化学式是C6H12O6.
(1)每个葡萄糖分子共有原子数为6+12+6=24.
(2)葡萄糖的相对分子质量=(12×6)+(1×12)+(16×6)=180.
(3)葡萄糖中C:H:O元素的质量比=(12×6):(1×12):(16×6)=6:1:8.
(4)C6H12O6中碳元素的质量分数=[6C
C6H1206=
72/180]×100%=40%
故答案为:(1)24;
(2)180;
(3)6:1:8;
(4)C6H12O6中碳元素的质量分数:[6C
C6H1206×100%=
72/180]×100%=40%.点评:
本题考点: 生命活动与六大营养素;相对分子质量的概念及其计算;元素质量比的计算;元素的质量分数计算.
考点点评: 化学式的计算是最基本的计算之一,要理解相对分子质量、元素质量比的含义,并熟记相关的计算公式.1年前查看全部
- (2004•镇江)如图所示,用食指托住一瓶质量为500g的矿泉水,使之处于静止状态.手指和瓶盖的接触面积约为1cm2.
 (2004•镇江)如图所示,用食指托住一瓶质量为500g的矿泉水,使之处于静止状态.手指和瓶盖的接触面积约为1cm2.
(2004•镇江)如图所示,用食指托住一瓶质量为500g的矿泉水,使之处于静止状态.手指和瓶盖的接触面积约为1cm2.
求:(1)这瓶矿泉水的重力.(g取10N/kg)
(2)食指端所受到重物的压强. sgnz1年前1
sgnz1年前1 -
 恋恋西城 共回答了19个问题
恋恋西城 共回答了19个问题 |采纳率89.5%(1)这瓶矿泉水的重力G=mg=0.5kg×10N/kg=5N;
答:这瓶矿泉水的重力为5N.
(2)食指端所受到重物的压强P=
F
S=
5N
1×10−4m2=5×104Pa;
答:食指端所受到重物的压强为5×104Pa.1年前查看全部
- (2011•镇江模拟)在平面直角坐标系中,若点P(m-3,m+1)在第二象限,则m的取值范围为______.
 走肖趙1年前1
走肖趙1年前1 -
 502328122 共回答了17个问题
502328122 共回答了17个问题 |采纳率94.1%解题思路:点在第二象限的条件是:横坐标是负数,纵坐标是正数,可得m-3<0,m+1>0,求不等式组的解即可∵点在第二象限,
∴点的横坐标是负数,纵坐标是正数,
即:
m−3<0
m+1>0,
解得:-1<m<3,
故答案为:-1<m<3.点评:
本题考点: 点的坐标;解一元一次不等式组.
考点点评: 此题主要考查了各象限内点的坐标的符号特征以及解不等式,记住各象限内点的坐标的符号是解决的关键,四个象限的符号特点分别是:第一象限(+,+);第二象限(-,+);第三象限(-,-);第四象限(+,-).1年前查看全部
- (2009•镇江模拟)如图所示,一根轻质木杆A端细线下所挂重为50N、底面积为2×10-2m2的重物静止在水平地面上.当
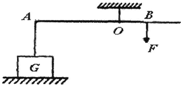 (2009•镇江模拟)如图所示,一根轻质木杆A端细线下所挂重为50N、底面积为2×10-2m2的重物静止在水平地面上.当在B点加竖直向下的力F=30N作用时,木杆能在水平位置处于平衡状态,此时细线竖直,已知OA=15cm,OB=5cm,则重物对水平地面的压强为______Pa;重物对杠杆的拉力为______N.
(2009•镇江模拟)如图所示,一根轻质木杆A端细线下所挂重为50N、底面积为2×10-2m2的重物静止在水平地面上.当在B点加竖直向下的力F=30N作用时,木杆能在水平位置处于平衡状态,此时细线竖直,已知OA=15cm,OB=5cm,则重物对水平地面的压强为______Pa;重物对杠杆的拉力为______N.  吴涟池1年前0
吴涟池1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2014•镇江二模)研究发现,光对被照射物体有力的作用,科学家正用这一原理制造“太阳帆”,为飞船提供动力.在地球附近,
(2014•镇江二模)研究发现,光对被照射物体有力的作用,科学家正用这一原理制造“太阳帆”,为飞船提供动力.在地球附近,正对太阳面积为1.0×106m2的平整光亮表面,受到太阳光的压力约为9N.太阳光的压力虽小,但只要时间足够长,安装面积为1.0×104m2的太阳帆的飞船,在1个月后速度会超过2倍声速.
(1)太阳光对这个“太阳帆”的压强约为______Pa.
(2)关于光的压力对太空中飞船的作用,下列说法中正确的是______.
A.只有飞船的质量很小时,光的压力才能推动它 B.光的压力可以使飞船加速前进
C.光的压力可以使飞船减速前进 D.太空中光的压力可能被空气阻力所抵消
(3)“太阳帆”飞船前进时,太阳能转化为______能. lg3911年前1
lg3911年前1 -
 浓浓妆 共回答了15个问题
浓浓妆 共回答了15个问题 |采纳率86.7%解题思路:(1)太阳光对这个平面的压强等于受到的太阳光的压力与平整光亮表面积的比值;
(2)根据题干提供的信息,对各个选项进行分析判断;
(3)“太阳帆”,为飞船提供动力,太阳能转化为机械能.(1)太阳光对这个平面的压强为:
p=[F/S]=
9N
1.0×106m2=9×10-6Pa;
(2)A、飞船的运动和质量没关系,故A错,
BC、光的压力非常小,但可以推动飞船运动,时间越长飞船速度越大,故B正确,C错误,
D、空气阻力小于压力,抵消不了,故D错.
(3)“太阳帆”,为飞船提供动力,是将太阳能转化为机械能.
故答案为:9×10-6;B;机械能.点评:
本题考点: 压强的大小及其计算;太阳能的利用.
考点点评: 本题考查压强的计算、力的作用效果、能量的转化,认真分析题意得出有用信息是本题的关键.1年前查看全部
- (2012•镇江模拟)俄国著名植物生理学家季米里亚捷夫曾这样写道:“它是窃取天火的普罗米修斯,它所获取的光和热,不仅养育
(2012•镇江模拟)俄国著名植物生理学家季米里亚捷夫曾这样写道:“它是窃取天火的普罗米修斯,它所获取的光和热,不仅养育了地球上的其他生物,而且使巨大的涡轮机旋转,使诗人的笔挥舞”.
(1)这段文字中的“它”指的是______,“它”在生态系统中所属的成分是______.
(2)“它”是通过______“窃取天火”,养育了地球上的其他生物的.
(3)“使巨大的涡轮机旋转,使诗人的笔挥舞”.所需的能量最终来源于______. waya95291年前1
waya95291年前1 -
 suitpopo 共回答了20个问题
suitpopo 共回答了20个问题 |采纳率90%解题思路:绿色植物通过叶绿体利用光能,把二氧化碳和水转化成储存能量的有机物(如淀粉),并且释放出氧气的过程,叫做光合作用,绿色植物能进行光合作用,制造有机物,为所有生物提供物质和能量.据此解答.(1)由上述资料可知,绿色植物能进行光合作用,在叶绿体里利用光能把二氧化碳和水合成有机物,释放氧气,同时把光能转变成化学能储存在合成的有机物中,因此,这段文字中的“它”是指绿色植物.光合作用完成了两个转化,①物质转变.把无机物转变成有机物,不仅用来构成植物体的本身,也为其它生物以及人类制造了食物和其他生活资料,属于生态系统中的生产者,同时释放出氧气,除了满足植物自身的需要外,还供给了动物呼吸利用.②能量转变,把光能转变为贮存在有机物中的化学能.因此,“它”是通过光合作用“窃取天火”,养育了地球上的其他生物;(2)“使巨大的涡轮机旋转,使诗人的笔挥舞.”所需的能量最终来源于太阳光,绿色植物把光能转变为贮存在有机物中的化学能,是自然界的能量源泉.
故答案为:(1)绿色植物;生产者;(2)光合作用;(3)阳光.点评:
本题考点: 生态系统的组成及各部分的作用;绿色植物通过光合作用制造有机物;绿色植物为所有生物提供食物和能量.
考点点评: 练掌握了绿色植物光合作用的意义,结合题意,即可正确答题.1年前查看全部
- (2014•镇江)若关于x的一元二次方程x2+x+m=0有两个相等的实数根,则m=[1/4][1/4].
 绝对白色1年前1
绝对白色1年前1 -
 andy12345 共回答了21个问题
andy12345 共回答了21个问题 |采纳率85.7%解题思路:根据判别式的意义得到△=12-4m=0,然后解一元一次方程即可.根据题意得△=12-4m=0,
解得m=[1/4].
故答案为[1/4].点评:
本题考点: 根的判别式.
考点点评: 本题考查了一元二次方程ax2+bx+c=0(a≠0)的根的判别式△=b2-4ac:当△>0,方程有两个不相等的实数根;当△=0,方程有两个相等的实数根;当△<0,方程没有实数根.1年前查看全部
- (2011•镇江模拟)如图甲所示的滑轮组,每个滑轮等重.不计绳重和摩擦,物体重G1从200N开始逐渐增加,直到绳子被拉断
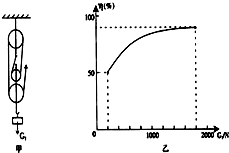 (2011•镇江模拟)如图甲所示的滑轮组,每个滑轮等重.不计绳重和摩擦,物体重G1从200N开始逐渐增加,直到绳子被拉断.每次均匀速拉动绳子将物体提升同样的高度.图乙记录了在
(2011•镇江模拟)如图甲所示的滑轮组,每个滑轮等重.不计绳重和摩擦,物体重G1从200N开始逐渐增加,直到绳子被拉断.每次均匀速拉动绳子将物体提升同样的高度.图乙记录了在
此过程中滑轮组的机械效率随物体重力的增加而变化的图象.
(1)每个滑轮重多少N?
(2)绳子能承受的最大拉力是多少N?
(3)当滑轮组的机械效率为80%时,物体重多少N?
(4)从图象中,你有什么发现? fenyunlang1年前1
fenyunlang1年前1 -
 xujun_911119 共回答了16个问题
xujun_911119 共回答了16个问题 |采纳率81.3%解题思路:在不考虑绳重和摩擦时,利用η=GG+G′×100%,求出相关的物理量是比较常用的方法.首先根据滑轮组提起200N的重物时,机械效率是50%时,根据机械效率公式η=GG+G′×100%,求出每个动滑轮的重.如图,滑轮组能提起的最大重物是1800N,根据F=G+G′n,求出拉力.知道机械效率和动滑轮的重,根据η=GG+G′×100%,求出物体的重.如图,同一滑轮组,提起的物体越重,滑轮组的机械效率越高.(1)∵η=
W有
W总=
G1•h
(G1+G′)•h=
G1
G1+G′×100%
∴η=
G1
G1+G′×100%=50%,
即[200N
200N+2G动=50%,
得G动=100N.
(2)滑轮组提升物体时,有4段绳子承担物体的重,
所以,F=
G物+G′/n]=[1800N+200N/4]=500N.
(3)η'=
G′物
G′物+G′×100%=80%
即
G′物
G′物+G′=80%,
得G'物=800N
(4)同一滑轮组,提升物重越大,机械效率越大.
答:(1)每个滑轮重100N.
(2)绳子能承受的最大拉力是500N.
(3)当滑轮组的机械效率为80%时,物体重800N.
(4)同一滑轮组,提升物重越大,机械效率越大.点评:
本题考点: 滑轮(组)的机械效率;滑轮组绳子拉力的计算;增大或减小机械效率的方法.
考点点评: 滑轮组提升物体时,在不考虑绳重和摩擦时,利用η=GG+G′×100%,计算相关的量,是比较常用的方法,一定要掌握.1年前查看全部
- (2014•镇江一模)四棱锥P-ABCD的底面ABCD是边长为2的正方形,PA⊥底面ABCD且PA=4,则PC与底面AB
(2014•镇江一模)四棱锥P-ABCD的底面ABCD是边长为2的正方形,PA⊥底面ABCD且PA=4,则PC与底面ABCD所成角的正切值为______.
 秋影说1年前0
秋影说1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2008•镇江)草酸晶体(H2C2O4•2H2O)熔点较低,加热会熔化、气化和分解.草酸(H2C2O4)受热会分解,它
(2008•镇江)草酸晶体(H2C2O4•2H2O)熔点较低,加热会熔化、气化和分解.草酸(H2C2O4)受热会分解,它与氢氧化钙的反应为:H2C2O4+Ca(OH)2=CaC2O4↓(白色)+2H2O.
甲、乙两同学对草酸受热分解的产物作如下探究:
(1)猜想与假设:第一种:草酸分解生成CO2和H2;第二种:草酸分解生成CO2、CO和H2O;
第三种:草酸分解:H2C2O4→CO2↑+H2O(未配平);
有同学从理论上就可判断第三种假设不成立,老师也认为这一判断是正确的,该同学判断的理论依据是______.
(2)设计与实验:
甲、乙两同学分别设计了下图所示的A、B两套实验装置(图中铁架台略去).
①甲同学按A装置实验,观察到澄清石灰水变浑浊,认为此现象是由草酸晶体受热分解产生的CO2所导致,此判断______(填“严密”或“不严密”).
②乙同学的B装置图方框内的仪器未画完整,请你帮他画完整(直接画在图上或答题卡上).
乙同学按B装置实验,看到无水硫酸铜由白变蓝,洗气瓶中溶液变浑浊.在尖嘴管口点燃剩余气体,火焰上方罩一个______烧杯,有白色固体生成,证明产物中有______;换一个干、冷烧杯罩在火焰上方,内壁无现象,证明产物中无H2.
(3)结论与思考:
①草酸受热分解的化学方程式为:H2C2O4
CO2↑+CO↑+H2O(2分);加热 ..H2C2O4.
CO2↑+CO↑+H2O(2分);加热 ..
②若省略B装置方框内的仪器,整套装置也能证明产物中有CO2(假设每步都反应完全),方法是:______. ujdf21年前1
ujdf21年前1 -
 zpp402423 共回答了12个问题
zpp402423 共回答了12个问题 |采纳率100%解题思路:猜想生成物首先考虑元素化合价反应前后肯定有升高的也又降低的,再根据图中设计的实验和二氧化碳的性质解决其它题目.(共8分)
(1)酸受热分解若只生成二氧化碳和水,氢氧元素化合价不变,而碳元素化合价升高,所以反应后应有化合价降低的元素,所以(1)答案:(1)无法进行配平、配不平或不符合质量守恒定律或只有化合价的升高,无化合价的降低(1分).
(2)烧杯敞口放置在空气中空气中也有二氧化碳,时间长了烧杯内的澄清石灰水也会变浑浊,故答案:①不严密(1分)注意洗气瓶要长进短出,进气的导管要浸没液体中,出气导管只要刚刚露出橡皮塞.故答案②如右下图(长管不伸入液面下不给分,不作美观要求)(1分)
因为无水硫酸铜由白变蓝,洗气瓶中溶液变浑浊,所以草酸受热分解肯定生成二氧化碳和水,但都被吸收.到最后点燃的是一氧化碳,燃烧生成二氧化碳.故答案:内壁附有澄清石灰水(其它合理答案均给分)(1分)CO(1分)
(3)根据实验现象和前面的分析知草酸受热分解生成二氧化碳、一氧化碳、水.故答案:①H2C2O4
△
.
CO2↑+CO↑+H2O(2分);
二氧化碳能和碱石灰中的氢氧化钠反应,虽没现象但干燥管因吸收它质量增加.故答案:②称量实验前后盛有碱石灰的干燥管的质量(意思相近的表述均给分)(1分)点评:
本题考点: 实验探究物质的性质或变化规律;化学实验方案设计与评价;化学方程式的配平;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题是实验探究题,综合考查到了质量守恒定律、物质的性质、化学用语相关知识.1年前查看全部
- (2010•镇江)两直线l1:y=2x-1,l2:y=x+1的交点坐标为( )
(2010•镇江)两直线l1:y=2x-1,l2:y=x+1的交点坐标为( )
A.(-2,3)
B.(2,-3)
C.(-2,-3)
D.(2,3) ljjsimu1年前1
ljjsimu1年前1 -
 weidao880770 共回答了21个问题
weidao880770 共回答了21个问题 |采纳率85.7%解题思路:根据题意知,两直线有交点,所以列出方程组,解方程组即可.根据题意得:
y=2x−1
y=x+1
解得:
x=2
y=3
∴两直线l1:y=2x-1,l2:y=x+1的交点坐标为(2,3),
故选D.点评:
本题考点: 两条直线相交或平行问题.
考点点评: 方程组的解就是使方程组中两个方程同时成立的一对未知数的值,而这一对未知数的值也同时满足两个相应的一次函数式.1年前查看全部
- (2008•镇江)某厂拟选用下列物质处理含硫酸的废水.现花最少的钱中和等量的废水应选择( )
(2008•镇江)某厂拟选用下列物质处理含硫酸的废水.现花最少的钱中和等量的废水应选择( )
A.NaCl
B.CaCO3
C.Ca(OH)2
D.NaOH 良良18901年前1
良良18901年前1 -
 flyingtree 共回答了15个问题
flyingtree 共回答了15个问题 |采纳率100%解题思路:花最少的钱中和等量的废水,需选用碱类物质来进行处理,通过计算求得所需物质的质量及花费.要中和含硫酸的废水,选用的物质为碱类物质,故AB不符合题意,只需比较氢氧化钙与氢氧化钠的花费即可.
Ca(OH)2+H2SO4=CaSO4+2H2O
74 98
处理98Kg硫酸需要氢氧化钙的花费为:2.0元/Kg×74Kg=148元,
2NaOH+H2SO4=Na2SO4+2H2O
80 98
处理98Kg硫酸需要氢氧化钠的花费为:11.5元/Kg×80Kg=920元,
比较可以发现,氢氧化钙的花费少.
故选C.点评:
本题考点: 中和反应及其应用;酸、碱性废水的处理.1年前查看全部
- (2008•镇江二模)下列叙述错误的是( )
(2008•镇江二模)下列叙述错误的是( )
A.
Ti和4822
Ti在周期表中位置相同,都在第4纵行5022
B.CO2的分子模型:
C.在CS2、PCl3中各原子最外层均能达到8电子的稳定结构
D.熵增加且放热的反应一定是自发反应 CRABCHN1年前1
CRABCHN1年前1 -
 乌布苏湖 共回答了16个问题
乌布苏湖 共回答了16个问题 |采纳率93.8%解题思路:A.同位素在元素周期表中位于同一位置;
B.二氧化碳是直线形分子;
C.原子的化合价的绝对值+其最外层电子数=8时,则该原子达到8电子结构;
D.△G=△H-T△S<0的反应是自发进行的反应.A.2248Ti和2250Ti属于同位素,在周期表中位于同一位置,且在第4列,故A正确;
B.二氧化碳是直线形分子,给出的CO2分子模型中2个O原子和C原子不在同一直线上,故B错误;
C.CS2中碳原子的化合价是4,碳原子最外层电子数是4,所以4+4=8,S原子化合价的绝对值是2,其最外层电子数是6,则2+6=8,PCl3中P原子化合价为+3,其最外层电子数是5,所以3+5=8,Cl原子的化合价的绝对值为1,其最外层电子数是7,则1+7=8,所以CS2、PCl3中各原子最外层均能达到8电子的稳定结构,故C正确;
D.熵增则△S>0,放热则△H<0,温度为正值,所以△G=△H-T△S<0,则该反应是自发进行的反应,故D正确;
故选B.点评:
本题考点: 判断简单分子或离子的构型;核素;原子核外电子排布;焓变和熵变.
考点点评: 本题考查较综合,涉及元素在周期表中的位置、分子的空间构型、8电子结构的判断等知识点,8电子结构的判断方法有:①ABn型分子,A的族序数+成键数=8,则满足所有原子均达到8e-稳定结构;②原子的化合价的绝对值+其最外层电子数=8时,则该原子达到8电子结构,难度不大.1年前查看全部
- (2010•镇江)现有一包固体粉末,可能是CaCO3、Na2CO3、Na2SO4、CuSO4、NaCl中的一种或几种,为
(2010•镇江)现有一包固体粉末,可能是CaCO3、Na2CO3、Na2SO4、CuSO4、NaCl中的一种或几种,为确定其组成,取适量试样进行下列实验.请根据实验现象判断:
(1)取试样溶于水,得到无色澄清溶液,则此固体粉末中一定没有______、______.
(2)取上述溶液适量,滴加过量的BaCl2溶液,出现白色沉淀,再加入过量的稀硝酸,沉淀部分消失并产生气泡.则此固体粉末中一定有______、______.
(3)取步骤(2)实验后的上层清液,加入稀硝酸、硝酸银溶液,出现白色沉淀,由此该同学得出此固体粉末中一定含有NaCl,你认为此结论是否正确______(填“是”或“否”).
(4)对于是否含有NaCl,你认为应对步骤(2)作如何改进______(若步骤(3)填“是”,此空不作答). nancyyun1年前1
nancyyun1年前1 -
 熟悉的ll 共回答了21个问题
熟悉的ll 共回答了21个问题 |采纳率81%(1)原溶液中CaCO3不溶于水,CuSO4为蓝色固体,所以原固体粉末中一定不含这两种物质;
(2)根据实验操作及物质的相互反应现象,可知固体中一定有Na2CO3、Na2SO4;
(3)加入稀硝酸、硝酸银溶液出现白色沉淀,只能确定清液中含氯离子,不能判断原溶液中一定含NaCl;
(4)在步骤(2)中就不能引入了氯离子,可将BaCl2溶液换成Ba(NO3)2溶液或Ba(OH)2溶液;
故答案为:(1)CaCO3、CuSO4(2)Na2CO3、Na2SO4(3)否 (4)将BaCl2溶液换成Ba(NO3)2溶液或Ba(OH)2溶液1年前查看全部
- (2003•镇江)下列物质久置于敞口的容器中,质量会增加的是( )
(2003•镇江)下列物质久置于敞口的容器中,质量会增加的是( )
A.浓盐酸
B.浓硫酸
C.碳酸钠晶体
D.食盐 风信子21年前1
风信子21年前1 -
 themuma 共回答了21个问题
themuma 共回答了21个问题 |采纳率95.2%解题思路:根据各物质久置于敞口的容器中,从质量增加的原因考虑,从浓硫酸具有吸水性、浓盐酸具有挥发性、结晶水合物易风化等知识考虑即可.A、浓盐酸具有挥发性,挥发出氯化氢气体,质量减少,故A错误.
B、浓硫酸具有吸水性,能吸收空气中水蒸气,质量增加,故B正确;
C、碳酸钠晶体在空气中会失去部分或全部结晶水而风化,质量减少,故C错误;
D、食盐在空气中质量几乎不会变化,故D错误;
故选B点评:
本题考点: 空气中常见酸碱盐的质量或性质变化及贮存法.
考点点评: 浓盐酸具有挥发性,浓硫酸具有吸水性,结晶水合物易风化,所以这些物质必须密封保存1年前查看全部
大家在问
- 1to the max line as indicated above这句英文翻译成汉
- 2带分数化假分数的方法
- 3求《孟子》中成语20个,说明出自哪一篇文章,哪一句话
- 4快递英语怎么说?
- 5师徒两人各加工480个零件,完成时所用的时间比是2:3,一直师傅每小时比徒弟多加工20个,师傅加工这批零件用
- 6解下列二元一次方程:1.3y^2+1=2√3y 2.(2x-√2)^2=32 3.4x^2+2=7x
- 7检修一台机器,甲小组单独做7.5h完成,乙小组单独做5h完成,两组合作1h后,再由乙小组单独做,还需几小时
- 8给出两个命题,p:事件“明天下雨”是必然事件;q:双曲线 的渐近线方程是 . 则 (
- 9用定义法证明y=x+4/x在区间(0,2)上递减
- 10Why are people tired on April Fool's Day?
- 11在【I-】=0.1mol/L的溶液中,PbI2的溶解度(s)可表示为 A.三次根号(Ksp/4) B.三次根号Ksp
- 12三国演义的作者是( )的( ),这部著名的( )小说写的是( )时期( ),( ),( )的故事,书中塑造的( ),(
- 13平面内的1条直线可以把平面分成2部分,2条直线最多可以把平面分成4部分,画图看看3条直线最多可以吧平面分
- 141.如果四个人的平均年龄是23岁,四人中没有小于18岁的,那么年龄最大的可能是( )岁. 2.李叔叔有2元和5元的人民币
- 15巧合与缘分 作文
