玻尔理论、量子力学理论都是对核外电子运动的描述方法,根据对它们的理解,下列叙述中正确的是(
 菊岸弃梅2022-10-04 11:39:541条回答
菊岸弃梅2022-10-04 11:39:541条回答| 玻尔理论、量子力学理论都是对核外电子运动的描述方法,根据对它们的理解,下列叙述中正确的是()
|

已提交,审核后显示!提交回复
共1条回复
 003yang 共回答了19个问题
003yang 共回答了19个问题 |采纳率78.9%- D
- 1年前
相关推荐
- 为量子力学的建立奠定基础的科学家不包括( ) A.普朗克 B.爱因斯坦 C.玻尔 D.
为量子力学的建立奠定基础的科学家不包括()
A.普朗克 B.爱因斯坦 C.玻尔 D.诺贝尔  bcud6q1年前1
bcud6q1年前1 -
 cell1900 共回答了18个问题
cell1900 共回答了18个问题 |采纳率100%D
继普朗克的量子假说提出后,爱因斯坦提出了光的量子理论,玻尔提出了原子的量子理论。1年前查看全部
- 下列叙述中,符合玻尔氢原子的理论的是( ) A.电子的可能轨道的分布只能是不连续的 B.大量原子发光的光谱应该是包含一
下列叙述中,符合玻尔氢原子的理论的是( ) A.电子的可能轨道的分布只能是不连续的 B.大量原子发光的光谱应该是包含一切频率的连续光谱 C.电子绕核做加速运动,不向外辐射能量 D.与地球附近的人造卫星相似,绕核运行,电子的轨道半径也要逐渐减小  绿色天使_ff1年前1
绿色天使_ff1年前1 -
 rong6 共回答了12个问题
rong6 共回答了12个问题 |采纳率83.3%A、电子的可能轨道的分布只能是不连续的,故A正确
B、氢原子轨道是量子化的,不连续.发光的光谱不是包含一切频率的连续光谱,故B错误
C、电子绕核做加速运动,不向外辐射能量,故C正确
D、电子的轨道半径不变,故D错误
故选AC.1年前查看全部
- 噬菌体与氢原子在玻尔量子力学模型中的地位
噬菌体与氢原子在玻尔量子力学模型中的地位
这个问题应该怎么回答."噬菌体在分子生物学的地位就相当于氢原子在玻尔量子力学模型中的地位一样“这句话指出了噬菌体作为实验材料具有什么样的特点? wdlal1年前1
wdlal1年前1 -
 yy还很远 共回答了18个问题
yy还很远 共回答了18个问题 |采纳率83.3%你是不是在做语文阅读题啊?文章的相关段落中应该能找到原话.
具有的特点是理想,简单,基础.1年前查看全部
- 根据玻尔理论,氢原子的电子由外层轨道跃迁到内层轨道后( )
根据玻尔理论,氢原子的电子由外层轨道跃迁到内层轨道后( )
A.原子的能量增加,电子的动能减少
B.原子的能量增加,电子的动能增加
C.原子的能量减少,电子的动能减少
D.原子的能量减少,电子的动能增加 nice55101年前1
nice55101年前1 -
 勇敢面对现实 共回答了25个问题
勇敢面对现实 共回答了25个问题 |采纳率88%解题思路:电子绕核运动时,半径减小,电场力做正功,势能减小,总能量减小;根据库仑力提供向心力可分析动能变化;和卫星绕地球运动类似.电子由外层轨道跃迁到内层轨道时,放出光子,总能量减小;根据K[qQ
r2=m
v2/r],可知半径越小,动能越大.故ABC错误,D正确.
故选:D.点评:
本题考点: 玻尔模型和氢原子的能级结构.
考点点评: 电子绕核运动的规律和卫星绕地球运动规律类似,在学习时可以类比进行学习,加强理解.1年前查看全部
- (1)下列说法正确的是A.居里夫妇发现了铀和含铀矿物的天然放射现象B.根据玻尔理论可知,氢原子辐射出一个光子后,氢原子的
(1)下列说法正确的是
A.居里夫妇发现了铀和含铀矿物的天然放射现象
B.根据玻尔理论可知,氢原子辐射出一个光子后,氢原子的电势能减小,核外电子的运动速度增大
C.原子核的半衰期由核内部自身因素决定,与原子所处的化学状态和外部条件无关
D.卢瑟福通过对α粒子散射实验的研究,揭示了原子核的组成
E.赫兹在实验时无意中发现了一个使光的微粒理论得以东山再起的重要现象--光电效应
(2)2005年7月4日13时52分,美国宇航局“深度撞击”号探测器释放的撞击器“击中”目标--坦普尔1号彗星,这次撞击只能使该彗星自身的运行速度出现1×10 -7 m/s的改变.探测器上所携带的重达370kg的彗星“撞击器”将以3.6×10 4 km/h的速度径直撞向彗星的彗核部分,撞击彗星后融化消失.根据以上数据,估算一下彗星的质量是多少?(保留两位有效数字) qiannianguo1年前1
qiannianguo1年前1 -
 tmm82 共回答了17个问题
tmm82 共回答了17个问题 |采纳率88.2%(1)A、贝克勒尔 发现了铀和含铀矿物的天然放射现象,故A错误.
B、氢原子辐射出一个光子后,从高能级向低能级跃迁,氢原子的能量减小,轨道半径减小,电子速率增大,动能增大,由于氢原子能量减小,则氢原子电势能减小.故B正确
C、原子核的半衰期由核内部自身因素决定,与原子所处的化学状态和外部条件无关,故C正确
D、卢瑟福通过对α粒子散射实验的研究提出了原子核式结构模型,故D错误
E、赫兹在实验时无意中发现了一个使光的微粒理论得以东山再起的重要现象--光电效应,故E正确.
故选BCE.
(2)以彗星和撞击器组成的系统为研究对象,设彗星的质量为M,初速度为v 1 ,撞击器质量m=3.7×10 2 kg,速度v 2 =3.6×10 4 km/h=1.0×10 4 m/s,撞击后速度为v
由动量守恒定律得:Mv 1 -mv 2 =(M+m)v
由于M远大于m,所以,上式可以化为:Mv 1 -mv 2 =Mv
解得: M=
m v 2
v 1 -v
由题给信息知,撞击后彗星的运行速度改变了1.0×10 -7 m/s,即v 1 -v=1.0×10 -7 m/s
代入数据,解得M≈3.7×10 13 kg
故答案为:(1)BCE
(2)彗星的质量是3.7×10 13 kg1年前查看全部
- 下列对玻尔原子理论的说法中,正确的是( ) A.玻尔原子理论继承了卢瑟福原子模型,但对原子能量和电子轨道引入了量子化假
下列对玻尔原子理论的说法中,正确的是( ) A.玻尔原子理论继承了卢瑟福原子模型,但对原子能量和电子轨道引入了量子化假设 B.玻尔原子理论对经典电磁理论中关于做加速运动的电荷要辐射电磁波的观点,提出了电子在可能轨道上运动时不辐射电磁波的假设 C.玻尔原子理论用能量转化与守恒的观点建立了原子发光频率与原子能量变化之间的定量关系 D.玻尔原子理论保留了较多的经典物理理论,圆满解释了原子光谱  yuan18911年前1
yuan18911年前1 -
 ytmfngah 共回答了14个问题
ytmfngah 共回答了14个问题 |采纳率100%A、玻尔原子理论继承了卢瑟福原子模型,但对原子能量和电子轨道引入了量子化假设.故A正确.
B、玻尔理论认为电子绕核旋转,不向外辐射能量,处于定态.故B正确.
C、能级间跃迁时辐射或吸收光子能量等于两能级间的能级差.故C正确.
D、玻尔原子理论保留了较多的经典物理理论,只能解释氢原子光谱现象,对于复杂的原子无法解释.故D错误.
故选ABC.1年前查看全部
- 将一个基态氢原子的电子转移到无限远的地方需要2.179×10⌒-18J的能量,将一个电子由n=3的玻尔轨道激发到n=∞的
将一个基态氢原子的电子转移到无限远的地方需要2.179×10⌒-18J的能量,将一个电子由n=3的玻尔轨道激发到n=∞的轨道所需的能量为?(我用轨道能量公式算的 结果完全不对)
 k16881年前1
k16881年前1 -
 niuniu0119 共回答了13个问题
niuniu0119 共回答了13个问题 |采纳率84.6%n=3的玻尔轨道能量是-13.6/9=-1.51电子伏特.所以只要1.51电子伏特能量就可以激发到n=∞的轨道.也就是1.51*1.6 * 10^(-19)=2.418* 10^(-19)焦耳能量.1年前查看全部
- 关于玻尔理论的问题根据玻尔理论(1)计算氢原子中电子在量子数为n的轨道上作圆周运动的频率(2)计算当该电子跃迁到(n-1
关于玻尔理论的问题
根据玻尔理论
(1)计算氢原子中电子在量子数为n的轨道上作圆周运动的频率
(2)计算当该电子跃迁到(n-1)的轨道上时所发出的光子的频率
(3)证明当n很大时,上述(1)和(2)的结果近似相等 m7pjv1年前2
m7pjv1年前2 -
 二十4桥明月夜 共回答了9个问题
二十4桥明月夜 共回答了9个问题 |采纳率100%给你一个粗略的回答:(下式中 pi 即 3.1415...)
1.电磁吸引力等于向心力:
m*v^2/r = k/r^2 (电荷为1库仑)
=> 频率:v1 = [1/(2pi)]*[(k/m)^1/2]*r^(-3/2)
估计这你推导了,还要用公式:r = n^2* r0 (n---主量子数,r0---氢原子第一轨道半径,是个常量),将此式代入上式:
频率 v = R * n^(-3),R是前面一大堆常量,自己去算,意思是v 与主量子数的-3次方成正比.
2.n能级跃迁到n-1能级
经典理论:n能级总能量,电子动能加电子势能:
E = 1/2*m*v^2 - k/r = 1/2 k/r
又量子假设:E = hv
=> 跃迁频率 v2 = 1/2 k/h* [(n - 1)^(-2) - n^(-2)]
(简记) = C* [n^(-2) - (n-1)^(-2)] (C为上面的常量)
当n很大时,上式的 (n-1)^(-2) - n^(-2) 项
=(2n - 1)/ n^2*(n -1)^2
近似= 2n / n^2*(n -1)^2
近似= 2n / n^4 = n^(-3) (系数 2 提到前边常数项中)
这样当n 很大时
跃迁频率 v2 = S * n^(-3),即与n^(-3)成正比.同情况1.
证毕.
注:(1)过程大致如此,细节上自己去算.
(2)严格比较的话,大概可以得出r0即第一轨道半径公式,可以与标准公式比较一下看看是否一样,标准公式自己查,我记不清了,大概是:
r = n^2*[h(bar)]^2/e^2* me 自己试试1年前查看全部
- 下列说法中正确的是 [ ] A.玻尔的原子轨道模型可以解释大多数原子的线
下列说法中正确的是 [ ]A.玻尔的原子轨道模型可以解释大多数原子的线状光谱的形成原因
B.线状光谱特征谱线对应的光的频率与原子中能级之间的能量差可表示为 hv=Ej-Ei
C.氢原子的1s电子云是平面圆形,其中的每一个小黑点代表一个电子
D.在s轨道上运动的所有电子的能量是相同的 sorock19831年前1
sorock19831年前1 -
 日暖蓝田1986 共回答了16个问题
日暖蓝田1986 共回答了16个问题 |采纳率93.8%B1年前查看全部
- 根据玻尔原子结构理论,氦离子(Ht+)少能级图如图所示.电子处在n=3轨道上比处在n=5轨道上离氦核少距离______(
 根据玻尔原子结构理论,氦离子(Ht+)少能级图如图所示.电子处在n=3轨道上比处在n=5轨道上离氦核少距离______(选填“近”或“远”).当大量Ht+处在n=4少激发态时,由于跃迁所发射少谱线有______条.
根据玻尔原子结构理论,氦离子(Ht+)少能级图如图所示.电子处在n=3轨道上比处在n=5轨道上离氦核少距离______(选填“近”或“远”).当大量Ht+处在n=4少激发态时,由于跃迁所发射少谱线有______条.  黑水河1年前1
黑水河1年前1 -
 chairliu 共回答了20个问题
chairliu 共回答了20个问题 |采纳率85%解题思路:根据玻尔原子理论,电子所在不同能级的轨道半径满足rn=n2r1,激发态跃迁的谱线满足
,从而即可求解.n(n−1) 2 根据玻尔原子理论,能级越高的电子离核距离越l,故电子处在我=3轨道上比处在我=5轨道上离氢核的距离近,
跃迁发出的谱线特条数为我=
手s我=
我(我−1)
s,代入我=4,解得6条谱线,
故答案为:近,6.点评:
本题考点: 氢原子的能级公式和跃迁.
考点点评: 本题主要考查德布罗意波和玻尔原子理论,在考纲中属于基本要求,作为2013年江苏高考题难度不是很大.1年前查看全部
- 由玻尔理论可知,当氢原子中的核外电子由一个轨道跃迁到另一轨道时,有可能( )
由玻尔理论可知,当氢原子中的核外电子由一个轨道跃迁到另一轨道时,有可能( )
A.发射出光子,电子的动能减少,原子的势能减少
B.发射出光子,电子的动能增加,原子的势能减少
C.吸收光子,电子的动能减少,原子的势能增加
D.吸收光子,电子的动能增加,原子的势能减少 飘雪雅子1年前1
飘雪雅子1年前1 -
 jayfans234 共回答了23个问题
jayfans234 共回答了23个问题 |采纳率87%解题思路:氢原子的核外电子由一个轨道跃迁到另一轨道时,若放出光子,轨道半径减小,电场力做正功,电子动能增加,原子的能量减小.若吸收光子,轨道半径增大,电场力做负功,电子动能减小,原子的能量增大.A、B放出光子时,电子的轨道半径减小,电场力做正功,电子动能增加,根据玻尔理论得知,原子的能量减小.故A错误,B正确.
C、D吸收光子时,电子的轨道半径增大,电场力做负功,电子动能减小,根据玻尔理论得知,原子的能量增大.故C正确,D错误.
故选:BC.点评:
本题考点: 氢原子的能级公式和跃迁.
考点点评: 本题关键要抓住氢原子的核外电子跃迁时电子轨道变化与吸收能量或放出能量的关系.1年前查看全部
- 为解释原子光谱是线状光谱这一事实,玻尔提出了核外电子的分层排布理论,下列说法中,不符合这一理论的是 [
为解释原子光谱是线状光谱这一事实,玻尔提出了核外电子的分层排布理论,下列说法中,不符合这一理论的是 [ ]A.电子绕核运动具有特定的半径和能量
B.电子在特定半径的轨道上运动时不辐射能量
C.电子跃迁时,会吸收或放出特定的能量
D.提示了氢原子光谱存在多条谱线 lolita19861年前1
lolita19861年前1 -
 紫雾迷漫 共回答了20个问题
紫雾迷漫 共回答了20个问题 |采纳率80%D1年前查看全部
- 根据玻尔理论,在氢原子中,量子数n越大,则( )
根据玻尔理论,在氢原子中,量子数n越大,则( )
A. 电子轨道半径越小
B. 核外电子速度越小
C. 原子能级的能量越小
D. 原子的电势能越小 无比期待1年前1
无比期待1年前1 -
 zj9831 共回答了19个问题
zj9831 共回答了19个问题 |采纳率100%解题思路:在氢原子中,量子数n越大,轨道半径越大,根据库仑引力提供向心力,判断核外电子运动的速度的变化,从而判断出电子动能的变化,根据能量的变化得出电势能的变化.在氢原子中,量子数n越大,电子的轨道半径越大,
根据
ke2
r2=m
v2
r 知,r越大,v越小,则电子的动能减小,即速度越小.
因为量子数增大,原子能级的能量增大,动能减小,则电势能增大.故B正确,A、C、D错误.
故选:B.点评:
本题考点: 玻尔模型和氢原子的能级结构;电势能.
考点点评: 解决本题的关键知道量子数越大,轨道半径越大,原子能级的能量越大,以及知道原子能量等于电子动能和势能的总和.1年前查看全部
- 下列说法正确的是( )A.用蓝光照射某金属时能够产生光电效应,如果用黄光照射该金属也一定能够产生光电效应.B.玻尔理论
下列说法正确的是( )
A.用蓝光照射某金属时能够产生光电效应,如果用黄光照射该金属也一定能够产生光电效应.
B.玻尔理论指出氢原子能级是分立的,原子跃迁时发射光子的频率也是不连续的
C.卢瑟福通过分析α粒子散射实验结果,发现了质子和中子
D.工业上利用γ射线来检查金属内部伤痕,是因为γ射线穿透能力很强 jb0f1年前1
jb0f1年前1 -
 symxdn 共回答了15个问题
symxdn 共回答了15个问题 |采纳率100%解题思路:当入射光的频率大于金属的极限频率时,可以发生光电效应;玻尔理论指出氢原子能级是量子化的,能级差也是量子化的;卢瑟福通过分析α粒子散射实验结果,得出了原子的核式结构模型;γ射线穿透能力很强;α衰变后电荷数少2,质量数少4.A、用蓝光照射某金属时能够产生光电效应,知蓝光的频率大于金属的极限频率,因为黄光的频率小于蓝光频率,所以用黄光照射不一定能发生光电效应.故A错误.
B、玻尔理论指出氢原子能级是量子化的,能级差也是量子化的,则释放的光子频率也是不连续的.故B正确.
C、卢瑟福通过分析α粒子散射实验结果,得出了原子的核式结构模型.故C错误.
D、工业上利用γ射线来检查金属内部伤痕,是因为γ射线穿透能力很强.故D正确.
E、釉核
23892U经过一次α衰变后,电荷数少2,质量数少4.变为钍核
23490Th.故E正确.
故选BDE点评:
本题考点: 氢原子的能级公式和跃迁;原子核衰变及半衰期、衰变速度.
考点点评: 本题考查了光电效应、能级跃迁、α粒子散射、衰变等基础知识点,比较简单,关键要熟悉教材,牢记这些基础知识点.1年前查看全部
- (选修模块3-5)(1)下列说法正确的是______.A.玻尔原子理论第一次将量子观念引入原子领域,提出了定态和跃迁的概
(选修模块3-5)
(1)下列说法正确的是______.
A.玻尔原子理论第一次将量子观念引入原子领域,提出了定态和跃迁的概念,成功地解释了氢原子光谱的实验规律
B.原子核发生α衰变时,新核与α粒子的总质量等于原来的原子核的质量
C.氢原子的核外电子由离原子核较远的轨道跃迁到离核较近的轨道上时氢原子的能量减少
D.在原子核中,比结合能越小表示原子核中的核子结合得越牢固
(2)如图所示为研究光电效应的电路图,对于某金属用紫外线照射时,电流表指针发生偏转.将滑动变阻器滑动片向右移动的过程中,电流表的示数不可能______(选填“减小”、“增大”). 如果改用频率略低的紫光照射,电流表______(选填“一定”、“可能”或“一定没”)有示数.
(3)在光滑水平面上,一个质量为m,速度为υ的A球,与质量也为m的另一静止的B球发生正碰,若它们发生的是弹性碰撞,碰撞后B球的速度是多少?若碰撞后结合在一起,共同速度是多少?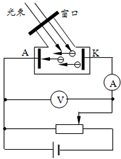
 lzqsgzh1年前1
lzqsgzh1年前1 -
 linlangyu2006 共回答了13个问题
linlangyu2006 共回答了13个问题 |采纳率100%(1)A、玻尔原子理论第一次将量子观念引入原子领域,提出了定态和跃迁的概念,成功地解释了氢原子光谱的实验规律.故A正确.
B、原子核发生α衰变时,由于有质量亏损,新核与α粒子的总质量不等于原来的原子核的质量.故B错误.
C、氢原子的核外电子由离原子核较远的轨道跃迁到离核较近的轨道上时,能级变小,则氢原子的能量减小.故C正确.
D、比结合能越大的原子核中的核子结合得越牢固.故D错误.
故选AC.
(2)AK间所加的电压为正向电压,发生光电效应后的光电子在光电管中加速,滑动变阻器滑动片向右移动的过程中,若光电流达到饱和,则电流表示数不变,若光电流没达到饱和电流,则电流表示数增大,所以滑动变阻器滑动片向右移动的过程中,电流表的示数不可能减小.
紫光的频率小于紫外线,紫外线照射能发生光电效应,但是紫光照射不一定能发生光电效应.所以电流表可能有示数.
(3)弹性碰撞的过程中,动量守恒,机械能守恒,有:mv=mv A +mv B ,
1
2 m v 2 =
1
2 m v A 2 +
1
2 m v B 2
解得v B =v,v A =0.
若碰撞后结合在一起,根据动量守恒定律得,
mv=2mv′
解得 v′=
v
2 .
答:若它们发生的是弹性碰撞,碰撞后B球的速度是v,若碰撞后结合在一起,共同速度是
v
2 .
故答案为:(1)AC(2)减小可能 (3)υ,
υ
21年前查看全部
- 下列说法正确的是( )A.居里夫妇发现了铀和含铀矿物的天然放射现象B.根据玻尔理论可知,氢原子辐射出一个光子后,氢原子
下列说法正确的是( )
A.居里夫妇发现了铀和含铀矿物的天然放射现象
B.根据玻尔理论可知,氢原子辐射出一个光子后,氢原子的电势能减小,核外电子的运动速度增大
C.德布罗意在爱因斯坦光子说的基础上提出物质波的概念,认为一切物体都具有波粒二象性
D.卢瑟福通过对α粒子散射实验的研究,揭示了原子核的组成. minikan1年前1
minikan1年前1 -
 shire 共回答了13个问题
shire 共回答了13个问题 |采纳率100%解题思路:根据物理学史和常识解答,记住著名物理学家的主要贡献即可.A、贝可勒尔发现了铀和含铀矿物的天然放射现象,故A错误;
B、氢原子辐射出一个光子后,从高能级向低能级跃迁,氢原子的能量减小,轨道半径减小,电子速率增大,动能增大,由于氢原子能量减小,则氢原子电势能减小,故B正确;
C、德布罗意在爱因斯坦光子说的基础上提出物质波的概念,认为一切物体都具有波粒二象性,故C正确;
D、卢瑟福通过对α粒子散射实验的研究,提出原子核式结构学说,故D错误;
E、赫兹在实验时无意中发现了一个使光的微粒理论得以东山再起的重要现象--光电效应,故E正确;
故选:BCE.点评:
本题考点: 光电效应;玻尔模型和氢原子的能级结构.
考点点评: 本题考查物理学史,是常识性问题,对于物理学上重大发现、发明、著名理论要加强记忆,这也是考试内容之一.1年前查看全部
- 如何掌握原子结构模型啊,比如什么玻尔原子机构模型呀,
如何掌握原子结构模型啊,比如什么玻尔原子机构模型呀,
什么原子轨道呀、4个量子数呀、电子云、什么能量级呀、基态原子中电子在原子轨道的排布等等的知识,高中阶段的,看到书上有讲,不过都很抽象,个人基本看不懂,有什么基础的书推荐一下么或者视频,从基础的开开始
Na原子 电子排布式1s²2s²2p6(右上角)3s1(右上角) 我这个都看不懂,所以最好基础一点,或者讲一下. 上课过程1年前1
上课过程1年前1 -
 祝成功 共回答了18个问题
祝成功 共回答了18个问题 |采纳率88.9%你问的这些都是大学化学一年级的无机化学部分,高中当然看不懂啦,
其实,很多大学生上完了无机化学照样搞不懂.第一,内容太抽象;第二,没有宏观物体可以参考.学不好是正常的!
楼主提前学习对于将来大学的学习是有好处的,加油!至于讲解,个人认为还是算了,即使面对面的讲也不见得能讲明白,何况是纸上谈兵?
具体的例子是没问题的:
1s²2s²2p6(右上角)3s1
s前面的1、2、3是电子所在的层数,用n表示,又叫主量子数;
s、p是层的下级单位,叫亚层,符号不同,形状也不同,分别是球形和哑铃形
右上角的数字表示电子数1年前查看全部
- 用玻尔理论解释:为什么各种原子吸收光谱中的每一条暗线都跟该种原子的发射光谱中的一条亮线相对应
用玻尔理论解释:为什么各种原子吸收光谱中的每一条暗线都跟该种原子的发射光谱中的一条亮线相对应
包含各种波长的复合光,被原子吸收了某些波长的光子之后,连续光谱中这些波长的位置上便出现了暗线,这样的光谱叫吸收光谱 可乐吧1年前1
可乐吧1年前1 -
 茶三酒四 共回答了14个问题
茶三酒四 共回答了14个问题 |采纳率85.7%因为氢原子在的电子有许多能级,不同能级间能量不同,且对于确定的两能级间能量差是恒定的,氢原子只吸收这些能量值,向高能级越迁,因此暗处就是被吸收的能量等于能量差的光子,等氢在释放这些光子后,又出现同样能量的光子,因能量和光子频率有关因此就是确定的频率的光,也就是吸收和放出的都是同种能量的光.1年前查看全部
- 下列说法正确确的是 A.玻尔对氢原子光谱的研究导致原子的核式结构模型的建立 B.可利用某些物质在紫外线照射下发出荧光来设
下列说法正确确的是
A.玻尔对氢原子光谱的研究导致原子的核式结构模型的建立 B.可利用某些物质在紫外线照射下发出荧光来设计防伪措施 C.天然放射现象中产生的射线都能在电场或磁场中发生偏转 D.观察者与波源互相远离时接收到波的频率与波源频率不同  冬雪伊人661年前1
冬雪伊人661年前1 -
 xurui199941 共回答了17个问题
xurui199941 共回答了17个问题 |采纳率100%解题思路:原子的核式结构模型源于卢瑟福的
α 粒子散射实验,故A 错误;紫外线可使荧光物质发光,此现象广泛应用于人民币等防伪措施,所以选项B 正确;天然放射现象中的γ 射线是电磁波,不会在电磁场中偏转,故C 错误;由多普勒效应可知,观察者与波源靠近或远离时,观察到的波的频率相对于波源会增大或减小,所以选项D 正确。BD
1年前查看全部
- 下列表述正确的是( )A.密立根通过著名的油滴实验测出了电子的电量B.玻尔理论可以解释所有原子光谱的实验规律C.汤姆孙
下列表述正确的是( )
A.密立根通过著名的油滴实验测出了电子的电量
B.玻尔理论可以解释所有原子光谱的实验规律
C.汤姆孙通过对阴极射线的研究发现了电子,并提出了原子核式结构模型
D.爱因斯坦发现的光电效应现象,有力的证明了光的粒子性 即心1年前1
即心1年前1 -
 r9ttw9r5j5 共回答了19个问题
r9ttw9r5j5 共回答了19个问题 |采纳率89.5%A、密立根通过著名的油滴实验测出了电子的电量,A正确;
B、玻尔理论可以解释氢原子光谱的实验规律,B错误;
C、汤姆孙通过对阴极射线的研究发现了电子,卢瑟福提出原子核式结构,C错误;
D、赫兹发现的光电效应现象,有力的证明了光的粒子性,D错误;
故选:A1年前查看全部
- 根据玻尔理论,某原子的电子从能量为E的轨道跃迁到能量为E’的轨道,辐射出频率为v的光子,以h表示普朗克常量,c表示真空的
根据玻尔理论,某原子的电子从能量为E的轨道跃迁到能量为E’的轨道,辐射出频率为v的光子,以h表示普朗克常量,c表示真空的光速,则该光子的质量是( )
A.m=hv
B.m=[E−E′c2  1201091年前1
1201091年前1 -
 yanglianbin123 共回答了19个问题
yanglianbin123 共回答了19个问题 |采纳率94.7%解题思路:根据玻尔理论得到光子的能量△E=E-E′=hγ,结合爱因斯坦质能方程△E=mc2求解.根据玻尔理论可知:氢原子跃迁时两轨道的能级差等于光子能量,则得光子的能量△E=E-E′=hγ,
又由爱因斯坦质能方程△E=mc2得:光子的质量为m=
E−E′
c2=
hγ
c2.
故选BC点评:
本题考点: 爱因斯坦质能方程.
考点点评: 玻尔理论和爱因斯坦质能方程是原子物理中的重点,也考试热点,要加强理解,牢固掌握.1年前查看全部
- 下列说法正确的是( ) A.用蓝光照射某金属时能够产生光电效应,如果用黄光照射该金属也一定能够产生光电效应. B.玻尔
下列说法正确的是( ) A.用蓝光照射某金属时能够产生光电效应,如果用黄光照射该金属也一定能够产生光电效应. B.玻尔理论指出氢原子能级是分立的,原子跃迁时发射光子的频率也是不连续的 C.卢瑟福通过分析α粒子散射实验结果,发现了质子和中子 D.工业上利用γ射线来检查金属内部伤痕,是因为γ射线穿透能力很强 E.釉核
U 经过一次α衰变后,变为钍核23892
Th23490  eahfj1年前1
eahfj1年前1 -
 可怜虫zx 共回答了23个问题
可怜虫zx 共回答了23个问题 |采纳率87%A、用蓝光照射某金属时能够产生光电效应,知蓝光的频率大于金属的极限频率,因为黄光的频率小于蓝光频率,所以用黄光照射不一定能发生光电效应.故A错误.
B、玻尔理论指出氢原子能级是量子化的,能级差也是量子化的,则释放的光子频率也是不连续的.故B正确.
C、卢瑟福通过分析α粒子散射实验结果,得出了原子的核式结构模型.故C错误.
D、工业上利用γ射线来检查金属内部伤痕,是因为γ射线穿透能力很强.故D正确.
E、釉核
23892 U 经过一次α衰变后,电荷数少2,质量数少4.变为钍核
23490 Th .故E正确.
故选BDE1年前查看全部
- 下列说法正确的是( )A.玻尔提出的原子模型,彻底否定了卢瑟福的原子核式结构学说B.巴尔末根据氢原子光谱分析,总结出了
下列说法正确的是( )
A.玻尔提出的原子模型,彻底否定了卢瑟福的原子核式结构学说
B.巴尔末根据氢原子光谱分析,总结出了氢原子光谱可见光区波长公式
C.在光电效应中,当入射光的波长大于截止波长时不发生光电效应
D.爱因斯坦提出的质能方程E=mc2中的E是发生核反应中释放的核能 xzw1987581年前1
xzw1987581年前1 -
 chengjinchuan 共回答了11个问题
chengjinchuan 共回答了11个问题 |采纳率90.9%A、玻尔在卢瑟福的原子核式结构学说的基础上提出的原子模型.故A错误;
B、巴尔末根据氢原子光谱分析,总结出了氢原子光谱可见光区波长公式;故B正确;
C、在光电效应中,当入射光的波长大于截止波长时,即入射光的频率小于截止频率,不发生光电效应,故C正确;
D、爱因斯坦提出的质能方程E=mc2中的E是物体所具有的能量,△E=△m•c2中△E才是发生核反应中释放的核能.故D错误.
E、根据玻尔理论可知,原子从一种定态跃迁到另一种定态时,可能吸收或辐射出一定频率的光子,光子的能量等于两个能级的差.故E正确;
故选:BCE.1年前查看全部
- 人类对原子结构的认识经过了一个漫长而曲折的过程,其中提出原子核外的电子是在一系列稳定的轨道上分层运动的是 A.玻尔 B
人类对原子结构的认识经过了一个漫长而曲折的过程,其中提出原子核外的电子是在一系列稳定的轨道上分层运动的是
A.玻尔 B.道尔顿 C.汤姆生 D.卢瑟福  wefgewgui1年前1
wefgewgui1年前1 -
 非常听讲 共回答了20个问题
非常听讲 共回答了20个问题 |采纳率90%A
1年前查看全部
- 根据玻尔理论,下列关于氢原子的论述正确的是( )
根据玻尔理论,下列关于氢原子的论述正确的是( )
A.若氢原子由能量为En的定态向低能级跃迁,则氢原子要辐射的光子能量为hν=En
B.电子沿某一轨道绕核运动,若圆周运动的频率为ν,则其发光的频率也是ν
C.一个氢原子中的电子从一个半径为ra的轨道自发地直接跃迁到另一半径为rb的轨道,已知ra>rb,则此过程原子要辐射某一频率的光子
D.氢原子吸收光子后,将从高能级向低能级跃迁 by46189811年前1
by46189811年前1 -
 摩呼逻迦 共回答了11个问题
摩呼逻迦 共回答了11个问题 |采纳率100%解题思路:本题考查波尔理论:电子在绕原子核运动的过程中轨道半径并不是连续的,氢原子的能量满足En=1n2E1;电子在绕原子核运动的过程中原子是稳定的并不向外辐射能量,当从高轨道向低轨道跃起时才会向外辐射能量,并且辐射的能量是由初末能级的能量差决定的,有:hν=Em-En.A、氢原子由能量为En的定态向低能级跃迁,则氢原子要辐射的光子能量为hν=En-E1;故A错误.
B、按照波尔理论电子在某一个轨道上运动的时候并不向外辐射能量,即其状态时稳定的,故B错误.
C、已知ra>rb,电子从较高能级的轨道自发地跃迁到较低能级的轨道时,会辐射一定频率的光子,故C正确.
D、按照波尔理论,氢原子吸收光子后,将从低能级向高能级跃迁,故D错误.
故选:C.点评:
本题考点: 玻尔模型和氢原子的能级结构.
考点点评: 本题考查波尔氢原子模型,重在记忆,重在积累,故要多看课本,注意掌握跃迁过程中能量的变化.1年前查看全部
- 如图所示,1、2、3、4为玻尔理论中氢原子最低的四个能级.处在n=4能级的一群氢原子向低能级跃迁时,能发出若干种频率不同
 如图所示,1、2、3、4为玻尔理论中氢原子最低的四个能级.处在n=4能级的一群氢原子向低能级跃迁时,能发出若干种频率不同的光子,在这些光中,波长最长的是( )
如图所示,1、2、3、4为玻尔理论中氢原子最低的四个能级.处在n=4能级的一群氢原子向低能级跃迁时,能发出若干种频率不同的光子,在这些光中,波长最长的是( )
A.n=4跃迁到n=1时辐射的光子
B.n=4跃迁到n=3时辐射的光子
C.n=2跃迁到n=1时辐射的光子
D.n=3跃迁到n=2时辐射的光子 察看1年前1
察看1年前1 -
 光明狂龙 共回答了14个问题
光明狂龙 共回答了14个问题 |采纳率92.9%解题思路:能级间跃迁辐射或吸收光子的能量等于两能级间的能级差,能级差越大,光子频率越大,波长越小.处在n=4能级的一群氢原子向低能级跃迁时,由n=4跃迁到n=3时,辐射的光子频率最小,则波长最长.故B正确,A、C、D错误.
故选:B.点评:
本题考点: 氢原子的能级公式和跃迁.
考点点评: 解决本题的关键知道能级间跃迁所满足的规律,即Em-En=hv.1年前查看全部
- 下列关于原子结构的说法中,正确的是( ) A.电子的发现说明原子是可分的 B.玻尔的原子理论完全否定了原子的核式结构学
下列关于原子结构的说法中,正确的是( ) A.电子的发现说明原子是可分的 B.玻尔的原子理论完全否定了原子的核式结构学说 C.玻尔的原子理论,能成功解释各种原子发光现象 D.大量氢原子从n=5的激发态向低能态跃迁时,最多可以产生15种不同频率的光子  世人醉了1年前1
世人醉了1年前1 -
 冯萧萧 共回答了15个问题
冯萧萧 共回答了15个问题 |采纳率60%A、电子的发现说明原子是可以再分的.故A正确.
B、玻尔原子理论并未完全否定原子核式结构,认为电子还是绕核旋转.故B错误.
C、玻尔原子理论不能解释所有原子的发光现象.故C错误.
D、根据数学组合公式
C 25 =10,知最多可以产生10种不同频率的光子.故D错误.
故选A.1年前查看全部
- 二十世纪杰出的物理学家爱因斯坦认为:( )玻尔等量子力学主要奠基人发现:( )
二十世纪杰出的物理学家爱因斯坦认为:( )玻尔等量子力学主要奠基人发现:( )
这是物理的题,在初二寒假作业最后一面. 草子幽幽1年前1
草子幽幽1年前1 -
 luozhill 共回答了21个问题
luozhill 共回答了21个问题 |采纳率100%二十世纪杰出的物理学家爱因斯坦认为:( 时间与空间是相对的,并且与运动密切相关);玻尔等量子力学主要奠基人发现:(微观粒子都具有波粒二象性,并且微观世界的规律是概率性的 ).1年前查看全部
- 据玻尔假设,当E初>E终时原子将产生发光现象为什么?
据玻尔假设,当E初>E终时原子将产生发光现象为什么?
希望各位兄弟姐妹们多多帮忙!我很需要 shirley18th1年前1
shirley18th1年前1 -
 zjk20030308 共回答了24个问题
zjk20030308 共回答了24个问题 |采纳率83.3%减少的能量以光子的形式放出,所以会发光
回答者:zouccc - 助理 二级 3-10 23:07
光子是能量子(原自光的波粒二相性)
它可以和能量相互转化,其公式表达为:E=hν(音:niu去声,代表光波频率)
当E初>E终时原子将放出能量,这种能量以光子(一种能量子)的形式放出
也就是所谓的“发光”1年前查看全部
- 玻尔对量子力学的建立做出了什么贡献啊?
 苏术1年前1
苏术1年前1 -
 Y502162696 共回答了18个问题
Y502162696 共回答了18个问题 |采纳率94.4%量子力学是在旧量子论的基础上发展起来的.旧量子论包括普朗克的量子假说、爱因斯坦的光量子理论和玻尔的原子理论.
1900年,普朗克提出辐射量子假说,假定电磁场和物质交换能量是以间断的形式(能量子)实现的,能量子的大小同辐射频率成正比,比例常数称为普朗克常数,从而得出黑体辐射能量分布公式,成功地解释了黑体辐射现象.
1905年,爱因斯坦引进光量子(光子)的概念,并给出了光子的能量、动量与辐射的频率和波长的关系,成功地解释了光电效应.其后,他又提出固体的振动能量也是量子化的,从而解释了低温下固体比热问题.
1913年,玻尔在卢瑟福有核原子模型的基础上建立起原子的量子理论.按照这个理论,原子中的电子只能在分立的轨道上运动,在轨道上运动时候电子既不吸收能量,也不放出能量.原子具有确定的能量,它所处的这种状态叫“定态”,而且原子只有从一个定态到另一个定态,才能吸收或辐射能量.这个理论虽然有许多成功之处,但对于进一步解释实验现象还有许多困难.
在人们认识到光具有波动和微粒的二象性之后,为了解释一些经典理论无法解释的现象,法国物理学家德布罗意于1923年提出了物质波这一概念.认为一切微观粒子均伴随着一个波,这就是所谓的德布罗意波.
德布罗意的物质波方程:e=04ω,p=h/λ,其中04=h/2π,可以由e=p05/2m得到λ=√(h05/2me).
由于微观粒子具有波粒二象性,微观粒子所遵循的运动规律就不同于宏观物体的运动规律,描述微观粒子运动规律的量子力学也就不同于描述宏观物体运动规律的经典力学.当粒子的大小由微观过渡到宏观时,它所遵循的规律也由量子力学过渡到经典力学.
量子力学与经典力学的差别首先表现在对粒子的状态和力学量的描述及其变化规律上.在量子力学中,粒子的状态用波函数描述,它是坐标和时间的复函数.为了描写微观粒子状态随时间变化的规律,就需要找出波函数所满足的运动方程.这个方程是薛定谔在1926年首先找到的,被称为薛定谔方程.
当微观粒子处于某一状态时,它的力学量(如坐标、动量、角动量、能量等)一般不具有确定的数值,而具有一系列可能值,每个可能值以一定的几率出现.当粒子所处的状态确定时,力学量具有某一可能值的几率也就完全确定.这就是1927年,海森伯得出的测不准关系,同时玻尔提出了并协原理,对量子力学给出了进一步的阐释.
量子力学和狭义相对论的结合产生了相对论量子力学.经狄拉克、海森伯(又称海森堡,下同)和泡利(pauli)等人的工作发展了量子电动力学.20世纪30年代以后形成了描述各种粒子场的量子化理论——量子场论,它构成了描述基本粒子现象的理论基础.
量子力学是在旧量子论建立之后发展建立起来的.旧量子论对经典物理理论加以某种人为的修正或附加条件以便解释微观领域中的一些现象.由于旧量子论不能令人满意,人们在寻找微观领域的规律时,从两条不同的道路建立了量子力学.
1925年,海森堡基于物理理论只处理可观察量的认识,抛弃了不可观察的轨道概念,并从可观察的辐射频率及其强度出发,和玻恩、约尔丹一起建立起矩阵力学;1926年,薛定谔基于量子性是微观体系波动性的反映这一认识,找到了微观体系的运动方程,从而建立起波动力学,其后不久还证明了波动力学和矩阵力学的数学等价性;狄拉克和约尔丹各自独立地发展了一种普遍的变换理论,给出量子力学简洁、完善的数学表达形式.1年前查看全部
- 物理之玻尔模型根据氢原子的玻尔模型,氢原子核外一个电子在第一轨道和第N轨道分别运行时,它运动的轨道半径之比为____,运
物理之玻尔模型
根据氢原子的玻尔模型,氢原子核外一个电子在第一轨道和第N轨道分别运行时,它运动的轨道半径之比为____,运动速度之比为____,运行周期之比为_____ 天很蓝797761年前3
天很蓝797761年前3 -
 ivygullit 共回答了12个问题
ivygullit 共回答了12个问题 |采纳率75%1:N^2 ,N:1 ,1:N^31年前查看全部
- 量子限域效应中的激子玻尔半径是怎么得到的,怎么算?
 鸭鸭蛋1年前2
鸭鸭蛋1年前2 -
 筱筱蟹 共回答了16个问题
筱筱蟹 共回答了16个问题 |采纳率93.8%先把限域中的量子势能算出来,再得出波函数,套入公式就算出玻尔半径咯1年前查看全部
- 人造地球卫星绕地球做圆周运动与玻尔氢原子模型中电子绕原子核做圆周运动相类似,下列说法正确的是( )
人造地球卫星绕地球做圆周运动与玻尔氢原子模型中电子绕原子核做圆周运动相类似,下列说法正确的是( )
A.它们做圆周运动的向心力大小跟轨道半径成反比
B.它们都只能在一系列不连续的轨道运动
C.电子轨道半径越大,氢原子能量越大
D.同一卫星在不同轨道运动时,机械能相等
请详细分析下,谢谢! 妖精似水1年前1
妖精似水1年前1 -
 mengmenglijun 共回答了19个问题
mengmenglijun 共回答了19个问题 |采纳率89.5%选C
a 跟半径的平方
b 卫星的轨道连续
c 对的,半径越大,能级越高
d 参考下卫星机械能公式就知道1年前查看全部
- 爱因斯坦和玻尔发现了什么物理规律与什么物理规律有很大的差异
 wxf1171年前2
wxf1171年前2 -
 jjs00 共回答了19个问题
jjs00 共回答了19个问题 |采纳率89.5%爱因斯坦——相对论,与经典力学有很大差异
玻尔——量子论,与电磁波与粒子有很大差异1年前查看全部
- 根据玻尔理论,氢原子的电子由n=4轨道跃迁到n=1轨道时,原子要放出一系列频率不同的光子,这句话对吗?
 网上抠泥1年前2
网上抠泥1年前2 -
 markrwx 共回答了17个问题
markrwx 共回答了17个问题 |采纳率82.4%对!从4轨道到3轨道;从4轨道到2轨道;从4轨道到1轨道;从3轨道到2轨道;从3轨道到1轨道;从2轨道到1轨道.1年前查看全部
- 原子的热辐射按照经典理论来讲,凡是温度大于-279.14C.的物体都可以发出电磁辐射,玻尔模型又说处与一个定态的原子不发
原子的热辐射
按照经典理论来讲,凡是温度大于-279.14C.的物体都可以发出电磁辐射,玻尔模型又说处与一个定态的原子不发射电磁辐射,量子力学又说热辐射是原子电磁辐射的机制,那么物体的温度和周围环境的温度都大于-279.14C,这个物体还发射电磁辐射吗?
以上的几个理论哪个是正确的啊?
以上的几个理论哪个是正确的啊,为什么呢? 2315882315881年前2
2315882315881年前2 -
 lxh520 共回答了12个问题
lxh520 共回答了12个问题 |采纳率91.7%当然它们都是正确的.首先由处于定态的原子构成的物体的温度应该是绝对零度,因为该原子无法发出电磁辐射,从而该物体便不会有辐射.反之其温度大于绝对零度的物体因构成其的原子不处于定态而会发出电磁辐射而会发出热辐射.1年前查看全部
- 玻尔对氢原子或类氢原子创造性地提出了两个著名的基本假设,是哪两个?
 射鹿1年前1
射鹿1年前1 -
 小手冷 共回答了21个问题
小手冷 共回答了21个问题 |采纳率90.5%定态假设 角度量量子化假设1年前查看全部
- 在玻尔氢原子中电子由量子数n=5的轨道跃迁到n=2的轨道时,求氢原子辐射光子的波
 文竹19701年前1
文竹19701年前1 -
 mary6697323 共回答了17个问题
mary6697323 共回答了17个问题 |采纳率94.1%就是氢原子的巴尔莫线系中的伽玛线,波长4347.40埃1年前查看全部
- 按照玻尔理论,氢原子从能级A跃迁到能级B时,释放频率为ν1的光子;氢原子从能级B跃迁到能级C时,吸收频率为ν2的光子,且
按照玻尔理论,氢原子从能级A跃迁到能级B时,释放频率为ν1的光子;氢原子从能级B跃迁到能级C时,吸收频率为ν2的光子,且ν1>ν2.则氢原子从能级C跃迁到能级A时,将( )
A.吸收频率为ν2-ν1的光子
B.吸收频率为ν1-ν2的光子
C.吸收频率为ν2+ν1的光子
D.释放频率为ν1+ν2的光子 jklopp1年前1
jklopp1年前1 -
 avz6 共回答了12个问题
avz6 共回答了12个问题 |采纳率91.7%解题思路:从高能级向低能级跃迁,释放光子,从低能级向高能级跃迁,吸收光子,根据光子频率的大小比较出A、C的能级高低,并求出两个能极差,从而求出光子的频率.因为ν1>ν2.AB的能极差为hv1,BC的能极差为hv2,AB的能级差大于BC的能级差,所以C的能级低于A的能级,两者的能级差为hv1-hv2,所以从能级C跃迁到能级A时,吸收光子,有hv3=hv1-hv2,所以v3=v1-v2.故B正确,A、C、D错误.
故选B.点评:
本题考点: 氢原子的能级公式和跃迁.
考点点评: 解决本题的关键知道能级差与光子频率的关系Em-En=hv.以及知道高能级向低能级跃迁,释放光子,从低能级向高能级跃迁,吸收光子.1年前查看全部
- 根据玻尔的氢原子理论,下列说法中错误的是( )
根据玻尔的氢原子理论,下列说法中错误的是( )
A.氢原子的轨道是不连续的
B.氢原子具有的稳定能量状态称为定态
C.氢原子在辐射光的同时能量也在减小
D.用任何光照射氢原子都可以使其发生跃迁 tiitee1年前1
tiitee1年前1 -
 铿锵铁嘴7人行 共回答了21个问题
铿锵铁嘴7人行 共回答了21个问题 |采纳率85.7%解题思路:根据玻尔的氢原子理论,知轨道、原子的能量都是量子化的,吸收光子,能量增大,辐射光子,能量减小.A、氢原子轨道是量子化的,不连续.故A正确.
B、氢原子具有的稳定能量状态称为定态.故B正确.
C、氢原子在辐射光子时,能量减小,吸收光子,能量增加.故C正确.
D、能级间跃迁吸收的光子必须等于两能级间的能级差,才能被吸收发生跃迁.故D错误.
本题选错误的,故选D.点评:
本题考点: 氢原子的能级公式和跃迁.
考点点评: 解决本题的关键知道玻尔理论的内容,以及知道能级间跃迁所满足的规律.1年前查看全部
- 根据玻尔理论,在氢原子中,量子数n越大,则( )
根据玻尔理论,在氢原子中,量子数n越大,则( )
A. 电子轨道半径越小
B. 核外电子运动速度越小
C. 原子能级的能量越小
D. 电子的电势能越大 lxcql3121年前1
lxcql3121年前1 -
 loveme821 共回答了22个问题
loveme821 共回答了22个问题 |采纳率86.4%解题思路:在氢原子中,量子数n越大,原子的能量越大,根据库仑引力提供向心力,根据轨道半径的变化,判断电子动能的变化.原子能量等于电子动能和势能的总和,从而确定电子势能的变化.n越大,轨道半径越大,原子能量越大,根据k
e2
r2=m
v2
r,知电子的动能越小,原子能量等于电子动能和势能的总和,知电阻的电势能越大.故B、D正确,A、C错误.
故选BD.点评:
本题考点: 玻尔模型和氢原子的能级结构.
考点点评: 解决本题的关键知道量子数越大,轨道半径越大,电子动能越小,原子能量越大,电子电势能越大.1年前查看全部
- 根据玻尔理论,某原子的电子从能量为E的轨道跃迁到能量为E′的轨道,辐射出波长为λ的光,以h表示普朗克常量,c表示真空中的
根据玻尔理论,某原子的电子从能量为E的轨道跃迁到能量为E′的轨道,辐射出波长为λ的光,以h表示普朗克常量,c表示真空中的光速,则E′等于E-h[C/λ]E-h[C/λ].如果大量氢原子处在n=4的能级,会辐射出______种频率的光.
 石榴大仙1年前1
石榴大仙1年前1 -
 扎毛 共回答了12个问题
扎毛 共回答了12个问题 |采纳率91.7%解题思路:因为Em-En=hγ,根据两轨道的能级差等于光子能量,求出E′大小.
根据数学组合公式
求出大量的氢原子从n=4能级轨道向低能级轨道跃迁所辐射的光子的频率的种数.C 2n根据两轨道的能级差等于光子能量,
E-E′=hγ=h[C/λ],
所以E′=E-h[C/λ].
根据
C24=6知,大量的氢原子从n=4能级轨道向低能级轨道跃迁所辐射的光子的频率最多有6种.
故答案为:E-h[C/λ],6.点评:
本题考点: 玻尔模型和氢原子的能级结构.
考点点评: 解决本题的关键知道高能级向低能级跃迁,辐射光子,从低能级向高能级跃迁,吸收光子.以及掌握能级差与光子频率的关系.
同时知道激发态不稳定,会向基态发生跃迁,不同的能级间有不同的能极差,辐射的光子频率不同.1年前查看全部
- 下列说法正确的是( )A.光电效应现象揭示了光具有粒子性B.阴极射线的本质是高频电磁波C.玻尔提出的原子模型,否定了卢
下列说法正确的是( )
A.光电效应现象揭示了光具有粒子性
B.阴极射线的本质是高频电磁波
C.玻尔提出的原子模型,否定了卢瑟福的原子核式结构学说
D.贝克勒尔发现了天然放射现象,揭示了原子核内部有复杂结构 卡卡小强1年前1
卡卡小强1年前1 -
 完颜玳佳 共回答了20个问题
完颜玳佳 共回答了20个问题 |采纳率90%解题思路:光电效应现象揭示了光具有粒子性,阴极射线的本质是高速电子流,玻尔提出的原子模型认为电子只能在特定的轨道上运行.A、光电效应现象揭示了光具有粒子性,A正确;
B、阴极射线的本质是高速电子流,B错误;
C、玻尔提出的原子模型认为电子只能在特定的轨道上运行,没否定卢瑟福的核式结构模型,C错误;
D、贝克勒尔发现了天然放射现象,揭示了原子核内部有复杂结构,D正确;
故选:AD点评:
本题考点: 光电效应;玻尔模型和氢原子的能级结构;原子核衰变及半衰期、衰变速度.
考点点评: 本题考查了原子的结构和物理学史,难度不大,注意基础知识的积累.1年前查看全部
- 关于玻尔原子理论的基本假设,下列说法中正确的是 ( )
关于玻尔原子理论的基本假设,下列说法中正确的是 ( )
A.原子中的电子绕原子核做圆周运动,库仑力提供向心力
B.电子绕核运动的轨道半径只能取某些特定的值,而不是任意的
C.原子的能量包括电子的动能和势能,电子动能可取任意值,势能只能取某些分立值
D.电子由一条轨道跃迁到另一条轨道上时,辐射(或吸收)的光子频率等于电子绕核运动的频率
D为什么不对? kuengyelong1年前2
kuengyelong1年前2 -
 鸟也不鸟你 共回答了16个问题
鸟也不鸟你 共回答了16个问题 |采纳率81.3%AB多选题.是能和动能都是分立的.与绕核运动频率无关,与能级差有关.1年前查看全部
- 带核原子结构模型是由那个科学家提出的 A.道尔顿 B.汤姆生 C.卢瑟福 D.玻尔 为什么不是B
 麦克巴拉克1年前2
麦克巴拉克1年前2 -
 鹰叼梅 共回答了13个问题
鹰叼梅 共回答了13个问题 |采纳率84.6%带核原子结构模型是一个专指地名词特指玻尔行星模型.汤姆孙的是西瓜模型1年前查看全部
- 根据玻尔理论,氢原子核外电子在n=1和n=2 轨道运动时轨道半径之比为1:4 怎么的出来的
根据玻尔理论,氢原子核外电子在n=1和n=2 轨道运动时轨道半径之比为1:4 怎么的出来的
Rn=R1×n2(n的平方),R1有具体的值,是5.29×10的-11次方。
n=1时,半径是R1;
n=2时,半径是R1×(2的平方)=4R1;
所以R1:R2=1:
没明白可以继续问。 蓝地丝的手指1年前1
蓝地丝的手指1年前1 -
 花溪南风 共回答了17个问题
花溪南风 共回答了17个问题 |采纳率100%你的解答是正确的.不过可以进一步简单.
设第1可能轨道半径为r1
由玻耳理论,得第2可能轨道半径为r2=2²r1=4r1
于是有r1:r2=1:4.1年前查看全部
- 关于玻尔理论,原子中各级电子轨道半径大小(数据).
关于玻尔理论,原子中各级电子轨道半径大小(数据).
电子轨道量子化理论 人养一样的人1年前1
人养一样的人1年前1 -
 我爱你婷 共回答了22个问题
我爱你婷 共回答了22个问题 |采纳率95.5%波尔半径是 5.29*10^-11 m
其他的数据是每个原子不同而不同的
要根据有效核电数还有波函数去共同判断的1年前查看全部
- 根据玻尔理论,氢原子中,量子数N越大,则下列说法中正确的是( )
根据玻尔理论,氢原子中,量子数N越大,则下列说法中正确的是( )
A.电子轨道半径越大
B.核外电子的速率越大
C.氢原子能级的能量越大
D.核外电子的电势能越小 空许1年前1
空许1年前1 -
 tlbbs 共回答了16个问题
tlbbs 共回答了16个问题 |采纳率81.3%解题思路:量子数越大,轨道半径越大,原子能量变大,根据库仑引力提供向心力得出电子动能的变化,通过能量变化和电子动能变化得出电势能的变化.在氢原子中,量子数越大,电子的轨道半径越大,原子能级的能量越大,
根据
ke2
r2=m
v2
r,知电子动能减小,核外电子速度减小.由于能量增大,电子动能减小,则电势能增大.故A、C正确,B、D错误.
故选:AC.点评:
本题考点: 玻尔模型和氢原子的能级结构.
考点点评: 解决本题的关键知道电子动能、原子能量与轨道半径的关系.知道原子能量等于电子动能和电势能之和.1年前查看全部
- 量子力学认为:微观粒子的波动是一种概率波.请以此阐明玻尔假说中的不足之处.
 浙林经济学会1年前3
浙林经济学会1年前3 -
 云清淡 共回答了20个问题
云清淡 共回答了20个问题 |采纳率95%波尔在研究微观粒子时引入了“轨道""向心力”等概念,但牛顿定律在微观世界不适用.1年前查看全部
大家在问
- 1一个长方形周长为24厘米,这个长方形的长减少3厘米宽增加1厘米长方形就变成了正方形求长方形的面积
- 2一栋楼有15层共42米,小红家住6楼.问小红家的地板到地面有多高?
- 3英语翻译(1):墙上有一幅画.(2):墙上有一扇窗.(3):桌上有一些面包.(4):桌上有一些面包和一个牛奶.
- 4(1)x 2 -2x-2=0.(用配方法)
- 5some与any的用法虽然已知道some用于肯定,any用于否定或疑问 但总是迷迷糊糊记得有时候some也可以用于肯定或
- 6求微分方程yy′+e2x+y2=0满足y(0)=0的特解为______.
- 7人类在新材料探索的道路上总在进行着不懈的努力,世界上密度最小的固体“气凝胶”就是新材料探索的重要成果,气凝胶是一种多孔状
- 8完形填空(共20小题;每小题1分,满分20分)
- 9(2010•启东市模拟)实验是化学研究的基础,下列是在实验室中完成的不同的化学实验,其中能达到实验目的是( )
- 10数字电路题目:所有的rs触发器都有着同样的约束条件()
- 11我心中的丑小鸭作文
- 12I can't cook the
- 13怎样学才能表达出流利的英语呢?学了这么多年的英语,到用的时候,就是说不出来,真的很惭愧!怎样才能做到用英语交流能想像汉语
- 14分别锻造直径为16cm,高为35cm和直径为20cm,高为20cm的圆柱零件毛坯各一个,需要取直径为40cm的圆钢多少厘
- 15to,home,itis,time,go,这些单词怎么可以变成句子
