挥发性物质有哪些 酸是不是 除了两个外都不挥发 那两个是什么啊
 有皮无心树2022-10-04 11:39:541条回答
有皮无心树2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 花间妲己 共回答了20个问题
花间妲己 共回答了20个问题 |采纳率95%- 高中化学里吸水物质主要有无水硫酸铜、无水氯化钙、浓硫酸、碱石灰这些.挥发性物质主要是浓盐酸、浓硝酸.
高中化学里不挥发的酸指的是硫酸(H2SO4)和磷酸(H3PO4) - 1年前
相关推荐
- 无水乙醇和异丙醇谁的挥发性
 yihy1年前2
yihy1年前2 -
 edmondchem 共回答了16个问题
edmondchem 共回答了16个问题 |采纳率93.8%涂料工业中,对纯溶剂挥发速率的表示是使用的相对挥发速率概念,依据ASTM3539-76
规定方法,用Shell薄膜挥发仪,将一定体积熔剂分布在标准面积的滤板上,在一定的温度和湿度下,气流以一定流量通过,记录一定时间间隔的挥发量,并将挥发量为90%的挥发时间与醋酸正丁酯.挥发量为90%的时间(t90=456s)的比值,称为该熔剂的相对挥发速率.
醋酸正丁酯的比挥发速度记为100,则乙醇的比挥发速度为203,异丙醇的比挥发速度为205.二者挥发速度相差不大.1年前查看全部
- 若实验室只提供氢氧化钠稀溶液,浓盐酸,酚酞试液,证明浓盐酸具有挥发性从而说明分子在不断运动.要求:1.写出实验过程2.描
若实验室只提供氢氧化钠稀溶液,浓盐酸,酚酞试液,证明浓盐酸具有挥发性从而说明分子在不断运动.要求:1.写出实验过程2.描述实验现象3.写有关的化学方程式
 vcciu661年前2
vcciu661年前2 -
 突然的温柔 共回答了14个问题
突然的温柔 共回答了14个问题 |采纳率78.6%弄个密封玻璃罩,里面放供氢氧化钠稀溶液,里面滴酚酞试液,边上放浓盐酸,过会儿发现红色褪去,说明浓盐酸具有挥发性,既分子在不断运动.
方程式就是HCL+NAOH=NACL+H2O1年前查看全部
- 把空气通入非挥发性溶质的溶液中.会带出什么(溶剂,还是溶质加溶剂)?(溶剂易挥发)
把空气通入非挥发性溶质的溶液中.会带出什么(溶剂,还是溶质加溶剂)?(溶剂易挥发)
rt tourmancc1年前2
tourmancc1年前2 -
 sftbg 共回答了15个问题
sftbg 共回答了15个问题 |采纳率93.3%前者:溶剂.
因为你自己已经回答这个问题:非挥发性溶质.不挥发当然不可能随空气带出.1年前查看全部
- 除了c2h5oh和hcl,还有哪些物质具有挥发性?
 雯武1年前1
雯武1年前1 -
 allgone 共回答了18个问题
allgone 共回答了18个问题 |采纳率88.9%浓硝酸 丙酮 氢卤酸 乙酸、丙酸、丁酸、异丁酸、戊酸、异戊酸、正丁酸、苯
等1年前查看全部
- 硝酸挥发性比盐酸强?
 寺面河1年前2
寺面河1年前2 -
 遍地英雄下夕烟 共回答了17个问题
遍地英雄下夕烟 共回答了17个问题 |采纳率100%对1年前查看全部
- 盐酸的挥发性与哪些因素有关?
 3733568801年前1
3733568801年前1 -
 大亮 共回答了17个问题
大亮 共回答了17个问题 |采纳率82.4%这个东西需要密封保存的,挥发一般都是和温度有关的,还有就是敞开的面积大小吧.当然盐酸本身的挥发性就很强,所以必须密封保存.与HCl的蒸汽分压有关,盐酸溶液中HCl的蒸汽压低,则意味着,HCl扩散至空气而返回的几率减小了(我们吹热水可加快蒸发也是使蒸汽压减小了的缘故),浓盐酸有更强的挥发性则因为其浓度更高则其变换的平衡常数越小1年前查看全部
- 化学中常见的气体和易挥发性物质有那些
 阿钟阿钟1年前1
阿钟阿钟1年前1 -
 huachin83 共回答了14个问题
huachin83 共回答了14个问题 |采纳率92.9%浓盐酸,浓氨水,酒精(包括醇类吧),甲醛(醛类?),溴水,浓硝酸
浓氨水和浓硝酸也应该是易分解的物质吧~
----单质:Br2,I2
----氧化物:CO2(干冰),
----氢化物:NH3(液氨),H2O,苯,汽油等烃类
----酸:HNO3(硫酸是难挥发性酸,其沸点300多度)
----很多有机物:乙醇,乙酸,乙醛,乙酸乙酯
1.易挥发的物质都是分子晶体
----晶体有四类:原子晶体离子晶体分子晶体金属晶体
----原子晶体离子晶体分子晶体中微粒间的相互作用分别是共价键离子键金属键,是化学键,是强相互作用,使微粒间的结合很牢固,使微粒间很难相互脱离开而挥发出来.
----分子晶体中分子间的相互作用是分子间作用力,不是化学键,是弱相互作用.使得分子间容易相互脱离开.
2.分子晶体中
----沸点越低的越易挥发.
----分子间作用力越大,沸点越高.
----分子间作用力的大小和分子的结构性质有关.
----结构相似的,分子量越大,分子间作用力越大,沸点越高,越难挥发.
----分子间存在氢键时,分子间作用力大沸点高,难挥发.
3.易挥发的物质
----一般是指常温下呈液态或固态的.
----单质:Br2,I2
----氧化物:CO2(干冰),
----氢化物:NH3(液氨),H2O,苯,汽油等烃类
----酸:HNO3(硫酸是难挥发性酸,其沸点300多度)
----很多有机物:乙醇,乙酸,乙醛,乙酸乙酯
----因为很多有机物是分子晶体.
----是的,鼻子接触到了挥发出的分子.1年前查看全部
- 易挥发性物质易挥发的液体有哪些啊?比如水也算,越多越好.
 qepaa1年前3
qepaa1年前3 -
 林音女 共回答了23个问题
林音女 共回答了23个问题 |采纳率95.7%酒精、汽油、丙酮、浓盐酸、氨水、液态溴 、丙烯酸1年前查看全部
- 甲烷中混有乙烯通入溴水,然后洗气,(溴和二溴乙烷的挥发性要考虑吗?)
 tommyking19821年前1
tommyking19821年前1 -
 断刀流水1147 共回答了17个问题
断刀流水1147 共回答了17个问题 |采纳率94.1%可以,且只能用溴水,乙烯与溴水加成生成液体,即被除去.
此处不可以用酸性高锰酸钾,因为酸性高锰酸钾会将乙烯氧化,可能生成二氧化碳,又引入新的杂质.
在除杂时一般不考虑挥发性,因为无需加热(特例:除去溶液中少量HCl可利用其挥发性,加热出去)1年前查看全部
- 甲烷与氯气反应产生白雾,那生成的HCL挥发性有这么强?有这么浓?
 夜空中飞翔的鱼1年前1
夜空中飞翔的鱼1年前1 -
 狼一样的男人 共回答了16个问题
狼一样的男人 共回答了16个问题 |采纳率93.8%CH4和Cl2反应生成的HCl是气态的,遇水就会产生白雾,这个和浓度无关
挥发性是指化合物由固体或液体变为气体或蒸汽的过程,这个时候的HCl是气态,不能说有挥发性
你要确定的是,是生成HCl气体,不是盐酸1年前查看全部
- 稀盐酸是否有挥发性一般题目中出现的盐酸是指稀盐酸还是指浓盐酸【在关于挥发性的题目中】
 huas20071年前3
huas20071年前3 -
 一斤米 共回答了13个问题
一斤米 共回答了13个问题 |采纳率92.3%浓盐酸具有挥发性而稀盐酸不具有,所以在涉及挥发性问题时会指出盐酸的浓度.1年前查看全部
- 盐酸具有那些性质酸性,氧化性、还原性、挥发性4选1
 安阳951年前1
安阳951年前1 -
 大庆VS小黑 共回答了14个问题
大庆VS小黑 共回答了14个问题 |采纳率100%31年前查看全部
- 散剂中如何含有少量的挥发性液体及含有酊剂,流浸膏时应如何制备?
 suzmb1年前1
suzmb1年前1 -
 海子_OK 共回答了17个问题
海子_OK 共回答了17个问题 |采纳率88.2%1)处方中含有少量的液体成分,如挥发油、酊剂、流浸膏等,可利用处方中其他固体成分吸收;
2)方中含有较多量的液体成分,可另加适量的吸收剂(如:磷酸钙、淀粉、蔗糖等)吸收至不显潮湿为度.1年前查看全部
- 浓盐酸有挥发性,会挥发岀HCl,敞口放置,为什么溶质质量会减小啊?
浓盐酸有挥发性,会挥发岀HCl,敞口放置,为什么溶质质量会减小啊?
溶质可以是气体对吧? 榕21年前1
榕21年前1 -
 huangsana 共回答了21个问题
huangsana 共回答了21个问题 |采纳率90.5%浓盐酸的溶剂是水,溶质是HCl,会发出HCl,溶质质量当然减少.1年前查看全部
- γ-羟基丁酸挥发性如何,暴露在空气中大概多久完全挥发
 财神路过了1年前2
财神路过了1年前2 -
 铅笔贼迷茫 共回答了15个问题
铅笔贼迷茫 共回答了15个问题 |采纳率86.7%有机酸随着碳链的增大,挥发性降低,再加入羟基使分子间作用力更加强大,所以该酸基本不挥发1年前查看全部
- 为什么打开浓盐酸时会有白雾HCl气体是白色的吗?不然就算是挥发性,能看到雾也必须有温度差?还是说它挥发时会吸热?
 竹案陈兵1年前1
竹案陈兵1年前1 -
 折柳寻秋 共回答了15个问题
折柳寻秋 共回答了15个问题 |采纳率80%HCL气体是无色的,看到的白色盐酸酸雾是盐酸挥发出来的氯化氢与空气中的水蒸气结合成的小液滴.
能不能形成酸雾与盐酸的浓度,温度和空气湿度有关,就和冬天可以看见呼吸的哈气原理差不多.
挥发是分子运动,就和水蒸发一样,都会吸点热.但是不会温度降的很低.1年前查看全部
- 浓硫酸制取盐酸 酸性浓硫酸和NaCl固体在加热条件下制取HCl气体体现了浓硫酸什么性质?答案:高沸点,低挥发性我不懂的是
浓硫酸制取盐酸 酸性
浓硫酸和NaCl固体在加热条件下制取HCl气体体现了浓硫酸什么性质?
答案:高沸点,低挥发性
我不懂的是,为什么没体显酸性?
它生成了新盐的嘛,咋会没体现难? 小wu29371年前3
小wu29371年前3 -
 elaine_leong 共回答了14个问题
elaine_leong 共回答了14个问题 |采纳率100%此反应为高沸点酸制取低沸点酸,浓硫酸是高沸点酸,难挥发,盐酸是低沸点酸,易挥发.浓硫酸和氯化钠反应时,由于反应剧烈放热,经过复分解产生的HCl在溶液中溶解度变小不断挥发出来.两者都是强酸 .1年前查看全部
- 氧化性有机气体谁知道那些有机气体或者挥发性有机液体是氧化性的
 jjzyb1年前1
jjzyb1年前1 -
 kangyuanku 共回答了18个问题
kangyuanku 共回答了18个问题 |采纳率88.9%羧酸有氧化性,醛应该也有,甲醛应该符合条件1年前查看全部
- 可燃性,助燃性,氧化性,挥发性哪个属于物理性质?
 google8081年前3
google8081年前3 -
 forkme 共回答了20个问题
forkme 共回答了20个问题 |采纳率100%挥发性1年前查看全部
- 用易挥发性的有机物质培养晶体时应注意什么
 kingcsg1年前1
kingcsg1年前1 -
 zidaye1981 共回答了22个问题
zidaye1981 共回答了22个问题 |采纳率81.8%防止其水解挥发,因此要注意温度的控制,因为水解为吸热,所以根据勒夏特列原理,温度不宜过高,否则会使平衡正向移动.
也可以添加这些挥发性物质,使平衡逆向移动,也可达到减少水解的作用.1年前查看全部
- 氨水的易挥发性为什么可鉴别挥发性酸的存在
氨水的易挥发性为什么可鉴别挥发性酸的存在
为什么不是氨水挥发后与玻璃棒上的酸接触而产生白烟,而非酸的挥发 gayboy83001年前2
gayboy83001年前2 -
 工大人 共回答了15个问题
工大人 共回答了15个问题 |采纳率93.3%形成了颗粒状铵盐
飘在空中可以看见,现象明显
他们飘在空中哈
要只是氨水的挥发
颗粒状盐只会粘在玻棒上1年前查看全部
- 乙酸钠再跟难挥发性的酸(如硫酸)共热,蒸馏得乙酸的原理.有化学式的写化学式.谢谢
 焦糖mm1年前1
焦糖mm1年前1 -
 ruyuexc 共回答了21个问题
ruyuexc 共回答了21个问题 |采纳率100%这是用难挥发性的酸质易挥发性的酸,乙酸易挥发,硫酸难挥发.
2CH3COONa+H2SO4==Na2SO4+2CH3COOH,条件是加热,乙酸写气体箭头.1年前查看全部
- 为什么浓盐酸具有挥发性我只是觉得很奇怪,稀盐酸就没有,浓盐酸为啥就有类?不要告诉我怎么证明出来的,我只想知道为什么,好奇
为什么浓盐酸具有挥发性
我只是觉得很奇怪,稀盐酸就没有,浓盐酸为啥就有类?
不要告诉我怎么证明出来的,我只想知道为什么,好奇而已. cumtzlp1年前2
cumtzlp1年前2 -
 keikei0907 共回答了24个问题
keikei0907 共回答了24个问题 |采纳率83.3%盐酸是氯化氢溶于水 浓盐酸中的氯化氢溶得很多而且会放出热量,气体受热么会跑出来的(就和可乐一样的原理)而空气中有水分形成盐酸小液滴白雾.
我坦白这是我贴的.但是感觉这是对的.
1楼太扯吧,浓硫酸咋没挥发性?纯物质咋没挥发性?
主要还是氯化氢在地球常态环境下是气体形式……1年前查看全部
- 英语翻译本文就竹叶挥发油化学组成、生物活性、应用,植物挥发性化合物在降脂降糖方面的应用进行综述,归纳了竹叶挥发物研究中存
英语翻译
本文就竹叶挥发油化学组成、生物活性、应用,植物挥发性化合物在降脂降糖方面的应用进行综述,归纳了竹叶挥发物研究中存在的不足,对竹叶挥发油在降糖脂方面的研究进行了展望.
就一句,不要用翻译工具! 深圳一生何求1年前1
深圳一生何求1年前1 -
 爱ee思远 共回答了16个问题
爱ee思远 共回答了16个问题 |采纳率93.8%This paper summarizes the chemical constituents, biological activities and applications of the volatile oil from leaves of phyllostachys pubescens, as well as the application of plant volatile semiochemicals in the aspects of lipid and glucose reduction. It generalizes the inadequacies in the research of phyllostachys pubescens leaf volatiles, and predicts its prospects in the lipid and glucose reduction researches.
【英语牛人团】1年前查看全部
- 浓盐酸的挥发性属于物理反应还是化学反应?
 hjl251年前2
hjl251年前2 -
 多么深的领悟 共回答了11个问题
多么深的领悟 共回答了11个问题 |采纳率90.9%物理反应 因为它的分子没有改变1年前查看全部
- 偏磷酸的溶解性,挥发性是否容易溶解?是否容易挥发?(受热)
 songdx1年前1
songdx1年前1 -
 泉州南安 共回答了26个问题
泉州南安 共回答了26个问题 |采纳率88.5%易溶 ,不易挥发1年前查看全部
- 氯化镍的挥发性和毒性氯化镍的水合物挥发性如何?如果皮肤接触有毒性吗?吸入呢?希望这方面的专家能回答一下
 prince9808161年前2
prince9808161年前2 -
 娃哈哈zh 共回答了28个问题
娃哈哈zh 共回答了28个问题 |采纳率89.3%氯化镍(II),是化学式为NiCl2的化合物.无水二氯化镍为黄色,但它在自然界中很少见,仅在水氯镍石这样的矿石中可以发现,而更为人们所熟悉的是绿色的六水合二氯化镍(NiCl2·6H2O).二氯化镍还有一系列已知的水合物,均为绿色.通常来讲,二氯化镍是化工合成中最重要的重要的镍源.镍盐均有致癌性.氯化镍的水合物挥发性基本是没有的.但如果皮肤接触还是有可能被毛孔吸收的,有致癌性的,所以我们做实验的时候都是戴手套保护的,一般不会让它接触到皮肤的,万一不小心接触到的话,赶紧用大量水冲洗.手机提问的朋友在客户端右上角评价点【满意】即可.互相帮助,祝共同进步1年前查看全部
- 熔沸点和挥发性有什么关系没有
 berlinqq1年前1
berlinqq1年前1 -
 三十六画生 共回答了17个问题
三十六画生 共回答了17个问题 |采纳率88.2%熔点是指物质有固态变为液态时所需要达到的温度点,而沸点是物质由液态变为气态所需要的温度点.而挥发也是由固态或液态变为气态,从变化结果来说,挥发性和沸点有相似之处,两者的不同在于沸腾的液体变为气体的过程是剧烈的,快速的,而挥发是缓慢的,不易察觉的.希望能够帮到你!1年前查看全部
- 就想了解硫酸与盐酸的特性,各种特性,浓的跟稀的又有什么特性?,物理性质中的颜色,气味,挥发性,就不用说了,关键的说清楚就
就想了解硫酸与盐酸的特性,各种特性,浓的跟稀的又有什么特性?,物理性质中的颜色,气味,挥发性,就不用说了,关键的说清楚就行了,如其中浓盐酸在空气中易产生白雾类似于这种的特点
 吉诺比利1年前3
吉诺比利1年前3 -
 vicly8551 共回答了18个问题
vicly8551 共回答了18个问题 |采纳率94.4%你是初中吧 上面那个感觉像说明文了(- -|||)
就是要帮你归纳下初中阶段 盐酸和硫酸的性质嘛!
盐酸(HCl)
实质是氯化氢气体溶于水(所以奥赛之类的不能写"HCl"来代替盐酸 写中文)
无色液体(工业上的盐酸因为还有杂质氯化铁 所以是淡黄色)
具有刺激性气味
浓盐酸 一般达到37%左右
具有强烈的挥发性
暴露在空气中会迅速挥发 与空气中的水蒸气接触形成可见的白雾
(但不是说稀盐酸就不会挥发 在综合实验题里 一般无论盐酸的浓度 都会考虑挥发的性质 因而必要的话要消除这一影响)长期放置在空气中会因挥发而是浓度降低
初中所学有关盐酸的反应是
CaCO3+2HCl=CaCl2+H2CO3 =>CaCl2+H2O+CO2↑(碳酸易分解成水和二氧化碳)这个是制取二氧化碳的反应式 因为石灰石加盐酸反应速度适中 产生二氧化碳多 别看有三个生成物 但绝对是复分解反应 通常用于考综合题 注意反应装置的选择
盐酸+碱=盐+水 酸碱中和反应 考分析题比较可能
还要注意盐酸与硝酸的反应生成不溶于硝酸的氯化银
硫酸(H2SO4)这个就考得很多啦!
无色液体 无挥发性 也无气味
浓硫酸 浓度可以达到98%左右 是一种较粘稠的液体
无色无味也不挥发
具有强烈的吸水性 脱水性 长期放置在空气中会因吸取空气中的水蒸气导致浓度降低 在实验室中常常当作干燥剂使用
常见的化学反应
各种活泼金属与其反应置换出氢气(化学式太多 懒得写了)这个作为初中置换反应的模本来学习 生成对应的硫酸盐和氢气 (但钾 钙 钠与其反应会直接将产生的氢气氧化成水因而无法得到氢气)
然后是硫酸与氧化铜生成硫酸的反应 只是工业上最普通的制取硫酸铜的做法
还要注意在综合题里浓硫酸做脱水剂的用法
就这么多了 我没看书打的 可能有些遗漏 还有酸的通性我都没打进去
其实初中的化学很简单 还是看书最好 不懂得再问老师1年前查看全部
- 关于浓硫酸性质氯化钠固体跟浓硫酸的混合物供热时产生氯化氢气体为什么利用的是浓硫酸的高沸点,难挥发性而不是吸水性
 吸血虫1年前3
吸血虫1年前3 -
 浪子777 共回答了17个问题
浪子777 共回答了17个问题 |采纳率88.2%氯化钠固体并没有水,和谈吸水性?吸水性从结果上说只是物理变化,硫酸夺去了其他物质的水分子(当然硫酸与水的结合也是化学反应过程)
氯化钠固体跟浓硫酸的混合物供热时产生氯化氢气体,是因为混合物中同时有浓硫酸(因为酸性产生氢离子、硫酸根离子)、氯离子和钠离子,加热时氯离子结合硫酸的氢离子挥发了,而硫酸沸点高不易挥发,氯化钠、硫酸钠也不挥发,所以利用浓硫酸的高沸点,难挥发性1年前查看全部
- 有多种有机物质溶入水中,我想用蒸馏技术分离它们,可溶液的温度最高就100度.其中有易挥发性的,请指教
 zhao41101年前1
zhao41101年前1 -
 sleepingpig 共回答了12个问题
sleepingpig 共回答了12个问题 |采纳率91.7%蒸不出来的,多种物质会形成共沸物.
首先看有机物质都是什么性质的,然后才好设计分离方法.1年前查看全部
- .离子反应成立的条件.离子反应的条件就是有难溶的物质或难电离的物质或挥发性的物质生成.为什么氯化亚铁溶液中通入氯气:2F
.离子反应成立的条件.
离子反应的条件就是有难溶的物质或难电离的物质或挥发性的物质生成.为什么氯化亚铁溶液中通入氯气:2FeCI2===2Fe3+ +2CI-可以写成离子反应式.目前就是这个问题了. 卢舍那3651年前1
卢舍那3651年前1 -
 heryla 共回答了14个问题
heryla 共回答了14个问题 |采纳率92.9%Cl2比Fe3+氧强 化学上有很多模棱两可如离子共存时
颜色
复分解 气体 沉淀 弱电解质 所谓的离子反应条件
氧化还原 一般考强氧:MO4- Fe3+ NO3-(H+) ClO-
还:S2- I- SO32- Fe2+
字不够1年前查看全部
- 有挥发性的物质可以说是气体吗?
 宋玉文1年前2
宋玉文1年前2 -
 oomm8 共回答了19个问题
oomm8 共回答了19个问题 |采纳率84.2%这个当然不能全说是气体了.比如:盐酸,本身来产就不是气体.挥发出来的物质是氯化氢,而盐酸本身是氯化氢的水溶液,所以,盐酸不是气体.又如:水,本身只是液体,而其有气态水蒸气,而这样不能说水是气体.1年前查看全部
- 盐酸的挥发性与哪些因素有关?
 chaochengluo1年前1
chaochengluo1年前1 -
 知子之来之 共回答了14个问题
知子之来之 共回答了14个问题 |采纳率92.9%这个东西需要密封保存的,挥发一般都是和温度有关的,还有就是敞开的面积大小吧.当然盐酸本身的挥发性就很强,所以必须密封保存.与HCl的蒸汽分压有关,盐酸溶液中HCl的蒸汽压低,则意味着,HCl扩散至空气而返回的几率减小了(我们吹热水可加快蒸发也是使蒸汽压减小了的缘故),浓盐酸有更强的挥发性则因为其浓度更高则其变换的平衡常数越小1年前查看全部
- 下列描述属于物质化学性质的是:A盐酸具有挥发性B浓硫酸的吸水性C:浓硝酸的强氧化性D:溶液的导电性
下列描述属于物质化学性质的是:A盐酸具有挥发性B浓硫酸的吸水性C:浓硝酸的强氧化性D:溶液的导电性
这不是一个答案的探索.而是一种严谨的讨论吼吼. 唐家三少爷1年前3
唐家三少爷1年前3 -
 風驶流云 共回答了14个问题
風驶流云 共回答了14个问题 |采纳率92.9%A盐酸具有挥发性:物理性质,都是以HCl的形式存在,没有新物质生成;
B浓硫酸的吸水性:物理性质,没有新物质生成,虽然浓度有变化;
C浓硝酸的强氧化性:化学性质,反应出氧化性,硝酸里面氮的价态务必发生变化即有新物质生成,所以属于化学变化;
D溶液的导电性:物理变化,因为无新物质生成.1年前查看全部
- 与元素周期律有关的相关问题1、如何比较同周期或同主族元素单质熔点如:碳、硅;2、稀硝酸有挥发性吗?3、如何比较对角线上(
与元素周期律有关的相关问题
1、如何比较同周期或同主族元素单质熔点如:碳、硅;
2、稀硝酸有挥发性吗?
3、如何比较对角线上(从左上到右下方)元素的金属性或非金属性,如N和s;铝和锗
4金属性与金属的活泼性有何区别?(为什么金属性中钠大于钙而活泼性中钙大于钠(根据金属活动顺序表))
5、原子核对核外电子吸引力如何判断?(如电子层数不同如氢和氯) 肖锋朗1年前2
肖锋朗1年前2 -
 13494 共回答了21个问题
13494 共回答了21个问题 |采纳率81%1:单质的熔点
(1)同一周期元素随原子序数的递增,元素组成的金属单质的熔点递增,非金属单质的熔点递减;
(2)同一族元素从上到下,元素组成的金属单质的熔点递减,非金属单质的熔点递增
2:不具有,盐酸具有挥发性,硝酸易分解.
3:对角线原则是指某些相邻两个主族上下相差一个周期的元素之间性质显示出的规律性的相似
比如锂和镁,钠和钙,铍和铝,氧和氯等
4:金属性常表示元素的原子失去电子的倾向;元素的非金属性是指元素的原子得电子的能力.
金属性比较规律:1、由金属活动性顺序表进行判断.1年前查看全部
- 下列为小萍同学在实验室制取CO 2 并检验CO 2 性质的实验装置示意图(浓HCl有挥发性,2HCl+Ca(OH) 2
下列为小萍同学在实验室制取CO 2 并检验CO 2 性质的实验装置示意图(浓HCl有挥发性,2HCl+Ca(OH) 2 ===CaCl 2 +2H 2 O),试回答: 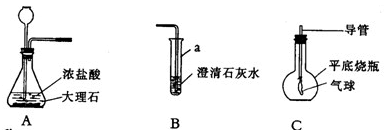
(1)仪器的名称:a ;
(2)用化学方程式表示实验室制取CO 2 的反应原理
(3)该同学在实验过程中,将A中产生的气体通入到B中,观察澄清石灰水的变化 (填浑浊或不浑浊),试分析其原因 。
(4)该同学用C瓶收集满一瓶由装置A中产生的气体后,往瓶中倒入浓氢氧化钠溶液,迅速用事先绑好一个小气球的胶塞塞紧,震荡,可以观察到小气球逐渐胀大,其原因是 ,请写出C中反应的化学方程式 。 nxxkeita1年前1
nxxkeita1年前1 -
 哈利小子 共回答了16个问题
哈利小子 共回答了16个问题 |采纳率81.3%(1)试管
(2) CaCO 3 + 2HCl===CaCl 2 + H 2 O + CO 2 ↑
(3)不浑浊,挥发出来的HCl和澄清石灰水反应
(4) 氢氧化钠和CO 2 ,HCl 反应,烧瓶内压强减小;
2NaOH + CO 2 ===Na 2 CO 3 + H 2 O ;HCl + NaOH===NaCl +H 2 O1年前查看全部
- 烟煤燃烧后的挥发性物质有哪些?
 nan_ge1年前1
nan_ge1年前1 -
 青蛙散步 共回答了22个问题
青蛙散步 共回答了22个问题 |采纳率95.5%二氧化硫、硫化氢、一氧化碳还有氮氧化物等1年前查看全部
- 那些气体的水溶液具有挥发性?那些酸碱盐溶液具有挥发性?
那些气体的水溶液具有挥发性?那些酸碱盐溶液具有挥发性?
最好能系统全面详细的介绍一下! 334808071年前2
334808071年前2 -
 qiuhanty 共回答了14个问题
qiuhanty 共回答了14个问题 |采纳率100%浓盐酸、浓硝酸易挥发,
碳酸一般马上分解成H2O和CO2↑,
NH4+遇到OH-马上生成NH3↑和H20.1年前查看全部
- 浓盐酸,稀盐酸,浓硫酸,稀硫酸,浓硝酸,稀硝酸的挥发性、强氧化性、腐蚀性分别如何,别的也可以补充.
浓盐酸,稀盐酸,浓硫酸,稀硫酸,浓硝酸,稀硝酸的挥发性、强氧化性、腐蚀性分别如何,别的也可以补充.
我不要复制的,请写清晰点.最好这种格式.
浓盐酸:
稀盐酸:
浓硫酸:
稀硫酸:
…… waitlly1年前0
waitlly1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 什么是化学性质的活泼性、物理性质的挥发性?
什么是化学性质的活泼性、物理性质的挥发性?
就这两个搞不懂?求懂! 出淤泥but不染1年前1
出淤泥but不染1年前1 -
 英木花痴 共回答了16个问题
英木花痴 共回答了16个问题 |采纳率100%活泼性是物质发生化学反应的难易程度,挥发性是物质气化由液态别成气态的性质1年前查看全部
- 什么叫难挥发性酸制易挥发性
 大铁锤搞破坏1年前1
大铁锤搞破坏1年前1 -
 蓝色20 共回答了15个问题
蓝色20 共回答了15个问题 |采纳率100%用H2SO4浓制HCl
因为H2SO4浓难挥发HCl易挥发
H2SO4浓+NaCl=加热=NaHSO4+HCl↑1年前查看全部
- 具有挥发性的物质如何判断其性质?
具有挥发性的物质如何判断其性质?
比如随时间推移的碳酸就变成水和CO2了,那他是不是一种酸?
氨水有挥发性,那他是不是一种缄?
过氧化氢电离时会产生H+,因此呈酸性.为什么他不是一种酸?(它也有挥发性) pyle7311年前1
pyle7311年前1 -
 hbr81cn 共回答了17个问题
hbr81cn 共回答了17个问题 |采纳率76.5%这里的酸有两种含义 ,一种是广义上的酸,一种是狭义上的酸,广义上的酸时只要能够在水溶液中电离出氢离子的,狭义上的酸就是日常生活中所称得了,譬如,盐酸,硫酸.如此等等.当然,你上边所说得都符合概念要求,所以说也是正确的.至于,具有挥发性的物质德行只要看他的状态而言,譬如说,你说的碳酸,当然是酸,但挥发之后,都已经不是碳酸了,当然不能再说是酸了.同理,也可知道其他.记住,碳酸的化学式是H2CO3,而不是co2.而氨水的化学式是nh3.h2o,而不是nh3而已,这是不同的,而过氧化氢则是没有发生变化的.1年前查看全部
- 为什么检验HCL挥发性,可以哈气?这是啥原理?
为什么检验HCL挥发性,可以哈气?这是啥原理?
为什么水蒸气和HCL两种气体相遇,会变成看得见的液体?什么原理啊? fuq81年前2
fuq81年前2 -
 王小浩 共回答了17个问题
王小浩 共回答了17个问题 |采纳率88.2%hcl很容易溶于水 哈气(水蒸气)提供溶剂1年前查看全部
- 硝酸具有挥发性说明硝酸不稳定?如题.
 yuanyou30001年前4
yuanyou30001年前4 -
 djspark 共回答了23个问题
djspark 共回答了23个问题 |采纳率91.3%不对
具有挥发性的东西不一定都不稳定,如浓盐酸也具有挥发性,但是盐酸比较稳定
硝酸不稳定是硝酸本身自有的性质,和挥发性无关
有挥发性的东西不一定不稳定,不具有挥发性的东西也不一定稳定1年前查看全部
- 北方建筑工人在秋冬季节和泥时,常用食盐水代替自来水,这是因为食盐水具有 A较好的流动性B较好的挥发性C较低的凝固性D较高
北方建筑工人在秋冬季节和泥时,常用食盐水代替自来水,这是因为食盐水具有 A较好的流动性B较好的挥发性C较低的凝固性D较高的凝固点
 小丁然1年前2
小丁然1年前2 -
 loveyuxi770614 共回答了21个问题
loveyuxi770614 共回答了21个问题 |采纳率76.2%C
北方冬天冷,和水泥容易冻,用凝固点低的食盐水和可以解决.1年前查看全部
- 盐酸的挥发性和硫酸的吸水性分别体现在哪些方面?
 kaoshibaomu21年前3
kaoshibaomu21年前3 -
 三萼 共回答了13个问题
三萼 共回答了13个问题 |采纳率92.3%1.浓盐酸有强挥发性,其中挥发出来的氯化氢会和空气中的水蒸气结合,形成盐酸的小液滴,扩散在空气中.所以盐酸要储存在密封容器当中,否则时间长以后盐酸的质量会逐渐下降,浓度也会下降.
2.浓硫酸吸水性
将一瓶浓硫酸敞口放置在空气中,其质量将增加,密度将减小,浓度降低,体积变大,这是因为浓硫酸具有吸水性.
(1)就硫酸而言,吸水性是浓硫酸的性质,而不是稀硫酸的性质.
(2)吸水性是浓硫酸的物理性质.浓硫酸只能干燥酸性和中性气体.1年前查看全部
- 属于化学性的是~导电性延展性酸碱性挥发性
 mycox1年前1
mycox1年前1 -
 sfaagaga 共回答了19个问题
sfaagaga 共回答了19个问题 |采纳率89.5%酸碱性1年前查看全部
大家在问
- 1愿得主人书遍读之是什么意思译文!
- 2概率论x~π(λ),求E[1/x+1],
- 3求EXCEL函数公式,满足以下条件自动等于分数。
- 4计算定积分∫(4,0)根号16-x^2 dx
- 5苏伊士运河的开通使船只不必绕经哪里
- 6【分块矩阵】 设A,C分别为m,n阶方阵,B为mxn矩阵,M={A B/O C},求证:|M|=|A||C|.
- 7在⊿ABC中三个角A,B,C的对边分别为a,b,c,若c=2,且cosA/cosB=b/a=√3,设圆O为⊿ABC的外接
- 8二项式(x+1/x)^n展开式中,前三项系数依次成等差数列,则展开式各项系数和是
- 9如图所示,质量为m、横截面为直角三角形的物块ABC,∠ABC=α,AB边靠在竖直墙面上,F是垂直于斜面BC的推力,现物块
- 10苏东坡的词句“但愿人长久,千里共婵娟”标准的翻译成英语是?
- 11a、b、c都是黑色固体物质,a+b加热后生成c+d,d加水e,e加热后d,d+a=f,f+b=c
- 12用英语猜动物It is the biggest animal on land .Tt has a very long n
- 13有一个高1.底面直径为0.8分米的圆柱瓶的体积是多少?
- 14Na3N是离子化合物,它能与水反应生成氨气.下列关于Na3N的说法中错误的是( )
- 15只在一种精密零件实际长度为2.5毫米画在图纸上为5厘米 这幅图纸的比例尺
