次氯酸钠中含有什么化学键我认识 所含的化学键有非极性共价键、记性共价键和离子键.但是我错了,.那它含有什么键/?.没有含
 萍水相逢19882022-10-04 11:39:546条回答
萍水相逢19882022-10-04 11:39:546条回答我认识 所含的化学键有非极性共价键、记性共价键和离子键.但是我错了,.那它含有什么键/?.没有含什么化学键呢、、 为什么呢?如何判断?

已提交,审核后显示!提交回复
共6条回复
 lovelace06 共回答了18个问题
lovelace06 共回答了18个问题 |采纳率100%- NaClO中含离子键和极性共价键.
Na+与ClO-有离子键;
Cl与O有极性共价键.
判断:1.金属与酸根之间形成的是离子键;
2.相同的非金属之间形成的是非极性共价键;
3.不同的非金属之间形成的是极性共价键.
特例,1.铵根NH4+看作金属,N和H极性共价键,NH4+与酸根之间形成的是离子键;
2.AlCl之间是共价键. - 1年前
 sherry2046 共回答了1个问题
sherry2046 共回答了1个问题 |采纳率- 次氯酸钠是活泼金属的阳离子与阴离子构成的,所以很容易看出这是离子化合物,含有离子键,氧和氯都是非金属,通常不同种非金属间以极性共价键结合,所以次氯酸根中氧和氯以极性共价键结合
- 1年前
 还风 共回答了13个问题
还风 共回答了13个问题 |采纳率84.6%- 次氯酸钠,化学式NaClO,有极性共价键和离子键
- 1年前
 123bca 共回答了13个问题
123bca 共回答了13个问题 |采纳率69.2%- 1,NaClO含极性共价键和离子键,2,稀有气体,如He,Ne,Ar等因为它们本身就具有稳定结构不需得到或失去电子,金属单质也不含离子键,气体单质一般含非极性共价键
- 1年前
 柳眼春相续 共回答了1个问题
柳眼春相续 共回答了1个问题 |采纳率- 有极性键和离子键
- 1年前
 林岫 共回答了11个问题
林岫 共回答了11个问题 |采纳率90.9%- NaClO
Na+[Cl:O]- 【将就地看吧=0=】
从电子式我们可以看到,Cl和O之间形成了一个共价键,这是极性的
【共价键:极性共价键,不同的非金属元素的原子间所形成的共价键;非极性共价键:相同的非金属元素的原子间所形成的共价键;配位键:一种原子(团)提供孤对电子,另一种原子(团)提供空轨道而形成的共价键】
并且它组成了一个原子团,带负电,与带正电的钠离子因离... - 1年前
相关推荐
- 次氯酸钠与稀盐酸混合方程式
 一苇渡河1年前1
一苇渡河1年前1 -
 wuswordcn 共回答了22个问题
wuswordcn 共回答了22个问题 |采纳率77.3%NaClO+HCl=NaCl+HClO1年前查看全部
- 请问,我想配制pH=11.3的次氯酸钠缓冲液,可以用次氯酸钠和盐酸配吗?不行的话,该用什么配制?
 richard_zh1年前1
richard_zh1年前1 -
 without17th 共回答了11个问题
without17th 共回答了11个问题 |采纳率90.9%一般来讲,缓冲溶液的pH值应当落在共轭酸碱对中酸形态pKa正负1之间,次氯酸的pKa为7.53,故其缓冲溶液pH应在6.53~8.53间,超过这个范围就失去了缓冲作用.pH=11.3的缓冲溶液可以用Na3PO4加盐酸获得1年前查看全部
- 请问,要对有机质含量较高的水进行消毒,最少要用多少次氯酸钠百分含量?ph值为6.3左右.
请问,要对有机质含量较高的水进行消毒,最少要用多少次氯酸钠百分含量?ph值为6.3左右.
要可靠的说法 jaden20051年前3
jaden20051年前3 -
 悲乐猪猪 共回答了19个问题
悲乐猪猪 共回答了19个问题 |采纳率94.7%啊.这个恐怕要有个国标才可能符合你的要求啊.暂且还不知道.这些值单单测起来就需要很多不一样的仪器进行测量.目前能提供你帮助的就是,用PH计,电导率1年前查看全部
- 亚硫酸中加入过量的次氯酸钠溶液反应的离子方程式是什么?
 天空如此美丽1年前2
天空如此美丽1年前2 -
 peachter 共回答了16个问题
peachter 共回答了16个问题 |采纳率93.8%少量亚硫酸钠滴入次氯酸钠中溶液仍呈碱性:ClO-+H2SO3+2OH-=SO42-+Cl-+2H2O
若两者恰好等物质的量时:ClO-+H2SO3=SO42-+Cl-+2H+
若次氯酸钠比亚硫酸钠稍多溶液呈酸性:ClO-+H2SO3=SO42-+Cl-+2HClO1年前查看全部
- 将氨气和次氯酸钠的反应设计成原电池则该原电池正极反应是
 raxxu1年前1
raxxu1年前1 -
 花影无踪 共回答了18个问题
花影无踪 共回答了18个问题 |采纳率88.9%原电池正极反应是还原反应,ClO-+2e+H2O=Cl-+2OH-1年前查看全部
- 氨气和次氯酸钠反应的方程式 求过程 写出推断产物过程和配平过程 谢谢
 hyfriends20061年前0
hyfriends20061年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 汞和次氯酸钠反应的方程式有一种产物是水
 盛开的雪花1年前1
盛开的雪花1年前1 -
 苍蝇小时候 共回答了20个问题
苍蝇小时候 共回答了20个问题 |采纳率85%汞和次氯酸能反应:2 Hg + 2 HClO = H2O + Hg2OCl2(碱式氯化汞)
和次氯酸钠反应可能是:
2Hg + 2 NaClO + 2HCl = Hg2OCl2 + H2O + 2 NaCl
(盐酸酸化,否则不能配平)1年前查看全部
- 次氯酸根离子具有漂白性么1.到底是次氯酸根离子具有漂白性 还是次氯酸具有2.那么 次氯酸钠为什么可以使品红退色发生氧化还
次氯酸根离子具有漂白性么
1.到底是次氯酸根离子具有漂白性 还是次氯酸具有
2.那么 次氯酸钠为什么可以使品红退色
发生氧化还原反应为什么就具有漂白性? 快被烦mm了1年前5
快被烦mm了1年前5 -
 ww军 共回答了12个问题
ww军 共回答了12个问题 |采纳率100%1.到底是次氯酸根离子具有漂白性 还是次氯酸具有
---- 次氯酸有漂白性.
----次氯酸根只有转化为次氯酸时,才有漂白性.如,固体漂白粉不能漂白,只有溶于水,才能转化生成次氯酸,才有漂白性.
----判断能否漂白的标准:看有没有次氯酸存在.
2.那么 次氯酸钠为什么可以使品红退色
----次氯酸钠是一个强碱弱酸盐,其溶于水时会发生水解反应
----NaCLO + H2O ==(可逆)==NaOH + HClO
----生成了次氯酸,故能漂白1年前查看全部
- 次氯酸钠能否用醋酸酸化在利用次氯酸钠氧化其他物质比如说碘化钾时,能否用醋酸酸化?如果可能的话,顺便解释一下为什么下题第一
次氯酸钠能否用醋酸酸化
在利用次氯酸钠氧化其他物质比如说碘化钾时,能否用醋酸酸化?
如果可能的话,顺便解释一下为什么下题第一问答案产物中是氯酸而不是其他氯系的酸.
26.(7分)将15.68L(标准状况)的氯气通入70℃500mL4.0 mo1.L-1氢氧化钠溶液中,充分反应后,吸取此溶液25mL稀释到250mL.再吸取此稀释液25mL,用醋酸酸化后,加入过量碘化钾溶液充分反应.用浓度为0.20 mo1.L-1的硫代硫酸钠溶液滴定析出的碘,消耗了硫代硫酸钠溶液5.0mL时恰好到终点.将滴定后的溶液用盐酸调至强酸性,此时析出的碘用上述硫代硫酸钠溶液再滴定到终点,需要硫代硫酸钠溶液30mL.已知:I2+2Na2S2O3==Na2S4O6+2NaI
(1)写出氯气通入氢氧化钠溶液后的总反应方程式.
(2)氢氧化钠溶液的体积在通入氯气前后的变化可忽略不计,计算通入氯气反应后溶液中各物质的物质的量浓度(稀释前).
26.(7分) (1)7C12+14NaOH==NaClO+2NaClO3+11NaCl+7H2O(3分);
(2)c(NaClO)=0.2mol•L-1;c(NaClO3)=0.4 mol•L-1;c(NaOH)=1.2 mol•L-1;c(NaCl)=2.2 mol•L-1(4分)
氯系的酸:比如亚氯酸,或者高氯酸 阴天细雨1年前2
阴天细雨1年前2 -
 dong8928 共回答了22个问题
dong8928 共回答了22个问题 |采纳率90.9%可以用醋酸酸化,但是这样的话测定的结果会有小量的误差
一般都推荐用2mol/L的硫酸酸化
至于你所说的产物问题
这是氧化电位差的问题1年前查看全部
- 写出下列的离子方程式:NaAlo2溶液加入过量Hcl 亚硫酸与次氯酸钠 Alcl3与过量氨气
 wuhanjianmin1年前1
wuhanjianmin1年前1 -
 小猪阿囡 共回答了19个问题
小猪阿囡 共回答了19个问题 |采纳率84.2%NaAlo2溶液加入过量Hcl
AlO2- + 4H+ = Al3+ +2H2O
亚硫酸与次氯酸钠
H2SO3 + ClO- = 2H+ + SO42- + Cl-
Alcl3与过量氨气
Al3+ + 3NH3 + 3H2O = Al(OH)3(沉淀)+3NH4+1年前查看全部
- 少量的二氧化碳通入次氯酸钠中到底生成碳酸钠还是碳酸氢钠?
少量的二氧化碳通入次氯酸钠中到底生成碳酸钠还是碳酸氢钠?
给我解释个清楚.还有,帮忙比较下碳酸根,碳酸氢根,次氯酸根结合质子能力的大小关系. nettie_jay1年前1
nettie_jay1年前1 -
 yulinmeihua 共回答了19个问题
yulinmeihua 共回答了19个问题 |采纳率94.7%一楼的别乱说.
生成碳酸氢钠.
结合质子能力
CO3 2->ClO->HCO3-
所以如果生成碳酸根,那么是2NaClO+CO2+H2O=Na2CO3+2HClO错错错.
这不显然是错的吗?碳酸根结合质子能力最强,又和次氯酸反应,就不会共存.
其实就一步NaClO+CO2+H2O=NaHCO3+HClO
CO2少量也是这样反应.1年前查看全部
- 怎样将次氯酸钠溶液里的氯气提炼出来?
 xiaoguang821年前2
xiaoguang821年前2 -
 secondiinone 共回答了15个问题
secondiinone 共回答了15个问题 |采纳率100%加盐酸1年前查看全部
- 次氯酸钙,次氯酸钠 与二氧化碳反应为什么现象不同
次氯酸钙,次氯酸钠 与二氧化碳反应为什么现象不同
为什么 次氯酸钠反应时只生成碳酸氢钠.次氯酸钙反应时会先生成碳酸钙 再生成碳酸氢钙 zhen11501年前3
zhen11501年前3 -
 相思的风 共回答了17个问题
相思的风 共回答了17个问题 |采纳率88.2%因为次氯酸酸性要稍强于HCO3-,所以正常情况下碳酸与次氯酸根反应只能得到HCO3-.但Ca(ClO)2由于有Ca2+离子的存在,形成碳酸钙沉淀会促进碳酸氢根电离反应更为彻底(化学平衡发生了移动),因此进一步反应变成碳酸钙.之后再是碳酸钙与碳酸反应变成碳酸氢钙.
次氯酸钠因为没有沉淀反应影响平衡,所以只能反应到碳酸氢根.1年前查看全部
- 二价镍与次氯酸钠在碱性溶液中反应生成黑色沉淀,是三价镍还是四价镍?
 491388331年前1
491388331年前1 -
 月桂兔 共回答了21个问题
月桂兔 共回答了21个问题 |采纳率90.5%能使二价镍离子氧化成三价镍,使镍离子完全沉淀.1年前查看全部
- 用氯消毒(次氯酸钠、氯气、二氧化氯)消毒生活饮用水,会有哪些消毒副产物?
用氯消毒(次氯酸钠、氯气、二氧化氯)消毒生活饮用水,会有哪些消毒副产物?
我的意思是消毒副产物,我知道的有氯代烃类的,非常多,最好将消毒副产物列出来名单。 凉月亮1年前3
凉月亮1年前3 -
 guizigu 共回答了10个问题
guizigu 共回答了10个问题 |采纳率90%首先会有少量氯气残留在里面,其次会有次氯酸根离子,甚至会有光气在里面.1年前查看全部
- 甲醇、次氯酸钠和硫酸反应的化学方程式
甲醇、次氯酸钠和硫酸反应的化学方程式
反应生成次氯酸二氧化碳、硫酸钠和水 并且注明电子转移数目
反应生成ClO2、CO2、硫酸钠、水 深只有霞1年前3
深只有霞1年前3 -
 dyykiss 共回答了16个问题
dyykiss 共回答了16个问题 |采纳率93.8%CH3OH + 6NaClO3 + 3H2SO4 == 3Na2SO4 + 6ClO2(气体) + CO2(气体) + 5H2O1年前查看全部
- 次氯酸钠与硫酸混合反应方程式
 supperice1年前3
supperice1年前3 -
 娃哈哈t715 共回答了19个问题
娃哈哈t715 共回答了19个问题 |采纳率94.7%2NaClO + H2SO4(少量)=2HClO + Na2SO4
NaClO + H2SO4(过量)=HClO + NaHSO41年前查看全部
- 一道化学浓度题500毫升中74.44克的次氯酸钠加多少水配成2%的浓度
 rain1131年前2
rain1131年前2 -
 漂亮oo结 共回答了24个问题
漂亮oo结 共回答了24个问题 |采纳率95.8%74.44/2% - 5001年前查看全部
- 次氯酸钠和二氧化氯一样吗
 白烟儿1年前2
白烟儿1年前2 -
 PoringBo 共回答了15个问题
PoringBo 共回答了15个问题 |采纳率100%不一样. 加氯机是氯气投加到水中,水解后主要以HCLO,CLO-杀菌.
二氧化氯发生器直接制备出二氧化氯溶液,CLO2杀菌21年前查看全部
- 电化学在日常生活中用途广泛,下图①是镁、次氯酸钠燃料电池的示意图,电池总反应式为:Mg+ClO-+H2O═Cl-+Mg(
电化学在日常生活中用途广泛,下图①是镁、次氯酸钠燃料电池的示意图,电池总反应式为:Mg+ClO-+H2O═Cl-+Mg(OH)2↓,图②是含Cr2O72-工业废水的电化学处理示意图.下列说法正确的是( )
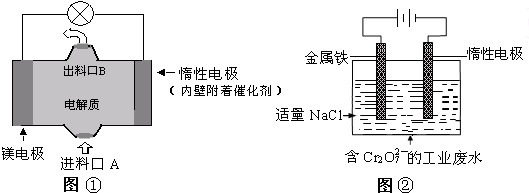
A.图②中Cr2O72-离子向惰性电极移动,与该极附近的OH-结合转化成Cr(OH)3除去
B.图②中阳极上的电极反应式为:Fe-3e-═Fe3+
C.图①中发生的还原反应是:Mg2++ClO-+H2O+2e-═Cl-+Mg (OH)2↓
D.若图①中3.6g镁溶解产生的电量用以图②废水处理,理论可产生10.7g氢氧化铁沉淀 江城子II1年前1
江城子II1年前1 -
 wuxiaozizi 共回答了19个问题
wuxiaozizi 共回答了19个问题 |采纳率94.7%解题思路:A.图②中惰性电极为阴极;
B.阳极铁被氧化生成Fe2+;
C.该原电池中,镁作负极,负极上镁失电子发生氧化反应,负极反应为Mg-2e-=Mg2+,电池反应式为Mg+ClO-+H2O=Mg(OH)2↓+Cl-,正极上次氯酸根离子得电子发生还原反应;
D.由电子守恒可知,Mg~2e-~Fe2+,由原子守恒可知Fe2+~Fe(OH)3↓,以此计算.A.图②中惰性电极为阴极,Fe电极为阳极,则Cr2O2-7离子向金属铁电极移动,与亚铁离子发生氧化还原反应生成的金属阳离子与惰性电极附近的OH-结合转化成Cr(OH)3除去,故A错误;
B.图②中阳极上的电极反应式为:Fe-2e-═Fe2+,故B错误;
C.该原电池中,镁作负极,负极上镁失电子发生氧化反应,负极反应为Mg-2e-=Mg2+,电池反应式为Mg+ClO-+H2O=Mg(OH)2↓+Cl-,正极上次氯酸根离子得电子发生还原反应,则总反应减去负极反应可得正极还原反应为Mg2++ClO-+H2O+2e-=Cl-+Mg(OH)2↓,故C正确;
D.由电子守恒可知,Mg~2e-~Fe2+,由原子守恒可知Fe2+~Fe(OH)3↓,则n(Mg)=[3.6g/24g/mol]=0.15mol,理论可产生氢氧化铁沉淀的质量为0.15mol×107g/mol=16.05g,故D错误;
故选C.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题综合考查电解原理,涉及电解、氧化还原反应、电子守恒的计算等问题,为高频考点,要求具有较好的分析和解决问题的能力,题目难度中等.1年前查看全部
- 求高锰酸钾、重铬酸钾、过氧化氢、氯化铁、次氯酸钠、浓硫酸、硝酸、氯酸钾的电极电势(只要结果).
求高锰酸钾、重铬酸钾、过氧化氢、氯化铁、次氯酸钠、浓硫酸、硝酸、氯酸钾的电极电势(只要结果).
还有高铁酸钠 skylq520201年前2
skylq520201年前2 -
 通宵加班 共回答了18个问题
通宵加班 共回答了18个问题 |采纳率100%酸性介质中
Mn2+-(0) -1.18V
Mn7+-Mn6+ 0.564V
Mn4+-Mn2+ 1.23V
Mn3+-Mn2+ 1.51V
Mn7+-Mn2+ 1.51V
Cr3+-(0) -0.74V
Cr3+-Cr2+ -0.41V
Cr6+-Cr3+ 1.33V
O-1-O-2 1.77V
Fe3+-Fe2+ 0.771V
Cl1+-(0) 1.63V
S6+-S4+ 0.17V
S4+-(0) 0.45V
N5+-N4+ 0.80V
Cl5+-Cl3+ 1.21V
Cl3+-Cl1+ 1.64V
高铁酸钠的没找到.1年前查看全部
- 25度时将少量二氧化碳通入足量次氯酸钠溶液中
25度时将少量二氧化碳通入足量次氯酸钠溶液中
算此反应平衡常熟,它计算时将二氧化碳浓度等于碳酸浓度,为什么? 绿裔儿1年前1
绿裔儿1年前1 -
 meojulice 共回答了29个问题
meojulice 共回答了29个问题 |采纳率93.1%因为少量二氧化碳基本就能完全溶于水形成碳酸了呀1年前查看全部
- 次氯酸钠与碳酸反应为什么次氯酸钠能与碳酸反应,它们反应没生成沉淀或气体或水啊?它们是什么反应啊?
 wrh20001年前2
wrh20001年前2 -
 viking8129 共回答了18个问题
viking8129 共回答了18个问题 |采纳率88.9%因为强酸可以制弱酸,反应的离子方程式如下:
2ClO- + CO2 + H2O = CO32- + 2HClO
没有沉淀生成,加热或光照时 HClO 可以分解,有氧气放出.
2HClO = 2HCl+O2 ↑ (条件是加热或光照)
分别属于复分解反应和分解反应
嗨嗨,这么全面的回答可要加分哦!1年前查看全部
- 自来水中用来消毒的主要化学物质是什么?二氧化氯、还是次氯酸钠?还是其他?
 amd75511年前1
amd75511年前1 -
 虾皮520 共回答了12个问题
虾皮520 共回答了12个问题 |采纳率100%消毒物质是漂白粉,但是漂白粉里面有效物质是次氯酸钠.它可以产生次氯酸根离子和少量的次氯酸.次氯酸起主要作用.1年前查看全部
- 漂白粉(次氯酸钙)在空气中变质,漂白液(次氯酸钠)为什么呢?
 leftist1年前4
leftist1年前4 -
 身长八尺周宽九丈 共回答了19个问题
身长八尺周宽九丈 共回答了19个问题 |采纳率94.7%次氯酸钙 在空气中易和二氧化碳和水反应生成碳酸钙和次氯酸,而次氯酸不稳定易分解,所以容易变质,次氯酸钠 比 次氯酸钙更稳定, 所以不会变质,其实原理都是 氯元素变价的问题.1年前查看全部
- 为什么次氯酸钠是漂白液而次氯酸钙是漂白粉?
为什么次氯酸钠是漂白液而次氯酸钙是漂白粉?
RT. 军中紫花1年前2
军中紫花1年前2 -
 三毛流浪儿 共回答了30个问题
三毛流浪儿 共回答了30个问题 |采纳率83.3%因为次氯酸钠在水中的溶解度很大,通常使用的也是不同浓度的水溶液,而次氯酸钙溶解度很小.我们通常使用的都是粉剂.
2者都能释放出次氯酸根,具有强氧化性,能漂白有色织物、油漆等,也能腐蚀金属和消毒.1年前查看全部
- 请问尿素与次氯酸钠反应在什么条件下会产生反应?产生反应时,尿素和次氯酸钠的浓度分别是多少,生成物是什么?
请问尿素与次氯酸钠反应在什么条件下会产生反应?产生反应时,尿素和次氯酸钠的浓度分别是多少,生成物是什么?
请回答详细些,做实验用.
谢谢! pinkladywang1年前2
pinkladywang1年前2 -
 莫愁WW_EN 共回答了13个问题
莫愁WW_EN 共回答了13个问题 |采纳率92.3%NaClO+NH2CONH2+2NaOH==N2H4.H2O+Na2CO3+NaCl
催化剂为高锰酸钾1年前查看全部
- 次氯酸盐是一些 ,和 的有效成分,如次氯酸钠是84消毒液的有效成分,次氯酸钙是漂白粉的有效成分,
次氯酸盐是一些 ,和 的有效成分,如次氯酸钠是84消毒液的有效成分,次氯酸钙是漂白粉的有效成分,
他们与 反应生成次氯酸,起到漂白的作用,有关反应方程式为 . wang13yu101年前3
wang13yu101年前3 -
 月伴弯 共回答了20个问题
月伴弯 共回答了20个问题 |采纳率90%消毒剂 漂白剂
CO2和水
Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO
2NaClO + H2O+CO2=2HClO + Na2CO31年前查看全部
- 次氯酸钠加热灼烧为什么得到的是氯化钠?
次氯酸钠加热灼烧为什么得到的是氯化钠?
1.NACLO-----HCLO+OH-然后次氯酸加热分解成的氧气和氯化氢不是蒸发了么?那不就应该是氢氧化钠么,为什么是氯化钠?2.为了除去氯化镁酸性溶液中的三价铁,为什么可以加碱性氧化物? f37300731年前3
f37300731年前3 -
 捉刀人 共回答了21个问题
捉刀人 共回答了21个问题 |采纳率81%楼上在胡说八道
NaClO加热时会发生歧化,温度高于75度时会迅速歧化完成,产物是NaCl和NaClO3
3NaClO=加热=2NaCl+NaClO3
至于沉淀Fe3+,因为Fe3+水解强于Mg2+,所以Fe3+基本沉淀完全时Mg2+还基本没有沉淀出来1年前查看全部
- 下列化学反应的离子方程式正确的是 A.次氯酸钠漂液中加浓盐酸产生氯气:ClO - + Cl - +2H + =Cl 2
下列化学反应的离子方程式正确的是
A.次氯酸钠漂液中加浓盐酸产生氯气:ClO - + Cl - +2H + =Cl 2 ↑+H 2 O B.少量SO 2 通入Ca(ClO) 2 溶液中:SO 2 +H 2 O+Ca 2+ +2ClO - =CaSO 3  +2HClO
+2HClOC.用稀HNO 3 溶解FeS固体:FeS+2H + =Fe 2+ +H 2 S 
D.氢氧化钙溶液与等物质的量的稀硫酸混合:Ca 2+ +OH - +H + +SO  =CaSO 4
=CaSO 4  +H 2 O
+H 2 O Oysten1年前1
Oysten1年前1 -
 zhangjin19850702 共回答了24个问题
zhangjin19850702 共回答了24个问题 |采纳率91.7%1年前查看全部
- 在实验室里可用如图所示装置来制取氯酸钠、次氯酸钠和探究氯水的性质. 图中:
在实验室里可用如图所示装置来制取氯酸钠、次氯酸钠和探究氯水的性质. 图中:
①为氯气发生装置;
②的试管里盛有15mL 30% NaOH溶液来制取氯酸钠,并置于热水浴中;
③的试管里盛有15mL 8% NaOH溶液来制取次氯酸钠,并置于冰水浴中;
④的试管里加有紫色石蕊试液;
⑤为尾气吸收装置.请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过______(填写仪器名称)向烧瓶中加入适量的浓盐酸.实验室制Cl2的化学方程式MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O△ .MnO2+4HCl(浓);
MnCl2+Cl2↑+2H2O△ .
实验时为了除去氯气中的HCl气体,可在①与②之间安装盛有______(填写下列编号字母)的净化装置.
A.碱石灰B.氢氧化钠溶液 C.饱和食盐水D.浓硫酸
(2)如果将过量二氧化锰与20mL 12mol•L-1的浓盐酸混合加热,充分反应后生成的氯气
______ 0.06mol.(填“大于”“小于”“等于”),若有17.4g的MnO2被还原,则被氧化的HCl质量为______.
(3)比较制取氯酸钠和次氯酸钠的条件,二者的差异是
①______;②______.
(4)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白.实验现象 原因 溶液最初从紫色逐渐变为红色 氯气与水反应生成的H+使石蕊变色 随后溶液逐渐变为无色 ______ 然后溶液从无色逐渐变为______色 ______  freebird281年前1
freebird281年前1 -
 呀呀呀哎 共回答了15个问题
呀呀呀哎 共回答了15个问题 |采纳率86.7%解题思路:(1)实验室制备氯气用浓盐酸和二氧化锰在加热条件反应,所用反应仪器为分液漏斗和圆底烧瓶,可用饱和食盐水除杂;
(2)氯化氢易挥发,二氧化锰只能与浓盐酸发生反应,与稀盐酸不反应;根据二氧化锰和作还原剂的HCl之间的关系式计算;
(3)在加热条件下,氯气与浓NaOH溶液反应生成氯酸钠,在常温以下,氯气与稀NaOH溶液反应生成次氯酸钠;
(4)氯气与水反应生成盐酸和次氯酸,反应生成的H+使石蕊变成红色,次氯酸具有强氧化性,将石蕊氧化为无色物质,所以反应现象为先变红,后褪色,反应后如继续通入氯气,氯气微溶于水,则为氯气的溶液,溶液呈黄绿色;(1)实验室制备氯气用浓盐酸和二氧化锰在加热条件反应,MnO2+4HCl(浓)
△
.
MnCl2+Cl2↑+2H2O,所用反应仪器为分液漏斗和圆底烧瓶,生成氯气混有HCl气体,根据氯气难溶于饱和氯化钠溶液,HCl易溶于水,可用饱和食盐水除杂,
故答案为:分液漏斗;MnO2+4HCl(浓)
△
.
MnCl2+Cl2↑+2H2O(2分);C;
(2)盐酸具有挥发性,加热促进氯化氢的挥发,随着反应的进行,盐酸的浓度逐渐减小,二氧化锰只能与浓盐酸发生反应,与稀盐酸不反应,所以反应生成氯气的物质的量小于0.06mol,17.4gMnO2的物质的量=[17.4g/87g/mol]=0.2mol,该反应中二氧化锰和被氧化的HCl的物质的量之比为1:2,有0.2mol二氧化锰参加反应,则有0.4molHCl被氧化,m(HCl)=nM=0.4mol×36.5g/mol=142g,
故答案为:小于;142g;
(3)根据题中信息可知,在加热条件下,氯气与浓NaOH溶液反应生成氯酸钠,在常温以下,氯气与稀NaOH溶液反应生成次氯酸钠,二者反应的浓度和温度都不相同.
故答案为:①所用NaOH浓度不同;②反应控制的温度不同;
(4)氯气与水反应生成盐酸和次氯酸,反应生成的H+使石蕊变成红色,次氯酸具有强氧化性,将石蕊氧化为无色物质,所以反应现象为先变红,后褪色,反应后如继续通入氯气,氯气微溶于水,则为氯气的溶液,溶液呈黄绿色,
故答案为:
HClO有强氧化性,体现漂白作用是其褪色.
溶液颜色变为浅绿色溶液中溶解了大量的氯气,体现浅绿色点评:
本题考点: 氯气的实验室制法;探究氯水、氯气的漂白作用.
考点点评: 本题考查了氯气的实验室制法,明确氯气的有关化学反应原理是解本题关键,题目难度中等.1年前查看全部
- 有效氯浓度为0.085%-0.12%次氯酸钠溶液的次氯酸钠浓度是多少?好像有效氯浓度得按cl2的量换算。怎么换算。
 我说爱你1年前1
我说爱你1年前1 -
 zhanzhonm 共回答了18个问题
zhanzhonm 共回答了18个问题 |采纳率77.8%次氯酸钠溶于水之后,有效的氯指的是次氯酸根,与其水解生成的氯离子和氯气没有关系的。因为存在水解的关系,不可能全部以次氯酸根的形式存在的,最多就是0.12%,这个就是极限,也就是次氯酸的浓度。1年前查看全部
- 被次氯酸钠漂白的衣服,是否能染回来
被次氯酸钠漂白的衣服,是否能染回来
衣服用84消毒液洗了,退色了,怎么恢复 带刀御猫1年前4
带刀御猫1年前4 -
 flightflight 共回答了17个问题
flightflight 共回答了17个问题 |采纳率88.2%不可以了,次氯酸钠的漂白是不可恢复的,特是把染料给氧化了,所以不能还原,估计唯一的补救方法就是你DIY一下吧,看看能不能把那个褪色的地方变成特点了.1年前查看全部
- 请问,0.25%次氯酸钠水溶液中能够加入适量高锰酸钾吗?两者稳定吗?
 yynb1年前2
yynb1年前2 -
 tianmo0313 共回答了19个问题
tianmo0313 共回答了19个问题 |采纳率94.7%两者都是强氧化剂,可以共存的吧,不太确定.仅作参考.1年前查看全部
- ①氯化钾②氯水③氯酸钾④盐酸⑤液氯⑥氯仿(CHCl3)⑦高氯酸(HClO4)⑧次氯酸钠(NaClO)
①氯化钾②氯水③氯酸钾④盐酸⑤液氯⑥氯仿(CHCl3)⑦高氯酸(HClO4)⑧次氯酸钠(NaClO)
其中含有氯元素的是________,含氯分子的是_________,含氯离子的是______________ 海飞丝1年前2
海飞丝1年前2 -
 budmiao 共回答了20个问题
budmiao 共回答了20个问题 |采纳率95%12345678
25
1241年前查看全部
- 求解几道高中化学反应方程式1.氯气与硫代硫酸钠溶液:2.酸性高锰酸钾溶液与草酸溶液:3.次氯酸钠与尿素反应,生成物除盐外
求解几道高中化学反应方程式
1.氯气与硫代硫酸钠溶液:
2.酸性高锰酸钾溶液与草酸溶液:
3.次氯酸钠与尿素反应,生成物除盐外,都是能参与大气循环的物质: 来生请你爱我1年前5
来生请你爱我1年前5 -
 alva1983 共回答了11个问题
alva1983 共回答了11个问题 |采纳率100%1、Na2S2O3+4Cl2+5H2O=2NaCl+2H2SO4+6HCl
2、2KMnO4+5K2C2O4+8H2SO4=6K2SO4+2MnSO4+10CO2↑+8H2O
3、3NaClO+NH2CONH2+2NaOH==N2↑+3H2O+Na2CO3+3NaCl1年前查看全部
- 次氯酸钙ca(clo2)2和次氯酸钠naclo2好像配不平的样子,
 我是乖乖也1年前3
我是乖乖也1年前3 -
 tt的 共回答了18个问题
tt的 共回答了18个问题 |采纳率83.3%次氯酸钙 Ca(ClO)2
次氯酸钠,化学式NaClO
你把化学式写错 ,怎么配平?1年前查看全部
- 在实验室中可用如图1所示装置制取氯酸钾、次氯酸钠和探究氯水的性质.
在实验室中可用如图1所示装置制取氯酸钾、次氯酸钠和探究氯水的性质.

图1中:①为氯气发生装置;②的试管里盛有15mL 30% KOH溶液,并置于热水浴中;③的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置.
请填写下列空白:
(1)制取氯气时,在烧瓶里加人一定量的二氧化锰,通过______(填写仪器名称)向烧瓶中加人适量的浓盐酸.实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有______(填写下列编号字母)的净化装置.
A.碱石灰B.饱和食盐水C.浓硫酸D.饱和碳酸氢钠溶液
(2)比较制取氯酸钾和次氯酸钠的条件,二者的差异是______.反应完毕经冷却后,②的试管中有大量晶体析出.图2中符合该晶体溶解度曲线的是______(填写编号字母);从②的试管中分离出该晶体的方法是
______(填写实验操作名称).
(3)本实验中制取次氯酸钠的离子方程式是:______.
(4)实验中可观察到④的试管里溶液的颜色发生了如下变化:紫色→______→______→黄绿色. 七朵半rr1年前1
七朵半rr1年前1 -
 flying_78 共回答了18个问题
flying_78 共回答了18个问题 |采纳率88.9%解题思路:(1)实验室制备氯气用浓盐酸和二氧化锰在加热条件反应,所用反应仪器为分液漏斗和圆底烧瓶,可用饱和食盐水除去氯气中的氯化氢气体;
(2)在加热条件下,氯气与浓KOH溶液反应生成氯酸钾,在常温以下,氯气与稀NaOH溶液反应生成次氯酸钠,溶质的溶解度随温度的降低而降低;
(3)氯气在常温下与NaOH反应生成次氯酸钠和氯化钠;
(4)氯气与水反应生成盐酸和次氯酸,反应生成的H+使石蕊变成红色,次氯酸具有强氧化性,将石蕊氧化为无色物质,所以反应现象为先变红,后褪色,反应后如继续通入氯气,氯气微溶于水,则为氯气的溶液,溶液呈黄绿色.( l )实验室制备氯气用浓盐酸和二氧化锰在加热条件反应,所用反应仪器为分液漏斗和圆底烧瓶,通过分液漏斗向烧瓶中加人适量的浓盐酸;用饱和食盐水除去氯气中的氯化氢气体,故在①与②之间安装盛有饱和食盐水的洗气瓶,
故答案为:分液漏斗;B;
( 2 )根据题中信息可知,在加热条件下,氯气与浓KOH溶液反应生成氯酸钾,在常温以下,氯气与稀NaOH溶液反应生成次氯酸钠,二者反应的浓度和温度都不相同,反应完毕经冷却后,②的试管中有大量晶体析出,说明溶质的溶解度随温度的降低而降低,只有M符合,不溶性固体与液体的分离常采用过滤的方法,
故答案为:碱溶液(或反应物)的浓度不同,反应温度不同; M;过滤;
( 3 )氯气在常温下与NaOH反应生成次氯酸钠和氯化钠,二者在水中溶解且电离,反应的离子方程式为Cl2+2OH-═ClO-+Cl-+H2O,
故答案为:Cl2+2OH-=ClO-+Cl-+H2O;
( 4 )氯气与水反应生成盐酸和次氯酸,反应生成的H+使石蕊变成红色,次氯酸具有强氧化性,将石蕊氧化为无色物质,所以反应现象为先变红,后褪色,反应后如继续通入氯气,氯气微溶于水,则为氯气的溶液,溶液呈黄绿色,
故答案为:红色;无色.点评:
本题考点: 氯、溴、碘及其化合物的综合应用.
考点点评: 本题考查氯气的制备、性质、实验方案的设计、评价,该类试题综合性强,有利于培养学生的逻辑推理能力和规范严谨的实验设计能力,注意该类试题常以常见仪器的选用、实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确及灵活运用知识解决实际问题的能力,该题难度中等.1年前查看全部
- 次氯酸钠 分析纯 的标签说明杂质含量 游离氯 不少于6% 碱(以NAOH)计 7-8% 最好把说明书发下那个化学纯的次氯
次氯酸钠 分析纯 的标签说明
杂质含量 游离氯 不少于6% 碱(以NAOH)计 7-8% 最好把说明书发下
那个化学纯的次氯酸钠浓度是多少 何小如1年前2
何小如1年前2 -
 肖无盐 共回答了11个问题
肖无盐 共回答了11个问题 |采纳率72.7%文名称:sodium hypochlorite
分子式:NaClO
分子量:74.44
性状:微黄色溶液,有似氯气的气味.熔点(℃):-6 ,沸点(℃):102.2 ,相对密度(水=1):1.10 .
用途:用于水的净化,以及作消毒剂、纸浆漂白等,医药工业中用制氯胺等.
储存:密闭阴凉干燥保存.
项目名称Item
分析纯AR
活性氯Active Chlorine
>=5.5%
游离碱(以NaOH计)Free alkali(as NaOH)
0.1%-1.0%
铁Iron(Fe)1年前查看全部
- 次氯酸钠和双氧水能发生反应吗次氯酸钠跟双氧水能发生反应吗?Naclo+H2O2—?
 日出彩虹1年前1
日出彩虹1年前1 -
 童话20068 共回答了16个问题
童话20068 共回答了16个问题 |采纳率81.3%NaClO+H2O2-----NaCl+H2O+O21年前查看全部
- 告诉我制氯气的方法.不能用浓盐酸,浓硫酸,浓硝酸,但不限浓磷酸,稀硫酸,稀盐酸,稀硝酸.次氯酸钠可以吗?
 海誓山盟庄1年前1
海誓山盟庄1年前1 -
 hilanhai 共回答了18个问题
hilanhai 共回答了18个问题 |采纳率94.4%有没有氯化钠?用电解食盐水的方法最简单啦1年前查看全部
- 有效氯60%的次氯酸钠,怎么配成有效氯含量100mg/L的次氯酸钠溶液
 happy_grass1年前1
happy_grass1年前1 -
 a02064378 共回答了15个问题
a02064378 共回答了15个问题 |采纳率86.7%有效氯是以氯的质量分数计算的
60%有效氯,相当于含有效氯0.6kg/L即600000mg/L,故需稀释6000倍1年前查看全部
- (2014•齐齐哈尔)84消毒液是一种消毒剂,主要成分为次氯酸钠(化学式是NaClO).它的消毒原理是:2NaClO+C
(2014•齐齐哈尔)84消毒液是一种消毒剂,主要成分为次氯酸钠(化学式是NaClO).它的消毒原理是:2NaClO+CO2+H2O═X+2HClO则X的化学式为( )
A.NaCl
B.NaOH
C.Na2CO3
D.Cl2 s366s3661年前1
s366s3661年前1 -
 伊荻鸶 共回答了25个问题
伊荻鸶 共回答了25个问题 |采纳率88%解题思路:化学反应前后,元素的种类不变,原子的种类、总个数不变.由2NaClO+CO2+H2O═X+2HClO可知,
反应前钠原子的相对个数是2个,反应后应该是2个,包含在X中;
反应前氯原子的相对个数是2个,反应后是2个;
反应前氧原子的相对个数是5个,反应后应该是5个,其中3个包含在X中;
反应前碳原子的相对个数是1个,反应后1个,包含在X中;
反应前氢原子的相对个数是2个,反应后是2个;
由分析可知,X是碳酸钠,化学式是Na2CO3.
故选C.点评:
本题考点: 质量守恒定律及其应用.
考点点评: 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、进行相关方面计算的基础.1年前查看全部
- 次氯酸钠水溶液呈什么性
 少年龍1年前4
少年龍1年前4 -
 蓝汕 共回答了23个问题
蓝汕 共回答了23个问题 |采纳率87%由于次氯酸是弱酸,而它的盐的水溶液呈碱性,ClO- + H2O = HCLO + OH-1年前查看全部
- 次氯酸钠溶液,氯化铝溶液,双氧水,哪个不具有杀菌消毒作用?
 奕奕铃1年前1
奕奕铃1年前1 -
 天齿铜涯 共回答了15个问题
天齿铜涯 共回答了15个问题 |采纳率86.7%氯化铝溶液1年前查看全部
- 少量CO2与苯酚钠或次氯酸钠反应都生成NaHCO3,但漂白粉溶液为什么又是生成CaCO3的?如果少量CO2与硅酸钠反应生
少量CO2与苯酚钠或次氯酸钠反应都生成NaHCO3,但漂白粉溶液为什么又是生成CaCO3的?如果少量CO2与硅酸钠反应生成的是碳酸钠还是碳酸氢钠?
 巫仙女1年前1
巫仙女1年前1 -
 zhaoming01 共回答了21个问题
zhaoming01 共回答了21个问题 |采纳率95.2%无论少量还是大量CO2与苯酚钠都是生成NaHCO3.因为; 因为酸性:H2CO3>C6H5OH>HCO3-
CO2与次氯酸钠:
少量CO2,CO2 + H2O + 2NaClO = 2HClO + Na2CO3
过量CO2,CO2 + H2O + NaClO = HClO + NaHCO3
CO2与漂白粉溶液
少量CO2,CO2 + H2O + Ca(ClO)2 = 2HClO + CaCO3
过量CO2,2CO2 + 2H2O + 2Ca(ClO)2 = 2HClO + Ca(HCO3)2
少量CO2与硅酸钠
CO2 + H2O+ Na2SiO3 ===Na2CO3 + H2SiO3
过量CO2与硅酸钠
2CO2 + 2H2O+ Na2SiO3 ===2NaHCO3 + H2SiO31年前查看全部
- 二氧化硫与次氯酸钠反应铁二价与次氯酸根离子反应
 寒沙空独1年前1
寒沙空独1年前1 -
 feiyang19731 共回答了27个问题
feiyang19731 共回答了27个问题 |采纳率88.9%NaClO+SO2 H2O=H2SO4 NaCl 酸性条件下2Fe2+ + HClO + H+= 2Fe3+ + H2O + Cl-碱性条件下2Fe(OH)2 + ClO- + H2O = 2F e(OH)3 + Cl-1年前查看全部
- 治牙用双氧水,生理盐水,和次氯酸钠,都有哪些用途
 会唱歌的草1年前2
会唱歌的草1年前2 -
 robbert922 共回答了14个问题
robbert922 共回答了14个问题 |采纳率92.9%双氧水 次氯酸钠 杀菌消毒
生理盐水 正常冲洗 其实用不着 用蒸馏水就行1年前查看全部
- “漂白粉溶液可使淀粉碘化钾试纸变蓝”“次氯酸钠可以与亚硫酸钠共存”这2句话对不对?
 xahjp6661年前1
xahjp6661年前1 -
 麻团儿炖蘑菇 共回答了17个问题
麻团儿炖蘑菇 共回答了17个问题 |采纳率94.1%在中学阶段,第一句是对的.漂白粉中有Ca(ClO)2,会与KI发生反应:ClO- + 2I- + H2O = Cl- + I2 + 2OH-,产生I2,使淀粉变蓝.
第二句……如果是固体,那么是正确的;如果是溶液,就是错的,因为会反应:ClO- + SO32- = Cl- + SO42-1年前查看全部
大家在问
- 130--50字小作文求大神帮助请用“生命像……”开头,写几句话(30——50字)表达你对生命的理解
- 2设计方案可行,且化学方程式书写正确的是( ) A.实验室用稀硫酸与铜片反应制取氢气:Cu+H 2 SO 4 =CuSO
- 3some where i belong中文
- 4离子所带电荷由什么决定?RT.(以下见于离子晶体——百度百科)离子晶体熔沸点高低比较离子所带电荷越高,离子半径越小,则离
- 5the singing-master used to be a popular singer
- 6getting ready=?
- 7怎样求二次函数大题中平行四边形的存在性?.已知三点求另一点符合题意的坐标.求思路 火速~
- 8=cos24cos36-sin24sin36① =cos(24+36)②
- 9在三角形ABC中,已知a+b=12,角A=60度,角B=45度,则a=?b=?
- 10作文《---里的新鲜事》怎么写
- 11在直角坐标系中,O是坐标原点,点P(m,n)在反比例函数y=k/x的图像上,若m+n=√2,OP=2,且此反比例函数y=
- 12She can drive a car 的意思
- 13(2011•张家界)将下列各项与相应的成分用线连起来.
- 14已知椭圆中心再原点,焦点在x轴上,焦距为6,长轴等于短轴的2倍,求这椭圆的方程
- 15若|x-y+2|与4次√x+2y-1互为相反数,求x+y的平方根