足球烯是仅由一个分子所命名的单质,还是由单一的分子组成的物质?(看不懂可提问)
 yy珊2022-10-04 11:39:546条回答
yy珊2022-10-04 11:39:546条回答现在的回答者没有看清楚问题..= =||汗颜
看懂了再说嘛,拜下
那么..足球烯到底是由分子还是原子构成的............

已提交,审核后显示!提交回复
共6条回复
 幸福袜子 共回答了19个问题
幸福袜子 共回答了19个问题 |采纳率89.5%- 足球烯不是指单一的某种物质,它指的是一类物质,该类物质都由碳元素组成,有类似足球的空间构型,不一定都是C60
- 1年前
 爱说说 共回答了23个问题
爱说说 共回答了23个问题 |采纳率- 足球烯C60 碳单质 ,属于分子晶体
- 1年前
 蜀山vs逍遥 共回答了19个问题
蜀山vs逍遥 共回答了19个问题 |采纳率- 足球烯其实只含C元素,只是其结构是以C=C相连成一个类似与足球,所以 才叫足球烯。所以其是由单一的元素组成的分子。
- 1年前
 飘渺中地云或雾 共回答了5个问题
飘渺中地云或雾 共回答了5个问题 |采纳率- 一个分子!是C60!
- 1年前
 Hbeb 共回答了56个问题
Hbeb 共回答了56个问题 |采纳率- 足球烯C60 碳单质
- 1年前
 25ovh4sa2s6s1c4 共回答了31个问题
25ovh4sa2s6s1c4 共回答了31个问题 |采纳率- 都是
符合单质的定义
也是由C60组成的物质 - 1年前
相关推荐
- 足球烯分子结构中存在正六边形个数
足球烯分子结构中存在正六边形个数
足球烯是由60个碳原子构成的一种新型分子,在它的分子结构中,存在正五边形和正六边形两种形状,那么它的分子结构中存在正六边形
A、12个 B、18个 C、20个 D、24个 aeonia1年前1
aeonia1年前1 -
 52c10 共回答了13个问题
52c10 共回答了13个问题 |采纳率84.6%设有x个五边形,y个六边形.足球稀定点数为V,边数为E,面数为F.
先由欧拉定理:V + F - E = 2
再由两面共享一边:5*x + 6*y = 2*E
再由两点共享一边:3*V = 2*E
以及 :x + y = F ,V = 60
解方程组的 x = 12,y = 20 ,V = 60,E = 90,F = 32
选 C1年前查看全部
- 下面列出了几组物质,①金刚石与“足球烯”C60; ②D2 O与H2
下面列出了几组物质,
①金刚石与“足球烯”C60;②D2 O与H2 O;③16O、18O;
④氧气(O2)与臭氧(O3);⑤乙醇(CH3CH2OH)和甲醚(CH3OCH3);
⑥CH4和CH3CH2CH3; ⑦CH3CH3和 ;⑧CH3CH2CH2CH3与CH3CH(CH3)2
;⑧CH3CH2CH2CH3与CH3CH(CH3)2
其中互为同位素的是______;互为同系物的是______;互为同素异形体的是______;互为同分异构体的是______. 小岛珊瑚1年前1
小岛珊瑚1年前1 -
 snail04831 共回答了18个问题
snail04831 共回答了18个问题 |采纳率94.4%解题思路:有相同质子数,不同中子数的原子或同一元素的不同核素互为同位素;
具有相同分子式而结构不同的化合物互为同分异构体;
结构相似、分子组成相差若干个“CH2”原子团的有机化合物互相称为同系物;
相同元素组成,不同形态的单质互为同素异形体.①金刚石与“足球烯”C60都是由碳元素形成的不同单质,互为同素异形体,
②D2O与H2O都是氢的同位素与氧元素形成的化合物,
③16O与18O质子数相同,中子数不同,互为同位素,
④氧气(O2)与臭氧(O3)都是由氧元素形成的不同单质,互为同素异形体,
⑤乙醇(CH3CH2OH)和甲醚(CH3OCH3)分子式相同,但结构不同,互为同分异构体,
⑥CH4和CH3CH2CH3结构相似,分子组成相差2个“CH2”原子团,互为同系物,
⑦CH3CH3和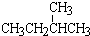 结构相似,分子组成相差3个“CH2”原子团,故互为同系物,
结构相似,分子组成相差3个“CH2”原子团,故互为同系物,
⑧CH3CH2CH2CH3与CH3CH(CH3)2分子式相同,但结构不同,互为同分异构体,
故互为同位素的是:③;互为同系物的是:⑥⑦;互为同素异形体的是:①④;互为同分异构体的是:⑤⑧,
故答案为:③;⑥⑦;①④;⑤⑧.点评:
本题考点: 芳香烃、烃基和同系物;同位素及其应用;同分异构现象和同分异构体.
考点点评: 本题考查同位素、同素异形体、同分异构体、同系物的概念,难度不大.对于元素、核素、同位素、同素异形体、同分异构体、同系物、同种物质等概念的区别是考试的热点问题.1年前查看全部
- 求足球烯C60的不饱和度!按不饱和度=(2n+2-m)/2算,该是61,但是由于它是立体图形,不饱和度比面数少1,...
求足球烯C60的不饱和度!按不饱和度=(2n+2-m)/2算,该是61,但是由于它是立体图形,不饱和度比面数少1,...
求足球烯C60的不饱和度!按不饱和度=(2n+2-m)/2算,该是61,但是由于它是立体图形,不饱和度比面数少1,就该是31, 肥肉比瘦肉好吃1年前1
肥肉比瘦肉好吃1年前1 -
 冰封的诺言 共回答了22个问题
冰封的诺言 共回答了22个问题 |采纳率90.9%不饱和度Ω=(C原子数×2+2-氢原子数)÷2,代入公式得到不饱和度=61;
立体封闭有机物分子(多面体或笼状结构)不饱和度的计算,其成环的不饱和度比面数少数1.C60是立体有机分子,其成环的不饱和度即为311年前查看全部
- 碳原子的同位素金刚石和石墨是原子,足球烯是分子.能不能给我分析一下?谢谢!
 httpll1年前4
httpll1年前4 -
 wangpengyi66 共回答了23个问题
wangpengyi66 共回答了23个问题 |采纳率95.7%金刚石和石墨是采用共价键连接的原子晶体,足球烯是56个碳原子组成的一个大分子!为什么由同一种碳原子组成的物质,外貌、性质却大不相同呢?科学家研究后,发现原来是由于原子的排列形式不一样引起的.金刚石是结晶碳,每一个碳原子周围有4个碳原子,距离都是相等的,原子之间组成一个强有力的整体.而石墨内部的一个碳原子同相邻的碳原子间的距离是不相等的.离得较远的两原子之间的“拉力”较弱,容易断裂“分手”,这样,金刚石和石墨就出现了硬和软的不同“个性”.1年前查看全部
- 硅可以形成C60的结构吗就是硅可以形成足球烯这样的分子吗 为什么呢
 夜晚的晨曦1年前3
夜晚的晨曦1年前3 -
 Tattu 共回答了16个问题
Tattu 共回答了16个问题 |采纳率87.5%不能,硅的半径比碳大很多,无法像C那样相互之间形成稳定的共价键.
这也是为什么自然界的有机物由C组成,形成碳链,而硅不能形成长链硅化物的原因1年前查看全部
- 足球烯用途
 miyakokazuya1年前1
miyakokazuya1年前1 -
 飞在我身边 共回答了24个问题
飞在我身边 共回答了24个问题 |采纳率79.2%1985年,Rice大学的H.W.Kroto和R.E.Smalley等发现用激光束使石墨蒸发,用10大气压的氦气产生超声波,在喷咀上能生成性质十分稳定的一种新的碳的同素异形体.经过飞行时间质谱证实,它的确不含其它元素,其组成主要是C60.Kroto等为了纪念前驱研究者Buckminster Fuller,将这个球形分子称为Buckminsterfullerene或者简称为“布克球”(Buckyball).
他们认为这种碳单质既然具有确定的组成,显然就不会像石墨或金刚石一样构成无限庞大的分子.按照碳原子价键的要求,它可能具有球形结构.它以60个碳原子作为顶点,组成一个32面体.其中12个面是正边形,20个面是六边形.正好是一个削20面体的每个顶点,像足球一样的多边形体,如图1所示.在这样的分子中,每个碳原子都满足sp2杂化轨道的要求:与其它三个碳原子相连,等价地组成一个五员环和两个六员环.由于它具有这种特殊结构,因此现在更形象地称它为足球烯(footballene,soccerballene).
按照正常的碳—碳键的键长计算,C60构成的球体直径大约为7 A0 ,它的内腔至少可以容纳一个直径为5 A0 的客体原子.根据这种思想,Smalley又设计将石墨板浸泡在沸腾的三氯化镧饱和溶液中,干燥后将它作为靶子,用激光蒸发,使镧原子嵌入球体内部.从而发现了一系列分别由44个到76个碳原子和一个镧原子组成的碳—镧化合物.显然这是一种包合物[2].
事实上,12个正五边形不仅只能和20个六边形构成C60的封闭壳,还可以和其它若干个六边形组成蛋形的多面体,而镧原子的存在,使其它形式的多面体也趋于稳定.
和C60分子有关的“碗烯”(corranulene)分子[3],C20H10,具有一个由五个正六边形环绕的正五边形结构,如图2所示.这个化合物早已于1966年由Michigan大学的R.G.Lawton合成成功.它的分子构型像一个碗,有芳香性,而且很稳定.而足球烯分子的表面,就存在着这样的12个正五角形单元.C60分子具有Ih点群的对称性,是一个“非交替烃”(non-alternant hydrocarbon).
曾经有好几位学者对C60作过HMO计算[4],并将C60和其它芳香烃的离域能(delocalization energy)和共振能进行比较.结果表明其共振稳定性大约是苯分子中每个碳原子的平均共振能的两倍.虽然在这个分子中碳原子并不都是完全共平面的,因此会出现一些张力,但是它的共振结构数高达12500,因而可以使体系稳定化.如果考虑到C60多面体分子中π键与σ键的交角大约是11.60,用0.877校正其共振积分,按POAV1/3D HMO法计算,仍然可以明显地看出它具有较高的π电子能.
回答者:lzy7777 - 见习魔法师 三级 6-28 20:38
足球烯(footballene)是单纯由C元素结合形成的稳定分子,它具有60个顶点和32个面,其中12个面为正五边形,20个面为正六边形,整个分子形似足球,因此得名.其结构图如下所示:
足球烯的分子式为C60,60个碳原子占据60个顶点,处于顶点的碳原子与相邻顶点的碳原子各用sp2杂化轨道重叠形成σ键,每个碳原子的三个σ键分别为一个五边形的边和两个六边形的边.碳原子的三个σ键不是共平面的,键角约为108°或120°,因此整个分子为球状.每个碳原子用剩下的一个p轨道互相重叠形成一个含60个π电子的闭壳层电子结构,因此在近似球形的笼内和笼外都围绕着π电子云.分子轨道计算表明:足球烯具有较大的离域能.足球烯的共振结构数高达12500个,按每个碳原子的平均共振能比较,共振稳定性约为苯的两倍.因此足球烯是一个具有芳香性的稳定体系.
足球烯是美国德克萨斯州休斯敦赖斯(Rice)大学的克罗脱(Kroto,H.W.)和史沫莱(Smalley,R. E.)等人于1985年提出的.他们用大功率的激光束轰击石墨使其汽化,用1MPa压力的氦气产生超声波,使被激光束汽化的碳原子通过一个小喷嘴进入真空膨胀,并迅速冷却形成新的碳原子,从而得到了C60.C60已为质谱所证明.足球烯的发现为有机化学开辟了一个新的领域,其意义是十分重大的.
“足球烯”本身更有着无数优异的性质,它本身是半导体,掺杂后可变成临界温度很高的超导体,由它所衍生出来的碳微管比相同直径的金属强度高100万倍.1年前查看全部
- 9.足球烯(C60)是科学家于1985年发现的一种物质.这种物质属于( ) A.化合物, B. 混合物C.单质 D 无法
 曹芳独用1年前1
曹芳独用1年前1 -
 asdfngasdfj 共回答了15个问题
asdfngasdfj 共回答了15个问题 |采纳率93.3%先看一下这个
然后就知道了选c1年前查看全部
- (1)1985年科学家发现了C60分子,它是由60个碳原子构成的形状象足球的大分子,又叫足球烯.1991年科学家又发现了
(1)1985年科学家发现了C60分子,它是由60个碳原子构成的形状象足球的大分子,又叫足球烯.1991年科学家又发现了由碳原子构成的管状大分子--碳纳米管.足球烯、碳钠米管和金刚石、石墨都是由碳元素组成的单质,但它们的物理性质有较大的差异,其原因是______.
(2)现在,北京大街上行驶的“清洁燃料车”是以CNG或LPG为燃料的.“CNG”是压缩天然气的缩写,成分以甲烷为主;“LPG”是液化石油气的缩写,主要成分是丙烷、丙烯、丁烷、丁烯等化合物,其中丙烷(用A表示)燃烧的化学方程式如下A+5O2
3CO2+4H2O根据质量守恒定律可以确定丙烷的化学式为______.点燃 .. 力佳刘1年前1
力佳刘1年前1 -
 llsky21 共回答了23个问题
llsky21 共回答了23个问题 |采纳率100%解题思路:(1)同素异形体物理性质的差异要从结构上分析,即原子排列方式的不同造成了其物理性质的差异;(2)根据化学变化前后原子的种类、数目不变,由反应的化学方程式:A+5O2
3CO2+4H2O推断反应中丙烷的分子构成,根据分子的构成确定丙烷的化学式.点燃 ..(1)金刚石、石墨、足球烯、碳纳米管等由碳元素组成的单质中碳原子的排列方式不同,从而使得它们的物理性质不同;
(2)由化学方程式:A+5O2
点燃
.
.3CO2+4H2O可判断反应前后C、H、O三种原子的个数为
反应前 反应后
C原子 0 3
O原子 10 10
H原子 0 8
根据化学变化前后原子的种类、数目不变,可判断丙烷分子由3个C原子、8个H原子构成,则丙烷的化学式为C3H8
故答案为:(1)碳原子的排列方式不同;(2)C3H8.点评:
本题考点: 碳元素组成的单质;质量守恒定律及其应用.
考点点评: 根据化学变化前后原子的种类、数目不变,由反应的化学方程式,可以推断反应中某物质的分子构成及物质化学式的确定.1年前查看全部
- 什么是足球烯
 难道301年前1
难道301年前1 -
 t0nyt1vk 共回答了25个问题
t0nyt1vk 共回答了25个问题 |采纳率88%1985年,Rice大学的H.W.Kroto和R.E.Smalley等发现用激光束使石墨蒸发,用10大气压的氦气产生超声波,在喷咀上能生成性质十分稳定的一种新的碳的同素异形体.经过飞行时间质谱证实,它的确不含其它元素,其组成主要是C60.Kroto等为了纪念前驱研究者Buckminster Fuller,将这个球形分子称为Buckminsterfullerene或者简称为“布克球”(Buckyball).
他们认为这种碳单质既然具有确定的组成,显然就不会像石墨或金刚石一样构成无限庞大的分子.按照碳原子价键的要求,它可能具有球形结构.它以60个碳原子作为顶点,组成一个32面体.其中12个面是正边形,20个面是六边形.正好是一个削20面体的每个顶点,像足球一样的多边形体,如图1所示.在这样的分子中,每个碳原子都满足sp2杂化轨道的要求:与其它三个碳原子相连,等价地组成一个五员环和两个六员环.由于它具有这种特殊结构,因此现在更形象地称它为足球烯(footballene,soccerballene).
按照正常的碳—碳键的键长计算,C60构成的球体直径大约为7 A0 ,它的内腔至少可以容纳一个直径为5 A0 的客体原子.根据这种思想,Smalley又设计将石墨板浸泡在沸腾的三氯化镧饱和溶液中,干燥后将它作为靶子,用激光蒸发,使镧原子嵌入球体内部.从而发现了一系列分别由44个到76个碳原子和一个镧原子组成的碳—镧化合物.显然这是一种包合物[2].
事实上,12个正五边形不仅只能和20个六边形构成C60的封闭壳,还可以和其它若干个六边形组成蛋形的多面体,而镧原子的存在,使其它形式的多面体也趋于稳定.
和C60分子有关的“碗烯”(corranulene)分子[3],C20H10,具有一个由五个正六边形环绕的正五边形结构,如图2所示.这个化合物早已于1966年由Michigan大学的R.G.Lawton合成成功.它的分子构型像一个碗,有芳香性,而且很稳定.而足球烯分子的表面,就存在着这样的12个正五角形单元.C60分子具有Ih点群的对称性,是一个“非交替烃”(non-alternant hydrocarbon).
曾经有好几位学者对C60作过HMO计算[4],并将C60和其它芳香烃的离域能(delocalization energy)和共振能进行比较.结果表明其共振稳定性大约是苯分子中每个碳原子的平均共振能的两倍.虽然在这个分子中碳原子并不都是完全共平面的,因此会出现一些张力,但是它的共振结构数高达12500,因而可以使体系稳定化.如果考虑到C60多面体分子中π键与σ键的交角大约是11.60,用0.877校正其共振积分,按POAV1/3D HMO法计算,仍然可以明显地看出它具有较高的π电子能.1年前查看全部
- 金刚石、石墨、足球烯、碳纳米管的物理性质有什么差别
 gz87761年前1
gz87761年前1 -
 铁路小工 共回答了16个问题
铁路小工 共回答了16个问题 |采纳率87.5%因为物质本质的不同 就是元素固定结构不同 元素都是一样的 都是C 他们是碳元素构成的同素异形体
金刚石:一个碳分子中含有60个碳原子 是金字塔状稳定
石墨:石墨也分好多种 但是基本形状是片层 值得一提的是石墨的特征是由于石墨碳原子的最外电子层还有共价键的存在
足球烯:这种物质因为碳原子构成稳定的形态类似于足球而得名 其形状我不用多说你也应该明白了吧 因为其有32面 构成环状的形态形成的键位统一 所以它是分子晶体
碳纳米管:碳纳米管易拉伸的特征决定于它的化学结构 C60卷曲而形成的结构 管厚度和直径都精细到了纳米的程度..1年前查看全部
- 金刚石,石墨和足球烯都是由( )什么组成
金刚石,石墨和足球烯都是由( )什么组成
它们的化学性质( ).但是由于( )不一样,它们的物理性质不同 假装懂你1年前4
假装懂你1年前4 -
 wangqihao1 共回答了26个问题
wangqihao1 共回答了26个问题 |采纳率84.6%金刚石,石墨和足球烯都是由(碳元素)组成
它们的化学性质(相同).但是由于(原子排列)不一样,它们的物理性质不同1年前查看全部
- 12 14 C6 C 6 C 60的联系质量数为12的碳质量数为14的碳60个碳原子组成的足球烯碳这些的关系
 edo02111年前1
edo02111年前1 -
 ktp1870628 共回答了23个问题
ktp1870628 共回答了23个问题 |采纳率95.7%12C、14C都是碳元素的原子,属于同位素关系,质子数相同,但是中子数不同,放射性不同.
C60足球烯,属于单质,它和金刚石、石墨等为同素异形体的关系,与12C、14C没有概念关系.
凡是讨论同种元素的不同单质,都是同素异形体
凡是讨论同种元素的不同原子,都是同位素1年前查看全部
- 原子的排列是会使化学性质发生改变吗?但是原子是保持物质在化学变化中的一种微粒(如石墨和足球烯等
原子的排列是会使化学性质发生改变吗?但是原子是保持物质在化学变化中的一种微粒(如石墨和足球烯等
原子构成)两者应该化学性质相同,但按照一的说法又不相同,该怎样理解?
为什么 kaihk1年前3
kaihk1年前3 -
 女博士cc 共回答了18个问题
女博士cc 共回答了18个问题 |采纳率88.9%注意:保持物质化学性质的最小微粒是 分子 !
原子排列的变化一般来说就意味着分子结构的变化——比如1,2-二氯乙烯的顺反异构.
另外要注意石墨和足球烯的化学性质不能说相同——它们有一些相似的地方,比如说与O2反应——就这个性质上,两者之间也不完全一样,比如燃点等肯定不同.1年前查看全部
- (2013•松江区三模)以下结构示意图表示足球烯(C60)结构模型的是( )
(2013•松江区三模)以下结构示意图表示足球烯(C60)结构模型的是( )
A.
B.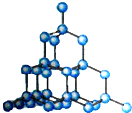
C.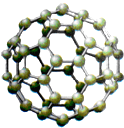
D.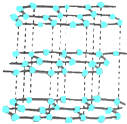
 wylwxy1年前1
wylwxy1年前1 -
 snowwhite123 共回答了12个问题
snowwhite123 共回答了12个问题 |采纳率75%解题思路:根据各种碳单质的结构图中原子的排列方式进行分析,C60分子是一种足球状结构.A、由图示可知,A的结构是一种管状结构.符合碳纳米管的结构.故A不符合题意;
B、B的结构是一种立体的正四面结构,属于金刚石的结构.故B不符合题意;
C、C60分子是由60个原子构成的分子,C60分子形似足球.故C符合题意;
D、D的结构是一种正六边形平面结构,属于石墨的结构.故D不符合题意.
故选C.点评:
本题考点: 碳元素组成的单质.
考点点评: 解答本题要掌握图中分子结构的特点,只有这样才能对相关方面的问题做出足球的判断.1年前查看全部
- 金刚石、石墨、足球烯、碳纳米管物理性质有较大差异的原因是什么?
 六维空间1年前3
六维空间1年前3 -
 hhp1980 共回答了18个问题
hhp1980 共回答了18个问题 |采纳率83.3%因为物质本质的不同 就是元素固定结构不同 元素都是一样的 都是C 他们是碳元素构成的同素异形体
金刚石:一个碳分子中含有60个碳原子 是金字塔状稳定
石墨:石墨也分好多种 但是基本形状是片层 值得一提的是石墨的特征是由于石墨碳原子的最外电子层还有共价键的存在
足球烯:这种物质因为碳原子构成稳定的形态类似于足球而得名 其形状我不用多说你也应该明白了吧 因为其有32面 构成环状的形态形成的键位统一 所以它是分子晶体
碳纳米管:碳纳米管易拉伸的特征决定于它的化学结构 C60卷曲而形成的结构 管厚度和直径都精细到了纳米的程度..1年前查看全部
- 足球烯的分子质量是多少?它一个分子中有多少个碳原子?它的相对分子质量是多少?
 sd88661年前2
sd88661年前2 -
 伤水流风 共回答了23个问题
伤水流风 共回答了23个问题 |采纳率87%足球烯就是C60,一个分子中有60个碳原子,相对分子质量7201年前查看全部
- 质量相等的石墨和C60(足球烯)谁含的质子数多
质量相等的石墨和C60(足球烯)谁含的质子数多
我认为是一样多,因为都是C原子构成的,为什么参考书上说C60多一些呢? cqy88cn1年前0
cqy88cn1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 金刚石、石墨、足球烯都是由碳原子构成的,但它们的物理性质却差别很大,这是由于什么
 wwwdd02041年前1
wwwdd02041年前1 -
 lphust 共回答了20个问题
lphust 共回答了20个问题 |采纳率95%这里涉及到一个概念:同素异形体
同一种元素形成的多种单质互为同素异形体.例如金刚石和石墨是碳的同素异形体.许多元素都能形成同素异形体,形成方式有:(1)分子里原子个数不同,如氧气和臭氧;(2)晶体里原子的排列方式不同,如金刚石和石墨;(3)晶体里分子的排列方式不同,如斜方硫和单斜硫.同素异形体之间物理性质不同,化学性质略有差异.例如氧气是没有颜色、没有气味的气体,而臭氧是淡蓝色、有鱼腥味的气体;氧气的沸点-183℃,而臭氧的沸点-111.5℃;氧气比臭氧稳定,没有臭氧的氧化性强等.
而你所说的正属于第二种:原子的排列方式不同
更为具体的,我们说金刚石是由碳原子以共价键连接形成的正“四面体空间网状结构”的“原子晶体”,石墨是一种“层状结构”的“过渡型晶体”:层内碳原子以共价键结合形成正六边形网状结构,层与层之间距离较大,相当于分子间力的作用;金刚石是硬度最大的物质、不能导电,而石墨的硬度较小、层之间可以相对滑动、导电性好,化学性质较金刚石活泼.足球烯是一个较为前沿的物质,它是由若干个碳原子相互结合成为类似足球状的分子,所以它属于分子晶体.而一般来说分子晶体较原子晶体和过渡性晶体的熔沸点更低.
然而他们都是由碳元素组成,所以化学性质相差不大.
另外类似于此的,还有白磷和红磷.白磷是由正四面体结构的分子(P4)组成,为白色腊状固体,有剧毒,易溶于CS2,着火点低(40℃),在空气中可自燃;红磷是较复杂的层状晶体,红色粉末无毒,不溶于CS2,着火点240℃,隔绝空气加热,温度升至260℃时白磷转变成红磷,红磷受热,在416℃时,先升华蒸气,冷却又变为白磷.1年前查看全部
- 继1985年科学家发现C60分子后,1991年科学家又发现了一种管状的碳单质——碳纳米管.(1)金刚石,石墨,足球烯,碳
继1985年科学家发现C60分子后,1991年科学家又发现了一种管状的碳单质——碳纳米管.(1)金刚石,石墨,足球烯,碳纳米管的物理性质有较大差异的原因是_____________
___________.(2)请你推测在常温下C60和碳纳米管可能具有的化学性质_____________
__________________.简述你的理由_____________________________. 阳光明寐1年前1
阳光明寐1年前1 -
 tjenj 共回答了17个问题
tjenj 共回答了17个问题 |采纳率82.4%继1985年科学家发现C60分子后,1991年科学家又发现了一种管状的碳单质——碳纳米管.
(1)金刚石,石墨,足球烯,碳纳米管的物理性质有较大差异的原因是:碳原子的排列方式不同
(2)请你推测在常温下C60和碳纳米管可能具有的化学性质:燃烧产生二氧化碳
简述你的理由:C60和碳纳米管都由碳元素组成1年前查看全部
- (2006•自贡模拟)科学界拟合成一种“双重结构”的球形分子,即把足球烯C60分子容纳在Si60分子中,外面的硅原子与里
(2006•自贡模拟)科学界拟合成一种“双重结构”的球形分子,即把足球烯C60分子容纳在Si60分子中,外面的硅原子与里面的碳原子以共价键结合.下列有关叙述正确的是( )
A.该物质是一种新型化合物
B.该反应属于置换反应
C.该晶体属于原子晶体
D.该物质具有极高的熔沸点 guildwarsize1年前1
guildwarsize1年前1 -
 215452446 共回答了19个问题
215452446 共回答了19个问题 |采纳率89.5%解题思路:A.混合物是由两种或两种以上物质组成的物质,化合物是由不同种元素组成的纯净物;
B.置换反应中应是单质与化合物反应生成单质和化合物;
C.根据科学界拟合成一种“双重结构”的球形分子解题;
D.该晶体是由分子构成的,属于分子晶体.A.由题中信息,该物质是由一种“二重构造”的球形分子构成的,该分子是由60个碳原子和60个硅原子结合而成,由同种分子构成,是纯净物,故A正确;
B.把足球烯C60分子容纳在Si60分子中属于化合反应,故B错误;
C.根据题意知,该晶体是由分子构成的,属于分子晶体,故C错误;
D.该晶体属于分子晶体,熔沸点较低,故D错误.
故选:A.点评:
本题考点: 单质和化合物;化学基本反应类型.
考点点评: 本题考查了新型物质,正确理解题给信息是解本题关键,难度不大.1年前查看全部
- 金刚石、石墨、足球烯、碳纳米管 1.金刚石、石墨、足球烯、碳纳米管物理性质有较大差的原因是什么?2.常温下金刚石、石墨、
金刚石、石墨、足球烯、碳纳米管
1.金刚石、石墨、足球烯、碳纳米管物理性质有较大差的原因是什么?
2.常温下金刚石、石墨、足球烯、碳纳米管的化学性质是否活泼?说明原因.为何它们的化学性质相似? AJULY1年前4
AJULY1年前4 -
 davidauspure 共回答了19个问题
davidauspure 共回答了19个问题 |采纳率89.5%1.原子排列方式不同,晶型不同.
2.不活泼,因为这三种物质都是由碳原子组成,碳原子最外层电子数为4,不容易得电子形成8电子稳定结构和失电子形成2电子稳定结构,所以化学性质很稳定.
物质化学性质与原子的物理构型无关,只与原子类型和得失电子能力有关,这三种物质都是由碳原子组成,所以化学性质相似.
纯手打,很辛苦,1年前查看全部
- 现有两种碳的单质,石墨,化学式是C,足球烯,化学式是C60,
现有两种碳的单质,石墨,化学式是C,足球烯,化学式是C60,
等质量的这两种物质中含有的碳原子的个数的关系是
A.石墨中的碳原子个数大于足球烯中的碳原子个数
B.石墨中的碳原子个数小于足球烯中的碳原子个数
C.石墨中的碳原子个数等于足球烯中的碳原子个数
D.原子很小,数目很大,无法确定 卖女骇的小火柴1年前4
卖女骇的小火柴1年前4 -
 matic12345 共回答了20个问题
matic12345 共回答了20个问题 |采纳率100%C
虽然化学式不同,但都是由同一种碳元素组成,都是普通的C12,即每个原子的相对质量是12.原子数目等于总质量除以每个原子的质量.题中两种物质的质量相等,组成两种物质的原子的相对质量也相等,结果(原子个数)当然也相等.
但如果问题是分子个数,就不是这个答案了.因为石墨的分子就是C,分子相对质量是12.而足球烯的相对分子质量是12*60=720.这样的话,等质量的石墨和足球烯,石墨的分子书量就是足球烯的60倍.
所以本题的答案就是C.1年前查看全部
- 关于C60(足球烯)的问题C60中有多少个五边形、六边形?C60是否是人造的?它存在的形态和物理性质是什么?什么叫“只有
关于C60(足球烯)的问题
C60中有多少个五边形、六边形?C60是否是人造的?它存在的形态和物理性质是什么?
什么叫“只有这样C60分子才不存在双键”?难道C60还有不同的成键方式和结构吗? youzexun1年前3
youzexun1年前3 -
 simya 共回答了17个问题
simya 共回答了17个问题 |采纳率94.1%C60是由60个碳原子组成的球形32面体,即由12个五边形和20个六边形组成,只有这样C60分子才不存在双键.碳60是灰黑色的固体1年前查看全部
- 足球烯的结构特点
 wollend1年前1
wollend1年前1 -
 凌乱不堪135 共回答了16个问题
凌乱不堪135 共回答了16个问题 |采纳率100%C60是一种碳原子簇.它有确定的组成,60个碳原子构成像足球一样的32面体,包括20个六边形,12个五边形.由于这个结构的提出是受到建筑学家富勒(Buckminster Fuller)的启发.富勒曾设计一种用六边形和五边形构成的球形薄壳建筑结构.因此科学家把C60叫做足球烯,也叫做富勒烯(Fullerence),因为32面体的每个顶点上的碳原子跟三个其它的碳原子相邻.如同苯环上每个碳原子都是sp2杂化.p轨道在环的上、下形成π键一样,足球烯每个顶角上的碳原子也都满足sp2杂化的要求,(类似萘环上两个不带氢原子的碳原子)剩余的p轨道在C60分子的外围和内腔形成π键.所以C60是一种烯.
因为C60是石墨、金刚石的同素异形体,因此有科学家联想到用廉价的石墨作原料合成C60,也有人想到它含有苯环单元的结构,或许可以选用苯作原料合成C60.这些设想最后都实现了.1000g苯可以制得3gC70和C60的混合物(它们的比率为0.26~5.7).
大自然鬼斧神工的巧合,这60个C原子在空间进行排列时,形成一个化学键最稳定的空间排列位置,恰好与足球表面格的排列一致.
C60由14C标记.1年前查看全部
- (2012•闵行区二模)有下列晶体:①冰、②石英、③足球烯(C60)、④食盐、⑥白磷、⑥冰醋酸、⑦晶体氩.这些晶体中除了
(2012•闵行区二模)有下列晶体:①冰、②石英、③足球烯(C60)、④食盐、⑥白磷、⑥冰醋酸、⑦晶体氩.这些晶体中除了原子与原子间的共价键外,同时也存在范德华力的共有( )
A.3种
B.4种
C.5种
D.6种 angeloeb1年前1
angeloeb1年前1 -
 xuxian 共回答了25个问题
xuxian 共回答了25个问题 |采纳率80%解题思路:共价化合物是只含有共价键的化合物,大多非金属元素之间的化学键是共价键,分子晶体之间存在范德华力.①冰是水分子构成的分子晶体,碳原子和氧原子间是共价键,分子间存在范德华力,故①正确;
②二氧化硅是硅原子和氧原子间通过共价键形成的原子晶体,不存在范德华力,故②错误;
③足球烯分子中碳原子之间是共价键,属于分子晶体,存在范德华力,故③正确;
④食盐是钠离子和氯离子之间通过离子键星恒的离子晶体,不存在共价键和范德华力,故④错误;
⑤白磷分子中P原子之间是共价键,属于分子晶体,存在范德华力,故⑤正确;
⑥冰醋酸中碳原子、碳原子间以及碳原子之间均存在共价键,属于分子晶体,存在范德华力,故⑥正确;
⑦晶体氩是单原子分子,不存在化学键,故⑦错误.
故选:B.点评:
本题考点: 化学键和分子间作用力的区别.
考点点评: 本题考查学生化学键和分子间作用力方面的知识,注意知识的归纳和整理是关键,难度不大.1年前查看全部
- 证明足球烯和纳米碳管都是由碳元素组成的方案(用澄清石灰水)
 我爱芸豆1年前2
我爱芸豆1年前2 -
 老刘 共回答了24个问题
老刘 共回答了24个问题 |采纳率91.7%将等质量的两种物质,放入充足的氧气中充分燃烧,然后将生成的气体分别通入足量澄清的石灰水,澄清的石灰水变浑浊说明有碳元素.反应后得到的碳酸钙的质量相等,且其中碳元素的质量和开始时反应的两种物质质量相等.说明两种物质都是由碳元素组成的单质.或者用氢氧化钠溶液吸收,溶液质量的增加相同,且增加的质量中碳元素质量相同.就能说明了.1年前查看全部
- 如何制作一个实验证明足球烯是由碳元素组成的
 cools_liang1年前1
cools_liang1年前1 -
 skybird_5 共回答了19个问题
skybird_5 共回答了19个问题 |采纳率94.7%燃烧,产生碳黑1年前查看全部
- 金刚石,石墨,足球烯,碳纳米管物理性质有较大差异的原因是?
 天下无疆1年前2
天下无疆1年前2 -
 2众里寻她千百度 共回答了24个问题
2众里寻她千百度 共回答了24个问题 |采纳率91.7%原来排列方式不同1年前查看全部
- 类似足球烯(C60)的N60是一种很好的火箭燃料.有关N60的说法正确的是( )
类似足球烯(C60)的N60是一种很好的火箭燃料.有关N60的说法正确的是( )
A.它是一种化合物
B.它由60种元素组成
C.它的相对分子质量是840
D.它属于混合物 smzx1年前1
smzx1年前1 -
 oroeniyl 共回答了22个问题
oroeniyl 共回答了22个问题 |采纳率95.5%解题思路:A、由不同种元素组成的纯净物是化合物.
B、根据N60化学式的含义进行分析判断.
C、根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析判断.
D、根据N60是由N60一种物质组成的进行分析判断.A、N60是由一种元素组成的纯净物,属于单质,故选项说法错误.
B、N60是由氮元素一种元素组成的,故选项说法错误.
C、它的相对分子质量是14×60=840,故选项说法正确.
D、N60是由N60一种物质组成的,属于纯净物,故选项说法错误.
故选:C.点评:
本题考点: 化学式的书写及意义;纯净物和混合物的判别;单质和化合物的判别;相对分子质量的概念及其计算.
考点点评: 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.1年前查看全部
- 由原子直接构成?足球烯也是碳原子直接构成的吗?那为什么又说60个碳原子构成一个足球烯分子呢?还有由原子直接构成是不是指这
由原子直接构成?
足球烯也是碳原子直接构成的吗?
那为什么又说60个碳原子构成一个足球烯分子呢?
还有由原子直接构成是不是指这个物质里的原子结构都是
精密的排列在一起 不像水分子那样是一个一个的 教taohe1年前1
教taohe1年前1 -
 cmtcmt 共回答了22个问题
cmtcmt 共回答了22个问题 |采纳率86.4%真正意义上的由原子直接构成的物质指的是以原子晶体形式存在的物质.换个说法就是属于原子晶体的物质.
像金刚石、水晶(二氧化硅)、碳化硅、晶体硅等都是由原子直接构成的物质.
金属严格而言不是由原子直接构成的物质,因金属属于金属晶体.金属晶体是由金属阳离子和自由电子构成的.
稀有气体也不是由原子直接构成的物质,稀有气体是分子晶体.但因稀有气体是单原子分子,有人把它也说成是由原子直接构成的物质.这不妥.
碳60是分子晶体,因此它不是由原子直接构成的物质.60个碳原子形成一个分子,许多分子形成分子晶体.1年前查看全部
- C60(足球烯)的相对分子质量
 wwwaaannnppp1年前1
wwwaaannnppp1年前1 -
 liangwei511028 共回答了13个问题
liangwei511028 共回答了13个问题 |采纳率100%12*60=7201年前查看全部
- 微观世界里是很神奇的.诺贝尔化学奖曾授于发现C60(又称足球烯)的三位科学家,现在C70也已制得.对C60 和
 微观世界里是很神奇的.诺贝尔化学奖曾授于发现C60(又称足球烯)的三位科学家,现在C70也已制得.对C60 和C70这两种物质的叙述正确的是( )
微观世界里是很神奇的.诺贝尔化学奖曾授于发现C60(又称足球烯)的三位科学家,现在C70也已制得.对C60 和C70这两种物质的叙述正确的是( )
A.仅由一种元素组成
B.是两种新型的化合物
C.若C相对原子质量12,则质量分别为720与840
D.分子可以再分,可见一个C70由一个C60和一个C10构成 handsomecamble1年前1
handsomecamble1年前1 -
 lhqgyl 共回答了24个问题
lhqgyl 共回答了24个问题 |采纳率87.5%解题思路:根据物质的组成进行分析,C60 和C70这两种物质都是由碳元素组成的单质.A、C60 和C70这两种物质都是由碳元素组成的单质,故说法正确;
B、C60 和C70这两种物质都是由碳元素组成的单质,故说法错误;
C、C60 的相对分子质量为12×60=720,C70的相对分子质量为12×70=840,故说法正确;
D、一个C70由70个碳原子构成的,故说法错误;
故选C.点评:
本题考点: 碳元素组成的单质;单质和化合物的判别;相对分子质量的概念及其计算.
考点点评: 本题考查了碳的单质,完成此题,可以依据具体物质的化学式进行.1年前查看全部
- 足球烯的物理性质,如:颜色状态等
 人就是用来折腾的1年前1
人就是用来折腾的1年前1 -
 付岩岩 共回答了16个问题
付岩岩 共回答了16个问题 |采纳率87.5%足球烯
1985年,Rice大学的H.W.Kroto和R.E.Smalley等发现用激光束使石墨蒸发,用10大气压的氦气产生超声波,在喷咀上能生成性质十分稳定的一种新的碳的同素异形体.经过飞行时间质谱证实,它的确不含其它元素,其组成主要是C60.Kroto等为了纪念前驱研究者Buckminster Fuller,将这个球形分子称为Buckminsterfullerene或者简称为“布克球”(Buckyball).
他们认为这种碳单质既然具有确定的组成,显然就不会像石墨或金刚石一样构成无限庞大的分子.按照碳原子价键的要求,它可能具有球形结构.它以60个碳原子作为顶点,组成一个32面体.其中12个面是正边形,20个面是六边形.正好是一个削20面体的每个顶点,像足球一样的多边形体,.在这样的分子中,每个碳原子都满足sp2杂化轨道的要求:与其它三个碳原子相连,等价地组成一个五员环和两个六员环.由于它具有这种特殊结构,因此现在更形象地称它为足球烯(footballene,soccerballene).
按照正常的碳—碳键的键长计算,C60构成的球体直径大约为7 A0 ,它的内腔至少可以容纳一个直径为5 A0 的客体原子.根据这种思想,Smalley又设计将石墨板浸泡在沸腾的三氯化镧饱和溶液中,干燥后将它作为靶子,用激光蒸发,使镧原子嵌入球体内部.从而发现了一系列分别由44个到76个碳原子和一个镧原子组成的碳—镧化合物.显然这是一种包合物.
事实上,12个正五边形不仅只能和20个六边形构成C60的封闭壳,还可以和其它若干个六边形组成蛋形的多面体,而镧原子的存在,使其它形式的多面体也趋于稳定.
和C60分子有关的“碗烯”(corranulene)分子,C20H10,具有一个由五个正六边形环绕的正五边形结构.这个化合物早已于1966年由Michigan大学的R.G.Lawton合成成功.它的分子构型像一个碗,有芳香性,而且很稳定.而足球烯分子的表面,就存在着这样的12个正五角形单元.C60分子具有Ih点群的对称性,是一个“非交替烃”(non-alternant hydrocarbon).
曾经有好几位学者对C60作过HMO计算,并将C60和其它芳香烃的离域能(delocalization energy)和共振能进行比较.结果表明其共振稳定性大约是苯分子中每个碳原子的平均共振能的两倍.虽然在这个分子中碳原子并不都是完全共平面的,因此会出现一些张力,但是它的共振结构数高达12500,因而可以使体系稳定化.如果考虑到C60多面体分子中π键与σ键的交角大约是11.60,用0.877校正其共振积分,按POAV1/3D HMO法计算,仍然可以明显地看出它具有较高的π电子能.1年前查看全部
- 足球烯中的碳原子之间的键是双键还是单键,化学键是共价键还是离子键?
 scottludong1年前3
scottludong1年前3 -
 火舞天使 共回答了19个问题
火舞天使 共回答了19个问题 |采纳率94.7%足球烯之间的键是不能用经典价键理论解释的,就像苯一样,既不是单键也不是双键(楼上说“既有双键又有单键”是不正确的).C与C间杂化类型介于sp2与sp3之间,是sp2.28杂化,如苯中sp2杂化一样.未杂化轨道,形成了60个C公用的大π健(类比于苯6个Cπ键).
是非极性共价键.
希望回答对你有所帮助1年前查看全部
- 金刚石与“足球烯”C60是同一种物质吗?
 春利1年前1
春利1年前1 -
 j_we 共回答了25个问题
j_we 共回答了25个问题 |采纳率84%同素异形体.1年前查看全部
- 石墨和足球烯为什么有类似的化学性质
 qiqiloveyong1年前1
qiqiloveyong1年前1 -
 迦兰轩主 共回答了12个问题
迦兰轩主 共回答了12个问题 |采纳率100%石墨为sp2杂化 球碳为sp2.28 都有一定的共轭 有一定的芳香性 可能导致化性相近 个人观点1年前查看全部
- 足球烯和碳纳米管的化学性质是否活泼,为什么
 杂品1年前1
杂品1年前1 -
 opens007 共回答了19个问题
opens007 共回答了19个问题 |采纳率84.2%它们的化学结构稳定~~原子处于稳定状态 所以不活泼~~1年前查看全部
- 足球烯中的碳原子的杂化方式是Sp2杂化,可为什么得到的三个西格玛键不在一个平面
 我爱小凤凰1年前1
我爱小凤凰1年前1 -
 草地里的石头 共回答了13个问题
草地里的石头 共回答了13个问题 |采纳率92.3%其实C60更多的是sp3杂化,而且在杂化中形成的电子对为了整个原子的稳定性在空间分布上也会表现出一点点的差异,简单的说你可以理解为为了C60分子的稳定性,sp2杂化的碳原子让其杂化形成的西格玛键在空间上出现了一点微妙的差异1年前查看全部
- 碳60即足球烯属于过渡晶体吗?
 xiaolu19771年前1
xiaolu19771年前1 -
 bachelor_xf 共回答了20个问题
bachelor_xf 共回答了20个问题 |采纳率80%不是
是碳的另一种同素异型体
相对于活性炭和金刚石1年前查看全部
- 请问怎样证明足球烯由碳元素组成
 wqcz78791年前1
wqcz78791年前1 -
 GUO88888888 共回答了10个问题
GUO88888888 共回答了10个问题 |采纳率90%燃烧它
把气体排进石灰水中
有沉淀1年前查看全部
- 关于C60(足球烯)的芳香性C60有60个pai电子,不符合休克尔规则,为什么说它有芳香性?
 阳光所及处1年前1
阳光所及处1年前1 -
 徐鉴 共回答了19个问题
徐鉴 共回答了19个问题 |采纳率84.2%如果我没记错的话休克尔规则是指平面上的多烯而言的吧 不知道能不能推广到立体范围内
由于每个C用一个p轨道互相重叠形成一个含60个π电子的闭层电子结构,因此在近似球体的笼内和笼外都围绕着π电子云,所以其具有较大的离域能,其共振式达到12500个,按每个C的平均共振能比较,其共振稳定性约为苯的2倍,因此足球烯是具有芳香性的稳定体系1年前查看全部
- 金刚石 碳 足球烯 的熔点比较如题
 那些花儿漂了1年前2
那些花儿漂了1年前2 -
 班主阿呆 共回答了23个问题
班主阿呆 共回答了23个问题 |采纳率91.3%足球烯为分子单质晶体,金刚石为原子晶体,碳(举例有石墨)熔点比较高,所以熔点:金刚石>碳>足球烯1年前查看全部
- 下列说法中正确的一组是( )A.H2和D2互为同位素B.和为同一物质C.碳链为与的烃为同系物D.金刚石、石墨和“足球烯
下列说法中正确的一组是( )
A.H2和D2互为同位素
B.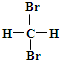 和
和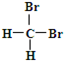 为同一物质
为同一物质
C.碳链为 与
与 的烃为同系物
的烃为同系物
D.金刚石、石墨和“足球烯”C60为同素异形体 na0000051年前1
na0000051年前1 -
 沧有泪 共回答了16个问题
沧有泪 共回答了16个问题 |采纳率93.8%解题思路:具有相同质子数,不同中子数(或不同质量数)同一元素的不同核素互为同位素;
有机化合物中具有同一通式、组成上相差一个或多个CH2原子团、在结构与性质上相似的化合物互为同系物;
具有相同分子式而结构不同的化合物互为同分异构体;
素异形体是同种元素形成的不同单质,据此进行判断.A.H2和D2都是氢气,二者为同一种物质,不属于同位素,故A错误;
B.甲烷中四个氢原子位置等效,则二溴乙烷不存在同分异构体,二者为同一种物质,故B正确;
C. 中含有碳碳双键,而
中含有碳碳双键,而 中含有环,二者结构不同,分子式相同,属于同分异构体,故C错误;
中含有环,二者结构不同,分子式相同,属于同分异构体,故C错误;
D.金刚石、石墨和“足球烯”C60为是碳元素的不同单质,它们互为同素异形体,故D正确;
故选BD.点评:
本题考点: 芳香烃、烃基和同系物;同位素及其应用;同素异形体.
考点点评: 本题考查了同系物、同位素、同分异构体、同分异构体的判断,题目难度不大,注意掌握同分异构体与同系物的概念及判断方法,明确同位素与同系物、同素异形体的区别;选项A为易错点,注意二者为同一种物质,同位素研究对象为原子.1年前查看全部
- 怎样证明碳纳米管、石墨和足球烯都是由碳元素组成的?
怎样证明碳纳米管、石墨和足球烯都是由碳元素组成的?
要设计一个方案! littlepig_keke1年前3
littlepig_keke1年前3 -
 lhdycz 共回答了25个问题
lhdycz 共回答了25个问题 |采纳率80%分别点燃,再把燃烧生成的气体全部通入足量澄清石灰水中,生成白色沉淀(碳酸钙),即可证明它们都是碳元素组成的.1年前查看全部
- 分别组成石墨,金刚石,足球烯,的原子是一模一样的,还是碳的同位素原子
 wanglixian1年前5
wanglixian1年前5 -
 连云港31 共回答了18个问题
连云港31 共回答了18个问题 |采纳率100%都是相同的碳原子组成的,只是它们的原子排列的方式不同,形成了三种不同的物质,
石墨碳原子排成细鳞片状、金刚石是正八面体、C60排成足球状结构.与碳的同位素无关.1年前查看全部
- 请你设计一个方案,证明足球烯和碳纳米管都是由碳元素组成的
 蝴蝶翩翩飞991年前3
蝴蝶翩翩飞991年前3 -
 dawei2010 共回答了15个问题
dawei2010 共回答了15个问题 |采纳率93.3%在密闭容器里加热(容器里有空气)
在把混合气体先通入品红,再通入石灰水
若品红不褪色,石灰水变浑浊,则证明生成的气体都是CO21年前查看全部
- 金刚石,石墨,足球烯都是由碳原子构成的,但它们的物理性质差别很大,这是因为
金刚石,石墨,足球烯都是由碳原子构成的,但它们的物理性质差别很大,这是因为
A原子内部结构不同 B原子组成的分子不同
C原子的排列顺序不同 D原子的质量不同
为什么选c,A、B不对吗 qiugou1231年前1
qiugou1231年前1 -
 nanjinrennanjin 共回答了26个问题
nanjinrennanjin 共回答了26个问题 |采纳率92.3%首先,这三种物质中除了足球烯以外都不存在分子这一说,这个金刚石是原子晶体,石墨是混合晶体,足球烯是分子晶体,金刚石和石墨中都木有分子,B不对.
此外,他们都是由碳原子直接构成的,所以说原子内部结构也是相同的,A不对.1年前查看全部
- 下列物质中属于有机酸的酸是?A.碳酸B.足球烯C.醋酸D.酒精为什么是不是碳酸
 葵花公公1年前3
葵花公公1年前3 -
 云滔天 共回答了22个问题
云滔天 共回答了22个问题 |采纳率95.5%所谓有机物通常指含碳元素的化合物,或碳氢化合物及其衍生物总称为有机物.因此醋酸算作有机酸.而无机物是无机化合物的简称,通常指不含碳元素的化合物.少数含碳的化合物,如一氧化碳、二氧化碳、碳酸盐、氰化物等也属于无机物.无机物大致可分为氧化物、酸、碱、盐等.由于碳酸是由二氧化碳溶于水形成的,因此碳酸算作无机酸.1年前查看全部
大家在问
- 17.91-3.99的简便方法
- 2梅子涵《快递》中人与人之间的关系
- 3能否把一个正方形纸片剪成四块,用这四块拼成两个正方形?
- 4箱子里放着3个苹果,5个橘子,2个桃子,7个梨,小明随便拿出一个水果,有______种可能,拿到______的可能性最小
- 5一间教室的容积大约是200()填单位
- 6彩票中奖的概率问题市面上的福利彩票36选7,全中的概率是多少?希望能给出计算过程,可以的话请带有解释.7个号码中其中6个
- 7英语翻译资金流的处理是传统商务也是电子商务的重要环节.然而由于传统的交易模式和支付方式的影响,以及对电子支付与结算知识的
- 8如图,抛物线y=-x²+2x+3与x轴交于A、B两点,与y轴交于点C,点P(2,m)是抛物线与直线l:y=k(
- 9根据下列信息向大家解释这位朋友:30-40词.
- 10帮忙翻译下下面的谚语,要完整点,It is no use crying over spilt milk.
- 112000Ω 1w的电阻额定电压是多少?
- 12皎洁的月光正照在盲姑娘那恬静的脸上 怎么缩句
- 13.观察下面一幅漫画,回答问题。 (6分)
- 14inventory reported on balance sheet at LOWER OF COST OR MARK
- 15不降低温度,只增大压强也可能使物质从气态变成液态对吗?
