氧化银纽扣电池把什么能转化为电能
 远钧QQ2022-10-04 11:39:542条回答
远钧QQ2022-10-04 11:39:542条回答Zn+Ag2O=ZnO+2Ag ,把什么能转化为电能?

已提交,审核后显示!提交回复
共2条回复
 shamomiao 共回答了22个问题
shamomiao 共回答了22个问题 |采纳率90.9%- 化学能,所有化学电池都是将化学能专化为电能
- 1年前
 甘拜下风 共回答了74个问题
甘拜下风 共回答了74个问题 |采纳率- 化学能转化为电能
- 1年前
相关推荐
- 把0.7摩尔的氧化银在空氧中加热,可取得多少克的银?
 zyzff1年前1
zyzff1年前1 -
 都市的骆驼 共回答了19个问题
都市的骆驼 共回答了19个问题 |采纳率100%2AG2O= 4AG+ O2
2MOL 432
0.7MOL X=151.2克可取得151.2克的银1年前查看全部
- 银锌蓄电池是一种高能电池,它的两极材料分别为锌和氧化银,电解质溶液为KOH溶液,放电时它的正、负两极的电极反应式如下:
银锌蓄电池是一种高能电池,它的两极材料分别为锌和氧化银,电解质溶液为KOH溶液,放电时它的正、负两极的电极反应式如下: Ag 2 O+H 2 O+2e - =2Ag+2OH - Zn+2OH - -2e - =Zn(OH) 2 下列判断正确的是 [ ]A.锌为负极,氧化银为正极
B.锌为正极,氧化银为负极
C.原电池工作时,负极区溶液pH增大
D.原电池反应的化学方程式为:Zn+Ag 2 O+H 2 O=Zn(OH) 2 +2Ag longcheng0091年前1
longcheng0091年前1 -
 洞中幽静 共回答了17个问题
洞中幽静 共回答了17个问题 |采纳率88.2%AD1年前查看全部
- 常见复杂化合物就写出这几个 \\\1.碘化氢2.氧化银3.氧化钡4.氧化亚铜5.氯化锰6.氯化铵7.硫化亚铁8.另外 那
常见复杂化合物
就写出这几个 \
1.碘化氢
2.氧化银
3.氧化钡
4.氧化亚铜
5.氯化锰
6.氯化铵
7.硫化亚铁
8.另外 那个亚铁 是什么?
要化学式 陌上听箫1年前2
陌上听箫1年前2 -
 魔鬼降临7 共回答了23个问题
魔鬼降临7 共回答了23个问题 |采纳率95.7%1 HI
2 Ag2O
3 BaO
4 Cu2O
5 MnCl2
6 NH4Cl
7 FeS
8 亚铁指化合价态比较低的铁,是+2价的.亚铜就是+1价的.1年前查看全部
- 纽扣电池的两极材料分别为锌和氧化银,电解质溶液为KOH溶液。放电时两个电极反应分别为:
纽扣电池的两极材料分别为锌和氧化银,电解质溶液为KOH溶液。放电时两个电极反应分别为:
Zn +2OH - -2e - = Zn(OH) 2 Ag 2 O + H 2 O + 2e - = 2Ag +2OH - 下列说法正确的是:()A.溶液中OH - 向正极移动,K + 、H + 向负极移动 B.锌发生还原反应,氧化银发生氧化反应 C.锌是负极,氧化银是正极 D.在电池放电过程中,电解质溶液的酸碱性基本保持不变  lana5261年前1
lana5261年前1 -
 266100 共回答了21个问题
266100 共回答了21个问题 |采纳率71.4%C
1年前查看全部
- 如何用配位反应溶解Ag2O(氧化银)?
如何用配位反应溶解Ag2O(氧化银)?
最好写出反映方程式 讨厌ggee1年前1
讨厌ggee1年前1 -
 han0705 共回答了14个问题
han0705 共回答了14个问题 |采纳率92.9%加入氰氢酸,很快溶解:
Ag2O + 2HCN == H2O + 2AgCN
AgCN + HCN == H[Ag(CN)2](配合物)1年前查看全部
- 一颗氧化银纽扣电池的电压是多少伏?
 和月玉人1年前1
和月玉人1年前1 -
 芝芝love 共回答了17个问题
芝芝love 共回答了17个问题 |采纳率70.6%要看什么型号的,有1.5v 也有3v 等,各产品要求不同.1年前查看全部
- 氧化银和过氧化氢反应生成银,氧气和水的反应中,双氧水体现了什么性(氧化性/还原性/氧化性和还原性)
 sunny52091年前1
sunny52091年前1 -
 bslp 共回答了16个问题
bslp 共回答了16个问题 |采纳率87.5%Ag2O中的Ag为+1价,变成了银单质,化合价降低.
H2O2中的O为-1价,变成氧气单质,化合价升高.
所以H2O2是还原剂,还原性.
Ag2O + H2O2 = 2Ag + H2O + O2↑
考虑到过氧化氢可以自身氧化还原,所以根据方程式配平的不同,过氧化氢也可能即是氧化剂又是还原剂.
2H2O2 = 2H2O + O2↑
例如:上面两个方程式按照1:1(这个比例可以任意)相加等到
Ag2O + 3H2O2 = 2Ag + 3H2O + 2O2↑ 在这个方程式中,过氧化氢就不单纯是还原剂了.1年前查看全部
- (2014•温州二模)现有氧化银、氧化镁、氧化铝的混合物,按如图所示的方法制取金属单质,下列叙述正确的是( )
(2014•温州二模)现有氧化银、氧化镁、氧化铝的混合物,按如图所示的方法制取金属单质,下列叙述正确的是( )
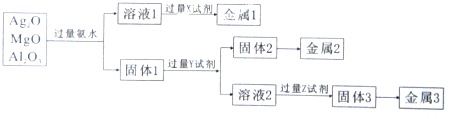
A.试剂X可能是葡萄糖
B.试剂Z一定是CO2
C.工业上可用CO还原固体2制取金属2
D.工业上用固体3经一步反应制取金属3 jy002392091年前1
jy002392091年前1 -
 逸云雨枫 共回答了16个问题
逸云雨枫 共回答了16个问题 |采纳率87.5%解题思路:混合物中仅有氧化银与氨水反应生成银氨溶液,则溶液1为银氨溶液,试剂X可为葡萄糖,金属1为银,固体1为氧化镁和氧化铝的混合物,试剂Y可为氢氧化钠溶液,则固体2为氧化镁,金属2为镁,溶液2为偏铝酸钠,固体3为氢氧化铝,金属3为铝,以此解答该题.混合物中仅有氧化银与氨水反应生成银氨溶液,则溶液1为银氨溶液,试剂X可为葡萄糖,金属1为银,固体1为氧化镁和氧化铝的混合物,试剂Y可为氢氧化钠溶液,则固体2为氧化镁,金属2为镁,溶液2无i偏铝酸钠,固体3为氢氧化铝,金属3为铝,
A.混合物中仅有氧化银与氨水反应生成银氨溶液,则溶液1为银氨溶液,能与银氨溶液反应生成银的物质含有醛基,可为葡萄糖,故A正确;
B.溶液2为偏铝酸钠,Z可为二氧化碳或弱酸,故B错误;
C.金属2为镁,工业用可用电解法或用碳作还原剂冶炼镁,不能用CO,故C错误;
D.固体3为氢氧化铝,不能通过一步反应生成铝,应先生成氧化铝,然后电解,故D错误.
故选A.点评:
本题考点: 物质分离和提纯的方法和基本操作综合应用.
考点点评: 本题综合考查物质的分离、提纯以及金属的冶炼,为高频考点,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,注意把握相关物质的性质,为解答该题的关键,难度中等.1年前查看全部
- 电子表所用的纽扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应式是:Zn+2OH - -2e - =Zn
电子表所用的纽扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应式是:Zn+2OH - -2e - =ZnO+H 2 O;Ag 2 O+H 2 O+2e - =2Ag+2OH - .总反应式为:Ag 2 O+Zn=2Ag+ZnO,下列说法正确的是( ) A.Zn为正极,Ag 2 O为负极 B.Zn为负极,Ag 2 O为正极 C.原电池工作时,正极区溶液PH值增大 D.原电池工作时,负极区溶液PH值增大  r27061年前1
r27061年前1 -
 BCDAIH 共回答了14个问题
BCDAIH 共回答了14个问题 |采纳率100%A、根据化合价变化可知Zn被氧化,应为原电池的负极,则正极为Ag 2 O,故A错误;
B、根据化合价变化可知Zn被氧化,应为原电池的负极,则正极为Ag 2 O,故B正确;
C、原电池工作时,正发生反应Ag 2 O+H 2 O+2e - =2Ag+2OH - ,该极区溶液PH值增大,故C正确;
D、原电池工作时,负发生反应Zn+2OH - -2e - =ZnO+H 2 O,溶液PH值减小,故D错误.
故选BC.1年前查看全部
- 相同质量的高锰酸钾、氯酸钾、氧化银与过氧化氢在一定条件下使之完全反应,生成氧气最多的是什么物质/
 cctv_71年前1
cctv_71年前1 -
 bshuangning 共回答了22个问题
bshuangning 共回答了22个问题 |采纳率86.4%因为:相对原子质量Ag2O>KMnO4>KClO3>H2O2 所以:等质量的这些物质中H2O2的量较多,所以H2O2产生氧气最多1年前查看全部
- 氯化镁怎么写氯化镁,氧化钠,氯化铜,氧化银,硫酸铝,碳酸铜,硝酸钙,氢氧化铜,氧化铵,碳酸钠,怎么写 _____!
 以身犯险1年前4
以身犯险1年前4 -
 影子漂浮 共回答了15个问题
影子漂浮 共回答了15个问题 |采纳率100%氯化镁 MgCl2
氧化钠 Na2O
氯化铜 CuCl2
氧化银 Ag2O
硫酸铝 Al2(SO4)3
碳酸铜 CuCO3
硝酸钙 Ca(NO3)2
氢氧化铜 Cu(OH)2
氧化铵 不存在这种物质,应该是氨水:NH3.H2O
碳酸钠 Na2CO31年前查看全部
- 1.氧化银受热分解成银和氧气.若0.2mol硝酸银,AgNO3受强热至质量不变,残余物的质
1.氧化银受热分解成银和氧气.若0.2mol硝酸银,AgNO3受强热至质量不变,残余物的质
量为多少?
A.34.0g B.21.6g C.17.0g D.12.4g
2.当 0.1g 的镁与过量的盐酸反应,在室温和气压的环境下,生成气体的体积为多少?
A.10cm3 B.24cm3 C.48cm3 D.100cm3
3.8g 的氧与16g的X 元素有相同的原子数.X 的相对原子质量Ar为多少?
A.4 B.8 C.16 D.32
4.在 2mol/dm3的硫酸钠中哪种离子呈现最高的浓度?
A.氢离子,H+(aq)
B.氢氧离子,OH-(aq)
C.钠离子,Na+(aq)
D.硫酸根离子,SO4
2-(aq)
5.一体积的乙烷,C2H6在r.t.p下质量为20g.相同体积下的丙烯C3 H6 在r.t.p下质量为多少?
A.28g B.21g C.20g D.42g 李家老四1年前2
李家老四1年前2 -
 sheader 共回答了22个问题
sheader 共回答了22个问题 |采纳率100%1.B
2AgNO3 == 2Ag + 2NO2 + O2,所以0.2molAgNO3生成0.2molAg.
2.D
常温下,气体的摩尔体积不是22.4L/mol,而是比之稍大(24.4),可以先按标准状况求体积,再选择比它稍大的答案.
0.1g/24g/mol * 22400mL/mol =93.3mL,比它稍大的就是100.
3.D
原子数相同时,质量是2倍,则相对原子质量也是O原子的2倍.
4.C
1molNa2SO4可电离出2molNa+.
5.A.
相同条件下,气体的体积之比等于物质的量之比,体积相同,物质的量相同.
则两气体的质量之比等于它们的摩尔质量之比.
20:X=30:42
X=281年前查看全部
- 人们利用原电池原理,制作了多种电池,如电子计算机所用钮扣电池就是其中一种.它的两极材料为锌和氧化银,电解质溶液为KOH溶
人们利用原电池原理,制作了多种电池,如电子计算机所用钮扣电池就是其中一种.它的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应是:Zn+2OH - -2e - ===ZnO+H 2 O;Ag 2 O+H 2 O+2e - ===2Ag+2OH - .下列判断正确的是 [ ]A.锌为正极,Ag 2 O为负极
B.锌为负极,Ag 2 O为正极
C.原电池工作时,负极区溶液pH减小
D.原电池工作时,负极区溶液pH增大 yy的男人男人1年前1
yy的男人男人1年前1 -
 taotaorani1 共回答了25个问题
taotaorani1 共回答了25个问题 |采纳率88%BC1年前查看全部
- 电子表中电源常用银—锌微型电池,电极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应是:Zn+2OH - -2e -
电子表中电源常用银—锌微型电池,电极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应是:Zn+2OH - -2e - =ZnO+H 2 O Ag 2 O+H 2 O+2e - =2Ag+2OH - 电池的总反应式为:Ag 2 O+Zn= 2Ag+ZnO,下列判断不正确的是
A.锌为负极,Ag 2 O为正极 B.锌发生还原反应,氧化银发生氧化反应 C.原电池工作时,负极附近溶液的pH值减小 D.原电池工作时,电子流动方向为Zn→Ag 2 O  瑕疵11年前1
瑕疵11年前1 -
 langziwuzhe 共回答了26个问题
langziwuzhe 共回答了26个问题 |采纳率96.2%B
1年前查看全部
- 如何使氧化银还原
 xss12281年前2
xss12281年前2 -
 xiaohuan3118 共回答了16个问题
xiaohuan3118 共回答了16个问题 |采纳率93.8%加热就可以
黑银是由于氧化所致,氧化银(Ag2O)是黑色的故银的表面会呈现出黑色状.因此可以通过使用强还原剂甲醛(HCHO)通过氧化还原反应来将氧化银还原成银.另外还有一种方法是用碱性物质洗涤或者擦拭,这是因为氧化银偏酸性,用碱性物质可以与之中和,楼上的用火灰擦也是这个道理,就是因为火灰中含有少量的氢氧化钾(KOH),而氢氧化钾呈碱性与氧化银反应就会除去黑色的氧化银.据说还可以用锡纸包住银饰,撒上食言,放在火上稍微加热一下也可通过置换反应还原银.1年前查看全部
- 氧化银的溶解度是13mg/L,当溶于水时,是以氧化银状态还是电离为银离子?
 红酒ff1年前3
红酒ff1年前3 -
 dtjt0513 共回答了19个问题
dtjt0513 共回答了19个问题 |采纳率78.9%溶解的部分是以氧化银状态存在于水中,不电离.1年前查看全部
- 氧化银 的化学式( )?
 gszyyxl1年前3
gszyyxl1年前3 -
 aileen247 共回答了19个问题
aileen247 共回答了19个问题 |采纳率78.9%氧化银是黑色的粉末,不溶于水,易溶于酸和氨水.受热易分解成单质.Ag2O1年前查看全部
- 过氧化氢H2O2俗名双氧水,医疗上利用它有杀菌消毒作用来,题目中氧化银和过氧化氢氧化性强弱怎么看 .如
过氧化氢H2O2俗名双氧水,医疗上利用它有杀菌消毒作用来,题目中氧化银和过氧化氢氧化性强弱怎么看 .如
、过氧化氢H2O2,(氧的化合价为-1价),俗名双氧水,医疗上利用它有杀菌消毒作用来 清洗伤口.对于下列A~D涉及H2O2的反应,填写空白:A.Na2O2 +2HCl= 2NaCl+H2O2 B.Ag2O+ H2O2=2Ag+O2+ H2O C.2 H2O2=2 H2O+O2 D.3 H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8 H2O (4)上述反应说明H2O2、Ag2O、K2CrO4氧化性由强到弱的顺序是:氧化银和过氧化氢的氧化性怎么看啊 . snakeivan1年前1
snakeivan1年前1 -
 闪电12358 共回答了14个问题
闪电12358 共回答了14个问题 |采纳率92.9%每个找出氧化物,还原物,因为氧化性:氧化物>还原物,因而可以判断氧化银和过氧化氢的氧化性.首先:氧化物是:氧化银,还原物是:过氧化氢,所以:氧化性:氧化银>过氧化氢1年前查看全部
- 向溴化银中加入碳酸钠的现象是白色沉淀(碳酸银)还是黑色沉淀(氧化银)也就是碳酸银是否水解了又分解
 lsj962211年前3
lsj962211年前3 -
 年本法 共回答了23个问题
年本法 共回答了23个问题 |采纳率91.3%向溴化银中加入碳酸钠生成白色沉淀的可能性很小,因为溴化银的溶解度远小于碳酸银,反应不会发生.
如果说变黑了,那你用紫外光多照照可能就会实现,因为溴化银见光会分解为银单质,是黑色的小颗粒.1年前查看全部
- 电子表所用的纽扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应式是:Zn+2OH--2e-=ZnO+H2
电子表所用的纽扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应式是:Zn+2OH--2e-=ZnO+H2O;Ag2O+H2O+2e-=2Ag+2OH-.总反应式为:Ag2O+Zn=2Ag+ZnO,下列说法正确的是( )
A.Zn为正极,Ag2O为负极
B.Zn为负极,Ag2O为正极
C.原电池工作时,正极区溶液PH值增大
D.原电池工作时,负极区溶液PH值增大 ruyi3611年前1
ruyi3611年前1 -
 transparentear 共回答了27个问题
transparentear 共回答了27个问题 |采纳率92.6%解题思路:根据化合价变化可知Zn被氧化,发生氧化反应,应为原电池的负极,则正极为Ag2O,得电子发生还原反应;从总反应方程式分析,氢氧根离子的物质的量没变化但溶剂的量减少,所以碱性增大;电池工作时电子由负极通过外电路流向正极,由电荷守恒可知,带负电荷的阴离子应该移向负极,带正电荷的离子移向正极.A、根据化合价变化可知Zn被氧化,应为原电池的负极,则正极为Ag2O,故A错误;
B、根据化合价变化可知Zn被氧化,应为原电池的负极,则正极为Ag2O,故B正确;
C、原电池工作时,正发生反应Ag2O+H2O+2e-=2Ag+2OH-,该极区溶液PH值增大,故C正确;
D、原电池工作时,负发生反应Zn+2OH--2e-=ZnO+H2O,溶液PH值减小,故D错误.
故选BC.点评:
本题考点: 化学电源新型电池.
考点点评: 本题考查原电池知识,题目难度不大,可以根据所学知识来回答.1年前查看全部
- 氧化银常温下是固体、液体还是气体?
 hzbjhbbb1年前1
hzbjhbbb1年前1 -
 夏伊 共回答了19个问题
夏伊 共回答了19个问题 |采纳率94.7%应该是黑色固体.1年前查看全部
- 硝酸银溶液中通入氨气,先生成的沉淀是什么?氧化银?
 芊芊小百合1年前5
芊芊小百合1年前5 -
 KerryLogistics 共回答了14个问题
KerryLogistics 共回答了14个问题 |采纳率100%沉淀是氢氧化银和氧化银,白色氢氧化银沉淀不稳定变成棕黑色的氧化银沉淀1年前查看全部
- 氧化银溶于硫代硫酸钠溶液的反应式怎么写
 我爱麻绳1年前1
我爱麻绳1年前1 -
 草尖上的阳光 共回答了13个问题
草尖上的阳光 共回答了13个问题 |采纳率84.6%Ag2O + H2O + 4Na2S2O3 = 2Na3[Ag(S2O3)2] + 2NaOH1年前查看全部
- 氧化银热分解的化学方程式怎么写得? 知道的帮帮忙! 谢谢
 翔翔_ww1年前3
翔翔_ww1年前3 -
 风过林动 共回答了19个问题
风过林动 共回答了19个问题 |采纳率89.5%2Ag2O=4Ag+O2条件加热1年前查看全部
- 过氧化氢和氧化银反应表现出过氧化氢什么化学性质?是否表现酸性?为什么?
 richardwang7771年前1
richardwang7771年前1 -
 xiayula 共回答了21个问题
xiayula 共回答了21个问题 |采纳率76.2%氧化性和还原性,酸性没表现
因为氧化银在其中只是催化剂作用1年前查看全部
- 氧化银与一氧化碳反应生成银和二氧化碳的化学方程式
 杰西S1年前2
杰西S1年前2 -
 夏立 共回答了20个问题
夏立 共回答了20个问题 |采纳率100%AgO+CO=Ag+CO21年前查看全部
- 锌和氧化银生成的一种单质和一种氧化物,此反应的方程式中锌的化合价怎么变化
 wxq1xiaoyan1年前3
wxq1xiaoyan1年前3 -
 sandaimian 共回答了11个问题
sandaimian 共回答了11个问题 |采纳率81.8%这个是银锌电池的反应 Ag2O+Zn=2Ag+ZnO 锌变成正二价.1年前查看全部
- 从矿石中提取氧化银的方法
 玉茜1年前1
玉茜1年前1 -
 一棵树Y 共回答了20个问题
一棵树Y 共回答了20个问题 |采纳率90%要看你的题目给的杂质是什么了,我感觉直接用硫酸,过滤,往滤液里加氢氧化钠过滤不就好了1年前查看全部
- 氧化银如何用银单质制取RT
 德克拉1年前3
德克拉1年前3 -
 maimaty 共回答了16个问题
maimaty 共回答了16个问题 |采纳率81.3%向银单质上加入(1mol/L以下、0.2mol/L以上)稀硝酸,生成硝酸银、一氧化氮和水;再向硝酸银溶液中加氢氧化钠等碱溶液,获得氢氧化银和硝酸盐溶液,常温下氢氧化银分解为氧化银和水,所以直接过滤就行了!1年前查看全部
- 氢氧化银在水中的状态是什么样的?是银离子和氢氧根粒子,还是分解成水和氧化银?
 bczhongbo1年前2
bczhongbo1年前2 -
 感悟人生82 共回答了13个问题
感悟人生82 共回答了13个问题 |采纳率84.6%氢氧化银在水中分解成水和氧化银1年前查看全部
- 过氧化氢与氧化银和K2CRO4氧化性由强到弱顺序
 野风南海1年前2
野风南海1年前2 -
 chonve 共回答了15个问题
chonve 共回答了15个问题 |采纳率86.7%K2CrO4 > H2O2(H+) > Ag2O1年前查看全部
- 氢氧化银与硝酸盐溶液如何提纯氧化银?硝酸银溶液中加苛性碱溶液获得氢氧化银和硝酸盐溶液.
 xiaoduote1年前2
xiaoduote1年前2 -
 先做个小记号 共回答了22个问题
先做个小记号 共回答了22个问题 |采纳率100%你所说的氢氧化银本身极不稳定,注意是极不稳定.在AgNO3中加入NaOH得到的就是Ag2O.如果你想提纯的话,可以过滤后洗几遍沉淀,然后用氨水溶解沉淀
Ag2O+4NH3+H2O→2[Ag(NH3)2]+ +2OH-
再向其中加入含有醛基的物质即可得到单质银沉淀.
2[Ag(NH3)2]+ +HCHO+3OH-→2Ag+COOH- +4NH3+H2O1年前查看全部
- 向稀盐酸中加氧化银或碳酸银后,其ph值变大是什么原因呀
 阳光下沐浴的鱼1年前3
阳光下沐浴的鱼1年前3 -
 在眼泪中游泳的鱼 共回答了11个问题
在眼泪中游泳的鱼 共回答了11个问题 |采纳率90.9%Ag离子与盐酸中的Cl离子反应生成AgCl沉淀,酸中的H离子与O离子还有CO3离子分别生成水和碳酸,H2CO3不稳定二氧化碳挥发掉了就剩下水了,所以溶液中有水了pH值会变大.---------------1年前查看全部
- 还是那个原电池的问题,为什么在纽扣电池(碱性)正极反应式是氧化银与水得电子生成银与氢氧根离子?
还是那个原电池的问题,为什么在纽扣电池(碱性)正极反应式是氧化银与水得电子生成银与氢氧根离子?
铅蓄电池正极也是正极材料二氧化铅与电解质中硫酸根离子.氢离子共同得电子形成硫酸铅与水?铅与氧化铅也构成了原电池啊,为什么正极氧化铅不只是在传递电子,也还在得到电子发生反应被氧化? 古黛风神社1年前1
古黛风神社1年前1 -
 心怡Z 共回答了14个问题
心怡Z 共回答了14个问题 |采纳率92.9%对于原电池,电极与它们的溶液直接影响正负电极的反应方程式
你说得对,但是纠正下铅蓄电池正极是正极材料二氧化铅得电子与电解质中硫酸根离子.氢离子共同形成硫酸铅与水,正极的氧化铅是二氧化铅,有强氧化性的,虽然溶液里氢离子也有氧化性却比不上PbO2,
原电池放电时,正极区域得到电子,但电子归谁有是取决于电极材料与电解液的氧化性强弱(当然也有例外),无论纽扣电池还是铅蓄电池,它们正极电极材料氧化性均比电解液的强
至于那个铜锌原电池,正极的铜是不能被还原的,只能传递电子而已,由溶液里氢离子得到它
如果你将铜锌原电池的铜改成二氧化锰之类的,就如平常用的酸性锌锰电池,就与上述的差不多了1年前查看全部
- 氢氧化银变成氧化银的化学方程式
 seahll88991年前3
seahll88991年前3 -
 jin_xiuhua 共回答了16个问题
jin_xiuhua 共回答了16个问题 |采纳率93.8%2AgOH==Ag2O+H2O1年前查看全部
- 锌和氧化银的反应.已知总反应,负极反应怎样求正极反应?
 guoa111年前2
guoa111年前2 -
 飘泊帆船 共回答了19个问题
飘泊帆船 共回答了19个问题 |采纳率100%将总反应减去负极反应1年前查看全部
- 钮扣电池是一种常用的微型银锌电池,在电池内装有氧化银和锌等物质.当电池工作时,主要是锌与氧化银发生置换反应,从而产生电流
钮扣电池是一种常用的微型银锌电池,在电池内装有氧化银和锌等物质.当电池工作时,主要是锌与氧化银发生置换反应,从而产生电流,此反应的化学方程式______.
 我是管钱的1年前3
我是管钱的1年前3 -
 bclz112 共回答了19个问题
bclz112 共回答了19个问题 |采纳率89.5%解题思路:根据锌和氧化银发生置换反应,所以生成物中一定有单质和化合物进行分析.根据置换反应的生成物中有单质和化合物,结合质量守恒定律可以判断生成物是氧化锌和银,锌和氧化银发生置换反应生成氧化锌和银,
故答案为:Zn+Ag2O═ZnO+2Ag,点评:
本题考点: 书写化学方程式、文字表达式、电离方程式;置换反应及其应用.
考点点评: 在解此类题时,首先根据置换反应的原理和质量守恒定律判断出生成物,然后根据方程式的书写规则书写方程式.1年前查看全部
- 过氧化氢和氧化银反应的化学方程式是什么?
 abcdd3221年前2
abcdd3221年前2 -
 于东山 共回答了18个问题
于东山 共回答了18个问题 |采纳率88.9%H2O2+Ag2O→H2O+2Ag+O2↑1年前查看全部
- 锌与氧化银反应的化学方程式
 zwp11041年前1
zwp11041年前1 -
 only小芸 共回答了17个问题
only小芸 共回答了17个问题 |采纳率88.2%Zn + Ag2O = 2Ag + ZnO
置换反应1年前查看全部
- 碳酸铁在水中会怎么样?(就像氢氧化银会在水中分解成氧化银和水)
 zykhwang1年前1
zykhwang1年前1 -
 sunnyexist 共回答了19个问题
sunnyexist 共回答了19个问题 |采纳率94.7%碳酸铁在水溶液中无法存在.因为碳酸根和铁离子发生双水解.生成氢氧化铁二氧化碳和水.1年前查看全部
- 氧化银跟过氧化氢谁的氧化性较强
 zhang_4608201年前1
zhang_4608201年前1 -
 ai215355 共回答了12个问题
ai215355 共回答了12个问题 |采纳率100%过氧化氢的氧化性较强1年前查看全部
- 氧化银和氢氧化钠反应生成什么大神们帮帮忙
 gbxjtu1年前1
gbxjtu1年前1 -
 lailai9453 共回答了17个问题
lailai9453 共回答了17个问题 |采纳率94.1%生成Ag(OH)2-配离子 补充: Ag2O在 强碱 溶液中比在水中容易溶解,因为它形成了Ag(OH)2-,这里2是下标,这离子带一单位 负电荷 .反应为Ag2O+H2O=Ag(OH)2- 补充: 这是我在大学 无机化学 书上看到的,应该不会错
采纳哦1年前查看全部
- 氧化银能与氢氧化钠反应吗Ag2O+NaOH=?百科说:水中难溶。溶于氨水、氢氧化钠溶液,稀硝酸,硫代硫酸钠溶液。不溶于乙
氧化银能与氢氧化钠反应吗
Ag2O+NaOH=?
百科说:水中难溶。溶于氨水、氢氧化钠溶液,稀硝酸,硫代硫酸钠溶液。不溶于乙醇。那么它溶于氢氧化钠是不是应为和氢氧化钠反应呢? 秋叶长1年前6
秋叶长1年前6 -
 ximhbk253 共回答了24个问题
ximhbk253 共回答了24个问题 |采纳率95.8%不能.
一般金属氧化物都不能与碱反应.1年前查看全部
- AG(OH)2及其他沉淀相关AG(OH)2是否存在?还是一生成就会被氧化成黑色的氧化银?Na K等投入水中会生成h2及相
AG(OH)2及其他沉淀相关
AG(OH)2是否存在?
还是一生成就会被氧化成黑色的氧化银?
Na K等投入水中会生成h2及相应碱,那么只有Na K
还是只有可溶性碱么?
抱歉。我想都没想就打成AGOH2了。
你最后的话还没说完?之所以&……是因为什么? 一天的记忆1年前1
一天的记忆1年前1 -
 adsgh23ikes 共回答了17个问题
adsgh23ikes 共回答了17个问题 |采纳率88.2%纠正一个错误,AG(OH)2应为AGOH.AGOH在水中不稳定,易分解为黑色的氧化银.Na K等投入水中之所以会生成h2及相应碱,是因为他们处于第一主族,还原性极强,易失电子.另外,K,Na,Rb,Cs,Fr(除H外的第一主族元素)等投入水中之...1年前查看全部
- 某溶液中含有1种铁的氧化物1g,与过量的硝酸银溶液反应,生成氧化银沉淀2.65g,则此溶液中铁的氧化物是什么?
 sophia_whq1年前1
sophia_whq1年前1 -
 yire123 共回答了16个问题
yire123 共回答了16个问题 |采纳率93.8%氧化银沉淀2.65g中氧元素来自此氧化物
O:0.18275862g
Fe:0.817241379g
题目是不是错了?
Fe2O3?1年前查看全部
- 硝酸银与氢氧化钠在多低的温度下反应,生成的氢氧化银不会分解为氧化银和水
 千里孤影1年前2
千里孤影1年前2 -
 CQZKLM 共回答了13个问题
CQZKLM 共回答了13个问题 |采纳率92.3%-氢氧化银不是不存在而是分解极快,一般用碱金属氢氧化物和硝酸银的90%酒精溶液反应,不过温度很苛刻,要低于-45°C1年前查看全部
- 碳酸银 水反应要是碳酸银放入水中不是会水解吗?之后氢氧化银再分解成氧化银,水解的同时产生了氢离子,氢离子在和氧化银反应生
碳酸银 水反应
要是碳酸银放入水中不是会水解吗?之后氢氧化银再分解成氧化银,水解的同时产生了氢离子,氢离子在和氧化银反应生成了碳酸银.为什么 cityporter1年前4
cityporter1年前4 -
 hcdc9521 共回答了23个问题
hcdc9521 共回答了23个问题 |采纳率87%呃,碳酸只有钾,钠,铵(只有KCO3,Na2CO3,(NH4)2CO3溶于水).
Ag2CO3不溶于水.1年前查看全部
- 纽扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液
纽扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液
其电极反应式是:Zn-2e+2OH-=ZnO+H2O,Ag2O+H2O+2e=2Ag+2OH-,总反应式为:Ag2O+Zn=2Ag+ZnO.
请问原电池工作时,负极区的pH是变大还是变小,为什么 流浪的孩子很幸福1年前3
流浪的孩子很幸福1年前3 -
 女研究生的男朋友 共回答了16个问题
女研究生的男朋友 共回答了16个问题 |采纳率87.5%变小;原电池工作时,负极供出电子,发生氧化反应:Zn-2e+2OH-=ZnO+H2O,消耗OH-,PH变小1年前查看全部
- 电子表所用的纽扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应式是:Zn+2OH ― ―2e - =Zn
电子表所用的纽扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应式是:Zn+2OH ― ―2e - =ZnO+H 2 O;Ag 2 O+H 2 O+2e - =2Ag+2OH - 。总反应式为:Ag 2 O+Zn=2Ag+ZnO,下列说法正确的是()
A.Zn为正极,Ag 2 O为负极 B.Zn为负极,Ag 2 O为正极 C.原电池工作时,正极区溶液PH值减小 D.原电池工作时,负极区溶液PH值增大  do_i_wanna1年前1
do_i_wanna1年前1 -
 cocomei 共回答了17个问题
cocomei 共回答了17个问题 |采纳率82.4%B
从电极反应式可以看出:Zn失电子为负极,且该区消耗OH - 溶液PH值减小;Ag 2 O得电子为正极,且该区产生OH - 溶液PH值增大。1年前查看全部
大家在问
- 1我应该什么时候打电话给他?用英语怎么说
- 2为什么说我们活在过去?宇宙本来就是过去,那活着还有什么意义?
- 3英语翻译1,边吃饭边谈这个问题2,违反交通规责的人3已经没有…这种事4自己是一个比以往任何时候都自毫的母亲
- 4修改病句:报晓的雄鸡是催人早起的信号.
- 51、一个圆锥形砂堆,底面积是12.56平方米,高是6米,用这堆砂在10米宽的公路上铺20厘米厚的路面,能铺多少米长?(用
- 6一篇作文 以 我读懂了爱为主题
- 7如图所示,OB为一轻质杠杆,O为支点,OA=0.3m,AB=0.1m,将重30N的物体悬挂在B点,求:在A点至少需加多大
- 8I am pricing the Dell computer 翻译?
- 9电工学问题:怎样求一点电位啊?给出一个电路,告诉几个点的电压,或电源,接地点,求某点的点位?
- 10学校合唱队有56人,其中女生有49人,女生人数占和合唱队总人数的百分之几?
- 11在三角形ABC中,顶点A为(3,-1),AB边上的中线所在方程为3X+7Y+19=0,AC边上高所在的直线方程为6X-5
- 12下列说法错误的是( )A.空气中的氧气主要来自于植物的光合作用B.氧气的化学性质比较活泼,能与许多物质发生化学反应C.
- 13解字高手请进谁能帮我读懂下面这段字,谢谢了! 籋恳顊$羣剼垚bQ ?Fg颍i?杊j鼩?gOl黀捼?呔?: 蛏=輱竁鼓貟
- 14选词填空 广告公司为你的noodle house设计了一则广告,但有些空格需要你从广告公司提供的词汇或图案中选择来填充。
- 15八年级物理上册有关显微镜和望远镜的知识
