往浅绿色的硝酸亚铁溶液中逐滴加入稀盐酸,溶液的颜色变化是
 飞翔的西红柿sky2022-10-04 11:39:541条回答
飞翔的西红柿sky2022-10-04 11:39:541条回答A颜色变浅 B变为绿色 C没有改变 D变为棕黄色

已提交,审核后显示!提交回复
共1条回复
 wyf_nj 共回答了18个问题
wyf_nj 共回答了18个问题 |采纳率88.9%- 选D.
因为加入盐酸,为硝酸亚铁溶液提供了氢离子,而酸化的硝酸根离子具有强氧化性,会氧化亚铁离子.亚铁离子变成铁离子,所以容易颜色变为三价铁离子的颜色,即棕黄色. - 1年前
相关推荐
- 硫酸亚铁与过氧化氢的反应我用铁粉去置换硫酸铜溶液,若干天后,至无铜析出,溶液呈浅绿色.反复过滤,溶液澄清透明.此时,加入
硫酸亚铁与过氧化氢的反应
我用铁粉去置换硫酸铜溶液,若干天后,至无铜析出,溶液呈浅绿色.反复过滤,溶液澄清透明.此时,加入过氧化氢做氧化剂,溶液立刻变为红色,而非三价铁离子的橙黄色溶液,会是浓度的原因吗?同时,过氧化氢被催化分解,生成氧气(应该是有三价铁离子啊)但是,当我向溶液中加入氢氧化钠溶液时,所得沉淀均为灰绿色的氢氧化亚铁沉淀,没有任何红褐色的氢氧化铁沉淀,这是为什么呢? 醉里看你1年前1
醉里看你1年前1 -
 红刺猬榴莲 共回答了21个问题
红刺猬榴莲 共回答了21个问题 |采纳率95.2%1、Fe+CuSO4=FeSO4+Cu
2、溶液的亚铁离子作为双氧水的催化剂,而不主要是把亚铁离子氧化为铁离子,双氧水的氧化性大于亚铁离子,但铁离子的氧化性又大于双氧水,当双氧水把亚铁离子氧化为铁离子以后,铁离子又可以氧化双氧水,把双氧水氧化为氧气!亚铁离子只是作为催化剂而已!但一定有铁离子生成,溶液中铁离子和亚铁离子都存在,而且部分铁离子转化为氢氧化铁,为红褐色,和原来的颜色混合,看上去为红色!
反应1:2Fe2+ +2H+ +H2O2====2Fe3+ +2H2O
反应2:2Fe3+ + H2O2 ==== 2Fe2++O2 + 2 H+
3、灰绿色并不是氢氧化亚铁,氢氧化亚铁为白色,白色的氢氧化亚铁和红褐色的氢氧化铜混合就是灰绿色的混合沉淀!在氯化亚铁溶液中,加氢氧化钠溶液,先得到白色沉淀,慢慢变灰绿色,最后才变红褐色!这里的原因是溶液中有氧气的存在!氢氧化亚铁很容易和溶液中的氧气反应,得到氢氧化铁的!两种不同颜色的沉淀混合就是灰绿色!4Fe(OH)2+O2+2H2O=4Fe(OH)31年前查看全部
- 下列表示对应化学反应的离子方程式正确的是 A.铁溶于稀硝酸,溶液变为浅绿色:Fe+4H + +NO 3 - =Fe 3+
下列表示对应化学反应的离子方程式正确的是
A.铁溶于稀硝酸,溶液变为浅绿色:Fe+4H + +NO 3 - =Fe 3+ +NO↑十2H 2 O B.用KIO 3 氧化酸性溶液中的KI: 5I - +IO 3 - +3H 2 O =3I 2 +6OH - C.向水杨酸( 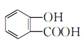 )中滴加NaHCO 3 溶液,放出无色气体:
)中滴加NaHCO 3 溶液,放出无色气体: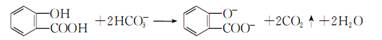
D.0.01mol·L -l NH 4 Al(SO 4 ) 2 溶液与0.02 mol·L -l Ba(OH) 2 溶液等体积混合:NH 4 + +Al 3 + +2SO 4 2 - +2Ba 2 + +4OH - =2BaSO 4 ↓十Al(OH) 3 ↓+NH 3 ·H 2 O  myq97891年前1
myq97891年前1 -
 xiaoxiaoasa 共回答了22个问题
xiaoxiaoasa 共回答了22个问题 |采纳率95.5%D
1年前查看全部
- 有一化合物X,其水溶液为浅绿色,可发生如下的转化关系(部分反应物、生成物已略)。其中,B、D、E、F均为无色气体,M、L
有一化合物X,其水溶液为浅绿色,可发生如下的转化关系(部分反应物、生成物已略)。其中,B、D、E、F均为无色气体,M、L为常见的金属单质,C为难溶于水的红褐色固体。在混合液中加入BaCl 2 溶液可生成不溶于稀盐酸的白色沉淀,H和M反应可放出大量的热。请回答下列问题 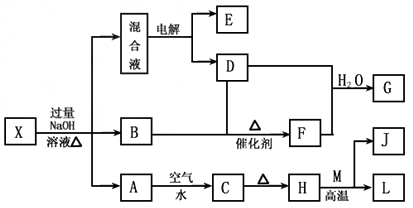
(1)X的化学式为________,M的原子结构示意图为________,L在周期表中的位置________ 。
(2)写出电解混合液时阳极的的反应式________________
(3)在CuCl 2 溶液中通入过量的B气体,可观察到的现象是________,写出总的离子反应方程式________________________。
(4)有同学设想用气体F和液态水来生产B,该反应可行?解释之。
________________________ 。
(5)已知 E气体在D中完全燃烧生成稳定的化合物时,放出b kJ的热量,写出该反应的热化学方程式________________________ 。
E气体在D中完全燃烧生成稳定的化合物时,放出b kJ的热量,写出该反应的热化学方程式________________________ 。  狠思进取1年前1
狠思进取1年前1 -
 dxy780403 共回答了13个问题
dxy780403 共回答了13个问题 |采纳率69.2%1年前查看全部
- 往FeCl3和BaCl2的混合溶液中通入SO2,溶液颜色由棕黄色变成浅绿色,同时有白色沉淀产生.为什么能够说明反应后的溶
往FeCl3和BaCl2的混合溶液中通入SO2,溶液颜色由棕黄色变成浅绿色,同时有白色沉淀产生.为什么能够说明反应后的溶液酸性增强
 天堂ヴss1年前3
天堂ヴss1年前3 -
 想不起来叫啥 共回答了20个问题
想不起来叫啥 共回答了20个问题 |采纳率100%因为Fe3+可以把SO2氧化为SO42-,同时生成H+,酸性增强.
SO2 + 2H2O + 2Fe3+ = SO42- + 2Fe2+ + 4H+1年前查看全部
- 请将以下颜色翻译成英文:灰色 浅蓝色 水蓝色 浅绿色 紫色 玫瑰红 米黄色 粉红色 咖啡色
 bruce25181年前2
bruce25181年前2 -
 小璐子 共回答了12个问题
小璐子 共回答了12个问题 |采纳率91.7%等等哦`~`偶去查查~偶有一个颜色表的.
灰色 grey
浅蓝色 lightblue
水兰色 Royalblue
浅绿色 lightgreen
紫色 purple
玫瑰红 rosyred
米黄色 Lightyellow或者Khaki
粉红色 pink
咖啡色 Brown 或者Maroon1年前查看全部
- 将SO2通入略显酸性的Fe(NO3)3溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色,请写出该化学方程式
 feiyu52113141年前3
feiyu52113141年前3 -
 rikirk 共回答了18个问题
rikirk 共回答了18个问题 |采纳率94.4%如果我没看错 应该是Fe3+先把SO2氧化成了硫酸根
方程式:2Fe(NO3)3+SO2+2H2O= FeSO4+4HNO3+Fe(NO3)2
离子式其实就是2Fe3+ + SO2 + 2H2O = 2Fe2+ +SO42- + 4H+
这时候溶液是浅绿色
又变回棕黄色 是因为溶液中有H+还有NO3- 此时相当于溶液中存在硝酸,其强氧化性将Fe2+氧化
离子式: Fe2+ + NO3- + 2H+ = Fe3+ + NO2↑ + H2O
如果硝酸根比较少会生成一氧化氮 你自己配平就行了1年前查看全部
- 化学兴趣小组发现,往CuSO4溶液中加入一定浓度的Na2CO3溶液得到的蓝色沉淀,若加入NaOH溶液则得到浅绿色沉淀.为
化学兴趣小组发现,往CuSO4溶液中加入一定浓度的Na2CO3溶液得到的蓝色沉淀,若加入NaOH溶液则得到浅绿色沉淀.为此,小组同学对沉淀成份作了如下探究:
I.探究蓝色沉淀的成份
[猜想]:蓝色沉淀①可能是CuCO3;②可能是Cu(OH)2;③是两者的混合物.
[设计方案]:小组同学利用下列装置通过实验测定其组成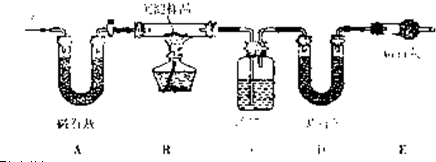
[问题与讨论]
(1)写出②猜想的依据______.
(2)装置A中碱石灰的作用是______.
(3)检查装置气密性并装好药品后,点燃酒精灯前应进行的操作是______.
(4)若沉淀样品的质量为mg.装置C质量增加了ng,则沉淀中CuCO2的质量分数为______.
II.通过查找资料得知,该浅绿色沉淀物可能是溶解度最小的碱式硫酸铜(化学式为CUSO4•3Cu(OH)2).请你设计一个实验,证明浊液中的浅绿色沉淀物中是否含有硫酸根离子的方法______. 雨打番茄1年前1
雨打番茄1年前1 -
 仰望也是一种幸福 共回答了18个问题
仰望也是一种幸福 共回答了18个问题 |采纳率88.9%解题思路:Ⅰ、(1)碱性环境下存在氢氧根离子可以和铜离子反应生成氢氧化铜沉淀;
(2)碱石灰作干燥剂,可以吸收水、二氧化碳;
(3)试验通过验证并测定水以及二氧化碳的存在、质量来确定沉淀的组成情况;
(4)根据氢氧化铜分解的化学方程式来计算;
Ⅱ、根据硫酸根的特征离子反应:可以和钡离子反应生成硫酸钡沉淀来分析.I.(1)CO32-水解成碱性,溶液中存在较多的氢氧根离子,而Cu2-与OH-结合生成沉淀Cu(OH)2,
故答案为:CO32-水解成碱性,Cu2+与OH-结合生成Cu(OH)2;
(2)该实验原理是通过验证并测定水以及二氧化碳的存在、质量来确定沉淀的组成情况,为了防止空气中水以及二氧化碳的干扰,要用碱石灰来吸收空气中的H2蒸汽和CO2,故答案为:吸收空气中的H2蒸汽和CO2;
(3)该实验原理是通过验证并测定水以及二氧化碳的存在、质量来确定沉淀的组成情况,为了防止装置中的空气对实验结果的影响,必须在点燃酒精灯之前通过量的空气,排除空气,并称量C、D的质量,
故答案为:通过量的空气并称量C、D的质量;
(4)装置C质量增加了ng,则生成水的质量是ng,根据氢氧化铜的分解方程式:Cu(OH)2
△
.
CuO+H2O,当生成ng的水时,则含有氢氧化铜的质量是[49n/9]g,则沉淀中CuCO3的质量为:m-[49n/9]g,所以沉淀中CuCO3的质量分数为:
m−
49n
9
m×100%=1-[49n/9m],故答案为:1-[49n/9m];
II.硫酸根的特征离子反应:可以和钡离子反应生成硫酸钡沉淀,证明浊液中的浅绿色沉淀物中是否含有硫酸根离子时可以先将沉淀洗涤干净,在加入足量稀盐酸溶解浅绿色沉淀,再用BaCl2溶液检验,故答案为:将浊液过滤,并把沉淀用蒸馏水洗涤至洗涤液用BaCl2溶液检验不出SO42-后,加入足量稀盐酸溶解浅绿色沉淀,再用BaCl2溶液检验,若溶液中有大量白色沉淀生成,则浅绿色没淀中有SO42-.点评:
本题考点: 铜金属及其重要化合物的主要性质;探究物质的组成或测量物质的含量.
考点点评: 本题是一道实验探究物质的化学组成的题目,考查学生分析和解决问题的能力,难度较大.1年前查看全部
- 已知高价铁盐与铁粉在溶液中能发生化合反应,生成亚铁盐,且亚铁盐溶液呈浅绿色.现有一研究性学习小组的同学将一带锈的铁钉浸入
已知高价铁盐与铁粉在溶液中能发生化合反应,生成亚铁盐,且亚铁盐溶液呈浅绿色.现有一研究性学习小组的同学将一带锈的铁钉浸入足量稀硫酸中,发现最终溶液显浅绿色.请你帮他们写出整个实验过程中发生反应的化学方程式:
①______,
②______,
③______. 本人正迷茫1年前1
本人正迷茫1年前1 -
 回贴第一oo 共回答了17个问题
回贴第一oo 共回答了17个问题 |采纳率94.1%带锈的铁钉浸入足量稀硫酸中,铁锈的主要成分氧化铁与硫酸反应生成硫酸铁和水,当铁锈反应完露出铁时,铁与硫酸反应生成硫酸亚铁和氢气,铁还能与硫酸铁溶液反应生成硫酸亚铁;化学方程式为:
Fe 2 O 3 +3H 2 SO 4 =Fe 2 (SO 4 ) 3 +3H 2 OFe+H 2 SO 4 =FeSO 4 +H 2 ↑ Fe 2 (SO 4 ) 3 +Fe=3FeSO 4
故答案为:①Fe 2 O 3 +3H 2 SO 4 =Fe 2 (SO 4 ) 3 +3H 2 O②Fe+H 2 SO 4 =FeSO 4 +H 2 ↑③Fe 2 (SO 4 ) 3 +Fe=3FeSO 41年前查看全部
- 1.溶液呈蓝色是因为存在____离子;溶液呈黄色是因为存在____离子;溶液呈浅绿色是因为存在___离子.
1.溶液呈蓝色是因为存在____离子;溶液呈黄色是因为存在____离子;溶液呈浅绿色是因为存在___离子.
2.初中化学书中不溶于水又不溶于酸的两种沉淀为____和____.蓝色沉淀的碱是_____,红褐色沉淀的碱是_____.不溶于水的白色沉淀举二例____、_____.
3.中和反应是指___和____反应生成___和___,中和反应过程中一定会____(吸热或放热),并且一定是________反应.一些中和反应没有现象,例如氢氧化钠溶液和盐酸反应是,往往需加_________来判断反应进行是否完全.服用含氢氧化铝的药物治疗胃酸的化学方程式:______________. 王琼峰1年前3
王琼峰1年前3 -
 b395814085 共回答了14个问题
b395814085 共回答了14个问题 |采纳率92.9%1.溶液呈蓝色是因为存在__Cu2+__离子;溶液呈黄色是因为存在___Fe3+_离子;溶液呈浅绿色是因为存在_Fe2+__离子.
2.初中化学书中不溶于水又不溶于酸的两种沉淀为__AgCl__和_BaSO4___.蓝色沉淀的碱是__Cu(OH)2___,红褐色沉淀的碱是__Fe(OH)3___.不溶于水的白色沉淀举二例__CaCO3__、__Mg(OH)2___.
3.中和反应是指__酸_和_碱___反应生成_盐__和_水__,中和反应过程中一定会____放热),并且一定是___放热_____反应.一些中和反应没有现象,例如氢氧化钠溶液和盐酸反应是,往往需加___石蕊______来判断反应进行是否完全.服用含氢氧化铝的药物治疗胃酸的化学方程式:_____Al(OH)3 + 3HCl = AlCl3 + 3H2O_________.1年前查看全部
- 浅绿色属于什么色调?冷色系还是暖色系?
浅绿色属于什么色调?冷色系还是暖色系?
浅绿色浅蓝色粉红色浅黄色青色浅紫色 这些分别属于什么色系啊 0771100861年前2
0771100861年前2 -
 五分钱的 共回答了25个问题
五分钱的 共回答了25个问题 |采纳率92%粉红,浅黄 也就是第一行的是暖色系,下面的是冷色系
看上去感觉温暖的颜色就是暖色,浅黄肯定是暖色啊!1年前查看全部
- 醋酸铜和铁反应,怎么先变成浅绿色,然后竟然变成了红色!到底是怎么一回事的尼?
 zgc12311年前2
zgc12311年前2 -
 有只燕子 共回答了19个问题
有只燕子 共回答了19个问题 |采纳率89.5%由于铁的金属活泼性 比铜要强 所以反应开始时 铜被置换出来 溶液变成浅绿色的 醋酸亚铁溶液.
但是亚铁离子 会被空气中的氧气氧化 最终形成 红褐色的 三价铁离子.所以 变成了 红色1年前查看全部
- (2007•南宁)有A、B、C、三种固体金属,如果把B和C放入稀盐酸中,B溶解并产生氢气,溶液由无色逐渐变为浅绿色,C不
(2007•南宁)有A、B、C、三种固体金属,如果把B和C放入稀盐酸中,B溶解并产生氢气,溶液由无色逐渐变为浅绿色,C不反应;如果把A和C放入硝酸银溶液中,过一会儿,在C表面有银析出,而A没有变化.根据以上实验事实,回答下列问题:
(1)A、B和C的金属活动性顺序为:______;
(2)举出符合上述金属活动性顺序的三种常见金属:______;
(3)上述实验事实可以给你的启示:
①______;
②______. 2743988651年前1
2743988651年前1 -
 感情盲流 共回答了10个问题
感情盲流 共回答了10个问题 |采纳率100%解题思路:在金属活动性顺序中,只有氢前的金属才可以置换出常见的稀酸溶液中的氢,生成氢气;而只有前面的金属可以把排在它后面的金属从盐溶液中置换出来.(1)根据题意可知,金属B能够和稀盐酸反应生成氢气,而C不反应,说明金属B在氢前,而C在氢后;而C能够置换出硝酸银溶液的银,而A不能,说明C的化学性质比银活泼,故A、B、C三种物质的金属活动性关系是B>C>A,
故答案为:B>C>A;
(2)由于金属B和稀盐酸反应时生成的是浅绿色溶液,说明金属B是Fe;C在氢后,而它的化学性质又比银活泼,且C为金属固体,因此C为金属Cu;A不能把银从盐溶液中置换出来,因此A可能为银、铂、金中的一种,
故答案为:Fe Cu Ag(合理即可);
(3)根据金属活动性顺序,可以判断反应的发生,根据反应的进行也可以验证金属的活动性顺序,
故答案为:
①在金属活动性顺序中,位于氢前面的金属能置换出盐酸、稀硫酸中的氢;
②位于前面的金属能把位于后面的金属从它们的盐溶液里置换出来.点评:
本题考点: 金属活动性顺序及其应用.
考点点评: 本题难度不是很大,主要考查了根据反应的发生来判断金属的活动性强弱,从而加深学生对金属活动性顺序的立解和应用.1年前查看全部
- 翡翠A货,总质量48.06g,形状,花件,颜色,浅绿色,折射率1.66点测,光性特征,非均质集合体,放大检查,粒状纤维交
翡翠A货,总质量48.06g,形状,花件,颜色,浅绿色,折射率1.66点测,光性特征,非均质集合体,放大检查,粒状纤维交织结构,备注红外检测见天然翡翠吸收峰.证书编号No .6913650642识别码No.50427323帮忙查下媲銶是真的吗?
 时都要1年前1
时都要1年前1 -
 男模先生 共回答了14个问题
男模先生 共回答了14个问题 |采纳率100%经查询得知
这是一只天然翡翠A货雕件
雕的是什么呢?看不太清楚
貔貅还是什么?
糯种 整体种水品相很一般
个头不小
但是无纹裂情况下
这物件 不超过300
有不明白的地方请继续追问1年前查看全部
- FeCl2溶液呈浅绿色,存在下列平衡 Fe+2 H20+ Fe(OH)2+2H 往溶液中滴加盐酸,发生的变化是
FeCl2溶液呈浅绿色,存在下列平衡 Fe+2 H20+ Fe(OH)2+2H 往溶液中滴加盐酸,发生的变化是
a.平衡逆向移动 B 平衡正向移动 C 溶液由浅绿变黄 D 溶液由浅绿变深绿
求每一个选项的详细讲解. wintrygirl1年前3
wintrygirl1年前3 -
 野性ff 共回答了16个问题
野性ff 共回答了16个问题 |采纳率93.8%平衡是逆向移动没错 Fe2+浓度增加也没错 但是深度是不增加的 因为此离子方程式 是水解方程式 水解的程度很小 你们老师应该讲过 所以本来是浅绿也不会变成深绿 就好像 一滴水进入大海 对大海没有任何的影响一样 楼主应该明白的 所以只能选A BCD都是错误的1年前查看全部
- 用化学用语回答下列问题:(1)将稀硫酸滴加到过量的铁粉中,可观察到有气泡产生,同时溶液由无色变成了浅绿色.①产生的气泡中
用化学用语回答下列问题:
(1)将稀硫酸滴加到过量的铁粉中,可观察到有气泡产生,同时溶液由无色变成了浅绿
色.①产生的气泡中含有的气体______;②反应后溶液中含有的金属离子是______.
(2)红宝石和蓝宝石的矿物材料(刚玉)的化学成分为氧化铝,氧化铝中铝的化合价为______. 蓝妮娅1年前1
蓝妮娅1年前1 -
 canna8586 共回答了15个问题
canna8586 共回答了15个问题 |采纳率93.3%铁与稀硫酸反应生成氢气和硫酸亚铁,所以产生的气泡是氢气,所含的金属离子是Fe 2+ .
铝只有一个价态,所以氧化铝中铝的化合价
+3
Al 2 O 3
故答案为:(1)H 2 ;Fe 2+ .
(2)
+3
Al 2 O 3 .1年前查看全部
- 初中各种化学物质或离子颜色比如说硫酸铁溶液是浅绿色,+3价的铁离子溶液时浅黄色之类的,有没有什么比较好的背诵口诀
 talcjt1年前6
talcjt1年前6 -
 大方哥 共回答了16个问题
大方哥 共回答了16个问题 |采纳率100%一、初中化学常见物质的颜色
(一)、固体的颜色
1、红色固体:铜,氧化铁
2、绿色固体:碱式碳酸铜
3、蓝色固体:氢氧化铜,硫酸铜晶体
4、紫黑色固体:高锰酸钾
5、淡黄色固体:硫磺
6、无色固体:冰,干冰,金刚石
7、银白色固体:银,铁,镁,铝,汞等金属
8、黑色固体:铁粉,木炭,氧化铜,二氧化锰,四氧化三铁,(碳黑,活性炭)
9、红褐色固体:氢氧化铁
10、白色固体:氯化钠,碳酸钠,氢氧化钠,氢氧化钙,碳酸钙,氧化钙,硫酸铜,五氧化二磷,氧化镁
(二)、液体的颜色
11、无色液体:水,双氧水
12、蓝色溶液:硫酸铜溶液,氯化铜溶液,硝酸铜溶液
13、浅绿色溶液:硫酸亚铁溶液,氯化亚铁溶液,硝酸亚铁溶液
14、黄色溶液:硫酸铁溶液,氯化铁溶液,硝酸铁溶液
15、紫红色溶液:高锰酸钾溶液
16、紫色溶液:石蕊溶液
(三)、气体的颜色
17、红棕色气体:二氧化氮
18、黄绿色气体:氯气
19、无色气体:氧气,氮气,氢气,二氧化碳,一氧化碳,二氧化硫,氯化氢气体等大多数气体.
二、初中化学溶液的酸碱性
1、显酸性的溶液:酸溶液和某些盐溶液(硫酸氢钠、硫酸氢钾等)
2、显碱性的溶液:碱溶液和某些盐溶液(碳酸钠、碳酸氢钠等)
3、显中性的溶液:水和大多数的盐溶液1年前查看全部
- 请问浅绿色的溶液是氯化亚铁溶液还是硫酸亚铁溶液?(是前者吗?)
 我哭了谁知道1年前1
我哭了谁知道1年前1 -
 2cif 共回答了21个问题
2cif 共回答了21个问题 |采纳率100%都是浅绿色1年前查看全部
- 翠鸟背上的羽毛像浅绿色的外衣.怎么照样子写打比方的句子?
翠鸟背上的羽毛像浅绿色的外衣.怎么照样子写打比方的句子?
还有一个问题,我们难道能离开太阳吗?把句子换一种说法,而句子的意思不变 hao8481年前2
hao8481年前2 -
 kelly1011 共回答了13个问题
kelly1011 共回答了13个问题 |采纳率69.2%我们不能离开太阳.
孔雀开屏像一把美丽的大扇子.1年前查看全部
- 在FeCl3和FeCl2的混合溶液中通入SO2气体,观察到有白色沉淀产生,并且溶液变为浅绿色,可以得出的结论是
在FeCl3和FeCl2的混合溶液中通入SO2气体,观察到有白色沉淀产生,并且溶液变为浅绿色,可以得出的结论是
在FeCl3和FeCl2的混合溶液中通入SO2气体,观察到有白色沉淀产生,并且溶液变为浅绿色,由此可以得出的结论是( )
A.白色沉淀是单质硫
B.白色沉淀是
C.白色沉淀是
D.三氯化铁被还原为绿化亚铁
不好意思,打错了。正确的题目是这样的:
在FeCl3和BaCl2的混合溶液中通入SO2气体,观察到有白色沉淀产生,并且溶液变为浅绿色,由此可以得出的结论是( )
A.白色沉淀是单质硫
B.白色沉淀是BaSO4
C.白色沉淀是BaSO3
D.三氯化铁被还原为绿化亚铁 xieqingfa1年前1
xieqingfa1年前1 -
 愁为心上秋 共回答了29个问题
愁为心上秋 共回答了29个问题 |采纳率89.7%发生的反应如下:
2Fe3+ + SO2 + 2H2O = 2Fe2+ + SO42- + 4H+
Ba2+ + SO42- = BaSO4↓
所以答案是BD
A不选,因为没有物质有足够的还原性,能将SO2还原到S单质.
C不选,因为在H+存在的非氧化性溶液中,是不可能生成BaSO3沉淀的.1年前查看全部
- SO2通入足量的Fe(NO3)3稀溶液中,溶液由棕色变为浅绿色,但立即又变成棕黄色,这时若滴入BaCl2溶液,会产生白色
SO2通入足量的Fe(NO3)3稀溶液中,溶液由棕色变为浅绿色,但立即又变成棕黄色,这时若滴入BaCl2溶液,会产生白色沉淀.针对上述一系列变化,下列说法不正确的是( )
A.假设通入的SO2完全反应,则同温同压下,SO2和逸出气体的体积比为1:1
B.从上述反应可以得出结论,氧化性:HNO3>Fe3+>稀硫酸
C.上述过程中,会产生一种无色难溶于水的气体
D.上述过程中,最终被还原的是NO3- 我能5881年前1
我能5881年前1 -
 zxp145 共回答了23个问题
zxp145 共回答了23个问题 |采纳率87%解题思路:根据滴入BaCl2溶液,则会产生白色沉淀,则具有还原性的SO2通入Fe(NO3)3溶液中发生了氧化还原反应,反应时硫元素的化合价升高被氧化为硫酸,铁元素化合价的变化可以依据现象判断,溶液由黄色变为浅绿色,但立即又变为黄色,三价铁离子变为亚铁离子,后又被氧化为三价铁离子,注意NO3-在酸性条件下具有强氧化性.A、上述过程中,最终被还原的是NO3-,故相当于二氧化硫与硝酸根离子之间的氧化还原,3SO2~2NO3-,之比为3:2,故A错误;
B、由溶液有棕色变为浅绿色,说明三价铁的氧化性强于稀硫酸,但在硝酸存在的前提下立即又变成棕黄色,说明亚铁迅速被氧化成铁离子,故硝酸的氧化性强三价铁,综上所述氧化性:HNO3>Fe3+>稀硫酸,故B正确;
C、硝酸根离子和二氧化硫被氧后产生的氢离子构成强氧化性体系,氧化亚铁时生成无色的难溶于水的一氧化氮气体,故C正确;
D、溶液由黄色变为浅绿色,但立即又变为黄色,三价铁离子变为亚铁离子,后又被氧化为三价铁离子,所以最终被还原的是NO3-,故D正确;
故选A.点评:
本题考点: 二氧化硫的化学性质.
考点点评: 本题考查氧化还原反应的综合应用,注意利用信息来判断发生的氧化反应,明确硝酸根离子在酸性条件下具有强氧化性是解答的关键,题目难度中等.1年前查看全部
- 新制氯水使FeCl2溶液由浅绿色变为棕黄色,为什么证明了有存在Cl2,而不是HClO?
新制氯水使FeCl2溶液由浅绿色变为棕黄色,为什么证明了有存在Cl2,而不是HClO?
亚铁离子和氯水中的次氯酸能反应吗? moonlightshadow_1年前1
moonlightshadow_1年前1 -
 kan3kan 共回答了14个问题
kan3kan 共回答了14个问题 |采纳率92.9%能反映,但不能把亚铁离子氧化成铁离子1年前查看全部
- 写出下列句子运用的修辞手法。1 .翠鸟背上的羽毛像浅绿色的外衣。( )
写出下列句子运用的修辞手法。
1 .翠鸟背上的羽毛像浅绿色的外衣。( )
2 .小鱼悄悄地把头露出水面,吹了个小泡泡。( )
3 .***圣地成了培养***青年的摇篮。( )
4 .一颗有生命的种子落在瓦砾里,它决不悲 观、决不叹气。( ) 煜荣1年前1
煜荣1年前1 -
 杨庆煌 共回答了25个问题
杨庆煌 共回答了25个问题 |采纳率84%1.比喻 2.拟人 3.比喻 4.拟人1年前查看全部
- 为研究某矿石成分,小涛做了下列实验:取一小块矿石加入稀盐酸中,反应后溶液呈浅绿色,同时生成无色气体,该气体是澄清石灰水变
为研究某矿石成分,小涛做了下列实验:取一小块矿石加入稀盐酸中,反应后溶液呈浅绿色,同时生成无色气体,该气体是澄清石灰水变浑浊.你认为此矿石主要成份为______(填名称),它与盐酸反应的化学方程式为______.  cwcrcwcr1年前1
cwcrcwcr1年前1 -
 书生凤凰 共回答了17个问题
书生凤凰 共回答了17个问题 |采纳率100%由题意可知:取一小块矿石加入稀盐酸中,反应后溶液呈浅绿色,说明了矿石中含有铁;由生成无色气体,该气体是澄清石灰水变浑浊,说明了矿石中含有碳酸根,综合以上分析,矿石主要成份为碳酸亚铁.碳酸亚铁与盐酸反应的方程式是:FeCO 3 +2HCl=FeCl 2 +2H 2 O+CO 2 ↑.
故答为:碳酸亚铁,FeCO 3 +2HCl=FeCl 2 +2H 2 O+CO 2 ↑.1年前查看全部
- 硫酸亚铁溶液久置于空气中,发现溶液由浅绿色逐渐变为黄褐色,并在容器的底部出现了褐色沉淀,则反应的离子方程式是?
 冰淇淋81年前2
冰淇淋81年前2 -
 qiudake 共回答了14个问题
qiudake 共回答了14个问题 |采纳率92.9%应该是
4Fe(2+)+O2+10H2O=4Fe(OH)3 (沉淀)+8H(+)1年前查看全部
- 某种含结晶水的浅绿色晶体a溶于水 取出少量溶液加入BaCl2溶液 生成不溶于酸的白色沉淀b 另取少量a溶液加入NaOH溶
某种含结晶水的浅绿色晶体a溶于水 取出少量溶液加入BaCl2溶液 生成不溶于酸的白色沉淀b 另取少量a溶液加入NaOH溶液 生成白色沉淀c c很快变色 最后变为红褐色d d溶于盐酸的e 再加入KSCN生成血红色的f离子
写出他们的化学式:a:b:c:d:e:f:
写出以下反应的离子方程式:
a→c:
c→d:
d→e:
e→f: 87685481年前1
87685481年前1 -
 小浏 共回答了23个问题
小浏 共回答了23个问题 |采纳率95.7%浅绿色晶体一般为FeSO4晶体,加入氯化钡得白色沉淀b ,b为硫酸钡,加入氢氧化钠后的现象是典型的亚铁离子生成氢氧化铁(白色)再在氧气作用下生成氢氧化铁(红褐色),氢氧化铁可溶于盐酸得氯化铁,三价铁加入KSCN得血红色溶液.
答案:
a:FeSO4·7H2O b:BSO4 c:Fe(OH)2 d:Fe(OH)3 e:FeCl3 f:Fe(SCN)2+
写出以下反应的离子方程式:
a→c:Fe2++2OH-=Fe(OH)2 ↓
c→d:4Fe(OH)2+O2+2H2O=4Fe(OH)3
d→e:Fe(OH)3 +3H+=Fe3++3H2O
e→f:Fe3++SCN-=Fe(SCN)2+(离子可溶于水,血红色)1年前查看全部
- 初中化学溶液颜色问题1红棕色固体 2黑色固体 3浅绿色溶液 4红棕色金属氧化物 还有初中常见的带颜色的溶液 谢谢
 bangzi31331年前13
bangzi31331年前13 -
 爱哭的小猪猪 共回答了17个问题
爱哭的小猪猪 共回答了17个问题 |采纳率88.2%1.氧化铁,2四氧化三铁3氯化亚铁溶液3氧化铁
紫色石蕊试液,无色酚酞试液,蓝色石蕊试液
= =1年前查看全部
- so2与Fecl3反应生成二价铁,是浅绿色,为什么so2不使他再从浅绿色变成无色
 老老老光棍1年前1
老老老光棍1年前1 -
 rqmildog 共回答了18个问题
rqmildog 共回答了18个问题 |采纳率88.9%这关系到SO2和亚铁离子的还原性强弱比较,SO2在遇铁离子时,还原性SO2大于三价铁,但与二价铁相遇时,亚铁离子的还原性与SO2相差无几,所以不再发生反应.(也就是亚铁离子不能再还原成单质铁)
而且更重要的是:铁在离子状态下只有二价和三价,没有无色的离子状态.SO2也不能再与二价铁化合生成无色的不稳定化合物.故此时溶液中亚铁离子与SO2共存.1年前查看全部
- 把镁条投入硫酸铜溶液中出现浅绿色絮状物
 158699591年前1
158699591年前1 -
 劫财不劫色 共回答了22个问题
劫财不劫色 共回答了22个问题 |采纳率95.5%你说是蓝绿色我还相信
因为CuSO4水解呈酸性,而Mg过於活泼,不仅跟Cu2+反应还跟水解得到的H+反应,促进了水解导致Cu2+变成Cu(OH)2析出1年前查看全部
- 化合物甲与单质X生成单质Y和化合物乙(1)若乙的溶液是浅绿色,Y是红色固体,则X是
化合物甲与单质X生成单质Y和化合物乙(1)若乙的溶液是浅绿色,Y是红色固体,则X是
化学方程式表达:
(2)在常温下若乙是气体,则X是----(用方程式表达):------
(3)在常温下若甲是固体,乙是无色液体,则X是:------
(化学方程式表达):------ 大漠银洲1年前4
大漠银洲1年前4 -
 modengai 共回答了21个问题
modengai 共回答了21个问题 |采纳率90.5%(1)X是Fe,CuSO4+Fe=FeSO4+Cu(任举一例)
(2)X是Fe(Al,Mg,Zn……),2HCl+Fe=FeCl2+H2
(3)X是H2,CuO+H2=Cu+H2O1年前查看全部
- 一道化学实验题,急①铁锈逐渐消失,溶液变为黄色②铁片表面有气泡生成,溶液由橙黄色逐渐变为浅绿色问:为弄清溶液由橙黄色变为
一道化学实验题,急
①铁锈逐渐消失,溶液变为黄色
②铁片表面有气泡生成,溶液由橙黄色逐渐变为浅绿色
问:为弄清溶液由橙黄色变为浅绿色的原因,小军猜想是否是铁与黄色溶液中的溶质发生了反应,请你设计出探究方案(简要写出实验内容) aaiid1年前2
aaiid1年前2 -
 屏幕背后 共回答了20个问题
屏幕背后 共回答了20个问题 |采纳率80%1、用FeCl3和NaOH制取氢氧化铁,将制得的氢氧化铁在空气中灼烧,值得纯净氧化铁,使纯净氧化铁与稀盐(硫)酸充分反应,发现溶液最终为橙黄色未变绿;(这步说明氧化铁和酸反应不能使溶液变绿)
2、把过量铁粉放入氯化(硫酸)铁中,充分反映后溶液由橙黄色变浅绿色;
这样就说明了铁和氯化(硫酸)铁发生了反应.1年前查看全部
- 请问微拟球藻在实验室培养中,若是生长良好会出现浅绿色、有点带白色的类似絮状物沉淀在培养瓶底部吗?
请问微拟球藻在实验室培养中,若是生长良好会出现浅绿色、有点带白色的类似絮状物沉淀在培养瓶底部吗?
我用的是海水BG-11培养基,请教微拟球藻在实验室中培养生长的正常形态描述,最好有图片!真的是谢谢啦!
 你美丽的1年前0
你美丽的1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 把一定量的二氧化硫通入硝酸铁溶液中,溶液由棕色变为浅绿色,但立即又变为棕黄色.被还原的是?
把一定量的二氧化硫通入硝酸铁溶液中,溶液由棕色变为浅绿色,但立即又变为棕黄色.被还原的是?
把一定量的二氧化硫通入硝酸铁溶液中,溶液由棕色变为浅绿色,但立即又变为棕黄色.此时若滴入氯化钡溶液,则会产生白色沉淀.最终被还原的是? 小昵子1年前1
小昵子1年前1 -
 悠扬琴声5577 共回答了16个问题
悠扬琴声5577 共回答了16个问题 |采纳率100%最终被还原的硝酸根
根据溶液棕色变为浅绿色,但立即又变为棕黄色可知三价铁把二氧化硫氧化 自身被还原成二价铁 然而这个过程使得溶液酸性提高(SO2+H2O+FE2+===H2SO4+FE3+) 酸性下的硝酸根强氧化性 把二价铁氧还 自身被还原 所以最终被还原的硝酸根1年前查看全部
- 离子反应存在问题某盐溶液呈浅绿色,进行如下实验1.取少量溶液加入KSCN,未见溶液变红2.往1中所得溶液中滴加氯水,溶液
离子反应存在问题
某盐溶液呈浅绿色,进行如下实验
1.取少量溶液加入KSCN,未见溶液变红
2.往1中所得溶液中滴加氯水,溶液立即变红,继续滴加氯水至一定体积时,溶液由红色变为棕黄色并有无色气体产生;气体通过足量澄清石灰水时,有白色沉淀产生,并仍有气体排出
3.取2溶液分别加入硝酸银和氯化钡溶液,均产生白色沉淀.则下列推论正确的是---
a 原溶液肯定有Fe2+ b 原溶液肯定有硫酸根
c 无色气体肯定不含二氧化硫 d 原溶液肯定没有氯离子
key:ac
与现象对应的都是什么离子? 折翼天使3131年前2
折翼天使3131年前2 -
 txj007855 共回答了21个问题
txj007855 共回答了21个问题 |采纳率85.7%溶液立即变红:是Fe2+被氧化成Fe3+并与SCN-反应生成[Fe(SCN)n]3-n变为血红色.
继续滴加氯水至一定体积时,溶液由红色变为棕黄色并有无色气体产生;气体通过足量澄清石灰水时,有白色沉淀产生,并仍有气体排出 :SCN-右被氯水氧化,变为二氧化碳和氮气,二氧化碳使澄清石灰水浑浊,剩余气体为氮气.1年前查看全部
- 往浅绿色的硝酸亚铁溶液中逐渐加稀盐酸,溶液的颜色应该是?
 lf_chun20001年前1
lf_chun20001年前1 -
 jjzhong2006 共回答了25个问题
jjzhong2006 共回答了25个问题 |采纳率88%变为棕黄色
因为加入盐酸,为硝酸亚铁溶液提供了氢离子,而酸化的硝酸根离子具有强氧化性,会氧化亚铁离子.亚铁离子变成铁离子,所以容易颜色变为三价铁离子的颜色,即棕黄色.1年前查看全部
- 溶液中由浅绿色变为黄色的化学反应方程式为
 thrsh1年前1
thrsh1年前1 -
 想嫁的女子 共回答了20个问题
想嫁的女子 共回答了20个问题 |采纳率85%2价铁粒子变成3价1年前查看全部
- 由硫酸铜与铁反应制得的浅绿色硫酸亚铁为什么一宿后变黄色了?
由硫酸铜与铁反应制得的浅绿色硫酸亚铁为什么一宿后变黄色了?
补:硫酸铜:常温下硫酸铜的饱和溶液; 铁:生铁; 硫酸亚铁:过滤了两次的硫酸亚铁. patrickgui1年前3
patrickgui1年前3 -
 lglmlj 共回答了22个问题
lglmlj 共回答了22个问题 |采纳率90.9%硫酸亚铁和空气中的氧气发生氧化反应,生成了硫酸铁,所以成黄色的了1年前查看全部
- 二价铁的颜色二价铁是绿色吗?是不是它与其他溶液发生反应,多数溶液都会变成浅绿色?稀盐酸和硫酸铜溶液和铁反应,那个铁都是二
二价铁的颜色
二价铁是绿色吗?
是不是它与其他溶液发生反应,多数溶液都会变成浅绿色?
稀盐酸和硫酸铜溶液和铁反应,那个铁都是二价的吧?
溶液是不是都是浅绿色了? lwj48821年前2
lwj48821年前2 -
 deancool 共回答了24个问题
deancool 共回答了24个问题 |采纳率83.3%通常情况下二价铁离子的溶液都是浅绿色的.
但是要考虑有无其他有颜色的离子的影响,例如如果含Cu离子,由于蓝色很深,有可能绿色不明显.
稀盐酸和铁反应,溶液是浅绿色
硫酸铜和铁反应,溶液是由蓝色逐渐转浅绿.1年前查看全部
- 往浅绿色的Fe(NO3)2溶液中逐滴加稀盐酸后,溶液的颜色变棕黄色.
往浅绿色的Fe(NO3)2溶液中逐滴加稀盐酸后,溶液的颜色变棕黄色.
能不能用有关方程式说明一下 平儿凡子1年前3
平儿凡子1年前3 -
 hlcb5201 共回答了25个问题
hlcb5201 共回答了25个问题 |采纳率92%3Fe2+ + 4H+ + NO3- ==3Fe3+ + NO + 2H2O1年前查看全部
- 请问往浅绿色的Fe(NO3)2溶液中逐滴加稀盐酸后,溶液的颜色变棕黄色.为什么?
请问往浅绿色的Fe(NO3)2溶液中逐滴加稀盐酸后,溶液的颜色变棕黄色.为什么?
最好详细点.谢谢.
 robinliu1年前1
robinliu1年前1 -
 13067153349 共回答了17个问题
13067153349 共回答了17个问题 |采纳率94.1%加入 HCL之后 其实是等于加入了 H离子 和CL离子,H离子和 水中的HNO3离子会结合形成HNO3 而HNO3是具有氧化性的 ,这样 就把原来的2价FE离子氧化成3价FE离子,而3价FE离子是棕黄色的.1年前查看全部
- 往浅绿色的Fe(NO3)溶液中逐滴加入稀盐酸,溶液的颜色变化应是?
往浅绿色的Fe(NO3)溶液中逐滴加入稀盐酸,溶液的颜色变化应是?
A颜色变浅 B逐渐变红色 C没有改变 D变棕黄色 小涛很淘气1年前1
小涛很淘气1年前1 -
 wenkeshanew 共回答了19个问题
wenkeshanew 共回答了19个问题 |采纳率100%选D,Fe2+和NO3-在溶液中可以大量共存,但加入盐酸后,NO3-在酸性条件下表现出强氧化性,(即可认为H+与NO3-结合成HNO3)把Fe2+氧化成了Fe3+ 所以溶液由浅绿色变成了棕黄色1年前查看全部
- 含有硝酸银的液体中加入铁屑,锌屑后,得到固体和浅绿色滤液,滤液中溶质的组成有何物质
 JEFH1年前2
JEFH1年前2 -
 ystmxw 共回答了21个问题
ystmxw 共回答了21个问题 |采纳率85.7%固体 银、铁
浅绿色溶液:Fe2+、Zn2+1年前查看全部
- 写出向浅绿色的Fe(NO3)2溶液中逐滴加入少量稀盐酸时的化学方程式
写出向浅绿色的Fe(NO3)2溶液中逐滴加入少量稀盐酸时的化学方程式
不要写离子式 srtnjs361年前3
srtnjs361年前3 -
 Polaris82 共回答了16个问题
Polaris82 共回答了16个问题 |采纳率93.8%写化学方程式很无聊 应该有很多种 给你提供一个
9Fe(NO3)2+12HCL=====5Fe(NO3)3+4FECL3+3NO+6H2O1年前查看全部
- 主要记什么物质的颜色?如硫酸亚铁溶液为浅绿色硫酸铁溶液为黄色C 为黑色Fe 为银白色还有很多!物质 颜色?记目前我知道的
主要记什么物质的颜色?
如硫酸亚铁溶液为浅绿色
硫酸铁溶液为黄色
C 为黑色
Fe 为银白色
还有很多!物质 颜色?
记
目前我知道的 Cu 紫红色 Fe 银白色 C 黑色 Mg 白色 CuSO4溶液 蓝色 硫酸亚铁溶液 浅绿色 硫酸铁溶液 黄色 四氧化三铁 黑色 三氧化二铁 红色 氧化铜 黑色!还要记点什么其他的吗? whiskeycd1年前2
whiskeycd1年前2 -
 chongrubujing 共回答了15个问题
chongrubujing 共回答了15个问题 |采纳率93.3%硫酸铜 蓝 铜 红 碳酸钙 氯化银 硫酸钡 白 四氧化三铁 黑1年前查看全部
- 我在浅绿色硫酸亚铁溶液中加入氢氧化钠后,白色沉淀很快变成绿色但是最终没有变成棕红色,
 SYSCO131年前2
SYSCO131年前2 -
 昊瀚心旅2 共回答了16个问题
昊瀚心旅2 共回答了16个问题 |采纳率75%把NaOH加至过量,再看看.二价铁离子一般颜色都是浅绿的,就像绿色玻璃里面也是二价铁的颜色.开始时白色?那估计是反应的中间色哈.最终没有成为红棕色 那是时间不够.你想快点看到的话不妨多摇摇 或者把溶液吸点出来,平铺在烧杯底部.这样应该能快点.变色.实在慢,你加加热同时摇晃烧杯.1年前查看全部
- (2006•赤峰)把一根洁净的铁钉放在稀硫酸中:①在铁钉表面产生气泡;②溶液由无色逐渐变为浅绿色;③铁钉的质量减少;④溶
(2006•赤峰)把一根洁净的铁钉放在稀硫酸中:①在铁钉表面产生气泡;②溶液由无色逐渐变为浅绿色;③铁钉的质量减少;④溶液的质量增加.以上叙述正确的是( )
A.①②③
B.①②③④
C.①④
D.①③④ 最后的四首歌1年前1
最后的四首歌1年前1 -
 yxl830316 共回答了26个问题
yxl830316 共回答了26个问题 |采纳率84.6%解题思路:洁净的铁钉主要成分是铁,铁能与稀硫酸反应生成氢气和硫酸亚铁,利用这个反应的现象解决此题.铁能与稀硫酸反应生成氢气和硫酸亚铁,硫酸亚铁的溶液是浅绿色的,而铁与硫酸反应时由于生成的氢气质量远远小于反应的铁的质量,所以溶液质量会增加,综合以上信息可得答案.
故选B点评:
本题考点: 金属的化学性质;酸的化学性质.
考点点评: 此题是对生锈铁钉与稀硫酸反应的考查,解题的关键是要知道发生了两个相关联的反应,并知道其反应的现象.1年前查看全部
- 求初中化学常见单质、氧化物、酸、碱、盐、有机物、黑色固体、红色固体、蓝色固体、黄色固体、浅绿色固体、紫色固体
求初中化学常见单质、氧化物、酸、碱、盐、有机物、黑色固体、红色固体、蓝色固体、黄色固体、浅绿色固体、紫色固体
答的好可以再加分 宝宝rabbit1年前2
宝宝rabbit1年前2 -
 蝶恋花开 共回答了19个问题
蝶恋花开 共回答了19个问题 |采纳率89.5%单质:稀有气体、氧气(O2)、氮气(N2),S、P、Mg、Cu、Fe等.
氧化物:CuO、FeO、Fe2O3、Fe3O4、CO2、SO2等
酸:HCI、H2SO4、HNO3
碱:NaOH、Ca(OH)2、NH3*H2O(氨水)等
盐:Na2CO3、CuSO4、NH4CI、NaCI等
有机物:CH4(甲烷)、C6H12O6(葡萄糖)、C2H5OH(酒精)、CH3COOH(醋酸)
1、红色固体:铜,氧化铁
2、绿色固体:碱式碳酸铜
3、蓝色固体:氢氧化铜,硫酸铜晶体
4、紫黑色固体:高锰酸钾
5、淡黄色固体:硫磺
6、无色固体:冰,干冰,金刚石
7、银白色固体:银,铁,镁,铝,汞等金属
8、黑色固体:铁粉,木炭,氧化铜,二氧化锰,四氧化三铁,(碳黑,活性炭)
9、红褐色固体:氢氧化铁
10、白色固体:氯化钠,碳酸钠,氢氧化钠,氢氧化钙,碳酸钙,氧化钙,硫酸铜,五氧化二磷,氧化镁1年前查看全部
- 有一结晶水合物X•6H2O,其水溶液为浅绿色,可发生如图的转化(部分反应物、生成物从略).其中B、D、E、F均为无色气体
有一结晶水合物X•6H2O,其水溶液为浅绿色,可发生如图的转化(部分反应物、生成物从略).其中B、D、E、F均为无色气体,G为难溶于水的红褐色固体.在A溶液中加入BaCl2溶液可生成不溶于稀盐酸的白色沉淀.
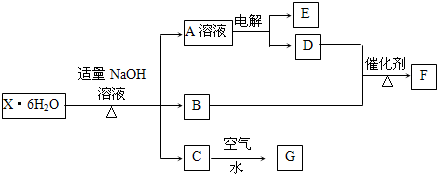
请回答下列问题:
(1)指出C→G的基本反应类型:______反应.
(2)用惰性电极电解溶液A时得到E的电极反应式为______.
(3)B与D反应生成F的化学方程式为4NH3+5O2
4NO+6H2O催化剂 .△ 4NH3+5O2.
4NO+6H2O催化剂 .△
(4)该晶体水合物的化学式为______. 风中的秋虫1年前1
风中的秋虫1年前1 -
 huahuazhang 共回答了26个问题
huahuazhang 共回答了26个问题 |采纳率84.6%解题思路:X的水溶液为浅绿色,说明X含有亚铁离子,碱性条件下生成的B为NH3,G为难溶于水的红褐色固体,应为Fe(OH)3,
则C为Fe(OH)2,在A溶液中加入BaCl2溶液可生成不溶于稀盐酸的白色沉淀,说明X中含有SO42-,应为Na2SO4溶液,电解生成氢气和氧气,能与氨气反应的D为O2,则E为H2,F为NO,结合对应物质的性质以及题目要求解答该题.X的水溶液为浅绿色,说明X含有亚铁离子,碱性条件下生成的B为NH3,G为难溶于水的红褐色固体,应为Fe(OH)3,则C为Fe(OH)2,在A溶液中加入BaCl2溶液可生成不溶于稀盐酸的白色沉淀,说明X中含有SO42-,应为Na2SO4溶液,电解生成氢气和氧气,能与氨气反应的D为O2,则E为H2,F为NO,
(1)由以上分析可知C→G的反应为氢氧化亚铁的氧化反应,反应的方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,为化合反应,故答案为:化合;
(2)用惰性电极电解溶液A时得到E的电极反应式为阴极反应生成氢气,电极方程式为2H++2e-=H2↑,故答案为:2H++2e-=H2↑;
(3)B与D反应生成F的反应为氨气的催化氧化,化学方程式为4NH3+5O2
催化剂
.
△4NO+6H2O,故答案为:4NH3+5O2
催化剂
.
△4NO+6H2O;
(4)由以上分析可知X中含有NH4+、Fe2+和SO42-,应为(NH4)2Fe(SO4)2•6H2O,故答案为:(NH4)2Fe(SO4)2•6H2O.点评:
本题考点: 无机物的推断.
考点点评: 本题考查无机物的推断,侧重于学生的分析能力的考查,为高考常见题型和高频考点,注意把握物质的特性以及用途,为推断题目的突破口,明确物质的种类为解答该题的关键,难度中等,注意物质的性质的学习.1年前查看全部
- 现榨的苹果汁在空气中会由浅绿色变成棕黄色,猜测其可能原因是( )
现榨的苹果汁在空气中会由浅绿色变成棕黄色,猜测其可能原因是( )
A.苹果汁中的正2价的Fe变成正3价的Fe
B.苹果汁中有正2价的铜
C.苹果汁中有负1价的OH
D.苹果汁中有正1价的Na wangkun1281年前1
wangkun1281年前1 -
 yiuben 共回答了22个问题
yiuben 共回答了22个问题 |采纳率86.4%选A,因为二价铁是浅绿色的,三价铁是棕黄色的1年前查看全部
- 有难度.一种黑色粉末A,加入盐酸后,粉末溶解得到浅绿色溶液,且有气体放出.将气体通入硫酸铜溶液产生黑色沉淀.在浅绿色溶液
有难度.
一种黑色粉末A,加入盐酸后,粉末溶解得到浅绿色溶液,且有气体放出.将气体通入硫酸铜溶液产生黑色沉淀.在浅绿色溶液中滴入氯水,溶液转为棕黄色,写出以上实验中各步反应的化学方程式. 我是真真1年前5
我是真真1年前5 -
 applede3233 共回答了13个问题
applede3233 共回答了13个问题 |采纳率92.3%FeS+2HCL=FeCL2+H2S(气体)
H2S+CuSO4=CuS(沉淀)+H2SO4
2FeCL2+CL2=2FeCL31年前查看全部
大家在问
- 1请按下列题目的要求完成作图:(1)将图甲中的光路图补充完整(2)作出图乙中平面镜镜面所在的位置(3)一束光从空气斜射向水
- 2改正下列句中的错别字。(1)流经小白杨树林时,溪水融融像一个湖,然后集中向一个角落…… (____改为____)(2)小
- 3父亲今年比儿子大30岁,3年后,父亲的年龄是儿子的4倍,儿子今年多少岁?
- 4l have a headache my nose____
- 5She__ __milk__ __.(填单词)
- 6谢太傅寒雪日内集是什么古汉语句式?还有白雪纷纷何所似.
- 7的规则填空 (1)1 3 3 9 ( ) 81 ( ).
- 8Your browser does not support the canvas element
- 9甲行走的速度相当于乙的[3/2]倍,两人分别从A、B两地同时出发,如果相向而行1小时相遇,那么同向而行(乙在前甲在后),
- 101、they were all pleased with ( )them
- 11关于感叹句在英文的感叹句里面,有没有以下的说法:how + adj/adv + 名词+主谓比如说:how lovely
- 12我是《夸父逐日》反方,该如何辩论夸父最太阳的行为是自不量力的?
- 13医生检查视力时,人眼与视力表应相距5m,但某眼科室两墙间隔只有3m,于是医生在挂视力表的对面墙上挂一块平面镜,则被检查者
- 14He's wearing a red shirt.(对划线部分提问)Beef comes from cows.(对划线部
- 15烯醇的结构式