回收再利用生锈的铁制品是保护金属资源的一种有效途径.某废铁粉中Fe2O3含量大约在80%左右(其余20%为铁)
 skyhappy5552022-10-04 11:39:541条回答
skyhappy5552022-10-04 11:39:541条回答回收后在工业上常用一氧化碳将其还原若回收100t这样的废铁粉可以得到 t铁.

已提交,审核后显示!提交回复
共1条回复
 celiaway1006 共回答了12个问题
celiaway1006 共回答了12个问题 |采纳率58.3%- Fe2O3+3CO=高温=2Fe+3CO2
160 112
100t*80% x
160/112=100t*80%/x
x=56t
所以用一氧化碳将其还原若回收100t这样的废铁粉可以得到56t铁. - 1年前
相关推荐
- (2009•道外区一模)电镀厂的废水中含有AgNO3和Cu(NO3)2为回收金属Cu和Ag.有下列操作.试回答:
(2009•道外区一模)电镀厂的废水中含有AgNO3和Cu(NO3)2为回收金属Cu和Ag.有下列操作.试回答:
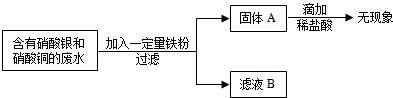
(1)固体A中一定含______
(2)确定滤液B中溶质化学式有多种情况.你认为有(填化学式):______. mrfish_111年前1
mrfish_111年前1 -
 超级女生牌nn 共回答了18个问题
超级女生牌nn 共回答了18个问题 |采纳率94.4%解题思路:根据回收流程图,过滤后固体A滴加稀盐酸无现象,说明固体中不含铁粉,即铁全部反应;废水为AgNO3和Cu(NO3)2混合溶液,由于金属铜的活动性大于银,铁粉先与AgNO3反应置换出银,银全部置换后再与Cu(NO3)2反应置换铜.(1)铁全部反应时固体A有四种可能:
①铁粉恰好与废水中的AgNO3和Cu(NO3)2完全反应,固体A为Cu、Ag混合物;
②铁粉恰好只与废水中的AgNO3完全反应,固体A为Ag;
③铁粉未能完全反应废水中的AgNO3,固体A为Ag;
④铁粉未能完全反应废水中Cu(NO3)2而完全反应的AgNO3,固体A为Cu、Ag.综合以上分析,固体A中一定含有金属Ag;
故选Ag;
(2)若Fe粉恰好与混合溶液完全反应,则AgNO3和Cu(NO3)2全部反应,滤液中不含这两种物质,滤液为Fe(NO3)2溶液;若Fe粉不足且恰好与混合溶液中的AgNO3完全反应,滤液中不含这种物质,滤液为Cu(NO3)2、Fe(NO3)2溶液;若Fe粉不足且未能把混合溶液中的AgNO3完全反应,滤液中仍含这种物质,滤液为AgNO3、Cu(NO3)2、Fe(NO3)2溶液;
故答:Fe(NO3)2,Cu(NO3)2、Fe(NO3)2,AgNO3、Cu(NO3)2、Fe(NO3)2.点评:
本题考点: 金属的化学性质;金属活动性顺序及其应用.
考点点评: 金属与盐的混合溶液或盐与酸的混合溶液发生反应时,根据金属活动性从小到的大顺序依次反应.1年前查看全部
- 某文具店出售一种电子辞典,每售出一台可获得利润15元,售出[4/5]后,为了尽快回收资金,每台降价3元出售,当全部售完后
某文具店出售一种电子辞典,每售出一台可获得利润15元,售出[4/5]后,为了尽快回收资金,每台降价3元出售,当全部售完后,共获利润864元.文具店共卖出这种电子辞典多少台?
 陈零LOVE1年前3
陈零LOVE1年前3 -
 zjjzqllq 共回答了15个问题
zjjzqllq 共回答了15个问题 |采纳率86.7%解题思路:解答此题时应先设共卖出这种辞典X台,然后根据降价前获得的利润+降价后获得的利润=864列出方程解答即可.设文具店共卖出这种辞典X台.
[4/5]X×15+(1-[4/5])X×(15-3)=864,
12X+[12/5]X=864,
X=60;
答:文具店共卖出这种辞典60台.点评:
本题考点: 分数四则复合应用题.
考点点评: 解答此题时应先设共卖出这种辞典X台,再找出等量关系式:降价前获得的利润+减价后获得的利润=864列出方程解答即可.1年前查看全部
- 某工厂的废液中含有较多的铜离子,铁离子,锌离子,如何回收铜,并得到氯化亚铁.第一步加金属,再加盐酸.
 uu才子1年前1
uu才子1年前1 -
 zxszxs35849 共回答了17个问题
zxszxs35849 共回答了17个问题 |采纳率100%先加金属锌置换出铁和铜的混合物,然后向混合物中加入稀盐酸溶解铁.因为铜不能被稀盐酸所溶解,所以最终获得的溶液为氯化亚铁溶液,剩余金属为铜.1年前查看全部
- 一定条件下发生下列反应可实现燃煤烟气中硫的回收:SO2(g)+2CO(g) 催化剂 .&
一定条件下发生下列反应可实现燃煤烟气中硫的回收:SO2(g)+2CO(g)
2CO2(g)+S(l)△H<0,若反应在恒容的密闭容器中进行,下列有关说法正确的是( )催化剂 .
A.平衡前,随着反应的进行,容器内的压强始终不变
B.平衡时,其他条件不变,分离出硫,正反应速率加快
C.平衡时,其他条件不变,使用合适的催化剂,可提高SO2的转化率
D.其他条件不变,使用不同催化剂,该反应的平衡常数不变 江南好之宝贝1年前1
江南好之宝贝1年前1 -
 理想的小树苗 共回答了14个问题
理想的小树苗 共回答了14个问题 |采纳率100%解题思路:该可逆反应正反应是气体体积减小、放热反应,在反应达到平衡之前,容器内气体的压强在不断减小,分离出液体硫,不影响平衡移动,反应速率不变,使用催化剂只改变化学反应速率但不影响平衡的移动,注意平衡常数只与温度有关,与物质的浓度无关.A.该反应是一个反应前后气体体积减小、放热的可逆反应,在反应达到平衡之前,随着反应的进行,气体的物质的量逐渐减小,则容器的压强在逐渐减小,故A错误;
B.硫是液体,分离出硫,不影响平衡移动,气体反应物和生成物浓度都不变,所以不影响反应速率,故B错误;
C.平衡时,其他条件不变,使用合适的催化剂,不影响平衡移动,不能提高SO2的转化率,故C错误;
D.平衡常数只与温度有关,与使用催化剂无关,故D正确;
故选D.点评:
本题考点: 化学平衡建立的过程.
考点点评: 本题考查了影响化学平衡的因素,难度不大,易错选项是B,注意固体和纯液体改变用量对反应速率无影响,催化剂只影响反应速率不影响平衡的移动.1年前查看全部
- 拜托大家看下低压注塑料PMMA怎么样回收再利用?
 asdgkjhawgsrthdf1年前1
asdgkjhawgsrthdf1年前1 -
 154191763 共回答了21个问题
154191763 共回答了21个问题 |采纳率81%唯的么他的个,
的阔视野阅沧桑,读书的中沁墨香
他们在青中岁一中
我就是你的那泪光
为么·在暮色来临的后1年前查看全部
- 用10千克废纸能生产好纸7千克.照这样计算,废品回收站回收废纸780千克,可以生产好纸多少千克?
 annie19901年前1
annie19901年前1 -
 辉色世界 共回答了17个问题
辉色世界 共回答了17个问题 |采纳率88.2%好纸=780÷10×7=546千克1年前查看全部
- 某化学兴趣小组回收利用废旧干电池.
某化学兴趣小组回收利用废旧干电池.
实验1:回收填料中的二氧化锰和氯化铵
查阅资料:废旧干电池填料的主要成分为二氧化锰、炭粉、氯化铵和氯化锌等,其中氯化铵、氯化锌可溶于水.兴趣小组的同学们设计回收物质的流程如图1所示.
(1)操作1和操作2的名称都是______,该操作中玻璃棒的作用是______.
(2)灼烧滤渣l的目的是______.
实验2:利用外壳回收物锌制取氢气及相关探究
(3)用锌和稀硫酸制取氢气.己知氢气密度比空气小且难溶于水,提供装置如图2.
①应选择:发生装置为______(填编号),排空气法收集装置为______(填编号).
②若用排水法收集并测定气体的体积,气体从装置B导管口______(填“a”或“b”) 进;选用仪器F测量排出水的体积,仪器F名称是______.
(4)探究影响锌与稀硫酸反应快慢的因素.反应过程中,用前10min内收集的氢气体积比较反应的快慢.控制其他条件相同,进行下表四组实验,获得数据如表.
①比较实验a和实验b,可以得到的结论是______.验实号编 试剂 前 10min 内产生的氢气体积(mL) 不同纯度的锌 不同体积和浓度的稀硫酸 a 纯锌 30mL 30% 564.3 b 含杂质的锌 30mL 30% 634.7 c 纯锌 30mL 20% 449.3 d 纯锌 40mL 30% 602.8
②为了研究硫酸浓度对反应快慢的影响,需比较实验______和实验______(填编号).
③控制其他条件相同,需控制的条件是______(列举一种条件即可). 依淮听风1年前1
依淮听风1年前1 -
 又是一天_002 共回答了14个问题
又是一天_002 共回答了14个问题 |采纳率92.9%解题思路:(1)根据操作1分离混合物的状态及过滤可用于难溶性固体和可溶性固体的分离进行分析;
(2)根据碳和氧气反应生成二氧化碳进行解答;
(3)根据锌粒和稀硫酸制取氢气属于固体和液体混合制取气体且不需要加热以及氢气的密度比空气的密度小进行解答;
(4)①通过表格比较实验的相同点和不同点得出结论;
②利用控制变量法分析自变量是硫酸的浓度,因变量是反应的快慢进行分析选择对比组;
③从外因寻找需要控制的条件:温度,颗粒大小等.(1)根据流程图操作1和2都是不溶性固体和液体的分离,因此是过滤操作,过滤时玻璃棒起到引流的作用;
(2)因为废旧干电池填料的主要难溶性物质为二氧化锰、炭粉,因此溶解过滤后的滤渣含有二氧化锰和碳粉,而回收二氧化锰,因此通过灼烧可以把碳粉变成二氧化碳,因此灼烧滤渣l的目的是除去碳粉;
(3)用锌和稀硫酸制取氢气,因此发生装置属于固液常温型的B装置;因为氢气密度比空气小且难溶于水,因此可以采用排水法或向下排空气法收集;
排水法收集时导管要短进长出才能排出装置中的水;
(4)①实验a和实验b,相同点是同体积同浓度的稀硫酸,不同点是含杂质的锌和纯锌,结果含杂质的锌比纯锌反应速率要快;
②要研究硫酸浓度对反应快慢的影响,需要不同浓度的硫酸,而要控制锌的纯度相同,比较产生氢气的快慢,因此对比组是a和c;
③控制变量法需要考虑的是自变量和因变量,而其它外界条件均保存相同,因此控制其他条件相同,需控制的条件如;温度(或锌粒形状大小).
故答案为:(1)过滤;引流;
(2)除去炭粉;
(3)B;D;b;量筒;
(4)①与同体积同浓度的稀硫酸反应,含杂质的锌比纯锌反应速率要快;②a;c;③温度.点评:
本题考点: 混合物的分离方法;影响化学反应速率的因素探究;量气装置;过滤的原理、方法及其应用;氢气的制取和检验.
考点点评: 本题考查了废电池的物质的回收及有关氢气的制取的探究,知识点较多,属于化学实验基本实验技能的考查,要求在平时的学习中要注意掌握常见的化学操作及其原理,熟练运用.1年前查看全部
- 神舟号飞船发射回收过程,及其原理
神舟号飞船发射回收过程,及其原理
物理研究性课题. 草莽人生1年前1
草莽人生1年前1 -
 tangyar 共回答了14个问题
tangyar 共回答了14个问题 |采纳率78.6%详细只给这么点分?
我简单说说吧
首先发射后,开始慢慢调整姿态,从垂直地面逐渐到平行地面飞行,期间助推器依次分离.
最终平衡时,高度和达到平衡后就算是成功发射和到达预定轨道了.
回收时飞船用火箭前前进方向喷射,形成反冲,降低速度,离心趋势变弱,地心吸力的影响逐渐增强,飞船向地面下路,最后进入大气后打开降落伞然后落地.
你问问题最后范围小点,你这问题的范围足够作为博士后论文的研究范围了1年前查看全部
- 现有一含Ba2+ Mg2+ Na+ Cl- I2 的溶液 欲将Ba2+ Mg2+除去 回收NaCl I2
现有一含Ba2+ Mg2+ Na+ Cl- I2 的溶液 欲将Ba2+ Mg2+除去 回收NaCl I2
设计实验方案!
能不能详细一点!比如说第一步 用XXXX除掉Ba 第二步............... huang_zb1年前1
huang_zb1年前1 -
 weigo535 共回答了12个问题
weigo535 共回答了12个问题 |采纳率75%先向溶液中加入过量氢氧化钡,除去镁离子,再加过量的碳酸钠,除去钡离子,过滤,然后加入适量的盐酸(适量的标准:滴加到无气泡产生即可,刚开始无现象,酸会先跟碱反应)
补充:碱溶于水的只有铵、钾、钠、钡、钙,所以楼上的加氢氧化钠除去钡离子是错的!1年前查看全部
- 卫星回收仓返回大气先变加速,最后匀速运动.若回收仓质量为m,空气阻力大小与速率关系:F=kv^2,求收尾速
卫星回收仓返回大气先变加速,最后匀速运动.若回收仓质量为m,空气阻力大小与速率关系:F=kv^2,求收尾速
收尾速率为卫星回收仓的,收尾速率即最终匀速运动的速率 达瓦2101年前1
达瓦2101年前1 -
 uu12 共回答了19个问题
uu12 共回答了19个问题 |采纳率63.2%当匀速是,重力等于阻力
有mg = KV^2
得V = sqr(mg/K)1年前查看全部
- 一个垃圾处理厂平均每天收到70车生活垃圾,每车垃圾重3吨,平均每车垃圾中可回收在再利用的约是三分之一吨
一个垃圾处理厂平均每天收到70车生活垃圾,每车垃圾重3吨,平均每车垃圾中可回收在再利用的约是三分之一吨
15天收到了多少垃圾 疯鱼象1年前1
疯鱼象1年前1 -
 夏天来了吗 共回答了16个问题
夏天来了吗 共回答了16个问题 |采纳率75%15*70*3*三分之一=1050(吨)1年前查看全部
- 一棵大树一年大约可以吸收二氧化碳200分之9t.回收1吨废纸大约可以少砍17棵大树,
一棵大树一年大约可以吸收二氧化碳200分之9t.回收1吨废纸大约可以少砍17棵大树,
金星小学全校师生一个学期共回收废纸17分之9t.
(1)回收这些废纸可以少砍多少棵大树?
(2)这些大树一年可以吸收二氧化碳多少吨? villiams1年前1
villiams1年前1 -
 罗纳这多 共回答了13个问题
罗纳这多 共回答了13个问题 |采纳率84.6%您回收的纸与大树的关系基本可以忽略,还是从技术革命的角度支持环保吧!1年前查看全部
- 有关电池的详细分类和回收办法每种电池如何分类?每种电池对环境的危害各有哪些?有没有可降解电池?
 zs65191年前1
zs65191年前1 -
 4cevr 共回答了19个问题
4cevr 共回答了19个问题 |采纳率89.5%现今的各种电池1.化学电池化学电池,是指通过电化学反应,把正极、负极活性物质的化学能,转化为电能的一类装置.经过长期的研究、发展,化学电池迎来了品种繁多,应用广泛的局面.大到一座建筑方能容纳得下的巨大装置,小到...1年前查看全部
- 化学题 帮帮我吧有一些工业废水 大多是FeSO4 还有Cu离子 少量Na离子 要废水回收FeSO4 和Cu离子 在方框和
化学题 帮帮我吧
有一些工业废水 大多是FeSO4 还有Cu离子 少量Na离子 要废水回收FeSO4 和Cu离子 在方框和括号内填物质名称或化学式 和操作方法
---( ) → 加入( )I ---- ( )
↑ 操作( )I
I I ----( )
工业废水→ I ↑ ---------FeSO4·7H2O
I →( )----------------------------------- ↑ 操作( )
实在对不起各位 太穷了 千万帮帮我啊
 南北距离1年前1
南北距离1年前1 -
 vinceshow 共回答了15个问题
vinceshow 共回答了15个问题 |采纳率100%在一些工业废水中,加过量的Fe,过滤,得到滤液和沉淀Cu、Fe,将沉淀溶于过量的稀硫酸,过滤出Cu,将滤液与上述滤液合并,将滤液蒸发浓缩、冷却结晶,得FeSO4·7H2O1年前查看全部
- 下图是一组垃圾箱及说明: 生活垃圾分类 可回收垃圾 不可回收垃圾 有害垃圾 1. 纸类2. 玻
下图是一组垃圾箱及说明: 生活垃圾分类 可回收垃圾 不可回收垃圾 有害垃圾 1. 纸类2. 玻
下图是一组垃圾箱及说明:
(1)小明在整理房间时,清理出如下物品,A.废作业本;B.可乐易拉罐;C.生锈铁钉;D.矿泉水瓶;E.烂苹果;F.涂改液瓶;G.废布料,它们应分别放入哪个垃圾箱(填序号):生活垃圾分类 可回收垃圾 不可回收垃圾 有害垃圾 1. 纸类
2. 玻璃
3. 金属
4. 塑料
5. 橡胶
6. 纺织品1. 厨房垃圾
2. 灰土
3. 杂草
4. 枯枝
5. 花卉1. 日光灯
2. 电池
3. 喷雾罐
4. 指甲油瓶
5. 药品瓶
6. 涂改液瓶
应放入“可回收垃圾箱”的是:______.
应放入“不可回收垃圾箱”的是:______.
应放入“有害垃圾箱”的是:______.
(2)小明用盐酸除去铁钉上的锈(主要成分为氧化铁),以便重新使用它,请写出除铁锈的化学方程式______.
(3)世界卫生组织把铝确定为食品污染源之一并加以控制使用,在①制铝合金;②制电线;③制餐饮具;④制银色漆的原料;⑤制装饮料的易拉罐;⑥包装糖果和小食品中,应加以控制使用的是______(填序号)
(4)解决“白色污染”问题,下列做法不宜提倡的是______
A.使用新型可降解塑料 B.用布袋代替塑料袋C.回收废弃塑料 D.焚烧废弃塑料
(5)检验一块废布料中是否含有羊毛成分的方法是______.
(6)环境问题的重要性也成为各国申办奥运会的注意点,各国纷纷打出“环境”牌,并且放在第一位.北京为申办2008年奥运会提出申办的三个理念:人文奥运、科技奥运、______.
 WY2191年前1
WY2191年前1 -
 ffgrj 共回答了21个问题
ffgrj 共回答了21个问题 |采纳率95.2%(1)A、废作业本属于纸类,为可回收垃圾;B、可乐易拉罐属于金属材料,为可回收垃圾;C、生锈铁钉属于金属材料,为可回收垃圾;D、矿泉水瓶属于塑料制品,为可回收垃圾;E、烂苹果属于厨房垃圾,为不可回收垃圾;F、涂改液瓶属于有害垃圾;G、废布料为可回收垃圾.
(2)氧化铁能与盐酸反应生成氯化铁和水,反应的化学方程式为:Fe2O3+6HCl=2FeCl3+3H2O.
(3)①制铝合金用于制炊具外的材料,这些材料不会直接接触消化系统,不必控制使用;
②制电线,电线不会直接接触消化系统,难以被吸收,不必控制使用;
③制餐饮具,一定有部分铝元素通过食物进入人体,必须控制使用;
④银色油漆不会直接接触消化系统,难以被吸收,不必控制使用;
⑤用铝易拉罐,饮料中会含有铝元素,其中的铝元素会随饮料喝进人体内,必须控制使用;
⑥用铝包装糖果和小食品,铝会污染糖果和小食品,食品中的铝元素通过食物进入人体,必须控制使用.
(4)A、使用新型可降解塑料能减少白色污染,做法宜提倡;B、用布袋代替塑料袋能减少塑料袋的使用,可以减少白色污染,做法宜提倡;C、回收废弃塑料能减少白色污染,做法宜提倡;D、焚烧废弃的塑料易生成有害气体,造成空气污染,做法不宜提倡.
(5)羊毛燃烧时会产生焦羽毛味,这也是检验羊毛存在的最简单的方法.
(6)北京在申办2008年奥运会时提出了“科技奥运、人文奥运、绿色奥运”的口号.
故答案为:(1)A、B、C、D、G;E;F;(2)Fe2O3+6HCl=2FeCl3+3H2O;(3)③、⑤、⑥;(4)D;(5)将其燃烧,闻是否有烧焦头发的气味;(6)绿色奥运.1年前查看全部
- 回收电池,四年级840节,是六年级的八分之七,五年级所交的是六年级的十分之五,节
 aeoaeo31年前1
aeoaeo31年前1 -
 sky0041 共回答了22个问题
sky0041 共回答了22个问题 |采纳率95.5%840除以八分之七=960(节) 960乘十分之五=480(节)
答:五年级共480节.1年前查看全部
- 回收纯银,废液里含有Ag离子,锌离子,亚铁离子
回收纯银,废液里含有Ag离子,锌离子,亚铁离子
费液(加过量X;操作I)得溶液C和固体A 然后固体A(加过量Y;操作II)得固体B和溶液D 然后溶液D(蒸发结晶)得固体E
回收的纯银存在于字母:中 X和Y的化学式是什么 gybfbb6go7cb81年前1
gybfbb6go7cb81年前1 -
 zwn126 共回答了17个问题
zwn126 共回答了17个问题 |采纳率100%X Fe
Y HCl1年前查看全部
- 鉴别氯化钠和氯化铵固体的混合物能否利用加热并回收气体的方法
 heroliu3241年前1
heroliu3241年前1 -
 darvey 共回答了19个问题
darvey 共回答了19个问题 |采纳率89.5%氯化钠和氯化铵固体的混合物加热后,
氯化铵固体会分解成氨气和氯化氢,
剩余的固体就是氯化钠,
因此可以利用加热并回收气体的方法1年前查看全部
- (2008•杭州)某化工厂排出的废水中含有硝酸银,硝酸钡,为了不污染环境并充分利用资源,需要从废水中回收金属银并制得碳酸
(2008•杭州)某化工厂排出的废水中含有硝酸银,硝酸钡,为了不污染环境并充分利用资源,需要从废水中回收金属银并制得碳酸钡,操作步骤和实验结果如下表,请填出表中未完成部分(写化学式)
操作步骤 实验结果 (1)向废水中加入适量______后过滤 分离出滤液A和滤出物______ (2)向滤液A中加入______溶液后过滤 滤出物是蓝色沉淀,滤液B中只含一种溶质 (3)向滤液B中加入______溶液后过滤 得到碳酸钡晶体  xiaonn8208211年前1
xiaonn8208211年前1 -
 oo是Id 共回答了12个问题
oo是Id 共回答了12个问题 |采纳率83.3%解题思路:根据题意:要从废水中回收金属银,可向废水中加入适量的排在银前的金属,由(2)滤出物是蓝色沉淀,说明该沉淀是氢氧化铜,可知(1)中加入的金属是铜,与硝酸银反应生成硝酸铜和银;(2)向滤液A中加入溶液过滤得到氢氧化铜沉淀,说明加入的是一种碱,又滤液B中只含一种溶质,说明该碱溶液与硝酸铜反应生成氢氧化铜和硝酸钡,据复分解反应原理可知加入的是氢氧化钡溶液;硝酸钡溶液可与碳酸钠、碳酸钾溶液反应生成碳酸钡沉淀.要从废水中回收金属银,可向废水中加入适量的排在银前的金属,由(2)滤出物是蓝色沉淀,说明该沉淀是氢氧化铜,由此说明(1)中加入的金属是铜,与硝酸银反应生成硝酸铜和银;(2)向滤液A中加入溶液过滤得到氢氧化...
点评:
本题考点: 金属的化学性质;盐的化学性质.
考点点评: 了解顺序表中前面的金属可将后面的金属从其盐溶液中置换出来,氢氧化铜是蓝色沉淀,及复分解反应的原理,才能结合题意正确分析解答,本题能很好考查学生依据所学分析、解决问题的能力.1年前查看全部
- 导电银漆回收汇鑫回收金渣硝酸钯吗?
 红尘无我1年前1
红尘无我1年前1 -
 xatyzz 共回答了20个问题
xatyzz 共回答了20个问题 |采纳率95%有的1年前查看全部
- 某建设项目前两年每年年末投资400万元,从第3年开始,每年年末等额回收260万元,项目计算期为10年.
某建设项目前两年每年年末投资400万元,从第3年开始,每年年末等额回收260万元,项目计算期为10年.
设基准收益率(ic)为10%,则该项目的财务净现值为( )万元.求过程解释(不套用复利等),只求每年数学计算解释, 青涩浪漫1年前1
青涩浪漫1年前1 -
 不是一个人 共回答了22个问题
不是一个人 共回答了22个问题 |采纳率86.4%NPV=260(P/A,10%,10-P/A,10%,2)-400(P/A,10%,2)
都是年金计算,不用复利,怎么行呢?一个一个加,多麻烦呀,建议你还是好好学学年金1年前查看全部
- 一元一次不等式 共两题 (1)某批发商经销一种服装,进价为每件60元,原计划按每件90元销售.为了减少库存以回收资金,现
一元一次不等式 共两题
(1)某批发商经销一种服装,进价为每件60元,原计划按每件90元销售.为了减少库存以回收资金,现决定进行优惠促销:以原销售价为基准,若顾客购买1~20件,则按九折优惠;若购买21~50件,则按八折优惠;若购买51~100件,则按七五折优惠;若购买100件以上则按七折优惠.某天该批发商共经手了两次业务,共售出105件,试问:这天他最多赚多少元?最少赚多少元?
(2)一次青年歌手大奖赛的评分规则规定:每位评委给选手的最高的得分情况如下全体评委所给分数的平均分是9.72分;去掉一个最低分,其余评委所给分数的平均分为9.76分;去掉一个最高分,其余评委所给分数的平均分为9.68分.试问:给这名选手最低分的那位评委打的分数是多少分?一共有多少评委?
不然没分
快 rawio1年前1
rawio1年前1 -
 呼唤爱心奉献爱心 共回答了22个问题
呼唤爱心奉献爱心 共回答了22个问题 |采纳率90.9%设y为利润,x为销售数量,k为优惠折扣,则
y=(90k-60)x,其中
当1≤x≤20时,k=90%;
当21≤x≤50时,k=80%;
当51≤x≤100时,k=75%;
当x>100时,k=70%;
则,2次共卖出105件,可能的销售方案是:
105=101+4:y=(90*0.70-60)*101+(90*0.9-60)*4=¥387
同理:若105=104+1:y=333
同理:若105=51+54:y=787.5
同理:若105=50+55:y=1012.5
同理:若105=5+100:y=810
同理:若105=20+85:y=877.5
可见,最大,最小利润为1012.5和3331年前查看全部
- 请问用PCR克隆已知基因的步骤中为何要将回收的目的基因重组在大肠杆菌质粒上去呢?
 灰hui1年前1
灰hui1年前1 -
 yyq73 共回答了15个问题
yyq73 共回答了15个问题 |采纳率93.3%1、这是作为保藏的手段,不然你怎么保存你的基因?
2、这是获得自引物之间完整序列的必要途径,因为测序是无法获得待测序列起始部分和约800-1000bps之后的序列,因此需要连接到质粒上测序,俗称TA克隆.为什么会这样我就不说了,懒得打字.1年前查看全部
- 回收的甲苯应放在哪种容器中
 Crymonkey1年前1
Crymonkey1年前1 -
 flamecc2 共回答了23个问题
flamecc2 共回答了23个问题 |采纳率91.3%首先甲苯是有机液体,见光不发生反应,所以应该放在无色细口玻璃瓶中,用玻璃塞或木塞.
橡皮塞可以和有机液体发生反应,所以不用1年前查看全部
- 下列有关资源、能源、环境的叙述正确的是( ) A.空气是一种宝贵的能源,空气污染主要来自于化石燃料的燃烧 B.回收废旧
下列有关资源、能源、环境的叙述正确的是( ) A.空气是一种宝贵的能源,空气污染主要来自于化石燃料的燃烧 B.回收废旧金属不仅能节约金属资源,还能节约能源和保护环境 C.地球上的水储量是丰富的,所以淡水资源也极其丰富 D.可燃冰主要成分是甲烷,就是化石燃料,不属于新能源  YY灭美dd1年前1
YY灭美dd1年前1 -
 就是nn 共回答了12个问题
就是nn 共回答了12个问题 |采纳率83.3%A、空气是一种宝贵的能源,空气污染主要来工厂排放的废气、汽车尾气以及可吸入颗粒物,故A错误;
B、回收利用废旧金属不仅能节约金属资源,还能节约能源和保护环境,故B正确;
C、人类能直接利用的淡水资源仅占全球水量的0.3%,淡水资源不丰富,不是取之不尽用之不竭的,故C错误;
D、可燃冰可燃冰主要成分是甲烷,属于新能源,故D错误.
故选:B.1年前查看全部
- 每年的6月5日是国际环保日.今年,实验小学高年级的学生在环保日参加回收废旧电池活动,部分年级收集数量如表: 年级 四年级
每年的6月5日是国际环保日.今年,实验小学高年级的学生在环保日参加回收废旧电池活动,部分年级收集数量如表:
(1)四、五年级一共回收了多少节废旧电池?年级 四年级 五年级 六年级 数量(节) 198 365
(2)六年级回收的数量比四、五年级的总和还多76节,六年级回收了多少节?计算完后将上表补充完整. 懒臣1年前1
懒臣1年前1 -
 fan283160541 共回答了19个问题
fan283160541 共回答了19个问题 |采纳率94.7%解题思路:(1)把四、五年级回收的废旧电池加起来即可;
(2)六年级回收的数量比四、五年级的总和还多76节,用四、五年级回收的总和,再加76即可,计算完后将上表补充完整.(1)198+365=563(节);
答:四、五年级一共回收了563节废旧电池.
(2)563+76=639(节);
答:六年级回收了639节.
补充表如下:
年级 四年级 五年级 六年级
数量(节) 198 365 639点评:
本题考点: 整数的加法和减法;简单的统计表.
考点点评: 此题考查了整数加法的意义及运用.1年前查看全部
- 某工厂排出的废水中含有大量的Fe2+、Cu2+和SO42-.为了减少污染,变废为宝,工程师们设计了如下流程,以回收铜和硫
某工厂排出的废水中含有大量的Fe2+、Cu2+和SO42-.为了减少污染,变废为宝,工程师们设计了如下流程,以回收铜和硫酸亚铁.请回答:

(1)原料①为______(填化学式).
(2)写出加入原料②后反应的离子方程式:______.
(3)若在实验室中完成该流程,操作②需要用到的玻璃仪器的名称是______、
______、______;整个实验操作过程中不可能用到的装置是______(填字母).
 青天大人1年前1
青天大人1年前1 -
 william蟑螂 共回答了18个问题
william蟑螂 共回答了18个问题 |采纳率83.3%解题思路:(1)根据该题要求:回收铜且不引进新的杂质判断原料①;
(2)先判断操作①后的固体成分,再根据流程图知:操作①后的溶液中的溶质与操作②后的溶液中的溶质相同写离子方程式;
(3)根据混合物的状态确定实验操作,根据实验操作确定实验仪器;根据各装置用途确定选项;(1)根据题意知,该物质能和铜离子反应且不引进新的杂质离子,所以只能是铁,故答案为:Fe.
(2)操作①中加入过量的铁才能使铜离子完全反应,所以所得固体的成分是铁和铜;分离铁和铜且回收铜,所以加入某物质与铁反应,与铜不反应,且与铁反应后的物质与操作①所得溶液中溶质的成分一样,加入的物质只能是稀硫酸,所以发生的离子反应为Fe+2H+═Fe2++H2↑,故答案为:Fe+2H+═Fe2++H2↑.
(3)操作②的分离是固体、液体分离,所以应用过滤的方法,故用到的玻璃仪器有玻璃棒、漏斗、烧杯;
操作①、②的分离是固体、液体分离,所以应用过滤的方法;操作③是蒸发掉水分,使溶质从溶液中析出,所以应用蒸发结晶的方法;
a、该装置是过滤装置,分离固体和液体;
b、该装置是萃取装置,根据溶解度的不同分离;
c、该装置是蒸发结晶装置,分离溶剂和溶质;
d、该装置是蒸馏装置,根据沸点的不同分离液体和液体;
所以选bd
故答案为:玻璃棒、漏斗、烧杯;bd.点评:
本题考点: 金属的回收与环境、资源保护;常见金属元素的单质及其化合物的综合应用;物质的分离、提纯的基本方法选择与应用.
考点点评: 本题考查了学生对高中化学实验装置图的理解和掌握程度.1年前查看全部
- 有没有 化学精英人士 给提供一下食品包装塑料袋的化学成分包括表面花纹图案的化学成分 是否有回收再利用价值
 dearlzx1年前3
dearlzx1年前3 -
 hu01 共回答了15个问题
hu01 共回答了15个问题 |采纳率93.3%pe=聚乙烯
还有种是聚氯乙烯,这个不能装肉或有油脂的食物
食品包装袋上的是喷绘或压制的,成分跟用的染料有关,各个厂家都不太一样,色泽也不一样,
回收塑料可以打碎成粉,压制成块装,造日常塑料用具如:脸盆等1年前查看全部
- 下列有关金属的说法正确的是 A钠铁严重锈台不值得回收 B纯铝的硬度大于铝合金 C 铝有很好的抗腐蚀性 D钢是
 lzy05511年前5
lzy05511年前5 -
 胶皮钉子 共回答了18个问题
胶皮钉子 共回答了18个问题 |采纳率100%下列有关金属的说法正确的是 C 铝有很好的抗腐蚀性 ,铝会在表面形成致密的氧化膜 氧化铝,阻止铝被腐蚀1年前查看全部
- 有人说:“垃圾是放错地方的资源。”以下是几种常见垃圾:①废纸 ②废塑料③废金属④果皮⑤废电池。属于可回收的有 A.①②⑤
有人说:“垃圾是放错地方的资源。”以下是几种常见垃圾:①废纸 ②废塑料③废金属④果皮⑤废电池。属于可回收的有
A.①②⑤ B.①②③ C.①②③⑤ D.①②③④⑤  多喜多1年前1
多喜多1年前1 -
 lxy2210 共回答了11个问题
lxy2210 共回答了11个问题 |采纳率90.9%C
果皮属于不可回收的,直接由微生物将其分解。1年前查看全部
- 某金属加工厂排放的污水中含有CUSO4、ZNSO4、FESO4,某研究小组利用该污水回收工业重要原料ZNSO4和有关金
 鸿蒙一道1年前1
鸿蒙一道1年前1 -
 zz张3 共回答了17个问题
zz张3 共回答了17个问题 |采纳率100%1)滤液A和滤液B含有相同的溶质,其名称是 硫酸锌 ;固体B的化学式为 Fe .
(2)写出步骤①其中一个反应的化学方程式__①Zn+CuSO4=ZnSO4 +Cu 或Zn+FeSO4=ZnSO4+ Fe__ ;
步骤④发生反应的化学方程式为 ④Zn+H2SO4=ZnSO4+H2↑ .
(3)要检验步骤④中加入的稀硫酸是否足量的方法是 取步骤④的滤渣于试管中加入少量稀硫酸,若有气泡产生则酸不足量(或若无气泡产生,则酸已足量). ___.
(4)若实验过程中的物质损失可以忽略,要计算该废液中硫酸锌的质量分数,必须称量:废液的质量和 .
硫酸锌的质量、锌粉的质量(或硫酸锌、固体B、固体C、铜的质量)1年前查看全部
- 现有含硝酸锌、硝酸亚铁和硝酸银的混合废液。下列有关说法正确的是 A.若要回收银,较为经济合理的方案是向废液中加稍过量的铁
现有含硝酸锌、硝酸亚铁和硝酸银的混合废液。下列有关说法正确的是
A.若要回收银,较为经济合理的方案是向废液中加稍过量的铁粉,过滤后向滤渣中加过量盐酸 B.若向废液中加入过量的锌粉,先置换出来的是铁 C.若向废液中加入一定量锌粉充分反应后过滤,向滤液中加入稀盐酸一定无现象 D.若向废液中加入一定量锌粉充分反应后过滤,滤液与原溶液相比,质量一定减小  wswchen1年前1
wswchen1年前1 -
 v9egleni 共回答了13个问题
v9egleni 共回答了13个问题 |采纳率76.9%A
1年前查看全部
- 回收一千克废纸,可生产0.8千克再生纸.四(1)班有54名学生,每人每天回收1千克废纸,5月份(31天)回收的
回收一千克废纸,可生产0.8千克再生纸.四(1)班有54名学生,每人每天回收1千克废纸,5月份(31天)回收的
废纸可生产多少千克的再生纸 苍原白狼1年前1
苍原白狼1年前1 -
 忘记过去123 共回答了12个问题
忘记过去123 共回答了12个问题 |采纳率91.7%1*31*54*0.8=1339.2千克1年前查看全部
- 如何分离CTAB和NaCl回收的时候得到了CTAB和NaCl还有乙醇的混合物,想要除掉NaCl,50%就可以,但无论是加
如何分离CTAB和NaCl
回收的时候得到了CTAB和NaCl还有乙醇的混合物,想要除掉NaCl,50%就可以,但无论是加乙醇还是冷却结晶,效果都不是很好,要做到无毒且尽量不损失CTAB,不知道有没有好的办法.
再将CTAB和NaCl尽量蒸干后(除去大部分水),加乙醇效果可以,但要8倍体积,与工业上节约的原则相违背,有没有可以减少乙醇用量,或别的办法... lihaoma1年前1
lihaoma1年前1 -
 aa149333 共回答了16个问题
aa149333 共回答了16个问题 |采纳率93.8%醇对CTABNaCl胶束体系流变性及CTAB分子1年前查看全部
- 有一种工业废水,已知其中含有大量的FeSO4,少量的Ag+和Na+,以及部分污泥.试设计一个既经济又合理的方法以回收金属
有一种工业废水,已知其中含有大量的FeSO4,少量的Ag+和Na+,以及部分污泥.试设计一个既经济又合理的方法以回收金属银、硫酸亚铁.分步列出实验步骤,并说明每一步骤的目的(不必写化学方程式).
 ea357zx1年前1
ea357zx1年前1 -
 apple是天使 共回答了11个问题
apple是天使 共回答了11个问题 |采纳率81.8%解题思路:在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.Ag+:加入过量的铁粉,使Ag+还原为Ag,将混有Fe粉的Ag用稀H2SO4处理,使Fe溶解,过滤,分离出银,据此分析解答.要从工业废水中回收金属银和硫酸亚铁,首先需要将其中的污泥通过过滤除去,然后根据铁能将银离子置换出来的性质,加入过量的铁粉,使银全部被置换出来,过滤得到银和铁的混合物,然后根据铁可以和酸发生置换反应而银不与酸发生置换反应的性质,将得到的固体混合物加入稀硫酸,使铁反应,过滤得到银,最后将溶液混合,根据物质溶解度的不同,加热得到饱和溶液,然后降温使硫酸亚铁晶体析出,然后加热使硫酸亚铁晶体失去结晶水从而得到硫酸亚铁,
答:①过滤除去污泥,②向滤液中加入过量的铁粉,使Ag+还原为Ag,③过滤,将Ag和过量的铁粉从溶液中分离出来,④将混有Fe粉的Ag用稀H2SO4处理,使Fe溶解,⑤过滤,分离出银,⑥将③、⑤两步的滤液合并,蒸发浓缩,冷却结晶,⑦趁热过滤,除去其中的Na+得硫酸亚铁晶体,加热晶体使其失去结晶水得到FeSO4.点评:
本题考点: 金属的回收与环境、资源保护.
考点点评: 本题考查了混合物的分离和提纯的实验方案的设计,完成此题,可以依据金属活动性顺序及其意义进行,题目难度不大.1年前查看全部
- 再生纸是以废纸做原料加工生产出来的纸张.回收的废纸可以加工出相当于废纸原重的五分之四的再生纸,因
再生纸是以废纸做原料加工生产出来的纸张.回收的废纸可以加工出相当于废纸原重的五分之四的再生纸,因
被誉为低能耗、轻微污染的环保型用纸.
据中国造纸协会统计,2010年全国纸及纸板消费量约9200万吨,如果有五分之二可以回收利用,可回收利用的纸和纸板大约有多少万吨? falaosao11年前1
falaosao11年前1 -
 mbhandsome 共回答了23个问题
mbhandsome 共回答了23个问题 |采纳率87%这取决于国家的政策引导以及国民素质.1年前查看全部
- 高中化学——三大合成材料塑料、合成纤维、合成橡胶能代替金属材料的是_________可回收后重新软化加工的是______
高中化学——三大合成材料
塑料、合成纤维、合成橡胶
能代替金属材料的是_________
可回收后重新软化加工的是__________ lanqian1111年前1
lanqian1111年前1 -
 liqiurong 共回答了17个问题
liqiurong 共回答了17个问题 |采纳率94.1%能代替金属材料的是 合成纤维_________
可回收后重新软化加工的是 塑料__________1年前查看全部
- (2013•眉山)桔杆野外焚烧,既不安全又不环保,且浪费能源,若回收再利用,既可产生沼气,又可产生肥料.100kg桔杆可
(2013•眉山)桔杆野外焚烧,既不安全又不环保,且浪费能源,若回收再利用,既可产生沼气,又可产生肥料.100kg桔杆可产生沼气1m3,若完全燃烧这部分沼气可产生热量______J,不计热量损失,这些热量可以使______kg的水温度升高50℃.[已知沼气热值为4.2×107J/m3、水的比热容为4.2×103J/(kg•℃)].
 tianj0010011年前1
tianj0010011年前1 -
 逸之狐 共回答了18个问题
逸之狐 共回答了18个问题 |采纳率100%解题思路:根据Q放=Vq,从而计算出沼气燃烧的量;又根据热量的计算公式,可以计算出水的质量.完全燃烧这部分沼气可产生热量Q放=Vq=1m3×4.2×107J/m3=4.2×107J;
∵由Q吸=cm△t,Q吸=Q放=4.2×107J;
∴m=
Q吸
c△t=
4.2×107J
4.2×103J/m3×50℃=200kg.
故答案为:4.2×107;200.点评:
本题考点: 热平衡方程的应用.
考点点评: 本题考查了燃料完全燃烧放热公式的应用,注意固体(液体)燃料完全燃烧放热公式Q放=mq、热值单位J/kg;气体燃料完全燃烧放热公式Q放=Vq、热值单位J/m3.1年前查看全部
- 某化工厂排放的废液中含有大量的硫酸锌和硫酸铜,化学兴趣小组的同学根据所学知识设计了一个方案,用来回收金属铜并得到硫酸锌晶
某化工厂排放的废液中含有大量的硫酸锌和硫酸铜,化学兴趣小组的同学根据所学知识设计了一个方案,用来回收金属铜并得到硫酸锌晶体,主要过程如图所示:

请回答下列问题:
(1)步骤②中分离物质的方法是______.
(2)固体A的成分是______.
(3)步骤②中发生反应的化学方程式为______,
(4)步骤③中加入的B物质是______. 老汤1年前1
老汤1年前1 -
 lclclc20909 共回答了15个问题
lclclc20909 共回答了15个问题 |采纳率80%解题思路:一般的除杂质题必须同时满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应②反应时不能加入新的杂质.根据题目给出的流程图和信息:固体与液体分开的方法叫过滤;硫酸锌和硫酸铜的混合液中加入过量的锌粉,锌与硫酸铜反应生成硫酸锌和铜,过滤后固体A是铜和锌的混合物,滤液是硫酸锌溶液;铜和锌的混合物中加入适量的稀硫酸,铜不反应,锌与硫酸反应生成硫酸锌和氢气,过滤得到铜,滤液是硫酸锌;然后把硫酸锌溶液蒸发结晶得到硫酸锌晶体.(1)固体与液体分开的方法叫过滤,故答案为:过滤
(2)硫酸锌和硫酸铜的混合液中加入过量的锌粉,锌与硫酸铜反应生成硫酸锌和铜,过滤后固体A是铜和锌的混合物,滤液是硫酸锌溶液;故答案为:锌和铜
(3)锌与硫酸铜反应生成硫酸锌和铜,故答案为:Zn+CuSO4═Cu+ZnSO4
(4)铜和锌的混合物中加入适量的稀硫酸,铜不反应,锌与硫酸反应生成硫酸锌和氢气,过滤得到铜,滤液是硫酸锌;故答案为:稀硫酸点评:
本题考点: 物质除杂或净化的探究;书写化学方程式、文字表达式、电离方程式.
考点点评: 本考点属于物质的除杂或净化的探究,还考查了化学方程式的书写,是中考的一个难点,也是学生经常出错的题型.根据物质的溶解性和除杂质的条件,要认真分析,综合把握.还要加强记忆除去常用离子的方法和物质的溶解性,从而突破难点,本考点经常出现在填空题和实验题中.1年前查看全部
- 小丁每天从报社以每份0.5元买进报纸200份,以1元/份价格卖出,当日卖不完的以0.2元/份回收给废旧站
小丁每天从报社以每份0.5元买进报纸200份,以1元/份价格卖出,当日卖不完的以0.2元/份回收给废旧站
平均卖出x份,纯收入为y元.如果每月30天计算,至少要卖多少才能保证收入不少于2000元 qq1906758651年前2
qq1906758651年前2 -
 weichen77 共回答了19个问题
weichen77 共回答了19个问题 |采纳率94.7%y=(X+(200-X)x0.2-200x0.5)x30 这个是纯收入和份之间的关系,简化后为Y=24X-1800
Y要大于等于2000时,且Y为整数时,最小为1591年前查看全部
- 某同学收集了班级其他同学做的“氢气还原氧化铜“的实验后的固体残渣(含铜和氧化铜),欲从中回收单质铜和制取硫酸铜溶液,他设
某同学收集了班级其他同学做的“氢气还原氧化铜“的实验后的固体残渣(含铜和氧化铜),欲从中回收单质铜和制取硫酸铜溶液,他设计了如下实验方案:
(1)称量.称量收集到的固体残渣20g,需要的仪器名称是______.
(2)溶解.将20g称量好的固体残渣放入烧杯中,加入过量的稀硫酸溶液,用玻璃棒不断搅拌,直至反应完全.烧杯中发生反应的化学方程式为______
(3)过滤.除滤纸外,还需要从下图中选用哪些仪器______(填字母).
(4)洗涤干燥.洗净滤纸上的固体,干燥后称量,此固体名称为______.
(5)收集滤液.滤液中所含溶质的化学式是______
(6)分析.为了除去滤液中过量的硫酸,应往滤液中加入过量的下列______(填编号)固体粉末,过滤.
①氧化铜②氢氧化钠③铁④硫酸铜
判断固体过量的实验现象是______. tiger_lisa1年前1
tiger_lisa1年前1 -
 鬼爷 共回答了12个问题
鬼爷 共回答了12个问题 |采纳率100%(1)称量固体使用的仪器是托盘天平,所以本题答案为:托盘天平;
(2)氧化铜能与硫酸反应生成硫酸铜和水,所以本题答案为:CuO+H 2 SO 4 ═CuSO 4 +H 2 O;
(3)过滤所用的仪器有漏斗、烧杯、玻璃棒和铁架台,所以本题答案为:A,C,E,F;
(4)铜不与硫酸反应,过滤后留在滤纸上,所以本题答案为:铜;
(5)硫酸过量,故滤液中含有硫酸和生成的硫酸铜,所以本题答案为:H 2 SO 4 和CuSO 4 ;
(6)要除去滤液中的硫酸,不能引入新的杂质,选用氧化铜比较合适,当硫酸全部参加反应时,加入的氧化铜不再溶解,有固体剩余,所以本题答案为:①,有固体不溶解.1年前查看全部
- 关于化学的题一道题,某工厂的工业废水中含有大量的FeSo4、较多的Cu2+和Na+。为了减少污染,工厂计划从废水中回收硫
关于化学的题
一道题,某工厂的工业废水中含有大量的FeSo4、较多的Cu2+和Na+。为了减少污染,工厂计划从废水中回收硫酸亚铁和金属铜。请说明操作方法,完成回收硫酸亚铁和铜的简单实验方案。谢了!尽量说仔细一点!
各位高手,我赶时间!我先谢谢了! 当午妹锄禾哥又要1年前1
当午妹锄禾哥又要1年前1 -
 yukiwa 共回答了15个问题
yukiwa 共回答了15个问题 |采纳率93.3%用铁屑将Cu置换出来,再用硫酸洗涤过量的铁粉,过滤可以得到纯净的铜单质,然后对滤液进行加热浓缩,冷却结晶,可以得到含有结晶水的硫酸亚铁,最后烘干晶体。1年前查看全部
- 下列有关金属和金属材料的认识中,不正确的是( ) A.生铁和钢的性能相同 B.赤铁矿的主要成分是氧化铁 C.回收废旧金
下列有关金属和金属材料的认识中,不正确的是( ) A.生铁和钢的性能相同 B.赤铁矿的主要成分是氧化铁 C.回收废旧金属有利于节约资源 D.铁粉做“双吸剂”和铁生锈原理相同  未激活6261年前1
未激活6261年前1 -
 流光璀璨 共回答了15个问题
流光璀璨 共回答了15个问题 |采纳率93.3%A、生铁硬而脆易断,钢较硬有良好的延性、展性和弹性.故选项错误;
B、赤铁矿的主要成分是氧化铁;故选项正确;
C、废旧金属的回收有利于节约资源;故选项正确;
D、铁生锈的原理,是在氧气和水的共同作用下发生的;“双吸剂”就是吸收氧气和水;故选项正确;
故选A.1年前查看全部
- DNA片段的回收实验中,wash solution当中为什么要加入乙醇
DNA片段的回收实验中,wash solution当中为什么要加入乙醇
DNA片段的回收当中wash solution中要加入乙醇 有的是要用乙醇稀释 水果fruit1年前1
水果fruit1年前1 -
 gto991 共回答了14个问题
gto991 共回答了14个问题 |采纳率92.9%乙醇可以沉淀DNA,离心后是DNA沉淀于管底,从而不会被洗去.1年前查看全部
- 常用的化学电池的种类、名称、形状、电极、电解质、可否再充电、价格、存放期、特点、用途、回收途径有哪
常用的化学电池的种类、名称、形状、电极、电解质、可否再充电、价格、存放期、特点、用途、回收途径有哪
希望可以快点,
我星期一急需.. 涂雅小盐1年前1
涂雅小盐1年前1 -
 来上网吧003 共回答了17个问题
来上网吧003 共回答了17个问题 |采纳率94.1%碳性氯化锌电池,包括D、C、AA、AAA、N及9伏型号
氯化锌电池的化学成份 - 正极:二氧化锰 负极:锌壳 电解液:氯化锌水.
氧化银钮扣型电池
化学成份 - 正极:氧化银 负极:锌 电解液:氢氧化钾
碱性钮扣型电池
化学成份 - 正极:二氧化锰 负极:锌 电解液:氢氧化钾
专用电池
化学成份:锂离子或镍金属氢化物(NiMH)
充电电池
化学成份:镍金属氢化物(NIMH)
一次性锂电池
化学成份:锂,碱 这个是在朋友问题里摘的 请看1年前查看全部
- 、从实验室用氯酸钾于二氧化锰制取氧气后的残渣中(假定反应充分)回收氯化钾和二氧化锰.
 zjx21cn1年前4
zjx21cn1年前4 -
 小鱼蛮儿 共回答了16个问题
小鱼蛮儿 共回答了16个问题 |采纳率93.8%加水后,用过滤纸过滤氯化钾和二氧化锰,把过滤纸上的水分蒸发掉,就可以得到干燥的氯化钾和二氧化锰.1年前查看全部
- 常有的化学电池有那几种?要求:电池种类、名称、形状、电极、电解质、电压、可否能充电、价格、存放期、特点、用途.回收途径等
常有的化学电池有那几种?
要求:电池种类、名称、形状、电极、电解质、电压、可否能充电、价格、存放期、特点、用途.回收途径等. 玉笔幽灵1年前1
玉笔幽灵1年前1 -
 angel7wing 共回答了14个问题
angel7wing 共回答了14个问题 |采纳率85.7%化学电池按工作性质可分为:一次电池(原电池);二次电池(可充电电池);铅酸蓄电池.其中:一次电池可分为:糊式锌锰电池、纸板锌锰电池、碱性锌锰电池、扣式锌银电池、扣式锂锰电池、扣式锌锰电池、锌空气电池、一次锂锰电池等.二次电池可分为:镉镍电池、氢镍电池、锂离子电池、二次碱性锌锰电池等.铅酸蓄电池可分为:开口式铅酸蓄电池、全密闭铅酸蓄电池.1年前查看全部
- (2012•泰安)某兴趣小组的同学从实验室收集到一桶含有FeSO4、CuSO4的废液,他们想从中回收金属铜和硫酸亚铁晶体
(2012•泰安)某兴趣小组的同学从实验室收集到一桶含有FeSO4、CuSO4的废液,他们想从中回收金属铜和硫酸亚铁晶体,设计了如下实验方案.结合实验方案回答下列问题:

(1)步骤①中,金属X是______,该反应的化学方程式为______;
(2)步骤②中,加入过量稀硫酸的目的是______;
(3)从滤液中获得硫酸亚铁晶体采用的方法是______. 踩了谁的尾巴1年前1
踩了谁的尾巴1年前1 -
 流浪的ll 共回答了14个问题
流浪的ll 共回答了14个问题 |采纳率92.9%解题思路:(1)由于目的是获得铜单质和硫酸亚铁,所以需要将铜离子转化为铜单质,而溶液中需要的是硫酸亚铁而不能引入新的杂质,所以加入的能够将铜离子转化为铜单质的只能是单质铁;
(2)由于加入的铁是过量的,加入过量稀硫酸的目的是除去铜中的铁;
(3)蒸发从溶液中获得晶体常采用的方法.(1)由题意可知,由于需要将铜离子转化为铜单质,而溶液还必须为硫酸亚铁,即不能引入新的杂质,所以可以加入铁将铜离子转化为铜单质.该反应的化学方程式为:Fe+CuSO4 ═FeSO4 +Cu;
(2)步骤②中,加入过量稀硫酸的目的是:使铁完全反应,除去铜中的铁;
(3)从滤液中获得硫酸亚铁晶体采用的方法是蒸发.
故答为:(1)铁,Fe+CuSO4 ═FeSO4 +Cu;(2)使铁完全反应,除去铜中的铁;(3)蒸发.点评:
本题考点: 金属活动性顺序及其应用.
考点点评: 解答本题时要注意混合物的分离要考虑为彻底分开而加入过量试剂,所以后一环节需要将之除去.1年前查看全部
- 题目为废酸中含有硫酸和盐酸,要就分离和回收,第一步是加氨水,生成了硫酸铵和氯化铵,接下来分离他们
题目为废酸中含有硫酸和盐酸,要就分离和回收,第一步是加氨水,生成了硫酸铵和氯化铵,接下来分离他们
最终分别要得到氯化铵和硫酸铵,提示是用溶解性,我不知道具体的, haifeng5321年前2
haifeng5321年前2 -
 yang_cheng7261 共回答了22个问题
yang_cheng7261 共回答了22个问题 |采纳率81.8%查找一下在不同温度下两种物质的溶解度,找一个合适的温度可以分离出两种物质的晶体!1年前查看全部
大家在问
- 1甲苯氧化成苯甲酸的方程式怎么写?
- 2直流电源请问12v 7.2A直流电源接在1.5A的负载上 如何变流 是否需要加限流电阻 阻值多大
- 3如果函数f(x)在x=x0处取得极值,则点(x0,f(x0))称为函数f(x)的一个极值点.已知函数f(x)=ax3+b
- 4高数微分方程问题一个齐次微分方程的问题,他把y/x换成了u,我想知道d(u)=什么?在线等
- 5翻译句子,你必须阻止他闯进房间.
- 6在行驶的汽车上看路边的行人和同方向行驶的自行车,观察者往往习惯于以——作参照物
- 7在三角形ABC中,角A 角B角C满足下列条件,角A减角B等于30度,角B减角C等于36度试判断三角形ABC的形状
- 8(4x-20)除以(3x-20)=三分之二的方程怎么解?我很急
- 9细胞跟分子,原子哪个更大一些啊,它们之间有什么关系
- 10若x^2+y^2-4x-6y=-13,求分式(x^2-2y^2)/2xy的值.
- 11一根电话线,第一次用去12米,第二次用去余下的百分之四十,还剩24米,这根电话线长多少米 0 | 离
- 12有一堆鸡蛋,3个3个数,余2个;4个4个数,余3个;5个5个数,余4个;6个6个数,余5个,问鸡蛋最少有多少个?
- 131.三角形中如果有两个内角大小相等,第三个内角是一个钝角,那么这个三角形按边分是( )三角形,按角分是( )三角形
- 14解方程解应用题解方程①y加二分之一等于三分之二减y②三分之x减一减六分之x加二等于一减二分之二x减一③y减二分之y减一等
- 15初二几何题:三角形ABC中,AB=AC,CE为AB的中线,延长AB到D,使BD=AB,连结CD.求证:DE=2CE.
