苯与水的溶解性,(我要20度与100度两种,重要的是100度),并希望解释苯酚加热与水互溶的原因
 凡斗Di斗2022-10-04 11:39:541条回答
凡斗Di斗2022-10-04 11:39:541条回答工业上有以苯带水的方法,但常温水与苯的溶解性很差,这又如何做到的?此外为何苯酚的溶解度随温度的变化差别这么大,仅仅是因为O-H---O氢键吗?苯会否提供派电子以形成氢键吗?
还有,芳杂环的水溶性如何,高温呢?
请高手作答.要拿的准的答案.
当然,我更喜欢定量化的.可是毕竟定量化的数据太少,我只是想问苯在不同温度下的水中的溶解性是否有苯酚一样有“突跃”.并不打算深究溶解性及其判断依据.问此题也主要是为了了解其中的分子间作用力.
正如Ba(OH)2,&LiOH,溶解度谁大,好象LiOH稍大.
这些,就不管了.
如有兴趣,

已提交,审核后显示!提交回复
共1条回复
 65203579 共回答了19个问题
65203579 共回答了19个问题 |采纳率94.7%- 用苯来除去其他有机物中的水是利用了共沸现象.两种液体,分子间若有一定的相互作用,就可能产生一定组成下沸腾时蒸汽相组成和液相组成相同的情况,称为共沸.此时二者无法分离,但工业上恰恰可以利用这种性质除水.下面是一些有机物与水的共沸物组成.
名 称 共沸点(度) x1 含水量(%)
乙 苯 92 0.744 5.52
苯 69.3 0.295 35.55
甲 苯 84.1 0.444 19.68
间二甲苯 92 0.767 4.91
至于你用溶解度解释,我想不太妥当.除水是在液体沸腾情况下实现的,此时,两种组分均蒸发,进入气相的多寡主要取决于各自的蒸汽压;况且这种状态不能称之为溶解.NaCl的溶解度很大,但就是利用蒸馏的方法进行除盐,可见气相组成还是取决于组分的气化能力.
溶解性的突跃问题希望你能列举出数据,比如苯酚的熔点和突跃温度.一起讨论一下.是否由于相变或其他原因造成的. - 1年前
相关推荐
- 怎样判断盐在水中溶解性?专业解.
 lantianbaiyu1年前1
lantianbaiyu1年前1 -
 aywabb 共回答了10个问题
aywabb 共回答了10个问题 |采纳率90%书后边有一个 溶解性表
这个要背下来的,非常重要
表中含义:
溶 该物质可溶于水
不 该物质不溶于水
微 该物质微溶于水
挥 该物质溶于水且有挥发性1年前查看全部
- 如何去除污水中的溶解性总磷?
 徒步流浪1年前1
徒步流浪1年前1 -
 太阳是块煎饼 共回答了21个问题
太阳是块煎饼 共回答了21个问题 |采纳率81%生物法和化学法,生物法不用说了 A2O之类的;化学法就是用铝盐或者铁盐将溶解性磷转化为磷酸盐沉淀,然后去除.1年前查看全部
- 【高一化学】溶解性在元素周期表中的规律》》
【高一化学】溶解性在元素周期表中的规律》》
如题,物质(包括化合物)的溶解性在元素周期表的趋势是怎样的?
溶解性:AgF 小笑世上士1年前3
小笑世上士1年前3 -
 雯婕小小 共回答了16个问题
雯婕小小 共回答了16个问题 |采纳率81.3%看后面酸根的氧化性强弱,越强则结合成的物质越稳定,溶解性就越弱,楼上的人在乱说1年前查看全部
- 重结晶过程中如果溶剂对杂质溶解的很少,对有机物的溶解性比较强,那么过滤后
重结晶过程中如果溶剂对杂质溶解的很少,对有机物的溶解性比较强,那么过滤后
A有机物在滤液中 B杂质在滤液中
C有机物在滤纸中 D杂质在滤纸中
这个我真不怎么办,谁能说的详细些,为什么.像它类似的题,假如说,对有机物溶解性弱,还有对杂质溶解多,与它类似的,怎么看? ChaoLei81年前1
ChaoLei81年前1 -
 xtgirl 共回答了12个问题
xtgirl 共回答了12个问题 |采纳率83.3%这种情况当然是有机物在滤液中,杂质在滤纸上.将滤液冷却结晶可得有机物,然后再次过滤,这次有机物在滤纸上,滤液中是还没有析出的有机物.1年前查看全部
- (2007•昌平区二模)酸、碱、盐溶解性表是学习化学的重要工具.下表为部分酸、碱、盐在水中的溶解性(20℃).试回答:
 (2007•昌平区二模)酸、碱、盐溶解性表是学习化学的重要工具.下表为部分酸、碱、盐在水中的溶解性(20℃).试回答:
(2007•昌平区二模)酸、碱、盐溶解性表是学习化学的重要工具.下表为部分酸、碱、盐在水中的溶解性(20℃).试回答:
(1)某碱溶液和某盐溶液混合生成两种难溶物质,请你从上表找出物质写出该反应的化学方程式______.阴离子 Ba2+ Ca2+ Mg2+ Zn2+ Fe2+ Cu2+ Ag+ OH- 溶 微 不 不 不 不 -- SO42- 不 微 溶 溶 溶 溶 微 CO32- 不 不 微 不 不 不 不 Cl- 溶 溶 溶 溶 溶 溶 不
(2)有A、B、C、D四种物质的稀溶液,如图为常温时上述溶液两两混合的实验现象,其中“↓”表示生成沉淀,“↑”表示生成气体,“-”表示无明显现象或生成微溶物.请你结合上表,将推断的可能情况填写出来.
①写出A、D的化学式:A______、C______;
②B可能是______.
③写出A和D反应的化学方程式______. 幽幽05041年前1
幽幽05041年前1 -
 sibo99 共回答了18个问题
sibo99 共回答了18个问题 |采纳率88.9%解题思路:(1)碱和盐反应生成新的碱和盐,且反应物须可溶,生成物均为沉淀,然后结合溶解性表进行分析;
(2)AD反应生成气体,所以二者可能是碳酸盐与酸的反应,然后结合复分解反应的条件和四种物质之间的反应现象进行分析,并写出反应方程式.(1)碱和盐反应生成新的碱和盐,且反应物须可溶,生成物均为沉淀,由表中信息可知氢氧化钡和硫酸铜、或硫酸镁、硫酸铁均可;
故答案为:Ba(OH)2+CuSO4═Cu(OH)2↓+BaSO4↓(答案不唯一)
(2)AD反应生成气体,所以二者可能是碳酸盐与酸的反应,A可能是碳酸镁,D是稀盐酸,AB反应生成沉淀,可以是盐和盐的反应,也可以是碱和盐的反应,反应物须可溶,故B可能是氯化钡或氢氧化钡,BC反应生成沉淀沉淀是硫酸钡,C可能是硫酸铜、硫酸锌等可溶性硫酸盐;
故答案为:①MgCO3CuSO4;②BaCl2 ;③MgCO3+2HCl═MgCl2+CO2↑H2O(答案合理即可).点评:
本题考点: 复分解反应及其发生的条件;物质的鉴别、推断.
考点点评: 本题综合性较强,通过物质的推断和复分解反应条件利用能较好的考查学生分析能力和对知识的应用能力,解答时一定要抓住反应现象的不同,细心辨别、推断.1年前查看全部
- 溶解性只能粗略地表示物质的溶解能力.如蔗糖和食盐都易溶于水,怎样比较蔗糖和食盐哪一个更易溶于水
 boofeixue1年前1
boofeixue1年前1 -
 heyun10321 共回答了17个问题
heyun10321 共回答了17个问题 |采纳率82.4%比较溶解度.溶解度大的根为易溶.
在一定温度下,某固态物质在100g溶剂中达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂中的溶解度.1年前查看全部
- 钠的重要化合物填空Na2O Na2O2物质类别与水反应与二氧化碳反应Na2CO3 NaHCO3俗名状态\颜色溶解性比较酚
钠的重要化合物填空
Na2O Na2O2
物质类别
与水反应
与二氧化碳反应
Na2CO3 NaHCO3
俗名
状态颜色
溶解性比较
酚酞反应
与盐酸反应速率比较
热稳定性 czf391091年前3
czf391091年前3 -
 柠檬C 共回答了17个问题
柠檬C 共回答了17个问题 |采纳率82.4%Na2O Na2O2 物质类别 氧化物 过氧化物与水反应 Na2O+H2O=2NaOH 2Na2O2+2H2O=4NaOH+O2↑与二氧化碳反应 Na2O+CO2=Na2CO3 2Na2O2+2CO2=2Na2CO3+O2↑Na2CO3 NaHCO3 俗名 苏打 小苏打状态颜色 固体颗粒白色 细小固体颗...1年前查看全部
- 酸、碱、盐溶解性表是学习自然科学的重要工具,下表列出了“部分酸、碱、盐在20℃时的溶解性。”请利用表完成下列任务。 (1
酸、碱、盐溶解性表是学习自然科学的重要工具,下表列出了“部分酸、碱、盐在20℃时的溶解性。”请利用表完成下列任务。 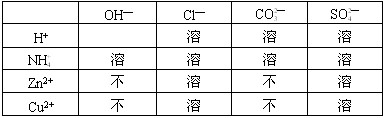
(1)查Zn(OH) 2 的溶解性:_______(选填“溶”或“不溶”);
(2)用化学方程式表示铁与表中的一种盐溶液的反应:____________________。 baihehua99211年前1
baihehua99211年前1 -
 绍兴E网 共回答了18个问题
绍兴E网 共回答了18个问题 |采纳率94.4%(1)不溶
(2)Fe+CuCl 2 ==FeCl 2 +Cu1年前查看全部
- 溶解度曲线能直观定量描述物质的溶解性。请根据右图的溶解度曲线回答下列问题:
溶解度曲线能直观定量描述物质的溶解性。请根据右图的溶解度曲线回答下列问题:
①请指出右图中的一个错误并纠正 ( 13 ) 。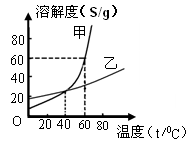 ②20℃时,甲物质的溶解度 ( 14 ) (填“大于”、“等于”或
②20℃时,甲物质的溶解度 ( 14 ) (填“大于”、“等于”或
“小于”)乙物质的溶解度。
③ ( 15 ) ℃时,两种物质的溶解度相等。
④60℃时,将80 g甲物质放入80 g水中,充分溶解所得溶
液的总质量为 ( 16 ) g。此时,若要进一步增大溶液的溶质
质量分数,可以采用的方法是 (17 ) 。 tianlan1691681年前1
tianlan1691681年前1 -
 yaya520 共回答了23个问题
yaya520 共回答了23个问题 |采纳率95.7%(13)溶解度单位是g/100g水
(14)小于(15)40
(16)128(17)加热溶液(升高温度)
分析:由题目中图的溶解度曲线可知:
①可知图中的一个错误为溶解度单位.
②由图可知:20℃时,甲物质的溶解度与乙物质的溶解度大小.
③由图可知:40℃时,两种物质的溶解度相等.
④60℃时,由此温度下的溶解度,可计算将80g甲物质放入80g水中,充分溶解所得溶液的总质量.因为甲物质的溶解度随温度增加而增大,故可知,若要进一步增大溶液的溶质质量分数,可以采用的方法.
溶解度曲线能直观定量描述物质的溶解性.由题目中图的溶解度曲线可知:
①图中的一个错误并纠正为:溶解度单位是g/100g水.
②由图可知:20℃时,甲物质的溶解度小于乙物质的溶解度.
③由图可知:40℃时,两种物质的溶解度相等.
④60℃时,甲物质的溶解度为60克,将80g甲物质放入80g水中,设80g水可以溶解x甲物质,故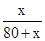 =
= ,x=48克,故充分溶解所得溶液的总质量为48+80=128g.此时,若要进一步增大溶液的溶质质量分数,可以采用的方法是加热溶液(升高温度).
,x=48克,故充分溶解所得溶液的总质量为48+80=128g.此时,若要进一步增大溶液的溶质质量分数,可以采用的方法是加热溶液(升高温度).
故答为:①溶解度单位是g/100g水;②小于;③40;④128;加热溶液(升高温度)1年前查看全部
- 碳酸氢钠、碳酸钠、氢氧化钠的溶解性大小怎么用元素周期律来比较?
 rufeng371年前2
rufeng371年前2 -
 kaikai1109 共回答了24个问题
kaikai1109 共回答了24个问题 |采纳率79.2%都是金属钠呀,
他们溶解度不同不是那个原因
记注就可以了.氢氧化钠 > 碳酸钠 > 碳酸氢钠1年前查看全部
- 求碳酸氢盐在水中的的溶解性
 zuozuo_best1年前4
zuozuo_best1年前4 -
 jy0820 共回答了22个问题
jy0820 共回答了22个问题 |采纳率86.4%你是初中还是高中?
这个是不需要掌握的,题目会给条件(初中:溶解度表、高中:溶度积)
要说真的来判断,要从构型来判断
由于水是非极性分子,所以极性比较大的分子会更容易溶于水.
举个例子:比较AgF和AgCl(没学过吧~)
看成Ag+ F-和Ag+ 和Cl-
由于F-的吸电子能力极强,Ag+难以把电子吸向自己,所以电子严重偏向F-,导致分子极性非常强,溶解度比较大
而Ag+ 和Cl-之间,相比F-来说Cl-抢电子能力要温和的多,所以电子不会非常偏向Cl-,电子会向中间靠近,导致分子的共价程度增高,极性下降,溶解度下降.
所以AgF的溶解性大于AgCl
从分子极性角度可以解决很大一部分溶解性的问题.
总之课内,不是竞赛的话,记住下面的就行了
钾钠铵盐硝酸盐①,
氢氧根多钡离子②,
硫酸盐除钡钙银③,
碳酸溶氢钾钠铵④,
生成沉淀氯化银⑤.
①钾盐、钠盐、铵盐、硝酸盐都溶于水;
②除了上述四种情况,氢氧根和钡离子结合也溶于水;
③硫酸根除了和钡离子、钙离子、银离子结合声称沉淀外,其余都溶于水;
④碳酸根除了跟氢离子、钾离子、钠离子、铵离子结合溶于水外,其他都不溶于水;
⑤氯离子只有和银离子结合不溶于水.1年前查看全部
- 蛋白质溶液遇到较浓的盐溶液时会降低其溶解性而析出,称之为__,属于__(填“物理”或“化学”)变化;蛋白质受__或遇到_
蛋白质溶液遇到较浓的盐溶液时会降低其溶解性而析出,称之为__,属于__(填“物理”或“化学”)变化;蛋白质受__或遇到__、__、__、__等,会发生__(填“物理”或“化学”)变化,失去原有的生理功能,称为__.
 烟雾飘飘男1年前2
烟雾飘飘男1年前2 -
 江讲胡说 共回答了16个问题
江讲胡说 共回答了16个问题 |采纳率68.8%称之为_盐析_,属于__物理(填“物理”或“化学”)变化;蛋白质受_热_或遇到_酸_、碱__、紫外线__、重金属__等,会发生__化学(填“物理”或“化学”)变化,失去原有的生理功能,称为_变性_.1年前查看全部
- M是一种活动性比铁强的金属,M离子(M2+)与其它几种离子构成的化合物的溶解性见下表:
M是一种活动性比铁强的金属,M离子(M2+)与其它几种离子构成的化合物的溶解性见下表:
有下列各组物质:①M+HCl;②M(NO3)2+BaCl2;③MO+HCl;④M(0H)2+NaCl;⑤M(0H)2+HCl;⑥M(NO3)2+HCl;⑦MCO3+HCl;⑧MSO4+BaCl2,其中不能直接反应制取MCl2的是( )O2- OH - CO32- Cl一 SO42- NO3- M 2+ 难溶 难溶 难溶 易溶 易溶 易溶
A. ②④⑥
B. ⑤⑥⑦⑧
C. ①②④⑦
D. ①③⑤⑧ tangege1年前9
tangege1年前9 -
 阿土伯11 共回答了14个问题
阿土伯11 共回答了14个问题 |采纳率85.7%解题思路:根据金属活动性顺序和复分解反应发生的条件解答,复分解反应发生的条件为有气体、沉淀、水等物质产生.金属M在铁的前边,可以和盐酸反应生成氯化物和氢气,所以①可行;根据酸的性质可以知道金属氧化物和碱都可以和盐酸反应,故③⑤可行;⑦⑧的生成物中分别有气体和沉淀,能够发生复分解反应⑦⑧也可行;②④⑥反应生成物中既无沉淀也无气体或者水生成,因此不能直接制取MCl2.
故选A.点评:
本题考点: 复分解反应及其应用;金属活动性顺序及其应用;物质的相互转化和制备.
考点点评: 本题考查的是复分解反应发生条件的综合拓展及盐酸的有关性质.1年前查看全部
- 初中化学的复分解反应为什么总提到“不溶于稀硝酸的白色沉淀”,与硝酸溶解性有什么关联?
初中化学的复分解反应为什么总提到“不溶于稀硝酸的白色沉淀”,与硝酸溶解性有什么关联?
为什么baso4和agcl不溶于稀硝酸? 洛Ζ风1年前4
洛Ζ风1年前4 -
 cz19860529 共回答了18个问题
cz19860529 共回答了18个问题 |采纳率94.4%AgCl与稀硝酸反应会生成什么?硝酸银和稀盐酸?那么Ag+与Cl-还是能结合生成AgCl沉淀.AgCl在水中的溶度积太小了.如果是比它溶度积还小的物质就能转化.比如加入NaI,就能转化为AgI沉淀.BaSO4也是一样的道理.而CaCO3这种可以生成CO2跑出去.AgNO2能被稀硝酸氧化.而AgCl,BaSO4这两种既不能被氧化.也不能与稀硝酸反应生成更难溶的物质.因而不能反应.1年前查看全部
- 氢氧化铁的颜色在水中和酸中的溶解性怎么写?硫酸钡的颜色在水中和酸中的溶解性怎么写?
氢氧化铁的颜色在水中和酸中的溶解性怎么写?硫酸钡的颜色在水中和酸中的溶解性怎么写?
氯化银的颜色在水中和酸中的溶解性怎么写?
氧化铜的颜色在水中和酸中的溶解性怎么写?
铁锈的颜色在水中和酸中的溶解性怎么写 rebeccaml9291年前1
rebeccaml9291年前1 -
 chuhj122 共回答了21个问题
chuhj122 共回答了21个问题 |采纳率85.7%Fe(OH)3红褐色溶于水1年前查看全部
- 关于高一化学碱金属的问题碱金属化学性质都完全相同吗?为什么锂的溶解性,热稳定性都和其他碱金属不同呢
 砺石寒1年前2
砺石寒1年前2 -
 善之花 共回答了24个问题
善之花 共回答了24个问题 |采纳率87.5%锂的半径很小 所以金属性弱一些 形成的盐溶解性也低一些
由于半径小 吸引电子能力弱 所以各类性质都弱一些1年前查看全部
- 气体种类是影响气体溶解性的因素吗?
 wenghaiyun1年前1
wenghaiyun1年前1 -
 maidi1669 共回答了25个问题
maidi1669 共回答了25个问题 |采纳率96%因该气体特性1年前查看全部
- 溶解性口诀钾、钠、铵、硝溶水间;碱溶钠、钾、钡、钙、铵;氯化物不溶氯化银;硫酸盐不溶钡和铅.碳酸盐多数是沉淀,但是全都溶
溶解性口诀
钾、钠、铵、硝溶水间;
碱溶钠、钾、钡、钙、铵;
氯化物不溶氯化银;
硫酸盐不溶钡和铅.
碳酸盐多数是沉淀,
但是全都溶于酸. james11120021年前1
james11120021年前1 -
 ltff2006 共回答了21个问题
ltff2006 共回答了21个问题 |采纳率90.5%钾盐、钠盐、铵盐、硝酸盐都能溶于水.÷
氢氧化钠、氢氧化钾、氢氧化钡、氢氧化钙、铵溶于水!
氯化银.氯化亚汞不溶于水和一般的酸
硫酸钡和硫酸铅不溶于水和一般的酸
碳酸盐多数是沉淀,
但是全都溶于酸1年前查看全部
- 求溶解性的分类的标准易溶、可溶、微溶、难溶是按什么标准来分类的?
 kyoyo_mm1年前2
kyoyo_mm1年前2 -
 xgjoni 共回答了18个问题
xgjoni 共回答了18个问题 |采纳率94.4%不是溶解性,溶解性没有单位的,只能用文字形容,如微溶于水,易溶于水,难溶于水等.而溶解度有单位,表示在一定温度下,某固态物质在100克溶剂里达到饱和状态(不能继续溶解)时所溶解的质量,单位是g.如果不指明溶剂是什么,一般所说的溶解度是指物质在水里的溶解度.溶解性就是根据溶解度大小区别的:
溶解度/g 溶解性
<0.01 难溶
0.01-1 微溶
1-10 可溶
>10 易溶1年前查看全部
- 求助2取代苯并咪唑后处理求助做过2取代苯并咪唑的人后处理是怎样处理的?溶解性不太好,如果用柱层析的话展开液用的是怎样的?
 shaoye0001年前1
shaoye0001年前1 -
 liu5953349 共回答了15个问题
liu5953349 共回答了15个问题 |采纳率100%含氮杂环在二氯甲烷里溶解度应该会好一些,
试一试二氯甲烷+甲醇的展开剂!
苯并咪唑结构非常刚性,很容易结晶,最好选择重结晶来纯化!1年前查看全部
- 影响蔗糖溶解性大小的因素主要有a溶剂的种类,蔗糖的质量 B溶剂的种类,温度的高低 C温度的高低 ,密度的大小 D溶剂的质
影响蔗糖溶解性大小的因素主要有
a溶剂的种类,蔗糖的质量 B溶剂的种类,温度的高低 C温度的高低 ,密度的大小 D溶剂的质量,蔗糖的质量 独孤开远1年前1
独孤开远1年前1 -
 雾水音律 共回答了17个问题
雾水音律 共回答了17个问题 |采纳率100%B
很明显1年前查看全部
- 物质溶解性与哪些因素有关:①()②()③()
 笨妮甜欣1年前2
笨妮甜欣1年前2 -
 pty_cobra 共回答了25个问题
pty_cobra 共回答了25个问题 |采纳率84%A 温度的高低
B 溶质的种类
C 溶剂的种类
对于气体还压强有关1年前查看全部
- 关于甲烷的溶解性甲烷 能溶与 四氯化碳溶液 吗
 至tt方休1年前3
至tt方休1年前3 -
 毛三那 共回答了22个问题
毛三那 共回答了22个问题 |采纳率86.4%根据有机物易溶于有机物,是可以的.1年前查看全部
- 磷酸一氢.二氢盐的溶解性如何?
 恨水东逝1年前1
恨水东逝1年前1 -
 kidault1 共回答了13个问题
kidault1 共回答了13个问题 |采纳率100%磷酸一氢盐只溶钾、钠、铵;磷酸二氢盐全部溶于水.1年前查看全部
- 部分酸、碱盐的溶解性口诀
 wcf885881年前2
wcf885881年前2 -
 lcr1699wa7dfa 共回答了21个问题
lcr1699wa7dfa 共回答了21个问题 |采纳率90.5%部分酸碱盐溶解性表的顺口溜:(初中)
钾钠铵盐皆可溶,
硝酸盐入水无影;,
难溶硫酸钡和铅,
还有氯化银、亚汞;
若问磷酸、碳酸盐,
此类物质多不溶;
酸易溶,碱难溶;,
CaSO4、Ag2SO4 、Ca(OH)2是微溶.1年前查看全部
- 通过实验探究比较白糖和食盐在水中的溶解性时,下列条件不必控制的是( )
通过实验探究比较白糖和食盐在水中的溶解性时,下列条件不必控制的是( )
A. 温度相同
B. 水的质量相同
C. 颗粒的大小一致
D. 都达到饱和溶液 二笨牛牛1年前1
二笨牛牛1年前1 -
 微笑之影 共回答了21个问题
微笑之影 共回答了21个问题 |采纳率95.2%解题思路:控制变量法是化学实验探究常采用的方法,其原理是通过控制变量的方法,把多变量的问题变成多个单变量的问题而进行逐一探究.影响物质溶解性的因素有溶质的性质、溶剂的性质、温度.而溶质颗粒的大小只是会影响溶解速度的快慢对结果没有影响.因此在探究白糖与氯化钠溶解性大小时,需要控制的变量有温度、溶剂的质量、种类及溶解的状态.
故选C点评:
本题考点: 固体溶解度的影响因素.
考点点评: 本题主要学生对影响物质溶解性因素的理解和控制变量法的应用,掌握影响物质溶解性的因素是解题的关键.1年前查看全部
- 只能用向上排空气法,“只能”为什么能说明溶解性
只能用向上排空气法,“只能”为什么能说明溶解性
不懂啊 123456789asx1年前6
123456789asx1年前6 -
 fenziyuanzi 共回答了29个问题
fenziyuanzi 共回答了29个问题 |采纳率93.1%气体的收集一般有排空气法和排水法
只能就说明不能用排水法
而气体不能用排水法说明其溶于水
也就是溶解性
wanbi~1年前查看全部
- 根据酸、碱和盐的性质及在水中的溶解性(20℃)回答下列问题:
根据酸、碱和盐的性质及在水中的溶解性(20℃)回答下列问题:
(1)NaNO3()(填“溶”或“不溶”,下同)于水,Mg(OH)2()于水.
(2)Na2CO3溶液与CaCl2溶液反应的化学方程式为(),该反应的基本类型为()反应
(3)NaCl、CaSO4、Cu(NO3)2三种溶液两两之间()(填“能”或“不能”)发生反应.理由:()
(4)若NaOH+A→B+C,且A的溶液呈蓝色,B为沉淀.写出B与H2SO4溶液反应的化学方程式:()
(5)写出铁与一种盐溶液反应的化学方程式:()
(6)写出一个中和反应的化学方程式:() 嘿嘿哈哈嘿1年前1
嘿嘿哈哈嘿1年前1 -
 wucway 共回答了21个问题
wucway 共回答了21个问题 |采纳率90.5%(1)NaNO3(溶)(填“溶”或“不溶”,下同)于水,Mg(OH)2(不溶)于水.
(2)Na2CO3溶液与CaCl2溶液反应的化学方程式为(CaCl2+Na2CO3==CaCO3↓+2NaCl),该反应的基本类型为(复分解)反应
(3)NaCl、CaSO4、Cu(NO3)2三种溶液两两之间(不能)(填“能”或“不能”)发生反应.理由:(没有气体、水、沉淀生成)
(4)若NaOH+A→B+C,且A的溶液呈蓝色,B为沉淀.写出B与H2SO4溶液反应的化学方程式:(Cu(OH)2+H2SO4==CuSO4+2H2O )
(5)写出铁与一种盐溶液反应的化学方程式:(Fe+CuSO4==Cu+FeSO4)
(6)写出一个中和反应的化学方程式:(NaOH+HCl==NaCl+H2O )1年前查看全部
- 为什么2012年济宁九下化学课本上写的溶解性与溶剂的量有关呢
 非常妹1年前1
非常妹1年前1 -
 dm_gyz 共回答了15个问题
dm_gyz 共回答了15个问题 |采纳率80%这么给你说吧,两个水槽里分别放着水和食用油,把氯化钠放到里面去,水的溶解性比食用油的要好,因为水的密度没有油的密度大,所以和溶剂的密度有关系有关系1年前查看全部
- 化学溶解性口诀急!
 闲人32517081年前3
闲人32517081年前3 -
 clqy1981 共回答了24个问题
clqy1981 共回答了24个问题 |采纳率91.7%钾钠铵硝四盐溶,盐酸除银汞,再说硫酸盐,不溶有钡铅,磷酸碳酸盐,只溶钾钠铵,最后说碱类,能溶钾钠钡1年前查看全部
- 碘能否溶解在汽油中?它的溶解性是易溶还是其他?
 aeglede1年前1
aeglede1年前1 -
 jinge1314 共回答了19个问题
jinge1314 共回答了19个问题 |采纳率94.7%汽油主要成分为碳原子数量4—7的烷烃,可溶解碘1年前查看全部
- 如果按不溶算,就可以看作是沉淀了.所以,溶解性中微溶算溶还是不溶?
 yangkai46841年前2
yangkai46841年前2 -
 XIANWUCH 共回答了16个问题
XIANWUCH 共回答了16个问题 |采纳率100%这要根据具体情况来看,微溶是介于溶和不溶之间的,如看复分解反应能否发生如果生成了微溶的物质就当做沉淀,该反应可以发生;但如果是关于溶解的问题又要按能溶来做,但溶解度一定要注意1年前查看全部
- 下表中列出了空气、NH3(氨气)、CH4、HCl四种气体在标准状况下的密度和溶解性,回答下列问题:
下表中列出了空气、NH3(氨气)、CH4、HCl四种气体在标准状况下的密度和溶解性,回答下列问题:
①其中,既可用排水法收集,又可用向下排空气法收集的气体是______.空气 NH3 CH4 HCl 密度(g/L) 1.293 0.771 0.717 1.629 溶解性 - 极易溶 极难溶 极易溶
②若用图中装置收集NH3,则气体应从______(填“a”或“b”)端通入.
 budsvdds1年前1
budsvdds1年前1 -
 man10127 共回答了13个问题
man10127 共回答了13个问题 |采纳率100%解题思路:可以根据气体的水溶性和密度来选择收集气体的方法.①因为甲烷的密度比空气小,极难溶于水,既可用排水法收集,又可用向下排空气法收集;
②因为氨气的密度比空气小,所以氨气应该从短导管--b端进入,将空气挤压到集气瓶底部排出;
故答案为:①CH4;②b.点评:
本题考点: 常用气体的收集方法.
考点点评: 本题主要考查了收集气体的方法,了解相关知识即可顺利解答.1年前查看全部
- 下表是物质的溶解性(20℃),利用表中的信息回答问题:
下表是物质的溶解性(20℃),利用表中的信息回答问题:
(1)NaOH和Ba(NO3)2两种溶液混合后能否发生反应?理由是什么?OH- NO3− SO42− Na+ 溶 溶 溶 Ba2+ 溶 溶 不 Cu2+ 不 溶 溶
(2)根据表中信息写出一个复分解反应的化学方程式:______. zhang03241年前1
zhang03241年前1 -
 rh7l0nj 共回答了20个问题
rh7l0nj 共回答了20个问题 |采纳率85%解题思路:(1)NaOH为碱,Ba(NO3)2为盐,碱和盐反应生成新碱和新盐,是复分解反应,反应发生的条件是:反应物都可溶,生成物中必须有沉淀.
(2)可根据经验:硫酸或可溶性硫酸盐的鉴定方法,滴加氯化钡溶液生成不溶于水和酸的硫酸钡沉淀.也可通过以下分析解答:根据复分解反应发生的特点,生成硫酸钡则反应物应为可溶性含钡化合物即可溶性钡盐或氢氧化钡、可溶性的含硫酸根的化合物即硫酸或榀溶性硫酸盐.然后结合题中溶解性表找出符合要求的物质.(1)根据溶解性表可知:NaOH、Ba(NO3)2、Ba(OH)2、NaNO3都可溶,反应中没有生成不溶的沉淀,不符合此类复分解反应发生的条件.故答:不能反应,没有气体、沉淀或水生成不符合复分解反应发生的条件;
(2)可溶性的钡盐氢氧化钡、硝酸钡都可以与可溶性的硫酸盐发生反应,生成符合条件要求的硫酸钡沉淀.氢氧化铜属于蓝色沉淀,所以可溶性碱与可溶性铜盐反应,所以氢氧化钠与硫酸铜反应生成氢氧化铜沉淀和硫酸钠.故答案:2NaOH+CuSO4═Na2SO4+Cu(OH)2↓或Ba(NO3)2+Na2SO4═BaSO4↓+2NaNO3(合理即可).
故答案为:(1)否,因为不符合复分解反应发生条件(或因为生物中无沉淀或气体或水生成);
(2)2NaOH+CuSO4═Na2SO4+Cu(OH)2↓(或Ba(NO3)2+Na2SO4═BaSO4↓+2NaNO3)(合理即可).点评:
本题考点: 复分解反应及其发生的条件;书写化学方程式、文字表达式、电离方程式.
考点点评: 复分解反应是通过化合物相互交换成分而发生的反应,反应必须生成沉淀或气体或水这类难电离的物质才能进行.1年前查看全部
- 导电性、溶解性类似于这种的算不算化学性质啊?如果不算,那哪些XX性质是化学性质啊?
 焚身以火投进网络1年前2
焚身以火投进网络1年前2 -
 14156256 共回答了16个问题
14156256 共回答了16个问题 |采纳率81.3%那些是物理性质
化学性质:物质在发生化学变化时才表现出来的性质叫做化学性质.牵涉到物质分子(或晶体)化学组成的改变.
如可燃性、不稳定性、酸性、碱性、氧化性、助燃性、还原性、络合性、毒性、热稳定性、腐蚀性、金属性、非金属性跟某些物质起反应呈现的现象等.用使物质发生化学反应的方法可以得知物质的化学性质.
物理性质:物质不需要发生化学变化就能表现出来的性质.如指 化学性质 酸性液体
:颜色、状态、气味、密度、硬度、光泽、溶解性、挥发性、导电性、延展性等、熔点、沸点、导热性等.1年前查看全部
- 关于糊精溶解性羟丙基环糊精在水中的溶解性很好,但是我想找一种溶剂,使羟丙基糊精在这种溶剂中的溶解度减小,先谢过了!
 屿梵1年前2
屿梵1年前2 -
 j90ij 共回答了22个问题
j90ij 共回答了22个问题 |采纳率90.9%加氯化钠吧,有机物在盐溶液中的溶解度降低1年前查看全部
- 酸、碱、盐溶解性表是学习化学的重要工具.下表列出了“部分酸、碱、盐在20℃时的溶解性”,请利用此表完成以下任务:
酸、碱、盐溶解性表是学习化学的重要工具.下表列出了“部分酸、碱、盐在20℃时的溶解性”,请利用此表完成以下任务:
(1)查:Ba(OH)2的溶解性______.OH- NO3- Cl- CO32- SO42- H+ - 溶、挥 溶、挥 溶、挥 溶 Na+ 溶 溶 溶 溶 溶 Ca2+ 微 溶 溶 不 微 Ba2+ 溶 溶 溶 不 不 Cu2+ 不 溶 溶 不 溶 Ag+ - 溶 不 不 微
(2)写化学式:一种酸______,一种不溶于水的盐______.
(3)判断:氯化钠溶液与硝酸钙溶液能否发生反应______,理由是______.
(4)写化学方程式:铁与表中的一种盐反应______. 慵懒的睡猫1年前1
慵懒的睡猫1年前1 -
 潘毛毛 共回答了15个问题
潘毛毛 共回答了15个问题 |采纳率100%解题思路:(1)查表可知氢氧化钡溶于水;
(2)表中酸有盐酸、硫酸、硝酸、碳酸;不溶于水的盐有碳酸钙、碳酸钡、硫酸钡、碳酸铜;
(3)根据复分解反应发生的条件进行分析,两种物质互换成分后必须有水、气体或沉淀生成,反应才能发生;
(4)根据金属活动性顺序中排在前面的金属能把后面的金属从它的盐溶液中置换出来,从表中所给金属可知,铁只能置换出金属铜,所以可以写铁和硫酸铜或铁和氯化铜的反应方程式;(1)氢氧化钡溶于水,
(2)酸有盐酸、硫酸、硝酸、碳酸;不溶于水的盐有碳酸钙、碳酸钡、硫酸钡、碳酸铜,
(3)氯化钠溶液和硝酸钙溶液互换成分后没有水、气体或沉淀生成,所以反应不会发生,
(4)铝排在铜之前,所以铁能置换出硫酸铜或氯化铜中的铜;只要合理均可,
故答案为:(1)可溶;
(2)HCl(或H2SO4、H2CO3、HNO3),CaCO3(或BaCO3、BaSO4、CuCO3);
(3)不能反应,因为互换成分无沉淀、气体或水产生,不满足复分解反应的条件;
(4)Fe+CuSO4═FeSO4+Cu;Fe+CuCl2═FeCl2+Cu(或其它合理答案).点评:
本题考点: 酸碱盐的溶解性;复分解反应及其发生的条件;化学式的书写及意义;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查了常见酸碱盐的溶解性以及物质间的反应,完成此题,可以依据已有的知识进行,书写反应的化学方程式要注意配平.1年前查看全部
- 近几年一种新型的甜味剂“木糖醇”悄悄地走入人们的生活,木糖醇是一种理想的蔗糖代替品,它具有甜味足,溶解性好,防踽齿,适合
近几年一种新型的甜味剂“木糖醇”悄悄地走入人们的生活,木糖醇是一种理想的蔗糖代替品,它具有甜味足,溶解性好,防踽齿,适合糖尿病患者的优点.木糖醇是一种白色粉末状的结晶,结构简式为CH2OH(CHOH)3CH2OH,下列关于木糖醇的叙述中正确的是( )
A.木糖醇不属于糖类
B.木糖醇能跟新制的氢氧化铜浊液反应生成砖红色沉淀
C.它与葡萄糖互为同分异构体
D.可以与乙酸在一定条件下发生酯化反应 浩日1年前1
浩日1年前1 -
 过马路的蛋 共回答了26个问题
过马路的蛋 共回答了26个问题 |采纳率100%解题思路:A.在化学上一般把多羟基醛或多羟基酮或水解后能变成以上两者之一的有机化合物称为糖;
B.能与新制Cu(OH)2悬浊液反应生成红色沉淀的糖类物质中应含有醛基,即为还原性糖;
C.同分异构体是分子式相同,结构不同的化合物;
D.木糖醇含有5个羟基.A.木糖醇结构简式CH2OH(CHOH)3CH2OH,可知木糖醇是一种五元醇,不属于糖类,故A正确;
B.木糖醇不含有醛基,不能与新制的氢氧化铜浊液反应生成红色沉淀,故B错误;
C.木糖醇(CH2OH(CHOH)3CH2OH)与葡萄糖(CH2OH(CHOH)4CHO)分子式不同,不是同分异构体,故C错误;
D.分子中含有羟基,能羧基发生酯化反应,故D正确;
故选AD.点评:
本题考点: 烃的衍生物官能团.
考点点评: 本题考查有机物的结构和性质,为高考常见题型,侧重于考查学生化学知识的应用能力,难度不大,注意把握有机物的结构和官能团的性质1年前查看全部
- 在研究物质溶解性的实验中,小明将5g硝酸钾加入10g水中,充分振荡后静置,现象如图甲所示.
在研究物质溶解性的实验中,小明将5g硝酸钾加入10g水中,充分振荡后静置,现象如图甲所示.
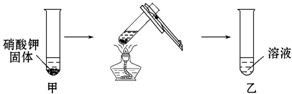
(1)小明认为图甲试管中的溶液为该温度下硝酸钾的饱和溶液,判断的依据是______.
(2)对该试管进行加热,得到如图乙所示的溶液,小明认为该溶液为不饱和溶液,请对小明的判断作出评价:______.
(3)晓龙通过实验对该溶液是否饱和作出了正确判断,他的做法是______. 黑圣1年前1
黑圣1年前1 -
 petpet444 共回答了22个问题
petpet444 共回答了22个问题 |采纳率90.9%解题思路:(1)根据通过观察法可知,试管底部还有未溶解的硝酸钾固体,该温度下硝酸钾溶液一定是饱和溶液进行解答;
(2)根据当溶液底部没有硝酸钾固体剩余时,也不能说该溶液就一定是硝酸钾的不饱和溶液,因为此时的溶液可能是不饱和溶液,也可能恰好为饱和溶液进行解答;
(3)根据饱和溶液是指该温度下不能再继续溶解该溶质的溶液进行解答.(1)通过观察法可知,试管底部还有未溶解的硝酸钾固体,该温度下硝酸钾溶液一定是饱和溶液;
(2)当溶液底部没有硝酸钾固体剩余时,也不能说该溶液就一定是硝酸钾的不饱和溶液,因为此时的溶液可能是不饱和溶液,也可能恰好为饱和溶液,所以小明的判断是错误的;
(3)饱和溶液是指该温度下不能再继续溶解该溶质的溶液,所以若要作出正确判断,可通过实验法,即向该溶液加入少量硝酸钾,搅拌后,若能溶解,表明该溶液不饱和;若不能溶解,则表明该溶液已饱和.
故答案为:(1)试管底部还有硝酸钾固体;
(2)小明的判断不正确,因为该溶液可能恰好为饱和溶液;
(3)向该溶液中加入少量的硝酸钾,看其能否继续溶解,若能继续溶解,表明该溶液不饱和;若不能继续溶解,则表明该溶液已饱和.点评:
本题考点: 饱和溶液和不饱和溶液.
考点点评: 饱和溶液部分是溶液的重难点,也是历年中考热点之一,学习中要透彻理解饱和溶液以及溶解度的有关知识.1年前查看全部
- 酸、碱、盐溶解性表是学习化学的重要工具,右表列出了部分酸、碱、盐在20℃时的溶解性,我能利用此表完成以下任务:
酸、碱、盐溶解性表是学习化学的重要工具,右表列出了部分酸、碱、盐在20℃时的溶解性,我能利用此表完成以下任务:
(1)查:Ba(OH)2的溶解性______.OH- NO3- Cl- CO32- SO42- H+ -- 溶、挥 溶、挥 溶、挥 溶 Na+ 溶 溶 溶 溶 溶 Ca2+ 微 溶 溶 不 微 Ba2+ 溶 溶 溶 不 不 Cu2+ 不 溶 溶 不 溶
(2)写化学式:一种酸______;一种不溶于水的盐______.
(3)判断:氯化钠溶液与硝酸钙溶液能否发生反应及其______.
(4)写化学方程式:铝与表中的可溶性盐发生的反应(只写1个)______.
表中物质发生的有沉淀生成的复分解反应(只写1个)______. 憨包包1年前1
憨包包1年前1 -
 133ok 共回答了16个问题
133ok 共回答了16个问题 |采纳率87.5%解题思路:(1)查表可知氢氧化钡溶于水;
(2)表中酸有盐酸、硫酸、硝酸、碳酸;不溶于水的盐有碳酸钙、碳酸钡、硫酸钡、碳酸铜;
(3)根据复分解反应发生的条件进行分析,两种物质互换成分后必须有水、气体或沉淀生成,反应才能发生;
(4)根据金属活动性顺序中排在前面的金属能把后面的金属从它的盐溶液中置换出来,从表中所给金属可知,铝只能置换出金属铜,所以可以写铝和硫酸铜或铝和氯化铜的反应方程式;复分解反应可以写生成碳酸钡、硫酸钡、碳酸钙等沉淀的反应,只要合理都正确.(1)氢氧化钡溶于水,故答案为:可溶;
(2)酸有盐酸、硫酸、硝酸、碳酸;不溶于水的盐有碳酸钙、碳酸钡、硫酸钡、碳酸铜,故答案为:HCl(或H2SO4、H2CO3、HNO3),CaCO3(或BaCO3、BaSO4、CuCO3);
(3)氯化钠溶液和硝酸钙溶液互换成分后没有水、气体或沉淀生成,所以反应不会发生,故答案为:不能反应,因为互换成分无沉淀、气体或水产生,不满足复分解反应的条件;
(4)铝排在铜之前,所以铝能置换出硫酸铜或氯化铜中的铜;表中沉淀有碳酸钡、硫酸钡、碳酸钙等,所以可以写氯化钡和硫酸反应生成硫酸钡和盐酸,也可以写氯化钙和碳酸钠反应生成碳酸钙和氯化钠,只要合理均可,故答案为:2Al+3CuSO4═Al2(SO4)3+3Cu;BaCl2+H2SO4═BaSO4↓+2HCl(或其它合理答案).点评:
本题考点: 酸碱盐的溶解性;复分解反应及其发生的条件;化学式的书写及意义;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查复分解反应发生的条件,要求我们能从表中所给物质中选择恰当的物质进行反应.1年前查看全部
- 铬酸铜在氨水中的溶解性和在水中的溶解性
 夏柳儿1年前2
夏柳儿1年前2 -
 丢丢的梦想 共回答了19个问题
丢丢的梦想 共回答了19个问题 |采纳率94.7%铬酸铜溶于酸,不溶于水和氨水.1年前查看全部
- 石墨烯分子层与层间的作用力是怎样的?溶解性如何?
 fanyu1年前4
fanyu1年前4 -
 种地不糊涂 共回答了12个问题
种地不糊涂 共回答了12个问题 |采纳率100%它是分子构成 属于分子晶体 作用力肯定是范德华力了 溶解性可以根据相似相溶原理解释1年前查看全部
- 化学酸碱盐溶解性顺口溜“钾钠铵盐硝酸溶,盐酸盐中除去银,碳磷酸溶钾钠铵,硫酸铅和钡不溶”是什么意思?
 怎么爱都不够1年前3
怎么爱都不够1年前3 -
 longjingbinbin 共回答了19个问题
longjingbinbin 共回答了19个问题 |采纳率73.7%就是初中阶段常见盐的溶解性
以一句就是指钾钠铵的盐溶液易溶于水,例如碳酸钾碳酸钠氯化钠氯化铵硫酸钾,等等
第二句指AgCl不易溶于水(极难溶)
第三句知此俩酸根离子盐只有钾钠铵溶,即碳酸钠,碳酸钾,碳酸铵,其他不溶,如碳酸钡,碳酸钙等等不溶.
最后一句与第2句类似1年前查看全部
- 溶解度是对物质溶解性的定量表示,在理解固体物质和气体物质溶解度的定义时,你认为应分别抓住哪些关键因素?
 牛人杰1年前1
牛人杰1年前1 -
 瓦拉杜利德 共回答了19个问题
瓦拉杜利德 共回答了19个问题 |采纳率100%固体 温度 单位是g
气体 温度和压强 单位是体积
都有溶质和溶剂的性质 饱和状态1年前查看全部
- 酸碱和盐的溶解性表的读法~例如:H2SO4(硫酸),HCL(盐酸),HNO3(硝酸) NaOH(氢氧化钠),KOH(氢氧
酸碱和盐的溶解性表的读法~
例如:H2SO4(硫酸),HCL(盐酸),HNO3(硝酸)
NaOH(氢氧化钠),KOH(氢氧化钾),NH4OH(氨水)
Na2CO3(碳酸钠),CuSO4(硫酸铜) ,NH4NO3(硝酸铵) bmx9991年前1
bmx9991年前1 -
 13aizjb 共回答了14个问题
13aizjb 共回答了14个问题 |采纳率92.9%H2CO3【碳酸】.HF【氢氟酸】
CaOH【氢氧化钙】.Cu(OH)2【氢氧化铜】.Fe(OH)2【氢氧化亚铁】.Fe(OH)3【氢氧化铁】.
CaCO3【碳酸钙】.Ca2NO3【硝酸钙】.Na2CO3【碳酸钠】.AgCl【氯化银】1年前查看全部
- 酸碱盐溶解性口诀是怎么用的?碱:钾钙钡溶 钙微溶硝酸盐全溶氯化物只有银不溶硫酸盐:钙银微溶钡不溶碳酸盐:铵钾钠溶镁微溶到
酸碱盐溶解性口诀是怎么用的?
碱:钾钙钡溶 钙微溶
硝酸盐全溶
氯化物只有银不溶
硫酸盐:钙银微溶钡不溶
碳酸盐:铵钾钠溶镁微溶
到底是什么意思 ?
怎么算是溶怎么算是不溶 ?
列几个化学方程式 来说明下 谢谢. fransico1年前2
fransico1年前2 -
 屋檐de风铃 共回答了20个问题
屋檐de风铃 共回答了20个问题 |采纳率90%钾,钠,铵,盐,硝酸盐, 都能溶解水中间. 盐酸盐不容银,亚汞, 硫酸盐不容钡和铅, 碳酸盐照顾溶钾钠铵
溶解性口诀一
钾钠铵盐溶水快 , ① 硫酸盐除去钡铅钙. ② 氯化物不溶氯化银, 硝酸盐溶液都透明. ③ 口诀中未有皆下沉. ④ 注: ①钾钠铵盐都溶于水; ②硫酸盐中只有硫酸钡、硫酸铅、硫酸钙不溶; ③硝酸盐都溶于水; ④口诀中没有涉及的盐类都不溶于水;
溶解性口诀二
钾、钠、铵盐、硝酸盐; 氯化物除银、亚汞; 硫酸盐除钡和铅; 碳酸、磷酸盐,只溶钾、钠、铵. 说明,以上四句歌谣概括了8类相加在水中溶解与不溶的情况.
溶解性口诀三
钾钠铵硝皆可溶、盐酸盐不溶银亚汞; 硫酸盐不溶钡和铅、碳磷酸盐多不溶. 多数酸溶碱少溶、只有钾钠铵钡溶
溶解性口诀四
钾、钠、硝酸溶, (钾盐、钠盐和硝酸盐都溶于水.) 盐酸除银(亚)汞, (盐酸盐里除氯化银和氯化亚汞外都溶.) 再说硫酸盐,不容有钡、铅, (硫酸盐中不溶的是硫酸钡和硫酸铅.) 其余几类盐, (碳酸盐、亚硫酸盐、磷酸盐、硅酸盐和硫化物) 只溶钾、钠、铵, (只有相应的钾盐、钠盐和铵盐可溶) 最后说碱类,钾、钠、铵和钡. (氢氧化钾、氢氧化钠、氢氧化钡和氨水可溶) 另有几种微溶物,可单独记住.
溶解性口诀五
钾钠铵盐硝酸盐 完全溶解不困难 氯化亚汞氯化银 硫酸钡和硫酸铅 生成沉淀记心间 氢硫酸盐和碱类 碳酸磷酸硝酸盐 可溶只有钾钠铵
溶解性口诀六(仅适用于初中)
钾钠铵盐都可溶 硝酸盐入水无影踪 氯化物不容氯化银 硫酸盐不溶硫酸钡 碳酸盐只溶钾钠铵 减溶钾钠钙和钡
谢谢,望采纳
谢谢,1年前查看全部
- 在氢氧化钠,氢氧化钡,氢氧化钙,氨气中按溶解性,按电离程度排序
 2007yexin1年前3
2007yexin1年前3 -
 佩玉女子SOPHIA 共回答了17个问题
佩玉女子SOPHIA 共回答了17个问题 |采纳率88.2%楼上及基本正确,但最后一个错了.因为在有两级电离的情况下,是先发生一级电离,然后再二级电离,而且第二个可忽略.
NaOH = Na+ + OH-
Ba(OH)2 = Ba2+ + 2OH-
Ca(OH)2 = Ca2+ + 2OH-
MgCI2 = Mg2+ + 2CI-
CuSO4 = Cu2+ + SO42-
NaCO3 = 2Na+ + CO32-
K2SO4 =2 K+ + SO42-
FeCI3 = Fe3+ + 3CI-
(NH4)2CO3 = 2NH4+ + CO32-
NaHCO3 = Na+ + HCO3- ,HCO3-=H+ + CO32-1年前查看全部
- 【求助】一般说来,丙酮和THF哪个溶解性好
 wzd11年前1
wzd11年前1 -
 aflv_e_2dcf0545 共回答了12个问题
aflv_e_2dcf0545 共回答了12个问题 |采纳率91.7%这个主要得看你的物质结构,一般说来,THF的溶解性要稍微好点吧!从极性上考虑是的1年前查看全部
- 部分酸碱盐溶解性亚硫酸钡沉淀是否溶于稀硝酸?硫酸钙和亚硫酸钙哪个溶解性强?硫酸银是否是沉淀(微溶还是不溶),如果是是否溶
部分酸碱盐溶解性
亚硫酸钡沉淀是否溶于稀硝酸?
硫酸钙和亚硫酸钙哪个溶解性强?
硫酸银是否是沉淀(微溶还是不溶),如果是是否溶于稀硝酸?
碳酸银是否溶于稀硝酸?碳酸银是否溶于稀硝酸?亚硫酸银是否溶与稀硝酸?
请帮助我的朋友按步骤答,不然我会看不懂的 .谢谢大家了(以上问题如有涉及水解问题暂不考虑,以上物质均在20°的时候考虑) yanglu20082001年前2
yanglu20082001年前2 -
 桑梓印象 共回答了16个问题
桑梓印象 共回答了16个问题 |采纳率81.3%亚硫酸钡沉淀是否溶于稀硝酸?不能溶于稀硝酸(其氧化性会将亚硫酸根氧化成硫酸根)
硫酸钙和亚硫酸钙哪个溶解性强?硫酸钙
硫酸银是否是沉淀(微溶还是不溶),如果是是否溶于稀硝酸?微溶,不溶于稀硝酸
碳酸银是否溶于稀硝酸?亚硫酸银是否溶与稀硝酸?碳酸银溶于稀硝酸,亚硫酸银不溶于稀硝酸(其氧化性会将亚硫酸根氧化成硫酸根)1年前查看全部
大家在问
- 1“七”和"二"的篆书写法
- 2英语翻译随着经济组织的不断扩大和其内部结构复杂化,经济组织之间的联系更加紧密,而伴随的是经济纠纷趋于多样化和复杂化,经济
- 3幼儿园买来五箱香蕉,每箱重20千克,平均分给4个班的小朋友,每个班分到的香蕉占总数的几分之几?
- 4森林的树冠就像一把把大伞.(改成问句,保持句意不变)
- 5浓硫酸与铜的反应中,浓硫酸只表现强氧化性是错误的?
- 6构造一个一元二次方程要求常数项不为0且一个根为-2
- 7With the machine( )all the work,we will finish our task in t
- 8一道烦死人的物理题:甲和乙两位同学骑着自行车沿一条笔直的马路相对而行,甲骑车的速度是.
- 9下列不是巴金的作品有?A海上日出 B家 C春 D秋 E荷塘月色
- 10I know Thanksgiving is a traditional festival in
- 11赞美地球美丽的句子急
- 12英语 (22 19:12:39)
- 13宇航员在地球表面以一定初速度竖直上抛一小球,经过时间t小球落回原处;若他在某星球表面以相同的初速度竖直上抛同一小球,需经
- 14已知函数f(x)=㏑x-a/x,若对于任意x属于(1,正无穷)都有f(x)>-x+2,求a的取值范围
- 15英语翻译A.于是沛公起,摄衣谢之,延上坐.这时候,沛公站起来,整理衣服,并把郦食其请到上座.B.然嬴欲就公子之名,故久立
