有17,8g碳酸氢钾与氢氧化钾的固体混合物,在密闭容器中加热充分反应后排出剩余气体,
 102320062022-10-04 11:39:541条回答
102320062022-10-04 11:39:541条回答
有17,8g碳酸氢钾与氢氧化钾的固体混合物,在密闭容器中加热充分反应后排出剩余气体,
固体质量减小了4g,问原混合物中各组分的含量.
我只能判断出碳酸氢钾过量,然后怎么算,
差量法怎么算呢?
固体质量减小了4g,问原混合物中各组分的含量.
我只能判断出碳酸氢钾过量,然后怎么算,
差量法怎么算呢?

已提交,审核后显示!提交回复
共1条回复
 悠悠22 共回答了18个问题
悠悠22 共回答了18个问题 |采纳率100%- 应该会有两种结果:
一】KOH过量,加热后排出的是水蒸气,4g就是水蒸气的质量
二】KHCO3过量,这时比较麻烦,可以按照K的物质的量守恒来算,因为最后只剩下K2CO3,可以列二元一次方程组,解算相对复杂,不过好理解,需要详细过程继续追问 - 1年前
相关推荐
- 高一上册物质的量浓度计算题1.白色粉末A是碳酸氢钠和碳酸氢钾的混合物,取甲、乙、丙三份质量不同的A样品分别于50ml相同
高一上册物质的量浓度计算题
1.白色粉末A是碳酸氢钠和碳酸氢钾的混合物,取甲、乙、丙三份质量不同的A样品分别于50ml相同浓度的盐酸充分反应,得到的气体的体积(标准状况)与A的质量关系如下表所示:
求:(1)盐酸的物质的量浓度.
(2)混合物中氢氧化钠的质量分数.
这节课跟不上.以后的化学就不用学了~在下感激不尽~
不好意思,是碳酸氢钠~手误手误~对不起~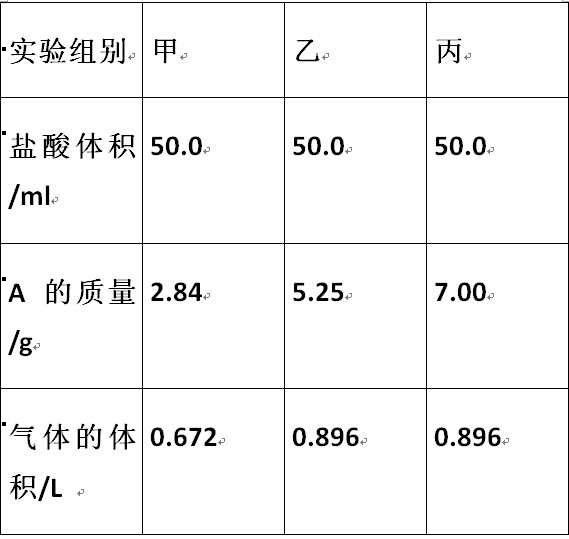
 lql3445081年前1
lql3445081年前1 -
 blaze_001 共回答了15个问题
blaze_001 共回答了15个问题 |采纳率93.3%(1)图中所示乙丙最后所得气体体积相同,可知丙反应的盐酸已反应完全.
0.896/22.4=0.04mol 则盐酸反应的量也是0.04mol
所以盐酸的物质的亮的浓度为:0.04mol/0.05L=0.8mol/L
(2)由图可知甲反应的混合物已反应完全.
0.672/22.4=0.03mol 则可知参加反应的碳酸氢根离子为0.03mol
设碳酸氢钠为Xmol,则碳酸氢钾为(0.03-X)mol
84X+100(0.03-X)=2.84 得X=0.01mol
所以碳酸氢钠的质量分数为 0.01*84/2.84=29.6%
楼上的明明就做错了,竟然不采纳我的.1年前查看全部
- 鉴别碳酸钾和碳酸氢钾,加入少量的盐酸为什么就不行呢?
 hzxrqifb1年前1
hzxrqifb1年前1 -
 最后yy枫叶 共回答了17个问题
最后yy枫叶 共回答了17个问题 |采纳率64.7%因为你控制不好量.少量又不是适量,你也不知道什么时候加过了.如果盐酸加过了,现象就一样了.而你又不知道药品有多少,所以不行.鉴定要排除量的关系,量不能影响鉴定现象,否则就不能作为鉴定手段.鉴定就是要根据特殊性来看.1年前查看全部
- 两个质量相等的烧杯中,分别盛500ml0.2mol/L的盐酸然后分别加m克碳酸钙和碳酸氢钾,
两个质量相等的烧杯中,分别盛500ml0.2mol/L的盐酸然后分别加m克碳酸钙和碳酸氢钾,
若反应后两烧杯质量相等,则m、n为 风雨无名哥1年前1
风雨无名哥1年前1 -
 237343 共回答了24个问题
237343 共回答了24个问题 |采纳率100%相等.
分析:因为两个质量相等的烧杯中,分别盛500ml0.2mol/L的盐酸,说明两个烧杯中盐酸的质量相等,加入m克碳酸钙和n克碳酸氢钾后,若反应后两烧杯质量相等,说明两烧杯内增加质量相等,
设烧杯内增加质量分别为W
CaCO3 + 2HCl =CaCl2 + H2O + CO2↑ △m
100 44 56
m W
m=25W/14
KHCO3 + HCl =KCl + H2O + CO2↑ △m
100 44 56
n W
n=25W/14
所以m=n1年前查看全部
- 将m克碳酸钙与n克碳酸氢钾分别加入100毫升0.5摩尔/毫升的盐酸中.若反应后两种溶液的质量相等,则m与n的关系是:
将m克碳酸钙与n克碳酸氢钾分别加入100毫升0.5摩尔/毫升的盐酸中.若反应后两种溶液的质量相等,则m与n的关系是:
(要解题思路与做题全过程,细致的)谢谢.
有四个选项
A m=n小等2.5
B m=n大于2.5
C m=n大等5
D m小于n小于2.5
希望不要用排除法,或极值法解。
另外,希望诸位高人能对此类题型指点一二。 马镇的春天1年前3
马镇的春天1年前3 -
 bf109eee 共回答了16个问题
bf109eee 共回答了16个问题 |采纳率100%这种题目,尝试用作图的方式分析
CaCO3 + 2HCl = CaCl2 + H2O + CO2
KHCO3 + HCl = KCl + H2O + CO2
现在,n(HCl)=0.05mol
需要CaCO3,0.025mol,即2.5g,需要KHCO3,0.05mol,即5g
--------2.5g------------5g-------------------->m(固体)
几种情况
1、m5,即固体过量,盐酸不足量,用HCl计算,注意两个方程式,1mol的HCl生成CO2不等,即m=n时,产生CO2不等,不能平衡
4、同样,m>2.5时,若m=n,则生成CO2不等,不能平衡
所以,答案是A
此类题形式很多,可以是金属与酸反应生成H2,也可以是碳酸盐与酸反应生成CO2,还可以是Al与HCl或NaOH反应生成H2等等,特点相似,都是加入固体,会生成气体,判断天平是否平衡
都可以采用数轴分析,找到几个反应的恰好点,再分成几种情况讨论,注意都是比较的
m(固体)-m(气体)1年前查看全部
- 碳酸氢钾与氢氧化钡等物质的量反应方程式
 宇傲07071年前2
宇傲07071年前2 -
 疯雨人生 共回答了18个问题
疯雨人生 共回答了18个问题 |采纳率77.8%KHCO3 + Ba(OH)2 == BaCO3(沉淀) + KOH + H2O1年前查看全部
- 电解质和非电解质分类碳酸氢钾溶液不是混合物吗,为什么是电解质?氯水为什么可以导电?硫化氢和氢氧化铝的弱电解性是怎么来的?
 命运我要与你抗争1年前1
命运我要与你抗争1年前1 -
 lili311 共回答了16个问题
lili311 共回答了16个问题 |采纳率87.5%KHCo3溶液是混合物啊~大概是没说全面吧~这个应该叫电解质溶液
Cl2溶在水中,实际是Cl2与水发生反应,产生了可电解的HCl等东东,可以看看高中化学书卤素元素那一章.
H2S&AL(OH)3的弱电解性.H2S和水发生反应生成氢硫酸,微弱电离.
AL(OH)3是两性的氢氧化物,既是弱酸又是弱碱,可以看高中化学的金属元素那一章.1年前查看全部
- 一个简单的计算题有ag等物质的量的碳酸氢钠和碳酸氢钾的混合物与100ML的盐酸反应求,若反应完全,则HCL的物质的量浓度
一个简单的计算题
有ag等物质的量的碳酸氢钠和碳酸氢钾的混合物与100ML的盐酸反应
求,若反应完全,则HCL的物质的量浓度是多少?
我算的是5a/92
答案是5a/46
tell me why? 笨笨火1年前3
笨笨火1年前3 -
 jalenlyx 共回答了19个问题
jalenlyx 共回答了19个问题 |采纳率94.7%设碳酸氢钠和碳酸氢钾的物质的量都为x
则84x+100x=a 得x=a/(84+100)
碳酸氢钠和碳酸氢钾的物质的量和:2a/(84+100)
设HCL的物质的量浓度为n
由于无论碳酸氢钠还是碳酸氢钾与HCL1:1反应
根据物质的量守恒:2a/(84+100)=100n/1000
求得n=5a/461年前查看全部
- 碳酸氢钾溶液与石灰水反应的离子反应方程式
 无盐胜雪1年前1
无盐胜雪1年前1 -
 frienzero 共回答了28个问题
frienzero 共回答了28个问题 |采纳率85.7%分过量与少量;
KHCO3过量,就生成碳酸钾盐、碳酸钙与水;
石灰水过量,就生成,水,碳酸钙与氢氧化钾.1年前查看全部
- 氢氧化钠与碳酸氢钾反应方程式急
 说话的老虎1年前3
说话的老虎1年前3 -
 qq3456233 共回答了20个问题
qq3456233 共回答了20个问题 |采纳率90%2NaOH+2KHCO3=Na2CO3+K2CO3+2H2O1年前查看全部
- 氯化钡和碳酸氢钾的反应的化学方程式
氯化钡和碳酸氢钾的反应的化学方程式
BaCl2+2KHCO3=BaCO3↓+2KCl+CO2↑ +H2O
BaCl2+KHCO3=BaCO3↓+KCl +HCl
这两个哪个不合理 理由是什么 zlzz90371年前1
zlzz90371年前1 -
 weige888 共回答了9个问题
weige888 共回答了9个问题 |采纳率88.9%2不合理
因为所有反应都是强电解质反应生成弱电解质,强酸是强电解质,弱酸是弱电解质.所以反应不会发生.
1合理.有沉淀生成1年前查看全部
- 碳酸氢镁 碳酸氢铵 碳酸氢钾 碳酸氢钠 它们分别属于酸碱盐里的哪一种?为什么?它们能溶于水吗?
 大肥羊和小老虎1年前2
大肥羊和小老虎1年前2 -
 只是交流而已 共回答了14个问题
只是交流而已 共回答了14个问题 |采纳率85.7%他们都属于盐,且都是酸式盐,都能溶于水
判断酸碱盐的方法如下:
一般方法:酸:阳离子:只有氢离子,阴离子失酸根离子
碱:阳离子:金属离子(或铵根离子),阴离子只有氢氧根离子
盐:只要有酸根离子和金属离子(或铵根离子)就是盐
比如碱式碳酸铜、碳酸氢铵比较复杂吧,但是根据以上就可判断他们都是盐,因为他们有酸根离子和金属离子(或铵根离子),其他离子就不要管了.
怎么排除酸和碱:如碳酸氢铵中,阳离子除了氢离子还有铵根离子所以不是酸
再如碱式碳酸铜:不是碱,因为阴离子除了氢氧根还有碳酸根.1年前查看全部
- 碳酸氢钾与硫酸反应方程式和离子方程式
 加钢淬火1年前1
加钢淬火1年前1 -
 luherjin 共回答了12个问题
luherjin 共回答了12个问题 |采纳率83.3%2KHCO₃+ H₂SO₄==== K₂SO₄+ 2H₂O + 2CO₂↑
HCO₃- + H+ ==== H₂O + CO₂↑1年前查看全部
- 碳酸氢钾与石灰水反应的离子方程式(过量与少量石灰水)
 灰姑娘_keinly1年前3
灰姑娘_keinly1年前3 -
 小钉一个 共回答了16个问题
小钉一个 共回答了16个问题 |采纳率93.8%HCO3- + Ca2+ + OH- -----> CaCO3 + H2O(过量石灰水)
2HCO3- + Ca2+ + 2OH- -----> CaCO3 + CO32- + 2H2O(少量石灰水)1年前查看全部
- 水蒸气 碳酸氢钾一到方程式
 10福临门1年前2
10福临门1年前2 -
 bo820308 共回答了24个问题
bo820308 共回答了24个问题 |采纳率91.7%H2O+CO2+K2CO3=2KHCO3
是不是这个
或者倒过来
2KHCO3==△==H2O+CO2↑+K2CO31年前查看全部
- 相同质量的碳酸钙和碳酸氢钾的物质的量之比是___物质的量相同的氧化钙和氢氧化钾的质量之比是__;
相同质量的碳酸钙和碳酸氢钾的物质的量之比是___物质的量相同的氧化钙和氢氧化钾的质量之比是__;
氧气、二氧化碳、二氧化硫三者的物质的量之比为__时,它们所含的氧原子数相同;三氧化硫、二氧化硫、氧气三者的质量之比为5:4:2时,它们的分子个数比是__,物质的量之比是__ 纤纤洁1年前2
纤纤洁1年前2 -
 daisy070707 共回答了24个问题
daisy070707 共回答了24个问题 |采纳率100%相同质量的碳酸钙和碳酸氢钾的物质的量之比是1:1物质的量相同的氧化钙和氢氧化钾的质量之比是
1:1
氧气、二氧化碳、二氧化硫三者的物质的量之比为1:1:1_时,它们所含的氧原子数相同;三氧化硫、二氧化硫、氧气三者的质量之比为5:4:2时,它们的分子个数比是4:3:2,物质的量之比是1:1:1_1年前查看全部
- 25.6克氢氧化钾和碳酸氢钾混合物在250℃煅烧冷却后固体质量20.7克,原混合物中氢氧化钾和碳酸氢钾质量比
25.6克氢氧化钾和碳酸氢钾混合物在250℃煅烧冷却后固体质量20.7克,原混合物中氢氧化钾和碳酸氢钾质量比
A 大于56:100 B小于56:100 C等于56:100 D任意比例混合
请问选择哪个,为什么? 炽血天使1年前1
炽血天使1年前1 -
 cifjeek 共回答了21个问题
cifjeek 共回答了21个问题 |采纳率81%应该选择的是B,首先看到的是当氢氧化钾和碳酸氢钾1:1充分反应时,质量比为56:100.
假设他们是1:1反应,那么反应生成的水的质量大约在2.9左右(设反应的物质的量为X,解得的数据即为反应生成水的物质的量),然而反应损失的质量大于2.9,因此反应不止生成了水,还有其他物质生成,即为碳酸氢钾分解.因此答案为B1年前查看全部
- 已知固体混合物A有碳酸氢钠 碳酸氢钾 碳酸镁 碳酸钙四种物质中的两种物质混合而成,通过计算和推理回答下面问题:
已知固体混合物A有碳酸氢钠 碳酸氢钾 碳酸镁 碳酸钙四种物质中的两种物质混合而成,通过计算和推理回答下面问题:
⑴ 取A与足量盐酸反应:
①若A的总物质的量为定值,生成气体的量也为定值,则A的组成最多有几种
②若A的总质量为定值,生成气体的量也为定值,则A的组成可能是什么
⑵若先将A加热一段时间后,冷却后的剩余固体再与足量盐酸反应且先后两次产生的气体分别通入足量的澄清石灰水中,生成的沉淀均为10克,则A的总物质量为多少?A的组成有几种?可能是什么? 偶然在转角1年前1
偶然在转角1年前1 -
 香猪猪 共回答了16个问题
香猪猪 共回答了16个问题 |采纳率93.8%四种物质的式量分别为84,100,84,100
1.1 任意两种的组合均满足,故有6种组合
1.2 必须两种物质式量相等,所以可能是碳酸氢钠和碳酸镁,也可能是碳酸氢钾和碳酸钙
2.加热放出CO2 0.1 mol,加入盐酸又放出0.1 mol,这次没的商量了,只能是两种碳酸氢盐的混合物,两者的总量为0.2 mol.加热放出二氧化碳0.1 mol,加入盐酸又放出二氧化碳0.1 mol.
如果含有碳酸镁或者碳酸钙,那么加热放出的二氧化碳一定比加入盐酸放出的二氧化碳少.1年前查看全部
- 碳酸钾和碳酸氢钾的混合物与硫酸反应 随着混合物质量的增加 生成的CO2从0.03到0.0375到0.03 为什么
 暖FF1年前1
暖FF1年前1 -
 wulin1200 共回答了13个问题
wulin1200 共回答了13个问题 |采纳率100%首先是碳酸氢钾与硫酸反应,生成二氧化碳0.2,接着碳酸钾再反应.最后有部分又与水反应,所以最后剩的只有0.31年前查看全部
- 取9.2g碳酸氢钠和碳酸氢钾组成的混合物加入足量的某浓度的盐酸中,
取9.2g碳酸氢钠和碳酸氢钾组成的混合物加入足量的某浓度的盐酸中,
取9.2g碳酸氢钠喝和碳酸氢钾组成的混合物加入足量的某浓度的盐酸中,产生标准状况下2.24L气体球混合物中碳酸氢钠和碳酸氢钾的物质的量之比 **也要说谎1年前1
**也要说谎1年前1 -
 moke100 共回答了13个问题
moke100 共回答了13个问题 |采纳率100%1:1
CO2的物质的量是n=V/Vm=2.24/22.4=0.1mol
设NaHCO3的物质的量为x,KHCO3的质量为y.
NaHCO3+HCl=NaCl+H2O+CO2↑
1 1
x x
KHCO3+HCl=KCl+H2O+CO2↑
1 1
y y
x+y=0.1
84x+100y=9.2
x=0.05mol
y=0.05mol
碳酸氢钠和碳酸氢钾的物质的量之比是0.05:0.05=1:11年前查看全部
- 化学反应先后硫酸氢铵比硫酸铵先和氢氧化钠溶液反应,为什么?碳酸钾比碳酸氢钾先和稀硫酸反应,为什么?(“碳酸根离子加氢离子
化学反应先后
硫酸氢铵比硫酸铵先和氢氧化钠溶液反应,为什么?
碳酸钾比碳酸氢钾先和稀硫酸反应,为什么?(“碳酸根离子加氢离子生成碳酸氢根离子”的反应) huyjh1年前3
huyjh1年前3 -
 伯德 共回答了15个问题
伯德 共回答了15个问题 |采纳率100%硫酸氢铵能电离出氢离子,酸性更强,所以氢氧化钠先和硫酸氢铵反应
碳酸钾的碱性更强,所以稀硫酸先和它反应1年前查看全部
- 可溶性碳酸氢盐的溶解度是如何变化的 例如碳酸氢钠的溶解度为何比碳酸氢钾小,
 fishbh1年前1
fishbh1年前1 -
 castorli1980 共回答了17个问题
castorli1980 共回答了17个问题 |采纳率88.2%物质溶解性影响因素很多.如果非要回答的话:由于K+的半径大于Na+,它们与HCO3-形成的离子键中,Na+的极化要强些,换句话说,NaHCO3中的离子键强,晶格能要大一些,所以要难溶一些.1年前查看全部
- 碳酸钾和碳酸氢钾水溶液都呈碱性是否就意味着都是碱式盐?
 蓬莱仙阁1001年前3
蓬莱仙阁1001年前3 -
 东北地 共回答了21个问题
东北地 共回答了21个问题 |采纳率95.2%碱式盐和其水溶液呈碱性完全是两码事,碱式盐都是诸如 Cu2(OH)2CO3这种含氢氧根的盐1年前查看全部
- 碳酸钾和碳酸氢钾的区别方法鉴别方法,至少3种
 -恋之风景-1年前1
-恋之风景-1年前1 -
 失去眼泪 共回答了10个问题
失去眼泪 共回答了10个问题 |采纳率100%溶于水后用盐酸滴加立即有气泡的是碳酸氢钾 溶于水后 用氯化钙溶液滴加有沉淀的是碳酸氢钾 加热比较重量变轻的是碳酸氢钾1年前查看全部
- 为了测定碳酸钾和碳酸氢钾混合物的组成,某学生每次取一定质量的混合物溶于水配成溶液,向其中加入相同浓度的氢氧化钡溶液,每次
为了测定碳酸钾和碳酸氢钾混合物的组成,某学生每次取一定质量的混合物溶于水配成溶液,向其中加入相同浓度的氢氧化钡溶液,每次试验均充分反映,实验结果记录如下表.
为了测定碳酸钾和碳酸氢钾混合物的组成,某学生每次取一定质量的混合物溶于水配成溶液,向其中加入相同浓度的氢氧化钡溶液,每次试验均充分反映,实验结果记录如下表.
(1)第二次实验中产生沉淀的质量是__________g.
(2)求所用氢氧化钡溶液的物质的量浓度,
(3)求混合物中碳酸钾和碳酸氢钠的物质的量之比 sisilbs1年前1
sisilbs1年前1 -
 风子6 共回答了19个问题
风子6 共回答了19个问题 |采纳率89.5%由表中的沉淀数据可知,
1)第二次实验中产生沉淀的质量是2.758克.且第四次混合物与氢氧化钡恰好完全反应.
有反应K2CO3+Ba(OH)2=BaCO3+2KOH 2KHCO3+Ba(OH)2=BaCO3+H2O+K2CO3可得:
5.516克碳酸钡物质的量为:5.516除以197=0.028摩尔
Ba(OH)2—————— BaCO3
1摩尔 1摩尔 所以反应的氢氧化钡物质的量为0.028摩尔.
(2)所用氢氧化钡溶液的物质的量浓度:0.028除以0.5=0.056摩尔每升
(3)设碳酸钾物质的量为x,碳酸氢钾物质的量为y
x+y=0.028 ---------(1)
138x+100y=3.432-------(2)
解(1)、(2)组成的方程组得x=0.011 y=0.017
混合物中碳酸钾和碳酸氢钠的物质的量之比11:171年前查看全部
- 硫酸氢钠与碳酸氢钾的反应方程式
 zmc351年前1
zmc351年前1 -
 452863509 共回答了17个问题
452863509 共回答了17个问题 |采纳率82.4%2NaHSO4+2KHCO3==Na2SO4+K2SO4+2H2O+2CO2↑1年前查看全部
- 10微升的2M高氯酸和1.5M的碳酸氢钾中和至中性,需要多少碳酸氢钾?反应方程式怎么写啊?
10微升的2M高氯酸和1.5M的碳酸氢钾中和至中性,需要多少碳酸氢钾?反应方程式怎么写啊?
反应方程式到底怎么写?需要多少碳酸氢钾,计算就可以还是需要滴定才可确定? 来电查询1年前2
来电查询1年前2 -
 znqkkkk 共回答了18个问题
znqkkkk 共回答了18个问题 |采纳率88.9%由强到弱依次为:高氯酸,氢碘酸,硫酸,氢溴酸,盐酸,硝酸,碘酸,三氯乙酸(以上为强酸,了解即可,大学涉及强弱排序),草酸(乙二酸),顺丁烯二酸,亚硫酸,磷酸,丙酮酸,丙二酸,氯乙酸,邻苯二甲酸,水杨酸,酒石酸,亚硝酸(以上十一种为中强酸),反丁烯二酸,柠檬酸,氢氟酸,苹果酸,葡萄糖酸,甲酸,乳酸,苯甲酸,丙烯酸,甲基丙烯酸,丁烯酸,乙酸,丙酸,油酸,硬脂酸,碳酸,氢硫酸,次氯酸,硼酸,硅酸,苯酚(其余为弱酸或极弱酸)!1年前查看全部
- 什么东西跟碳酸氢钾反应生成氢氧化钾?
 phxiaoy1年前1
phxiaoy1年前1 -
 无根小小草 共回答了17个问题
无根小小草 共回答了17个问题 |采纳率100%碳酸氢钾和氢氧化钙加热生成氢氧化钾和碳酸氢钙 碳酸氢钙不稳定加热会变成碳酸钙和二氧化碳和水 2NaHCo3+Ca(oH)2==加热==2NaoH+CaCo3+H2o+Co2气体符号
麻烦采纳,谢谢!1年前查看全部
- 硫酸氢钠与碳酸氢钾离子反应方程式是什么啊
 jabo1年前3
jabo1年前3 -
 晓庆 共回答了17个问题
晓庆 共回答了17个问题 |采纳率100%H+ + HCO3- = H20 + CO21年前查看全部
- 以下物质是强电解质还是弱电解质硫酸氢钾,碳酸氢钙,亚硫酸氢钠,溴化亚铁,明矾,碳酸氢钾.化学式是什么``
 ztj5161年前4
ztj5161年前4 -
 jssqakfire 共回答了19个问题
jssqakfire 共回答了19个问题 |采纳率100%都是强电解质
Ca(HCO3)2 NaHSO3 FeBr2 KAl(SO4)2*12H2O KHCO31年前查看全部
- 这里有几道关于除杂质的问题1,碳酸氢钾中含有少量的碳酸钾2,食盐中混有少量的硝酸钾3,苛性钠中混有少量纯碱4,过氧化钠中
这里有几道关于除杂质的问题
1,碳酸氢钾中含有少量的碳酸钾
2,食盐中混有少量的硝酸钾
3,苛性钠中混有少量纯碱
4,过氧化钠中混有少量的氧化钠 天空城市1年前3
天空城市1年前3 -
 zxg740629 共回答了21个问题
zxg740629 共回答了21个问题 |采纳率90.5%1.碳酸氢钾中含有少量的碳酸钾 ----通入CO2或SO2
2.食盐中混有少量的硝酸钾 ----高温下配制成(饱和)溶液,冷却结晶过滤
3.苛性钠中混有少量纯碱 ------加入澄清石灰水过滤,再加少量稀盐酸,加热蒸发结晶
4,过氧化钠中混有少量的氧化钠 -----在氧气流中加热1年前查看全部
- 怎样鉴别碳酸钾和碳酸氢钾?给写出方程式来,
 baypcc1年前5
baypcc1年前5 -
 tangjiba 共回答了16个问题
tangjiba 共回答了16个问题 |采纳率81.3%加入氯化钙 有沉淀生成的是碳酸钾 另一是碳酸氢钾
要注意是不可以使用碱的 因为会和碳酸氢根反应生成碳酸根 会影响检验.1年前查看全部
- 碳酸钾中混入碳酸氢钾怎么除去?
 天天56951年前1
天天56951年前1 -
 xixili1984 共回答了20个问题
xixili1984 共回答了20个问题 |采纳率100%加热
碳酸氢钾受热分解生成碳酸钾,二氧化碳,水
方程式为2KHCO3=H2O+K2CO3+CO2
把钾元素换成钠元素或者钙元素也是一样的.1年前查看全部
- 碳酸钾和碳酸氢钾的溶解性请问谁知道碳酸钾和碳酸氢钾在一些非极性有机溶剂中是否有溶解性?特别是能告知其能溶于某种具体的有机
碳酸钾和碳酸氢钾的溶解性
请问谁知道碳酸钾和碳酸氢钾在一些非极性有机溶剂中是否有溶解性?特别是能告知其能溶于某种具体的有机溶剂. 现在几点钟了1年前1
现在几点钟了1年前1 -
 jbwzqpst 共回答了16个问题
jbwzqpst 共回答了16个问题 |采纳率81.3%不溶于非极性有机溶剂.甲醇或乙醇等极性很强的有机溶剂也许可以溶解一些,注意甲醇毒性很强,需在通风橱中操作.1年前查看全部
- 碳酸氢钾与盐酸反应的化学方程式是什么
 2006051207181年前3
2006051207181年前3 -
 恨_天 共回答了19个问题
恨_天 共回答了19个问题 |采纳率94.7%KHCO3 + HCl = KCl + H2O + CO21年前查看全部
- 氢氧化钾与碳酸氢钾反应化学方程式
 检举a1年前1
检举a1年前1 -
 蓝幻 共回答了14个问题
蓝幻 共回答了14个问题 |采纳率100%KOH+KHCO3=K2CO3+H2O1年前查看全部
- 碳酸氢钠与碳酸氢钾反应方程式对不起打错了是硫酸氢钾,最好写一下离子方程式
 wshefeng1年前3
wshefeng1年前3 -
 gfsdghdfhjgfjk 共回答了22个问题
gfsdghdfhjgfjk 共回答了22个问题 |采纳率95.5%二者应该不反应吧,可能是硫酸氢钾
2NaHCO3 + 2KHSO4 = Na2SO4 + K2SO4 + 2 H2O + 2 CO2↑1年前查看全部
- 碳酸钠能用结晶法提取码?在碳酸钠,碳酸钾和碳酸氢钾的混合物中,碳酸钠能否用结晶法提取?具体怎样做?
 池花落无声1年前1
池花落无声1年前1 -
 ivycch 共回答了27个问题
ivycch 共回答了27个问题 |采纳率88.9%碳酸钠能用结晶法提取.具体操作如下:把碳酸钠,碳酸钾和碳酸氢钾的混合物溶于水制成较高温度的饱和溶液,然后冷却热饱和溶液到10 ℃,在10 ℃碳酸钠的溶解度为12.2克、碳酸氢钠的溶解度为8.15克、碳酸钾的溶解度为109...1年前查看全部
- 73、目前比较典型的化学干粉有碳酸氢钠、碳酸氢钾和()等三大类.A、碳酸钠 B磷酸二氢铵 C氯化氢 D碳酸
 angeltree1年前2
angeltree1年前2 -
 轩风蔚子 共回答了21个问题
轩风蔚子 共回答了21个问题 |采纳率95.2%选A
B不稳定容易分解
C是气体,还具有腐蚀性
D不稳定……而且是液体……1年前查看全部
- 碳酸氢钾和硝酸反应的方程式急求啊
 ameko03191年前1
ameko03191年前1 -
 Z_Amada 共回答了20个问题
Z_Amada 共回答了20个问题 |采纳率95%KHCO3+HNO3=KNO3+H2O+CO21年前查看全部
- 氯化钙和碳酸氢钾化学反应方程式化学反应的方程式是什么哪一个错了
 麦谷1年前1
麦谷1年前1 -
 liuzhaohuo 共回答了20个问题
liuzhaohuo 共回答了20个问题 |采纳率90%第一个是错的,楼主要明白的是这是一个特别活泼的可逆反应,反应几乎一正向反应后就被逆向进行,所以我们平时几乎认定他们不反应1年前查看全部
- 求下列反应的离子方程式1 往澄清石灰水中通入过量二氧化碳2 用3氯化铁溶液腐蚀印刷电路板3 氯化钙与碳酸氢钾溶液混合4
求下列反应的离子方程式
1 往澄清石灰水中通入过量二氧化碳
2 用3氯化铁溶液腐蚀印刷电路板
3 氯化钙与碳酸氢钾溶液混合
4 碳酸氢钙溶液加到醋酸中
5 锌片插入硝酸银溶液中
6 碳酸氢钙溶液和氢氧化钠溶液混合 fgw10051年前2
fgw10051年前2 -
 dongqing815 共回答了21个问题
dongqing815 共回答了21个问题 |采纳率76.2%1、OH- + CO2 ==HCO3-
2、2Fe3+ +Cu == 2Fe2+ +Cu2+
3、不反应
4、HCO3- + CH3COOH==CH3COO- + CO2(气体) +H2O
5、Zn +2Ag+ == Zn2+ +2Ag
6、有两种情况
Ca2+ +HCO3- +OH- ==CaCO3(沉淀) + H2O 氢氧化钠少量
Ca2+ +2HCO3- +2OH- ==CaCO3(沉淀) + CO32-+H2O 氢氧化钠过量1年前查看全部
- 已知固体混合物A由碳酸氢钠、碳酸氢钾、碳酸镁和碳酸钙四种物质中的两种混合而成,若先将A加热,剩余固体再和足量的盐酸反应,
已知固体混合物A由碳酸氢钠、碳酸氢钾、碳酸镁和碳酸钙四种物质中的两种混合而成,若先将A加热,剩余固体再和足量的盐酸反应,且先后两次产生的气体分别通过澄清石灰水,生成的沉淀均为10克,则A得物质的量为多少摩尔?
我需要具体的解题过程, ss13951年前1
ss13951年前1 -
 zhxguan_88 共回答了18个问题
zhxguan_88 共回答了18个问题 |采纳率94.4%先将A加热,--说明A受热能分解,生成CO2,即含NaHCO3,或KHCO3
剩余固体--即含Na2CO3,或K2CO3,再和足量的盐酸反应,
且先后两次产生的气体分别通过澄清石灰水,生成的沉淀均为10克,--即A只含NaHCO3和KHCO3
因为,若含MgCO3,或CaCO3,受热时不分解生成CO2,会导致前后两次CO2的量不等
生成的沉淀均为10克,--即前后生成CO2各为0.1mol,即共CO2为0.2mol,据C元素守恒,则源混合物为0.2mol1年前查看全部
- 60g碳酸钙与碳酸氢钾的混合物和足量的盐酸反应生成二氧化碳的分子数为多少
 yinyan8801061年前1
yinyan8801061年前1 -
 jokej 共回答了15个问题
jokej 共回答了15个问题 |采纳率100%两个化合物的相对分子质量都是100,碳原子和分子比都是1:1,即每个分子中有一个碳原子,与足量盐酸反应碳原子全部生成二氧化碳
原来碳原子的物质的量是 0.6mol 所以生成二氧化碳为0.6mol即0.6Na个分子1年前查看全部
- 已知固体混合物A由碳酸氢钠、碳酸氢钾、碳酸镁、碳酸钙四种物质中的两种混合而成
已知固体混合物A由碳酸氢钠、碳酸氢钾、碳酸镁、碳酸钙四种物质中的两种混合而成
已知固体混合物A由NaHCO3,KHCO3,MgCO3,CaCO3四种物质中的两种混合而成.
1.取A与足量的盐酸反应:
当A的物质的量一定时,无论两种物质以何种比例混合,生成气体的量均为一定值,则A的组成可能有____种.
当A的质量一定时,无论两种物质以何种比例混合,生成气体的量均为一定值,则A的组成可能(填化学式)___,___;____,____:____'_____.(可以不填满) 智者不很锐1年前1
智者不很锐1年前1 -
 小步爱雯婕 共回答了17个问题
小步爱雯婕 共回答了17个问题 |采纳率94.1%当A的物质的量一定时,无论两种物质以何种比例混合,生成气体的量均为一定值,则A的组成可能有__6__种.
当A的质量一定时,无论两种物质以何种比例混合,生成气体的量均为一定值,则A的组成可能(填化学式)NaHCO3,KHCO3 ;MgCO3,CaCO3 :.(可以不填满)1年前查看全部
- 要除去下列物质中括号内的杂质甲:碳酸钙(碳酸钠) 乙氢氧化钠(碳酸钠) 丙:氯化钾(碳酸氢钾) 丁:炭粉(氧化铜)可选用
要除去下列物质中括号内的杂质甲:碳酸钙(碳酸钠) 乙氢氧化钠(碳酸钠) 丙:氯化钾(碳酸氢钾) 丁:炭粉(氧化铜)可选用的试剂和操作方法有:①加入适量稀盐酸,搅拌、过滤 ②加入适量岁,搅拌过滤③加入适量稀盐酸,搅拌蒸发 ④溶解,加入适量澄清石灰水,过滤,蒸发.下列组合正确的是
A 甲——②,乙——③ B 乙——③,丙——①
C丙——①,丁——② D 丙——③,丁——① 朱嘉奇1年前1
朱嘉奇1年前1 -
 whpd 共回答了20个问题
whpd 共回答了20个问题 |采纳率80%D 丙——③, 丁——①1年前查看全部
- 物质的量浓度相同的碳酸钠与碳酸氢钾的碱性为什么是碳酸钠的碱性强?
物质的量浓度相同的碳酸钠与碳酸氢钾的碱性为什么是碳酸钠的碱性强?
同上
不是说碳酸根的酸性强于碳酸氢根的酸性,氢氧化钾的碱性强于氢氧化钠的碱性吗? dgsdfgdsg1年前1
dgsdfgdsg1年前1 -
 stanfreny 共回答了17个问题
stanfreny 共回答了17个问题 |采纳率76.5%这主要是CO32-和HCO3-的问题.
HCO3-是酸式盐,物质的量浓度相同时其水溶液的碱性比CO32-小
不知道你听谁说的碳酸根的酸性强于碳酸氢根的酸性,你可以看看:http://iask.sina.com.cn/b/9566675.html
然后你再看看http://zhidao.baidu.com/question/145840992.html1年前查看全部
- 碳酸氢钠与碳酸钠那个溶解度更小?碳酸氢钾和碳酸氢钠呢?如何判断?与范德华力有关?还是别的什么?
 kip1231年前1
kip1231年前1 -
 了他几眼他 共回答了23个问题
了他几眼他 共回答了23个问题 |采纳率87%分子晶体溶解度与是否极性有关 相似相容
对于结构相似(很重要这一点)的分子晶体范德华力的大小与其溶沸点有关
当然是范德华力越大溶沸点越高啦1年前查看全部
- 为什么氯化钙与碳酸氢钾溶液不能发生离子反应…
为什么氯化钙与碳酸氢钾溶液不能发生离子反应…
如题 伯拉图爱人1年前2
伯拉图爱人1年前2 -
 居楠溪畔 共回答了16个问题
居楠溪畔 共回答了16个问题 |采纳率100%因为Ca(HCO3)2是溶于水的,不是难溶物.
如果是KHCO3与Ca(OH)2是不能共存的,因为OH-会与HCO3-反应生成CO32-,CO32-与Ca2+会生成难溶的CaCO3沉淀.1年前查看全部
- 强酸的酸式盐以及弱酸的酸式盐 如碳酸氢钾显什么性?
 foolish_jr1年前3
foolish_jr1年前3 -
 白蛇传的小编剧 共回答了25个问题
白蛇传的小编剧 共回答了25个问题 |采纳率88%酸式盐可能是酸性,也可能是碱性的,这就要看酸式盐的电离和水解程度那个大,水解能力大的则碱性强,例如:KHCO3,HCO3-的水解能力大于电力能力,所以是碱性的;若电解能力强,则显酸性,例如:KH2PO4酸性的.1年前查看全部
大家在问
- 1随想 作文
- 2数 学 奥 林 匹 克 乘 奥 等于:奥 林 匹 克 数 学 数/...
- 3橘子里除含有维生素还含有什么为什么橘子不能直接被消化道吸收,它除了还有维生素还含有什么水果蔬菜是不是只含有维生素?那么纤
- 4__Lily__Lucy may go with you because one of them must stay a
- 5求有关于比例(包括正比例 反比例 比例尺等)的所有知识重点!
- 63. Bill is a student of No. 6 Middle School. _________ are _
- 7_____(be not)this skirt nice?
- 8一块梯形的花圃中(如图),三角形地的面积是9.5㎡,计划栽种小雏菊,平行四边形地里计划栽种月季花,求这块梯形花圃的面积.
- 9听材料,回答问题。 1. Where is the man going? A. To the post office.
- 10万有引力定律的发现实现了物理学史上的第一次大统一:“地上力学”和“天上力学”的统一.它表明天体运动和地面上物体的运动遵循
- 11fall in love的中文意思
- 121.下列关于现金流量表的描述正确的是 A:现金流量表是反映企业在一定会计期间现金和现金等价物流入和流出
- 13翻译一下:这是一个苹果 翻译成英文!急
- 14初次见面说好久不见说请人批评说求人原谅说求人帮忙说求给方便说麻烦别人说向人祝贺说求人看稿说求人解答说求人指点说托人办事说
- 15[D48] After having followed the thief for half an hour ,they
