纳米级四氧化三铁是应用最为广泛的软磁性材料之一。共沉淀法是目前制备纳米四氧化三铁的重要方法,其流程如图示:
 a56447882022-10-04 11:39:541条回答
a56447882022-10-04 11:39:541条回答| 纳米级四氧化三铁是应用最为广泛的软磁性材料之一。共沉淀法是目前制备纳米四氧化三铁的重要方法,其流程如图示: 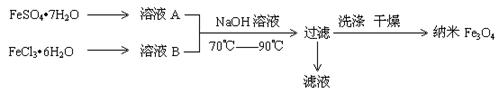 下列说法不正确的是
|

已提交,审核后显示!提交回复
共1条回复
 望湖楼主 共回答了17个问题
望湖楼主 共回答了17个问题 |采纳率88.2%- D
- 1年前
相关推荐
- 中国科学技术大学的钱逸泰教授等以CCl4和金属钠为原料,在700℃时反应制造出纳米级金刚石粉末和另一种化合物.该成果被科
中国科学技术大学的钱逸泰教授等以CCl4和金属钠为原料,在700℃时反应制造出纳米级金刚石粉末和另一种化合物.该成果被科学家们高度评价为“稻草变黄金”.同学们对此有下列一些“理解”,你认为其中不正确的( )
A.金刚石属于单质
B.制造过程中有新元素形成
C.CCl4是由碳氯两种元素组成
D.这个反应是化合反应 甄丽娜1年前1
甄丽娜1年前1 -
 依帆之蓝 共回答了21个问题
依帆之蓝 共回答了21个问题 |采纳率85.7%解题思路:A、金刚石是碳元素组成的单质,属于非金属单质;
B、化学反应前后遵循元素守恒的思想;
C、根据CCl4元素组成考虑;
D、一种单质和一种化合物反应生成新的单质和化合物的反应叫做置换反应.A、金刚石属于非金属单质,故A说法正确;
B、化学反应前后遵循元素守恒的思想,制造过程中元素种类没有改变,故B说法错误;
C、由CCl4化学式可知CCl4是由碳氯两种元素组成,故C说法正确;
D、CCl4和金属钠为原料,在700℃时制造出纳米级金刚石粉末的过程是钠单质置换出碳单质的过程,属于置换反应,故D说法错误.
故选BD.点评:
本题考点: 物质的相互转化和制备;单质和化合物的判别;反应类型的判定.
考点点评: 解答本题要掌握物质的分类方法和反应类型,只有这样才能对问题做出正确的判断.1年前查看全部
- 用特殊方法把固体物质加工到纳米级(1nm~100nm,1nm=10-9m)的超细粉末粒子,然后制得纳米材料.下列分散系中
用特殊方法把固体物质加工到纳米级(1nm~100nm,1nm=10-9m)的超细粉末粒子,然后制得纳米材料.下列分散系中的分散质的微粒直径和这种粒子具有相同数量级的是( )
A. 溶液
B. 胶体
C. 悬浊液
D. 乳浊液 海棠春睡足1年前1
海棠春睡足1年前1 -
 sun-right 共回答了16个问题
sun-right 共回答了16个问题 |采纳率100%解题思路:根据溶液、胶体、浊液微粒的直径判断,胶体微粒的直径为1-100nm之间.溶液的微粒直径为小于1nm,浊液的微粒直径大于100nm,胶体微粒的直径为1-100nm之间,把固体物质加工到纳米级的超细粉末粒子,与胶体的微粒直径相当,
故选B.点评:
本题考点: 分散系、胶体与溶液的概念及关系.
考点点评: 本题以纳米材料为载体考查了胶体微粒的本质特征,胶体能产生丁达尔现象,这是胶体独有的现象.1年前查看全部
- 将纳米级微粒物质溶解于液体溶剂中形成一种分散系,对该分散系及分散质颗粒的下列叙述中不正确的是( )
将纳米级微粒物质溶解于液体溶剂中形成一种分散系,对该分散系及分散质颗粒的下列叙述中不正确的是( )
A.该分散系能发生丁达尔现象
B.分散质颗粒能透过滤纸
C.该分散质颗粒大小在1~100nm之间
D.该分散系很稳定 dd88731年前1
dd88731年前1 -
 vincelove 共回答了12个问题
vincelove 共回答了12个问题 |采纳率75%解题思路:纳米粒子的直径在1-100nm之间,将纳米级微粒物质溶解于液体溶剂中形成的分散系是胶体.该分散系具有胶体的性质.胶体具有下列特点:胶体粒子的直径在1-100nm之间、胶体能透过滤纸但不能透过半透膜、能产生定丁达尔效应、具有介稳性.所以A、B、C正确.
故选:D点评:
本题考点: 纳米材料;胶体的重要性质.
考点点评: 本题考查的是胶体及其重要性质,胶体能透过滤纸但不能透过半透膜,能产生定丁达尔效应,具有介稳性.胶体与其它分散系的本质区别是:胶体粒子的直径在1-100nm之间.1年前查看全部
- 科学家在2000年8月10日出版的英国《自然》杂志上报告说,他们用DNA制造出一种臂长只有7nm的纳米级镊子,这种镊子能
科学家在2000年8月10日出版的英国《自然》杂志上报告说,他们用DNA制造出一种臂长只有7nm的纳米级镊子,这种镊子能钳起分子或原子,并对它们随意组合。下列分散系中分散质的微粒直径与纳米粒子具有相同数量级的是 [ ]A.溶液
B.胶体
C.悬浊液
D.乳浊液 ma133591年前1
ma133591年前1 -
 童子拜观音 共回答了14个问题
童子拜观音 共回答了14个问题 |采纳率92.9%B1年前查看全部
- “纳米铁”(初中化学)颗粒大小达到纳米级的单质铁具有很强的反应活性,俗称“纳米铁”1.高温条件下,用氢气与氯化亚铁反应,
“纳米铁”(初中化学)
颗粒大小达到纳米级的单质铁具有很强的反应活性,俗称“纳米铁”
1.高温条件下,用氢气与氯化亚铁反应,可生成“纳米铁”和一种溶于水显强酸性的气体,写出该反应的化学方程式()
2.预测“纳米铁”的其他化学性质,用化学方程式表示() 默默一米刘1年前2
默默一米刘1年前2 -
 oymf321 共回答了19个问题
oymf321 共回答了19个问题 |采纳率100%1.FeCl2+H2=2HCl+Fe
2.可燃性
3Fe+2O2=点燃或撞击=Fe3O4
还原性
2Fe+3H2O=高温=Fe2O3+3H2(气体符号)
2Fe+3CuO=高温=Fe2O3+3Cu1年前查看全部
- 人们会利用纳米级(1-100nm)微粒物质制造出更加优秀的材料和器件,使化学在材料、能源、环境和生命科学等领域发挥越来越
人们会利用纳米级(1-100nm)微粒物质制造出更加优秀的材料和器件,使化学在材料、能源、环境和生命科学等领域发挥越来越重要的作用.将纳米级微粒物质溶解于液体分散剂中形成一种分散系,对该分散系及分散质颗粒的叙述中正确的是( )
A.该分散系为溶液
B.该分散系能发生丁达尔效应
C.该分散系属于悬浊液
D.该分散系放置一段时间可能很快出现分层现象 wx111年前1
wx111年前1 -
 FL202fl 共回答了22个问题
FL202fl 共回答了22个问题 |采纳率90.9%解题思路:胶体的粒子直径在1~100nm之间,性质较稳定,具有丁达尔效应.该分散系的分散质颗粒粒子直径在1~100nm之间,应属于胶体,性质稳定,是均一、透明的分散系,具有丁达尔效应.
故选B.点评:
本题考点: 胶体的重要性质;纳米材料.
考点点评: 本题考查胶体的性质,题目难度不大,注意基础知识的积累.1年前查看全部
- 用特殊方法把固体物质加工到纳米级(1nm~100nm,1nm=10 —9m) 的超细粉末粒子,然后制得纳米材料。下列分散
用特殊方法把固体物质加工到纳米级(1nm~100nm,1nm=10 —9m) 的超细粉末粒子,然后制得纳米材料。下列分散系中的分散质的微粒直径和这种粒子具有相同数量级的是
A.溶液 B.胶体 C.悬浊液 D.乳浊液  涅确呢嘎1年前1
涅确呢嘎1年前1 -
 IA245731776 共回答了21个问题
IA245731776 共回答了21个问题 |采纳率90.5%B
1年前查看全部
- 纳米科技是21世纪经济发展的发动机.人们会利用纳米级(1-100nm,1nm=10-9m)微粒物质制造出更加优秀的材料和
纳米科技是21世纪经济发展的发动机.人们会利用纳米级(1-100nm,1nm=10-9m)微粒物质制造出更加优秀的材料和器件,使化学在材料、能源、环境和生命科学等领域发挥越来越重要的作用.请解答11、12两题.
11.下列分散系与纳米级微粒在直径上具有相同数量级的是( )
12.将纳米级微粒物质溶解于液体溶剂中形成一种分散系,对该分散系及分散质颗粒的叙述中不正确的是( )
A.该分散系不能发生丁达尔现象
B.该分散质颗粒能透过滤纸
C.该分散质颗粒能透过半透膜
D.该分散质颗粒能发生布朗运动 西土城路10号1年前1
西土城路10号1年前1 -
 晕198 共回答了20个问题
晕198 共回答了20个问题 |采纳率95%解题思路:纳米粒子的直径在1-100nm之间,将纳米级微粒物质溶解于液体溶剂中形成的分散系是胶体,该分散系具有胶体的性质.纳米粒子的直径在1-100nm之间,将纳米级微粒物质溶解于液体溶剂中形成的分散系是胶体,该分散系具有胶体的性质.
A.胶体能发生丁达尔现象,故A错误;
B.胶体能透过滤纸,故B正确;
C.胶体能透过滤纸但不能透过半透膜,故C错误;
D.胶粒能发生布朗运动,故D正确.
故选AC.点评:
本题考点: 胶体的重要性质.
考点点评: 本题考查的是胶体及其重要性质,难度不大,胶体能透过滤纸但不能透过半透膜,能产生定丁达尔效应,具有介稳性.胶体与其它分散系的本质区别是:胶体粒子的直径在1-100nm之间.1年前查看全部
- 中国科学技术大学钱逸泰教授等以CCl4和金属钠为原料,在700℃时制造出纳米级金刚石粉末.该成果发表在世界权威的《科学》
中国科学技术大学钱逸泰教授等以CCl4和金属钠为原料,在700℃时制造出纳米级金刚石粉末.该成果发表在世界权威的《科学》杂志上,立即被科学家高度评价为“稻草变黄金”.同学们对此展开了讨论,下列的一些理解不正确的是( )
A.制造中元素的种类没有变化
B.钠是金属单质
C.金刚石属于非金属单质
D.CCl4是一种混合物 glcfwlyh1年前1
glcfwlyh1年前1 -
 GD毛十八 共回答了14个问题
GD毛十八 共回答了14个问题 |采纳率92.9%解题思路:可以根据制取金刚石的过程中的变化、物质的组成和类别进行分析、判断,从而得出正确的结论.A、化学反应都遵守质量守恒定律,制造中元素的种类没有变化,故A正确.
B、钠是金属单质,故B正确.
C、金刚石属于非金属单质,故C正确;
D、CCl4是一种化合物,属于纯净物.故D错误
故选D.点评:
本题考点: 物质的相互转化和制备;纯净物和混合物的判别;单质和化合物的判别;质量守恒定律及其应用.
考点点评: 解答本题要掌握物质的分类方法和反应类型,只有这样才能对问题做出正确的判断.1年前查看全部
- (1)用纳米级的某种氧化物作催化剂,使汽车尾气中的CO跟NO反应转化为两种气体,其中一种可参与植物的光合作用,另一种是空
(1)用纳米级的某种氧化物作催化剂,使汽车尾气中的CO跟NO反应转化为两种气体,其中一种可参与植物的光合作用,另一种是空气中含量最多的气体.写出NO和CO反应的化学方程式2CO+2NO
2CO2+N2纳米级的某种氧化物 .2CO+2NO.
2CO2+N2纳米级的某种氧化物 .
(2)夏天的变色眼镜的玻璃片中含溴化银(AgBr),溴化银见光分解为银(Ag)和溴 (Br2),镜自动变暗.光线弱时,溴与银又化合生成溴化银.眼镜变亮,试写出化学方程式.见光2AgBr
2Ag+Br2光 .2AgBr,避光______.
2Ag+Br2光 . llj_microsoft1年前1
llj_microsoft1年前1 -
 我的**我tt 共回答了20个问题
我的**我tt 共回答了20个问题 |采纳率95%解题思路:首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.(1)用纳米级的某种氧化物作催化剂,使汽车尾气中的CO跟NO反应转化为两种气体,其中一种可参与植物的光合作用(二氧化碳),另一种是空气中含量最多的气体(氮气),反应的化学方程式为:2CO+2NO
纳米级的某种氧化物
.
2CO2+N2.
(2)溴化银见光分解为银(Ag)和溴(Br2),镜自动变暗,反应的化学方程式为:2AgBr
光
.
2Ag+Br2.光线弱时,溴与银又化合生成溴化银,眼镜变亮,反应的化学方程式为:2Ag+Br2═2AgBr.
故答案为:(1)2CO+2NO
纳米级的某种氧化物
.
2CO2+N2;(2)2AgBr
光
.
2Ag+Br2;2Ag+Br2═2AgBr.点评:
本题考点: 书写化学方程式、文字表达式、电离方程式.
考点点评: 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.1年前查看全部
- 中国科学技术大学钱逸泰教授等人以CCl 4 和金属钠为原料,在700℃时制造出了纳米级金刚石粉末和氯化钠。该成果发表在世
中国科学技术大学钱逸泰教授等人以CCl 4 和金属钠为原料,在700℃时制造出了纳米级金刚石粉末和氯化钠。该成果发表在世界权威的《科学》杂志上,立即被科学家们高度评价为“稻草变黄金”。同学们对此的一些“理解”,不正确的是
A.CCl 4 是一种化合物 B.制造过程中元素种类没有改变 C.金刚石属于金属单质 D.这个反应是置换反应  登高而呼1年前1
登高而呼1年前1 -
 顶用的说 共回答了16个问题
顶用的说 共回答了16个问题 |采纳率81.3%C
1年前查看全部
- 用特殊方法把固体物质加工到纳米级(1-100nm,1nm=10-9m即10-9m~10-7m)的超细粉末粒子,然后制得纳
用特殊方法把固体物质加工到纳米级(1-100nm,1nm=10-9m即10-9m~10-7m)的超细粉末粒子,然后制得纳米材料.下列分散系中的分散质的微粒直径和这种粒子具有相同数量级的是( )
A.胶体
B.悬浊液
C.溶液
D.乳浊液 破破的hh鞋1年前1
破破的hh鞋1年前1 -
 ninylwho 共回答了15个问题
ninylwho 共回答了15个问题 |采纳率93.3%解题思路:根据溶液、胶体、浊液微粒的直径判断,胶体微粒的直径为1-100nm之间.溶液的微粒直径为小于1nm,浊液的微粒直径大于100nm,胶体微粒的直径为1-100nm之间,把固体物质加工到纳米级的超细粉末粒子,与胶体的微粒直径相当,
故选A.点评:
本题考点: 分散系、胶体与溶液的概念及关系.
考点点评: 本题以纳米材料为载体考查了胶体微粒的本质特征,胶体能产生丁达尔现象,这是胶体独有的现象,题目难度不大.1年前查看全部
- 空气中含量最多的气体等纳米材料和纳米技术应用很广.用纳米级的某种氧化物作催化剂,使汽车尾气中的CO和NO反应,并转化为两
空气中含量最多的气体等
纳米材料和纳米技术应用很广.
用纳米级的某种氧化物作催化剂,使汽车尾气中的CO和NO反应,并转化为两种气体.
其中一种可参与植物的光合作用,另一种是空气中含量最多的气体.
这两种气体是()和().
写出CO和NO反应的化学方程式.
感激不尽 judy88051年前1
judy88051年前1 -
 ouzhunjie 共回答了21个问题
ouzhunjie 共回答了21个问题 |采纳率81%是二氧化碳 和 氮气
2CO+2NO=2CO2+N21年前查看全部
- 纳米是长度单位,1纳米等于1×10-9m,物质的颗粒达到纳米级时,具有特殊的性质.例如将单质铜制成“纳米铜”时具有非常强
纳米是长度单位,1纳米等于1×10-9m,物质的颗粒达到纳米级时,具有特殊的性质.例如将单质铜制成“纳米铜”时具有非常强的化学活性,在空气中可以燃烧.下列对“纳米铜”的有关叙述正确的是( )
A. 常温下“纳米铜”比铜片的金属性强,反应时反应速率快
B. 常温下“纳米铜”比铜片更易失电子,反应时反应速率快
C. 常温下“纳米铜”比铜片的还原性强
D. “纳米铜”颗粒更细小,化学反应时接触面大,所以反应速率快 xt520991年前4
xt520991年前4 -
 路过看看44 共回答了19个问题
路过看看44 共回答了19个问题 |采纳率100%解题思路:“纳米铜”的表面积较大,与空气充分接触,反应速率较大,在空气中可以燃烧.“纳米铜”和铜片都由铜元素组成,化学性质一样,但是“纳米铜”的表面积较大,与空气充分接触,反应速率较大,在空气中可以燃烧.
故选D.点评:
本题考点: 化学反应速率的影响因素.
考点点评: 本题考查铜的性质,题目难度不大,注意影响化学反应速率的因素,“纳米铜”和铜片都由铜元素组成,化学性质一样.1年前查看全部
- 纳米材料和纳米技术的应用涉及现代工业的各个领域.用纳米级的某种氧化物做催化剂,可以使汽车尾气中的CO和NO迅速反应转化为
纳米材料和纳米技术的应用涉及现代工业的各个领域.用纳米级的某种氧化物做催化剂,可以使汽车尾气中的CO和NO迅速反应转化为两种气体,其中一种是空气中含量最多的气体.请你写出该反应的化学方程式 ___ .
 ArsRead1年前1
ArsRead1年前1 -
 shouliu 共回答了17个问题
shouliu 共回答了17个问题 |采纳率100%解题思路:根据一种是空气中含量最多的气体,可以知道该气体是氮气,根据化学反应前后的元素种类不变,另一种也是气体,所以应该是二氧化碳,然后根据题目的叙述和上面的推导确定反应物、生成物、反应条件,再结合化学方程式的书写原则写出方程式.空气中含量最多的是氮气,另一种是二氧化碳,反应物是一氧化碳和一氧化氮,生成物是氮气和二氧化碳,反应条件是氧化物作催化剂,所以方程式为:2CO+2NO
氧化物
.
.N2+2CO2点评:
本题考点: 书写化学方程式、文字表达式、电离方程式;空气的成分及各成分的体积分数.
考点点评: 在解此类方程式的书写题时,关键是根据反应物判断出生成物,再依据条件写方程式.1年前查看全部
- 为了观察到纳米级的微小结构,需要用到分辨率比光学显微镜更高的电子显微镜。下列说法中正确的是(
为了观察到纳米级的微小结构,需要用到分辨率比光学显微镜更高的电子显微镜。下列说法中正确的是( )
A.电子显微镜所利用电子物质波的波长可以比可见光短,因此不容易发生明显衍射 B.电子显微镜所利用电子物质波的波长可以比可见光长,因此不容易发生明显衍射 C.电子显微镜所利用电子物质波的波长可以比可见光短,因此更容易发生明显衍射 D.电子显微镜所利用电子物质波的波长可以比可见光长,因此更容易发生明显衍射  风云起秦州1年前1
风云起秦州1年前1 -
 55个realtree 共回答了20个问题
55个realtree 共回答了20个问题 |采纳率75%A
电子的波长较小,不易发生衍射现象,放大倍数较高,A对;1年前查看全部
- (2005•盐城三模)为了观察到纳米级的微小结构,需要用到分辨率比光学显微镜更高的电子显微镜.下列说法中正确的是( )
(2005•盐城三模)为了观察到纳米级的微小结构,需要用到分辨率比光学显微镜更高的电子显微镜.下列说法中正确的是( )
A.电子显微镜所利用电子物质波的波长可以比可见光短,因此不容易发生明显衍射
B.电子显微镜所利用电子物质波的波长可以比可见光长,因此不容易发生明显衍射
C.电子显微镜所利用电子物质波的波长可以比可见光短,因此更容易发生明显衍射
D.电子显微镜所利用电子物质波的波长可以比可见光长,因此更容易发生明显衍射 yqh89361年前1
yqh89361年前1 -
 十三虎 共回答了18个问题
十三虎 共回答了18个问题 |采纳率83.3%解题思路:衍射是波特有的性质,是光遇到障碍物时发生的现象,发生明显的衍射现象的条件时:孔、缝的宽度或障碍物的尺寸与波长相近或比波长还小.光在同一均匀介质中沿直线传播.A、分辨率比光学显微镜更高的电子显微镜,因为电子显微镜所利用电子物质波的波长可以比可见光短,因此不容易发生明显衍射,所以A正确;
B、分辨率比光学显微镜更高的电子显微镜,因为电子显微镜所利用电子物质波的波长可以比可见光短,因此不容易发生明显衍射,所以B错误;
C、分辨率比光学显微镜更高的电子显微镜,因为电子显微镜所利用电子物质波的波长可以比可见光短,因此不容易发生明显衍射,所以C错误;
D、分辨率比光学显微镜更高的电子显微镜,因为电子显微镜所利用电子物质波的波长可以比可见光短,因此不容易发生明显衍射,所以D错误;
故选:A点评:
本题考点: 光的衍射.
考点点评: 注重对基础知识的积累,加强对基本概念的深入理解,是学习物理的关键.掌握了衍射现象的特点即可顺利解决此题,这就需要同学们一定要不遗余力的加强基础知识的理解和记忆.1年前查看全部
- 中国科学技术大学钱逸泰教授等以CCl4和金属钠为原料,在700℃制造出纳米级金刚石粉末和另一种化合物.该成果发表在世界最
中国科学技术大学钱逸泰教授等以CCl4和金属钠为原料,在700℃制造出纳米级金刚石粉末和另一种化合物.该成果发表在世界最权威的《科学》杂志上,立即被科学家们高度评价为“稻草变黄金”.同学们对此的一些“理解”,不正确的是( )
A.CCl4是一种化合物
B.制造金刚石过程中发生了化学变化
C.金刚石属于金属单质
D.这个反应是置换反应 qdy_5171年前1
qdy_5171年前1 -
 micky_0533swj 共回答了20个问题
micky_0533swj 共回答了20个问题 |采纳率80%解题思路:可以根据制取金刚石的过程进行分析、判断,从而得出正确的结论.A、CCl4是一种化合物,故A正确.
B、制造金刚石过程中有新物质生成,发生了化学变化,故B正确.
C、金刚石属于非金属单质,故C错误.
D、CCl4和金属钠反应生成金刚石和氯化钠,属于置换反应,故D正确.
故选C.点评:
本题考点: 物质的相互转化和制备;单质和化合物的判别;置换反应及其应用.
考点点评: 解答本题要掌握物质的分类方法和反应类型,只有这样才能对问题做出正确的判断.1年前查看全部
- 将纳米级微粒物质溶解于液体溶剂中形成一种分散系,对该分散系及分散质颗粒的叙述中不正确的是( )
将纳米级微粒物质溶解于液体溶剂中形成一种分散系,对该分散系及分散质颗粒的叙述中不正确的是( )
A.该分散系能发生丁达尔现象
B.分散质颗粒能透过半透膜
C.该分散质粒子直径大小在1~100 nm之间
D.该分散系很稳定 mxdaius1年前1
mxdaius1年前1 -
 坏椰子 共回答了16个问题
坏椰子 共回答了16个问题 |采纳率81.3%解题思路:纳米粒子的直径在1-100nm之间,将纳米级微粒物质溶解于液体溶剂中形成的分散系是胶体.该分散系具有胶体的性质.胶体具有下列特点:胶体粒子的直径在1-100nm之间、胶体分散质颗粒能透过滤纸但不能透过半透膜、能产生定丁达尔效应、具有介稳性.所以A、B、C正确.
故选:D.点评:
本题考点: 胶体的重要性质.
考点点评: 本题考查的是胶体及其重要性质,胶体能透过滤纸但不能透过半透膜,能产生定丁达尔效应,具有介稳性.胶体与其它分散系的本质区别是:胶体粒子的直径在1-100nm之间.1年前查看全部
- 以CCl4和金属钠为原料,在700℃时制造出纳米级金刚石粉末,这个反应是置换反应吗?
 zyg6151年前1
zyg6151年前1 -
 都江堰621 共回答了12个问题
都江堰621 共回答了12个问题 |采纳率91.7%根据题意:CCl4 + 4 Na === C + 4 NaCl
所以是置换反应1年前查看全部
- 关于化学方程式的题目.“纳米材料”特指直径为1~100nm的颗粒.用纳米级的某种氧化物作催化剂,使汽车尾气中的CO与NO
关于化学方程式的题目.
“纳米材料”特指直径为1~100nm的颗粒.用纳米级的某种氧化物作催化剂,使汽车尾气中的CO与NO反应转化成为两种气体,其中一种气体可参与植物的光合作用,另一种是空气中含量最多的气体.写出反映的化学方程式— __________________ qqbb20021年前2
qqbb20021年前2 -
 精彩_人生 共回答了16个问题
精彩_人生 共回答了16个问题 |采纳率75%参与光合作用的气体就是CO^2了,空气中含量最多的气体是N^2.
化学方程式为
催化剂
2 CO+2 NO==2 CO^2+N^21年前查看全部
- 颗粒达到纳米级的单质铁具有很强的反应活性,俗称“纳米铁”.实验室制备的方法是:以高纯氮气作保护气,在高温条件下用H2和F
 颗粒达到纳米级的单质铁具有很强的反应活性,俗称“纳米铁”.实验室制备的方法是:以高纯氮气作保护气,在高温条件下用H2和FeCl2发生置换反应,生成“纳米铁”和氯化氢气体.请回答以下问题:
颗粒达到纳米级的单质铁具有很强的反应活性,俗称“纳米铁”.实验室制备的方法是:以高纯氮气作保护气,在高温条件下用H2和FeCl2发生置换反应,生成“纳米铁”和氯化氢气体.请回答以下问题:
(1)写出生成“纳米铁”的化学方程式FeCl2+H2
Fe+2HCl高温 .FeCl2+H2.
Fe+2HCl高温 .
(2)反应中需要保护气的原因是______.
(3)阅读材料,回答问题:
【材料1】氯元素(Cl)是一种重要的非金属元素,氯气是双原子分子,在通常情况下为黄绿色气体.
【材料2】氯原子的结构示意图如图,在化学反应中易得到1个电子,达到8电子的稳定结构,氯气化学性质很活泼,具有较强的氧化性,能与多种金属和非金属直接化合,还能与水、碱等化合物反应.
【材料3】燃烧不一定要有氧气参加,任何发光、发热的剧烈的化学反应,都可以叫做燃烧,氢气可以在氯气中燃烧生成氯化氢(HCl).
(1)氯气的化学式为______.
(2)请总结氯气的有关性质:①物理性质______;②化学性质______.
(3)写出材料3中的化学方程式Cl2+H2
2HCl点燃 .Cl2+H2.
2HCl点燃 . Rhh08061年前1
Rhh08061年前1 -
 lg_han 共回答了24个问题
lg_han 共回答了24个问题 |采纳率91.7%解题思路:(1)根据反应物生成物进行书写解决,注意条件.
(2)铁在热的时候活动性很强,故应使用保护气.
(3)物质的物理性质是指不需要通过化学变化表现出来的性质.例如,颜色、状态、气味、密度、熔点、沸点等.物质的化学性质是指通过化学变化表现出来的性质.例如,稳定性、氧化性、还原性、毒性、可燃性等.(1)由题中信息在高温条件下用H2和FeCl2发生置换反应,生成“纳米铁”.可知反应物为氢气和氯化亚铁,生成物为铁,根据反应前后元素种类不变可知另一生成物为氯化氢,化学方程式为FeCl2+H2
高温
.
Fe+2HCl
(2)铁在热的时候活动性很强,故应使用保护气防止它在和其他物质发生反应.
(3)氯气的化学式为:Cl2.
物理性质有:黄绿色气体.化学性质有:具有较强的氧化性、能与多种金属和非金属直接化合,还能与水、碱等化合物反应.
(3)氢气在氯气中燃烧生成氯化氢(HCl),反应的方程式是Cl2+H2
点燃
.
2HCl.
故答案为:(1)FeCl2+H2
高温
.
Fe+2HCl;
(2)防止铁在高温下与氧气反应;
(3)Cl2;黄绿色气体;具有较强的氧化性、能与多种金属和非金属直接化合,还能与水、碱等化合物反应;Cl2+H2
点燃
.
2HCl.点评:
本题考点: 金属的化学性质;原子结构示意图与离子结构示意图;化学式的书写及意义;化学性质与物理性质的差别及应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 此题考查了金属铁的活动性、置换反应以及化学方程式的书写等,题目不难.1年前查看全部
- (10分)将一些能较好吸收和发射红外线的纳米级金属氧化物(如氧化铁、氧化铝、氧化锌等)通过特殊工艺织人纤维,然后用该种纤
(10分)将一些能较好吸收和发射红外线的纳米级金属氧化物(如氧化铁、氧化铝、氧化锌等)通过特殊工艺织人纤维,然后用该种纤维制成***,称之为红外保暖内衣。对于红外保暖内衣和普通保暖内衣在人体运动时,通气和散热的效果比较,某人设计如下实验:
①上午某时间穿红外保暖内衣,跳绳前测前胸体表温度,跳绳10分钟,再次测前胸体表温度。
②下午某时间同一人穿普通保暖内衣(假设普通保暖内衣和红外保暖内衣除材质不同外,其余都相同),在通风状况相同的同一房间里,重复上午相同的实验步骤。
③比较上、下午跳绳前后的体表温度变化量,得出两种保暖内衣通气散热效果强弱结论。
请回答下列问题:
(1)洗涤红外保暖内衣时,不宜选用的洗涤剂是 (选填“弱酸性洗涤剂”、“弱碱性洗涤剂”、“中性洗涤剂”)
(2)若该人跳绳后腿部发酸,是因为肌肉细胞进行了
(3)有人认为根据该实验得出的结果不可靠,你认为该实验设计中变量控制不严密的地方是 、 (写两点)
(4)为了得出更可靠的结论,请写出你认为该实验最需改进的具体方面(写一点)
 4079090451年前1
4079090451年前1 -
 xxiieang 共回答了23个问题
xxiieang 共回答了23个问题 |采纳率91.3%(1)弱酸性洗涤剂
(2)无氧呼吸产生乳酸
(3)实验时间不同;跳绳10分钟
(4)应改为同时在上午测或同时在下午测
考查金属氧化物的性质,无氧呼吸,生物实验分析。红外保暖内衣中含有金属氧化物,会与酸反应,因此不能用弱酸性洗涤剂洗涤。人体肌肉细胞无氧呼吸产生乳酸,会使肌肉发酸。实验的变量是保暖内衣的种类,因此实验时间必须统一。1年前查看全部
- (12分)在浓CaCl 2 溶液中通入NH 3 和CO 2 ,可以制得纳米级碳酸钙。下图所示A—E为实验室 常见的仪器装
(12分)在浓CaCl 2 溶液中通入NH 3 和CO 2 ,可以制得纳米级碳酸钙。下图所示A—E为实验室
 常见的仪器装置(部分固定夹持装置略去),请根据要求
常见的仪器装置(部分固定夹持装置略去),请根据要求 回答问题。
回答问题。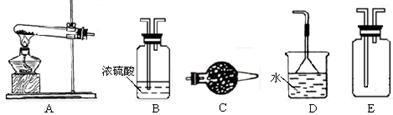
(1)实验室制取、收集干燥的NH 3 ,需选用上述仪器装置中的 ▲ 。
(2)向浓CaCl 2 溶液中通入NH 3 和CO 2 气体制纳米级碳酸钙时,应先通入的气体是
▲ ,写出制纳米级碳酸钙的化学方程式: ▲ 。
(3)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级。
▲ 。 云如之何1年前1
云如之何1年前1 -
 宁静风车 共回答了22个问题
宁静风车 共回答了22个问题 |采纳率86.4%1)ACDE(3分)
(2)NH 3 (3分) CaCl 2 + CO 2 + 2NH 3 + H 2 O=CaCO 3 + 2NH 4 Cl(3分)
(3)取少量样品和水混合形成分散系,用一束光照射,若出现一条光亮的通路,则是纳米级,否则不是(3分)
略1年前查看全部
- 用纳米级的某种氧化物作催化剂,使汽车尾气中的一氧化碳和一氧化氮反应转化为的两种气体是------和------,写出一氧
用纳米级的某种氧化物作催化剂,使汽车尾气中的一氧化碳和一氧化氮反应转化为的两种气体是------和------,写出一氧化碳和一氧化氮反应的文字表达式-----------------------------------------.
 kivvy1年前2
kivvy1年前2 -
 miko119 共回答了23个问题
miko119 共回答了23个问题 |采纳率91.3%生成二氧化碳和氮气
一氧化碳+一氧化氮催化剂二氧化碳+氮气1年前查看全部
- 中国科学技术大学的钱逸泰教授等以CCl4和金属钠为原料,在700°C时反应制造出纳米级金刚石粉末和另一种化合物.该成果发
中国科学技术大学的钱逸泰教授等以CCl4和金属钠为原料,在700°C时反应制造出纳米级金刚石粉末和另一种化合物.该成果发表在世界权威的《科学》杂志上,立即被科学家们高度评价为“稻草变黄金”.同学们对此有下列一些“理解”,你认为其中错误的是( )
A.这个反应是氧化还原反应
B.制造过程中元素种类没有改变
C.另一种化合物为NaCl
D.金刚石属于金属单质 thhdfbgdfhgd1年前1
thhdfbgdfhgd1年前1 -
 chen6230 共回答了19个问题
chen6230 共回答了19个问题 |采纳率94.7%解题思路:A.根据元素的化合价变化判断;
B.CCl4和金属钠定律知该制造过程中元素种类没有改变;
C.根据元素守恒判断;
D.金刚石的构成元素为碳.A.CCl4和金属钠反应生成金刚石(碳单质),碳元素的化合价降低,有元素的化合价变化属于氧化还原反应,故A正确;
B.根据元素守恒定律可知制造过程中元素种类没有改变,故B正确;
C.CCl4和金属钠反应生成金刚石(碳单质)和NaCl,故C正确;
D.金刚石的构成元素为碳,属于非金属单质,故D错误;
故选D.点评:
本题考点: 氧化还原反应.
考点点评: 本题考查了氧化还原反应、单质的分类、元素守恒的应用等,题目难度不大,解题时注意守候思想的应用.1年前查看全部
- (2011•上海模拟)纳米是长度单位,1nm=10-9m,当物质的颗粒达到纳米级时,具有特殊的性质.例如将铜制成“纳米铜
(2011•上海模拟)纳米是长度单位,1nm=10-9m,当物质的颗粒达到纳米级时,具有特殊的性质.例如将铜制成“纳米铜”时具有非常强的化学活性,在空气中可以燃烧.下列关于“纳米铜”的叙述正确的是( )
A.常温下“纳米铜”比铜片的金属性强
B.常温下“纳米铜”比铜片更易失去电子
C.常温下“纳米铜”的还原性与铜片相同
D.常温下“纳米铜”比铜片的氧化性强 liuxing68991年前1
liuxing68991年前1 -
 uu小小郎 共回答了19个问题
uu小小郎 共回答了19个问题 |采纳率73.7%解题思路:纳米铜之所以具有较强的化学活性是由于纳米材料的颗粒较小,表面积较大,与氧气的接触面积较大而能在空气中的燃烧,而铜的金属性、活泼性等没有发生变化.A.金属性属于元素的性质,都为铜元素,金属性相同,故A错误;
B.纳米铜之所以具有较强的化学活性是由于纳米材料的颗粒较小,表面积较大,与氧气的接触面积较大而能在空气中的燃烧,都是不活泼金属,失电子能力相同,故B错误;
C.在相同条件下,纳米铜和铜片的还原性是相同的,物质的性质是决定化学反应速率主要因素,故C正确;
D.铜为金属,在反应中只能失去电子,据有还原性,不具有氧化性,故D错误.
故选C.点评:
本题考点: 原子结构与元素的性质;胶体的重要性质.
考点点评: 本题为信息给予题,题目难度中等,本题注意影响化学反应速率的因素,易错点为B、C,注意物质的本身的性质与外界因素影响的不同.1年前查看全部
- (2014•镇江)新制Cu(OH)2与肼(N2H4)反应可制备纳米级Cu2O,同时放出N2,向红色的Cu2O固体中加入过
(2014•镇江)新制Cu(OH)2与肼(N2H4)反应可制备纳米级Cu2O,同时放出N2,向红色的Cu2O固体中加入过量稀盐酸,溶液由无色变为蓝绿色,容器底部仍有红色固体.
(1)生成Cu2O反应的化学方程式中,Cu2O的化学计量数为2,其化学方程式为______;
(2)溶液由无色变为蓝绿色反应的化学方程式为______. 优明数码1年前1
优明数码1年前1 -
 tomiscat 共回答了18个问题
tomiscat 共回答了18个问题 |采纳率94.4%解题思路:根据题意,新制Cu(OH)2与肼(N2H4)反应可制备纳米级Cu2O,同时放出N2,由质量守恒定律,反应前后元素种类不变,同时还生成水;向红色的Cu2O固体中加入过量稀盐酸,溶液由无色变为蓝绿色(生成氯化铜溶液),容器底部仍有红色固体(铜),由质量守恒定律,反应前后元素种类不变,同时还生成水;写出反应的化学方程式即可.(1)新制Cu(OH)2与肼(N2H4)反应可制备纳米级Cu2O,同时放出N2,由质量守恒定律,反应前后元素种类不变,因此反应后还生成水,Cu2O的化学计量数为2,反应的化学方程式为:N2H4+4Cu(OH)2=2Cu2O+N2↑+6H2O.
(2)向红色的Cu2O固体中加入过量稀盐酸,溶液由无色变为蓝绿色(生成氯化铜溶液),容器底部仍有红色固体(生成的铜),由质量守恒定律,反应前后元素种类不变,因此反应后还生成水,反应的化学方程式为:Cu2O+2HCl=CuCl2+Cu+H2O.
故答案为:(1)N2H4+4Cu(OH)2=2Cu2O+N2+6H2O;(2)Cu2O+2HCl=CuCl2+Cu+H2O.点评:
本题考点: 书写化学方程式、文字表达式、电离方程式.
考点点评: 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.1年前查看全部
- 最强的光学显微镜能看到纳米级物质吗?
 罗知音1年前7
罗知音1年前7 -
 hx4207 共回答了23个问题
hx4207 共回答了23个问题 |采纳率91.3%最新的光学显微镜是可以看到50nm的,液体也可以.有种荧光显微镜可以看到单个的蛋白.此外近场光学显微镜好象可以1年前查看全部
- 下列分散系中的分散质的粒子大小属于纳米级(1~100nm)的是
下列分散系中的分散质的粒子大小属于纳米级(1~100nm)的是
Fe(OH) 3 胶体 B、Fe(OH) 3 沉淀
C、FeCL 3 溶液 D、碘水与CCL 4 溶液振荡后的混合液 万雁同悲1年前1
万雁同悲1年前1 -
 imsl 共回答了25个问题
imsl 共回答了25个问题 |采纳率80%A
胶体分散质微粒的直径在1nm-100nm之间,所以,应选分散系为胶体的才符合条件,只有A 是胶体,故选A。1年前查看全部
- 中国科学技术大学的钱逸泰教授等曾以CCl 4 和金属钠为原料,在700℃时制造出了纳米级金刚石粉末。该成果在世界权威杂志
中国科学技术大学的钱逸泰教授等曾以CCl 4 和金属钠为原料,在700℃时制造出了纳米级金刚石粉末。该成果在世界权威杂志《科学》上发表后,立即被科学家们高度评价为“稻草变黄金”的成功。下列关于这一事实的理解错误的是 [ ]A.金刚石属于金属单质
B.制造过程中元素种类没有改变
C.CCl 4 是一种化合物
D.这个反应是置换反应 爱到风起1年前1
爱到风起1年前1 -
 opkl01 共回答了24个问题
opkl01 共回答了24个问题 |采纳率83.3%A1年前查看全部
- (2011•姜堰市二模)在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙.下图所示A-E为实验室常见的仪器装
(2011•姜堰市二模)在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙.下图所示A-E为实验室常见的仪器装置(部分固定夹持装置略去),请根据要求回答问题.

(1)实验室制取、收集干燥的NH3,需选用上述仪器装置中的______.
(2)向浓CaCl2溶液中通入NH3和CO2气体制纳米级碳酸钙时,应先通入的气体是______,写出制纳米级碳酸钙的化学方程式:______.
(3)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级______. 赛敖曹1年前1
赛敖曹1年前1 -
 有点蠢有点笨 共回答了29个问题
有点蠢有点笨 共回答了29个问题 |采纳率86.2%解题思路:(1)根据反应物的状态、反应条件选取反应装置,根据气体的溶解性、密度选择收集装置.
(2)根据二氧化碳和氨气的溶解性判断先通入的气体,由反应物和生成物写出反应方程式.
(3)碳酸钙样品颗粒如果为纳米级,纳米级的颗粒在胶体范围内,所以根据胶体的性质确定实验方案.(1)实验室制取氨气采用固体、固体加热型装置,所以应选A为反应装置;生成物中含有水,氨气属于碱性气体,所以应选择碱性物质吸收水蒸气,故选C;氨气极易溶于水,且氨气的密度小于空气的密度,所以应采用向下排空气法收集,故选E;氨气有刺激性气味,所以不能直接排空;氨气极易溶于水,所以尾气处理应采用防止倒吸装置,用水吸收即可,故选D.
故答案为:ACDE.
(2)氨气极易溶于水,二氧化碳不易溶于水,所以应先通入氨气;氨气溶于水生成氨水,溶液呈碱性,二氧化碳是酸性气体,能和碱反应生成碳酸铵,碳酸铵和氯化钙发生复分解反应生成碳酸钙和氯化铵CaCl2+CO2+2NH3+H2O=
CaCO3↓+2NH4Cl.
故答案为NH3;CaCl2+CO2+2NH3+H2O=CaCO3↓+2NH4Cl.
(3)碳酸钙样品颗粒如果为纳米级,纳米级的颗粒在胶体范围内,所以具有胶体的性质,运用胶体的丁达尔效应判断;取少量样品和水混合形成分散系,用一束光照射,若出现一条光亮的通路,则是纳米级,否则不是.
故答案为:取少量样品和水混合形成分散系,用一束光照射,若出现一条光亮的通路,则是纳米级,否则不是.点评:
本题考点: 氨的实验室制法;胶体的重要性质;氨的化学性质.
考点点评: 本题考查了氨气的实验室制法,难度不大,注意根据反应物的状态、反应条件选取反应装置,根据气体的溶解性、密度选择收集装置.1年前查看全部
- (2003•湘潭)纳米级材料由于具备传统材料不具备的奇异或反常的物理、化学性质,而被广泛应用于建筑、家电制造等行业,其实
(2003•湘潭)纳米级材料由于具备传统材料不具备的奇异或反常的物理、化学性质,而被广泛应用于建筑、家电制造等行业,其实纳米(nm)是一种长度度量单位,1纳米=0.000000001米,用科学记数法表示:6.19纳米=______米.
 刁谗公主1年前1
刁谗公主1年前1 -
 北岸的风cz 共回答了18个问题
北岸的风cz 共回答了18个问题 |采纳率94.4%∵1纳米=0.000 000 001米,
∴6.19纳米=6.19×0.000 000 001米=0.000 000 006 19米=6.19×10-9米.
答:6.19纳米=6.19×10-9米.1年前查看全部
- 求翻译!英文全程负责项目立项、开题答辩、方案的制定及实施.成功的将纳米级TiO2于玻璃表面镀膜,可得到耐腐蚀、自洁型玻璃
求翻译!英文
全程负责项目立项、开题答辩、方案的制定及实施.成功的将纳米级TiO2于玻璃表面镀膜,可得到耐腐蚀、自洁型玻璃,并有望在纳米晶太阳能电池方向取得进展.
收获:①科研期间,将项目合理分解为小课题,指导6名本科生完成科研任务及本科毕业论文
②在科研过程中掌握了丰富的理论知识,学会了各种仪器的操作规范和对材料性能的评估标准
③在科研分工及项目交流会的过程中,明白只有团队合作才能取得成功.
④将课题生产的光触媒及镀膜玻璃应用于实际,认识到所用科研目的是为解决现有问题,创造利润
 jumajixxh1年前1
jumajixxh1年前1 -
 lftwins126 共回答了17个问题
lftwins126 共回答了17个问题 |采纳率76.5%Responsible for the project throughout the project, open title defense, program development and implementation. The success of the nano-TiO2 coating on the glass surface can be obtained corrosion-resistant, self-cleaning glass, and nano-crystalline solar cells is expected in the direction of progress.
Harvest: ① research during the project broken down into small issues a reasonable guide to complete six undergraduate students and undergraduate thesis research tasks
② In the research process to master a wealth of theoretical knowledge, learn a variety of devices in the operating norms and standards for the assessment of material properties
③ In the research division of labor and project exchange process, understand the only team to succeed.
④ photocatalyst and the subject of the production of coated glass used in practical, recognizing that research is intended to be used to solve the existing problems and create profits1年前查看全部
- 纳米级材料由于具备传统材料不具备的奇异或反常的物理、化学性质,而被广泛应用于建筑、家电制造等行业,其实纳米(nm)是一种
纳米级材料由于具备传统材料不具备的奇异或反常的物理、化学性质,而被广泛应用于建筑、家电制造等行业,其实纳米(nm)是一种长度度量单位,1纳米=0.000000001米,用科学记数法表示:6.19纳米=______米.  蓝泪真嗳1年前1
蓝泪真嗳1年前1 -
 龟背上的舞者 共回答了21个问题
龟背上的舞者 共回答了21个问题 |采纳率95.2%∵1纳米=0.000 000 001米,
∴6.19纳米=6.19×0.000 000 001米=0.000 000 006 19米=6.19×10 -9 米.
答:6.19纳米=6.19×10 -9 米.1年前查看全部
- 公司纳米级气泡污水处理系统荣获“2008年SIP第二届科技领军人才项目”.英语翻译
 有梦飞翔1年前1
有梦飞翔1年前1 -
 心雅繁思 共回答了21个问题
心雅繁思 共回答了21个问题 |采纳率90.5%The company's nano-level bubbles sewage disposal system won the "2008 SIP Second Annual Scientific and Technological Leading Talent Projects."1年前查看全部
- 科学家在2000年8月10日出版的英国《自然》杂志上报告,他们用DNA制造出了一种臂长只有7纳米的纳米级镊子,以便能够钳
科学家在2000年8月10日出版的英国《自然》杂志上报告,他们用DNA制造出了一种臂长只有7纳米的纳米级镊子,以便能够钳起分子或原子并对它们随意组合.下列分散系中的分散质的粒子直径与纳米级镊子臂长具有相同数量级的是( )
A.溶液
B.悬浊液
C.乳浊液
D.胶体 rockrose1年前1
rockrose1年前1 -
 曾莎莎 共回答了16个问题
曾莎莎 共回答了16个问题 |采纳率93.8%解题思路:根据分散质的微粒直径大小判断.纳米级镊子的直径在1-100nm之间,溶液中溶质的直径<1~100nm,悬浊液、乳浊液分散质粒子直径>1~100nm,胶体粒子的直径在1~100nm之间,故答案为:D
点评:
本题考点: 纳米材料.
考点点评: 溶液、悬浊液、乳浊液的本质区别是:胶体粒子的直径在1-100nm之间,这是胶体的本质特征,1年前查看全部
- 中国科学技术大学的钱逸泰教授等以CCl4和金属钠为原料,在700℃时发生反应制造出纳米级金刚石粉末和另一种化合物.该成果
中国科学技术大学的钱逸泰教授等以CCl4和金属钠为原料,在700℃时发生反应制造出纳米级金刚石粉末和另一种化合物.该成果发表在世界权威的《科学》杂志上,立即被科学家们高度评价为“稻草变黄金”.同学们对此有下列一些“理解”,你认为其中不正确的是( )
A.科学家评价的“黄金”指的是金刚石
B.反应过程中CCl4是还原剂
C.“另一种化合物”指的是NaCl
D.这个反应是置换反应 粉色的天空1年前1
粉色的天空1年前1 -
 whldlcn 共回答了19个问题
whldlcn 共回答了19个问题 |采纳率89.5%解题思路:根据题目信息,结合质量守恒可知CCl4和金属钠在700℃时发生反应制造出纳米级金刚石粉末和氯化钠,以此来解答;CCl4和金属钠在700℃时发生反应制造出纳米级金刚石粉末和氯化钠,
A、科学家评价的“黄金”指的是金刚石,故A正确;
B、反应过程中CCl4碳元素的化合价降低,是氧化剂,故B错误;
C、“另一种化合物”指的是NaCl,故C正确;
D、CCl4和金属钠反应生成金刚石和氯化钠,属于置换反应,故D正确.
故选:B.点评:
本题考点: 纳米材料;化学基本反应类型.
考点点评: 本题主要考查了反应类型、氧化剂以及质量守恒定律等多种化学基础知识,难度不大,只要认真分析就会做出.1年前查看全部
- 中国科学技术大学钱逸泰教授等人以CCl 4 和金属钠为原料,在特定条件下制造出纳米级金刚石粉末。该成果发表在世界最权威的
中国科学技术大学钱逸泰教授等人以CCl 4 和金属钠为原料,在特定条件下制造出纳米级金刚石粉末。该成果发表在世界最权威的《科学》杂志上,立即被科学家们高度评价为“稻草变为黄金”。下列说法中不正确的是
A.金刚石为非金属单质 B.制造金刚石过程中碳元素的化合价没有改变 C.CCl 4 是一种化合物 D.制造金刚石的变化属于化学变化  说了你也不知道1年前1
说了你也不知道1年前1 -
 公子小渔 共回答了21个问题
公子小渔 共回答了21个问题 |采纳率95.2%B
1年前查看全部
- (2010•南通模拟)(1)新型材料纳米级Fe粉具有超强的磁性能,用作高密度磁记录的介质以及高效催化剂等.实验室采用气相
(2010•南通模拟)(1)新型材料纳米级fe粉具有超强的磁性能,用作高密度磁记录的介质以及高效催化剂等.实验室采用气相还原法制备纳米级fe,方法是:将fecl2•nh2o固体脱水、真空干燥得到fecl2,然后在高温条件下通入***氮气(作保护气)和氢气(作反应物)的混合气体,生成纳米级fe:则,生成纳米级fe的化学方程式为fecl2+h2
fe+2hcl高温 .fecl2+h2,该反应属于______反应(基本反应类型).纳米级fe粉在空气中易自燃成黑色固体,化学方程式为______.
fe+2hcl高温 .
(2)今年春节期间,我国南方地区普降大雪,给人们出行带来诸多不便,生产生活受到很大影响,损失十分严重.在道路除雪过程中,融雪剂发挥了很大的作用.已知某公司生产的融雪剂由nacl、nano3、mgcl2、、cuso4中的两种物质组成.小明为探究其成分,设计并完成了如图所示的实验.
根据以上实验,请你推断:
①该融雪剂一定没有的成分是______.
②该融雪剂中的组成可能为:(Ⅰ)______;
(Ⅱ)______.
③你认为第______种情况更利于植物和农作物的生长. dewdewchain1年前1
dewdewchain1年前1 -
 万宠网天使 共回答了21个问题
万宠网天使 共回答了21个问题 |采纳率76.2%解题思路:纳米级的铁的化学性质与铁类似,根据题目所提供的信息不难写出反应的化学方程式.由于硫酸铜溶于水后显蓝色,首先根据溶液的颜色确定硫酸铜的有无,然后根据酸碱盐之间的反应关系,必须通过两个特征反应,即加氢氧化钠溶液产生白色沉淀和无色溶液加入硝酸银溶液产生白色沉淀,并以此为依据初步确定其组成.根据题目所提供的信息可以写出反应的化学方程式.加水后为无色溶液,说明该融雪剂中一定无硫酸铜;与氢氧化钠反应生成的白色沉淀的只有氯化镁,所以肯定含有氯化镁;无色溶液加入硝酸银溶液产生白色沉淀,除氯化镁中的氯离子外,氯化钠中也含有氯离子,故推断可能含有氯化钠,而硝酸钠不与任何物质反应,溶于水后还为无色溶液,故可能含有硝酸钠.硝酸钠属于氮肥,有利于植物和农作物的生长.
故答案为:(1)FeCl2+H2
高温
.
Fe+2HCl 置换 3Fe+2O2═Fe3O4
(2)①CuSO4②(Ⅰ) NaCl、MgCl2(或NaNO3、MgCl2)(Ⅱ) NaNO3、MgCl2、(或NaCl、MgCl2、)
③Ⅱ(或Ⅰ)点评:
本题考点: 金属的化学性质;盐的化学性质;反应类型的判定;书写化学方程式、文字表达式、电离方程式.
考点点评: 解答此类题的关键是依据图示所给的信息、条件(现象、颜色等),抓住物质的特征,找出解题的突破口.1年前查看全部
- 中国科学技术大学钱逸泰教授等以CCl4和金属钠为原料,在700℃制造出纳米级金刚石粉末.该成果发表在世界最权威的《科学》
中国科学技术大学钱逸泰教授等以CCl4和金属钠为原料,在700℃制造出纳米级金刚石粉末.该成果发表在世界最权威的《科学》杂志上,立即被科学家们高度评价为“稻草变黄金”.同学们对此的一些“理解”中,正确的是______
A、金刚石属于金属单质 B、制造金刚石过程中发生了物理变化
C、CCl4是一种化合物 D、______. tianxiezy1年前1
tianxiezy1年前1 -
 扒吧扒吧不是罪 共回答了17个问题
扒吧扒吧不是罪 共回答了17个问题 |采纳率70.6%解题思路:可以根据制取金刚石的过程进行分析、判断,从而得出正确的结论.A、金刚石属于非金属单质,故A错误.
B、制造金刚石过程中有新物质生成,发生了化学变化,故B错误.
C、CCl4是一种化合物,故C正确.
D、CCl4和金属钠反应生成金刚石和氯化钠,属于置换反应.
故选C,D补充:该反应属于置换反应.点评:
本题考点: 碳元素组成的单质;单质和化合物的判别;化学变化和物理变化的判别.
考点点评: 解答本题要掌握物质的分类方法和反应类型,只有这样才能对问题做出正确的判断.1年前查看全部
- 纳米材料和纳米技术的应用涉及现代工业的各个领域.用纳米级的某种氧化物做催化剂,可以使汽车尾气中的CO和NO迅速反应转化为
纳米材料和纳米技术的应用涉及现代工业的各个领域.用纳米级的某种氧化物做催化剂,可以使汽车尾气中的CO和NO迅速反应转化为两种气体,其中一种是空气中含量最多的气体.请你写出该反应的化学方程式2CO+2NO
N2+2CO2氧化物 ..2CO+2NO.
N2+2CO2氧化物 .. kgkt1年前1
kgkt1年前1 -
 dt41902 共回答了16个问题
dt41902 共回答了16个问题 |采纳率87.5%解题思路:根据一种是空气中含量最多的气体,可以知道该气体是氮气,根据化学反应前后的元素种类不变,另一种也是气体,所以应该是二氧化碳,然后根据题目的叙述和上面的推导确定反应物、生成物、反应条件,再结合化学方程式的书写原则写出方程式.空气中含量最多的是氮气,另一种是二氧化碳,反应物是一氧化碳和一氧化氮,生成物是氮气和二氧化碳,反应条件是氧化物作催化剂,所以方程式为:2CO+2NO
氧化物
.
.N2+2CO2点评:
本题考点: 书写化学方程式、文字表达式、电离方程式;空气的成分及各成分的体积分数.
考点点评: 在解此类方程式的书写题时,关键是根据反应物判断出生成物,再依据条件写方程式.1年前查看全部
- (2014•怀柔区一模)纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
 (2014•怀柔区一模)纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
(2014•怀柔区一模)纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
(1)工业上常用方法Ⅱ和方法Ⅲ制取Cu2O而很少用方法Ⅰ,其原因是______.方法Ⅰ 用炭粉在高温条件下还原CuO 方法Ⅱ 电解法,反应为2Cu+H2O
Cu2O+H2↑.通电 .方法Ⅲ 用肼(N2H4)还原新制Cu(OH)2
(2)已知:2Cu(s)+[1/2]O2(g)=Cu2O(s)△H=-169kJ•mol-1
C(s)+[1/2]O2(g)=CO(g)△H=-110.5kJ•mol-1
Cu(s)+[1/2]O2(g)=CuO(s)△H=-157kJ•mol-1
则方法Ⅰ发生的反应:2CuO(s)+C(s)=Cu2O(s)+CO(g);△H=______kJ•mol-1.
(3)方法Ⅱ采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该电池的阳极反应式为______.
(4)方法Ⅲ为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2.该制法的化学方程式为4Cu(OH)2+N2H4
2Cu2O+N2↑+6H2O△ .4Cu(OH)2+N2H4.
2Cu2O+N2↑+6H2O△ .
(5)在相同的密闭容器中,用以上两种方法制得的Cu2O分别进行催化分解水的实验:2H2O(g)
2H2(g)+O2(g)△H>0光照 .Cu2O
水蒸气的浓度随时间t变化如下表所示.
下列叙述正确的是______(填字母代号).序号 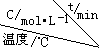
0 10 20 30 40 50 ① T1 0.050 0.0492 0.0486 0.0482 0.0480 0.0480 ② T1 0.050 0.0488 0.0484 0.0480 0.0480 0.0480 ③ T2 0.10 0.094 0.090 0.090 0.090 0.090
A.实验的温度:T2<T1
B.实验①前20min的平均反应速率 v(H2)=7×10-5 mol•L-1 min-1
C.实验②比实验①所用的催化剂催化效率高. 悠悠的小船1年前1
悠悠的小船1年前1 -
 满杯酒半盏茶 共回答了22个问题
满杯酒半盏茶 共回答了22个问题 |采纳率81.8%解题思路:(1)电解法消耗大量的能源,肼还原时会将氧化亚铜还原为金属铜;
(2)根据盖斯定律来计算反应的焓变;
(3)在电解池的阳极发生失电子得还原反应;
(4)根据“液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2”来书写化学方程式;
(5)A、根据温度对化学平衡移动的影响知识来回答;
B、根据反应速率v=[△c/△t]来计算;
C、催化剂不会引起化学平衡状态的改变,会使反应速率加快,活性越高,速率越快.(1)方法Ⅱ用到的电解法会消耗大量的能源,且反应不易控制,并且方法Ⅲ中,肼做还原剂时会将氧化亚铜还原为金属铜,故答案为:反应不易控制,易还原产生Cu;(2)根据盖斯定律可以得出反应2CuO(s)+C(s)=Cu2O(s...
点评:
本题考点: 铜金属及其重要化合物的主要性质;用盖斯定律进行有关反应热的计算;化学反应速率的影响因素;电解原理.
考点点评: 本题是一道有关热化学、电化学以及化学反应速率和反应限度的综合题,考查角度广,难度大.1年前查看全部
- 纳米级Cu2O由于具有优良的催化性能而受到关注.已知:
纳米级Cu2O由于具有优良的催化性能而受到关注.已知:
2Cu(s)+[1/2]O2(g)═Cu2O(s)△H=-169kJ•mol-1,
C(s)+[1/2]O2(g)═CO(g)△H=-110.5kJ•mol-1,
2Cu(s)+O2(g)═2CuO(s)△H=-314kJ•mol-1
则工业上在高温条件下C+2CuO=Cu2O+CO的热化学方程式为______. 调虎离山1年前1
调虎离山1年前1 -
 Google测试员4329 共回答了24个问题
Google测试员4329 共回答了24个问题 |采纳率91.7%解题思路:本题利用盖斯定律解答,首先分析待求反应中的反应物和生成物,看在已知反应中的位置,通过相互加减求得.已知
①2Cu(s)+[1/2]O2(g)═Cu2O(s)△H=-169kJ•mol-1,
②C(s)+[1/2]O2(g)═CO(g)△H=-110.5kJ•mol-1,
③2Cu(s)+O2(g)═2CuO(s)△H=-314kJ•mol-1
据盖斯定律,①+②-③可得:C(s)+2CuO(s)=Cu2O(s)+CO(g)△H=(-169kJ•mol-1)+(-110.5kJ•mol-1)-(-314kJ•mol-1)=+34.5kJ/mol
故答案为:C(s)+2CuO(s)=Cu2O(s)+CO(g)△H=+34.5kJ/mol.点评:
本题考点: 用盖斯定律进行有关反应热的计算.
考点点评: 有关盖斯定律的习题,首先要根据所求的反应分析,分析以下几点:
1、所求反应中的反应物在哪个反应了?是反应物还是生成物?
2、所给反应中哪些物质是所求反应中没有的?
3、如何才能去掉无用的?然后,通过相互加减,去掉无关物质.
将所对应的△H代入上述化学方程式的加减中就可以了.1年前查看全部
- 四氯化碳与钠反应生成纳米级金刚石粉末化学方程式
四氯化碳与钠反应生成纳米级金刚石粉末化学方程式
RT wdid0071年前1
wdid0071年前1 -
 你以不在 共回答了18个问题
你以不在 共回答了18个问题 |采纳率94.4%CCl4+4Na==C(金刚石)+4NaCl1年前查看全部
- 向浓氯化钙溶液中通入氨气和二氧化碳制取纳米级碳酸钙,为什么应该先通氨气
 abcdef_2071年前1
abcdef_2071年前1 -
 快乐大厨 共回答了27个问题
快乐大厨 共回答了27个问题 |采纳率77.8%中和产生的酸,要是后通,可能产生的碳酸钙又会反应,影响沉淀表面,得不到纳米的了
仅供参考1年前查看全部
- 在加热条件下用液态肼(N2H4)还原新制的氢氧化铜来制备纳米级Cu2O,同时放出N2.求该反应的化学方程式
 vv兒1年前3
vv兒1年前3 -
 小饼粒 共回答了21个问题
小饼粒 共回答了21个问题 |采纳率95.2%N2H4+4Cu(OH)2=2Cu2O+N2+6H2O1年前查看全部
- CCL4和金属钠反应,在700摄氏度时制造出纳米级金刚石粉末!问:制造过程中,元素种类没有变化?这个反应是置换反应?不知
CCL4和金属钠反应,在700摄氏度时制造出纳米级金刚石粉末!问:制造过程中,元素种类没有变化?这个反应是置换反应?不知是其中一个对,还是都错!还是都对!
 Kisa1年前1
Kisa1年前1 -
 爬上枝头摘红杏 共回答了18个问题
爬上枝头摘红杏 共回答了18个问题 |采纳率94.4%元素不变,根据元素守恒定律 置换反应1年前查看全部
- 纳米材料和纳米技术的应用涉及现代工业的各个领域.用纳米级的某种氧化物做催化剂,可以使汽车尾气中的CO和NO迅速反应转化为
纳米材料和纳米技术的应用涉及现代工业的各个领域.用纳米级的某种氧化物做催化剂,可以使汽车尾气中的CO和NO迅速反应转化为两种气体,其中一种是空气中含量最多的气体.请你写出该反应的化学方程式 ___ .
 xixuemao1年前1
xixuemao1年前1 -
 风之鱼 共回答了23个问题
风之鱼 共回答了23个问题 |采纳率95.7%解题思路:根据一种是空气中含量最多的气体,可以知道该气体是氮气,根据化学反应前后的元素种类不变,另一种也是气体,所以应该是二氧化碳,然后根据题目的叙述和上面的推导确定反应物、生成物、反应条件,再结合化学方程式的书写原则写出方程式.空气中含量最多的是氮气,另一种是二氧化碳,反应物是一氧化碳和一氧化氮,生成物是氮气和二氧化碳,反应条件是氧化物作催化剂,所以方程式为:2CO+2NO
氧化物
.
.N2+2CO2点评:
本题考点: 书写化学方程式、文字表达式、电离方程式;空气的成分及各成分的体积分数.
考点点评: 在解此类方程式的书写题时,关键是根据反应物判断出生成物,再依据条件写方程式.1年前查看全部
大家在问
- 1已知:如图,⊙O1,⊙O2外切于点C,AB为外公切线,AC的延长线交⊙O1于点D,若AD=4AC,则∠ABC的度数为 .
- 2初中化学检验NH4离子
- 3请问发【u】、【】、【i】、【e】的单词有哪些(每个音标5个,)
- 4卖油翁中从神态描写卖油翁看陈尧咨射箭的句子是?表现他对陈尧咨射技什么的态度?
- 5It is known to us all E-mail is______ efficient than sending
- 6五.按课文内容填空.闰土向我介绍的几件事分别是雪地捕鸟、夏日拾贝、瓜地刺猹、潮汛看鱼,重点写了()、().
- 7用氢气还原氧化铁时碱石灰的作用及为何去掉氧化铁质量分数会增大
- 8放假了,我可以尽情什么写作文
- 9求证:(1-2sinxcosx)/(tanx-1)=1/(tanx+cotx)-cos^2
- 10图中(单位:cm),梯形由平行四边形和直角三角形组成,这个梯形的面积是______平方厘米.
- 11如图表示闭合电路的一部分导体在磁场中运动时产生感应电流的情形,图中导体垂直纸面,V表示导体的运动方向,小圆圈“O”表示导
- 12高二物理选修3-1的题氢原子的核外电子绕核做圆周运动的轨道半径为r,电子质量为m,电荷量为e,求电子绕核运动的速率和周期
- 132011年3月,媒体上一则《家里90天没人住电表自走了300千瓦时》的报道
- 14第三十到第九十用英语怎么说,光要几十的,整十数.
- 15月球是不是行星
