a是b的充分条件则b是a的必要条件?对吗
 来生愿是鱼2022-10-04 11:39:541条回答
来生愿是鱼2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 七世为魔 共回答了15个问题
七世为魔 共回答了15个问题 |采纳率100%- 不对,如果a和b能互相推的话就叫做彼此的充分必要条件了.例如:a如果一个四边形是平行四边形,b那么他的内角和是360度,正推成立,反之不成立
- 1年前
相关推荐
- 浓度均为.1mol/L的下列溶液等体积混合,充分反应后没有沉淀生成的一组是
浓度均为.1mol/L的下列溶液等体积混合,充分反应后没有沉淀生成的一组是
A.BaCl2、NaOH、NaHCO3
B.Na2CO3、MgCl2、H2SO4
C.MgCl2、NH3·H2O、NaOH
D.Ba(OH)2、CaCl2、NaSO4 waterlibra1年前2
waterlibra1年前2 -
 mercury_rev 共回答了20个问题
mercury_rev 共回答了20个问题 |采纳率95%A.BaCO3(s)
B.MgCO3溶于H2SO4
C.Mg(OH)2(s)
D.BaSO4(s)
答案选B.1年前查看全部
- 6.5克锌粉加入过量的20%的稀盐酸充分反应后滤除106.3克溶液 求(1)反应中生成氢气的质量是多少
6.5克锌粉加入过量的20%的稀盐酸充分反应后滤除106.3克溶液 求(1)反应中生成氢气的质量是多少
(2)加入硫酸溶液的质量为多少克.
(3)反应后溶液中剩余的硫酸溶液中硫酸的质量为多少克. 细菊灵生1年前1
细菊灵生1年前1 -
 魔力多多 共回答了17个问题
魔力多多 共回答了17个问题 |采纳率100%(1)m(H2)=2*6.5/65=0.2g
(2)m(H2SO4溶液)=106.3+0.2-6.5=100g
(3)m(H2SO4)=100*20%-98*6.5/65=10.2g1年前查看全部
- 加热条件下,使足量的CO与Cu和Fe2O3的混合物18.8g充分反应,冷却后,称量剩余物的质量为14g,求剩余物中铜元素
加热条件下,使足量的CO与Cu和Fe2O3的混合物18.8g充分反应,冷却后,称量剩余物的质量为14g,求剩余物中铜元素的质量分数?
 wufei06291年前1
wufei06291年前1 -
 yiqitiaowu 共回答了25个问题
yiqitiaowu 共回答了25个问题 |采纳率92%解题思路:根据质量守恒定律分析固体减少的质量就是氧化铁中氧元素的质量,结合方程式中的比例关系求出参加反应的氧化铁的质量进行分析.根据质量守恒定律分析固体减少的质量就是氧化铁中氧元素的质量,设混合物中氧化铁的质量为x.
Fe2O3+3CO
高温
.
2Fe+3CO2 减少的质量
160 112 48
x 18.8g-14g
[160/x=
48
18.8g−14g]
x=16g
原混合物中铜的质量=18.8g-16g=2.8g
所以剩余物中铜元素的质量分数=
2.8g
14g×100%=20%
答:剩余物中铜元素的质量分数为20%.点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 此题主要考查学生根据化学方程式的计算,根据题意找出已知量和待求量的相关数据,根据化学方程式的解题格式进行计算解答.1年前查看全部
- 计算物质的量浓度?在50ml硫酸和盐酸的混合液中,加入50ml0.2mol/L氢氧化钠溶液,充分反应后恰好中和,然后加入
计算物质的量浓度?
在50ml硫酸和盐酸的混合液中,加入50ml0.2mol/L氢氧化钠溶液,充分反应后恰好中和,然后加入足量的硫酸钡溶液,生成0.233g沉淀,计算混合溶液中硫酸和盐酸的物质的量浓度?(最好有反应方程式)谢啦!
sorry!是加入硝酸钡溶液! 露露的心1年前3
露露的心1年前3 -
 不要对我说永远 共回答了24个问题
不要对我说永远 共回答了24个问题 |采纳率79.2%H2SO4+BaCl2==BaSO4↓+2HCl
1mol 233g
x 0.233g
x=0.001mol c(H2SO4)=0.001/0.050=0.02mol/L
n(NaOH)=0.2×0.050=0.01mol
2NaOH + H2SO4 = Na2SO4 + 2H2O
2 1
y 0.02×0.05 y=0.002mol
NaOH + HCl = NaCl + H2O
1 1
0.01-0.002 z z=0.008mol c(HCl)=0.008/0.050=0.16mol/L1年前查看全部
- 已知p、q都是r 的充分条件,s是r的必要条件,q是s的必要条件,那么p是q的什么条件?
 皮卡丘20031年前1
皮卡丘20031年前1 -
 疼我包容我 共回答了26个问题
疼我包容我 共回答了26个问题 |采纳率92.3%p=》r=》s=》q,q推不出p,估p是q的充分非必要条件1年前查看全部
- 将22gCO和O2的混合气体放入盛有足量的过氧化钠固体的容器中,用电火花不断点燃,充分反应后留下气体的质量为8g,则原混
将22gCO和O2的混合气体放入盛有足量的过氧化钠固体的容器中,用电火花不断点燃,充分反应后留下气体的质量为8g,则原混合气体中CO的质量为?
 hjxiou1年前1
hjxiou1年前1 -
 老木枯草 共回答了16个问题
老木枯草 共回答了16个问题 |采纳率93.8%充分反应后留下气体的质量为8g,即剩余氧气为8g;
2CO+O2=2CO2
2*28 32
x 32x/56 x+32x/56+8=22 x=8.91(g)1年前查看全部
- 把7.2g铁粉投入到某HNO3溶液中,充分反应后剩余固体1.6g,产生NO2和NO的混合气体0.08mol.若不考虑N2
把7.2g铁粉投入到某HNO3溶液中,充分反应后剩余固体1.6g,产生NO2和NO的混合气体0.08mol.若不考虑N2O4的存在,则原HNO3溶液中HNO3的物质的量为多少?
反应的化学方程式有什么, 白侠2孙71年前4
白侠2孙71年前4 -
 尻腻牟 共回答了13个问题
尻腻牟 共回答了13个问题 |采纳率100%把7.2g铁粉投入到某HNO3溶液中,充分反应后剩余固体1.6g,-----------即Fe剩余,即生成Fe2+,不可能有Fe3+,因为Fe3+与Fe是不能共存的,所以溶液中含Fe(NO3)2为(7.2-1.6)/56=0.1mol,即0.2mol的HNO3是酸的作用
产生NO2和NO的混合气体0.08mol.--------------即气体中N原子0.08mol,即氧化剂HNO3为0.08mol
若不考虑N2O4的存在,则原HNO3溶液中HNO3的物质的量为多少?------------0.28mol1年前查看全部
- 交通安全论文400字要求论点明确,论据充分那位帅哥美女帮帮忙
 jais4711年前1
jais4711年前1 -
 满心荒芜 共回答了29个问题
满心荒芜 共回答了29个问题 |采纳率86.2%交通安全在心中
交通事故时时刻刻都会发生,它就像颗威力十足的炸药,一时大意,这颗埋伏在我们生活中的炸药就会爆炸,炸得家庭破碎,炸得人心悲苦.所以我们要遵守交通规则.
我们家附近有一个小女孩,她的爸爸就是因为一次交通事故而离开了她.小女孩家里并不富裕,但是她和爸爸妈妈--起生活得很开心.每天早晨起来,妈妈都会给她和爸爸做上一顿美味的早餐,一家人很温馨.吃完早餐,爸爸骑车送她去上学.一路上,父女俩总是有说有笑.放学后,不管风雨多大,小女孩总是看见爸爸耐心地在等待着.回家的路上,小女孩总是开开心心地向爸爸诉说学校一天所发生的一些有趣的事.
有一天,小女孩的爸爸像平常一样到学校去接小女孩.然而,一辆迎面而来的大卡车由于违规行驶,把小女孩的爸爸撞倒在地,爸爸当场就死去了.一刹那间,死神就夺走了他的生命,他多么希望自己还活着,他多么希望陪在小女孩身边,他多么希望能够看着女儿长大小女孩并不知道自己的父亲己经去世了,她还是像平常一样在学校门口等她的爸爸来接,等了好久,还是没人来接她,小女孩心里想:为什么到这时候爸爸还没来接呢是不是出事了还是家里有什么事小女孩心里很着急.当小女孩得知自己的爸爸己经死去,她似乎傻了,她扑在爸爸的尸体上不断哀求:"爸爸快醒醒!我要爸爸!我要爸爸"她多么希望这场交通事故没有发生,多么渴望爸爸能够醒来,象平常一样用自行车载着她上下学啊!
交通事故是那么可怕,一刹那间,就夺走了人的生命.现在路上的车辆越来越多,马路越来越拥挤,同时交通事故也越来越多,每年,有多少的生命被夺走,有多少个家庭被破坏,有多少人要失去亲人了.如果我们每个人心中都有交通规则,每个人都能自觉遵守交通规则……1年前查看全部
- “真金不怕活来炼”能充分体现金具有的性质是什么?
 同喜同喜1年前2
同喜同喜1年前2 -
 solag 共回答了19个问题
solag 共回答了19个问题 |采纳率94.7%物理性质是熔点高,化学性质是稳定性.1年前查看全部
- 30℃时,将30克A物质投入50克水中充分搅拌恰好饱和,求30℃时A物质的溶解度及溶液的溶质质量分数
 linderxlj1年前1
linderxlj1年前1 -
 pgly 共回答了19个问题
pgly 共回答了19个问题 |采纳率100%溶解度指100克水中能够溶解的溶质的最大质量,所以溶解度为60克.
质量分数=溶质质量/溶液质量=30/(30+50)=37.5%1年前查看全部
- 求证:方程x^2+ax+1=0的两实数的平方和大于3的必要条件是a的绝对值大于3,这个条件是其充分条件吗?为什么
求证:方程x^2+ax+1=0的两实数的平方和大于3的必要条件是a的绝对值大于3,这个条件是其充分条件吗?为什么
尽量详细一点 小米噶1年前2
小米噶1年前2 -
 uu小肚兜儿 共回答了16个问题
uu小肚兜儿 共回答了16个问题 |采纳率87.5%证:
设方程两根分别为x1,x2.由韦达定理,得
x1+x2=-a
x1x2=1
已知条件为x1²+x2²>3
x1²+x2²=(x1+x2)²-2x1x2=a²-2>3
a²>5
|a|>√5
题目有问题,并不需要|a|>3,只要|a|>√5就可以了,命题不成立.1年前查看全部
- 将一定量碳酸钙高温一段时间后,再将固体剩余物投入到300g8.76%的稀盐酸中,充分反后,可生成4.84g二氧化碳,且溶
将一定量碳酸钙高温一段时间后,再将固体剩余物投入到300g8.76%的稀盐酸中,充分反后,可生成4.84g二氧化碳,且溶液中只含一种溶质.
求1固体剩余物中钙元素的质量分数
2生成溶液中溶质的质量分数 世事难两全1年前1
世事难两全1年前1 -
 我的等待1 共回答了16个问题
我的等待1 共回答了16个问题 |采纳率75%1、57.6%
2、12.48%1年前查看全部
- 1木炭不充分燃烧2 一氧化碳燃烧 3甲烷燃烧4 酒精燃烧5碳和二氧化碳反应6碳还原氧化铜7碳还原氧化铁8氢气还原氧化铜9
1木炭不充分燃烧2 一氧化碳燃烧 3甲烷燃烧4 酒精燃烧5碳和二氧化碳反应6碳还原氧化铜7碳还原氧化铁8氢气还原氧化铜9工业煅烧石灰石10一氧化碳还原氧化铜 11加热铜粉 最好发图片谢谢
 qwteryeru1年前1
qwteryeru1年前1 -
 cqitic-solow 共回答了14个问题
cqitic-solow 共回答了14个问题 |采纳率92.9%1、2C+O2=2CO
2、2CO+O2=2CO2
3、CH4+2O2=CO2+2H2O
4、C2H5OH+3O2=2CO2+3H20
5、C+CO2=2CO
6、C+CUO=CO+CU;C+2CUO=CO2+2CU
7、3C+Fe2O3=3CO+2Fe;3C+2Fe2O3=2CO2+4Fe
8、H2+CUO=CU+H2O
9、CaCO3=CaO+CO2
10、CO+CUO=CU+CO2
11、2CU+O2=2CUO
我的答题到此结束,谢谢
希望我的答案对你有帮助1年前查看全部
- 取2.9g生铁与足量的CuSO4溶液充分反应,过滤,得到3.2g铜单质,则所取铁合金中碳元素的质量分数
取2.9g生铁与足量的CuSO4溶液充分反应,过滤,得到3.2g铜单质,则所取铁合金中碳元素的质量分数
(假设该生铁中的杂质只有铁元素.) 何马1年前1
何马1年前1 -
 珊蔡姐 共回答了11个问题
珊蔡姐 共回答了11个问题 |采纳率90.9%CuSO4+Fe=Cu+FeSO4
56g 64g
mg 3.2g m=2.8g
碳的质量分数=(2.9-2.8)÷2.9×100%=3.4%1年前查看全部
- 简单概括下面这段话经过充分的准备,5月24日上午9时,登山队员王富洲、刘连满、屈银华和贡布向珠峰最后380米高度冲击.他
简单概括下面这段话
经过充分的准备,5月24日上午9时,登山队员王富洲、刘连满、屈银华和贡布向珠峰最后380米高度冲击.他们艰难地向前行进着.两个多小时后,著名的“第二台阶”挡住了他们的去路.他们沿着第三次行军侦察的路线,冒着严寒,花了五个多小时,用搭人梯的方式,爬上了不到7米高的“第二台阶”.这时,队员们又不得不面对另一个对手——黑夜的挑战.他们借着雪夜的反光,一步一步地前进.由于前面用时过多,他们背上的氧气已经所剩不多了,他们现在又受到缺氧的严重威胁.反应最强烈的是刘连满,他每前进一步都非常困难了.为了争取时间,大家决定刘连满留下,其余三人以最快速度突击登顶.严重缺氧的刘连满躺在一块避风的大石块旁边休息,开始进入一种半昏迷状态.这时,他冒着生命危险,毅然决定把自己所剩不多的氧气留给登山的同志,并留下了一封感人的短信.与此同时,三位登山队员正搏斗在前进的道路上.他们匍匐在地上,借着星光和反照的雪光,辨认路途,艰难前进.到8 830米时,三人的氧气已经全部用完,他们果断地抛掉背上的空氧气筒,开始了人类历史上从未有过的艰难而危险的无氧攀登.这样的攀登,其艰苦程度可想而知.他们四肢更加沉重了,行动更加迟缓了,有时攀过一米高的岩石,也要用半个多小时.但必胜的信念在支持着他们.凌晨,他们终于登上了珠穆朗玛峰,完成了人类历史上从北坡攀上世界最高峰的创举. glfxluo1年前1
glfxluo1年前1 -
 264763014 共回答了21个问题
264763014 共回答了21个问题 |采纳率85.7%5月24日上午9时,经过充分准备的登山队员王富洲、刘连满、屈银华和贡布,在天黑路滑等不利条件下,不畏严寒顽强拼搏,经过十几个小时的艰难攀登,终于在凌晨到达珠穆朗玛峰,完成了人类历史上从北坡攀上世界最高峰的创举.1年前查看全部
- 1 .在一个密闭的钢筒内有A,B,C,D四种物质,通过电火花引燃后,充分发生反应.经测定,钢筒内反应前后个物质的质量如下
1 .在一个密闭的钢筒内有A,B,C,D四种物质,通过电火花引燃后,充分发生反应.经测定,钢筒内反应前后个物质的质量如下:
物质 A B C D
反应前质量(g) 4 10 1 25
反应后质量(g)(未测) 21 10 9
若A的分子量为n,D的分子量为2n,则该反应中A与D的化学计量数之比为______.
2.现取2.3g有机物在足量的氧气中充分燃烧,生成4.4gCO2和2.7gH2O,判断正误.
A.分子中C.H的原子个数比为2:5
B.分子中C.H.O的元素质量比为12:3:8.
3.将铁粉加入含有铜离子和银离子的溶液中,充分反应后加入盐酸,发现无气泡产生,但却有白色沉淀产生,则加入盐酸前的物质中含有____.
A.铜离子、银离子、铁离子、银单质 B.铁离子、银离子、铜离子、铜单质
C.铜单质、银单质、银离子、铁离子 D.铜离子、银离子、铁单质、铁离子
4.某样品含有氢氧化钾、碳酸钾和水三种物质.室温下,向该样品中加入浓度为14.6%的稀盐酸100g,恰好完全反应得到中性溶液,蒸干该溶液得到的固体质量为_____.
A.74.5g B.29.8g C.10g D.7.45g
5.下图是某元素的原子结构示意图,下列对该元素的认识正确的是_____.
A.该元素属于金属元素
B.该元素的原子在化学反应中容易失电子
C.该元素的原子核外电子总数为18
D.该元素位于元素周期表的第四周期第VIA族
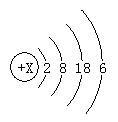
 xudiok1122111年前3
xudiok1122111年前3 -
 家居猫 共回答了22个问题
家居猫 共回答了22个问题 |采纳率86.4%1:2
错 对
A
B
D1年前查看全部
- 在锥形瓶中加入68g过氧化氢溶液4g过氧化锰充分反映锥形瓶内剩余液体质量68.8g 问氧气质量?溶液质量分数/
 走进湘情1年前1
走进湘情1年前1 -
 8937211 共回答了21个问题
8937211 共回答了21个问题 |采纳率85.7%解析:根据质量守恒定律,反应物总质量等于生成物的总质量.则有:
68 + 4 = 68.8+ m(O2) 所以m(O2)=3.2(g)
2H2O2 = MnO2= 2H2O +O2()
2*34 32
m(H2O2) 3.2 m(H2O2)= 6.8(g)
H2O2% = 6.8/68=10% 答:略1年前查看全部
- 充分反应与完全反应与恰好完全反应三者的区别!
 真实梦境1年前1
真实梦境1年前1 -
 带皮的红豆 共回答了17个问题
带皮的红豆 共回答了17个问题 |采纳率82.4%充分反应:就是至少有一种反应完了,不能反应了.
完全反应:就是充分反应,至少有一种反应完了,不能反应了
恰好完全反应:全反应完了,无剩余.1年前查看全部
- 充分反应是不是完全反应充分反应是不是反应物的质量全部转化为形成物?现有化学反应X+Y=Z 若将a克X和b克Y在一定条件下
充分反应是不是完全反应
充分反应是不是反应物的质量全部转化为形成物?
现有化学反应X+Y=Z
若将a克X和b克Y在一定条件下充分反应,生成物Z的质量为? 峰回路转又一村1年前2
峰回路转又一村1年前2 -
 jdfn3504 共回答了18个问题
jdfn3504 共回答了18个问题 |采纳率88.9%充分反应不是完全反应
完全反应指反应物全没了
充分反应指反应达到平衡,即反应物和生成物的量不变了
对你问题的补充:
因为该反应是不可逆反应,所以充分反应后X和Y都反应掉了,根据质量守恒Z的质量就是(a+b)g1年前查看全部
- 铁的合金60g在氧气中充分燃烧产生8.8g二氧化碳,通过计算确定该合金是生铁还是钢?,
 wh0071年前2
wh0071年前2 -
 gaotian007 共回答了15个问题
gaotian007 共回答了15个问题 |采纳率93.3%只有碳才能够氧化成为二氧化碳,根据题意:
C+O2=CO2
可知:8.8/44=0.2mol,由于化学反应C与CO2mol 比是1:1,所以消耗的也是0.2mol的碳.
0.2mol的碳为:0.2X12=2.4g碳,该60g的铁的合金含有2.4g碳,故含碳量为:
2.4/60=0.04=4%,由于铁碳合金中,含碳量0.0218~2.11%的为钢,含碳量2.11~6.69%为生铁,而本铁的合金含碳量为4%,含碳量>2.11…%,故为生铁.1年前查看全部
- 某溶液中含有 SiO32-、SO32- 、AlO2- 、NO3- 等四种阴离子,若向其中加入过量的盐酸溶液,充分反应,一
某溶液中含有 SiO32-、SO32- 、AlO2- 、NO3- 等四种阴离子,若向其中加入过量的盐酸溶液,充分反应,一段时间后,再加入过量的 NaOH 溶液,则 溶液中一定大量减少的阴离子是( ) A.NO3- B. SiO32- C.SO32-D.AlO2-
 Caryli82711年前2
Caryli82711年前2 -
 舞者狂野 共回答了21个问题
舞者狂野 共回答了21个问题 |采纳率76.2%3SO32- +2NO3-+2H+=3SO42-+2NO+H2O
答案AC1年前查看全部
- 有NaCl和KCl的混合物26.6g,溶于水形成溶液,加入含0.8摩尔硝酸银的溶液200克,充分反应后滤出沉淀,洗涤干燥
有NaCl和KCl的混合物26.6g,溶于水形成溶液,加入含0.8摩尔硝酸银的溶液200克,充分反应后滤出沉淀,洗涤干燥
称其质量为57.4g,求原混合物中NaCll,KCl的物质的量各为多少? 刘tt宇1年前2
刘tt宇1年前2 -
 彝家小妹妹 共回答了10个问题
彝家小妹妹 共回答了10个问题 |采纳率100%NaCl,KCl各有0.2mol.解析如下:
通过AgCl的质量57.4g,可得n(AgCl)=0.4mol,即原混合物中Cl为0.4mol.由于混合物可以写成XCl的形式,所以原混合物总物质的量就是0.4mol.于是我们可以算出该混合物的平均摩尔质量
M=26.6/0.4=66.5g/mol.正巧发现,NaCl和KCl二者摩尔质量的平均数(58.5+74.5)/2=66.5!所以二者物质的量之比就是1:1,各为0.2mol啦!
注:通过平均摩尔质量计算二者比例时,更普适的算法应该是十字交叉,如果楼主不懂,我可以详细解释~
希望对你有所帮助!1年前查看全部
- 两种有机物以任意比例混合,一定条件下aL(标况)足量O2中充分燃烧,再将剩余的氧气和全部的生成物通过足量的过氧化钠,得到
两种有机物以任意比例混合,一定条件下aL(标况)足量O2中充分燃烧,再将剩余的氧气和全部的生成物通过足量的过氧化钠,得到气体的体积大于aL(标况),下列组合中符合此条件的是
A、CH4 C2H4
B、CH3OH CH3COOH
C、C6H6 HCOOCH3
D、HCOOH HOCH2CH2COOH 一棹春风1年前1
一棹春风1年前1 -
 低音提琴 共回答了29个问题
低音提琴 共回答了29个问题 |采纳率93.1%答案:D
答案解析:试题分析:根据题意可知,反应前后氧气的体积是不变的,这说明反应的实质相当于是CO+Na2O2=Na2CO3、H2+Na2O2=2NaOH.所以要满足条件,则物质的组成必须满足(CO)n(H2)m,因此根据物质的化学式可知,选项AC不可能,B中以任意比例混合均可以.D中二者按照1:1混合即可,所以答案选D.1年前查看全部
- 将a克铜粉和木炭粉的混合物在空气中充分灼烧后,生成a克剩余物,求混合物中木炭粉和氧化铜质量
 11603656591033881年前3
11603656591033881年前3 -
 teachertan 共回答了12个问题
teachertan 共回答了12个问题 |采纳率91.7%生成CuO,得到的黑色物质与原混合物的质量相同,可知铜粉和木炭粉的质量=CuO的质量,所以混合物中铜与木炭的质量比=CuO中铜的质量:氧的质量=64:16=4:1.1年前查看全部
- x=1是(x-1)(x-2)=0的必要条件还是充分条件?为什么?
 我水域1年前3
我水域1年前3 -
 A超越梦想 共回答了20个问题
A超越梦想 共回答了20个问题 |采纳率90%充分条件,因为x=1时,后式显然成立
但后式成立时,x可为1或2,所以这不是必要条件.1年前查看全部
- 王昌龄的 出塞充分表达了历代人民对一代名将 李广 的( )之情,和()之情
 xmjanson1年前1
xmjanson1年前1 -
 莲子花落 共回答了21个问题
莲子花落 共回答了21个问题 |采纳率95.2%钦佩,敬仰1年前查看全部
- H2与O2混合气体26克充分反应所得再与NA2O2反应,是固体增加2克
H2与O2混合气体26克充分反应所得再与NA2O2反应,是固体增加2克
求原混合气体中H2与O2的质量 秋水封尘1年前2
秋水封尘1年前2 -
 九天冰海1 共回答了20个问题
九天冰海1 共回答了20个问题 |采纳率85%方程式:
2 Na2O2+2 H2O =4 NaOH +O2
用差量法算
设Na2O2物质的量是X,80*X-78*X=2
X=1
则水为1MOL
1:H2 10, O2 16
2:H2 2, O2 241年前查看全部
- 将鸡蛋壳洗净干燥并捣碎后称取10g放在烧杯里然后往烧杯中加入足量的稀盐酸90g充分反应后剩余物
将鸡蛋壳洗净干燥并捣碎后称取10g放在烧杯里然后往烧杯中加入足量的稀盐酸90g充分反应后剩余物
将鸡蛋壳洗净,干燥并捣碎后,称取10g放在烧杯里,然后往烧杯中加入足量的稀盐酸90g.充分反应后剩余物为97.14g产生二氧化碳气体多少g? 520hwx1年前1
520hwx1年前1 -
 成都亚明 共回答了28个问题
成都亚明 共回答了28个问题 |采纳率96.4%由题目可知反应物总重量为10+90=100克
反应剩余物为97.14克
可知产生CO2气体为100-97.14=2.86克
由反应方程式CaCO3+2HCl=CaCl2+H2O+CO2
100 44
x 2.86
解得CaCO3重量为6.5克
可知鸡蛋中CaCO3的质量分数为6.5/10*100=65%1年前查看全部
- 标况下,将20L,CO2和CO的混合气体通过足量的NA2O2粉末,充分反应后,在相同情况下气体体积减少至16L,原混合其
标况下,将20L,CO2和CO的混合气体通过足量的NA2O2粉末,充分反应后,在相同情况下气体体积减少至16L,原混合其中CO的体积是?
答案是12L.可是, 水木白1年前2
水木白1年前2 -
 错了就过了 共回答了21个问题
错了就过了 共回答了21个问题 |采纳率90.5%设二氧化碳体积x L
2 CO2+2 Na2O2=2 Na2CO3+O2
2 1
x x/2
减少的体积是x/2 L =16
x=81年前查看全部
- 12g氢气 氧气混合物气体在一定条件下充分反应后生成9g水 则原混合气体中氢气与氧气的质量比可能是___________
12g氢气 氧气混合物气体在一定条件下充分反应后生成9g水 则原混合气体中氢气与氧气的质量比可能是_____________或___________ 要求有过程 不急 过程一定要写明白
 圆圆2111年前2
圆圆2111年前2 -
 ccstar12 共回答了19个问题
ccstar12 共回答了19个问题 |采纳率100%如果氧气过量 9克水 里面含氢 1克 所以氢气1克 氧气11克 如果氢气过量 9克水 里面含氧 8克 所以氧气8克 氢气4克 质量比为 1比11 或1比21年前查看全部
- 哪有高一英语教学方案充分点
 人生如戏8101131年前2
人生如戏8101131年前2 -
 lonelystar119 共回答了17个问题
lonelystar119 共回答了17个问题 |采纳率94.1%这个是高一上的知识总结
这个是高一总复习
这个是新东方搞得针对高一的笔记
这个是针对性的高一试题1年前查看全部
- 将0.1mol铜与40ml10mol/LHNO3充分反应后,溶液中含有amolH+,由此可知生成的气体标准状况下的体积是
将0.1mol铜与40ml10mol/LHNO3充分反应后,溶液中含有amolH+,由此可知生成的气体标准状况下的体积是多少?
 lclclc009101年前2
lclclc009101年前2 -
 渔阳鼓动 共回答了20个问题
渔阳鼓动 共回答了20个问题 |采纳率80%这题可以运用守恒思想:硝酸在反应中起两个作用:一是显酸性,一是显氧化性.则可以得到:反应的硝酸=显酸性的 + 显氧化性的
显酸性的硝酸,也就是生成盐的硝酸.根据对应关系可以计算:
Cu------2NO3- -----2HNO3
1------------------------2
0.1mol-----------------x=0.2mol
因此,被还原的硝酸=0.04*10-a-0.2=(0.2-a) mol
又知,10mol/LHNO3浓硝为浓硝酸,还原产物为NO2.
则NO2的物质的量=被还原的硝酸=(0.2-a) mol
所以体积=22.4*(0.2-a)1年前查看全部
- 要让煤充分燃烧,通常采用的两种方法是
 weibsrr1年前1
weibsrr1年前1 -
 fandywj3 共回答了16个问题
fandywj3 共回答了16个问题 |采纳率100%1 增大氧气供应量;
2 增大氧气与燃料的接触面积,比如煤块变成煤粉,更容易充分燃烧.1年前查看全部
- 将质量为m 克的二氧化碳与过量过氧化钠固体充分反应,试分析固体质量的变化(谢谢大家)
 pretencer1年前3
pretencer1年前3 -
 楠喃 共回答了16个问题
楠喃 共回答了16个问题 |采纳率87.5%(1)差量法
2Na2O2+2CO2=2Na2CO3+O2 固体的分子量增大了(212-156=56)
88 56
m x
x=56m/88=7m/11 固体质量增加7m/11
(2)一般的设xy来解
2Na2O2+2CO2=2Na2CO3+O2
156 88 212
x m y x=156m/88 y=212m/88
固体质量增加=212m/88-156m/88=7m/111年前查看全部
- 〔急〕市售 黄金粉 是由Zn和Cu组成的合金粉,将此粉20g与93.7g稀硫酸充分反应,可得氢气0.2g.将反应后的混合
〔急〕
市售 黄金粉 是由Zn和Cu组成的合金粉,将此粉20g与93.7g稀硫酸充分反应,可得氢气0.2g.将反应后的混合物过虑,所虑出固体中只含Cu
1.求黄金粉中Zn的质量分数 amyloveamyhoho1年前1
amyloveamyhoho1年前1 -
 48480501 共回答了20个问题
48480501 共回答了20个问题 |采纳率100%Zn+H2SO4=ZnSO4+ H2↑
65 2
x 0.2
65/x=2/0.2,解得x=6.5
故黄金粉中含有6.5gZn,且质量分数为6.5/20*100%=32.5%1年前查看全部
- 现有一块金属钠放在水中充分反应,溶液质量增加4.4克.则消耗钠多少克.
 包晚娘1年前1
包晚娘1年前1 -
 summermore 共回答了17个问题
summermore 共回答了17个问题 |采纳率82.4%2Na+2NaOH=2NaOH+H2 △
46 36 80 80-36=44
X 4.4g
Na反应4.6g1年前查看全部
- 高数极限例题一问证x(n)=(-1)^(n-1)/(n+1)^2极限为0.书上是先放缩,后找充分条件n>1/E-1问:可
高数极限例题一问
证x(n)=(-1)^(n-1)/(n+1)^2极限为0.
书上是先放缩,后找充分条件n>1/E-1
问:可不可以直接不用放缩
|x(n)-0|=1/(n+1)^2
只需证n>|根号(1/E)-1|
然后取N=【|根号(1/E)-1|】
当n>N时…… 土石山川1年前2
土石山川1年前2 -
 tonywangm 共回答了11个问题
tonywangm 共回答了11个问题 |采纳率100%可以倒是可以,但不知道您那绝对值是怎么算出来的.
我是这么证的,您看看对不.
只需证存在正整数N,使n>N时,n>√(1/ε)-1
然后取N=[√(1/ε)],不取N=[√(1/ε)-1]是考虑到N非负,
然后您就会了吧.1年前查看全部
- 勤奋是成功的必要条件还是充分条件还是充分心要条件
勤奋是成功的必要条件还是充分条件还是充分心要条件
勤奋是成功的必要条件 还是 充分条件 还是 充分心要条件 红尘里的风1年前1
红尘里的风1年前1 -
 sushui626 共回答了17个问题
sushui626 共回答了17个问题 |采纳率88.2%因为勤奋才能成功,
成功未必是只依靠勤奋,
所以,
勤奋是必要但不充分条件.
勤奋+正确的方法+机遇=成功1年前查看全部
- 将10.2克氧化铝溶于浓度为1.2mol/L的盐酸500ml,充分反应后,再逐滴加入1mol/L的氢
将10.2克氧化铝溶于浓度为1.2mol/L的盐酸500ml,充分反应后,再逐滴加入1mol/L的氢
加入多少毫升NAOH溶液时,开始有沉淀?
再加入多少,沉淀最多?
再加多少,从最大值到恰好消失?
求具体点的解析 溪水竹帘1年前2
溪水竹帘1年前2 -
 glyoxylate 共回答了18个问题
glyoxylate 共回答了18个问题 |采纳率100%10.2克氧化铝是0.1mol,500ml 1.2mol/L的盐酸是0.6mol
Al2O3 + 6HCl Al(OH)3↓ + 3NaCl
1 3
0.2====》0.6
溶液中有0.2mol AlCl3,所以加入NaOH 0.6mol时,沉淀最多.既600ml.
3、 Al(OH)3+ NaOH===NaAlO2 + 2H2O
1 1
0.2====>0.2
操作二中生成0.2mol 氢氧化铝,根据方程式,加入氢氧化钠0.2mol后,沉淀消失,既200ml1年前查看全部
- 在一定温度下,将一包白色无水硫酸铜粉末投入到150g蒸馏水中,充分搅拌,过滤,得到一定质量的蓝色晶体和84g滤液,若此温
在一定温度下,将一包白色无水硫酸铜粉末投入到150g蒸馏水中,充分搅拌,过滤,得到一定质量的蓝色晶体和84g滤液,若此温度下无水硫酸铜的溶解度为40g,则此包无水硫酸铜的质量是多少?
 默儿爱李强1年前3
默儿爱李强1年前3 -
 光看不回帖 共回答了20个问题
光看不回帖 共回答了20个问题 |采纳率90%解题思路:根据饱和溶液中质量分数不变和溶解度计算出剩余饱和溶液中溶质和溶剂的质量,根据硫酸铜晶体组成计算晶体中溶质的质量,两者之和为此包无水硫酸铜的质量.把无水硫酸铜粉末加入150g蒸馏水中,得到一定量的蓝色晶体CuSO4•5H20,剩余溶液仍然是饱和溶液,设剩余溶液中的溶质为xg,
则[40g/100g+40g]=[xg/84g]得:x=24
结晶水的质量=150g-(84g-24g)=90g,设结晶中硫酸铜的质量为yg
CuSO4~5H20
160 90
yg90g
[160/90]=[yg/90g]
y=160,此包无水硫酸铜的质量为=160g+24g=184g.
答:此包无水硫酸铜的质量是184g.点评:
本题考点: 溶液中溶质的质量分数及相关计算.
考点点评: 本题考查质量守恒定律,质量分数的计算,解题时注意守恒思想的运用.1年前查看全部
- 已知氧化性Cl2>Br2>I2,向NaI和NaBr的混合溶液中通入足量的氯气,充分反应后将溶液蒸干,并灼烧残留物,最后得
已知氧化性Cl2>Br2>I2,向NaI和NaBr的混合溶液中通入足量的氯气,充分反应后将溶液蒸干,并灼烧残留物,最后得到的物质是(提示:溴单质易挥发、碘单质易华)( )
A. NaCl、I2
B. NaCl、NaBr
C. NaBr、I2
D. NaCl caicc1年前2
caicc1年前2 -
 喵呜呜呜呜呜 共回答了24个问题
喵呜呜呜呜呜 共回答了24个问题 |采纳率95.8%解题思路:因氧化性Cl2>Br2>I2,则在Br-、I-中,还原性由弱到强为Br-<I-,向含有NaBr和NaI的混合溶液中通入足量氯气发生:2NaI+Cl2=2NaCl+I2、2NaBr+Cl2=2NaCl+Br2,结合Br2和I2的性质分析.在Br-、I-中,还原性由弱到强为Br-<I-,向含有NaBr和NaI的混合溶液中通入足量氯气发生:2NaI+Cl2=2NaCl+I2、2NaBr+Cl2=2NaCl+Br2,将溶液蒸干并充分灼烧,溴易挥发,碘易升华,得到固体剩余物质的组成只有氯化钠,
故选D.点评:
本题考点: 卤素原子结构及其性质的比较.
考点点评: 本题考查卤素知识,为高频考点,注意把握物质的性质的异同,结合还原性强弱解答该题,题目难度不大,注意相关基础知识的积累.1年前查看全部
- 谁给我写篇关于想念的文章?要充分写出对一个人的想念,最好写的平民化一点,其次要写出已经放弃对方了!
 淡水妖妖1年前1
淡水妖妖1年前1 -
 西江弄影 共回答了12个问题
西江弄影 共回答了12个问题 |采纳率83.3%远方的你 现在还好吗 在没有你的夜里 再也闻不到你头发上的淡淡芳香 再也闻不到你的味道 再也看不见你微笑时那浅浅的酒窝 再也看不见你撒娇时害羞的表情 忘不了你最喜欢吃的菜 忘不了你最喜欢的颜色 忘不了你最喜欢的衣服的风格 忘不了你最爱的运动 忘不了你最爱说的口头禅 更忘不了我最爱吃的菜你却是最不敢吃的菜 可是 每一次 当我问你要吃吗?你却显得很喜欢 当上菜了 你却只是一个劲儿 給我夹菜 你却不动筷子 今夜注定又是一个无眠之夜 站在窗前抬头望着夜空 记得你曾说过 亲爱的 只要你 抬头看的见星星和月亮 那么 就还有希望还有未来 我以为我懂了 现在我知道了 原来我错了 远方的你 现在好吗 我许不了 你要的未来 我給不了 你要的幸福 所以你选择 离开 记得我曾说过 只要你幸福 我可以放弃所有的一切 因为只有你幸福了 所以我才会幸福 亲爱的 让我最后一次这样的称呼 过了今夜 我就不会再这样称呼了 放手 放爱一条生路 我把你的爱收起来 放在我心里的右边 远方的你 一定要幸福哦1年前查看全部
- 一道条件充分判断题:实数a,b满足l a l(a+b)>a l a+b l
一道条件充分判断题:实数a,b满足l a l(a+b)>a l a+b l
条件1.a< 0
条件2.b>-a JT_terry1年前1
JT_terry1年前1 -
 你明白了 共回答了25个问题
你明白了 共回答了25个问题 |采纳率76%由条件2可知a+b>0,条件1可知原试左边大于零,右边小于零,故|a|(a+b)>a|a+b|1年前查看全部
- 由CaO和CaCO3组成的混合物mg在高温下充分煅烧,所得固体质量是原混合物质量的67%,则原混合物中CaO与CaCO3
由CaO和CaCO3组成的混合物mg在高温下充分煅烧,所得固体质量是原混合物质量的67%,则原混合物中CaO与CaCO3的质量比为多少?
 幸福貝宝1年前3
幸福貝宝1年前3 -
 飞翼hj 共回答了19个问题
飞翼hj 共回答了19个问题 |采纳率94.7%解题思路:根据题干提供的数据结合反应的化学方程式进行分析解答即可.高温煅烧碳酸钙和氧化钙的混合物,会生成二氧化碳,故减少的质量为二氧化碳,其数值为:mg×(1-67%)=0.33mg,
设碳酸钙的质量为x
CaCO3
高温
.
CaO+CO2↑
100 44
x 0.33mg
[100/x=
44
0.33mg] x=0.75mg
故氧化钙的质量为:mg-0.75mg=0.25mg
氧化钙与碳酸钙的质量比为:0.25mg:0.75mg=1:3
答:原混合物中氧化钙与碳酸钙的质量比为1:3.点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 本题考查了根据化学方程式的计算,完成此题,可以依据题干提供的数据结合反应的化学方程式进行.1年前查看全部
- 有关混合物中求质量分数有二氧化碳和一氧化碳的混合物共70g,通入足量的灼热氧化铜,充分反应后,固体质量减少32g,二氧化
有关混合物中求质量分数
有二氧化碳和一氧化碳的混合物共70g,通入足量的灼热氧化铜,充分反应后,固体质量减少32g,二氧化碳的质量分数为多少?
(不求最快,只求最好的) chenxin1281年前1
chenxin1281年前1 -
 hlw3607353017 共回答了15个问题
hlw3607353017 共回答了15个问题 |采纳率93.3%CuO+CO=Cu+CO2
减少的32克都是CuO中的氧,也就是32/16=2mol
根据反应式与CuO反应的CO也是2mol,所以CO的质量为28*2=56g
CO2含量为70-56=14g
质量分数为14/70=20%1年前查看全部
- 人教A版P29“函数y=f(x)在一点的导数值为0是函数y=f(x)在这点取极值的必要条件而非充分条件”是否错误?
 XUGANG1231年前1
XUGANG1231年前1 -
 XjCys 共回答了18个问题
XjCys 共回答了18个问题 |采纳率94.4%我怎么觉得既不充分,也不必要呢,当然,可以探讨:
第一,函数f(x)在一点的导数为零,并不能说明在该点可以取极值,比如f(x)=x^3
第二,函数在一点取得极值,也不能说明函数在该点导数为零,前提须是函数在该点
可导,且导数为0才行,比如:y=sqrt(x^2)1年前查看全部
- 将一定质量的锌,氧化铁,氧化铜的混合粉末放入含有0.22molHCl中,充分反应后生成448mlH2(标准状况),残留
将一定质量的锌,氧化铁,氧化铜的混合粉末放入含有0.22molHCl中,充分反应后生成448mlH2(标准状况),残留
固体0.64g.过滤,滤液中无Cu2+.滤液中还有0.04molHCl.那么原混合物中Zn的质量为多少克? jlzh1年前2
jlzh1年前2 -
 卖精来上网 共回答了26个问题
卖精来上网 共回答了26个问题 |采纳率96.2%解;固体0.64g为铜,物质的量为0.01mol,氧化铜的物质的量为0.01mol.耗HCl 0.02mol
448mlH2(标准状况),物质的量为0.02mol,耗HCl 0.04mol.滤液中还有0.04molHCl.
所以氧化铁耗HCl 为0.22-0.02-0.04-0.04=0.12mol.发生反应如下:
Fe2O3+6HCl=2FeCl3+3H2O 2FeCl3+Zn=2FeCl2+ZnCl2
6mol 2mol 2mol 1mol
0.12mol 0.04mol 0.04mol 0.02mol
CuO +2HCl = CuCl2+H2O CuCl2 + Zn= ZnCl2+Cu
0.01mol 0.01mol 0.01mol 0.01mol
Zn+2HCl = ZnCl2+ H2
0.02mol 0.02mol
所以共消耗锌的物质的量为0.02mol+0.01mol+0.02mol =0.05mol
原混合物中Zn的质量为;0.05mol乘以65=3.25克1年前查看全部
- 氯化铁和氯化铜混合溶液中加入过量铁粉充分反应溶液的质量没有变则原混合溶液三价铁二价铜物质的量之间比
 knight1151年前2
knight1151年前2 -
 oldyan 共回答了14个问题
oldyan 共回答了14个问题 |采纳率85.7%反应完全后溶液中不含有铜离子
2FeCl3+Fe==3FeCl2 增加了56的相对质量
CuCl2+Fe==FeCl2+Cu 减少了8的相对质量
56/8=7
若使反应的量相等则应在第二个方程式前各加系数7
Fe3+:Cu2+ =2:71年前查看全部
- 将10.2g的氧化铝溶于一定浓度的500mL的盐酸溶液中,充分反应后,再逐滴加入1mol/L的氢氧化钠溶液,反应过程中生
将10.2g的氧化铝溶于一定浓度的500mL的盐酸溶液中,充分反应后,再逐滴加入1mol/L的氢氧化钠溶液,反应过程中生成沉淀的质量与加入氢氧化钠溶液的体积关系如下图,试计算:
1)最大沉淀的质量.2)当沉淀从最大值到恰好完全消失时,耗用多少毫升的氢氧化钠溶液?)
图在此网址,去掉空格!
h ttp://zhidao.baidu.com/question/122688934.html
觉得那个第二个答案不对. wujun25881年前1
wujun25881年前1 -
 V5840 共回答了24个问题
V5840 共回答了24个问题 |采纳率95.8%这道题很简单的 你一看图就应该知道之前加的HCL是过量的 中和之后 此时溶液中恰好AL3+单独存在 AL3+离子0.2mol AL离子守恒 那么0.2*M(Al(HO)3)=《M(Al2O3)+3M(O)+6》*0.1=15.6g
2.沉淀有0.2mol 因此需要NaHO也是0.2mol 也就是200ml 完了 算了那么复杂做什么?
第一问 看到沉淀就看沉淀是什么 这个题果断是AL(HO)3 根据第一句话可以得到AL3+有0.2mol 则沉淀氢氧化铝就是0.2mol嘛 又看 0.2molAL(HO)3 比0.1molAl2O3多了0.3个氧的质量 0.6个氢的质量 直接口算答案就出来了
第二问更没意思 关键是要看清题 别个问的是从沉淀最多到恰好完全消失 问的是这个过程 1mol氢氧化铝消耗一个氢氧根 1比1嘛 于是就有了三 消耗0.2mol 则200ml 够清楚吧 这种题 不要看过程 不要管变化 始终铝离子守恒 拿到傻算的都是莽夫1年前查看全部
大家在问
- 1张明读一本书,第一天读书的20%,第二天读了[5/8],第二天比第一天多读34页,张明一共读了多少页?
- 2关于硫和氮的氧化物的题目在氯化钡的水溶液中通入二氧化硫未见沉淀,把其分成两份,向其中一份中A加入NH3,另一份B加入CL
- 3在数轴上,距离表示3的点5.5个单位的数是
- 4什么是阳光心态,阳光心态的最终目标是什么?
- 5《秋天》本文描写了三幅图片,请用自己的语言将一幅图片描述出来.100字左右
- 6Is the student s' English teacher old or young?回答
- 7已知函数f(x)=log a (3-ax).
- 8下列关于生产者的叙述,不正确的是( )
- 9右表为甲、乙两人比赛投篮球的记录,以命中率(投进球数与投球次数的比值)来比较投球成绩的好坏,得知他们的成绩一样好,下面有
- 10第30届英国伦敦奥运会已于2012年7月开幕,第31届巴西里约热内卢奥运会将于2016年8月5日开幕.图1为英国和图2为
- 11论名利 作文
- 12一棱长为10厘米的正方体铁皮箱,改造成一个长20厘米,宽5厘米的长方体箱子,表面积不变,则新箱子的高是
- 13英语作文:在公园里(进行时)是四十词.还要翻译
- 14it's necessary that the problem__in some way or other
- 15读图,完成下列要求(1)在图中标出地球公转方向.(2)地球公转一周的周期为______.地球运行到D点附近时,北半球的季
