1.用O18(氧原子的同位素),标记的水(10%)和未标记的水(90%)参与光合作用,则光合作用产生的氧气中含有含放射性
 baikejia2022-10-04 11:39:542条回答
baikejia2022-10-04 11:39:542条回答2.不同的作物的顶端优势强弱程度差别很大,下列作物中,顶端优势最强的是
A.水稻 B.小麦 C.玉米 D.棉花
3.发菜是否是具有原核细胞的植物?
请高手答疑,并说明原因,

已提交,审核后显示!提交回复
共2条回复
 sue20 共回答了24个问题
sue20 共回答了24个问题 |采纳率91.7%- 含一个放射性氧原子氧气分子的比例是:0.1*0.9*2=0.18
含两个放射性原子的氧气分子的比例是:0.1*0.1=0.01
那么含有放射性原子的氧气占:0.18+0.01=0.19=19%
小麦水稻玉米的生长主要靠居间分生组织,而棉花靠的是茎尖,所以只有棉花有明显的顶端优势
发菜属于蓝藻门、念珠藻科植物.属于原核生物. - 1年前
 chaoyust 共回答了8个问题
chaoyust 共回答了8个问题 |采纳率- 1.10%2.c
3.不 - 1年前
相关推荐
- 画出一个氮原子和两个氧原子构成的二氧化氮分子模型?(请画出图形)谢谢啊!
 历史的碎片1年前1
历史的碎片1年前1 -
 chaojixiuxiu 共回答了17个问题
chaojixiuxiu 共回答了17个问题 |采纳率76.5%1年前查看全部
- 初二教的相对原子质量怎么求比如一个氢原子的质量为1.674×10负二十七次方 千克,一个氧原子的质量是2.657×10的
初二教的相对原子质量怎么求
比如一个氢原子的质量为1.674×10负二十七次方 千克,一个氧原子的质量是2.657×10的负二十六次方 千克, 当我们计算一个水分子的质量是多少时 中的 1.674×10负二十七次方和2.657×10的负二十六次方 这2个数是哪里来的 这里都不懂 求解
如一个氢原子的实际质量为1.674x10(-27)千克,(限于格式,10(-27)表示科学记数法,意为10的-27次幂,下同),一个氧原子的质量为2.657x10(-26)千克。一个碳-12原子的质量为1.993x10(-26)千克。 中的1.674x10(-27) 和2.657x10(-26) 这2个数是取哪里的 hblhkzt1年前1
hblhkzt1年前1 -
 瞬间的冬天 共回答了16个问题
瞬间的冬天 共回答了16个问题 |采纳率93.8%相对原子质量的求法:以碳6,12原子质量的1/12作为标准,其他原子的质量和该值相比较后得到的数值即为该原子的相对原子质量.1年前查看全部
- 由2个钠原子和3个氧原子1个硅原子组成的化学式有什么
 jlcqhh1年前2
jlcqhh1年前2 -
 苏黄 共回答了22个问题
苏黄 共回答了22个问题 |采纳率100%Na2SiO3
硅酸钠 一种弱酸强碱盐1年前查看全部
- 质量比为14:15的N2和NO混合,则混合气体中N2和NO的物质的量之比为______,氮原子和氧原子的个数比为____
质量比为14:15的N2和NO混合,则混合气体中N2和NO的物质的量之比为______,氮原子和氧原子的个数比为______,该混合气体的平均摩尔质量为______.
 zbwfff1年前1
zbwfff1年前1 -
 英_oo 共回答了17个问题
英_oo 共回答了17个问题 |采纳率94.1%解题思路:利用n=[m/M]计算物质的量及其比值,利用构成来计算原子个数比,利用总质量与总物质的量来计算混合气体的平均摩尔质量.由质量比为14:15的N2和NO混合,设混合气体中N2和NO的质量分别为28g、30g,则N2的物质的量为28g28g/mol=1mol,NO的物质的量为30g30g/mol=1mol,即混合气体中N2和NO的物质的量之比为1mol:1mol=1:1,氮原子和氧原子...
点评:
本题考点: 物质的量的相关计算.
考点点评: 本题考查物质的量的简单计算,巧设物质的质量可简化计算,并熟悉质量与物质的量的关系及常见物质的摩尔质量即可计算解答.1年前查看全部
- 关于氢键形成条件例如为什么甲酸甲酯不能和水形成氢键,上面不是有氧原子么?
 五月晓雨1年前4
五月晓雨1年前4 -
 wizardhyh 共回答了23个问题
wizardhyh 共回答了23个问题 |采纳率78.3%两个条件:一,必须同时存在氢原子和氟氧氮中的一种
二,氢原子和氟氧氮原子必须处在相邻的位置.
不论分子间或分子内皆是如此1年前查看全部
- SO2中“2”表示的意义如上,快氧原子还差不多
 我也蒙1年前2
我也蒙1年前2 -
 羊羽77 共回答了15个问题
羊羽77 共回答了15个问题 |采纳率86.7%一个氧化硫分子中含有两个氧原子1年前查看全部
- 为什么有氧呼吸时co2中的氧原子来自葡萄糖和水,产物H2O中的氧原子来自氧气?
 女人是被爱的1年前1
女人是被爱的1年前1 -
 天使般的美丽 共回答了15个问题
天使般的美丽 共回答了15个问题 |采纳率86.7%这个是通过同位素标记得出来的结论1年前查看全部
- 0.5mol胆矾的质量是125g,含有____个结晶水分子,____molCu2+离子,____mol氧原子.
 lianglight1年前3
lianglight1年前3 -
 a12_333 共回答了22个问题
a12_333 共回答了22个问题 |采纳率81.8%0.5mol胆矾的质量是125g,含有(2.5NA)个结晶水分子,(0.5)molCu2+离子,(4.5)mol氧原子.
注:NA为阿伏伽德罗常数1年前查看全部
- 下图是用来表示某物质发生化学变化的微观示意图,图中 和 分别表示氢原子和氧原子,反应条件是加热。
下图是用来表示某物质发生化学变化的微观示意图,图中  和
和  分别表示氢原子和氧原子,反应条件是加热。
分别表示氢原子和氧原子,反应条件是加热。
(1)A物质属于_____________________(填“混合物”、“单质”或“化合物”)。
(2)该反应所属基本类型为______________________。
(3)该反应的符号表达式为___________________________________。
(4)该反应前后没有发生变化的粒子是______________________。. tangjason20041年前1
tangjason20041年前1 -
 冰儿17 共回答了18个问题
冰儿17 共回答了18个问题 |采纳率94.4%1年前查看全部
- 如图是表示气体分子的示意图,图中“●”和“○”分别表示氢原子和氧原子,其中表示氧气的是( )
如图是表示气体分子的示意图,图中“●”和“○”分别表示氢原子和氧原子,其中表示氧气的是( )
A.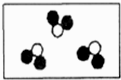
B.
C.
D.
 隆冬来临时1年前1
隆冬来临时1年前1 -
 kee315 共回答了19个问题
kee315 共回答了19个问题 |采纳率94.7%解题思路:氧气是由氧分子构成,每个氧分子是由两个氧原子构成的,根据气体分子的示意图,找出属于氧气的示意图.由于氧气是由氧分子构成,每个氧分子是由两个氧原子构成的,由图示可知,“○”表示氧原子,能表示氧气的是D.所以,D正确,A、B、C错误.
故选:D.点评:
本题考点: 微粒观点及模型图的应用;化学式的书写及意义.
考点点评: 通过给出微粒的模型,考查学生的观察能力和对基本概念的理解与运用能力;以检测考生从微观角度认识化学的意识和能力.1年前查看全部
- 49克H2SO4和H3PO4的混合物共有氧原子的数目是?
49克H2SO4和H3PO4的混合物共有氧原子的数目是?
以上为问题原题, zxcxzxc1年前2
zxcxzxc1年前2 -
 bestwilleng 共回答了23个问题
bestwilleng 共回答了23个问题 |采纳率91.3%H2SO4和H3PO4的相对分子质量相同 为98 它们中氧原子所占的比例也相同 为64:98 由49克得氧原子的质量为32克
而一个氧原子的质量为32*(约1.66×10-27kg) 所以氧原子的个数为32/(32*1.66×10-27)=6.024×10^261年前查看全部
- 下列说法中不正确的是( )A.1mol 氧气中含有12.04×1023个氧原子,在标准状况下占有体积22.4 LB.等
下列说法中不正确的是( )
A.1mol 氧气中含有12.04×1023个氧原子,在标准状况下占有体积22.4 L
B.等体积、浓度均为1mol/L的碳酸和盐酸,电离出的氢离子数之比为2:1
C.1mol臭氧和1.5mol氧气含有相同的氧原子数
D.等物质的量的干冰和葡萄糖(C6H12O6)中所含氧原子数之比为1:3 xujiguan1年前0
xujiguan1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 下图是用来表示某物质发生化学变化的微观示意图,图中 和 分别表示氢原子和氧原子,反应条件是加热。
下图是用来表示某物质发生化学变化的微观示意图,图中
 和
和 分别表示氢原子和氧原子,反应条件是加热。
分别表示氢原子和氧原子,反应条件是加热。
A B C
(1)A物质属于_____________________(填“混合物”、“单质”或“化合物”)。
(2)该反应所属基本类型为______________________。
(3)该反应的符号表达式为___________________________________。
(4)该反应前后没有发生变化的粒子是______________________。. kuks1年前1
kuks1年前1 -
 四oo非思 共回答了15个问题
四oo非思 共回答了15个问题 |采纳率86.7%1年前查看全部
- 科学化学式 在线等!用化学符号表示3个碘分子4个硫酸根离子4个氯化氢分子2个氧原子5个水分子2个镁离子1个氢分子2个铁离
科学化学式 在线等!
用化学符号表示
3个碘分子
4个硫酸根离子
4个氯化氢分子
2个氧原子
5个水分子
2个镁离子
1个氢分子
2个铁离子
m个碳酸氢根离子
带2个单位正电荷的铜离子
1个氢氧根离子
2个二氧化碳分子
写出下列符号中数字2的意义
H2
2H
2He
SO4 2-
2CO3
Ca2+
Mg+2O 刀若无锋1年前1
刀若无锋1年前1 -
 qinhyesung 共回答了16个问题
qinhyesung 共回答了16个问题 |采纳率87.5%3I2
4SO4(2-)
4HCl
2O
5H2O
2Mg(2+)
H2
Fe(3+)
mHCO3(-)
Cu(2+)
OH(-)
2CO2
一个氢气分子中含2个氢原子
2个氢原子
2个氦原子(或两个氦气分子,稀有气体是单原子分子)
每个硫酸根离子带有2个单位负电荷
2个碳酸根离子
一个钙离子带2个单位正电荷1年前查看全部
- 如图是某化学反应的微观模拟示意图,表示氢原子,表示氧原子.请你根据图示回答下列问题:
如图是某化学反应的微观模拟示意图,
 表示氢原子,
表示氢原子, 表示氧原子.请你根据图示回答下列问题:
表示氧原子.请你根据图示回答下列问题:
(1)甲、乙、丙三种物质中属于化合物的是______
(2)乙物质由______组成;丙物质由______构成
(3)用微粒的观点对质量守恒定律做出解释______. 这怎样那又怎样1年前1
这怎样那又怎样1年前1 -
 慧可家 共回答了13个问题
慧可家 共回答了13个问题 |采纳率100%解题思路:(1)由不同种原子构成的分子属于化合物分子;
(2)物质是由元素组成,粒子构成的,故根据物质的元素组成和分子构成填空;
(3)从微观角度解释质量守恒定律的关键是有关原子的种类、数目和质量都不变.(1)根据分子的构成,甲、乙、丙三种物质中属于化合物的是甲,因为它由两种元素组成;
(2)乙物质是氢气,由氢元素组成;丙物质是氧气,由氧分子构成;
(3)用微粒的观点解释质量守恒定律:化学反应前后,原子的种类、数目、质量不变.
故答案为:(1)甲;
(2)氢元素;氧分子;
(3)化学反应前后,原子的种类、数目、质量不变.点评:
本题考点: 微粒观点及模型图的应用;单质和化合物的判别;化学反应的实质.
考点点评: 根据变化微观示意图及粒子构成模拟图,根据分子由原子构成等特点,正确判断变化中的物质构成,是解答本题的基本方法.还需明确化学反应的实质是分子破裂为原子,原子重新组成新的分子,化学变化前后原子的种类、数目不变,分子的种类一定改变.1年前查看全部
- 1摩尔硫酸中含有___个氧原子,___克氧元素,____摩尔氢原子.
 等风的稻草人1年前3
等风的稻草人1年前3 -
 翩翩飞猪 共回答了21个问题
翩翩飞猪 共回答了21个问题 |采纳率81%1摩尔硫酸中,(1个H2SO4分子中含有4个氧原子)
含有__约2.408*10^24_个氧原子,
__16*4=64g_克氧元素,__2__摩尔氢原子.1年前查看全部
- 已知一个碳原子(含6个中子和6个质子)的质量是1.993×10-26 Kg,又知一个氧原子的质量为2.657×10-26
已知一个碳原子(含6个中子和6个质子)的质量是1.993×10-26 Kg,又知一个氧原子的质量为2.657×10-26 Kg,则氧原子的相对原子质量的计算表达式为是______.
 怎么生存1年前0
怎么生存1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 关于水的叙述正确的是( )A.水是由两个氢原子和一个氧原子构成的B.用明矾可以区别硬水和软水C.生活污水直接排放到大海
关于水的叙述正确的是( )
A.水是由两个氢原子和一个氧原子构成的
B.用明矾可以区别硬水和软水
C.生活污水直接排放到大海中不会造成水污染
D.生活中通过煮沸可降低水的硬度 何诈寐1年前1
何诈寐1年前1 -
 sikelaure 共回答了16个问题
sikelaure 共回答了16个问题 |采纳率87.5%解题思路:A、水的化学式是H2O,由此可看出水是由氢、氧两种元素组成的;
B、明矾可吸附水中杂质,达到净水目的;
C、生活污水的直接排放,是造成水体污染的重要原因之一;
D、降低水的硬度的方法为煮沸与蒸馏.A、水是由水分子构成的;故A说法不正确;
B、明矾可吸附水中杂质,达到净水目的,但不能区分硬水和软水,故B说法错误;
C、生活污水的直接排放,是造成水体污染的重要原因之一,所以生活污水直接排放到大海中会造成水污染,故C说法错误;
D、煮沸可以降低水的硬度,故D说法正确.
故选D.点评:
本题考点: 硬水与软水;水资源的污染与防治;分子、原子、离子、元素与物质之间的关系.
考点点评: 水是我们的宝贵资源,我们要了解水的特点,保护水资源不受污染.1年前查看全部
- 水是____化合物,水分子中的氢原子和氧原子之间以____形成分子.
 artzl5201年前2
artzl5201年前2 -
 helenahe 共回答了22个问题
helenahe 共回答了22个问题 |采纳率95.5%水是共价化合物,原子以共价键形成分子1年前查看全部
- 某芳香族化合物A含有C、H、O的质量分数分别为77.8%、7.4%、14.8%,该有机物一个分子中只含一个氧原子
某芳香族化合物A含有C、H、O的质量分数分别为77.8%、7.4%、14.8%,该有机物一个分子中只含一个氧原子
求该有机物分子式 知识人智1年前1
知识人智1年前1 -
 cect369 共回答了26个问题
cect369 共回答了26个问题 |采纳率84.6%一个氧原子.可知分子质量为:16÷14.8%=108
碳原子与氢原子质量为108-16=92
则有假设碳原子X个,氢原子Y个,可得下式;
92 = 12X + 1Y ; 解二元一次方程,有多个解,
因为是芳香化合物,即有机物碳原子与氢原子比例大概在1 :2
可带入具体数字解方程:如X=1、2、3、4、5、6、7.
综合上述信息得:
C7H8O1年前查看全部
- 氧化汞受热时的变化可用如图表示(图中大圆圈表示汞原子,小圆圈表示氧原子),据图得出的下列结论中,错误的是( )
氧化汞受热时的变化可用如图表示(图中大圆圈表示汞原子,小圆圈表示氧原子),据图得出的下列结论中,错误的是( )

A.氧化汞受热时能分解成汞和氧气
B.原子是化学变化中的最小粒子
C.分子在化学变化中可以再分
D.所有的物质都是由分子构成的 leeshangyin1年前1
leeshangyin1年前1 -
 simonluo009 共回答了17个问题
simonluo009 共回答了17个问题 |采纳率88.2%解题思路:根据氧化汞受热时的变化微观示意图,分析反应物、生成物,分析在化学反应中分子、原子的变化,分析构成物质的微粒有哪些等.由氧化汞受热时的变化微观示意图可知:A、氧化汞受热能分解成汞和氧气,故A说法正确;B、原子在化学反应中不能再分,原子是化学变化中的最小粒子,故B说法正确;C、加热氧化汞时,氧化汞分子分解成氧原子和汞原子,...
点评:
本题考点: 微粒观点及模型图的应用;化学反应的实质.
考点点评: 熟悉化学变化的实质,根据变化微观示意图及粒子构成模拟图,利用分子由原子构成等特点,正确判断变化中的物质构成,是解答本题的基本方法.1年前查看全部
- 2molO2约含有_个氧分子, _氧原子
2molO2约含有_个氧分子, _氧原子
要过程.快. asdse1101年前2
asdse1101年前2 -
 水中漫游 共回答了15个问题
水中漫游 共回答了15个问题 |采纳率86.7%2摩尔个氧分子,4摩尔个氧原子
因为1个氧气分子包含2个氧原子;2×2mol=4mol1年前查看全部
- 有关理论认为N 2 O与CO 2 分子具有相似的结构(包括电子式);已知N 2 O分子中氧原子只与一个氮原子相连,下列说
有关理论认为N 2 O与CO 2 分子具有相似的结构(包括电子式);已知N 2 O分子中氧原子只与一个氮原子相连,下列说法合理的是
A.N 2 O与SiO 2 为等电子体、具有相似的结构(包括电子式) B.N 2 O的电子式可表示 
C.N 2 O与CO 2 均不含非极性键 D.N 2 O为三角形分子  乱弹琴111年前1
乱弹琴111年前1 -
 不再仰望星空 共回答了16个问题
不再仰望星空 共回答了16个问题 |采纳率100%B
1年前查看全部
- 如何写HCN和O3的电子式回答哪两个元素间以多少个键相连.务必有分析过程.请问 为什么会形成碳氮三键。还有两个氧原子是以
如何写HCN和O3的电子式
回答哪两个元素间以多少个键相连.务必有分析过程.
请问 为什么会形成碳氮三键。
还有两个氧原子是以双键相连,两个以单键。请分析成因。
O3的结构式是书本上标准答案写的。 312621年前2
312621年前2 -
 Jadesleeve 共回答了22个问题
Jadesleeve 共回答了22个问题 |采纳率86.4%一楼说的对,正常啊,你到大学就知道了.
但是还是可以这样看的:
首先:一条共价键相当于2个电子共享,对每一方原子相当于多了个电子,对整个共价化合物相当于多了2个电子.
HCN:
H最外层有1个电子,达到稳定的2电子还要1条共价键,C最外层有4个电子,达到稳定的8电子要4条共价键,N最外层有5电子,达到稳定的8电子要3条共价键.所以必定是C与N形成碳氮三键和C-H.
O3:
O最外层有6个电子,所以共有6*3=18个,而每个O要达到8电子稳定状态,则一共要有8*3=24个电子,既要形成(24-18)/2=3 条共价键,所以就是你的答案了.
但实际是形成п键,是п(3,4)吧,不需要掌握.1年前查看全部
- 科学家最近发现2种粒子:一种是由四个中子构成的粒子,这种粒子称为“四中子”、另一种是由四个氧原子构成的分子(O 4 )。
科学家最近发现2种粒子:一种是由四个中子构成的粒子,这种粒子称为“四中子”、另一种是由四个氧原子构成的分子(O 4 )。下列有关这两种粒子的说法不正确的是
A.“四中子”不显电性 B.“四中子”的质量数为4 C.O 4 与O 2 互为同位素 D.O 4 与O 2 都具有氧化性  紫薄米1年前1
紫薄米1年前1 -
 wwwcom77 共回答了15个问题
wwwcom77 共回答了15个问题 |采纳率86.7%C
A、中子不带电;B、中子的质量数近似等于1;C、不正确,应为同素异形体;D、正确。1年前查看全部
- 1.A为淀粉,在一定条件下与水作用生成B.经实验知B分子中氢,氧原子数之比为2:1,氢原子数比碳原子数多10个,B的相对
1.A为淀粉,在一定条件下与水作用生成B.经实验知B分子中氢,氧原子数之比为2:1,氢原子数比碳原子数多10个,B的相对分子质量为342,B能溶于水并能发生银镜反应;B在一定条件下可水解生成C,C也能发生银镜反映,试回答B的名称,C的结构简式?
2.某天然油脂10g,需1.8gNaOH才能完全皂化,又知该油脂1000g催化加氢时消耗氢气12g,则该油脂1mol含碳碳双键几摩尔? maybach_bao1年前1
maybach_bao1年前1 -
 10001m 共回答了15个问题
10001m 共回答了15个问题 |采纳率93.3%1、B为麦芽糖,C为葡萄糖.
淀粉水解后生成麦芽糖,其分子式为C 12 H 22 O 11,麦芽糖可水解为葡萄糖,二者皆为还原糖,能发生银镜反应.
C的结构简式是CH2OH(CHOH)4CHO
2、
1.8g(40g/mol)=0.045mol,油脂和碱的反应比为1:3,则10g油脂的物质的量为0.015mol,1000g油脂对应则是1.5mol.它消耗了12g氢气,即6mol.1.5mol6mol=1molx.
x=4mol.
即1mol油脂需消耗4mol氢气,而每一个碳碳双键就需要一个氢分子加成,则1mol油脂中含碳碳双键4mol.1年前查看全部
- 0.3mol氧分子中含多少个氧分子,多少个氧原子
 becky_wen1年前2
becky_wen1年前2 -
 风岩残缺 共回答了11个问题
风岩残缺 共回答了11个问题 |采纳率100%1.806乘以10的23次方
3.612乘以10的23次方1年前查看全部
- N → n1.3.01×1023个CO2的物质的量是_____mol,_____mol碳原子,____mol氧原子.2.
N → n
1.3.01×1023个CO2的物质的量是_____mol,_____mol碳原子,____mol氧原子.
2.1.204×1024个H2O的物质的量是____ mol,____mol氢原子,____mol氧原子.
3.6.02 ´ 1023个氮分子相当於 mol,_________mol氮原子.
4.1.505 ´ 1023个Na2O含 mol Na+,mol O2–.
5.NA个C的物质的量是_________mol,_________mol质子,_______mol电子.
6.1.505 ´ 1023个SO4 2- 的物质的量是_________mol,_________mol质子,_______mol电子. guanbingjun1年前2
guanbingjun1年前2 -
 江上调玉琴 共回答了17个问题
江上调玉琴 共回答了17个问题 |采纳率88.2%1.3.01×1023个CO2的物质的量是0.5mol,0.5mol碳原子,1mol氧原子.
2.1.204×1.023个H2O的物质的量是2 mol,4mol氢原子,2mol氧原子.
3.6.02 ´ 1023个氮分子相当於1mol,2 mol氮原子.
4.1.505 ´ 1023个Na2O含3mol Na+,1.5 mol O2–.
5.NA个C的物质的量是NA/6.02X1023mol,6NAmol质子,6NAmol电子.
6.1.505 ´ 1023个SO4 2- 的物质的量是1.5mol,1.5x48mol质子,1.5x50mol电子.
第二题应该是掉了个小数点吧,已经不上去了.!1年前查看全部
- 常温常压下,氧气与臭氧的混合物16g中约含有6.02×1023个氧原子
常温常压下,氧气与臭氧的混合物16g中约含有6.02×1023个氧原子
为什么是对的 wersdfasdf1年前1
wersdfasdf1年前1 -
 流窜作案07 共回答了20个问题
流窜作案07 共回答了20个问题 |采纳率95%16克氧与臭氧都是由氧原子构成的,故可以看成是16克的氧原子,即1摩尔的氧原子,也即6.02*10^23个氧原子.1年前查看全部
- 1个水分子中氢原子和氧原子的质量比为_____拜托了各位
 darenxu1年前2
darenxu1年前2 -
 语粒子 共回答了18个问题
语粒子 共回答了18个问题 |采纳率83.3%1:81年前查看全部
- 三氧化硫和二氧化硫两物质的质量比为3:2,则两物质中硫元素的质量比,氧原子的个数比
 zcq100011年前2
zcq100011年前2 -
 niudawan 共回答了21个问题
niudawan 共回答了21个问题 |采纳率90.5%两物质中硫元素的质量比=3/80:2/64=6:5,所以两物质的物质的量比为6:5,
所以氧原子的个数比=6*3:5*2=9:51年前查看全部
- 物质的量1.0.2mol甲烷中,有____mol原子,共有几个原子.2.2mol酒精有____mol分子,氧原子的物质的
物质的量
1.0.2mol甲烷中,有____mol原子,共有几个原子.
2.2mol酒精有____mol分子,氧原子的物质的量为____mol,即____个,含氢原子____个,含碳原子____mol.
3.0.5mol乙烯分子中含有分子数____个.2mol乙烯中,有____个的乙烯分子,有____mol的碳原子和____个氢原子. governance1年前2
governance1年前2 -
 xiazf5988 共回答了21个问题
xiazf5988 共回答了21个问题 |采纳率95.2%1.
1mol;共有1NA=6.02×10^23个原子;
2.
2mol分子;氧原子2×2=4mol,即4NA=2.408×10^24个; 含氢原子2×4NA=4.816×10^24个,含碳原子2×2=4mol
3.
0.5×6NA=1.806×10^24个;
2NA=1.204×10^24个; 4mol的碳原子和8NA=4.816×10^24个氢原子1年前查看全部
- 过氧化氢是离子还是分子H2O2是如何构成的?是氢离子与过氧根离子?还是2个氢原子与两个氧原子有过氧根离子为什么不是离子呢
过氧化氢是离子还是分子
H2O2是如何构成的?是氢离子与过氧根离子?还是2个氢原子与两个氧原子
有过氧根离子为什么不是离子呢? Green_Leaves1年前1
Green_Leaves1年前1 -
 q8711917 共回答了16个问题
q8711917 共回答了16个问题 |采纳率81.3%是分子,连接顺序是,H-O-O-H
当然,它不是直线,而是像一本半打开的书,2个O在书的夹缝中,2个H,1个在前一页上,1个在后一页上
有过氧根离子,O2^2-,如过氧化钠Na2O2,过氧化钙CaO2,过氧化钡BaO2
但是这些物质都很不稳定,一遇到水,就立即反应了1年前查看全部
- 氧原子的电荷量是多少?
 wusuo_111a1年前2
wusuo_111a1年前2 -
 sdlh 共回答了18个问题
sdlh 共回答了18个问题 |采纳率88.9%氧原子不带电
氧离子带2个负电荷1年前查看全部
- amol硫酸中含有b个氧原子,则阿伏伽德罗常数可以表示为( )
amol硫酸中含有b个氧原子,则阿伏伽德罗常数可以表示为( )
A.a/4b B.b/4a C.a/b D.b/a lichuan88002201年前3
lichuan88002201年前3 -
 望天空空望天 共回答了20个问题
望天空空望天 共回答了20个问题 |采纳率80%又是你提问的啊
H2SO4里有B个氧原子
那么N=n*NA
那就是b/4a
选B1年前查看全部
- 光合作用产生的氧气中的氧原子是否全来自于水,如果是,那与化学式不符又该如何解释?
光合作用产生的氧气中的氧原子是否全来自于水,如果是,那与化学式不符又该如何解释?
一摩水中只有一摩氧原子,而根据化学式H2O+CO2→CH2O+O2却要两摩氧 蝶舞丛林1年前5
蝶舞丛林1年前5 -
 云中雾里飘 共回答了21个问题
云中雾里飘 共回答了21个问题 |采纳率95.2%实际反应为12H2O+6CO2=C6H12O6+6O2+6H2O,二氧化碳中的氧进入糖与水中,反应物水中的氧变成氧气.1年前查看全部
- CuO和SO2 NO2的区别答CuO中有一个氧原子,SO2 NO2中有两个氧原子对不对?注意是我说的对不对
 hxf__wu1年前1
hxf__wu1年前1 -
 youngtree 共回答了7个问题
youngtree 共回答了7个问题 |采纳率100%CuO和SO2 NO2的区别
答:CuO中有一个氧原子,SO2 NO2中有两个氧原子对不对?
这样答对于刚学化学的人还可以.
更准确的来说:
CuO是碱性氧化物,SO2 NO2两者都是酸性氧化物
或
CuO是金属氧化物,SO2 NO2是非金属氧化物1年前查看全部
- MgO的晶体结构与NaCl的晶体结构相似,Ni的堆积与MgO中氧原子堆积相同,Ni可以吸附H2,请以单个原子形式填入四面
MgO的晶体结构与NaCl的晶体结构相似,Ni的堆积与MgO中氧原子堆积相同,Ni可以吸附H2,请以单个原子形式填入四面体空隙,则Ni最大量吸收H2后,n(Ni):n(H)=( )
2,为什么? 风之舞者-20011年前2
风之舞者-20011年前2 -
 白果心情 共回答了14个问题
白果心情 共回答了14个问题 |采纳率100%Ni占据晶胞的顶点和面心,所以四面体空隙位于八个1/8晶胞的中心,一共为8个;而Ni显然为4个,所以是1:2.1年前查看全部
- H2O的相对分子质量= 1(氢原子的相对原子质量)×2(氢原子的个数)+16(氧原子的相对原子质量)=18
H2O的相对分子质量= 1(氢原子的相对原子质量)×2(氢原子的个数)+16(氧原子的相对原子质量)=18
表达时是用(氢原子)的相对原子质量还是(氢元素)相对原子质量,为什么?而且问一下这两种表达方式的区别 百合忧郁深蓝1年前1
百合忧郁深蓝1年前1 -
 dark_z 共回答了22个问题
dark_z 共回答了22个问题 |采纳率95.5%其实H2O中的原子的相对原子质量并不一定就是1和16,对于氢来说,它的同位素氘和氚的相对原子质量是2和3(氧也有同位素,比如氧18)
我们在计算中带入的1和16其实是指元素的平均相对质量,就是把所有的同位素考虑进去而算出来的一个平均值.
这个其实不必太深究的.1年前查看全部
- 90克水与多少克二氧化碳所含的氧原子的个数相等?
 sclsch1年前1
sclsch1年前1 -
 几千年前的脸 共回答了22个问题
几千年前的脸 共回答了22个问题 |采纳率86.4%45克1年前查看全部
- 1、都含有 1 mol 氧原子的Co、Co2、O3 三种气体的物质的量的比是多少?
1、都含有 1 mol 氧原子的Co、Co2、O3 三种气体的物质的量的比是多少?
2、 1 mol 氮气 含有 10 NA 个电子.为什么不对?
3、22.4L H2 和 O2 的混合气体 所含分子数为 NA .为什么不对,
4、实验室中需要配制 2mol/L 的 NaCl 溶液 950ml,配制时应选用的容量瓶的规格和称取得NaCl的质量分别是多少?
答案为100ml ,117g.
5、1.7 g NH3 所含电子数目 为 8NA .为什么错 枫茴露转1年前1
枫茴露转1年前1 -
 ifrom 共回答了16个问题
ifrom 共回答了16个问题 |采纳率93.8%1 因为CO中O为1,CO2中O为2,O3中O为3
所以CO为1,CO2为2分之1,O3为3分之1
通分之后为6:3:2
2 1mol氮气含有14NA电子,电子数=质子数=原子序数
3 没说是否为标况,所以不对
4 在实验室里,与950mL最接近的是1000mL,只能是配1000mL的然后再倒出5mL(之后的都不用算)
5 一个N中有7个电子,一个H中有1个电子,所以一个NH3分子中有10个电子
1.7g NH3为0.1mol
所以电子数为1mol1年前查看全部
- 1摩尔O2中含有多少个氧原子
 小猪驰米1年前5
小猪驰米1年前5 -
 kxingjik 共回答了17个问题
kxingjik 共回答了17个问题 |采纳率76.5%2mol,
1.204*10^24个1年前查看全部
- 是2O还是O2,2个氧原子如何表示?Ca(OH)2为什么要用括号?
 happyh11年前4
happyh11年前4 -
 tyxiaoqu 共回答了15个问题
tyxiaoqu 共回答了15个问题 |采纳率66.7%2个氧原子当然不能用02表示啦,O2表示的是氧气啊.
Ca(OH)2 在这里0H表示的是氢氧根离子.而氢氧根离子是-1价 钙离子是+2价,所以写成Ca(OH)21年前查看全部
- 以氧原子为例,说明构成原子的粒子有哪几种,它们是怎样构成原子的?为什么整个原子不显电性?
 薰衣的紫1年前3
薰衣的紫1年前3 -
 天堂即望 共回答了13个问题
天堂即望 共回答了13个问题 |采纳率84.6%解题思路:根据原子是由原子核和核外电子组成,原子核由质子和中子组成(质子带正电,中子不带电),相对原子质量=质子数+中子数;在原子中,质子数=核电荷数;进行分析解答本题根据原子的构成:原子是由原子核和核外电子组成,原子核由质子和中子组成(质子带正电,中子不带电).原子核带正电,电子带负电,两者的带电量相同,一正一负,所以整个原子显示的是电中性.
故答案为:
构成原子的粒子有质子、中子和电子;
氧原子有8个质子和8个中子构成原子核,8个电子在原子核外高速运动;
原子核中8个质子带8个单位的正电荷,8个电子带8个单位的负电荷,中子不带电,质子带的电量与核外电子带的电量相等,电性相反,因此整个原子不显电性.点评:
本题考点: 原子的定义与构成;原子的有关数量计算.
考点点评: 通过回答本题知道原子的构成,原子内各量所带电荷情况,整个原子不显电性的原因.1年前查看全部
- R元素的氧化物相对分子质量 142,其中氧原子相对原子质量和 80,R原子核16粒子不带电,儿核电荷数为15 求
R元素的氧化物相对分子质量 142,其中氧原子相对原子质量和 80,R原子核16粒子不带电,儿核电荷数为15 求
2.R元素化合价 babylady111年前3
babylady111年前3 -
 贫血的蚂蚁 共回答了19个问题
贫血的蚂蚁 共回答了19个问题 |采纳率94.7%P2O5
化合价为-3,+5 ,在P2O5中显示+5价1年前查看全部
- 写出下列各名称的符号 氮分子,三个氧原子,两个水分子,镁元素,磷原子,四氧化三铁,
写出下列各名称的符号 氮分子,三个氧原子,两个水分子,镁元素,磷原子,四氧化三铁,
写清楚啊 jollyjj1年前2
jollyjj1年前2 -
 flywinder2007 共回答了25个问题
flywinder2007 共回答了25个问题 |采纳率84%N2 3O 2H2O Mg P Fe3O41年前查看全部
- 题目出的很郁闷.关于水的组成,下列说法正确的是?A.水是由氢气和氧气组成B.水是由一个氧原子和二个氢原子构成的C.水是由
题目出的很郁闷.
关于水的组成,下列说法正确的是?
A.水是由氢气和氧气组成
B.水是由一个氧原子和二个氢原子构成的
C.水是由水分子构成的
D.水分子是由一个氧原子和二个氢原子构成的
题目错了还是我理解错了.请大家帮我分析下. hnbwsorgcn1年前2
hnbwsorgcn1年前2 -
 zwbook 共回答了13个问题
zwbook 共回答了13个问题 |采纳率92.3%A水由氢氧元素组成B水是宏观的 原子是微观的 不能混在一起 把水改为一个水分子 D一个水分子由一个氧原子和两个氢原子构成或者是水分子是由氢氧原子构成1年前查看全部
- 某物中碳、氢、氧元素质量比和某物中碳、氢、氧原子质量比题目意思一样吗
 yycj5311年前4
yycj5311年前4 -
 liyisheng2100 共回答了23个问题
liyisheng2100 共回答了23个问题 |采纳率91.3%作为计算意思一样 但前一种说法更准确 元素包括原子和离子1年前查看全部
- KO2中0价氧原子与-2价氧原子的个数比是多少
 fengsuiwuqi1年前1
fengsuiwuqi1年前1 -
 PKboy 共回答了13个问题
PKboy 共回答了13个问题 |采纳率100%设0价O的个数为x,-2价个数为y
个数守恒:x + y = 2
电荷数守恒:0 + 2y = 1
解得x = 1.5,y=0.5
所以个数比 = 3:11年前查看全部
大家在问
- 1(2012•南昌)已知,纸片⊙O的半径为2,如图1,沿弦AB折叠操作.
- 2小学二年级语文题目我的心里话-------老师,我想对您说:-------
- 3求高一物理受力分析图20个(附答案)!
- 4母亲,( )不要惊讶他无端入梦.填空
- 5函数f(x)=2sin(x-[π/3]),x∈[-π,0]的单调递增区间是( )
- 6梯形下底长是上底长的三分之二,把梯形分割成一个三角形和一个平行四边形,三角形面积占原梯形面积多少?
- 7y=x的平方乘以sin1\x求函数的导数
- 8一个长方体2的高减少2厘米,正好成一个正方体,表面积减少24平方厘米,原长方体的体积是多少立方厘米?
- 9Look at this photo.Han Mei is in her gaiden.It is
- 10also most europeans will open door for a woman or o___their
- 11关于烃的燃烧计算题怎么做?我遇到了2题选择题是关于烃的燃烧的,请懂的朋友教下我如何做.1,等物质的量的下列烃完全燃烧,消
- 12如何通过3轴加速度测量位移我这个3轴重力加速度,和它放的位置也有关系的
- 13(2013•如东县模拟)请结合图示实验装置,下列说法不正确的是( )
- 14用鬼,张牙舞爪,心惊胆战,恍然大悟 造句
- 15用500粒玉米种子做发芽试验,结果有485粒发芽,这批玉米种子的发芽率是( )%,如果要保证



