干燥管中常用的物质以及对应的用途 (如:碱石灰----吸收二氧化碳和水 ...)
 meimeikuai2022-10-04 11:39:542条回答
meimeikuai2022-10-04 11:39:542条回答我想知道“能”干燥哪些常见物质,而不是“不能”干燥哪些物质

已提交,审核后显示!提交回复
共2条回复
 笑傲江湖之高手 共回答了21个问题
笑傲江湖之高手 共回答了21个问题 |采纳率90.5%- 干燥剂主要有三类:
1、酸性:五氧化二磷、硅胶、浓硫酸(液态,一般放在洗气瓶中,不能放在干燥管中,不能干燥碱性气体、还原性气体硫化氢、碘化氢、溴化氢)
2、碱性:生石灰、碱石灰等
3、中性:无水氯化钙(不能干燥氨气,会反应)、无水硫酸铜(一般用其检验是否有水存在) - 1年前
 5npcb5h 共回答了4个问题
5npcb5h 共回答了4个问题 |采纳率- 无水硫酸铜,鉴定流出气体是否含有水;氯化钙,不能干燥氨气和乙醇;五氧化二磷,不能干燥碱性物质,我同学说这个好用。
- 1年前
相关推荐
- 某种塑料分解产物为某种烃;对这种烃进行以下实验:①取一定量的该烃,使其燃烧后气体通过干燥管
某种塑料分解产物为某种烃;对这种烃进行以下实验:①取一定量的该烃,使其燃烧后气体通过干燥管
干燥管增重7.2g;再通过石灰水石灰水增重17.6g
②经测定,该烃的密度是同种情况下氢气的14倍请回答:
(1)该烃的电子式为,该烃的名称是.
(2)0.1mol该烃能与多少克溴起加成反应;加成产物需多少mol溴蒸汽完全取代 888251年前1
888251年前1 -
 yang726 共回答了27个问题
yang726 共回答了27个问题 |采纳率85.2%首先,碳氢比为1比2,说明该塑料就是聚乙烯,该烃就是乙烯.分子式为C2H4,电子式我这边没法写.
该烃有一个双键,因此··0.1mol 能够跟0.1mol溴加成,加成产物需要0.2mol溴蒸汽取代1年前查看全部
- 氯化铵和氢氧化钙反应干燥管内可作用(碱石灰)做干燥剂碱石灰是由氢氧化钠和氧化钙组成的..那么其中的氢氧化钠不是会和氯化铵
氯化铵和氢氧化钙反应
干燥管内可作用(碱石灰)做干燥剂
碱石灰是由氢氧化钠和氧化钙组成的..
那么其中的氢氧化钠不是会和氯化铵反应..放出氨气的么..
为什么干燥剂选用碱石灰... jiangchuankyo1年前2
jiangchuankyo1年前2 -
 风盗铃 共回答了25个问题
风盗铃 共回答了25个问题 |采纳率92%干燥的是氨气,不是氯化铵,所以只能是氧化钙或氢氧化钠吸收氨气中的水,而不是氯化铵与氢氧化钠反应.1年前查看全部
- 固体干燥剂为什么是置于干燥管,而液体干燥剂置于洗气瓶
 44sonic1年前1
44sonic1年前1 -
 nerocc 共回答了15个问题
nerocc 共回答了15个问题 |采纳率86.7%固体干燥剂容易吸潮置于干燥管防止吸收外界潮气失效
液体干燥剂置于瓶中便于将干燥物质通过吸收需要干燥的物质1年前查看全部
- 为除去氯气中少量水蒸气,可使氯气通过一干燥管,管内应该是 A P2O5粉末 B浓硫酸 C碱石灰 D饱和食盐水
 南宫星辰1年前2
南宫星辰1年前2 -
 丁鹏123456 共回答了14个问题
丁鹏123456 共回答了14个问题 |采纳率85.7%参考一下
但是我觉得AB都对.1年前查看全部
- 小明用干燥管,烧杯,铜网等设计了一个在实验室中制取二氧化碳的装置
小明用干燥管,烧杯,铜网等设计了一个在实验室中制取二氧化碳的装置
请问如检验该装置气密性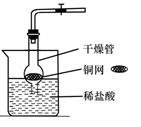
 zhangxiaorong1年前3
zhangxiaorong1年前3 -
 怯弱的勇敢 共回答了20个问题
怯弱的勇敢 共回答了20个问题 |采纳率90%把旋塞打开,把装置往下浸,再把塞子关紧了,把装置往上提,但不要脱离水面,看看干燥管内外的水是否在同一平面,是则漏气1年前查看全部
- 将下列A~D四组物质wg分别在O2中充分燃烧后,再通过装有足量Na2O2的干燥管,干燥管增重的质量大于wg的是
将下列A~D四组物质wg分别在O2中充分燃烧后,再通过装有足量Na2O2的干燥管,干燥管增重的质量大于wg的是
A .C4H8O2 B .C6H12O6
C.C2H4O3 D.H2和CO的混合气体
为什么我们老师说,有CO、H2,质量就不变啊? clover9771年前1
clover9771年前1 -
 隆盛耐材 共回答了14个问题
隆盛耐材 共回答了14个问题 |采纳率100%产物是CO2和H2O,它们都能与Na2O2反应的,变成NaOH、Na2CO3和O2,这儿O2在消耗又在生成,直接写总反应,忽略中间过程,
CO+Na2O2=Na2CO3 H2+Na2O2=2NaOH
你看是不是不变啊,全部被吸收,跟氧气没关系
质量是增加就是有一部分C是没有O与其配对的,它与氧气配对成CO,然后全部被吸收
就是说C的个数要比O的个数多的就能增加
不懂 追问1年前查看全部
- 为什么使用干燥管时气体从大口进入,从小口出来?
为什么使用干燥管时气体从大口进入,从小口出来?
化学老师没解释为什么、但是确实得有这么操作的原因吧.我很想了解.麻烦大家尽快回答.越快越好.
 枪响了1年前1
枪响了1年前1 -
 qqq022 共回答了16个问题
qqq022 共回答了16个问题 |采纳率93.8%同一压强下管径越大气体运动速度慢,使之接触的时间足够长,能够干燥的完全1年前查看全部
- 丙烷在空气中燃烧,产生的气体先经过浓硫酸的洗气瓶,洗气瓶增重3.6克,再经过碱石灰的干燥管
丙烷在空气中燃烧,产生的气体先经过浓硫酸的洗气瓶,洗气瓶增重3.6克,再经过碱石灰的干燥管
洗气瓶增重3.6克,再经过碱石灰的干燥管,干燥管增重2.2克,求反应掉氧气的质量为多少克?
我经过计算知道这个是不完全燃烧,所以我是这样做的
C3H8+4O2=2CO+CO2+4H2O
CO:0.1MOL CO2:0.05MOL H20:0.2MOL 这样做出来消耗氧气0.2mol,
但答案是0.4mol,我哪里错了? 绘雨1年前3
绘雨1年前3 -
 屗哈大乁 共回答了13个问题
屗哈大乁 共回答了13个问题 |采纳率100%你这条方程错了.3.6/18=0.2mol.H原子0.2mol,C3H8中c有0.075mol.2.2/44=0.05molCO2.1年前查看全部
- 某兴趣小组用干燥管、烧杯、铜网等设计装配了一个在实验室中制取二氧化碳气体的装置,如图所示.在干燥管内的铜网上应盛放___
某兴趣小组用干燥管、烧杯、铜网等设计装配了一个在实验室中制取二氧化碳气体的装置,如图所示.在干燥管内的铜网上应盛放______;若将铜网换成铁网,可能产生的后果是(用化学方程式表示)______.

 zihan86881年前1
zihan86881年前1 -
 jabo 共回答了23个问题
jabo 共回答了23个问题 |采纳率91.3%解题思路:实验室制取二氧化碳用大理石或石灰石和盐酸反应,铁是活泼金属可以和盐酸反应.在实验室中用大理石(或石灰石)和稀盐酸制取二氧化碳,不能将实验中的铜网换成铁网,是因为铁能够和稀盐酸反应生成氢气,制得的二氧化碳气体中混有氢气制得的CO2气体中混有H2
故答案为:大理石(或石灰石);Fe+2HCl═FeCl2+H2↑点评:
本题考点: 常用气体的发生装置和收集装置与选取方法;金属活动性顺序及其应用.
考点点评: 主要考查了实验室中制取二氧化碳的有关知识,从实验的创新加深了学生对二氧化碳制取装置的理解,培养学生分析问题、解决问题的能力.1年前查看全部
- 除氯气中的少量水蒸气除去氯气中混有的少量水蒸汽,可使含杂质的氯气通过某特定的干燥管,此干燥管中装有的药品是?A、P2O5
除氯气中的少量水蒸气
除去氯气中混有的少量水蒸汽,可使含杂质的氯气通过某特定的干燥管,此干燥管中装有的药品是?
A、P2O5粉末 B、浓硫酸 C、饱和食盐水 D、碱石灰
单选,请说明选什么,为什么其他三项不行,谢谢
如果不是干燥管,使用浓硫酸作干燥剂行吗 朕在搞1年前2
朕在搞1年前2 -
 远走低飞 共回答了19个问题
远走低飞 共回答了19个问题 |采纳率84.2%C 没用
D 吸收了氯气
B 没法放到干燥管里.人家是液体.
所以选A
楼上错了.
氯气和浓硫酸都是强氧化剂.他们不会发生氧化还原
不是干燥管 可以选浓硫酸1年前查看全部
- 把少量NO2气体通入过量小苏打溶液中,再使逸出的气体通过装有足量的过氧化钠颗粒的干燥管,最后收集到的气体是( )
把少量NO2气体通入过量小苏打溶液中,再使逸出的气体通过装有足量的过氧化钠颗粒的干燥管,最后收集到的气体是( )
A.氧气
B.二氧化氮
C.二氧化氮和氧气
D.二氧化氮和一氧化氮 64301331年前1
64301331年前1 -
 yjvzz 共回答了12个问题
yjvzz 共回答了12个问题 |采纳率91.7%解题思路:从反应的化学方程式分析,涉及的反应有:3NO2+H2O═2HNO3+NO,HNO3+NaHCO3═NaNO3+CO2↑+H2O,2Na2O2+2CO2═2Na2CO3+O2,2NO+O2═2NO2,设NO2为3mol,根据各步反应生成物的物质的量判断反应最终产物.设NO2为3mol,涉及的反应有:3NO2+H2O═2HNO3+NO,HNO3+NaHCO3═NaNO3+CO2↑+H2O,2Na2O2+2CO2═2Na2CO3+O2,2NO+O2═2NO2,则3molNO2生成2molHNO3和1molNO,通入小苏打后气体为2molCO2和1molNO,通入足量过氧化钠后生成1molO2和1molNO,1molO2和1molNO反应后生成1molNO2,剩余0.5molO2,故最后收集到的气体为1molNO2和0.5molO2,
故选C.点评:
本题考点: 氮的氧化物的性质及其对环境的影响;钠的重要化合物.
考点点评: 本题考查物质的性质,本题题目难度不大,解答本题的关键为根据反应的化学方程式计算各步反应的物质的物质的量,最后确定气体的组成.1年前查看全部
- 帮忙做一下这几道化学题第一题.某塑料的分解产物为泾,对这种泾进行一下实验 1,取一定量的它,使其燃烧后的气体通过干燥管,
帮忙做一下这几道化学题
第一题.某塑料的分解产物为泾,对这种泾进行一下实验 1,取一定量的它,使其燃烧后的气体通过干燥管,干燥管增重7.2g,再通过石灰水,石灰水增重17.6g.2、经测定泾的密度是相同状况下氢气密度的14倍.请回答(1)该泾的电子式是——,该泾的名称是——.(2)0.1mol该泾能与——g溴加成反应;加成产物需——mol溴蒸汽完全取代.(3)该塑料的结构简式是——,名称是——.
第二题.某烷泾A是汽油的主要成分之一,它是2,5二甲基-己烷.(1)取0.1mol的A与氯气发生取代反应,若只生成一氯代物和HCl,则生成的一氯代物最多有——种,生成的一氯代物在足量的氧气中完全燃烧生成二氧化碳、水、氯化氢,共消耗氧气——mol.(2)若A的稀泾有——种. ssoyren_ly1年前3
ssoyren_ly1年前3 -
 有权威的贵族 共回答了11个问题
有权威的贵族 共回答了11个问题 |采纳率90.9%1、m(H2O)=7.2g
H原子数=7.2/18*2=0.8mol
m(CO2)=17.6g
C原子数=17.6/44=0.4mol
C:H=0.4:0.8=1:2
烃的相对分子质量=2*14=28
所以是C2H4
该烃的电子式是 H:C::C:H
H H(C和下面的H还有一对共用电子对)
该烃的名称是 乙烯.
(2)0.1mol该烃能与 16g溴加成反应;加成产物需 0.2mol溴蒸汽完全取代.(3)该塑料的结构简式是 -[-CH2-CH2-]-n,名称是 聚乙烯.
2、
2,5二甲基-己烷:CH3-CH(CH3)-CH2-CH2-CH(CH3)-CH3
(1)取0.1mol的A与氯气发生取代反应,若只生成一氯代物和HCl,则生成的一氯代物最多有 3 种,生成的一氯代物在足量的氧气中完全燃烧生成二氧化碳、水、氯化氢,共消耗氧气 12 mol.(2)能生成A的稀烃有 3 种.1年前查看全部
- 如图所示是“H 2 流吹肥皂泡”实验装置图,请按下列要求回答各题: (1)在该实验中,球形干燥管里装的干燥剂的重要作用是
如图所示是“H 2 流吹肥皂泡”实验装置图,请按下列要求回答各题: 
(1)在该实验中,球形干燥管里装的干燥剂的重要作用是_______________。
(2)如上图把干燥管轻轻摆动,肥皂泡脱离管口,这时可以观察到_________,证明了H 2 的性质是____。
(3)肥皂泡遇火能发出“噗”的声音,肥皂泡破裂,产生火焰,说明H 2 有____性。 刻意放弃1年前1
刻意放弃1年前1 -
 huangqinyou 共回答了16个问题
huangqinyou 共回答了16个问题 |采纳率87.5%(1)干燥氢气
(2)肥皂泡慢慢上升;密度比空气小
(3)可燃1年前查看全部
- 为什么有些初中化学题里后面要连着两个碱石灰干燥管,作用分别是什么啊
为什么有些初中化学题里后面要连着两个碱石灰干燥管,作用分别是什么啊
尤其是后边那个 王正太我爱你1年前5
王正太我爱你1年前5 -
 我是ff顶帖 共回答了15个问题
我是ff顶帖 共回答了15个问题 |采纳率80%后面那个是防止空气中的水蒸气或者二氧化碳从末端管口进入第一个碱石灰干燥管被吸收,从而影响实验结果【这种实验往往是定量实验,第一个碱石灰干燥管用来吸收前面过来的水蒸气或者二氧化碳等的.】1年前查看全部
- 二氧化硫为什么不能通过盛有浓硫酸的U型干燥管
 奶油化梅1年前5
奶油化梅1年前5 -
 s021832 共回答了16个问题
s021832 共回答了16个问题 |采纳率87.5%会把浓硫酸从另一端压出U形管.
我说楼上二位不要胡扯,见到浓硫酸就想氧化是没前途的.1年前查看全部
- CO 2 是初中化学重点研究的气体之一。某化学兴趣小组设计了如下实验来探究CO 2 的制取和性质:该兴趣小组用干燥管、烧
CO 2 是初中化学重点研究的气体之一。某化学兴趣小组设计了如下实验来探究CO 2 的制取和性质:该兴趣小组用干燥管、烧杯、铜网等设计装配了一个在实验室中制取二氧化碳气体的装置,如下图所示。在干燥管内的铜网上应盛放_________;若将铜网换成铁网,可能产生的后果是_____________。 
 琦琦19801年前1
琦琦19801年前1 -
 白马kk 共回答了22个问题
白马kk 共回答了22个问题 |采纳率100%大理石(或石灰石);铁网被腐蚀,制得的CO 2 气体不纯1年前查看全部
- 化学试验图干燥管第一个装置,我看不懂!题目中说有干燥管!在哪里?是在烧杯里吗?在水里面吗?那个正方形的像木头桩一样的东西
化学试验图干燥管
第一个装置,我看不懂!题目中说有干燥管!在哪里?是在烧杯里吗?在水里面吗?
那个正方形的像木头桩一样的东西?

 redcolf_881年前1
redcolf_881年前1 -
 klgsy 共回答了21个问题
klgsy 共回答了21个问题 |采纳率76.2%干燥管应该就时那个东东吧
因为既然要干燥 肯定不希望有水么
一般干燥管都是和乘水的烧杯
连在一起的么~
一般不是用碱石灰么(固体) 液体就是浓硫酸
这个装置
可能是为了得到干净的气体
应该在水里
其实干燥管放水里又没什么~
一般 这种题 那个干燥的分不会很多
某班化代 、
PS.凹凸曼爱打小怪兽1年前查看全部
- 为了除去CO2气体中的SO2气体,下列对于仪器和药品组合中合理的是( )仪器:①洗气瓶 ②干燥管;药品 ③固态生石灰
为了除去CO2气体中的SO2气体,下列对于仪器和药品组合中合理的是( )仪器:①洗气瓶 ②干燥管;药品 ③固态生石灰 ④苏打溶液 ⑤小苏打溶液.
A. ①⑤
B. ②⑤
C. ①③
D. ①④ zhgary1年前1
zhgary1年前1 -
 198338 共回答了21个问题
198338 共回答了21个问题 |采纳率85.7%解题思路:气体除杂一般是利用洗气装置,导气管长进短出,所需要的试剂能把杂质转化为沉淀或提纯的物质,不引入新的杂质;洗气瓶与液态试剂对应,干燥管与固体试剂对应.小苏打是碳酸氢钠,苏打是碳酸钠;SO2既能与NaHCO3溶液反应,又能与Na2CO3溶液反应生成二氧化碳气体;CO2能与Na2CO3溶液反应,不能与NaHCO3溶液反应,所以可以利用饱和碳酸氢钠溶液除去二氧化硫;生石灰是固体在干燥管中用来干燥气体会除杂,但二氧化硫和二氧化碳气体都和生石灰反应.综上所述,除去CO2气体中的SO2气体,下列对于仪器和药品为①⑤
故选A.点评:
本题考点: 二氧化硫的化学性质.
考点点评: 本题考查了二氧化碳、二氧化硫气体的性质应用,同时考查了气体除杂的实验操作.1年前查看全部
- 铁与水蒸气反应干燥管中盛装的物质是什么,作用是什么,
铁与水蒸气反应干燥管中盛装的物质是什么,作用是什么,
碱石灰是什么 jeannezjw1年前0
jeannezjw1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 物理有关启普发生器的实验题最后的装置图是右面的那个,关上活塞,停止反应是因为球形干燥管里进行反应产生气体压强增大把液体压
物理有关启普发生器的实验题
最后的装置图是右面的那个,关上活塞,停止反应是因为球形干燥管里进行反应产生气体压强增大把液体压下去所以反应停止,对不,我不明白的是为什么打开活塞,液体会被大气压压到球形干燥管里,麻烦了,谢~~
 music19991年前1
music19991年前1 -
 爱摇15滚 共回答了14个问题
爱摇15滚 共回答了14个问题 |采纳率100%如果用图中最右边的实验装置来充当启普发生器,个人认为块状固体是放在球形干燥器里的,液体在烧杯里,且烧杯内液面要能够浸没球形干燥器内的固体颗粒,即活塞打开时反应就会进行.你所说的液体会被大气压“压”到球形干燥管里应该是相对于活塞关闭时的情况而言的.当活塞关闭时,干燥器内反应使内部页面下降,液体被排入烧杯;当活塞打开时,球形干燥器内与大气相同,内部压强为大气压,烧杯内液体表面也为大气压,两液面压强相同,又是连通器,因此烧杯内液体被大气压“压”到球形干燥器里,内外页面高度应该是大致相同的,反应继续进行.
很多年不学化学了,不知道这样解释你能不能懂,不懂再交流吧.1年前查看全部
- 干燥管除了干燥外还有什么作用,为什么?
 广西金鱼1年前1
广西金鱼1年前1 -
 等着嫁人 共回答了15个问题
等着嫁人 共回答了15个问题 |采纳率93.3%首先,要明确干燥管在整个装置中的位置以及里面所盛有的药品.
不论是在装置中间还是在装置的末端都可以吸水或者吸收某些气体杂质.比如:干燥管中盛有碱石灰,并至于装置的末端,当然是防止空气中的水蒸气进入,但如果在反应过程中有某些酸性气体存在,此时的干燥管也起到了尾气吸收的作用.
其次,干燥管还可以在简易启普发生器中使用,也可以在气体防倒吸的装置中起到与倒扣漏斗同样的作用.1年前查看全部
- 将含有C、H、O的有机物4.88g,装入元素分析装置,通入足量的O 2 使它完全燃烧,将生成的气体依次通过氯化钙干燥管A
将含有C、H、O的有机物4.88g,装入元素分析装置,通入足量的O 2 使它完全燃烧,将生成的气体依次通过氯化钙干燥管A和碱石灰干燥管B.测得A管质量增加了2.16g,B管增加了12.32g.已知该有机物的相对分子质量为122.
(1)通过计算确定该有机物的分子式.______
(2)如果该有机物1个分子中存在1个苯环和1个侧链,试写出它的所有同分异构体的结构简式.______. 664551年前0
664551年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 有一种无色混合气体,他可能由SO2、NH3.H2.H2S.NO.Cl2组成,若将混合气体通入盛P2O5的干燥管,体积无变
有一种无色混合气体,他可能由SO2、NH3.H2.H2S.NO.Cl2组成,若将混合气体通入盛P2O5的干燥管,体积无变化.再通入盛浓硫酸的洗气瓶.浓硫酸出现浑浊,剩余气体通过盛碱石灰的干燥管,气体体积减小,把最后残余的气体在空气中点燃,产生淡蓝色的火焰,若将盛原混合气体的容器打开,无明显现象,则混合气体中含有————————————
 whl12581年前1
whl12581年前1 -
 梦秋mabel 共回答了15个问题
梦秋mabel 共回答了15个问题 |采纳率100%无色混合说明没有黄绿色气体Cl2;通过酸性干燥物P2O5体积无变化,说明没有碱性气体NH3;通过浓硫酸浑浊,说明有H2S,浓硫酸把H2S氧化,生成了S沉淀进而浑浊;通过碱石灰气体体积减小,说明有酸性气体S02;点燃有淡蓝色火...1年前查看全部
- 某种塑料分解产物为烃,对这种烃进行以下实验:1、取一定量的该烃,使其燃烧后的气体通过干燥管,干燥管增重7.2g;再通过石
某种塑料分解产物为烃,对这种烃进行以下实验:1、取一定量的该烃,使其燃烧后的气体通过干燥管,干燥管增重7.2g;再通过石灰水,石灰水增重17.6.2、经测定,该烃(气体)的密度是相同状况下的氢气密度的14倍.
1、求该烃的电子式和该烃的名称
2、0.1mol该烃能与多少克溴起加成反应?加成产物需多少mol溴蒸汽完全取代? flyonthesnow1年前4
flyonthesnow1年前4 -
 iixcn 共回答了22个问题
iixcn 共回答了22个问题 |采纳率77.3%H2O 7.2g 0.4moL
CO2 17.6g 0.4mol
2*14=28
C2H4 乙烯
CH2=CH2 + Br2 ----CH2Br -CH2Br
1mol 160g 1
0.1mol X 0.1mol
列式解得 X= 16g
加成产物CH2Br -CH2Br0.1mol 含0.4mol氢原子,需要0.4molBr2 完全取代!1年前查看全部
- 把少量NO2通入过量的NaHCO3溶液中,再使逸出的气体通过装有足量氧化钠的干燥管,最后收集的气体是什么?
 jiduhuxi1年前1
jiduhuxi1年前1 -
 keaijing20 共回答了13个问题
keaijing20 共回答了13个问题 |采纳率100%NO一氧化氮1年前查看全部
- 将NO和CO2混合气体通过装有过氧化钠的干燥管后,出来的气体是红棕色,
将NO和CO2混合气体通过装有过氧化钠的干燥管后,出来的气体是红棕色,
将生成的气体全部通入盛满水倒立于水槽的试管,发现最后试管里仍然为一满试管液体.请问原气体中NO和CO2的体积比是多少?写出发生的化学方程式和解析过程. yotea1年前2
yotea1年前2 -
 李娜2089 共回答了19个问题
李娜2089 共回答了19个问题 |采纳率94.7%2CO2 + 2Na2O2 =2 Na2CO3 + O2
4NO +3 O2 + 2H2O = 4 HNO3
6:41年前查看全部
- 将ag水煤气充分燃烧,将燃烧生成的气体通过盛有过量的过氧化钠的干燥管,充分反应后干燥管增重bg,则a 跟b的关系如何?-
将ag水煤气充分燃烧,将燃烧生成的气体通过盛有过量的过氧化钠的干燥管,充分反应后干燥管增重bg,则a 跟b的关系如何?--大于\小于.
化学方程式麻烦打出来..! kks19841年前5
kks19841年前5 -
 illy1107 共回答了16个问题
illy1107 共回答了16个问题 |采纳率87.5%a=b
可以这样想:
2(CO)+(O2)=2(CO2)...*1
2(H2)+(O2)=2(H2O)...*2
由于:
2(Na2O2)+2(CO2)=2(Na2CO3)+(O2)...*3
2(Na2O2)+2(H20)=4(NaOH)+(O2)...*4
*1和*3可化简为:(Na2O2)+(CO)=(Na2CO3)
*2和*4可化简为:(Na2O2)+(H2)=2(NaOH)
就是把氧气约去
所以实际上水煤气首先燃烧消耗氧气
然后被过氧化钠吸收又放出氧气
氧气只是一个中间量
不影响吸收
所以原来有多少克水煤气
就吸收多少克.1年前查看全部
- (2006•揭阳二模)如图装置中,容器甲内充入0.1mol NO气体,干燥管内装有一定量Na2O2,从A处缓慢
 (2006•揭阳二模)如图装置中,容器甲内充入0.1mol NO气体,干燥管内装有一定量Na2O2,从A处缓慢通入CO2气体.恒温下,容器甲中活塞缓慢由D向左移动,当移至C处时容器体积缩小至最小,为原体积的[9/10],随着CO2的继续通入,活塞又逐渐向右移动.(不考虑活塞的摩擦)
(2006•揭阳二模)如图装置中,容器甲内充入0.1mol NO气体,干燥管内装有一定量Na2O2,从A处缓慢通入CO2气体.恒温下,容器甲中活塞缓慢由D向左移动,当移至C处时容器体积缩小至最小,为原体积的[9/10],随着CO2的继续通入,活塞又逐渐向右移动.(不考虑活塞的摩擦)
已知:2Na2O2+2CO2→2Na2CO3+O2
(1)已知当活塞移至C处时,干燥管中物质的质量增加了2.24g.
①此时,通入标准状况下的CO2气体多少L?
②容器甲中NO2转化为N2O4的转化率是多少?
③活塞移至C处后,继续通入a mol CO2,此时活塞恰好回至D处.则a值必______0.01(填大于、小于、等于),其理由是______.
(2)若改变干燥管中Na2O2的量,要通过调节甲容器的温度及通入的量CO2,使活塞发生从D到C,又从C到D的移动,则Na2O2的质量最小值应大于______g. gpjmds1年前1
gpjmds1年前1 -
 无心向月 共回答了15个问题
无心向月 共回答了15个问题 |采纳率93.3%解题思路:(1)①干燥管内质量增重,由于发生反应2Na2O2+2CO2=2Na2CO3+O2,利用差量法计算参加反应的二氧化碳的体积;
②容器甲中发生反应2NO+O2=2NO2,2NO2⇌N2O4,根据①计算生成氧气的体积,进而计算n(O2),根据过量计算,判断氧气与NO反应生成的二氧化氮的物质的量,此过程容器甲的体积不变,此后由于发生反应2NO2⇌N2O4,甲容器的体积减小,根据体积变化,判断混合气体物质的量减少量,根据差量法计算参加反应的二氧化氮的物质的量,再根据转化率定义计算;
③活塞移至C,体积不会再减少,则干燥管中Na2O2已反应完,活塞由C向D移动,体积扩大,2NO2⇌N2O4平衡左移,使二者物质的量增多,活塞移至D时,气体物质的量共增加0.01 mol,因此所需CO2必小于0.01 mol;
(2)实现从D→C的移动,只能通过降温使2NO2⇌N2O4的平衡向右移动(此反应为放热反应),气体物质的量减少量,根据差量法计算至少含有二氧化氮的物质的量,再根据关系式2Na2O2→O2→2NO→2NO2,计算过氧化钠的最少物质的量,再根据m=nM计算.(1)①设通入标准状况下CO2气体的体积为x,产生氧气的体积为y,则:
2Na2O2+2CO2=2Na2CO3+O2 质量装置△m
2×22.4 L22.4 L 56 g
x y 2.24 g
所以56 g:2.24g=2×22.4 L:x,解得x=1.792L,
56 g:2.24g=22.4 L:y,解得y=0.896L,
答:通入标准状况下的CO2气体1.792L.
②由①计算可知,生成氧气的物质的量n(O2)=[0.896L/22.4L/mol]=0.04mol,
2NO+O2=2NO2
2 1 2
0.08mol 0.04 mol0.08 mol
0.1 mol>0.08 mol,所以NO过量,生成NO2的物质的量为0.08 mol.
所以2NO2⇌N2O4物质的量减少△n
21 1
0.02 mol 0.1 mol×(1-[9/10])=0.01mol
所以NO2转化为N2O4的转化率为[0.02mol/0.08mol]×100%=25%,
答:NO2转化为N2O4的转化率为25%.
③活塞移至C,体积不会再减少,则干燥管中Na2O2已反应完,活塞由C向D移动,体积扩大,2NO2⇌N2O4平衡左移,使二者物质的量增多,活塞移至D时,气体物质的量共增加0.01 mol,因此所需CO2必小于0.01 mol,
故答案为:小于;活塞移至C,体积不会再减少,则干燥管中Na2O2已反应完,活塞由C向D移动,体积扩大,2NO2⇌N2O4平衡左移,使二者物质的量增多,活塞移至D时,气体物质的量共增加0.01 mol,因此所需CO2必小于0.01 mol;
(2)实现从D→C的移动,只能通过降温使2NO2⇌N2O4的平衡向右移动(此反应为放热反应).
即降温时 2NO2⇌N2O4物质的量减少△n
2 1 1
0.02 mol 0.1 mol×(1-[9/10])
即容器中至少应有0.02 mol的NO2,
根据转化关系式可知:2Na2O2→O2→2NO→2NO2,至少需要Na2O20.02 mol,所以其质量最小值为0.02 mol×78 g/mol=1.56 g.
故答案为:1.56g.点评:
本题考点: 有关范围讨论题的计算;化学方程式的有关计算;氮的氧化物的性质及其对环境的影响;钠的重要化合物.
考点点评: 考查NO、CO2和过氧化钠反应的有关计算与判断,试题综合性强,过程复杂,计算量很大,难度很大,为易错题目,该题是高考中的常见考点和题型,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和发散思维能力,侧重对学生能力的培养和解题方法的指导与训练.1年前查看全部
- 请教:干燥管连接在装置末端时为什么也是大口进,小口出.我觉得反过来也可以啊?
请教:干燥管连接在装置末端时为什么也是大口进,小口出.我觉得反过来也可以啊?
因为在末端时,它的作用不就是为了防止空气中的水分和二氧化碳进入反应容器吗. johnwang8112081年前2
johnwang8112081年前2 -
 西瓜女王 共回答了18个问题
西瓜女王 共回答了18个问题 |采纳率94.4%为了充分干燥,大口进小口处是的气体在干燥管内的时间较长,干燥也就更好.小口也使得空气中的液体不易进入1年前查看全部
- 有甲酸甲酯、丙酸、乙酸乙酯的混合物7.4g,将混合物完全燃烧后所得气体通过碱石灰干燥管,充分吸收后干燥管增重18.6g,
有甲酸甲酯、丙酸、乙酸乙酯的混合物7.4g,将混合物完全燃烧后所得气体通过碱石灰干燥管,充分吸收后干燥管增重18.6g,则混合物的平均相对分子质量为( )
A. 69
B. 74
C. 77
D. 82 zzdgwy1年前1
zzdgwy1年前1 -
 zx3465275 共回答了20个问题
zx3465275 共回答了20个问题 |采纳率80%解题思路:甲酸甲酯、丙酸、乙酸乙酯的分子式分别为C2H4O2、C3H6O2、C4H8O2,分子中C原子与H原子数目之比为1:2,则混合物中C原子与H原子数目之比为1:2,氧原子数目都相等,则平均分子组成为CnH2nO2.故生成二氧化碳与水的物质的量之比为1:1,令二者物质的量为xmol,干燥管增重为燃烧生成的二氧化碳与水的质量,据此计算二氧化碳与水的物质的量,再根据碳原子守恒计算平均分子组成中n的值,进而计算平均相对分子质量.甲酸甲酯、丙酸、乙酸乙酯的分子式分别为C2H4O2、C3H6O2、C4H8O2,分子中C原子与H原子数目之比为1:2,则混合物中C原子与H原子数目之比为1:2,氧原子数目都相等,则平均分子组成为CnH2nO2.故生成二氧化碳与水的物质的量之比为1:1,令二者物质的量为xmol,干燥管增重为燃烧生成的二氧化碳与水的质量,则:
44x+18x=18.6,解得x=0.3mol,
根据碳原子守恒,则[7.4/14n+32]×n=0.3,解得n=3,
故平均分子组成为C3H6O2,故平均相对分子质量为12×3+6+32=74,
故选B.点评:
本题考点: 有关有机物分子式确定的计算.
考点点评: 本题考查混合物的有关计算,难度中等,确定混合物中碳原子与氢原子数目之比为定比1:2是关键,注意利用平均组成进行解答.1年前查看全部
- 高中化学,此题中,为什么打开弹簧夹,干燥管中加碱石灰,再通入二氧化氮,充满二氧化氮,就可以排尽空气?
 yanpeng36691年前1
yanpeng36691年前1 -
 海之-2000 共回答了23个问题
海之-2000 共回答了23个问题 |采纳率82.6%二氧化氮把里面的空气“挤”出来了,所以先通入二氧化氮,过一会儿在加热1年前查看全部
- 为什么HCl溶于水会倒吸,为什么用肚容式(倒扣漏斗和球形干燥管)可以防止
为什么HCl溶于水会倒吸,为什么用肚容式(倒扣漏斗和球形干燥管)可以防止
鉴于度娘无满意答案要吞金所以我选择好以后再付 A200127821年前1
A200127821年前1 -
 柳承峻 共回答了21个问题
柳承峻 共回答了21个问题 |采纳率95.2%因为HCl在水中的溶解度十分大,所以溶解十分迅速.气体一旦接触水就会溶解,十分迅速会导致接触面以上一段导管内气体压强急剧减小,外界大气压相对的就很大,把水往导管里压.1年前查看全部
- 把少量NO2气体通入过量小苏打溶液中,再使逸出的气体通过装有足量的过氧化钠颗粒的干燥管,最后收集到的气体是( )
把少量NO2气体通入过量小苏打溶液中,再使逸出的气体通过装有足量的过氧化钠颗粒的干燥管,最后收集到的气体是( )
A. 氧气
B. 二氧化氮
C. 二氧化氮和氧气
D. 二氧化氮和一氧化氮 huachengfeng1年前1
huachengfeng1年前1 -
 yan_yuan 共回答了19个问题
yan_yuan 共回答了19个问题 |采纳率89.5%解题思路:从反应的化学方程式分析,涉及的反应有:3NO2+H2O═2HNO3+NO,HNO3+NaHCO3═NaNO3+CO2↑+H2O,2Na2O2+2CO2═2Na2CO3+O2,2NO+O2═2NO2,设NO2为3mol,根据各步反应生成物的物质的量判断反应最终产物.设NO2为3mol,涉及的反应有:3NO2+H2O═2HNO3+NO,HNO3+NaHCO3═NaNO3+CO2↑+H2O,2Na2O2+2CO2═2Na2CO3+O2,2NO+O2═2NO2,则3molNO2生成2molHNO3和1molNO,通入小苏打后气体为2molCO2和1molNO,通入足量过氧化钠后生成1molO2和1molNO,1molO2和1molNO反应后生成1molNO2,剩余0.5molO2,故最后收集到的气体为1molNO2和0.5molO2,
故选C.点评:
本题考点: 氮的氧化物的性质及其对环境的影响;钠的重要化合物.
考点点评: 本题考查物质的性质,本题题目难度不大,解答本题的关键为根据反应的化学方程式计算各步反应的物质的物质的量,最后确定气体的组成.1年前查看全部
- 如图所示,在三支干燥管内盛放的都是固体试剂,a为块状白色固体,是制玻璃的主要原料之一B中为淡黄色粉末
如图所示,在三支干燥管内盛放的都是固体试剂,a为块状白色固体,是制玻璃的主要原料之一B中为淡黄色粉末
C中为白色颗粒状固体b为具有刺激性气味的强酸溶液,b与a,B中的试剂都能反应,但不与C中试剂反应,以上都为常见试剂写出A中化学反应的方程式(因为手机功能有限所以不好画图,) 摘掉眼镜当mm1年前2
摘掉眼镜当mm1年前2 -
 qiyue_123 共回答了18个问题
qiyue_123 共回答了18个问题 |采纳率88.9%无图,这的很难判断,我只能告诉你一些可能的 b:HCl a:为CaCO3或Na2CO3 B:Na2O2或S1年前查看全部
- 把少量NO2气体通入过量小苏打溶液中,再使逸出的气体通过装有足量的过氧化钠颗粒的干燥管,最后收集到的气体是( )
把少量NO2气体通入过量小苏打溶液中,再使逸出的气体通过装有足量的过氧化钠颗粒的干燥管,最后收集到的气体是( )
A. O2
B. NO2
C. NO2和O2
D. NO2和NO od5w0daa1年前1
od5w0daa1年前1 -
 ldw123123123 共回答了8个问题
ldw123123123 共回答了8个问题 |采纳率87.5%解题思路:从反应的化学方程式分析,涉及的反应有:3NO2+H2O═2HNO3+NO,HNO3+NaHCO3═NaNO3+CO2↑+H2O,
2Na2O2+2CO2═2Na2CO3+O2,2NO+O2═2NO2,设NO2为3mol,根据各步反应生成物的物质的量判断反应最终产物.设NO2为3mol,涉及的反应有:3NO2+H2O═2HNO3+NO,HNO3+NaHCO3═NaNO3+CO2↑+H2O,
2Na2O2+2CO2═2Na2CO3+O2,2NO+O2═2NO2,则3molNO2生成2molHNO3和1molNO,
通入小苏打后气体为2molCO2和1molNO,通入足量过氧化钠后生成1molO2和1molNO,
1molO2和1molNO反应后生成1molNO2,剩余0.5molO2,故最后收集到的气体为1molNO2和0.5molO2,
故选C.点评:
本题考点: 氮的氧化物的性质及其对环境的影响.
考点点评: 本题考查物质的性质,本题题目难度不大,解答本题的关键为根据反应的化学方程式计算各步反应的物质的物质的量,最后确定气体的组成.1年前查看全部
- 将含有C.H、O的有机物3.24 g,装入元素分析装置,通入足量的O2使它完全燃烧,将生成的气体依次通过氯化钙干燥管A和
将含有C.H、O的有机物3.24 g,装入元素分析装置,通入足量的O2使它完全燃烧,将生成的气体依次通过氯化钙干燥管A和碱石灰干燥管B.测得A管质量增加了2.16g,B管增加了9.24g.已知该有机物的相对分子质量为108.⑴燃烧此化合物3.24g,须消耗氧气的质量是多少?⑵求此化合物的分子式?⑶该化合物1分子中存在1个苯环和1个羟基,试写出它的同分异构体的结构简式.
 lxjlxjlxj1年前1
lxjlxjlxj1年前1 -
 may80522 共回答了26个问题
may80522 共回答了26个问题 |采纳率96.2%3.24 g就是0.03mol,A中吸收的是水,质量增加了2.16g,说明水的质量是2.16g,可以算出水的物质的量为0.12mol,B管增加了9.24g,说明CO2是9.24g,CO2的物质的量为0.21mol,再由有机物是0.03mol,可知,在1mo该有机物含有7molC,8molH,再根据分子量为108可知,还有1个O
所以分子式为C7H8O,这样3个问题的答案就知道了
(1)8.16(3)3种,分别是邻甲基苯酚、间邻甲基苯酚、对邻甲基苯酚
第一问你在算算,我算的数不一定对,其他的问肯定没问题1年前查看全部
- 将10克CO2和CO混合气体,通过装有足量过氧化钠的干燥管.
将10克CO2和CO混合气体,通过装有足量过氧化钠的干燥管.
反应后干燥管的总质量增加了5.6克,则原混合气体中二氧化碳的质量分数是? jason_inve1年前1
jason_inve1年前1 -
 80zz 共回答了25个问题
80zz 共回答了25个问题 |采纳率88%CO和Na2O3不反应,CO2和Na2O2发生如下反应:
2Na2O2+2CO2=2Na2CO3+O2
.88..32
由此可见每反应88克CO2,会生成32克O2,即固体增加质量为88-32=56克
因为反应后干燥管的总质量增加了2.8克,
所以反应的CO2质量为2.8×88÷56=4.4克
所以原混合气体中CO2的质量分数为4.4÷10=44%
其实过氧化钠与CO2的反应时放热的,那么在此条件下CO会不会与生成的O2反应呢,不用考虑该反应,因为反应放出的热不足以使CO和O2反应.
如果不懂可以再问,祝您学习进步!1年前查看全部
- 为证明铜与稀硝酸反应生成一氧化氮,某校学生实验组设计了一个实验,b为一个用金属丝固定的干燥管,内装块
 bonbonbon1年前1
bonbonbon1年前1 -
 冯小末 共回答了18个问题
冯小末 共回答了18个问题 |采纳率94.4%:(1)用碳酸钙与稀硝酸反应产生的二氧化碳气体赶走装置内的空气
(3)CO2比空气重,从长管进入E,并没有把E中空气赶尽,致使部分NO先与未赶尽的空气生成少量红棕色NO2,当再从F鼓入空气时,E中有更多NO2生成,所以红棕色加深
(4)二氧化氮与水反应有硝酸生成,硝酸与碳酸钙反应使沉淀溶解
(5)吸收NO、NO2、CO2尾气,防止污染大气1年前查看全部
- 将碳酸氢铵在试管中加热,使放出的气体依次通过盛有足量浓硫酸的洗气瓶和碱石灰的干燥管,最后得到的气体有
将碳酸氢铵在试管中加热,使放出的气体依次通过盛有足量浓硫酸的洗气瓶和碱石灰的干燥管,最后得到的气体有
A氨气 B水 C二氧化碳 D无气体
求解释为什么是D _ey_t5b0afe16_b31年前4
_ey_t5b0afe16_b31年前4 -
 abc398698 共回答了25个问题
abc398698 共回答了25个问题 |采纳率84%碳酸氢铵受热分解得水蒸气、二氧化碳、氨气,浓硫酸吸水,中和氨,碱石灰吸二氧化碳,都被吸了~1年前查看全部
- 在试管前口通入C0到试管中与铁触媒反应,试管后口装置一个含碱石灰的干燥管B,称取 15.2g 铁触媒进行上述实验.充分反
在试管前口通入C0到试管中与铁触媒反应,试管后口装置一个含碱石灰的干燥管B,称取 15.2g 铁触媒进行上述实验.充分反应后,测得“干燥管 B”增重 11.0g,则该铁触媒的化学式可表示为 .(Fe405或2Fe0.Fe203)是怎样计算来的
 心火为你而起1年前5
心火为你而起1年前5 -
 nwutony 共回答了17个问题
nwutony 共回答了17个问题 |采纳率82.4%增重的是二氧化碳,二氧化碳的氧的质量:11×32/44=8g,但只有一个氧来自铁触媒,还有一个氧来自一氧化碳.
所以铁触媒中氧:8g/2=4g
铁元素:15.2-4=11.2
所以Fe:O=11.2:4=14:5
Fe405中Fe:O=(56*4):(16*5)=14:5
所以是Fe4051年前查看全部
- 若用干燥管除去氯气中的水蒸气,可以使用的试剂是
 土阿土1年前1
土阿土1年前1 -
 lj68817885 共回答了16个问题
lj68817885 共回答了16个问题 |采纳率81.3%浓硫酸1年前查看全部
- 0.1mol某有机物在0.3molO2中全部燃烧后,生成CO CO2和水蒸气 通入盛有cacl2的干燥管,发现干燥管增重
0.1mol某有机物在0.3molO2中全部燃烧后,生成CO CO2和水蒸气 通入盛有cacl2的干燥管,发现干燥管增重7.2g,剩余气体再通过灼热的cuo,使其减轻1.6g,到处的气体与足量Na2O2反应,产生的气体在标准状况下体积为3.36L求有机物燃烧后生成CO的物质的量!
以及该有机物的分子式. 烟色Y1年前2
烟色Y1年前2 -
 nn2188 共回答了28个问题
nn2188 共回答了28个问题 |采纳率92.9%CO:0.1mol ,有机物为C3H8
设有机物分子式为CxHyOz,
(1)通入盛有CaCl2的干燥管,吸收的是水蒸气,干燥管增重7.2g,说明水蒸气质量为7.2g,则水的物质的量为7.2/18=0.4mol,由于水中的氢全部来自有机物,所以0.1mol有机物中含氢0.4*2=0.8mol,可得y=8.
(2)通过灼热的CuO,发生的反应是CO+CuO=Cu+CO2,减轻的1.6g实际就是反应的CuO中氧元素质量,所以反应的CuO的量为1.6/16=0.1mol,即参与反应的CO的量也是0.1mol,同时产生0.1molCO2.
(3)与Na2O2反应的是CO2,反应式为2Na2O2+2CO2=Na2CO3+O2,产生的气体即氧气在标准状况下体积为3.36L,可得O2的量为3.36/22.4=0.15,则CO2的量为2*0.15=0.3mol,这里CO2包括两部分,一部分来自有机物燃烧生成,还有0.1mol由CO转化而来,所以有机物燃烧生成的CO2为0.3-0.1=0.2mol.碳原子来自有机物,所以有机物中碳原子个数为3(由0.3:0.1得),即x=3.
(4)由上,产物中氧原子(CO、CO2、H2O)数目为0.1+2*0.2+0.1=0.6,这些氧可能来自两部分,一是有机物本身,一是氧气,而所使用的氧气中的氧原子刚好为0.3*2=0.6,因为产物中含有CO,所以O2没有剩余,由此可知有机物中不含氧,即z=0,所以有机物分子式为C3H8.1年前查看全部
- 实验室制取氨气的实验中为何没看到用干燥管干燥
 血见山东1年前2
血见山东1年前2 -
 yangguang1972 共回答了16个问题
yangguang1972 共回答了16个问题 |采纳率93.8%可以用盛碱石灰的干燥管干燥.不少制法装置中不出现干燥装置.探究时再出现 .
如制氧气,氢气等1年前查看全部
- 制溴苯时的几个问题1.制溴苯时,干燥管中的碱石灰的作用是?2.反应过程中,(1)锥形瓶的上方的导管为什么不插入液面下?(
制溴苯时的几个问题
1.制溴苯时,干燥管中的碱石灰的作用是?
2.反应过程中,(1)锥形瓶的上方的导管为什么不插入液面下?(2)在导管的末端能看到什么实验现象?这是由于反应生成的(3)遇锥形瓶中的(4)而形成(5)的小液滴. 刺鱼鱼刺1年前1
刺鱼鱼刺1年前1 -
 清茶中的泪 共回答了15个问题
清茶中的泪 共回答了15个问题 |采纳率93.3%碱石灰是用于吸收溴化氢气体
导管不插入液面下是为了防倒吸
导管的末端出现小液滴是溴化氢凝结成的1年前查看全部
- 在标准状况下,将NO2和氧气按体积之比3:2混合后充入一支干燥管中,将试管倒立于水中,充分反应后试管中溶液的物质量浓度是
在标准状况下,将NO2和氧气按体积之比3:2混合后充入一支干燥管中,将试管倒立于水中,充分反应后试管中溶液的物质量浓度是多少?求过程!谢谢啦!
 布什绞qqff1年前1
布什绞qqff1年前1 -
 jgj小巧玲珑 共回答了15个问题
jgj小巧玲珑 共回答了15个问题 |采纳率86.7%3NO2 + H2O = 2HNO3 + NO.(1)
2NO + O2 = NO2.(2)
(1)x2+(2)x1:4NO2 + O2 + 2H2O = 4HNO3
4 1 4
3体积 2体积 3体积
2/3 > 1/4,说明氧气过量,应以NO2的量计算生成物HNO3的量.
设试管的容积为V,V(NO2) = V x 3/5 n(NO2) = V/Vm x 3/5 = n(HNO3)
剩余氧气体积:V x ( 2 - 3/4)/5 = V/4 V[HNO3(aq)] = V x3/4
c(HNO3) = n(HNO3)/V[HNO3(aq)] =(V/Vm x 3/5)/(V x 3/4) = 4/(5 x 22.4L/mol) = 0.036 mol/L1年前查看全部
- 用干燥管在常温下制备空气中的某种成分
用干燥管在常温下制备空气中的某种成分
用干燥***取空气的一种成分 通入的气体是什么?干燥管里装的固体是什么?方程式是什么? sherry辛兕1年前1
sherry辛兕1年前1 -
 1370 共回答了18个问题
1370 共回答了18个问题 |采纳率83.3%通入的气体CO2 干燥管里装的固体Na2O2 方程式CO2+Na2O2==O21年前查看全部
- 除去氢气中的盐酸和水的方法可不可以用通过盛有足量生石灰和烧碱混合固体的干燥管的方法?
 maoyuxiang1年前1
maoyuxiang1年前1 -
 咚咚123 共回答了24个问题
咚咚123 共回答了24个问题 |采纳率95.8%可以!
NaOH + HCl = NaCl + H2O
NaOH、CaO都具有吸水性.
生石灰和烧碱混合固体,俗称碱石灰.1年前查看全部
- 二氧化碳和氧气的混合气体多次通过盛有过氧化钠的干燥管后,体积减小到原来的4/5(条件相同时测定)则原混合气体中二氧化碳和
二氧化碳和氧气的混合气体多次通过盛有过氧化钠的干燥管后,体积减小到原来的4/5(条件相同时测定)则原混合气体中二氧化碳和氧气的体积比为
A.4:1
B.3:2
C.1:1
D.2:3
....谢谢`````````````` yifanlxk121年前3
yifanlxk121年前3 -
 库西 共回答了21个问题
库西 共回答了21个问题 |采纳率90.5%答案:V1:V2=2:3
设CO2的体积V1,O2的体积V2
根据一楼的方程式可知
2CO2—O2
即2倍CO2生成1倍O2
CO2完全与Na2O2反应生成O2
生成O2体积1/2V1
V2+1/2V1=4/5(V1+V2)
所以V1:V2=2:31年前查看全部
- 把少量NO2气体通入过量小苏打溶液中,再使逸出的气体通过装有足量的过氧化钠颗粒的干燥管,最后收集到的气体是( )
把少量NO2气体通入过量小苏打溶液中,再使逸出的气体通过装有足量的过氧化钠颗粒的干燥管,最后收集到的气体是( )
A. 氧气
B. 二氧化氮
C. 二氧化氮和氧气
D. 二氧化氮和一氧化氮 爱上老虎的猫11年前1
爱上老虎的猫11年前1 -
 铁-剑 共回答了13个问题
铁-剑 共回答了13个问题 |采纳率100%解题思路:从反应的化学方程式分析,涉及的反应有:3NO2+H2O═2HNO3+NO,HNO3+NaHCO3═NaNO3+CO2↑+H2O,2Na2O2+2CO2═2Na2CO3+O2,2NO+O2═2NO2,设NO2为3mol,根据各步反应生成物的物质的量判断反应最终产物.设NO2为3mol,涉及的反应有:3NO2+H2O═2HNO3+NO,HNO3+NaHCO3═NaNO3+CO2↑+H2O,2Na2O2+2CO2═2Na2CO3+O2,2NO+O2═2NO2,则3molNO2生成2molHNO3和1molNO,通入小苏打后气体为2molCO2和1molNO,通入足量过氧化钠后生成1molO2和1molNO,1molO2和1molNO反应后生成1molNO2,剩余0.5molO2,故最后收集到的气体为1molNO2和0.5molO2,
故选C.点评:
本题考点: 氮的氧化物的性质及其对环境的影响;钠的重要化合物.
考点点评: 本题考查物质的性质,本题题目难度不大,解答本题的关键为根据反应的化学方程式计算各步反应的物质的物质的量,最后确定气体的组成.1年前查看全部
大家在问
- 1在平面直角坐标系中,已知圆心在第二象限,半径为2庚号2的圆与直线Y=X相切于坐标原点O.求圆C的方程
- 2在一次才艺表演中,有50名选手参赛,结果26人获奖,获二等奖与获一等奖的人数比是4:1,获一等奖的人数是获三等奖人数的[
- 3七巧板中的图形包含的小于180度的角有只写具体角度
- 4甲醇,丙醛,甲醛,苯酚谁不能和纳反应
- 5兴趣和通顺的近义词是什么?
- 6()经()通,要近义词
- 7化简:3x根号8-5x根号32
- 8水沸腾的条件是什么?
- 9苯酚和碱反应生成什么?是什么颜色的?
- 10已知直线y=1.5x-4与-4/3x+k/3的交点在第四象限,求k的取值范围
- 11138元用英文怎么写啊!
- 12一个底面积是30平方厘米的圆柱形玻璃杯中装有水,水里放着一个底面半径为3厘米,高为10厘米的圆锥形
- 13Last Mother day写一篇英语作文
- 14苯环带一个 CH2OH 叫什么?苯环带一个 羧基 叫什么
- 15核酸和核糖体有关系吗?
