钮扣是什么意思
 cly252022-10-04 11:39:541条回答
cly252022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 shiwule 共回答了23个问题
shiwule 共回答了23个问题 |采纳率78.3%- 是纽扣 (niǔ kòu)不是“钮”
衣服上用来扣合的球状或片状小物件.
套入纽襻把衣服等扣合起来的小形球状物或片状物. - 1年前
相关推荐
- 1.儿童服装厂生产红上衣和黄上衣.每件红上衣需要2个纽扣,每件黄上衣,需要4个钮扣.做成的两种颜色的上衣,每30件装成一
1.儿童服装厂生产红上衣和黄上衣.每件红上衣需要2个纽扣,每件黄上衣,需要4个钮扣.做成的两种颜色的上衣,每30件装成一箱,每箱衣服共需要钮扣72个.每箱中有红上衣和黄上衣各多少件?2.从A城到B城,甲要行2小时,乙要行1小时40分钟.如果甲先行10分钟,那么乙出发后多少分钟,在何处追上甲?
 honbo731年前1
honbo731年前1 -
 天秤座的莉莉 共回答了20个问题
天秤座的莉莉 共回答了20个问题 |采纳率90%设红上衣为x黄上衣为Y,2X+4Y=72 X+Y=30 解X=24 Y=61年前查看全部
- 可能性 概率有2颗红钮扣和6颗蓝钮扣,随机取4颗,问共有多少种可能性,其中至少有一颗是红色的.概率是多少?C8 4=70
可能性 概率
有2颗红钮扣和6颗蓝钮扣,随机取4颗,问共有多少种可能性,其中至少有一颗是红色的.概率是多少?
C8 4=70种 这个是怎么算的?不好意思,太久没碰数学了,都忘光了 XMX77585211年前1
XMX77585211年前1 -
 寻视天下 共回答了22个问题
寻视天下 共回答了22个问题 |采纳率77.3%总共8个钮扣 所以C8 4=70种
求 至少有一颗是红色. 从反面入手
没有红色的有 C6 4=15种
所以 至少有一颗是红色概率=1-15/70=11/141年前查看全部
- (2007•长春)一根单线从钮扣的4个孔中穿过(每个孔只穿过一次),其正面情形如图所示,下面4个图形中可能是其背面情形的
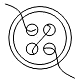 (2007•长春)一根单线从钮扣的4个孔中穿过(每个孔只穿过一次),其正面情形如图所示,下面4个图形中可能是其背面情形的是( )
(2007•长春)一根单线从钮扣的4个孔中穿过(每个孔只穿过一次),其正面情形如图所示,下面4个图形中可能是其背面情形的是( )
A.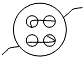
B.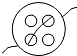
C.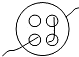
D.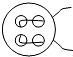
 gjqg1年前1
gjqg1年前1 -
 sampras88 共回答了18个问题
sampras88 共回答了18个问题 |采纳率94.4%解题思路:从正面即可看到背面将出现两条平行线,线头在相对的两个端点处.观察易得背面将有两条平行线,并且线头从正方形的对角线处出来,故选A.
点评:
本题考点: 几何变换的类型.
考点点评: 此题考查学生的识图能力和空间想象能力.1年前查看全部
- 有一位同学将2枚相同的钉子放在一架已调节平衡的托盘天平的左盘是,然后将5粒相同的钮扣或4只相同的螺母放在右盘上,托盘天平
有一位同学将2枚相同的钉子放在一架已调节平衡的托盘天平的左盘是,然后将5粒相同的钮扣或4只相同的螺母放在右盘上,托盘天平刚好平衡,他又将4粒钮扣放在左盘,在右盘放入了3只螺母加一个1克砝码,托盘天平也平衡.试问:每枚钉子、每粒钮扣、每只螺母的质量各是多少?
我知道答案是 10.4.5.我要的是过程 小蠡湖1年前1
小蠡湖1年前1 -
 marrybel 共回答了19个问题
marrybel 共回答了19个问题 |采纳率100%设钉子质量为A,钮扣质量为B,螺母质量为C
则有2A=5B=4C 即B=2A/5 C=A/2
由题意知 2A+4B=3C+5B+1 即2A=3A/2+2A/5+1→A=10
所以B=4 C=5
所以钉子质量为10g,钮扣质量为4g,螺母质量为5g1年前查看全部
- 常用的钮扣电池为银锌电池,它分别以锌和氧化银为电极.放电时锌极上的电极反应是:Zn+2OH--2e=Zn(OH)2,氧化
常用的钮扣电池为银锌电池,它分别以锌和氧化银为电极.放电时锌极上的电极反应是:Zn+2OH--2e=Zn(OH)2,氧化银电极上的反应是:Ag2O+H2O+2e=2Ag+2OH-,下列判断中,正确的是( )
A.锌是负极,发生氧化反应,氧化银是正极,发生还原反应
B.锌是正极,发生氧化反应,氧化银是负极,发生还原反应
C.锌是正极,发生还原反应,氧化银是负极,发生氧化反应
D.锌是负极,发生还原反应,氧化银是正极,发生氧化反应 火花塞子工1年前1
火花塞子工1年前1 -
 wo爱上sandy 共回答了13个问题
wo爱上sandy 共回答了13个问题 |采纳率92.3%解题思路:在原电池中,失电子的金属为负极,发生失电子的氧化反应,得电子的物质是正极,在正极发生还原反应.根据题意:放电时锌极上的电极反应是:Zn+2OH--2e=Zn(OH)2,则金属锌发生失电子的氧化反应,所以金属锌为负极,氧化银电极上的反应是:Ag2O+H2O+2e=2Ag+2OH-,则氧化银发生得电子得还原反应,素以氧化银点极是正极.
故选A.点评:
本题考点: 化学电源新型电池.
考点点评: 本题考查学生原电池的工作原理以及原电池中正负极的判断方法知识,可以根据所学知识进行回答,难度不大.1年前查看全部
- 一颗钮扣电池中的污染物全部释放后可污染60万升水,电池之所以有害,很大程度上是因为电池含汞,为此,国
 happytime-exe1年前1
happytime-exe1年前1 -
 w305296241 共回答了17个问题
w305296241 共回答了17个问题 |采纳率94.1%20061年前查看全部
- 有2007粒钮扣,两人轮流从中取几粒,但每人至少取1粒,最多取7粒,谁取到最后一粒,就算谁输.问:保证一定获胜的对策是什
有2007粒钮扣,两人轮流从中取几粒,但每人至少取1粒,最多取7粒,谁取到最后一粒,就算谁输.问:保证一定获胜的对策是什么?
只是看不太懂,能不能再详细些? haobole1年前6
haobole1年前6 -
 喃喃乖 共回答了21个问题
喃喃乖 共回答了21个问题 |采纳率95.2%2007÷(7+1)=n……7
要先取,第一次取7粒.以后无论对方取多少,你都要使你和对方相邻的一次和他的那次共取8粒(即他的第一次和你的第二次共取8粒),就能保证你能取走最后一粒.1年前查看全部
- 一颗钮扣电池中的污染物全部释放后可污染60万升水,电池之所以有害,很大程度上是因为电池含汞,为此,国
 红果子1年前1
红果子1年前1 -
 qianda 共回答了16个问题
qianda 共回答了16个问题 |采纳率93.8%20061年前查看全部
- 微型钮扣电池在现代生活中有广泛应用.有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH,电极总反应为:Zn+
微型钮扣电池在现代生活中有广泛应用.有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH,电极总反应为:Zn+Ag2O+H2O═Zn(OH)2+2Ag;根据上述反应式,判断下列叙述中正确的是( )
A.在使用过程中,电池负极区溶液的pH增大
B.电子由Ag20极经外电路流向Zn极
C.负极失去1mol电子时,正极生成108g银
D.Zn电极发生还原反应,Ag2O电极发生氧化反应 kuxiaotu1年前1
kuxiaotu1年前1 -
 qqandsh 共回答了18个问题
qqandsh 共回答了18个问题 |采纳率83.3%解题思路:该装置构成原电池,根据电极反应式知,锌作负极,氧化银作正极,负极上氢氧根离子参与反应,电子从负极沿导线流向正极,负极上发生氧化反应,正极上发生还原反应.A.根据电极反应式知,锌作负极,氧化银作正极,负极上氢氧根离子参与反应导致氢氧根离子浓度减小,则溶液的pH减小,故A错误;
B.锌是负极,氧化银是正极,电子从锌沿导线流向氧化银,故B错误;
C.负极失去1mol电子时,正极生成1mol银,质量为108g,故C正确;
D.负极锌失电子发生氧化反应,正极氧化银得电子发生还原反应,故D错误;
故选C.点评:
本题考点: 化学电源新型电池.
考点点评: 本题考查原电池原理,会根据得失电子判断正负极是解本题的关键,难度不大.1年前查看全部
- 原电池是一种将______转化为______的装置.电子表所用的某种钮扣电池的电极材料为Zn和Ag2O,电解质溶液为KO
原电池是一种将______转化为______的装置.电子表所用的某种钮扣电池的电极材料为Zn和Ag2O,电解质溶液为KOH,其电极反应式为:Zn+2OH--2e-=ZnO+H2O Ag2O+H2O+2e-=2Ag+2OH-
电池的负极是______,正极发生的是______反应(填反应类型),总反应式为______. 低调的uuuu1年前1
低调的uuuu1年前1 -
 xianfeng75 共回答了10个问题
xianfeng75 共回答了10个问题 |采纳率80%解题思路:原电池是将化学能转化为电能的装置,原电池中负极上失电子发生氧化反应,正极上得电子发生还原反应,在得失电子相等的条件下,将正负电极上电极反应式相加即得电池反应式.原电池是将化学能转化为电能的装置,该原电池中,Zn元素化合价由0价变为+2价、Ag元素化合价由+1价变为0价,所以Zn是负极、Ag2O是正极,负极上失电子发生氧化反应、正极上得电子发生还原反应,负极电极反应式为Zn+2OH--2e-=ZnO+H2O、正极电极反应式为 Ag2O+H2O+2e-=2Ag+2OH-,所以电池反应式为Zn+Ag2O=2Ag+ZnO,
故答案为:化学能;电能;氧化反应;还原反应;Zn+Ag2O=2Ag+ZnO.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题考查了原电池原理,根据元素化合价变化确定正负极及反应类型,将正负极电极反应式相加得电池反应式,难点是电极反应式的书写.1年前查看全部
- 初一科学题,天平初一科学题,用天平秤物体,左边放2个钉子,右边放5个钮扣和4个螺母,天平处于平衡,左边放4个钮扣,右边放
初一科学题,天平
初一科学题,用天平秤物体,左边放2个钉子,右边放5个钮扣和4个螺母,天平处于平衡,左边放4个钮扣,右边放3个螺母和1克重的砝码,天平处于平衡,问钉子、钮扣和螺母各重多少?
请简要回答一下过程和结果,
不好意思,看错了一个字,
右边放5个钮扣和4个螺母
应为
右边放5个钮扣或4个螺母,
难怪女儿做不出来。 江雪似寒1年前3
江雪似寒1年前3 -
 无缘_ss 共回答了17个问题
无缘_ss 共回答了17个问题 |采纳率94.1%只能列两个方程 没有办法求具体解 麻烦您看下条件是否齐全1年前查看全部
- 是纽扣还是钮扣两个到底是哪个?
 只为深秋1年前1
只为深秋1年前1 -
 79802669 共回答了16个问题
79802669 共回答了16个问题 |采纳率87.5%纽扣.因为,纽扣是关于衣服类,用于“纟”1年前查看全部
- 钮和纽有什么区别,如果单指衣服上的扣子是应该叫钮扣还是纽扣?
 本拉芳1年前1
本拉芳1年前1 -
 4221dwc 共回答了18个问题
4221dwc 共回答了18个问题 |采纳率94.4%目前“纽扣”和“钮扣”所指意思是一样的,没有区别,就“纽扣”本身来讲,分金属材质与非金属材质生产的,所以通常有些人会用“钮扣”来表示金属材质的“钮扣”,而非金属材质的则用“纽扣”来表示,这也是个人习惯问题,另外以地域来分,国内大部分是叫“纽扣”,港澳台则叫“钮扣”.
所以你说应该叫“纽扣”还是“钮扣”,全凭个人习惯,一般听到这两个不同写法的词组都会理解为相同的意思.1年前查看全部
- 耗电量计算 LED灯的一颗3V,0.006-0.020安培的LED灯泡..一颗35mah的钮扣电池可以点多少小时.麻烦附
耗电量计算 LED灯的
一颗3V,0.006-0.020安培的LED灯泡..一颗35mah的钮扣电池可以点多少小时.
麻烦附出计算公式.
晕死.我们那家工厂说的是一颗3V的锂电池可以用20多个小时呢.而且我们实际测试也达到了15个小时.不知道是不是他的电池有问题还是怎么样的. 2648350131年前1
2648350131年前1 -
 candycjj 共回答了21个问题
candycjj 共回答了21个问题 |采纳率81%如果这是题的话,就没什么可回答的了,如果是真的东西,20mA的LED一般是3.6V的.
假设电池的电压是恒定不变的,且你所说的钮扣电池是一次性锂电池,电池电压与LED工作电压相同,20mA的电流下,35mAh就是35mAh/20mA=1.5h,也就是1个半小时.
事实上是不可能得到这个时间的.标称3V的电池,初始放电电压大于3V,这样LED的工作电流也会超过额定电流,后期的时候,电压又低于3V,那么LED的工作电流也低于3V,由于LED的电压电流曲线和电池的放电曲线都不是直线,所以这么复杂的数字是不能用一个公式算出来的.计算值仅供参考使用.1年前查看全部
- 钮扣电池是一种常用的微型银锌电池,在电池内装有氧化银和锌等物质.当电池工作时,主要是锌与氧化银发生置换反应,从而产生电流
钮扣电池是一种常用的微型银锌电池,在电池内装有氧化银和锌等物质.当电池工作时,主要是锌与氧化银发生置换反应,从而产生电流,此反应的化学方程式______.  uff19851年前1
uff19851年前1 -
 余姿乐 共回答了16个问题
余姿乐 共回答了16个问题 |采纳率93.8%根据置换反应的生成物中有单质和化合物,结合质量守恒定律可以判断生成物是氧化锌和银,锌和氧化银发生置换反应生成氧化锌和银,
故答案为:Zn+Ag 2 O═ZnO+2Ag,1年前查看全部
- 1.已知“钮扣”电池的电极反应为:Zn 粉极:Zn+2OH--2e-=ZnO+H2O ;HgO 极:HgO+H2O+2e
1.已知“钮扣”电池的电极反应为:Zn 粉极:Zn+2OH--2e-=ZnO+H2O ;HgO 极:HgO+H2O+2e-=Hg+2OH-,据此判断 HgO 是( )
A.正极,被还原 B.负极,被氧化
C.负极,被还原 D.正极,被氧化
2.下列各组金属均有导线相连,并插入对应的液体中,其中不能组成原电池的是( )
A.Zn|H2SO4(稀)|C B.Cu|AgNO3(aq)|Ag
C.Zn|CCl4|Cu
D.Fe|H2SO4(稀)|Fe 此题答案为CD,请说明为什么选C
3.一种新型燃料电池,它是用两根金属做电极插入 KOH 溶液中,然后向两极分别通入甲烷和氧气,其电极反应为:
X 极:CH4+10OH--8e-=CO32-+7H2O
Y 极:4H2O+2O2+8e-=8OH-
关于此燃料电池的有关说法错误的是( )
A. X 为负极,Y 为正极
B. 工作一年时间后,KOH 的物质的量不变
C. 在标况下,通过 5.6L O2完全反应后,则有 1mol 电子发生转移
D.该电池工作时甲烷一极附近溶液pH升高
最好是简单易懂的. 渔缸1年前2
渔缸1年前2 -
 ilr2000 共回答了16个问题
ilr2000 共回答了16个问题 |采纳率87.5%原电池和电解池:当年有一个口诀,负失氧,正得还.负极失去电子是氧化反应;正极得到电子是还原反应.
1、第1题不难得出,答案是A.
2、构成原电池的本质:1、能够发生氧化还原反应2、能够电子转移(即能够构成回路),你看一下它们哪些能够发生氧化还原反应,显然Zn、Cu都不能与CCl4发生反应,电子无法转移,C不对.D不能发生氧化还原反应.
3、有口诀,AC对,总的反应中,氢氧根离子在不断减少,生成碳根离子,所以KOH物质的量会有变化,D明显氢氧根离子在减少,pH会下降.1年前查看全部
- 微型钮扣电池在现代生活中有广泛应用.有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH,电极反应为:
微型钮扣电池在现代生活中有广泛应用.有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH,电极反应为:
Zn+2OH--2e-=ZnO+H2O;Ag2O+H2O+2e-=2Ag+2OH-
根据上述反应式,判断下列叙述中正确的是( )
A.在使用过程中,电池负极区溶液的pH减小
B.使用过程中,电子由Ag20极经外电路流向Zn极
C.Zn是正极,Ag2O是负极
D.Zn电极发生还原反应,Ag2O电极发生氧化反应 景如1年前1
景如1年前1 -
 jennywu1226 共回答了16个问题
jennywu1226 共回答了16个问题 |采纳率100%解题思路:该装置为原电池,根据电极反应式知,锌作负极,氧化银作正极,负极上氢氧根离子参与反应,电子从负极沿导线流向正极,负极上发生氧化反应,正极上发生还原反应.A.根据电极反应式知,锌作负极,负极的电极反应为:Zn+2OH--2e-=ZnO+H2O,负极上氢氧根离子参与反应导致氢氧根离子浓度减小,则溶液的pH减小,故A正确;
B.锌是负极,氧化银是正极,电子从锌沿导线流向氧化银,故B错误;
C.根据电极反应式知,锌失电子作负极,氧化银得电子作正极,故C错误;
D.根据电极反应式知,负极锌失电子发生氧化反应,正极氧化银得电子发生还原反应,故D错误;
故选A.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题考查原电池原理,会根据得失电子判断正负极是解本题的关键,结合氧化还原反应原理分析,题目难度不大.1年前查看全部
- “钮扣”和“纽扣”哪个正确?
 dlj2003asd1年前1
dlj2003asd1年前1 -
 fireboyjh 共回答了22个问题
fireboyjh 共回答了22个问题 |采纳率95.5%纽扣正确1年前查看全部
- (2014•济宁模拟)据专家测定:一节钮扣电池如不经过很好的处理.扔进河里可以污染60万升水,相当于人一生中的饮水量.一
(2014•济宁模拟)据专家测定:一节钮扣电池如不经过很好的处理.扔进河里可以污染60万升水,相当于人一生中的饮水量.一节一号电池扔在泥土里能使一平方米的土地永远失去利用价值.如果植物吸收了土里的有害物质.人吃了已吸收有害物质的植物,就可能导致各种直接危害人体健康的病症,为此通过探究废电池浸出液对小麦种子萌发的实验来说明该问题.如图是两个相同条件下种子萌发的实验示意图,请根据图回答:
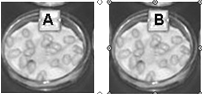
(1)在探究废电池浸出液对小麦种子萌发的实验时,你作出的假设:______.
(2)模拟试验中,老师提供了模拟的废电池浸出液,你们小组讨论设计的实验方案是:在A培养皿中放入100粒清水浸泡过的小麦种子,在B培养皿中放入______粒清水浸泡过的小麦种子.
(3)合理安排小组的每个成员,每天定时向A培养皿和B培养皿中分别喷洒______和______.B组培养皿在此模拟实验中起______作用. lxy62601851年前1
lxy62601851年前1 -
 zhaoka 共回答了25个问题
zhaoka 共回答了25个问题 |采纳率92%解题思路:(1)此题通过探究“废电池浸出液对小麦种子萌发影响”的实验为背景,考查学生的科学探究能力,实验设计、分析能力,实验数据的处理能力,通过此题体会科学探究的方法步骤.
(2)探究的一般过程:提出问题、作出假设、制定计划、实施计划、得出结论、表达和交流.
(3)对照实验:在探究某种条件对研究对象的影响时,对研究对象进行的除了该条件不同以外,其他条件都相同的实验.根据变量设置一组对照实验,使实验结果具有说服力.一般来说,对实验变量进行处理的,就是实验组.没有处理是的就是对照组.(1)假设是对问题肯定火否定的回答.根据“探究废电池浸出液对小麦种子萌发的影响”,作出的假设:废电池浸出液对小麦种子萌发有影响.
(2)对照实验是唯一变量实验,除了变量外其它条件都相同.因此模拟试验中,老师提供了模拟的废电池浸出液,设计的实验方案是:在A培养皿中放入100粒清水浸泡过的小麦种子,在B培养皿中放入100粒清水浸泡过的小麦种子.
(3)探究废电池浸出液对小麦种子萌发的影响,因此实验的唯一变量是否喷洒废电池浸出液.因此每天定时向A培养皿和B培养皿中分别喷洒废电池浸出液和清水.B组培养皿在此模拟实验中起对照作用.
故答案为:
(1)废电池浸出液对小麦种子萌发有影响;
(2)100;
(3)废电池浸出液;清水;对照.点评:
本题考点: 探究种子萌发的条件.
考点点评: 解答此类题目的关键是理解掌握科学探究的步骤以及对照实验的特点.1年前查看全部
- 银锌钮扣电池的两个电极分别是由氧化银与少量石墨组成的活性材料和锌汞合金构成,电解质为氢氧化钾溶液,电极反应为Zn+2OH
银锌钮扣电池的两个电极分别是由氧化银与少量石墨组成的活性材料和锌汞合金构成,电解质为氢氧化钾溶液,电极反应为Zn+2OH--2e-=ZnO+H2O;Ag2O+H2O+2e-=2Ag+2OH-,总反应为:Ag2O+Zn=2Ag+ZnO.下列判断正确的是( )
A.锌为正极,Ag2O为负极
B.OH-往负极移动
C.原电池工作时正极区pH减小
D.如果有1mol电子转移,就有65g Zn参加反应 心零度1年前1
心零度1年前1 -
 珍惜772 共回答了15个问题
珍惜772 共回答了15个问题 |采纳率93.3%解题思路:A、原电池中失电子的为负极,得到电子的为正极;
B、依据电极反应方向判断,氢氧根离子向负极移动;
C、依据正极电极反应中的区域离子浓度变化分析;
D、依据电子守恒分析计算.A、电极反应为Zn+2OH--2e-=ZnO+H2O、Ag2O+H2O+2e-=2Ag+2OH-,原电池中失电子的为负极,得到电子的反应为正极,锌做负极,氧化银做正极,故A错误;
B、负极电极反应为Zn+2OH--2e-=ZnO+H2O,消耗氢氧根离子,氢氧根离子移向负极,故B正确;
C、正极反应为Ag2O+H2O+2e-=2Ag+2OH-,生成氢氧根离子,正极区溶液pH增大,故C错误;
D、负极电极反应为Zn+2OH--2e-=ZnO+H2O,如果有1mol电子转移,就有32.5g Zn参加反应,故D错误;
故选B.点评:
本题考点: 化学电源新型电池.
考点点评: 本题考查了原电池原理的应用,电池电极反应,离子变化分析,依据电极反应分析判断是解题关键,题目难度中等.1年前查看全部
- 电子计算机所用钮扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应是:Zn+2OH--2e-═ZnO+H2
电子计算机所用钮扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应是:Zn+2OH--2e-═ZnO+H2OAg2O+H2O+2e-═2Ag+2OH-,下列判断正确的是( )
A.锌为正极,Ag2O为负极
B.锌为负极,发生还原反应
C.原电池工作时,负极区溶液pH减小
D.原电池工作时,负极区溶液pH增大 ruffei1年前1
ruffei1年前1 -
 杨文娜 共回答了14个问题
杨文娜 共回答了14个问题 |采纳率92.9%解题思路:根据化合价变化可知Zn被氧化,发生氧化反应,应为原电池的负极,则正极为Ag2O,得电子发生还原反应;根据电极反应判断溶液pH的变化.A、根据化合价变化可知Zn被氧化,应为原电池的负极,则正极为Ag2O,故A错误;
B、根据化合价变化可知Zn失电子被氧化,为原电池的负极,故B错误;
C、原电池工作时,负发生反应Zn+2OH--2e-=ZnO+H2O,溶液PH值减小,故C正确;
D、原电池工作时,负发生反应Zn+2OH--2e-=ZnO+H2O,溶液PH值减小,故D错误.
故选C.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题考查了原电池知识,题目难度不大,注意根据正负极发生的反应来判断溶液的PH的变化.1年前查看全部
- 电子计算机所用钮扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应是: Zn+2OH - -2e - ==
电子计算机所用钮扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应是: Zn+2OH - -2e - ===ZnO+H 2 O Ag 2 O+H 2 O+2e - ===2Ag+2OH - ,下列判断不正确的是
A.锌为正极,Ag 2 O为负极 B.锌为负极,Ag 2 O为正极 C.原电池工作时,负极区溶液pH减小 D.原电池工作时,正极区溶液pH增大  nrexll1年前1
nrexll1年前1 -
 shi213285 共回答了9个问题
shi213285 共回答了9个问题 |采纳率100%A
1年前查看全部
- (2009•嘉定区一模)电子计算器最常用的电池是氧化银(Ag2O)钮扣电池,其中银元素的化合价为( )
(2009•嘉定区一模)电子计算器最常用的电池是氧化银(Ag2O)钮扣电池,其中银元素的化合价为( )
A.+l
B.+2
C.+3
D.+4 悦声悦耳1年前1
悦声悦耳1年前1 -
 想也不想 共回答了20个问题
想也不想 共回答了20个问题 |采纳率85%解题思路:根据在化合物中正负化合价代数和为零,结合氧化银(Ag2O)的化学式进行解答本题.氧元素显-2,设银元素的化合价是x,根据在化合物中正负化合价代数和为零,可知氧化银(Ag2O)中银元素的化合价:2x+(-2)=0,则x=+1.
故选A.点评:
本题考点: 有关元素化合价的计算.
考点点评: 本题难度不大,考查学生利用化合价的原则计算指定元素的化合价的能力.1年前查看全部
- (2009•嘉定区一模)电子计算器最常用的电池是氧化银(Ag2O)钮扣电池,其中银元素的化合价为( )
(2009•嘉定区一模)电子计算器最常用的电池是氧化银(Ag2O)钮扣电池,其中银元素的化合价为( )
A. +l
B. +2
C. +3
D. +4 Rachel_Aries1年前1
Rachel_Aries1年前1 -
 zxr2008 共回答了21个问题
zxr2008 共回答了21个问题 |采纳率81%解题思路:根据在化合物中正负化合价代数和为零,结合氧化银(Ag2O)的化学式进行解答本题.氧元素显-2,设银元素的化合价是x,根据在化合物中正负化合价代数和为零,可知氧化银(Ag2O)中银元素的化合价:2x+(-2)=0,则x=+1.
故选A.点评:
本题考点: 有关元素化合价的计算.
考点点评: 本题难度不大,考查学生利用化合价的原则计算指定元素的化合价的能力.1年前查看全部
- 钮扣电池是一种常用的微型银锌电池,在电池内装有氧化银和锌等物质.当电池工作时,主要是锌与氧化银发生置换反应,从而产生电流
钮扣电池是一种常用的微型银锌电池,在电池内装有氧化银和锌等物质.当电池工作时,主要是锌与氧化银发生置换反应,从而产生电流,此反应的化学方程式______.
 麦田里的苏白1年前1
麦田里的苏白1年前1 -
 可可小老鼠 共回答了17个问题
可可小老鼠 共回答了17个问题 |采纳率94.1%解题思路:根据锌和氧化银发生置换反应,所以生成物中一定有单质和化合物进行分析.根据置换反应的生成物中有单质和化合物,结合质量守恒定律可以判断生成物是氧化锌和银,锌和氧化银发生置换反应生成氧化锌和银,
故答案为:Zn+Ag2O═ZnO+2Ag,点评:
本题考点: 书写化学方程式、文字表达式、电离方程式;置换反应及其应用.
考点点评: 在解此类题时,首先根据置换反应的原理和质量守恒定律判断出生成物,然后根据方程式的书写规则书写方程式.1年前查看全部
- 银锌钮扣电池的两个电极分别是由氧化银与少量石墨组成的活性材料和锌汞合金构成,电解质为氢氧化钾溶液,电极反应为负极:Zn+
银锌钮扣电池的两个电极分别是由氧化银与少量石墨组成的活性材料和锌汞合金构成,电解质为氢氧化钾溶液,电极反应为负极:Zn+2OH--2e-═ZnO+H2O;正极:Ag2O+H2O+2e-═2Ag+2OH-;总反应为:Ag2O+Zn═2Ag+ZnO,下列判断正确的是( )
A. 锌为正极,Ag2O为负极
B. 锌为阳极,Ag2O为阴极
C. 原电池工作时,负极区pH减小
D. 原电池工作时,负极区pH增大 凉粥1年前4
凉粥1年前4 -
 萧萧烟雨 共回答了30个问题
萧萧烟雨 共回答了30个问题 |采纳率83.3%解题思路:A、原电池中失电子的为负极,得到电子的为正极;
B、依据原电池中,电极名称分别为正极和负极来回答;
C、依据负极电极反应导致氢离子或是氢氧根离子浓度的变化情况来分析;
D、依据负极电极反应导致氢离子或是氢氧根离子浓度的变化情况来分析.A、根据电极反应负极:Zn+2OH--2e-═ZnO+H2O;正极:Ag2O+H2O+2e-═2Ag+2OH-,所以锌为负极,Ag2O为正极,故A错误;
B、根据电极反应负极:Zn+2OH--2e-═ZnO+H2O;正极:Ag2O+H2O+2e-═2Ag+2OH-,所以锌为负极,Ag2O为正极,故B错误;
C、根据负极电极反应为Zn+2OH--2e-═ZnO+H2O,消耗氢氧根离子,所以负极区pH减小,故C正确;
D、原电池工作时,负极电极反应为Zn+2OH--2e-═ZnO+H2O,消耗氢氧根离子,所以负极区pH减小,故D错误;
故选:C.点评:
本题考点: 化学电源新型电池.
考点点评: 本题考查了原电池原理的应用,电池电极反应,离子变化分析,依据电极反应分析判断是解题关键,题目难度中等.1年前查看全部
- 如图为一种钮扣微型电池,其电极分别为Ag2O和Zn电解质溶液是KOH溶液,俗称银锌电池,该电池的电极反应式为:Zn+Ag
 如图为一种钮扣微型电池,其电极分别为Ag2O和Zn电解质溶液是KOH溶液,俗称银锌电池,该电池的电极反应式为:Zn+Ag2O═ZnO+2Ag根据以上提供的资料,下列说法正确的是( )
如图为一种钮扣微型电池,其电极分别为Ag2O和Zn电解质溶液是KOH溶液,俗称银锌电池,该电池的电极反应式为:Zn+Ag2O═ZnO+2Ag根据以上提供的资料,下列说法正确的是( )
A.溶液中OH-向正极移动
B.放电时正极附近溶液的PH值升高
C.电池负极的电极反应为:Zn-2e-═Zn2+
D.电池工作时,生成1mol Ag就有2mol电子转移 喽喽豆1年前1
喽喽豆1年前1 -
 417271763 共回答了17个问题
417271763 共回答了17个问题 |采纳率94.1%解题思路:根据总方程式可知Zn为原电池的负极,发生反应为Zn+2OH--2e-═ZnO+H2O,Ag2O为原电池的正极,发生反应为Ag2O+H2O+2e-═2Ag+2OH-,原电池中电流从正极流向负极,溶液中阴离子流向负极,阳离子流向正极.A.溶液中OH-向负极移动,故A错误;
B.正极反应为Ag2O+H2O+2e-═2Ag+2OH-,放电时正极附近溶液的PH值升高,故B正确;
C.负极电极反应为Zn+2OH-=ZnO+H2O+2e-,故C错误;
D.正极电极反应为:Ag2O+H2O+2e-=2Ag+2OH-,当电路中每通过1mol电子,则生成1molAg,故D错误.
故选B.点评:
本题考点: 化学电源新型电池.
考点点评: 本题考查原电池知识,题目难度不大,注意根据电极反应判断原电池的正负极以及电池反应.1年前查看全部
- 下列各组词语中,没有错别字的一项是 [ ] A.钮扣 易拉罐 一诺千金
下列各组词语中,没有错别字的一项是 [ ]A.钮扣 易拉罐 一诺千金 独当一面
B.赃款 一副画 分庭抗礼 陈规陋习
C.先驱 入场券 风烛残年 蛛丝马迹
D.作客 坐月子 激浊扬清 三翻五次 人右1年前1
人右1年前1 -
 manman2a4 共回答了24个问题
manman2a4 共回答了24个问题 |采纳率75%C1年前查看全部
- 有1992粒钮扣,两人轮流从中取几粒,但每人至少取1粒,最多取4粒,谁取到最后一粒,就算谁输.问:保证一定获胜的对策是什
有1992粒钮扣,两人轮流从中取几粒,但每人至少取1粒,最多取4粒,谁取到最后一粒,就算谁输.问:保证一定获胜的对策是什么?
 一言而尽__1年前7
一言而尽__1年前7 -
 飘逸帅帅 共回答了19个问题
飘逸帅帅 共回答了19个问题 |采纳率100%解题思路:根据每人至少取1粒,最多取4粒,谁取到最后一粒,就算谁输,那就让每次取出的和是5,再根据1992除以5的余数,确定先取的数,以保证先取的人获胜.保证一定获胜的对策是:(1)先取1粒钮扣,这时还剩1991粒钮扣,
(2)下面轮到对方取,如果对方取n粒(1≤n≤4),自己就取“5-n“粒,
经过398个轮回后,就取出398×5=1990(粒)钮扣,
还剩1粒钮扣,这1粒必定留给对方取.
答:为保证一定获胜,则要先取1粒钮扣,然后让对方取n粒(1≤n≤4),自己就取“5-n“粒.点评:
本题考点: 最佳对策问题.
考点点评: 解答此题的关键是知道先取的数是多少,和每次应该怎么取,即可得出答案.1年前查看全部
- 生活中的圆形在我们的日常生活中有不少的物体是圆形的,如:硬币、瓶盖、钟面、圆桌、钮扣、圆形饼干、铁饼、光盘,还有那草原上
生活中的圆形
在我们的日常生活中有不少的物体是圆形的,如:硬币、瓶盖、钟面、圆桌、钮扣、圆形饼干、铁饼、光盘,还有那草原上的蒙古包和交通工具上的轮胎.在这生活中众多的圆形用具中,你们有没有想过,它们为什么是圆形的?
首先蒙古包为天穹式,呈圆形,木架外边用白羊毛毡覆盖.因为它是圆形的,所以立在草原上,大风雪中阻力小,再大的地震中也不会变形,顶上又不积雨雪,寒气不易侵入,是非常安全的住所.
然后说说轮胎吧.最开始的轮是实心的,边缘也不是磨圆光滑的,而是不规则多边形的.但是这样不仅在行进中颠簸得厉害,而且由于是实心的原因,十分耗材和沉重并且容易坏.后来历经多年的诸多木匠和工匠以及勤劳智慧的劳动人民的努力改进,不规则多边形逐渐被接近圆形的轮取代,轴和轮的关系在同时期也得到了改进,轴的出现使材料大为节省,车辆也变得轻盈起来.
西方数学、哲学史上历来有这么种说法:“上帝是按照数学原则创造这个世界的”.而现在想来,石子入水后浑然天成的圆形波纹,阳光下肆意绽放的向日葵,天体运行时近似圆形的轨迹,甚至于遥远天际悬挂的那轮明月、朝阳……而所有这一切,给予我们的不正是一种微妙的启示吗? woaizhang13141年前1
woaizhang13141年前1 -
 蟲蟲子 共回答了22个问题
蟲蟲子 共回答了22个问题 |采纳率86.4%我和你一样相信一切都是有原因的,生活中的圆形都是我们的前辈不断改进把数学知识并把它和生活紧密结合起来,最大限度的满足人们符合科学1年前查看全部
- 高三原电池、如图为一种钮扣微型电池,其电极分别为Ag2O和Zn,电解质溶液中KOH溶液,俗称银锌电池,该电池的总反应式为
高三原电池、
如图为一种钮扣微型电池,其电极分别为Ag2O和Zn,电解质溶液中KOH溶液,俗称银锌电池,该电池的总反应式为:Zn+Ag2O===ZnO+2Ag;根据以上提供的资料,判断下列说法正确的是( )
A.负极反应为Zn—2e-===Zn2+
B.放电时正极附近溶液的pH升高
C.放电时负极附近溶液的pH升高
D.溶液中阴离子向正极方向移动,阳离子向负极方向移动
为什么A是错的,ZN不是负极么~

 酽茗1年前1
酽茗1年前1 -
 cengduan 共回答了16个问题
cengduan 共回答了16个问题 |采纳率93.8%写原电池电极方程式应该注意:
1、判断原电池的电极(判断正负极)
2、判断反应物
3、判断生成物(看处于什么环境,譬如酸性环境和碱性环境还有有氧环境)
4、检查方程式前后电荷是否一样
你的题目,显然在碱性环境下的,锌离子在碱性环境下不可能在离子形式存在!所以其电极方程式为:Zn+2OH- —2e- === ZnO+H2O 但为什么是ZnO而不是Zn(OH)2,这是要依据题目本意来的!有些电池中却可能是Zn(OH)2,而如果是酸性介质,则A选项是正确的!
又如:高中阶段中的氢气氧气燃料电池就可能有两种情况,假如以氢氧化钾溶液为电解质,则负极的产物为水,正极的产物为氢氧根离子!假如以硫酸为电解质,则负极的产物为氢离子,而正极为水!1年前查看全部
- 微型钮扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是Ag 2 O和Zn,电解质溶液为
微型钮扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是Ag 2 O和Zn,电解质溶液为
KOH,电极反应为:Zn+2OH - -2e - =ZnO+H 2 O Ag 2 O+H 2 O+2e - =2Ag+2OH - 根据上述反应式,判断下列叙述正确的是[ ]A.在使用过程中,电池负极区溶液的pH减小
B.在使用过程中,电子由Ag 2 O极经外电路流向Zn极
C.Zn是负极,Ag 2 O是正极
D.Zn电极发生还原反应,Ag 2 O电极发生氧化反应 坐南朝北东升西落1年前1
坐南朝北东升西落1年前1 -
 sdf5f544sb2 共回答了17个问题
sdf5f544sb2 共回答了17个问题 |采纳率82.4%AC1年前查看全部
- 有1992粒钮扣,两人轮流从中取几粒,但每人至少取1粒,最多取4粒,谁取到最后一粒,就算谁输.问:保证一定获胜的对策是什
有1992粒钮扣,两人轮流从中取几粒,但每人至少取1粒,最多取4粒,谁取到最后一粒,就算谁输.问:保证一定获胜的对策是什么?
 左岸巫师1年前2
左岸巫师1年前2 -
 trip4959 共回答了14个问题
trip4959 共回答了14个问题 |采纳率92.9%解题思路:根据每人至少取1粒,最多取4粒,谁取到最后一粒,就算谁输,那就让每次取出的和是5,再根据1992除以5的余数,确定先取的数,以保证先取的人获胜.保证一定获胜的对策是:(1)先取1粒钮扣,这时还剩1991粒钮扣,
(2)下面轮到对方取,如果对方取n粒(1≤n≤4),自己就取“5-n“粒,
经过398个轮回后,就取出398×5=1990(粒)钮扣,
还剩1粒钮扣,这1粒必定留给对方取.
答:为保证一定获胜,则要先取1粒钮扣,然后让对方取n粒(1≤n≤4),自己就取“5-n“粒.点评:
本题考点: 最佳对策问题.
考点点评: 解答此题的关键是知道先取的数是多少,和每次应该怎么取,即可得出答案.1年前查看全部
- 银锌钮扣电池的电极反应式和电池化学方程式疑问
银锌钮扣电池的电极反应式和电池化学方程式疑问
这些是我搜到的 银锌电池负极:Zn + 2OH- -2e-=== ZnO + H2O
正极:Ag2O + H2O + 2e- === 2Ag + 2OH-
电池的总反应式为:Ag2O + Zn === 2Ag + ZnO
银锌蓄电池
负极:Zn+2OH- -2e- =Zn(OH)2
正极:Ag2O+H2O+2e- =2Ag+2OH-
总反应为:Zn + Ag2O +H2O = Zn(OH)2 + 2Ag
1.银锌电池的负极的电极反应式生成物为什么不能是H2?如果这样2Zn+2OH- 2e-=2ZnO+H2(上标)也是可以配平的啊2.如果负极确定了是Zn + 2OH- -2e-=== ZnO + H2O这个方程式,总反应我知道是Ag2O + Zn === 2Ag + ZnO,而正极我不清楚,能否用总反应方程式减去负极方程式?(因为我想,总反应方程式为正极方程式与负极方程式相加,那么反过来应该也能相减)3.银锌电池和银锌蓄电池究竟有何不同?它们的正极反应完全一样,负极却不一样(当然,如果正极一样负极不一样,那总反应肯定不一样)负极反应物相同,连系数都一样,可生成物为什么一个是ZnO和H20,一个却是Zn(OH)2? 330988aa1年前1
330988aa1年前1 -
 啃啃 共回答了11个问题
啃啃 共回答了11个问题 |采纳率100%1 锌的还原性不够把它还原成H2,就像双氧水不能把二氧化锰氧化成高锰酸钾一样,可以参考下电化学的电极电势2 可以相减啊,我们那时就那样讲的3 因为反应条件不同,就是他们反应时所处的环境,可以看到蓄电池反应是有水的,纽扣电池里有水吗1年前查看全部
- 是"纽扣",还是 "钮扣"?
 最爱vv1年前1
最爱vv1年前1 -
 bad12 共回答了10个问题
bad12 共回答了10个问题 |采纳率80%两个到底是哪个?各位,帮帮吧 纽扣.因为,纽扣是关于衣服类,用于“纟” 纽扣!纽扣是指一些事物之间的关联,如交通枢纽钮扣是指衣服上1年前查看全部
- 衬衫上少了粒钮扣英文怎么说?(酒店英语方向)
衬衫上少了粒钮扣英文怎么说?(酒店英语方向)
老外:我的衬衫交给你们拿去干洗的时候好好的,为什么现在却少了粒钮扣?(说完,拿着衬衫指给客房服务员看)
服务员:真的不好意思,我需要打个电话给房务中心,
老外:OK,
主管进来了:非常抱歉,我们送客衣进房间的时候您正好不在,本来想跟您解释的,洗衣厂送过来的时候就已经没有了,实在不好意思. 晕菜鱼鱼1年前2
晕菜鱼鱼1年前2 -
 xfaewa001 共回答了22个问题
xfaewa001 共回答了22个问题 |采纳率86.4%A button has been lost from my shirt.
My shirt has lost one of its buttons.1年前查看全部
- 银锌钮扣电池的电极反应式和电池化学方程式疑问
银锌钮扣电池的电极反应式和电池化学方程式疑问
这些是我搜到的 银锌电池负极:Zn + 2OH- -2e-=== ZnO + H2O 正极:Ag2O + H2O + 2e- === 2Ag + 2OH- 电池的总反应式为:Ag2O + Zn === 2Ag + ZnO银锌蓄电池负极:Zn+2OH- -2e- =Zn(OH)2正极:Ag2O+H2O+2e- =2Ag+2OH-总反应为:Zn + Ag2O +H2O = Zn(OH)2 + 2Ag问题:1.银锌电池的负极的电极反应式生成物为什么不能是H2?如果这样2Zn+2OH- 2e-=2ZnO+H2(上标)也是可以配平的啊2.如果负极确定了是Zn + 2OH- -2e-=== ZnO + H2O这个方程式,总反应我知道是Ag2O + Zn === 2Ag + ZnO,而正极我不清楚,能否用总反应方程式减去负极方程式?(因为我想,总反应方程式为正极方程式与负极方程式相加,那么反过来应该也能相减)3.银锌电池和银锌蓄电池究竟有何不同?它们的正极反应完全一样,负极却不一样(当然,如果正极一样负极不一样,那总反应肯定不一样)负极反应物相同,连系数都一样,可生成物为什么一个是ZnO和H20,一个却是Zn(OH)2? hh相识1年前2
hh相识1年前2 -
 lb810105 共回答了17个问题
lb810105 共回答了17个问题 |采纳率88.2%负极:Zn + 2OH- -2e-=== ZnO + H2O
正极:Ag2O + H2O + 2e- === 2Ag + 2OH-
电池的总反应式为:Ag2O + Zn === 2Ag + ZnO1年前查看全部
- 微型钮扣电池在现代生活中有广泛应用.有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH,电极反应为:Zn+2
微型钮扣电池在现代生活中有广泛应用.有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH,电极反应为:Zn+2OH--2e=ZnO+H2O,Ag2O+H2O+2e=2Ag+2OH-,总反应为:Ag2O+Zn=2Ag+ZnO 根据上述反应式,判断下列叙述中,正确的是( )
A.在使用过程中,电池负极区溶液pH值增大
B.在使用过程中,电子由Ag2O极经外电路流向Zn极
C.Zn是负极,Ag2O是正极
D.Zn电极发生还原反应,Ag2O电极发生氧化反应 打工祖母1年前1
打工祖母1年前1 -
 夜雨捂桐 共回答了18个问题
夜雨捂桐 共回答了18个问题 |采纳率83.3%解题思路:银锌电池的电极分别是Ag2O和Zn,电解质溶液为KOH,电极反应为:Zn+2OH--2e=ZnO+H2O;Ag2O+H2O+2e=2Ag+2OH-,则Zn为负极,发生氧化反应,Ag2O为正极,发生还原反应,电子由负极流向正极,以此来解答.A.负极发生Zn+2OH--2e=ZnO+H2O,c(OH-)减小,所以电池负极区溶液的pH减小,故A错误;
B.Zn为负极,Ag2O为正极,则使用过程中,电子由Zn极经外电路流向Ag20极,故B错误;
C.Zn失去电子,Zn为负极,Ag2O得到电子是正极,故C正确;
D.Zn电极发生氧化反应,Ag2O电极发生还原反应,故D错误;
故选C.点评:
本题考点: 化学电源新型电池.
考点点评: 本题考查原电池的工作原理,明确电极反应、正负极的判断、电子的流向即可解答,题目难度不大.1年前查看全部
- 银锌钮扣高能电池放电时的反应为: ,下列有关说法中不正确的是 [ ] A
银锌钮扣高能电池放电时的反应为: 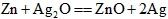 ,下列有关说法中不正确的是[ ]
,下列有关说法中不正确的是[ ]A.可用稀硝酸做电解质溶液
B.可用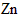 做负极
做负极
C.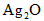 在正极上发生还原反应
在正极上发生还原反应
D.该反应属于置换反应 wangsea1年前1
wangsea1年前1 -
 happycindy 共回答了22个问题
happycindy 共回答了22个问题 |采纳率90.9%A1年前查看全部
- 如图为一种钮扣微型电池,其电极分别为Ag2O和Zn,电解质溶液是KOH溶液,俗称银锌
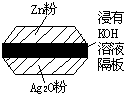 如图为一种钮扣微型电池,其电极分别为Ag2O和Zn,电解质溶液是KOH溶液,俗称银锌
如图为一种钮扣微型电池,其电极分别为Ag2O和Zn,电解质溶液是KOH溶液,俗称银锌
电池,该电池的总反应式为:Zn+Ag2O=ZnO+2Ag.根据以上提供的资料,判断下列说法正确的是( )
A.放电时锌为正极,Ag2O为负极
B.放电时正极附近溶液的pH升高
C.充电时电流流向阳极,阳极被氧化
D.充电时阳极的电极反应为:ZnO+H2O+2e-=Zn+2OH- yangkers1年前1
yangkers1年前1 -
 lauryn_hill 共回答了15个问题
lauryn_hill 共回答了15个问题 |采纳率93.3%解题思路:放电时,该电池反应式中元素化合价变化为:Zn元素由0价变为+2价,Ag元素化合价由+1价变为0价,所以锌作负极,氧化银作正极,电极反应式为Zn+2OH--2e-═ZnO+H2O、Ag2O+H2O+2e-═2Ag+2OH-,
充电时,阳极上失电子发生氧化反应,电流从原电池正极流向电解池阳极.A.放电时,该电池反应式中元素化合价变化为:Zn元素由0价变为+2价,Ag元素化合价由+1价变为0价,所以锌作负极,氧化银作正极,故A错误;
B.放电时,正极上电极反应式为Ag2O+H2O+2e-═2Ag+2OH-,正极附近生成氢氧根离子,导致氢氧根离子浓度增大,则溶液的pH增大,故B正确;
C.充电时,氧化银电极连接原电池正极,所以电流流向阳极,阳极上失电子发生氧化反应而被氧化,故C正确;
D.充电时,阳极上失电子发生氧化反应,电极反应式为2Ag+2OH--2e-═Ag2O+H2O,故D错误;
故选BC.点评:
本题考点: 化学电源新型电池.
考点点评: 本题考查了化学电源新型电池,明确原电池原理和电解池原理是解答本题关键,再结合电极反应式解答,注意电极反应式的书写,难度中等.1年前查看全部
- 钮扣电池是一种常用的微型银锌电池,在电池内装有氧化银和锌等物质.当电池工作时,主要是锌与氧化银发生置换反应,从而产生电流
钮扣电池是一种常用的微型银锌电池,在电池内装有氧化银和锌等物质.当电池工作时,主要是锌与氧化银发生置换反应,从而产生电流,此反应的化学方程式______.
 我是管钱的1年前3
我是管钱的1年前3 -
 bclz112 共回答了19个问题
bclz112 共回答了19个问题 |采纳率89.5%解题思路:根据锌和氧化银发生置换反应,所以生成物中一定有单质和化合物进行分析.根据置换反应的生成物中有单质和化合物,结合质量守恒定律可以判断生成物是氧化锌和银,锌和氧化银发生置换反应生成氧化锌和银,
故答案为:Zn+Ag2O═ZnO+2Ag,点评:
本题考点: 书写化学方程式、文字表达式、电离方程式;置换反应及其应用.
考点点评: 在解此类题时,首先根据置换反应的原理和质量守恒定律判断出生成物,然后根据方程式的书写规则书写方程式.1年前查看全部
- 钮扣 和 钮扣 哪个正确是 钮扣 和 纽扣 哪个正确?
 0aibby1年前1
0aibby1年前1 -
 lj588 共回答了17个问题
lj588 共回答了17个问题 |采纳率88.2%准确的说是第一个,只不过我们用拼音输入法,系统默认为第2个1年前查看全部
- (12分)(1)钮扣电池的电极材料为Zn和Ag 2 O,电解质溶液为KOH,其电极反应为:Zn + 2OH - -2e
(12分)(1)钮扣电池的电极材料为Zn和Ag 2 O,电解质溶液为KOH,其电极反应为:Zn + 2OH - -2e - =" ZnO" + H 2 O Ag 2 O + H 2 O + 2e - =" 2Ag" + 2OH -
电池的负极是 (填电极材料),正极发生的是 反应(填反应类型),
总反应式为 。
(2)图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从两极通入燃料电池时,便可在闭合回路中不断地产生电流.这被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点。试回答下列问题:
①图中通过负载的电子流动方向______ (填“向左”或“向右”).
②写出氢氧燃料电池工作时正极反应方程式 :
③放电过程中,负极附近溶液的pH (填“增大”,“减小”,“保持不变”) 悠长假期791年前1
悠长假期791年前1 -
 龙城岁月2006 共回答了15个问题
龙城岁月2006 共回答了15个问题 |采纳率100%(1)Zn 还原反应 Zn + Ag 2 O =" ZnO" + 2Ag
(2)①向右②O 2 +2H 2 O+4e - =4OH - ③减小
(1)考查原电池的有关概念和判断。在原电池中较活泼的金属作负极,失去电子,被氧化,发生氧化反应。较不活泼的金属作正极,正极得到电子,被还原,发生还原反应。根据电极反应式可得Zn是负极,氧化银是正极。将两电极反应式叠加即得到总反应式。
(2)在原电池中负极失去电子经导线传递到正极上,在氢氧燃料电池中氢气在负极通入,所以根据装置图可知电子的流动方向向右。氧气得到电子,在正极通入,电极反应式为O 2 +2H 2 O+4e - =4OH - 。因为负极氢气失去电子,氧化生成氢离子,氢离子中和溶液中的OH - 使pH减小。1年前查看全部
大家在问
- 1有哪有句子可以表达无人理解的感觉呢
- 2(2013•上海)下列感受器中属于化学感受器的是( )
- 3对1,2,3,4可作运算(1+2+3)×4=24,现有有理数3,4,-6,10,请运算加,减,乘,除法则写出三种不同
- 4考研数学高数求极限当x趋近于零时,变量x^2分之一乘以sin(1/x) A:无穷小量 B 无穷大量 C:有界,不无穷小量
- 5the desk is made ___wood and the wine is made___rice
- 6(2013•安庆一模)我们唱卡拉OK时,要用到话筒.如图是动圈式话筒构造示意图,其工作原理是______.
- 7不等式(4-3x)(2x+1)/(x-1)^2大于等于0的解集是多少?
- 812.下列现象中属于势能转化为动能的例子是( )
- 9— I hear the plane of MH370 has been found!
- 10食堂运来大米100袋,面粉50袋.运来面粉是大米的百分之几
- 11(2010•常德)计算:(−12)0+(−2)3+(13)−1+|−2|.
- 12变频器FED,REV,
- 13填方位词补全对话 1.where is hardin? it.s in the () of china 2.where
- 14德语中 spr str 开头的单词,r到底发不发音?我看到有人说sp st 后接辅音字母 此为r,辅音字母不发音?
- 1535.76-6.75=2.1 简算
