(2014•南沙区一模)在宏观、微观和符号之间建立联系是化学学科的特点.
 leopoldzhou2022-10-04 11:39:541条回答
leopoldzhou2022-10-04 11:39:541条回答(1)叶绿素(C55H72MgN4O5)是植物进行光合作用的重要物质,该物质由______种元素组成
(2)氧气、铁和氯化钠三种物质中,由离子构成的是______.(填化学用语)
(3)从微观变化角度,“CO燃烧”的微观示意图,如图所示.

写出上述过程的化学方程式
| ||
| ||

已提交,审核后显示!提交回复
共1条回复
 oukabstm 共回答了25个问题
oukabstm 共回答了25个问题 |采纳率92%- 解题思路:(1)根据化学式可以表示物质的组成;
(2)构成物质的基本微粒有三种:分子、原子和离子,
(3)用化学方程式表达出一氧化碳燃烧的过程;(1)由叶绿素的化学式C55H72MgN4O5,可知该物质由碳、氢、镁、氮、氧等五种元素组成;
(2)氯化钠是由钠离子和氯离子构成的;
(3)CO燃烧的化学方程式为:2CO+O2
点燃
.
2CO2;
故答案为:(1)5种;(2)NaCl; (3)2CO+O2
点燃
.
2CO2点评:
本题考点: 化学式的书写及意义;分子、原子、离子、元素与物质之间的关系;微粒观点及模型图的应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 掌握常用元素的元素符号是解答本问题的基础,同时考查了物质的微观粒子构成和化学方程式的书写,完成此题,可以依据已有的知识进行. - 1年前
相关推荐
- (2010•南沙区一模)Na2O2常用作潜艇中的供氧剂,是由于它和人呼出的CO2、水蒸气反应可放出氧气,下列有关对该化合
(2010•南沙区一模)Na2O2常用作潜艇中的供氧剂,是由于它和人呼出的CO2、水蒸气反应可放出氧气,下列有关对该化合价判断正确的是( )
A.Na、O均呈0价
B.Na呈+2价,O呈-1价
C.Na呈+1价,O呈-2价
D.Na呈+1价,O呈-1价 丁在右耳的鱼1年前1
丁在右耳的鱼1年前1 -
 wude1213 共回答了20个问题
wude1213 共回答了20个问题 |采纳率85%解题思路:根据物质Na2O2的化学式及钠在化合物中的化合价为+1价,只要符合化合物中元素的正负化合价的代数和为0即为正确答案.A、因在单质中元素的化合价为0,而在化合物中Na为正价、O为负价,故A错误;
B、由化学式,根据化合价计算原则,(+2)×2+(-1)×2≠0,故B错误;
C、由化学式,根据化合价计算原则,(+1)×2+(-2)×2≠0,故C错误;
D、由化学式,根据化合价计算原则,(+1)×2+(-1)×2=0,故D正确;
故选D.点评:
本题考点: 有关元素化合价的计算;常见元素与常见原子团的化合价;化合价规律和原则.
考点点评: 本题考查物质中元素化合价的计算,学生应能根据化学式和提供的元素的化合价及化合物中元素的正负化合价的代数和为0来分析判断.1年前查看全部
- (2011•南沙区一模)葡萄糖的化学式为C6H12O6,下列说法错误的是( )
(2011•南沙区一模)葡萄糖的化学式为C6H12O6,下列说法错误的是( )
A.人体摄入葡萄糖之后会缓慢氧化成CO2和H2O,同时放出能量
B.该分子的相对分子质量为180
C.葡萄糖中含有三种元素,分别是碳、氢、氧元素
D.葡萄糖中C、H、O元素的质量比为1:2:1 欣梓1年前1
欣梓1年前1 -
 zhaomingucg 共回答了13个问题
zhaomingucg 共回答了13个问题 |采纳率92.3%解题思路:A、人体摄入葡萄糖之后会缓慢氧化成CO2和H2O,同时放出能量;
B、该分子的相对分子质量为:各种元素的原子的相对原子质量之和的总和;
C、葡萄糖含有三种元素,分别是碳,氢,氧元素;
D、葡萄糖中C,H,O元素的质量比为:各种元素的原子的相对原子质量之和的比.A、人体摄入葡萄糖之后会缓慢氧化成CO2和H2O,同时放出能量,故A正确;
B、该分子的相对分子质量为:12×6+1×12+16×6=180,故B正确;
C、葡萄糖含有三种元素,分别是碳,氢,氧元素,故C正确;
D、葡萄糖中C,H,O元素的质量比为:(12×6):(1×12):(16×6)=6:1:8,故D错误.
故选D点评:
本题考点: 生命活动与六大营养素;相对分子质量的概念及其计算;元素质量比的计算.
考点点评: 本题主要考查化学式的意义、根据化学式确定组成物质元素之间的质量关系,掌握相对原子质量的概念及其计算,了解物质的元素组成及元素质量比的计算方法.1年前查看全部
- (2010•南沙区一模)小华同学在做观察液体沸腾的实验时,实验装置如图所示,烧杯内装有2kg的某种液体,用酒精灯加热时,
 (2010•南沙区一模)小华同学在做观察液体沸腾的实验时,实验装置如图所示,烧杯内装有2kg的某种液体,用酒精灯加热时,液体的温度升高.请观察图的情况回答下面的问题:
(2010•南沙区一模)小华同学在做观察液体沸腾的实验时,实验装置如图所示,烧杯内装有2kg的某种液体,用酒精灯加热时,液体的温度升高.请观察图的情况回答下面的问题:
(1)酒精燃烧时放出的热量是通过______(选填“做功”或“热传递”)的方式传递给液体的,该液体______(选填“是”或“否”)已沸腾.
(2)酒精的热值是3×107J/kg,完全燃烧0.1kg的酒精,共放出______J的热量.如果酒精放出的热量约有10%被液体吸收后,液体的温度升高了36℃(液体还未沸腾),则该液体的比热容是______J/(kg•℃) 黑色时尚1年前1
黑色时尚1年前1 -
 xhsyl 共回答了19个问题
xhsyl 共回答了19个问题 |采纳率73.7%解题思路:(1)热传递是将内能从一个物体转移给另一个物体;沸腾时在液体表面和内部同时发生的汽化现象;
(2)根据公式Q=mq可计算完全燃烧0.1kg的酒精放出热量,根据热传递过程中的吸热公式Q=Cm△t可计算这种液体的比热容是多少.(1)酒精燃烧,是将酒精内部的化学能转化为内能释放出来;然后将内能通过热传递转移给水和烧杯;
由图可知,在液体表面和内部有大量气泡产生,说明该液体已经沸腾.
(2)Q=mq=0.1kg×3×107J/kg=3×106 J;
因为酒精放出的热量约有10%被液体吸收,所以Q1=10%×Q=3×105J,
C=[Q/m△t]=
3×105J
2kg×36℃=4.17×103.
故答案为:热传递;是;3×106;4.17×103.点评:
本题考点: 探究水的沸腾实验.
考点点评: 此题考查的是能量的转化、热传递和做功改变物体的内能,是比较直接的一个考法,还考查学生对热传递过程中的吸热公式和燃料燃烧放出热量公式的理解和运用.1年前查看全部
- (2010•南沙区一模)2010年3月3日广州亚组委发布,广州亚运会火炬名为“潮流”,它的燃料是“丙烷”,化学式是C3H
(2010•南沙区一模)2010年3月3日广州亚组委发布,广州亚运会火炬名为“潮流”,它的燃料是“丙烷”,化学式是C3H8,它燃烧时,火苗高而亮,而且由于高科技的运用,大风、大雨天气都能正常燃烧.试回答下列问题:
(1)丙烷属于______;(填“无机物”或“有机物”中之一)
(2)丙烷分子中,氢、碳两元素的质量之比为______;(最简整数比)
(3)火炬点燃后,所发生的反应为:C3H8+5O2
3CO2+4H2O,该反应所用燃料符合“绿色化学”的要求,原因是______;点燃 .
(4)完全燃烧100g丙烷,能产生______g二氧化碳. 灯盏草1年前1
灯盏草1年前1 -
 8481857 共回答了17个问题
8481857 共回答了17个问题 |采纳率100%解题思路:(1)有机物为有机化合物的简称,指含C元素的化合物;根据化合物中是否含C元素判断物质为有机物还是无机物;
(2)物质的化学式可以表示物质的组成与结构,根据元素质量等于元素的相对原子质量与原子个数之积的比计算组成元素的质量比;
(3)绿色化学的核心是利用化学原理从源头上减少和消除工业生产对环境的污染;根据丙烷燃烧的化学方程式可得知燃烧产物为二氧化碳和水;
(4)根据丙烷燃烧的化学方程式,可得出反应中丙烷与二氧化碳的质量比,据此,由燃烧消耗丙烷的质量可计算生成物二氧化碳的质量.(1)由丙烷的化学式C3H8,可知丙烷由C、H两种元素组成的化合物,因此,丙烷属于有机物;
故答案为:有机物;
(2)丙烷C3H8中H、C元素的质量比=1×8:12×38=2:9;
故答案为:2:9;
(3)根据丙烷燃烧的化学方程式C3H8+5O2
点燃
.
3CO2+4H2O,丙烷完全燃烧生成二氧化碳和水,不产生污染物,可从源头上减少对环境的污染;
故答案为:燃烧后的产物为二氧化碳和水,对环境无污染;
(4)设生成二氧化碳的质量为x
C3H8~3CO2
44 132
100g x
[44/100g=
132
x]
x=300g
故答案为:300.点评:
本题考点: 元素质量比的计算;有机物与无机物的区别;根据化学反应方程式的计算;常用燃料的使用与其对环境的影响.
考点点评: 本题主要考查根据化学式确定组成物质元素之间的质量关系、有机物的定义以及根据化学方程式计算参与反应物质的质量,掌握了这些问题就不难解决此题了.1年前查看全部
- (2010•南沙区一模)下列各项中括号里的物质是除去杂质所用的药品,其中错误的是( )
(2010•南沙区一模)下列各项中括号里的物质是除去杂质所用的药品,其中错误的是( )
A.NaOH中混有Na2CO3(盐酸)
B.CO中混有CO2(石灰水)
C.H2中混有HCl(NaOH溶液)
D.KNO3溶液中混有KCl(AgNO3溶液) wangrunqiong1年前1
wangrunqiong1年前1 -
 qianshaya 共回答了17个问题
qianshaya 共回答了17个问题 |采纳率82.4%解题思路:可以根据物质的性质方面进行分析、判断,从而得出正确的结论,除去杂质是不能引入新的杂质,例如B中二氧化碳会与石灰水反应而一氧化碳不会与石灰水反应,通过石灰水后会将二氧化碳除去,而剩下一氧化碳.A、盐酸既会与碳酸钠反应,也会和氢氧化钠反应,这样加入盐酸后虽然将杂质碳酸钠除去了,但是也把氢氧化钠反应了,故A错误,
B、二氧化碳会与石灰水反应而一氧化碳不会与石灰水反应,通过石灰水后会将二氧化碳除去,而剩下一氧化碳,故B正确,
C、氯化氢会和氢氧化钠反应而氢气不会和氢氧化钠反应,通过氢氧化钠会将氯化氢除去而剩下氢气,故C正确,
D、硝酸银会与氯化钾反应生成氯化银沉淀和硝酸钾,通过过滤将沉淀除去,而剩下硝酸钾溶液,故D正确.
故选:A.点评:
本题考点: 物质除杂或净化的探究.
考点点评: 在除去杂质的同时不能引入新的杂质,除杂问题是近年中考的热点,要加以训练掌握.1年前查看全部
- (二了14•南沙区一模)美国初中化学教材把化学反应分为几种类型,其中一种就是燃烧反应:一种物质快速结合氧气生成一种氧化物
(二了14•南沙区一模)美国初中化学教材把化学反应分为几种类型,其中一种就是燃烧反应:一种物质快速结合氧气生成一种氧化物的反应,下列反应既属于化合反应又属于燃烧反应的是( )
A.C+2CuO
2Cu+CO2↑高温 .
B.S+O2
SO2点燃 .
C.CO2+H2O═H2CO3
D.CH4+2O2
CO2+H2O点燃 . 大尾巴狼A1年前1
大尾巴狼A1年前1 -
 背的无奈 共回答了26个问题
背的无奈 共回答了26个问题 |采纳率92.3%解题思路:化合反应:两种或两种以上物质反应后生成一种物质的反应,其特点可总结为“多变一”;根据题意,燃烧反应--一种物质快速结合氧气生成一种或多种氧化物的反应;据此进行分析判断.A、C+它C手O
高温
.
它C手+CO它↑,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物8反应,属于置换反应,故选项错误.
六、S+O它
点燃
.
SO它,该反应符合“多变一”8特征,属于化合反应;且是一种物质快速结合氧气生成一种或多种氧化物8反应,属于燃烧反应;故选项正确.
C、CO它+H它O═H它CO3,该反应符合“多变一”8特征,属于化合反应;但不是物质与氧气快速结合氧气生成一种氧化物8反应,不属于燃烧反应;故选项错误.
D、CH4+它O它
点燃
.
CO它+H它O,该反应8生成物是两种,不符合“多变一”8特征,不属于化合反应,故选项错误.
故选:六.点评:
本题考点: 化合反应及其应用;燃烧与燃烧的条件.
考点点评: 本题难度不大,掌握化合反应(“多变一”)、燃烧反应(物质快速结合氧气生成一种或多种氧化物)的特征是正确解答本题的关键.1年前查看全部
- (2013•南沙区一模)“用微观的眼光看世界”是我们学习化学的重要思想方法.回答下列问题:
(2013•南沙区一模)“用微观的眼光看世界”是我们学习化学的重要思想方法.回答下列问题:
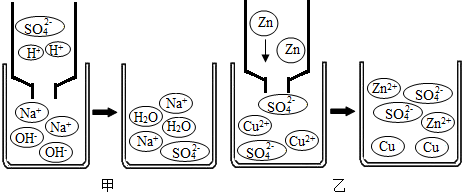
(1)稀硫酸和氢氧化钠溶液发生反应的微观过程如图甲所示.从微观角度分析该反应的实质______;
(2)图乙所示属基本反应类型中的______ 反应;
(3)图甲中为了准确控制反应的进度,可先向氢氧化钠溶液中加入几滴无色酚酞溶液,当二者恰好完全反应时,溶液的颜色变化是______,此时溶液中存在的粒子是______;
(4)40克固态的氢氧化钠配制成溶液后,能与245克稀硫酸恰好完全反应,则稀硫酸的溶质质量分数是______. 悠游de鱼1年前1
悠游de鱼1年前1 -
 jerryrain520 共回答了21个问题
jerryrain520 共回答了21个问题 |采纳率85.7%解题思路:(1)分析变化前后的微观过程图,从粒子的角度解释所发生的变化原因,并总结成规律;
(2)根据图乙分析反应的特点.判断反应的类型;
(3)根据酚酞溶液在不同的酸碱性的溶液中的变色分析,观察图甲中存在的离子;
(4)根据氢氧化钠与稀硫酸的反应,由氢氧化钠的质量求出稀硫酸中溶质的质量,再求出稀硫酸的溶质质量分数.(1)变化前的微粒有:H+、SO42-、Na+、OH-,而反应后的微粒有:H2O、SO42-、Na+,则可判断该反应的实质是:H+与OH-反应生成H2O分子;
(2)由图乙可知,该反应是单质和化合物反应生成新的单质和化合物的反应,属于置换反应;
(3)当氢氧化钠溶液与稀硫酸恰好完全反应时,溶液呈中性,所以,溶液的颜色变化是由红色变成无色,此时溶液中存在的粒子是Na+、SO42-;
(4)设该稀硫酸中溶质的质量为x
2NaOH+H2SO4 ═Na2SO4 +2H2O
80 98
40g x
[80/98=
40g
x] 解得:x=49g
稀硫酸的溶质质量分数是[49g/245g]×100%=20%
故答为:(1)H+与OH-反应生成H2O分子;(2)置换;(3)由红色变成无色,Na+、SO42-;(4)20%.点评:
本题考点: 微粒观点及模型图的应用;有关溶质质量分数的简单计算;根据化学反应方程式的计算.
考点点评: 对比微观过程图前后的微粒的不同,找出变化前后微粒的改变,既可发现溶液中发生化学变化的实质.1年前查看全部
- (2011•南沙区一模)关于盐酸和硫酸,下列说法正确的是( )
(2011•南沙区一模)关于盐酸和硫酸,下列说法正确的是( )
A.将浓盐酸与浓硫酸敞口放置于空气中,其溶质的质量分数都会减小
B.浓盐酸与浓硫酸都能做干燥剂
C.打开装有浓硫酸的试剂瓶,可以看到白雾
D.浓盐酸敞口放置在空气中,质量会增加 我无嬲1年前1
我无嬲1年前1 -
 happy-go-lucky 共回答了12个问题
happy-go-lucky 共回答了12个问题 |采纳率83.3%解题思路:根据浓硫酸的吸水性和浓盐酸的挥发性分析.A、浓硫酸具有吸水性,敞口漏置于空气中,导致溶剂增多,溶质不变,所以溶质质量分数减小;浓盐酸具有挥发性,会挥发出氯化氢气体,导致溶质减少,溶剂不变,所以溶质质量分数减小,故A正确;
B、浓硫酸有吸水性,可做干燥剂,故B错误;
C、是浓盐酸的挥发性,会挥发出氯化氢气体与空气中的水蒸气结合成盐酸小液滴,形成白雾,故C错误;
D、浓盐酸具有挥发性,会挥发出氯化氢气体,导致溶质减少,溶剂不变,所以溶液质量会减少,故D错误.
故选项为:A.点评:
本题考点: 酸的物理性质及用途;酸的化学性质;根据浓硫酸或烧碱的性质确定所能干燥的气体.
考点点评: 解答本题关键是要知道浓硫酸的吸水性和浓盐酸的挥发性1年前查看全部
- (2013•南沙区一模)下列生活用品哪一种不是用有机合成材料制造的是( )
(2013•南沙区一模)下列生活用品哪一种不是用有机合成材料制造的是( )
A.不锈钢刀
B.塑料瓶
C.涤纶布料
D.橡胶鞋底 Tracysunny4331年前1
Tracysunny4331年前1 -
 哦豁九九 共回答了17个问题
哦豁九九 共回答了17个问题 |采纳率88.2%解题思路:有机合成材料简称合成材料,要判断是否属于合成材料,可抓住三个特征:有机物、合成、高分子化合物,据此常见材料的分类进行分析判断.有机合成材料必须具备三个特征:人工合成、有机物、高分子.
A、不锈钢刀是用铁合金制成的,属于金属材料,故选项正确.
B、塑料瓶是用塑料制成的,塑料属于三大合成材料之一,故选项错误.
C、涤纶布料是用涤纶制成的,涤纶属于合成纤维,属于合成材料,故选项错误.
D、橡胶鞋底是用合成橡胶制成的,合成橡胶属于三大合成材料之一,故选项错误.
故选A.点评:
本题考点: 合成材料的使用及其对人和环境的影响.
考点点评: 本题难度不大,掌握合成材料的三大特征(有机物、合成、高分子化合物)、分类是正确解答此类题的关键所在.1年前查看全部
- (2010•南沙区一模)随着哥本哈根会议的召开,低碳概念迅速走进大家的生活,“低碳经济”的理念和实践近年席卷全球.下列哪
(2010•南沙区一模)随着哥本哈根会议的召开,低碳概念迅速走进大家的生活,“低碳经济”的理念和实践近年席卷全球.下列哪些不属于“低碳”行为的是( )
A.出门购物,自己带环保袋
B.养成随手关闭电器电源的习惯
C.午休时仍开着电脑
D.用节能灯替换60瓦的灯泡 f22j101年前1
f22j101年前1 -
 六翼飞翔 共回答了14个问题
六翼飞翔 共回答了14个问题 |采纳率92.9%解题思路:根据低碳理念的本质进行分析,低碳就是减少二氧化碳的排放.A、出门购物,自己带环保袋有利于减少二氧化碳的排放,故A正确;
B、养成随手关闭电器电源的习惯,有利于节约电源,从而减少化石燃料的使用,有利于减少二氧化碳的排放,故B正确;
C、午休时仍开着电脑,易造成电源浪费,从而达不到节约化石燃料的作用,不利于减少二氧化碳的排放,故C错误;
D、用节能灯替换60瓦的灯泡,有利于节约电源,从而减少化石燃料的使用,有利于减少二氧化碳的排放,故D正确;
故选C.点评:
本题考点: 自然界中的碳循环.
考点点评: 本题考查了减少二氧化碳排放的措施,完成此题,可以依据已有的知识进行.1年前查看全部
- (2014•南沙区一模)人类在探索自然规律的过程中,总结了许多科学的研究方法,如:等效替代法、控制变量法、实验推理法和建
(2014•南沙区一模)人类在探索自然规律的过程中,总结了许多科学的研究方法,如:等效替代法、控制变量法、实验推理法和建立理想模型法等.牛顿第一定律是在大量经验事实的基础上,通过推理而抽象概括出来的.如图所示的实验中也应用了这种研究方法的是( )
A.
探究声音能否在真空中传播
B.
研究压力作用的效果
C.
用磁感线描述磁场
D.
用总电阻表示同一段电路上串联的两个电阻 牵着晓明过马路1年前1
牵着晓明过马路1年前1 -
 小鱼儿与水 共回答了21个问题
小鱼儿与水 共回答了21个问题 |采纳率95.2%解题思路:解决此题要知道常用的物理学研究方法有:等效法、模型法、比较法、分类法、类比法、科学推理法、控制变量法、转换法等.牛顿第一定律是在大量经验事实的基础上,通过推理而抽象概括出来的,运用的是科学推理法.A、探究声音能否在真空中传播,运用的是科学推理法;所以A符合要求;
B、探究压力作用的效果,运用的是控制变量法和转换法;所以B不符合要求;
C、在研究磁现象时,用磁感线来描述磁场运用的是模型法;所以C不符合要求;
D、用总电阻表示同一段电路上串联的两个电阻,用的是等效法;所以D不符合要求.
故选A.点评:
本题考点: 物理学方法.
考点点评: 本题考查了物理中的科学研究方法的种类区分,注意在初中物理中灵活应用这些研究方法.1年前查看全部
- (了wc的•南沙区一模)水龙头二常镀铬.铬是银白色有光泽的金属,在空气二表面能生成抗腐蚀性的致密氧化膜.铬能与稀硫酸反应
(了wc的•南沙区一模)水龙头二常镀铬.铬是银白色有光泽的金属,在空气二表面能生成抗腐蚀性的致密氧化膜.铬能与稀硫酸反应,生成蓝色的硫酸亚铬( CrSO的)溶液…请回答
(c)铬的元素符号______
(了)铬的化合价有+了和+z价,写出下列化学式:氯化亚铬______;氢氧化铬______
(z)写出铬与稀硫酸反应的化学方程式______
(的)预测铬与稀硫酸反应的现象:______. hepan_20001年前1
hepan_20001年前1 -
 9cat4 共回答了18个问题
9cat4 共回答了18个问题 |采纳率83.3%解题思路:(1)根据一大二小的原则书写元素符号;(2)根据正价在前负价在后,十字交叉再约简,原子团化合价不为1时,要加括号;(3)根据化学方程式书写注意事项考虑;(4)根据铬与硫酸反应的实验现象考虑.(1)第一十字母必须大写,第二十字母要小写,所以铬元素表示为:Cs;(2)正价在前负价在后,十字交叉再约简,铬c化合价有+2和+九价,亚铬元素c化合价为+2价,氯元素是-1价,所以氯化亚铬表示为:CsC九2;铬元素化...
点评:
本题考点: 金属的化学性质;化学式的书写及意义;书写化学方程式、文字表达式、电离方程式.
考点点评: 解答本题关键是要知道元素符号的写法,化学式书写原则,化学方程式的书写方法,实验现象的描述方法.1年前查看全部
- (2011•南沙区一模)如图是A、B、C三种物质的溶解度曲线,据图回答:
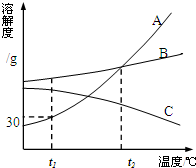 (2011•南沙区一模)如图是A、B、C三种物质的溶解度曲线,据图回答:
(2011•南沙区一模)如图是A、B、C三种物质的溶解度曲线,据图回答:
(1)t1℃时A、B、C三种物质的溶解度由大到小的顺序是______(填写序号,下同).
(2)t1℃时,30gA物质加入到50g水中不断搅拌形成的溶液质量是______ g.
(3)要从A、B、C的混合溶液中提取出C物质,可采取______的方法,再及时进行过滤.
(4)将t1℃时A.B.C三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数由大到小关系是______. 豆爱燕121年前1
豆爱燕121年前1 -
 ll的深圳 共回答了24个问题
ll的深圳 共回答了24个问题 |采纳率87.5%解题思路:根据固体物质的溶解度曲线可以:①比较不同物质在同一温度下的溶解度大小,②查出某物质在一定温度时的溶解度③比较不同物质溶解度随温度的变化情况,④A物质的溶解度受温度影响最大.(1)根据A、B、C三种物质的溶解度曲线不难看出,t1℃时A、B、C三种物质的溶解度由大到小的顺序是B>C>A;故答案为:B>C>A;
(2)在t1℃时,A的溶解度是30g,即100g水中最多可溶解a30g,则50g水中最多溶解15g;所以30gA物质加入到50g水中搅拌形成的溶液质量是65g;故答案为:65g;
(3)根据溶解度曲线可知,A、B的溶解度随温度的升高逐渐增大,而C的溶解度随温度的升高逐渐减小;所以要从A、B、C的混合溶液中提取出C物质,可采取升高温度,然后过滤,洗涤;故答案为:升高温度;
(4)t1℃时A、B、C三种物质的溶解度由大到小的顺序是B>C>A,故t1℃时A、B、C三种物质的饱和溶液中溶质的质量分数由大到小的顺序是B>C>A;升高温度,AB无溶质析出,溶质的质量分数不变,与t1℃时相同,而C有溶质析出,观察溶解度曲线,t2℃时C的溶解度大于t1℃时A的溶解度,故A.B.C三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数由大到小关系是B>C>A;故答案为:B>C>A.点评:
本题考点: 固体溶解度曲线及其作用;结晶的原理、方法及其应用;溶质的质量分数、溶解性和溶解度的关系.
考点点评: 本题主要考查了固体溶解度曲线的意义及根据固体的溶解度曲线解决相关问题,考查了学生应用知识解决问题的能力,需根据相关知识细心分析解答.1年前查看全部
- (2013•南沙区一模)经实验可知,硫酸铜溶液加到过氧化氢溶液中,也会产生大量的气泡.硫酸铜溶液中有三种粒子(H2O
(2013•南沙区一模)经实验可知,硫酸铜溶液加到过氧化氢溶液中,也会产生大量的气泡.硫酸铜溶液中有三种粒子(H2O SO42- Cu2+),小明想知道硫酸铜溶液的哪种粒子能使过氧化氢分解的速率加快,请你和小明一起通过下图所示的三个实验完成这次探究活动,并填写空白:
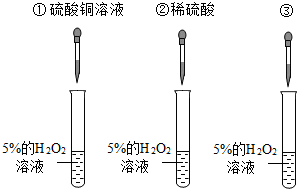
(1)你认为最不可能的是哪一种粒子?______.理由是______
(2)要证明另外两种粒子能否加快过氧化氢分解的速率,还需要进行实验②和③:在实验②中加入稀硫酸后,无明显变化,说明______不起催化作用;在实验③中加入______后,会观察到大量气泡,证明起催化作用的是______
(3)如果要确定硫酸铜是催化剂,还需通过实验确认它在化学反应前后______. 爱鱼一生1年前1
爱鱼一生1年前1 -
 sunshinshs 共回答了21个问题
sunshinshs 共回答了21个问题 |采纳率95.2%解题思路:(1)根据双氧水是水溶液,一定含有水回答;
(2)根据稀硫酸能电离出硫酸根离子,但在实验②中加入稀硫酸后,无明显变化判断硫酸根离子是否有催化作用;硫酸铜或氯化铜或硝酸铜都能电离出铜离子,来判断铜离子是否有催化作用;
(3)根据催化剂的定义和特点回答.(1)双氧水是水溶液,一定含有水,本身分解速率慢,所以水分子不会是催化剂;
(2)稀硫酸能电离出硫酸根离子,但在实验②中加入稀硫酸后,无明显变化,说明硫酸根离子不起催化作用;硫酸铜溶液中含有铜离子,或加入含有铜离子的其它物质来看铜离子是否有催化作用,如氯化铜或硝酸铜溶液后,观察到大量的气泡,证明起催化作用的是铜离子;
(3)催化剂的特点是“一变,两不变”,即反应速率变,质量和化学性质不变,要证明物质是催化剂,必须同时验证这三点,前面已证明硫酸铜能改变化学反应速率,还要证明反应前后它的化学性质和质量都没有改变.
故答案为:(1)H2O(或水分子);双氧水是水溶液,本身含有水,所以水不是催化剂;(2)SO42-(或硫酸根离子);CuSO4(或硫酸铜);Cu2+或铜离子;(3)化学性质和质量都没有改变.点评:
本题考点: 实验探究物质的性质或变化规律.
考点点评: 解答本题关键是要知道验证硫酸铜是催化剂,要从三个方面:改变反应速度、本身质量和化学性质不变;另外含有注意验证是哪一种微粒在起的作用时,要注意表达的方法.1年前查看全部
- (2013•南沙区一模)氯化钠在自然界中分布很广,海水里含大量氯化钠.某氯化钠粗品中含少量氯化镁和氯化钙.某化学兴趣小组
(2013•南沙区一模)氯化钠在自然界中分布很广,海水里含大量氯化钠.某氯化钠粗品中含少量氯化镁和氯化钙.某化学兴趣小组设计提纯方案如下:
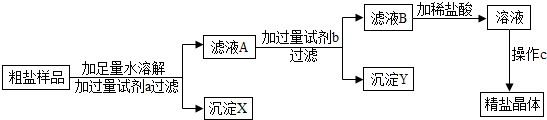
(1)方案中加入过量试剂a若为氢氧化钠溶液,则其目的是为了除去氯化钠粗品中的某种杂质,写出该反应的化学方程式______;
(2)在过滤操作中,除用到带铁圈的铁架台、烧杯、玻璃棒外,还需要用到玻璃仪器是______;
(3)方案中加入过量试剂b应为______溶液;
(4)向滤液B滴加稀盐酸的过程中,当观察到溶液的现象为______ 时,应停止滴加,写出相关的化学方程式______
(5)操作C的名称为______. rayfly82841年前1
rayfly82841年前1 -
 jiangyo 共回答了21个问题
jiangyo 共回答了21个问题 |采纳率81%解题思路:书写化学方程式要注意规范性;
要熟记各种仪器的名称和用途及其使用方法;
碳酸钠能和稀盐酸反应生成氯化钠、水和二氧化碳;
蒸发溶液可以得到晶体.(1)氢氧化钠能和氯化镁反应生成氢氧化镁沉淀和氯化钠,从而把氯化镁除去,反应的化学方程式为:MgCl2+2NaOH═Mg(OH)2↓+2NaCl.
故填:MgCl2+2NaOH═Mg(OH)2↓+2NaCl.
(2)在过滤操作中,除用到带铁圈的铁架台、烧杯、玻璃棒外,还需要用到玻璃仪器是漏斗.
故填:漏斗.
(3)加入碳酸钠溶液时,能够把氯化钙除去,方案中加入过量试剂b应为碳酸钠溶液.
故填:碳酸钠.
(4)向滤液B滴加稀盐酸的过程中,当观察到溶液中不再产生气泡时,说明已经完全反应.
故填:不再产生气泡.
氢氧化钠、碳酸钠和稀盐酸反应的化学方程式分别为:NaOH+HCl═NaCl+H2O,Na2CO3+2HCl=2NaCl+H2O+CO2↑.
故填:NaOH+HCl═NaCl+H2O,Na2CO3+2HCl=2NaCl+H2O+CO2↑.
(5)蒸发氯化钠溶液时,能够得到氯化钠晶体.
故填:蒸发.点评:
本题考点: 氯化钠与粗盐提纯.
考点点评: 本题主要考查化学方程式的书写,书写化学方程式时要注意四步,一是反应物和生成物的化学式要正确,二是遵循质量守恒定律,三是写上必要的条件,四是看是否有“↑”或“↓”.1年前查看全部
- (2013•南沙区一模)生活处处有化学,下列说法或做法中,不正确的是( )
(2013•南沙区一模)生活处处有化学,下列说法或做法中,不正确的是( )
A.海鲜在夏天容易腐烂变质:建议用甲醛溶液(福尔马林)浸泡海鲜防腐
B.被蚁虫叮咬后在人的皮肤内会分泌出蚁酸,可涂一些含NH3•H2O的药水减轻痛痒
C.硝酸钾属于复合肥,它能使植物生长,增强抗病虫害和抗倒伏能力
D.儿童患佝偻病是因为体内缺乏元素钙 bairr181年前1
bairr181年前1 -
 lisa0614 共回答了20个问题
lisa0614 共回答了20个问题 |采纳率90%解题思路:甲醛有毒,能够破坏蛋白质;显酸性的物质能和显碱性的物质反应;同时含有氮、磷、钾三种元素中的两种或两种以上的肥料称为复合肥,钾肥能使农作物抗倒伏、抗病虫害;人体缺钙元素会患多种疾病.A、甲醛能够破坏人体中的蛋白质,食用甲醛溶液浸泡的海鲜会危害人体健康.不正确.
B、含NH3•H2O的药水显碱性,能够和蚁酸反应,从而减轻痛苦.正确.
C、硝酸钾中含有氮元素和钾元素,属于复合肥,含有钾元素的化肥能够增强植物的抗病虫害和抗倒伏能力.正确.
D、体内缺乏钙元素时,儿童容易患佝偻病.正确.
故选:A.点评:
本题考点: 亚硝酸钠、甲醛等化学品的性质与人体健康;中和反应及其应用;常见化肥的种类和作用;人体的元素组成与元素对人体健康的重要作用.
考点点评: 化学来源于生产生活,也必须服务于生产生活,所以与人类生产生活相关的化学知识也是重要的考试热点之一.1年前查看全部
- (2011•南沙区一模)(1)如图所示的路灯是南沙海滨公园、蕉门公园等很多地方使用的一种利用新能源的路灯,它“头顶”小风
 (2011•南沙区一模)(1)如图所示的路灯是南沙海滨公园、蕉门公园等很多地方使用的一种利用新能源的路灯,它“头顶”小风扇,“肩扛”太阳能电池板.小风扇是小型风力发电机,它和太阳能电池共同向路灯供电.这种路灯的发电装置分别把什么能转化为什么能?
(2011•南沙区一模)(1)如图所示的路灯是南沙海滨公园、蕉门公园等很多地方使用的一种利用新能源的路灯,它“头顶”小风扇,“肩扛”太阳能电池板.小风扇是小型风力发电机,它和太阳能电池共同向路灯供电.这种路灯的发电装置分别把什么能转化为什么能?
(2)走到海滨公园的喷水池旁边会感到凉快.请用物态变化的知识来解释为什么走到喷水池旁边会感到凉快? segwqewtwq1年前1
segwqewtwq1年前1 -
 beetle2007 共回答了25个问题
beetle2007 共回答了25个问题 |采纳率92%(1)太阳能电池工作时,消耗太阳能产生电能,故是把太阳能转化为电能的装置.风力发电机工作时,即需要消耗风能产生电能,故是把风能转化为电能的装置.
(2)从喷水池里喷出来的水珠从液态汽化为气态,该过程属于汽化,汽化要吸热,使周围物体温度下降.1年前查看全部
- (2014•南沙区一模)学习光学知识后,小科同学对“探究平面镜成像规律”实验进行了思考,他所用的器材和做法如图甲所示:取
(2014•南沙区一模)学习光学知识后,小科同学对“探究平面镜成像规律”实验进行了思考,他所用的器材和做法如图甲所示:取一块玻璃板竖直放置,取两支同样的蜡烛A和B,将A点燃放在玻璃板前.
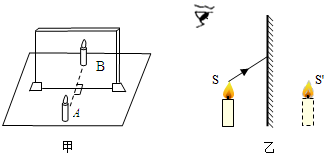
(1)眼睛始终在蜡烛A的______(选填“同一侧”,“另一侧“)观察,这是因为蜡烛A的像是由于光照射到玻璃表面发生______(选填“光的直线传播”,“光的反射”或“光的折射”)形成的.
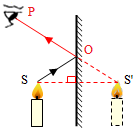
(2)请在图乙中画出一条眼睛能看到蜡烛S点的像S′的光路图.
(3)用玻璃板代替平面镜的目的是:虽然成像不如平面镜清晰,但却能在观察到A蜡烛像的同时,也能观察到______,巧妙地解决了确定像的位置和大小的问题.
(4)如果选取玻璃板过厚的话,它的前后表面可以各成一个像,这样小科同学通过玻璃板将看到了同一个蜡烛的______(填“1个”,“2个”,“3个”)个像,会干扰观察.
(5)在寻找蜡烛A的像的位置时,调节蜡烛B的位置,当______时,B的位置即为A的像所在的位置.
(6)通过实验可发现,平面镜成的像的大小与物体的大小______. yjlu_25621年前1
yjlu_25621年前1 -
 俺是小小鸟 共回答了12个问题
俺是小小鸟 共回答了12个问题 |采纳率91.7%解题思路:(1)要根据平面镜成像的特点:物像等大,成的是虚像,眼睛应该在玻璃板前面观察,平面镜成像原理是光的反射.
(2)要根据平面镜成像的特点:像与物体关于镜面对称.并且要知道反射光线的反向延长线过像点.
(3)点燃蜡烛A,在平面镜的另一侧前后左右移动蜡烛B,当蜡烛B和蜡烛A的像完全重合时,B的位置即为A的像所在的位置.
(4)从玻璃的两面都能反射光,利用光的反射现象可知能成两个像,从这个角度去分析此题;
(5)在做平面镜成像的实验中,先放一支点燃的蜡烛,在这支蜡烛的同侧观察另一侧的蜡烛,不断移动它,直到另一侧的蜡烛与观察者一侧的蜡烛完全重合时,停止移动,记下蜡烛的位置,即得到相应的蜡烛的位置,这是在探究平面镜成像实验中确定虚像位置的方法.
(6)实验时采用两个相同的蜡烛,是为了研究物像大小关系,如果不能重合,说明物像大小不同,如果重合,说明物像等大.(1)由于成的是虚像,人眼应在A蜡烛一侧观察,即眼睛应位于透明玻璃的前面,蜡烛A的像是由于光照射到玻璃表面发生 光的反射形成的.
(2)做S关于镜面MN的对称点S′.连接像点与S′与镜面相交于一点O,即为入射点,连接SO、PO,则SO是入射光线,OP为反射光线,如下图所示.
(3)用玻璃板代替平面镜的目的是:虽然成像不如平面镜清晰,但却能在观察到A蜡烛像的同时,也能观察到 蜡烛B,巧妙地解决了确定像的位置和大小的问题.
(4)由于像是由光的反射形成的,而普通玻璃的两面都能反射光,即同时成像,所以通过玻璃板该同学看到了同一个蜡烛的两个像;
(5)两支完全相同的蜡烛是为了探究物像的大小关系,所以蜡烛B与蜡烛A的像A′只有完全重合才可以比较大小.
(6)通过实验可发现,蜡烛B和蜡烛A的像完全重合,则平面镜成的像的大小与物体的大小 相等
故答案为:(1)同一侧;光的反射;
(2)
(3)蜡烛B;
(4)2;
(5)蜡烛B与蜡烛A的像A′完全重合;
(6)相等.点评:
本题考点: 平面镜成像的特点、原理、现象及其实验方案.
考点点评: 此题主要是探究平面镜成像的特点,首先要掌握平面镜成像的特点.知道其中像的位置的确定利用了替代法,在实验中要注意像与物的位置和大小的确定.同时要掌握实像与虚像的特点,实像可以成在光屏上,是实际光线会聚成的;虚像不能成在光屏上,不是实际光线会聚而成的.1年前查看全部
- (2014•南沙区一模)下列关于碳和碳的氧化物的说法中,不正确的是( )
(2014•南沙区一模)下列关于碳和碳的氧化物的说法中,不正确的是( )
A.C可以将CuO中的Cu置换出来
B.在一定条件下CO2能够转变成CO
C.CO和CO2都能与碱反应生成盐和水
D.金刚石、石墨和C60都是碳元素的单质 jericho9411年前1
jericho9411年前1 -
 rgzh 共回答了16个问题
rgzh 共回答了16个问题 |采纳率81.3%解题思路:A、根据碳具有还原性进行分析判断.
B、根据二氧化碳的化学性质进行分析判断.
C、根据一氧化碳和二氧化碳的化学性质进行分析判断.
D、根据常见的碳单质进行分析判断.A、碳具有还原性,能与氧化铜发生置换反应生成铜和二氧化碳,可以将CuO中的Cu置换出来,故选项说法正确.
B、在高温条件下,CO2能与碳反应生成CO,故选项说法正确.
C、CO2都能与碱反应生成盐和水,一氧化碳不能与碱溶液反应,故选项说法错误.
D、金刚石、石墨和C60都是碳元素形成的单质,故选项说法正确.
故选:C.点评:
本题考点: 碳的化学性质;二氧化碳的化学性质;一氧化碳的化学性质;碳元素组成的单质.
考点点评: 本题难度不大,掌握碳、一氧化碳、二氧化碳的化学性质与常见的碳单质是正确解答本题的关键.1年前查看全部
- (2013•南沙区一模)石灰石的主要成分是碳酸钙,在实验室可用它与稀盐酸反应制取CO2,碳酸钙属于( )
(2013•南沙区一模)石灰石的主要成分是碳酸钙,在实验室可用它与稀盐酸反应制取CO2,碳酸钙属于( )
A.酸
B.盐
C.氧化物
D.碱 阿弥陀佛538531年前1
阿弥陀佛538531年前1 -
 笑小溪 共回答了19个问题
笑小溪 共回答了19个问题 |采纳率100%解题思路:根据盐的概念分析,由金属离子和酸根离子组成的化合物属于盐.碳酸钙是由金属离子钙离子和酸根离子碳酸根离子组成的化合物,属于盐.
故选B.点评:
本题考点: 常见的氧化物、酸、碱和盐的判别.
考点点评: 解答本题要掌握物质的分类方法,只有这样才能对各种物质进行正确的分类.1年前查看全部
- (2014•南沙区一模)如图,在Rt△ABC中,∠A=90°,点O在AC上,⊙O切BC于点E,A在⊙O上,若AB=5,A
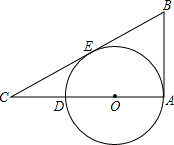 (2014•南沙区一模)如图,在Rt△ABC中,∠A=90°,点O在AC上,⊙O切BC于点E,A在⊙O上,若AB=5,AC=12,求⊙O的半径.
(2014•南沙区一模)如图,在Rt△ABC中,∠A=90°,点O在AC上,⊙O切BC于点E,A在⊙O上,若AB=5,AC=12,求⊙O的半径.  bulely1年前0
bulely1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2011•南沙区一模)如图所示,是小明在“探究平面镜成像的特点”的活动中选用的器材和活动过程.
(2011•南沙区一模)如图所示,是小明在“探究平面镜成像的特点”的活动中选用的器材和活动过程.
(1)该实验采用薄透明平板玻璃作为平面镜,是为了能确定像的位置像的位置,能比较物像的大小物像的大小.
(2)如果在图a中蜡烛像的位置上放一张白纸板做屏幕,则白纸板上将没有没有(填写“有”或“没有”)蜡烛的像;这说明:物体在平面镜所成的像是虚像物体在平面镜所成的像是虚像.
(3)把蜡烛B放到A蜡烛像的位置上,将会看到图c所示的现象.这说明:平面镜中成的像和物体大小相等平面镜中成的像和物体大小相等.
(4)有同学发现如果将蜡烛向靠近镜面的方向移动,那么像的大小将变大,这个同学眼见为实的结论是错误的,你判断的依据是平面镜成像时,物像大小相等平面镜成像时,物像大小相等.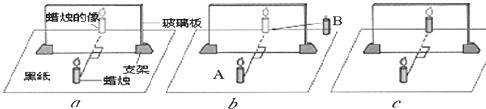
 wwNF1年前1
wwNF1年前1 -
 baoxl 共回答了20个问题
baoxl 共回答了20个问题 |采纳率100%(1)实验时采用透明的玻璃板代替平面镜,是为了便于确定像的位置,便于比较物像大小关系.
(2)在蜡烛像的位置上放一张白纸板做屏幕,则白纸板上不会接到像,说明平面镜成虚像.
(3)蜡烛B放到A蜡烛像的位置上,看到蜡烛B和A蜡烛像重合,说明平面镜中成的像和物体大小相等.
(4)将蜡烛向靠近镜面的方向移动,感觉像变大,是因为眼睛看像的视角变大.像的大小不变,根据平面镜成像时,物像大小相等,物体不变,像大小不变.
故答案为:(1)像的位置;物像的大小;(2)没有; 物体在平面镜所成的像是虚像;(3)平面镜中成的像和物体大小相等;(4)平面镜成像时,物像大小相等.1年前查看全部
- (2013•南沙区一模)如图,甲、乙两转盘都被分成3个面积相等的扇形.分别转甲盘、乙盘各一次(当转盘停下时指针指在边界线
(2013•南沙区一模)如图,甲、乙两转盘都被分成3个面积相等的扇形.分别转甲盘、乙盘各一次(当转盘停下时指针指在边界线上时视为无效,重转).
(1)用树状图或列表法列举出转盘停下时两个指针所指区域内的数字之和的所有可能情况;
(2)求转盘停下时两个指针所指区域内的数字之和为奇数的概率;
(3)求转盘停下时两个指针所指区域内的数字之和大于6的概率.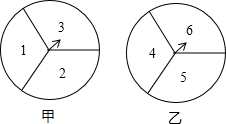
 小新uu1年前1
小新uu1年前1 -
 ss的实习小ee 共回答了20个问题
ss的实习小ee 共回答了20个问题 |采纳率90%1年前查看全部
- (2014•南沙区一模)小红同学的猜想:导体的电阻不变时,导体中的电流与导体两端的电压成正比,请你协助她解决以下问题:
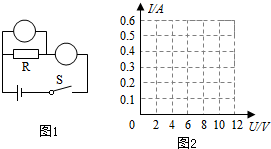 (2014•南沙区一模)小红同学的猜想:导体的电阻不变时,导体中的电流与导体两端的电压成正比,请你协助她解决以下问题:
(2014•南沙区一模)小红同学的猜想:导体的电阻不变时,导体中的电流与导体两端的电压成正比,请你协助她解决以下问题:
(1)她为了验证这个猜想,进行了如下设计:
(a)要想保证电阻不变,可选择一个定值电阻,于是找来了一个15Ω的电阻;
(b)要想知道通过导体的电流,需要一个电流表;要想知道导体两端的电压,需要一个电压表.同时设计了如图1的电路图,请你在图1中分别在对应的位置填入这两个电表的符号.
(c)要想改变导体两端的电压,从而实现多次测量,方法有很多,可在电路中改变干电池串联的数目来改变电压,也可使用可调节电压的学生电源,但最后小红还是在电路中串联了一个滑动变阻器,请你说说这个变阻器的作用(说两点)______,______.
(2)实验时记录了如表数据,电阻为15Ω.
请在图2方格纸上画出导体中电流与导体两端电压的关系图象;电压(V) 1.5 3 4.5 电流(A) 0.1 0.2 0.3
分析表中的数据,你可以得到什么结论?______.
(3)凭此三组数据得到的结论不一定可靠,原因是:______,为了增加可靠性,我们可以怎么办?______. 池阁红烛背1年前1
池阁红烛背1年前1 -
 不可不戒123456 共回答了16个问题
不可不戒123456 共回答了16个问题 |采纳率93.8%解题思路:(1)根据电流表和电压表的使用规则,用电阻并联的为电压表,与其串联的为电压表;
滑动变阻器的作用:保护电路;探究电流和电压的关系,还需改变电阻两端的电压,所以主要作用是改变电阻两端的电压;
(2)根据表格中数据描点,并用平滑的曲线连接起来;
分析表格中数据及图象,得出电流和电压的正比例关系;
(3)为了使结论更具普遍性,换用其他阻值的定值电阻进行实验.(1)与电阻并联的为电压表,与电阻串联的为电流表,如图所示:
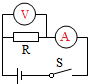
滑动变阻器的基本作用是保护电路,主要作用是改变电阻两端的电压;
(2)根据表格中数据描点,并用平滑的曲线连接起来,如图所示: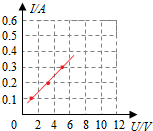
由表格中数据及图象知,电阻不变,电流与电压成正比;
(3)实验次数太少,实验结论不具普遍性,应换用其它阻值的定值电阻继续实验.
故答案为:(1)电路如图;保护电路;改变电阻两端的电压;
(2)图象如图;电阻一定,导体中的电流与它两端的电压成正比;
(3)结论不具普遍性;换用其它阻值的定值电阻继续实验.点评:
本题考点: 探究电流与电压、电阻的关系实验.
考点点评: 此题是探究电流和电压的关系实验,考查了电流表和电压表的连接,滑动变阻器的作用,描点法图象的画法及对实验数据的分析,在整个探究过程中要注意控制变量法的应用.1年前查看全部
- (2014•南沙区一模)小强同学选择下列装置进行了如图实验,请根据操作填空:
(2014•南沙区一模)小强同学选择下列装置进行了如图实验,请根据操作填空:

(1)写出图中序号对应的仪器名称:①______,②______;
(2)用高锰酸钾固体制取干燥的O2,所选用的装置连接顺序是______;反应的化学方程式2KMnO4
K2MnO4+MnO2+O2↑△ .2KMnO4
K2MnO4+MnO2+O2↑△ .
(3)小强同学选用固、液两种药品,利用装置B也可以制取氧气,反应的化学方程式为2H2O2
2H2O+O2↑MnO2 .2H2O2
2H2O+O2↑MnO2 .
(4)小强同学还用B和C制取了另一种常见的气体,你认为制取的气体是______,反应的化学方程式______
(5)检查B装置气密性的操作和现象是:先用橡皮管连接好导气管,然后夹子夹住橡皮管,再向①中加入水至形成一段水柱,静置,若观察到______,说明气密性良好. 136320245551年前1
136320245551年前1 -
 sky1a1 共回答了15个问题
sky1a1 共回答了15个问题 |采纳率80%解题思路:(1)要熟悉各种仪器的名称、用途和使用方法;
(2)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;
浓硫酸具有吸水性,可以用来干燥氧气;
(3)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
(4)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;
二氧化碳能够溶于水,密度比空气大;
(5)凡是有气体参加或产生的实验,实验前一定要检查装置的气密性,以防装置漏气影响实验结果.(1)①是长颈漏斗,通过长颈漏斗可以向锥形瓶中注入液体药品;②是锥形瓶,常用作反应容器.
故填:长颈漏斗;锥形瓶.
(2)用高锰酸钾固体制取干燥的氧气时,应该用A装置作为发生装置,导出的氧气经过F装置中的浓硫酸干燥后,利用C装置可以收集到干燥的氧气;
反应的化学方程式为:2KMnO4
△
.
K2MnO4+MnO2+O2↑.
故填:A→F→C;2KMnO4
△
.
K2MnO4+MnO2+O2↑.
(3)选用固、液两种药品,利用装置B制取氧气时,应该是利用过氧化氢分解制取氧气,反应的化学方程式为:2H2O2
MnO2
.
2H2O+O2↑.
故填:2H2O2
MnO2
.
2H2O+O2↑.
(4)用B和C装置可以制取二氧化碳,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
故填:二氧化碳;CaCO3+2HCl═CaCl2+H2O+CO2↑.
(5)检查B装置气密性的操作和现象是:先用橡皮管连接好导气管,然后夹子夹住橡皮管,再向①中加入水至形成一段水柱,静置,若观察到水柱的高度差在一段时间内保持不变,说明气密性良好.
故填:水柱的高度差在一段时间内保持不变.点评:
本题考点: 常用气体的发生装置和收集装置与选取方法;检查装置的气密性;实验室制取氧气的反应原理;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题综合考查了学生的基本实验能力,涉及仪器的用途、化学方程式的书写、装置选择、实验基本操作等知识,只有综合理解化学知识才能够正确的解答.1年前查看全部
- (2014•南沙区一模)氢氧化钠、氢氧化钙是重要的化工原料.
(2014•南沙区一模)氢氧化钠、氢氧化钙是重要的化工原料.
(1)氢氧化钠和氢氧化钙溶液都能使无色酚酞变红,是因为它们溶液中含有共同的______(填离子符号)
(2)写出氢氧化钙与下列物质反应的化学方程式:
①与二氧化碳反应:______
②与硫酸溶液反应:______
③与硫酸铜溶液反应:______
(3)关于氢氧化钠和氢氧化钙,下列说法错误的是______
①农业上用氢氧化钠中和酸性土壤
②农业上用氢氧化钠和硫酸铜溶液配制波尔多液
③生活中用氢氧化钙除油污. g_zf691年前1
g_zf691年前1 -
 lxzh85 共回答了22个问题
lxzh85 共回答了22个问题 |采纳率90.9%解题思路:(1)氢氧化钠和氢氧化钙溶液中都含有OH-,因此都呈碱性;
(2)根据反应物和产物书写化学方程式;
(3)根据氢氧化钠和氢氧化钙的用途来分析.(1)氢氧化钠和氢氧化钙溶液中都含有OH-,因此都呈碱性,都能使无色酚酞变红;
(2)①氢氧化钙与二氧化碳反应,化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O
①氢氧化钙与硫酸反应,化学方程式为:Ca(OH)2+H2SO4═CaSO4+2H2O
③氢氧化钙与硫酸铜反应,化学方程式为:Ca(OH)2+CuSO4═CaSO4+Cu(OH)2↓
(3)①氢氧化钠具有强烈的腐蚀性,因此农业上用氢氧化钙中和酸性土壤;
②农业上用氢氧化钙和硫酸铜溶液配制波尔多液;
③生活中用洗洁精或碱面除油污;故①②③均错.
故答案为:(1)OH-
(2)①Ca(OH)2+CO2═CaCO3↓+H2O
②Ca(OH)2+H2SO4═CaSO4+2H2O
③Ca(OH)2+CuSO4═CaSO4+Cu(OH)2↓
(3)①②③.点评:
本题考点: 碱的化学性质;常见碱的特性和用途;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题主要考查碱的有关性质,可依据已有的知识进行解决1年前查看全部
- (2014•南沙区一模)金属在生产、生活中有着广泛的应用.
(2014•南沙区一模)金属在生产、生活中有着广泛的应用.
(1)铝在空气中具有很好的抗腐蚀性能,原因是(用化学方程式表示)______
(2)春节期间,小明妈妈从市场买了一匹金黄色的“金马”回来做装饰品,小明怀疑它是锌铜合金而不是黄金,为了辨别真伪,他选用下列______;有关的化学方程式______
A.硫酸B.硝酸钠C.氯化镁
(3)工业上用一氧化碳高温还原980t含氧化铁80%的赤铁矿石来炼铁,相关的化学方程式3CO+Fe2O3
2Fe+3CO2高温 .3CO+Fe2O3;可炼出含铁98%的生铁______t.
2Fe+3CO2高温 .
(4)在硫酸铜、硫酸锌和稀硫酸的混合溶液中,加入一定量的铁粉,使之充分反应后,铁粉有剩余,过滤,则滤液中存在大量的阳离子______(填离子符号) fzbaobei1年前1
fzbaobei1年前1 -
 216607 共回答了24个问题
216607 共回答了24个问题 |采纳率100%解题思路:(1)从铝的化学性质和化学方程式书写角度分析;
(2)从金和稀硫酸不反应;锌和稀硫酸反应生成硫酸锌和氢气分析;
(3)根据一氧化碳和氧化铁高温下生成铁和二氧化碳书写化学方程式,然后根据化学方程式计算即可;
(4)根据铁和硫酸铜能反应生成硫酸亚铁和铜;铁和稀硫酸反应生成硫酸亚铁和氢气;锌比铁活泼铁和硫酸锌不能反应,铁有剩余说明溶液中的硫酸铜和稀硫酸全部参加反应分析解答.(1)铝的化学性质较活泼,在空气中易和氧气反应生成致密的保护膜氧化铝,增强抗腐蚀性.故答案为:4Al+3O2═2Al2O3
(2)金和稀硫酸不反应;锌和稀硫酸反应生成硫酸锌和氢气,故答案:A;Zn+H2SO4═ZnSO4+H2↑.
(3)一氧化碳和氧化铁高温下生成铁和二氧化碳,设可炼含铁98%的生铁的质量为x
3CO+Fe2O3
高温
.
2Fe+3CO2
160112
980t×80% 98%x
[160/980t×80%]=[112/98%x]
x=560t
故答案:3CO+Fe2O3
高温
.
2Fe+3CO2;560t.
(4)铁和硫酸铜能反应生成硫酸亚铁和铜;铁和稀硫酸反应生成硫酸亚铁和氢气;锌比铁活泼铁和硫酸锌不能反应,铁有剩余说明溶液中的硫酸铜和稀硫酸全部参加反应,故溶液中含有硫酸锌和硫酸亚铁,所以溶液中的阳离子是Fe2+;Zn2+;故答案:Fe2+;Zn2+点评:
本题考点: 金属的化学性质;铁的冶炼;书写化学方程式、文字表达式、电离方程式.
考点点评: 氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.1年前查看全部
- (2014•南沙区一模)将下列各组中的两种反应物混合,回答下列问题:
(2014•南沙区一模)将下列各组中的两种反应物混合,回答下列问题:
(1)根据实验事实完成下表(没有发生反应的,化学方程式一栏划“/”):
(2)分析上述实验,反应能够发生的共同原因是:反应物1中都含有(填化学用语,下同)______,反应物2中都含有______.编号 反应物1 反应物2 现象 化学方程式 1 碳酸钙 盐酸 有气泡产生 ______ 2 碳酸钠 硫酸 有气泡产生 ______ 3 碳酸铵 硝酸 有气泡产生 ______  lihong1983571年前1
lihong1983571年前1 -
 ben711 共回答了15个问题
ben711 共回答了15个问题 |采纳率93.3%解题思路:根据所学知识可以知道,酸和碳酸盐反应生成水和二氧化碳气体,符合复分解反应的条件.其实质是酸中的氢离子和碳酸盐中的碳酸根离子结合成水和二氧化碳.(1)盐酸与碳酸钙反应生成氯化钙、水和二氧化碳;硫酸与碳酸钠反应生成硫酸钠、水和二氧化碳;硝酸与碳酸铵反应生成硝酸铵、水和二氧化碳,化学方程式分别为:CaCO3+2HCl=CaCl2+CO2↑+H2O;Na2CO3+H2SO4=Na2SO4+CO2↑+H2O.(NH4)2CO3+2HNO3=2NH4NO3+CO2↑+H2O
(2)由上述方程式可以看出,酸与碳酸盐能反应,原因是酸中的氢离子与碳酸盐中的碳酸根离子结合成了水和二氧化碳的原因.
故答案为:(1)
化学方程式
1.CaCO3+2HCl=CaCl2+CO2↑+H2O
2.Na2CO3+H2SO4=Na2SO4+CO2↑+H2O
3.(NH4)2CO3+2HNO3=2NH4NO3+CO2↑+H2O(2)CO32-H+点评:
本题考点: 复分解反应的条件与实质;常见离子的检验方法及现象.
考点点评: 本题考查了复分解反应的条件,酸与碳酸盐反应的实质,要正确书写化学方程式,分析化学方程式的共同点得出反应的实质.1年前查看全部
- (2013•南沙区一模)下列各组对比实验,能达到实验目的是( )
(2013•南沙区一模)下列各组对比实验,能达到实验目的是( )
A.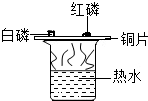
探究燃烧所有条件
B.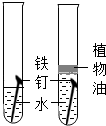
探究铁生锈所有条件
C.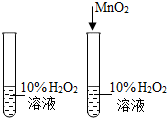
探究MnO2对过氧化氢溶液
分解速度的影响
D.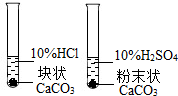
实验室制取二氧化碳的药品研究 syayu19771年前1
syayu19771年前1 -
 wuwukeke 共回答了18个问题
wuwukeke 共回答了18个问题 |采纳率72.2%解题思路:A、根据研究燃烧的条件,应采用两个变量,一是可燃物不一样,再就是隔绝氧气进行解答;
B、根据铁生锈的条件是氧气和水进行解答;
C、根据探究MnO2对过氧化氢溶液分解速度的影响只改变有无二氧化锰其他条件不变进行解答;、
D、根据该实验中有两个变量进行解答.A、研究燃烧的条件,应采用两个变量,一是可燃物不一样,再就是隔绝氧气,所以还应该在水中加入白磷看是否燃烧,故A错误;
B、铁生锈的条件是氧气和水,所以探究铁生锈所有条件,一是只有水看是否生锈,二是只有氧气看是否生锈,三是氧气和水同时存在看是否生锈,故B错误;
C、探究MnO2对过氧化氢溶液分解速度的影响只改变有无二氧化锰其他条件不变,所以可以达到实验目的,故C正确;
D、因为实验中同时改变两个条件,一是所取得酸不同,二是碳酸钙状态不同,所以实验结果没有意义,故D错误.
故选C.点评:
本题考点: 化学实验方案设计与评价.
考点点评: 此题主要考查了学生对控制变量法的理解和运用,涉及到了影响反应速率的条件、燃烧的条件和铁生锈所有条件的探究等,属常规性对比试验探究题.1年前查看全部
- (2010•南沙区一模)甲醛(CH2O)是室内空气污染物的主要成分,它来源于室内装潢所用的油漆、胶合板、化纤地毯等材料.
(2010•南沙区一模)甲醛(CH2O)是室内空气污染物的主要成分,它来源于室内装潢所用的油漆、胶合板、化纤地毯等材料.下列关于甲醛的说法中正确的是( )
A.甲醛分子是由一个碳原子和一个水分子构成的
B.甲醛中C,H,O三种元素的质量比是1:2:1
C.甲醛属于氧化物
D.甲醛分子中C,H,O三种元素的原子个数比为1:2:1 我有阳光1年前1
我有阳光1年前1 -
 九个棱角的花 共回答了23个问题
九个棱角的花 共回答了23个问题 |采纳率95.7%解题思路:本题可利用甲醛的化学式为CH2O,可判断其组成和构成,利用其组成和性质来判断物质的类别.A、由化学式可知,1个甲醛分子是由1个C原子、2个H原子、1个O原子构成,故A错误;
B、由化学式,C、H、O三种元素的质量比为1×12:2×1:1×16=6:1:8,故B错误;
C、氧化物中只有两种元素,而甲醛中有三种元素,则甲醛不属于氧化物,故C错误;
D、由甲醛的化学式为CH2O,则三种元素的原子个数比为1:2:1说法正确,故D正确;
故选D.点评:
本题考点: 元素质量比的计算;从组成上识别氧化物;分子和原子的区别和联系;原子的有关数量计算.
考点点评: 本题较简单,学生可直接利用习题中给出的物质的化学式来分析解答即可,学生应具有牢固的基础知识和基本技能,从容易的习题中可培养学生解答行为习惯.1年前查看全部
- (2014•南沙区一模)如图所示,用水平力F将一木块压在竖直的墙壁上并保持静止,下列说法中正确的是( )
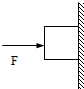 (2014•南沙区一模)如图所示,用水平力F将一木块压在竖直的墙壁上并保持静止,下列说法中正确的是( )
(2014•南沙区一模)如图所示,用水平力F将一木块压在竖直的墙壁上并保持静止,下列说法中正确的是( )
A.木块受到三个力作用而处于平衡状态
B.水平力F增大,木块对墙的压强不变
C.木块所受重力和水平力F是一对平衡力
D.木块所受重力和墙对木块的摩擦力平衡 ggllp1年前1
ggllp1年前1 -
 夏之冰冬之火 共回答了17个问题
夏之冰冬之火 共回答了17个问题 |采纳率88.2%解题思路:物体在受到两个力(或多个力)作用时,如果能保持静止状态或匀速直线运动状态,我们就说物体处于平衡状态.当一个物体受到两个力作用时,二力平衡的条件是:大小相等、方向相反、作用在同一直线上.对处于匀速下滑状态的木块进行受力分析,结合二力平衡的条件以及压强的计算公式即可确定答案.木块在水平方向上受压力和墙对木块的支持力,是一对平衡力;
木块在竖直方向上受重力和摩擦力,是一对平衡力;
A、木块受到四个力的作用处于平衡状态,故A错误;
B、木块对墙的压强P=[F/S],由于木块与墙的接触面积不变,因此当F增大时,木块对墙的压强增大,故B选项错误;
C、木块在竖直方向上受重力和摩擦力,是一对平衡力;故C错误.
D、木块在竖直方向上受到的重力与墙壁对它的静摩擦力这两个力大小相等,方向相反,并且共线、共物,根据二力平衡的条件可知这两个力是一对平衡力.故D正确.
故选D.点评:
本题考点: 平衡状态的判断;平衡力的辨别;压强大小比较.
考点点评: 解此类题判断平衡力是关键,找出物体受到成对的平衡力,根据二力平衡特点以及压强的大小比较进行解题.1年前查看全部
- (2010•南沙区一模)如图所示,是一个Z形杠杆,请在图中画出重物G受到的重力示意图和力F对支点O的力臂L.
 好活一哈1年前0
好活一哈1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2011•南沙区一模)下列图示实验操作中,正确的是( )
(2011•南沙区一模)下列图示实验操作中,正确的是( )
A.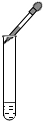
胶头滴管取用少量液体药品
B.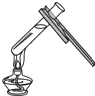
加热液体
C.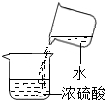
稀释浓硫酸
D.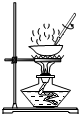
提取粗盐 无事也登三宝殿1年前1
无事也登三宝殿1年前1 -
 陶子_陶陶 共回答了13个问题
陶子_陶陶 共回答了13个问题 |采纳率92.3%解题思路:本题主要考查化学实验的基本操作,主要从操作要领上来分析,根据各种操作的要领及注意事项,对图示的操作进行分析与判断.A、向试管中滴加液体错误,不应伸到试管中接触试管,应垂悬滴加,故A操作错误;
B、给试管中的液体加热时,试管内液体的体积能超过试管容积的三分之一,故B操作错误;
C、浓硫酸稀释方法是将浓硫酸倒入水中,并用玻璃棒搅拌,故C操作错误;
D、蒸发操作时需要使用玻璃棒不断进行搅拌,防止液体受热不匀而溅出,故D操作正确;
故选D.点评:
本题考点: 液体药品的取用;给试管里的液体加热;浓硫酸的性质及浓硫酸的稀释;蒸发与蒸馏操作.
考点点评: 化学实验的基本操作是做好化学实验的基础,学生要在平时的练习中多操作,掌握操作要领,使操作规范;根据装置特点可以判断装置图的正误,根据操作要求可以判断操作是否符合实验室的规定.1年前查看全部
- (2010•南沙区一模)下列实验操作中,不正确的是( )
(2010•南沙区一模)下列实验操作中,不正确的是( )
A.使用酒精灯前,先向灯里添满酒精
B.给试管里的液体加热,液体体积不超过试管容积的1/3
C.稀释浓硫酸时,把浓硫酸沿器壁慢慢注入盛水的烧杯中
D.用漏斗过滤时,液面低于滤纸的边缘 kapopo1年前1
kapopo1年前1 -
 独孤马鸣风萧萧 共回答了21个问题
独孤马鸣风萧萧 共回答了21个问题 |采纳率85.7%解题思路:根据实验室常用仪器的使用注意事项及基本实验操作的原理、要求来解答此题.A、只有当酒精灯内酒精不足
1
3时才要添加酒精且不能超过
2
3并不是每次使用前都都添加酒精.故不正确;
B、给试管里的液体加热,液体体积不超过试管容积的1/3,且注意不能对头自己和别人以为喷出的蒸气伤人.故正确;
C、在稀释浓硫酸时,将浓硫酸沿器壁慢慢注入水中,并用玻璃棒不断的搅拌.切不可把水注入浓硫酸中.故正确;
D、用漏斗过滤时,液面低于滤纸的边缘以防止滤液浑浊.故正确.
故选A.点评:
本题考点: 实验操作注意事项的探究.1年前查看全部
- (2011•南沙区一模)小明用图所示的装置做“观察水的沸腾”实验,记录数据如下表,由数据可知,水的沸点是______℃;
(2011•南沙区一模)小明用图所示的装置做“观察水的沸腾”实验,记录数据如下表,由数据可知,水的沸点是______℃;沸腾时,杯口附近出现大量“白气”,“白气”是水蒸气遇冷______(填物态变化名称)形成的.根据记录的数据,在图中画出水沸腾前后温度随时间变化的图象.
时间(min) 0 1 2 3 4 5 6 7 温度(℃) 90 92 94 96 98 98 98 98 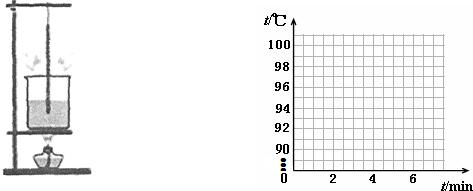
 haiou0981年前0
haiou0981年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2013•南沙区一模)夏日里想随时喝到凉爽的饮料,可以自制化学“冰箱”,即把一种化学试剂放入一定量的水中,就可以形成低
(2013•南沙区一模)夏日里想随时喝到凉爽的饮料,可以自制化学“冰箱”,即把一种化学试剂放入一定量的水中,就可以形成低温小环境.这种试剂可以是下列物质中的( )
A.固体氢氧化钠
B.熟石灰
C.硝酸铵
D.食盐 金视聚焦1年前1
金视聚焦1年前1 -
 lotus1006 共回答了20个问题
lotus1006 共回答了20个问题 |采纳率85%解题思路:物质溶于水分为两个过程:构成物质的微粒向水中扩散的过程,这一过程需吸热,构成物质的微粒与水分子形成水和分子的过程,这一过程需放热,如果吸热大于放热则溶于水表现为吸热,如果吸热小于放热则溶于水表现为放热,如果吸热等于放热则表现为溶于水温度不变.A、固体氢氧化钠溶于水放出热量,使环境温度升高,故A错;
B、生石灰溶于水放出热量,熟石灰溶于水,温度变化不大,故B错;
C、硝酸铵溶于水吸热,使周围温度降低,可以形成低温小环境,故C正确;
D、食盐溶于水温度变化不大,故D错.
故选C.点评:
本题考点: 溶解时的吸热或放热现象.
考点点评: 解答本题关键是要知道溶于水常见的放热物质有哪些?吸热物质有哪些?并能灵活运用解决实际问题.1年前查看全部
- (2014•南沙区一模)用下列方法鉴别各组无色溶液,能够达到目的是( )
(2014•南沙区一模)用下列方法鉴别各组无色溶液,能够达到目的是( )
待鉴别溶液 试剂(均为溶液) A HNO3和KNO3 酚酞 B HCl和NaCl AgNO3 C AgNO3和Na2SO4 BaCl2 D Ca(OH)2和NaOH Na2CO3
A.A
B.B
C.C
D.D 爱睡觉的鼠1年前1
爱睡觉的鼠1年前1 -
 gherthiour 共回答了19个问题
gherthiour 共回答了19个问题 |采纳率89.5%解题思路:A、根据酚酞遇酸性和中性溶液都不会变色进行分析;
B、根据盐酸和氯化钠都含有氯离子进行分析;
C、根据氯化银和硫酸钡都是沉淀进行分析;
D、根据碳酸钠和两种物质反应的现象不同进行分析.A、酚酞试剂遇碱变红色,遇其它溶液不变色.HNO3和KNO3都不呈碱性,酚酞试剂都不会变色,故A不适合;
B、AgNO3分别与HCl和NaCl反应,都会生成氯化银沉淀,不能鉴别,故B不适合;
C、BaCl2与AgNO3反应,生成氯化银白色沉淀,BaCl2与Na2SO4反应生成硫酸钡白色沉淀,现象相同,不能鉴别.故C不适合;
D、Na2CO3与Ca(OH)2反应,生成碳酸钙白色沉淀,Na2CO3与NaOH不能发生复分解反应,现象不同,可以鉴别,故D适合.
故选D.点评:
本题考点: 酸、碱、盐的鉴别.
考点点评: 在解此类题时,首先分析需要鉴别的物质的性质,然后选择适当的试剂和方法,出现不同的现象即可鉴别.1年前查看全部
- (2010•南沙区一模)现有一杯100g溶质质量分数为10%的食盐水,倒出一半后,下列说法正确的是( )
(2010•南沙区一模)现有一杯100g溶质质量分数为10%的食盐水,倒出一半后,下列说法正确的是( )
A.剩下溶液的溶质质量分数为5%
B.剩下溶液的溶质为5g
C.剩下溶液的溶质质量分数为20%
D.剩下溶液的溶质为10g 像这样的情歌1年前1
像这样的情歌1年前1 -
 安东丽 共回答了15个问题
安东丽 共回答了15个问题 |采纳率86.7%解题思路:溶液是均一、稳定的混合物;根据溶液质量和溶质质量分数可以进行相关方面的计算.因为溶液是均一的,所以剩下溶液的溶质质量分数为10%;
剩下的溶液中溶质质量为:50g×10%=5g.
故选B.点评:
本题考点: 溶液的概念、组成及其特点;溶液、溶质和溶剂的相互关系与判断.
考点点评: 解答本题要掌握溶液的特征和质量分数的含义,只有这样才能对问题做出正确的判断.1年前查看全部
- (2014•南沙区一模)有甲、乙、丙、丁四种金属,只有丁在自然界主要以单质的形式存在,将金属甲、乙、丙投入稀硫酸中,观察
(2014•南沙区一模)有甲、乙、丙、丁四种金属,只有丁在自然界主要以单质的形式存在,将金属甲、乙、丙投入稀硫酸中,观察到只有乙的表面有气泡产生,甲盐的水溶液不能用丙制的容器盛放,这四种金属的活动性由强到弱的顺序是( )
A.丁>乙>丙>甲
B.乙>甲>丙>丁
C.乙>丙>甲>丁
D.丁>乙>甲>丙 浪子吉1年前1
浪子吉1年前1 -
 杂货不收 共回答了16个问题
杂货不收 共回答了16个问题 |采纳率100%解题思路:在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,据此根据能否发生反应,可确定四种金属活动性由强到弱的顺序.只有丁在自然界主要以单质形式存在,说明丁是最稳定的金属;将金属甲、乙、丙投入稀硫酸中,观察到只有乙的表面有气泡产生,说明了乙在金属活动顺序表中位于氢的前边,甲、丙为与氢的后面,即乙的活动性大于甲、丙.由甲盐的水溶液不能用丙制的容器盛放.说明丙的活动性大于甲,由以上分析可知,四种金属的活动性由强到弱的顺序是乙>丙>甲>丁.观察选择项,C正确,A、B、D错误.
故选C.点评:
本题考点: 金属活动性顺序及其应用.
考点点评: 本题难度不大,考查金属活动性应用,掌握金属活动性应用“反应则活泼、不反应则不活泼”是正确解答此类题的关键.1年前查看全部
- (2014•南沙区一模)点A(2,3)向左平移3个单位长度得到点A′,则点A′的坐标为( )
(2014•南沙区一模)点A(2,3)向左平移3个单位长度得到点A′,则点A′的坐标为( )
A.(2,0)
B.(-1,3)
C.(-2,3)
D.(5,3) mdspmrp1年前1
mdspmrp1年前1 -
 胖人一个 共回答了17个问题
胖人一个 共回答了17个问题 |采纳率82.4%解题思路:让点A的横坐标减3,纵坐标不变即可求得平移后的坐标.∵点A(2,3)向左平移3个单位长度得到点A′,
∴点A′的横坐标为2-3=-1,纵坐标不变,即点A′的坐标为(-1,3).
故选B.点评:
本题考点: 坐标与图形变化-平移.
考点点评: 本题考查图形的平移变换,关键是要懂得左右平移点的纵坐标不变,而上下平移时点的横坐标不变.1年前查看全部
- (2013•南沙区一模)如图为氯化钠和硝酸钾的溶解度曲线,请回答:
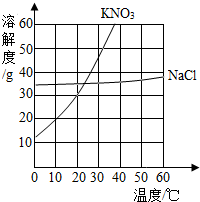 (2013•南沙区一模)如图为氯化钠和硝酸钾的溶解度曲线,请回答:
(2013•南沙区一模)如图为氯化钠和硝酸钾的溶解度曲线,请回答:
(1)硝酸钾、氯化钠都属于______ 物质(填“易溶”、“可溶”、“微溶”或“难溶”)
(2)当硝酸钾溶液从20℃升高30℃时,溶液中溶质质量分数将______ (选填“变大”或“变小”或“不变”).
(3)20℃时向lOOg水中加入25g硝酸钾,所得溶液为______ 溶液(填“饱和”或“不饱和”);将上述溶液恒温蒸发掉50g水后,析出的固体质量是______g. maxime_yang1年前1
maxime_yang1年前1 -
 猪头小yy 共回答了19个问题
猪头小yy 共回答了19个问题 |采纳率100%解题思路:(1)室温(20℃)时,溶解度大于10克的属于易溶物质,在1克和10克之间是可溶物质,在0.01克和1克之间属于微溶物质,小于0.01克的是不溶物质;并根据20℃时,氯化钠和硝酸钾的溶解度进行分析;
(2)根据硝酸钾的溶解度随温度的变化情况分析解答;
(3)据20℃时硝酸钾的溶解度及溶解度的含义分析解答.(1)观察图示可知:20℃时,氯化钠和硝酸钾的溶解度均大于10g,属于易溶物质;
(2)硝酸钾的溶解度随温度升高而增大,所以当硝酸钾溶液从20℃升高30℃时,溶质、溶剂的质量不变,溶液中溶质质量分数将不变;
(3)20℃时硝酸钾的溶解度是30g,即100g水中最多溶解30g的硝酸钾,所以向lOOg水中加入25g硝酸钾,所得溶液为不饱和溶液;将上述溶液恒温蒸发掉50g水后,溶液中还有50g水,最多溶解15g,所以析出的固体质量是10g;
故答案为:(1)易溶;(2)不变;(3)不饱和;10.点评:
本题考点: 固体溶解度曲线及其作用;物质的溶解性及影响溶解性的因素.
考点点评: 明确溶解度曲线的意义是解答本题关健,并会根据溶解度进行有关的分析、计算.1年前查看全部
- (2013•南沙区一模)将边长OA=8,OC=10的矩形OABC放在平面直角坐标系中,顶点O为原点,顶点C、A分别在x轴
(2013•南沙区一模)将边长OA=8,OC=10的矩形OABC放在平面直角坐标系中,顶点O为原点,顶点C、A分别在x轴和y轴上.在OA边上选取适当的点E,连接CE,将△EOC沿CE折叠.
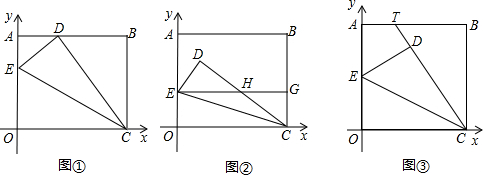
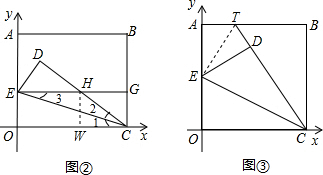
(1)如图①,当点O落在AB边上的点D处时,点E的坐标为______;
(2)如图②,当点O落在矩形OABC内部的点D处时,过点E作EG∥x轴交CD于点H,交BC于点G.求证:EH=CH;
(3)在(2)的条件下,设H(m,n),写出m与n之间的关系式m=
n2+51 20 m=;
n2+51 20
(4)如图③,将矩形OABC变为正方形,OC=10,当点E为AO中点时,点O落在正方形OABC内部的点D处,延长CD交AB于点T,求此时AT的长度. Whitewolf1年前1
Whitewolf1年前1 -
 风弄尘 共回答了22个问题
风弄尘 共回答了22个问题 |采纳率86.4%解题思路:(1)根据翻折变换的性质以及勾股定理得出BD的长,进而得出AE,EO的长即可得出答案;
(2)利用平行线的性质以及等角对等边得出答案即可;
(3)根据H点坐标得出各边长度,进而利用勾股定理求出m与n的关系即可;
(4)首先得出Rt△ATE≌Rt△DTE进而得出AT=DT.设AT=x,则BT=10-x,TC=10+x,在Rt△BTC中,BT2+BC2=TC2,求出即可.(1)∵将边长OA=8,OC=10的矩形OABC放在平面直角坐标系中,点O落在AB边上的点D处,
∴OC=DC=10,
∵BC=8,
∴BD=
102−82=6,
∴AD=10-6=4,
设AE=x,则EO=8-x,
∴x2+42=(8-x)2,
解得:x=3,
∴AE=3,
则EO=8-3=5,
∴点E的坐标为:(0,5);
(2)证明:(如图②)由题意可知∠1=∠2.
∵EG∥x轴,
∴∠1=∠3.
∴∠2=∠3.
∴EH=CH.
(3) 过点H作HW⊥OC于点W,
过点H作HW⊥OC于点W,
∵在(2)的条件下,设H(m,n),
∴EH=HC=m,WC=10-m,HW=n,
∴HW2+WC2=HC2,
∴n2+(10-m)2=m2,
∴m与n之间的关系式为:m=
1
20n2+5;
(4)(如图③)连接ET,
由题意可知,ED=EO,ED⊥TC,DC=OC=10,
∵E是AO中点,∴AE=EO.
∴AE=ED.
∵在Rt△ATE和Rt△DTE中,
TE=TE
AE=ED
∴Rt△ATE≌Rt△DTE(HL).
∴AT=DT.
设AT=x,则BT=10-x,TC=10+x,
在Rt△BTC中,BT2+BC2=TC2,
即(10-x)2+102=(10+x)2,
解得 x=2.5,
即AT=2.5.
故答案为:(0,5);m=
1
20n2+5.点评:
本题考点: 几何变换综合题.
考点点评: 此题主要考查了翻折变换的性质以及勾股定理和全等三角形的判定与性质等知识,熟练构建直角三角形利用勾股定理得出相关线段长度是解题关键.1年前查看全部
- (2010•南沙区一模)某同学设计如图装置进行实验:A是固体,B是液体,C是沾有石蕊试液的棉花团.
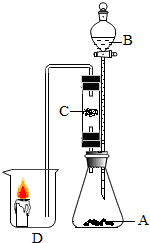 (2010•南沙区一模)某同学设计如图装置进行实验:A是固体,B是液体,C是沾有石蕊试液的棉花团.
(2010•南沙区一模)某同学设计如图装置进行实验:A是固体,B是液体,C是沾有石蕊试液的棉花团.
(1)实验一:观察到C没有明显现象,D处蜡烛火焰明显增大,则锥形瓶中加入的物质A是______,
B是______,反应现象说明生成的物质是______.
(2)实验二:①观察到D处蜡烛火焰逐渐熄灭,则锥形瓶中发生的化学反应方程式是______;
②观察到C的现象是______;
③检验能使D处蜡烛火焰逐渐熄灭的气体的操作是______,现象______. 彭转转3021年前1
彭转转3021年前1 -
 zhusuzi 共回答了18个问题
zhusuzi 共回答了18个问题 |采纳率83.3%解题思路:(1)由D装置中的现象判断所制取的气体为氧气;由于氧气具有支持燃烧的性质,可燃物在氧气中燃烧与在空气中更旺;黑色固体二氧化锰催化液体过氧化氢分解制取氧气,是实验室常用的制取氧气的方法;
(2)由于二氧化碳气体不能燃烧也不支持燃烧且密度比空气大,常用于灭火;二氧化碳与水反应可生成能使此色石蕊试液变红的碳酸;二氧化碳能使澄清的石灰水变浑浊,常用澄清石灰水检验气体二氧化碳.(1)由“D处蜡烛火焰明显增大”的实验现象可判断,装置内产生的气体为氧气;锥形瓶中加入的固体物质A为二氧化锰,分液漏斗B中加入的液体为过氧化氢溶液;
故答案为:二氧化锰(MnO2);过氧化氢(H2O2)溶液;氧气(O2);
(2)①由“D处蜡烛火焰逐渐熄灭”可判断装置内制取的气体为二氧化碳,制取二氧化碳的反应原理的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
故答案为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
②二氧化碳气体与棉花团中的紫色石蕊试液中的水能生成碳酸,而使试液变红红色;
故答案为:棉花团由紫色变成红色;
③为检验气体二氧化碳,可向烧杯内加入澄清石灰水,观察到澄清石灰水变浑浊,可说明气体为二氧化碳;
故答案为:往烧杯中滴入适量澄清石灰水;澄清石灰水变浑浊.点评:
本题考点: 实验室制取氧气的反应原理;二氧化碳的实验室制法;二氧化碳的检验和验满.
考点点评: 利用二氧化碳能使澄清石灰水变浑浊的实验事实,实验室通常使用澄清石灰水检验气体二氧化碳,澄清石灰水变浑浊则气体为二氧化碳.1年前查看全部
- (2011•南沙区一模)海洋是地球上最大的储水库,浩瀚的海洋蕴藏着丰富的化学资源,从海水中可以提取出大量的镁.其主要步骤
(2011•南沙区一模)海洋是地球上最大的储水库,浩瀚的海洋蕴藏着丰富的化学资源,从海水中可以提取出大量的镁.其主要步骤如下:
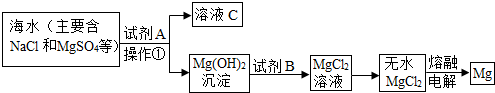
(1)提取Mg的过程中,试剂A可以选用______,试剂B选用______.写出加入试剂A之后的化学方程式______.
(2)操作①的名称是______.
(3)分离出Mg(OH)2后的溶液C中含有较多的氯化钠,也还含有CaCl2、Na2SO4等杂质.工业上为了获得较纯净NaCl溶液,在分离后的溶液中先加入过量的BaCl2溶液,可以除去______;再加入过量的Na2CO3溶液的目的是______.写出加入碳酸钠后的反应的化学方程式①______;②______.最后再加入过量的盐酸,并蒸发结晶.蒸发结晶的过程中用到了与操作①相同的玻璃仪器是______. 精彩人生19781年前1
精彩人生19781年前1 -
 散落的梦 共回答了18个问题
散落的梦 共回答了18个问题 |采纳率88.9%解题思路:根据物质的性质以及已有的知识进行分析,要提取镁,需要将海水中的硫酸镁逐步转化生成氯化镁,所加入的试剂在除去其他杂质的同时不能引入新的杂质.(1)要提取镁,可以首先使海水中的硫酸镁与碱反应生成氢氧化镁沉淀,要使氢氧化镁转化成氯化镁,可以加入盐酸,硫酸镁能与氢氧化钠反应生成硫酸钠和氢氧化镁沉淀,故填:NaOH,HCl,MgSO4+2NaOH═Mg(OH)2↓+Na2SO4;
(2)要将生成的氢氧化镁沉淀与溶液分离,可以使用过滤的方法,故填:过滤;
(3)要除去氯化钠中的CaCl2、Na2SO4等杂质,可以首先加入氯化钡溶液除去硫酸钠,加入的碳酸钠溶液能与氯化钙溶液反应生成碳酸钙沉淀,能与上一步中多加的氯化钡反应生成碳酸钡沉淀,蒸发结晶和过滤操作都需要用到玻璃棒,故填:Na2SO4,除去CaCl2和过量的BaCl2,Na 2CO3+CaCl2 ═CaCO3↓+2NaCl,Na 2CO3+BaCl2 ═BaCO3↓+2NaCl,玻璃棒.点评:
本题考点: 对海洋资源的合理开发与利用;过滤的原理、方法及其应用;蒸发与蒸馏操作;盐的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查了物质提纯的知识,完成此题,可以依据物质的性质进行.选择的除杂试剂与杂质反应时不能引入新的杂质.1年前查看全部
- (2014•南沙区一模)为了节能环保,小明开始骑电动自行车上班(如图1所示),如表是他与电动自行车的有关数据:
(2014•南沙区一模)为了节能环保,小明开始骑电动自行车上班(如图1所示),如表是他与电动自行车的有关数据:
求:人的质量m人/kg 电动自行车质量m车/kg 行驶时电动机平均功率P/W 50 20 180
(1)小明在其中一段平直公路上做匀速运动时,该段路程运动的s-t图象如图2所示,则电动自行车行驶速度为多少?
(2)行驶时,车轮与地面接触的总面积为触面积4×10-3m2,则小明骑车时,电动自行车对地面的压强为多大?(g=10N/kg)
(3)在该段路程行驶过程,受到的阻力与时间关系如图3所示,则使电动自行车前进时的牵引力应是多大?你的依据是什么?前进90m牵引力做功为多少?
(4)该车在这15s内消耗的电能转化为机械能的效率是多少?
 我是小vv1年前1
我是小vv1年前1 -
 奈若何啊 共回答了19个问题
奈若何啊 共回答了19个问题 |采纳率94.7%解题思路:(1)根据图2得出电动自行车的行驶速度;
(2)已知车轮与地面接触的总面积为触面积,人和自行车的质量根据公式G=mg求出电动自行车对地面的压力,再根据公式p=[F/S]求出电动自行车对地面的压强;
(3)根据图3得出电动自行车行驶时的阻力,因为匀速行驶,牵引力和阻力是一对平衡力,根据公式W=Fs求出电动自行车前进90m牵引力所做的功;
(4)已知电动自行车行驶时电动机平均功率,根据公式W=Pt求出电动自行车做的总功,再根据η=
×100%求出电能转化为机械能的效率.W有用 W总 (1)由图可知电动自行车行驶90m,用时15s,所以电动自行车的行驶速度v=[s/t]=[90m/15s]=6m/s;
(2)已知人的质量是50kg,自行车的质量是20kg,
电动自行车对地面的压力F=G=(50kg+20kg)×10N/kg=700N,
受力面积S=4×10-3m2,
自行车对地面的压强p=[F/S]=[700N
4×10−3m2=1.75×105Pa;
(3)根据图3,因为电动自行车是匀速直线运动,所以F=f=20N,
前进90m牵引力做功W=Fs=20N×90m=1800J;
(4)已知P=180W,电动自行车15s做功:
W电=Pt=180W×15s=2700J,
η=
W
W电=
1800J/2700J]=66.7%.
答:(1)电动自行车行驶速度为6m/s;
(2)电动自行车对地面的压强为1.75×105Pa;
(3)则使电动自行车前进时的牵引力应是20N,依据是二力平衡条件,前进90m牵引力做功为1800J;
(4)电能转化为机械能的效率是66.7%.点评:
本题考点: 速度公式及其应用;压强的大小及其计算;功的计算;机械效率.
考点点评: 本题的关键是能够从表中和图象中找出对解题有用的东西,然后再由速度公式、压强公式,功的公式和效率公式分别算出.1年前查看全部
- (2011•南沙区一模)欲除去物质中的少量杂质(括号内为杂质),方法和反应的基本反应类型均正确的是( )
(2011•南沙区一模)欲除去物质中的少量杂质(括号内为杂质),方法和反应的基本反应类型均正确的是( )
选项 物质 加入的试剂和操作 基本反应类型 A HCl气体(CO2) 将气体通过澄清石灰水后干燥 化合反应 B Fe(Cu) 加足量稀盐酸、过滤、洗涤 置换反应 C NaCl(Na2CO3) 加足量稀硫酸、蒸发 复分解反应 D CuCl2(CuSO4) 加适量氯化钡溶液,过滤 复分解反应
A.A
B.B
C.C
D.D statan1年前1
statan1年前1 -
 yoajc 共回答了19个问题
yoajc 共回答了19个问题 |采纳率78.9%解题思路:根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.A、CO2和HCl气体均能与澄清的石灰水反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则;故选项所采取的方法错误.
B、铁能与稀盐酸反应生成氯化亚铁和氢气,铜不与稀盐酸反应,加足量稀盐酸反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
C、Na2CO3能与稀硫酸反应生成硫酸钠、水、二氧化碳,能除去杂质但引入了新的杂质硫酸钠,不符合除杂原则,故选项所采取的方法错误.
D、CuSO4能与氯化钡溶液反应生成硫酸钡沉淀和氯化铜,再过滤除去沉淀,能除去杂质且没有引入新的杂质,该反应是两种化合物相互交换成分生成另外两种化合物的反应,属于复分解反应,故选项所采取的方法和反应的基本反应类型均正确.
故选D.点评:
本题考点: 物质除杂或净化的探究;常见气体的检验与除杂方法;金属的化学性质;盐的化学性质;反应类型的判定.
考点点评: 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.1年前查看全部
- (2014•南沙区一模)如图所示,点燃蜡烛会使它上方的扇叶旋转起来.这是因为蜡烛的火焰使附近空气的温度升高,体积膨胀,空
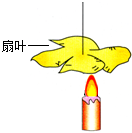 (2014•南沙区一模)如图所示,点燃蜡烛会使它上方的扇叶旋转起来.这是因为蜡烛的火焰使附近空气的温度升高,体积膨胀,空气的密度变______,所以热空气______(选填“上升”或“下降”)形成气流,气流流过扇叶时,带动扇叶转起来,实验说明温度能够改变气体的______.根据气体的这种变化规律,房间里的冷气机一般都安装在接近天花板的墙上,由冷风口吹出的冷气会______(选填“上升”或“下降”),使房间的空气迅速流动起来.
(2014•南沙区一模)如图所示,点燃蜡烛会使它上方的扇叶旋转起来.这是因为蜡烛的火焰使附近空气的温度升高,体积膨胀,空气的密度变______,所以热空气______(选填“上升”或“下降”)形成气流,气流流过扇叶时,带动扇叶转起来,实验说明温度能够改变气体的______.根据气体的这种变化规律,房间里的冷气机一般都安装在接近天花板的墙上,由冷风口吹出的冷气会______(选填“上升”或“下降”),使房间的空气迅速流动起来.  徐庆霞1年前1
徐庆霞1年前1 -
 沙头角 共回答了13个问题
沙头角 共回答了13个问题 |采纳率84.6%点燃蜡烛上方的空气,吸收热量,温度升高,体积膨胀,密度变小,密度小的热空气上升,形成对流,吹动扇叶转动;实验说明温度能够改变气体的密度,根据气体的这种变化规律,房间里的冷气机一般都安装在接近天花板的墙上,由冷风口吹出的冷气会下降,使房间的空气迅速流动起来.
故答案为:小;上升;密度;下降.1年前查看全部
- 广州南沙区2013年初中七年级英语是什么版的?
广州南沙区2013年初中七年级英语是什么版的?
是人教版的吗? bat-bat1年前1
bat-bat1年前1 -
 yanrantianshi 共回答了16个问题
yanrantianshi 共回答了16个问题 |采纳率75%如果是公办学校的,都是用人教版的教材!民办的就不是很清楚了1年前查看全部
- 英语翻译广州市天河区五山华南农业大学正门香园餐厅对面学生宿舍 要写成英文地址格式要正确怎么写?广州市南沙区南沙街珠江东路
英语翻译
广州市天河区五山华南农业大学正门香园餐厅对面学生宿舍
要写成英文地址格式要正确怎么写?
广州市南沙区南沙街珠江东路86号 写成英文地址又是怎么写的呢? inchla1年前1
inchla1年前1 -
 苏醒7788 共回答了22个问题
苏醒7788 共回答了22个问题 |采纳率100%从小范围到大范围,比如students' dormitory opposite the Zhengxiangyuan Cafeteria at the gate of Huanan Agriculture University
再继续写后面的地址1年前查看全部
大家在问
- 1化学平衡中的forward rate在这里是指比率还是速率?如有例证最好.
- 2阅读下文,完成下面问题。 麻鞋之歌
- 3“把鸡蛋放入水中沉入水底,把鸡蛋放入不再溶解的盐水里仍然称在水底.
- 4He could do nothing except_TV A.watch B.watches C.watching D
- 5如图,在四边形ABCD中,∠B=∠ACD,AB=6,BC=4,AC=5,CD=7又1/2,求AD的长
- 6The man (having been put )in prison for more than twenty yea
- 7如图14,矩形ABCD中,AB=1cm,BC=2cm,以B为圆心,BC为半径作¼圆弧交AD于F,交BA的延长线
- 8在投递简历时经常看见FAQ这个词例如:总结客户提出的技术问题,反馈给技服和运行部门,并制定相应的FAQ;
- 9在长方体ABCD-A1B1C1D1中,E,P分别是BC,A1D1的中点,M,N分别是AE,CD1的中点,AD=AA1=a
- 10商店原来有100千克饺子粉,每袋5千克,卖出一些后还有40千克,卖出了几袋
- 11小明为一个矩形娱乐场所提供了如下的设计方案,其中半圆形休息区和矩形游泳池以外的地方都是绿地.
- 12With his son _______, the old man felt unhappy. [
- 13意料之中用 然
- 14(2010•威海模拟)小王家新买的电热淋浴器的铭牌如表所示.小王按说明书要求给淋浴器装满水,通电50min,观察到淋浴器
- 15听句子,根据你所听到的内容,选择正确的图画顺序。每个句子读两遍。