燃煤暖气炉一冬天能烧多少煤啊?具体多少平M 我也说不清 平房一间大厅 两边卧室 可说是4大间屋 打算用5块暖气片,两块1
 横盘2022-10-04 11:39:541条回答
横盘2022-10-04 11:39:541条回答具体多少平M 我也说不清 平房一间大厅 两边卧室 可说是4大间屋 打算用5块暖气片,两块16个的 三个12个的?用多大的炉子,3个月烧多少煤?

已提交,审核后显示!提交回复
共1条回复
 zlizhi1 共回答了14个问题
zlizhi1 共回答了14个问题 |采纳率100%- 1000kg就够了.
- 1年前
相关推荐
- 某农场附近新建了一座燃煤火力发电厂后该农场的小麦产量急剧下降.经农场技术员测定:雨水pH约为4、土壤pH约为5.已知一些
某农场附近新建了一座燃煤火力发电厂后该农场的小麦产量急剧下降.经农场技术员测定:雨水pH约为4、土壤pH约为5.已知一些重要作物最适宜生长的土壤的pH如下表:
作物
①水稻
②小麦
③玉米
④油菜
⑤马铃薯
PH
6~7
6.3~7.5
6~7
6~7
4.8~5.5 (1)根据上表数据,你认为这种土壤最适合种植的作物是(填编号)______.
(2)若继续种小麦,你认为最好选用以下(填编号)______试剂来改良土壤.
①工业盐酸 ②熟石灰 ③纯碱
(3)该地区形成酸雨的主要原因是______. q1bp1年前1
q1bp1年前1 -
 kuaijii 共回答了13个问题
kuaijii 共回答了13个问题 |采纳率92.3%(1)由表中信息可知,马铃薯适合于在显酸性的土壤中生长,土壤的PH为5,显酸性.故填:⑤
(2)因为小麦适合于在中性或弱酸性的土壤中生长,若要种小麦,需要减弱土壤的酸性.熟石灰显碱性,可以中和显酸性的土壤.故填:②
(3)煤燃烧时能生成大量的二氧化硫气体,二氧化硫气体和雨水反应生成亚硫酸或硫酸,从而使雨水的酸性增强.故填:火力发电厂燃煤生成的二氧化硫直接排放到空气中与水反应形成酸雨.1年前查看全部
- 日常生活中,人们常把煤做成蜂窝状(如图),这样做的目的是______,燃煤取暖若通风不畅,常引发煤气中毒事故,煤产生“煤
 日常生活中,人们常把煤做成蜂窝状(如图),这样做的目的是______,燃煤取暖若通风不畅,常引发煤气中毒事故,煤产生“煤气”的过程用化学方程式表示为2C+O2
日常生活中,人们常把煤做成蜂窝状(如图),这样做的目的是______,燃煤取暖若通风不畅,常引发煤气中毒事故,煤产生“煤气”的过程用化学方程式表示为2C+O2
2CO点燃 .2C+O2.除排放煤气外,燃煤与多种环境污染问题有关,下列环境污染与燃煤没有直接关系的是______.
2CO点燃 .
A.酸雨B.温室效应C.臭氧层破坏D.可吸入颗粒增加. sunnie21年前1
sunnie21年前1 -
 猫猫蒋 共回答了17个问题
猫猫蒋 共回答了17个问题 |采纳率76.5%解题思路:煤做成蜂窝状增大了煤与氧气的接触面积;燃煤不充分燃烧生成一氧化碳,写出反应的化学方程式即可;根据燃煤燃烧的生成物对环境的影响进行分析解答.将煤做成蜂窝状,能增大与氧气的接触面积,使煤与氧气充分接触而发生完全燃烧;燃煤不充分燃烧生成一氧化碳,反应的化学方程式为2C+O2 点燃 . 2CO;燃煤燃烧产生的二氧化碳是造成温室效应的主要气体...
点评:
本题考点: 完全燃烧与不完全燃烧;常用燃料的使用与其对环境的影响.
考点点评: 生活处处有化学,本题难度不大,但综合性较强,考查同学们灵活运用所学知识进行解题的能力.1年前查看全部
- 下列观点,你认为不正确的是 A.燃煤时,在房间里放一盆水可防止CO中毒 B.在做硫燃烧的实验时,在瓶里盛少量的水可减少对
下列观点,你认为不正确的是
A.燃煤时,在房间里放一盆水可防止CO中毒 B.在做硫燃烧的实验时,在瓶里盛少量的水可减少对环境的污染 C.计算机房失火不能用泡沫灭火器灭火 D.活性炭可以吸附水中的色素和异味  追随着131年前1
追随着131年前1 -
 w142105707 共回答了16个问题
w142105707 共回答了16个问题 |采纳率87.5%A
1年前查看全部
- 如图是某燃煤发电厂处理废气的装置示意图.下列说法正确的是( )
 如图是某燃煤发电厂处理废气的装置示意图.下列说法正确的是( )
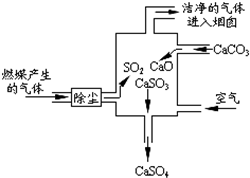
如图是某燃煤发电厂处理废气的装置示意图.下列说法正确的是( )
A.使用此废气处理装置可减少酸雨的形成
B.此过程中没有分解反应
C.此过程中S元素的化合价未发生改变
D.整个过程的反应可表示为:2SO2+2CaCO3+O2=2CaSO4+2CO2 581665181年前1
581665181年前1 -
 scg456789321 共回答了20个问题
scg456789321 共回答了20个问题 |采纳率90%解题思路:根据图示进行分析,燃煤中含有硫,燃烧后生成二氧化硫,生成的二氧化硫可以使用碳酸钙处理,从而减少二氧化硫的排放.A、经过此废气处理减少了二氧化硫的排放,从而减少了酸雨的形成,故A正确;
B、该过程中碳酸钙发生分解反应生成氧化钙,故B错误;
C、硫燃烧生成二氧化硫,硫元素的化合价由0变为+4,故C错误;
D、整个过程中可以表示为2SO2+2CaCO3+O2=2CaSO4+2CO2,故D正确;
故选AD.点评:
本题考点: 酸雨的产生、危害及防治;有关元素化合价的计算;反应类型的判定;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查了化学与环境保护的知识,完成此题,可以依据已有的物质的性质进行.1年前查看全部
- PM2.5是指大气中直径小于或等于2.5微米的颗粒物,主要来自化石燃料的燃烧(如机动车尾气、燃煤等).下列有关空气和PM
PM2.5是指大气中直径小于或等于2.5微米的颗粒物,主要来自化石燃料的燃烧(如机动车尾气、燃煤等).下列有关空气和PM2.5的说法错误的是( )
A.空气是混合物
B.PM2.5与形成雾霾天气无关
C.大力发展氢能源,减少燃油汽车尾气的排放可改善空气质量
D.PM2.5专用口罩中使用了活性炭,是利用了活性炭的吸附性 cbnew211年前1
cbnew211年前1 -
 yun203009 共回答了16个问题
yun203009 共回答了16个问题 |采纳率100%解题思路:A、根据混合物的定义考虑;
B、根据PM2.5是指大气中直径小于或等于2.5微米的颗粒物考虑;
C、根据燃油汽车的尾气考虑本题;
D、根据活性炭的结构特点考虑.A、空气中含有氮气、氧气、二氧化碳等物质,所以属于混合物,故A说法正确;
B、PM2.5是指大气中直径小于或等于2.5微米的颗粒物,由于这些颗粒物的集合体会造成灰雾天气,故B说法错误;
C、燃油汽车的尾气中会含有大量的一氧化碳、二氧化氮、二氧化硫等空气污染物,大力发展电动车、减少燃油汽车的尾气排放量可改善空气质量,故C说法正确;
D、活性炭具有疏松多孔的结构,具有吸附性,能把小的颗粒吸附在它的表面,故D说法正确.
故选B.点评:
本题考点: 空气的污染及其危害.
考点点评: 解答本题的关键是要知道混合物最少由两种物质组成,知道汽车尾气的危害,活性炭的吸附性,了解PM2.5的含义.1年前查看全部
- 高中化学能减少酸雨的形成对燃煤进行脱硫B人工收集雷电作用产生的氮的氧化物
高中化学能减少酸雨的形成对燃煤进行脱硫B人工收集雷电作用产生的氮的氧化物
3.下列有关防止或减少酸雨的措施中不可行的是 A.对燃煤及燃煤烟气进行脱硫 ...C.人工收集大气雷电产生的氮的氧化物 D.推广天然气、甲醇等作为汽车的燃料 A ①②③④ B ①②③ C ①②④ D ①③④ A-ha1年前1
A-ha1年前1 -
 1314520zl 共回答了16个问题
1314520zl 共回答了16个问题 |采纳率87.5%大气雷电产生的氮氧化物被豆科植物直接吸收,人工不可以1年前查看全部
- 下列有关化学知识描述正确的是A合成纤维和光导纤维都是化学纤维B发电厂的燃煤在燃烧时加入适量石灰石,有利于保护环境C铝合金
下列有关化学知识描述正确的是
A合成纤维和光导纤维都是化学纤维
B发电厂的燃煤在燃烧时加入适量石灰石,有利于保护环境
C铝合金的大量使用归功于人们能使用一氧化碳、氢气等还原剂从氧化铝中获得铝
D因为氯化钠能使细菌内蛋白质发生变性,所以食盐腌制过的食品能较长时间不变质
请教下为什么
能顺便解释下其他答案不 minpan1年前4
minpan1年前4 -
 sato707 共回答了21个问题
sato707 共回答了21个问题 |采纳率100%A、错误.化学纤维用天然的或人工合成的高分子物质为原料、经过化学或物理方法加工而制得的纤维的统称.光导纤维是SiO2,不是有机高分子材料
B、正确.煤中含有硫,燃烧时会产生SO2,当加入石灰石时其分解产生的CaO 可以吸收SO2得CaSO3,避免了SO2的直接排放,有利于环保
C、错误.制备Al采用电解Al2O3的方法.
D、错误.食物腌制,是用NaCl这种高渗溶液,使细胞脱水死亡,并不是蛋白质变性的原理.重金属盐才能使蛋白质变性
选择B1年前查看全部
- 如图是某燃煤发电厂处理废气的装置示意图.下列说法错误的是( )
 如图是某燃煤发电厂处理废气的装置示意图.下列说法错误的是( )
如图是某燃煤发电厂处理废气的装置示意图.下列说法错误的是( )
A.使用此废气处理装置可减少酸雨的形成
B.装置内发生的反应有化合、分解、置换和氧化还原反应
C.整个过程的反应可表示为:2SO2+2CaCO3+O2=2CaSO4+2CO2
D.若烟囱的气体排放不达标,则此气体可使酸性高锰酸钾溶液褪色 sazhl11年前1
sazhl11年前1 -
 fengying52 共回答了14个问题
fengying52 共回答了14个问题 |采纳率92.9%解题思路:A、根据二氧化硫易造成酸雨,此装置将二氧化硫吸收转化分析.
B、碳酸钙受热生成氧化钙和二氧化碳的反应属于分解反应;二氧化硫与石灰水反应生成CaSO3和CaSO4是复分解反应和氧化还原反应;
C、根据反应过程可以书写反应的化学方程式;
D、二氧化硫具有还原性,易被高锰酸钾溶液氧化反应使溶液褪色.A、二氧化硫是形成酸雨的重要物质,此装置将二氧化硫吸收转化,减少酸雨的形成,故A正确;
B、碳酸钙受热生成氧化钙和二氧化碳的反应属于分解反应;二氧化硫与石灰水反应生成CaSO3和CaSO4是中和反应、化合反应,氧化还原反应,但没有置换反应,故B错误;
C、整个过程中,二氧化硫与碳酸钙和氧气反应生成了硫酸钙和二氧化碳,化学反应式可表示为:2SO2+2CaCO3+O2=2CaSO4+2CO2,故C正确;
D、二氧化硫具有还原性,易被高锰酸钾溶液氧化反应使溶液褪色,所以可用酸性高锰酸钾溶液检验废气处理是否达标,故D正确;
故答案:B;点评:
本题考点: 常见的生活环境的污染及治理;化学基本反应类型;二氧化硫的化学性质.
考点点评: 本题考查二氧化硫气体的污染和治理,解答本题要充分理解处理废气的过程,只有这样才能对相关方面的问题做出正确的判断.1年前查看全部
- PM2.5(可入肺颗粒物)污染跟冬季燃煤密切相关,燃煤还同时排放大量的CO 2 、SO 2 和NO x
PM2.5(可入肺颗粒物)污染跟冬季燃煤密切相关,燃煤还同时排放大量的CO 2 、SO 2 和NO x
(1)最近有科学家提出构想:把空气吹入饱和碳酸钾溶液,然后再把CO 2 从溶液中提取出来,经化学反应后使之变为可再生燃料甲醇。
①已知在常温常压下:
2CH 3 OH(l)+3O 2 (g) = 2CO 2 (g)+4H 2 O(g) ∆H = -1275.6 kJ/mol
2CO(g)+O 2 (g)=2CO 2 (g)∆H = -566.0 kJ/mol
H 2 O(g)=H 2 O(1) ∆H = -44.0 kJ/mol
则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为_____________________。
②以甲醇和氧气反应制成的燃料电池如图所示,该电池工作过程中O 2 应从______(填“c”或“b”)口通入,电池负极反应式为__________________。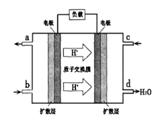
③25℃时,将甲醇燃烧生成的足量CO 2 通入到浓度为0.lmol·L -1 ,NaOH溶液中,所得溶液的pH=8,溶液中离子浓度由大到小的顺序是_________________。
(2)已知在一定条件下,NO与NO 2 存在下列反应:NO(g)+NO 2 (g)=N 2 O 3 (g),ΔH<0若该反应在绝热、恒容的密闭体系中进行,下列示意图能说明t l 时刻达到平衡状态的是____________。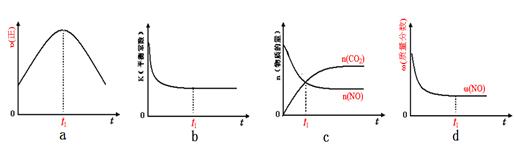
(3)在一个固定容积为5L的密闭容器中充入0.20molSO 2 和0.l0molO 2 ,半分钟后达到平衡,测得容器中含SO 3 0.18mol,则v(O 2 )=__________,若继续通入0.20mo1SO 2 和0.lmolO 2 ,则平衡____________移动(填“向正反应方向”、“向逆反应方向”或“不”)。
(4)在一定条件下,NO 2 可以被NH 3 还原为N 2 来消除NO 2 对环境造成的污染。25℃时,将NH 3 溶于水得l00mL 0.lmol·L - 的氨水,测得pH=11,则该条件下NH 3 ·H 2 O的电离平衡常数约为___________。 jackylujie1年前1
jackylujie1年前1 -
 圈圈是我 共回答了19个问题
圈圈是我 共回答了19个问题 |采纳率84.2%(16分)
(1) ①CH 3 OH(l)+O 2 (g)=CO(g)+2H 2 O(l) △H=-442.8kJ·mol -1 (2分);
②c (2分) CH 3 OH+ H 2 O-6e - =CO 2 ↑+6H + (2分);
③c(Na + )> c(HCO- 3)> c(OH - )> c(H + )> c(CO2- 3) (2分);
(2) bd (2分)
(3) 0.036mol·L -1 ·min -1 或0.0006mol·L -1 ·s -1 (2分);向正反应方向(2分);
(4) 1.01×10 -5 (2分)
1年前查看全部
- 下列有关环境问题正确的是:A燃煤时加入适量的石灰石,可减少废气忠中的二氧化硫的量B臭氧的体积分数超过10^-4%的空气有
下列有关环境问题正确的是:
A燃煤时加入适量的石灰石,可减少废气忠中的二氧化硫的量
B臭氧的体积分数超过10^-4%的空气有利于人体健康
Cph在5.6-7.0之间的降雨通常称为酸雨 比比大世界1年前1
比比大世界1年前1 -
 猫呷呷 共回答了19个问题
猫呷呷 共回答了19个问题 |采纳率94.7%A,生成CaSO4,减少SO2
B,低于时对身体有利
C,5.6-7.0为正常,故选A1年前查看全部
- (1)天然气代替燃煤是防止空气污染的措施之-.请写出天然气燃烧的化学方程式:CH4+2O2 点燃 .
(1)天然气代替燃煤是防止空气污染的措施之-.请写出天然气燃烧的化学方程式:CH4+2O2
CO2+2H2O点燃 .CH4+2O2.
CO2+2H2O点燃 .
(2)在催化剂的作用下,可使汽车尾气中CO和NO反应,并转化为两种气体.其中一种可以参与植物的光合作用,另-种是空气中含量最多的气体,该反应的化学方程式为4CO+2NO2
4CO2+N2催化剂 .4CO+2NO2.
4CO2+N2催化剂 .
(3)近期世界石油价格飙升,寻找替代能源具有重要的现实意义.请写出能代替汽油来驱动汽车、具有开发前景的二种能源:______、______. wensizhao1年前1
wensizhao1年前1 -
 犹太拉比 共回答了18个问题
犹太拉比 共回答了18个问题 |采纳率100%解题思路:(1)根据天然气燃烧生成水和二氧化碳解答;
(2)根据植物的光合作用的原料和空气中各成分的含量考虑,再结合质量守恒定律,反应前后各元素种类不变.根据化学方程式的书写步骤正确书写化学方程式.
(3)具有开发前景的新能源是太阳能、风能等,据此解答.(1)甲烷燃烧的化学方程式为:CH4+2O2
点燃
.
CO2+2H2O.
(2)植物的光合作用的原料是水和二氧化碳,而反应物CO和NO中不存在氢元素,不可能是水,只有二氧化碳了,空气中各成分及体积分数为:氮气:78%、氧气:21%、稀有气体:0.94%、二氧化碳0.03%、水蒸气和杂质:0.03%.所以空气中含量最多的气体是氮气.
由题意可知:CO与NO2反应的化学方程式为:4CO+2NO2
催化剂
.
4CO2+N2;
(3)具有开发前景的新能源是太阳能、风能等,故填:太阳能,风能.
答案:
(1)CH4+2O2
点燃
.
CO2+2H2O
(2)4CO+2NO2
催化剂
.
4CO2+N2
(3)太阳能,风能点评:
本题考点: 常用燃料的使用与其对环境的影响;书写化学方程式、文字表达式、电离方程式;资源综合利用和新能源开发.
考点点评: 该题属于新信息题,对于培养学生提取信息、迁移信息的解题能力是非常有利的.本题考查了化学与能源的知识,完成此题,可以依据已有的知识进行.1年前查看全部
- 使用化学手段可以消除某些环境污染.下列主要依靠化学手段消除环境污染的是( ) A.在燃煤中添加生石灰 B.将某些废旧塑
使用化学手段可以消除某些环境污染.下列主要依靠化学手段消除环境污染的是( ) A.在燃煤中添加生石灰 B.将某些废旧塑料融化后再成型 C.把放射性核废料深埋于地下岩层 D.用多孔吸附剂清除水面油污  流浪的小虾1年前1
流浪的小虾1年前1 -
 hju84kut 共回答了20个问题
hju84kut 共回答了20个问题 |采纳率90%A.生石灰能和氧气、煤燃烧生成的二氧化硫等物质反应生成硫酸钙,属于化学变化,故A正确;
B.将某些废旧塑料融化后再成型的过程中没有新物质生成,属于物理变化,故B错误;
C.把放射性核废料深埋于地下岩层的过程中没有新物质生成,属于物理变化,故C错误;
D.用多孔吸附剂清除水面油污的过程中没有新物质生成,属于物理变化,故D错误.
故选A.1年前查看全部
- (2010•六合区模拟)利用海水法脱硫的工艺大致流程是:①将燃煤(含硫)产生的烟气通过海水洗去SO2,)
(2010•六合区模拟)利用海水法脱硫的工艺大致流程是:①将燃煤(含硫)产生的烟气通过海水洗去SO2,)
②向洗过烟气后的海水中通入氧气,可生产获得硫酸钠和盐酸.)试用化学方程式表示上述变化:SO2+H2O═H2SO3、2H2SO3+O2+4NaCl═2Na2SO4+4HClSO2+H2O═H2SO3、2H2SO3+O2+4NaCl═2Na2SO4+4HCl. 沙漠里的烟灰缸1年前1
沙漠里的烟灰缸1年前1 -
 没那个必要 共回答了21个问题
没那个必要 共回答了21个问题 |采纳率76.2%二氧化硫和水反应生成亚硫酸,化学方程式为:SO2+H2O═H2SO3
亚硫酸和氧气、氯化钠等物质反应生成硫酸钠和盐酸,化学方程式为:2H2SO3+O2+4NaCl═2Na2SO4+4HCl.1年前查看全部
- 火力发电厂释放出大量的氮氧化物(NO x )、二氧化硫和二氧化碳等气体会造成环境污染.对燃煤废气进行脱硝、脱硫和脱碳等处
火力发电厂释放出大量的氮氧化物(NO x )、二氧化硫和二氧化碳等气体会造成环境污染.对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的.
(1)脱硝.利用甲烷催化还原NO x :
CH 4 (g)+4NO 2 (g)=4NO(g)+CO 2 (g)+2H 2 O(g)△H 1 =-574kJ•mol -1
CH 4 (g)+4NO(g)=2N 2 (g)+CO 2 (g)+2H 2 O(g)△H 2 =-1160kJ•mol -1
甲烷直接将NO 2 还原为N 2 的热化学方程式为______.
(2)脱碳.将CO 2 转化为甲醇的热化学方程式为:CO 2 (g)+3H 2 (g)═CH 3 OH(g)+H 2 O(g)△H 3
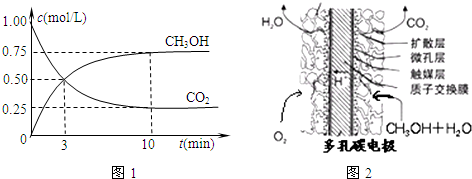
①取五份等体积的CO 2 和H 2 的混合气体(物质的量之比均为1:3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH 3 OH) 与反应温度T的关系曲线如图1所示,则上述CO 2 转化为甲醇的反应的△H 3 ______0(填“>”、“<”或“=”).
②在一恒温恒容密闭容器中充入1mol CO 2 和3mol H 2 ,进行上述反应.测得CO 2 和CH 3 OH(g)的浓度随时间变化如图2所示.试回答:0~10min内,氢气的平均反应速率为______mol/(L•min);该温度下,反应的平衡常数的值为______;第10min后,向该容器中再充入1mol CO 2 和3mol H 2 ,则再次达到平衡时CH 3 OH(g)的体积分数______(填变大、减少、不变).
(3)脱硫.某种脱硫工艺中将废气经处理后,与一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物作为副产品化肥.硫酸铵和硝酸铵的水溶液的pH<7,其原因用离子方程式表示为______;在一定物质的量浓度的硝酸铵溶液中滴加适量的NaOH溶液,使溶液的pH=7,则溶液中c(Na + )+c(H + )______c(NO 3 - )+c(OH - )(填写“>”“=”或“<”) 刺鸟腹语录1年前1
刺鸟腹语录1年前1 -
 天天6170 共回答了23个问题
天天6170 共回答了23个问题 |采纳率95.7%(1)已知:①CH 4 (g)+4NO 2 (g)=4NO(g)+CO 2 (g)+2H 2 O(g)△H 1 =-574kJ•mol -1 ②CH 4 (g)+4NO(g)=2N 2 (g)+CO 2 (g)+2H 2 O(g)△H 2 =-1160kJ•mol -1 则CH 4 (g)+2NO 2 (g)=N 2 ...1年前查看全部
- 下图是某燃煤发电厂利用海水洗脱燃煤烟气中的SO 2 装置示意图。已知洗过烟气后的海水与氧气反应的产物是硫酸钠和盐酸。下列
下图是某燃煤发电厂利用海水洗脱燃煤烟气中的SO 2 装置示意图。已知洗过烟气后的海水与氧气反应的产物是硫酸钠和盐酸。下列说法不正确的是 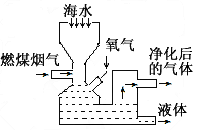 [ ]
[ ]A.该脱硫过程发生的是化学变化
B.使用此废气处理装置可减少酸雨的形成
C.海水法脱硫工艺要求设备耐腐蚀
D.海水中只有氯化钠参与脱硫过程 hh才子1年前1
hh才子1年前1 -
 ths1984 共回答了17个问题
ths1984 共回答了17个问题 |采纳率76.5%D1年前查看全部
- 某研究人员按如图所示流程进行“燃煤烟气的脱硫研究”.实验中,SO 2 和O 2 的混合气体连续通入,水和铁在起始时一次性
某研究人员按如图所示流程进行“燃煤烟气的脱硫研究”.实验中,so 2 和o 2 的混合气体连续通入,水和铁在起始时一次性加入,反应液多次循环. 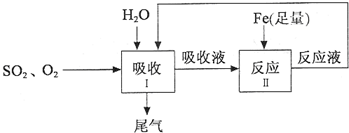
(1)Ⅰ中发生反应的化学方程式是2so 2 +2h 2 o+o 2 ═2x,则x的化学式是______.
(2)Ⅱ中发生反应的化学方程式是______.
(3)随着反应液流入Ⅰ中,吸收液中x的生成速率明显加快,其原因可能是______.
(4)经过多次循环后,反应液可以用来制备feso 4 •7h 2 o,它在医疗上常用于治疗______(选填字母).
a.甲状腺肿***.佝偻病c.龋齿d.贫血症. hw20051年前1
hw20051年前1 -
 jasowood 共回答了19个问题
jasowood 共回答了19个问题 |采纳率89.5%(1)反应前S:2,O:8,H:4,反应后一个X分子的组成为2个氢原子、1个硫原子、4个氧原子,故化学式为:H 2 SO 4 ;
(2)铁与硫酸反应生成硫酸亚铁和氢气的写出化学方程式为:Fe+H 2 SO 4 =FeSO 4 +H 2 ↑;
(3)吸收液中X的生成速率明显加快,其原因可能是生成的Fe 2+ 对Ⅰ中发生的反应起催化作用;
(4)贫血可能缺少铁元素,故选D.
答案:
(1)H 2 SO 4
(2)Fe+H 2 SO 4 =FeSO 4 +H 2 ↑
(3)反应液中的Fe 2+ 对Ⅰ中发生的反应起催化作用
(4)D1年前查看全部
- 如图是某燃煤发电厂处理废气的装置示意图,装置内发生的主要反应中不含( )。
如图是某燃煤发电厂处理废气的装置示意图,装置内发生的主要反应中不含( )。
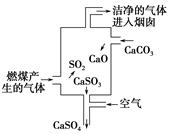
A.化合反应 B.分解反应 C.置换反应 D.氧化还原反应  OliverBierhoff1年前1
OliverBierhoff1年前1 -
 sbyacx 共回答了17个问题
sbyacx 共回答了17个问题 |采纳率100%1年前查看全部
- 在燃煤的火炉中,会发生多个化学反应.
在燃煤的火炉中,会发生多个化学反应.
在火炉中,最底层是空气,中间是煤,最上层是蓝色火焰.
在炉底,充足的空气和红热的煤发生的只要反应方程式为___;产生的气体上升与上一层红热的煤反应,方程式为___;生成的气体继续上升,遇到从炉口进入的空气,发生反应并发出蓝色火焰的方程式为___.
(请一一回答,) 花香浓1年前1
花香浓1年前1 -
 anboooo 共回答了14个问题
anboooo 共回答了14个问题 |采纳率85.7%C+O2=CO2(点燃)
CO2+C=2CO(高温)
2CO+O2=2CO2(点燃)1年前查看全部
- 酸雨给人类带来了种种灾祸,严重地威胁着地球生命生存的生态环境,下列有关减少或防止酸雨形成的措施中可行的是 ①对燃煤进行脱
酸雨给人类带来了种种灾祸,严重地威胁着地球生命生存的生态环境,下列有关减少或防止酸雨形成的措施中可行的是 ①对燃煤进行脱硫;②对含SO 2 、NO 2 等的工业废气进行无害处理后,再排放到大气中;③人工收集雷电作用所产生的氮的氧化物;④飞机、汽车等交通工具采用清洁燃料,如天然气、甲醇等。()
A.①②③④ B.①②③ C.①②④ D.①③④  chenyu8211年前1
chenyu8211年前1 -
 太空水 共回答了22个问题
太空水 共回答了22个问题 |采纳率63.6%C
1年前查看全部
- 下列说法中错误的是( )A.放热反应可能开始需要加热才能发生B.只有达到活化能的分子才能发生有效碰撞C.燃煤火电厂能量
下列说法中错误的是( )
A.放热反应可能开始需要加热才能发生
B.只有达到活化能的分子才能发生有效碰撞
C.燃煤火电厂能量转换过程是:化学能→热能→机械能→电能
D.增加炼铁高炉的高度,可以降低高炉气中CO的含量 li_dong1年前1
li_dong1年前1 -
 心不变价 共回答了16个问题
心不变价 共回答了16个问题 |采纳率68.8%解题思路:A.放反应是放热反应还是吸热反应与反应条件无关系;
B.能够发生有效碰撞的一定是活化分子,但是活化分子不一定发生有效碰撞;
C.燃料在锅炉中燃烧加热水使成蒸汽,将燃料的化学能转变成热能,蒸汽压力推动汽轮机旋转,热能转换成机械能,然后汽轮机带动发电机旋转,将机械能转变成电能;
D.增加炼铁高炉的高度,不能改变平衡状态.A.反应是放热反应还是吸热反应与反应条件无关系,只与反应物和生成物总能量的相对大小有关系,因此放热反应可能开始需要加热才能发生,故A正确;
B.只有达到活化能的分子即活化分子才能发生有效碰撞,故B正确;
C.燃煤火电厂能量转换过程是:燃料在锅炉中燃烧加热水使成蒸汽,将燃料的化学能转变成热能,蒸汽压力推动汽轮机旋转,热能转换成机械能,然后汽轮机带动发电机旋转,将机械能转变成电能,即化学能→热能→机械能→电能,故C正确;
D.增加炼铁高炉的高度,不能改变平衡状态,因此不可以降低高炉气中CO的含量,故D错误.
故选D.点评:
本题考点: 反应热和焓变.
考点点评: 本题考查放热反应、活化能、能量转化和化学平衡,题目难度不大,注意掌握增加炼铁高炉的高度,不能改变平衡状态,因此不可以降低高炉气中CO的含量.1年前查看全部
- (3分)下图是某燃煤发电厂处理废气的装置示意图。
(3分)下图是某燃煤发电厂处理废气的装置示意图。
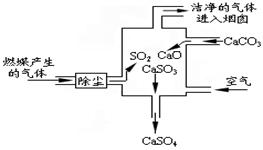
1、使用此废气处理装置,可减少 的排放,从而减少酸雨对环境造成的危害;
2.写出该电厂处理废气的总的化学反应方程式 蔚水1年前1
蔚水1年前1 -
 幸福着快乐着 共回答了23个问题
幸福着快乐着 共回答了23个问题 |采纳率87%(1)SO 2 (2)2CaCO 3 +O 2 +SO 2 =2CaSO 4 +2CO 2
1年前查看全部
- 我国北方地区冬季用燃煤取暖所造成的大气污染,已越来越引起人们的关注.现在有些家庭已经改用燃油取暖,以降低对大气的污染.小
我国北方地区冬季用燃煤取暖所造成的大气污染,已越来越引起人们的关注.现在有些家庭已经改用燃油取暖,以降低对大气的污染.小明家的住房面积约为110m^2,若将住房的门窗关闭好,用燃烧柴油来取暖,并使室温升高10摄氏度,以知柴油的热值为4.3*10^7J/kg,空气的密度约为1.3kg/m^3,空气的比热容为1.0*10^3J/(kg℃),所需的柴油为 多少千克?
 米花饭团t341年前1
米花饭团t341年前1 -
 接龙777 共回答了16个问题
接龙777 共回答了16个问题 |采纳率93.8%假设房子高是3m
房子中空气质量=3*110*1.3=429kg
Q=Cm(t-t0)=1000*10*429=4.29*10^6J
Q=mq
4.29*10^6J÷4.3*10^7J=0.09977kg
约为0.1kg1年前查看全部
- 不属于“雾霾”等灾害性天气治理的措施是 A.外出时使用 PM2.5 口罩,减少有害物质的吸入 B.改燃煤为燃气,可减少废
不属于“雾霾”等灾害性天气治理的措施是
A.外出时使用 PM2.5 口罩,减少有害物质的吸入 B.改燃煤为燃气,可减少废气中SO 2 等有害物质的量 C.利用太阳能、潮汐能、风力发电,以获取清洁能源 D.使用“乙醇汽油”,减少汽车尾气中有害气体的排放  秋水伊伊1年前1
秋水伊伊1年前1 -
 小焰火 共回答了15个问题
小焰火 共回答了15个问题 |采纳率73.3%A
1年前查看全部
- 下列能量转化中,由化学能转化为电能的是( ) A.水力发电 B.燃煤发电 C.太阳能发电 D.风力发电
 云591年前1
云591年前1 -
 尘念佛心 共回答了16个问题
尘念佛心 共回答了16个问题 |采纳率87.5%物质的状态变化一般伴随着能量变化.物理变化中不一定存在能量变化,但物质的化学变化过程一定伴随能量变化.
判断的关键是看是否发生了化学变化.选项A、C、D中尽管有能量的转化,但是没有新物质的生成,均属于物理变化.
只有B项燃煤发电,通过煤的燃烧释放能量,有新物质的生成,属于化学变化.
故选B.1年前查看全部
- (2014•浙江模拟)最近,我国大部分地区多次出现雾霾天气,一个重要的原因是燃煤、机动车尾气排放等,进行煤的综合利用,使
(2014•浙江模拟)最近,我国大部分地区多次出现雾霾天气,一个重要的原因是燃煤、机动车尾气排放等,进行煤的综合利用,使用清洁能源有利于减少环境污染.以下是对煤进行处理的方法:
(1)将水蒸气通过红热的碳即可产生水煤气,其反应为:
C(s)+H2O(g)⇌CO(g)+H2(g)△H=+131.3kJ•mol-1,该反应在______下能自发进行(填“高温”或“低温”);
(2)合成氨工业原料气的来源之一水煤气法,在催化剂存在条件下有下列反应:
H2O(g)+CO(g)⇌CO2(g)+H2(g),控制反应条件CO转化率随氢碳比的变化如图甲所示:
①该反应△H______0(填“>”或“<”);
②对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(cB)也可以表示平衡常数(记作KP),则该反应的KP=P(CO2)P(H2) P(CO)P(H2O) ,提高P(CO2)P(H2) P(CO)P(H2O)
比,则KP______(填“变大”、“变小”或“不变”),实际上,在使用铁镁催化剂的工业流程中,一般采用400℃左右,H2O(气):CO=3~5:1;其原因可能是______.H2O(气) CO
③将1mol CO和1mol H2O(g)充入某固定容积的反应器,在某条件下达到平衡,此时有[2/3]的CO转化为CO2.在t1时,再充入1mol H2O(g),请在该图乙中画出t1时刻后CO2的体积分数变化趋势曲线.
(3)用半水煤气(CO、H2)来合成甲醇汽油可以有效的减少汽车尾气中CO的含量.如图丙是甲醇燃料电池原理示意图,回答下列问题:
电池的负极是______(填“a”或“b”)电极,该极的电极反应是:______. likeupc1年前1
likeupc1年前1 -
 wcmei86 共回答了24个问题
wcmei86 共回答了24个问题 |采纳率91.7%解题思路:(1)根据△G=△H-T△S判断,△G<0,反应自发进行;
(2)①结合图象根据其他条件相同时,温度升高,平衡向吸热的方向移动;
②将化学平衡常数中的浓度c换成压强P就可以得到KP;根据平衡常数只与温度有关,与浓度无关;
投料比太低,CO的转化率不太高,投料比太高,经济上不合算以及考虑催化剂的活性来解答;
③根据三段式解题法,求出平衡时各组分的物质的量,求出平衡时CO2的体积分数;假设加入1mol水蒸气时平衡不移动,求出此时CO2的体积分数,设1molCO完全转化,求出CO2的最大体积分数,从而得出CO2 体积分数范围,最后作图;
(3)根据燃料电池中燃料在负极发生反应,氧气在正极发生反应;甲醇失电子和氢氧根离子反应生成碳酸根离子和水.(1)由热化学反应方程式可知,该反应为焓增、熵增过程,即△H>0、△S>0,必须满足△G=△H-T△S<0反应才能自发进行,所以在高温下能够自发进行;
故答案为:高温;
(2)①结合图象可知,升高温度,CO的转化率降低,平衡逆向移动,而其他条件相同时,温度升高,平衡向吸热的方向移动,即正反应为放热反应,△H<0;
故答案为:<;
②CH4(g)+H2O(g)⇌CO(g)+3H2(g),对于气相反应,用某组分(B)的平衡压强(pB)代替物质的量浓度也可以表示平衡常数(记作Kp),反应的平衡常数=
P(CO2)P(H2)
P(CO)P(H2O);平衡常数只与温度有关,与浓度无关,所以提高
H2O(气)
CO比,则KP不变;
故答案为:
P(CO2)P(H2)
P(CO)P(H2O);不变;
③由图象可知,投料比太低,CO的转化率不太高,而投料比3~5:1时转化率已经很高达到96%~98%,再增加投料比,需要大大的增加蒸汽添加量,这样在在经济上不合算,催化剂的活性温度在400℃左右,所以一般采用400℃左右,H2O(气):CO=3~5:1;
故答案为:投料比太低,CO的转化率不太高,而投料比3~5:1时转化率已经很高达到96%~98%,再增加投料比,需要大大的增加蒸汽添加量,这样在在经济上不合算,催化剂的活性温度在400℃左右;
③CO(g)+H2O(g)⇌H2(g)+CO2(g)
起始(mol):1 1 0 0
转化(mol):[2/3] [2/3] [2/3] [2/3]
平衡(mol):[1/3] [1/3] [2/3] [2/3]
反应前后气体的体积不变,所以平衡时,混合气体的总的物质的量为1mol+1mol=2mol,
所以平衡混合物中CO2的体积分数为
2
3mol
2mol×100%=33.3%;
假设加入1mol 水蒸气时平衡不移动,此时CO2占
2
3mol
3mol=[2/9] 即22.2%,设1molCO完全转化,生成1molCO2 占[1mol/3mol]=[1/3]即33.3%,所以CO2体积分数在22.2%~33.3%之间,要比原平衡低,图象为: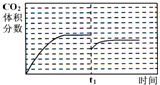 ;
;
答:t1时刻后CO2的体积分数变化趋势曲线为: ;
;
(3)由图可知,在a极燃料甲醇发生反应,所以负极是a点评:
本题考点: 反应热和焓变;化学电源新型电池;物质的量或浓度随时间的变化曲线;产物的百分含量随浓度、时间的变化曲线.
考点点评: 本题考查了反应的自发性、外界条件对化学平衡的影响、图象分析判断的方法、平衡三段法的计算、原电池原理的分析判断和电极反应的分析判断,掌握基础是解题的关键,题目难度中等.1年前查看全部
- 下列说法中,错误的是( ) A.用熟石灰处理含酸量超标的工业污水 B.煤气中毒通常是指一氧化碳中毒 C.使用燃煤脱硫技
下列说法中,错误的是( ) A.用熟石灰处理含酸量超标的工业污水 B.煤气中毒通常是指一氧化碳中毒 C.使用燃煤脱硫技术防止二氧化硫污染 D.铵态氮肥可与碱性物质混合使用  whitebirdzr1年前1
whitebirdzr1年前1 -
 烧火凤凰 共回答了20个问题
烧火凤凰 共回答了20个问题 |采纳率95%A、熟石灰显碱性,所以可以处理含酸量超标的工业污水,故A正确;
B、煤气中毒通常是指一氧化碳中毒,故B正确;
C、硫燃烧生成二氧化硫,使用燃煤脱硫技术防止二氧化硫污染,故C正确;
D、铵态氮肥可与碱性物质混合会放出氨气,所以不可混用,故D错误.
故选:D.1年前查看全部
- 科盲再酿悲剧!2008年12月1日,陕西某小学用炭炉直接燃煤取暖,不慎导致11名学生中毒身亡!
 科盲再酿悲剧!2008年12月1日,陕西某小学用炭炉直接燃煤取暖,不慎导致11名学生中毒身亡!
科盲再酿悲剧!2008年12月1日,陕西某小学用炭炉直接燃煤取暖,不慎导致11名学生中毒身亡!
(1)煤、______和天然气都属于化石燃料,煤等燃料燃烧时,如果______不足,燃烧就不完全,会产生大量的______气体,污染空气;煤中所含的硫、氮等元素燃烧时还会产生______等大气污染物,是导致酸雨形成的主要原因.
(2)为减少煤燃烧对大气造成的污染,目前采取了改善燃煤质量、改进燃烧装置和燃烧技术等多种措施,如向煤中加入适量的石灰石,反应如下:
2CaCO3+O2+2X═2CaSO4+2CO2,则X的化学式为______.
(3)科学家预言,氢能将成为21世纪的主要绿色能源,而水是自然界中广泛存在的物质,你认为获取氢气的最佳途径是______.氢能源的优点有______、发热高、来源广、是再生能源等.
(4)为了缓解化石能源面临耗尽的问题,世界各国都在开发利用其它新能源.利用高纯单质硅的半导体性能,可以制成光电池,将______能直接转化为电能.光电池可以用作计算器、人造卫星、登月车等的动力,是极有发展前景的新型能源. 三月丫头Q娃娃1年前1
三月丫头Q娃娃1年前1 -
 风舞玥 共回答了19个问题
风舞玥 共回答了19个问题 |采纳率94.7%解题思路:化石燃料不完全燃烧时能产生大量的污染空气的物质,如一氧化碳、二氧化硫等物质,根据化学方程式可以判断物质的化学式,要充分理解节能环保的重要性.(1))煤、石油和天然气都属于化石燃料,煤等燃料燃烧时,如果氧气不足,燃烧就不完全,会产生大量的一氧化碳气体,污染空气;煤中所含的硫、氮等元素燃烧时还会产生二氧化硫、二氧化氮等大气污染物,是导致酸雨形成的主要原因.
故填:石油;氧气;一氧化碳;二氧化硫、二氧化氮.
(2)根据2CaCO3+O2+2X═2CaSO4+2CO2可知,X中含有1个硫原子和2个氧原子,是二氧化硫.故填:SO2;
(3)获取氢气的最佳途径是利用太阳能分解水;故填:太阳能分解水;
氢能源的优点有无污染、发热高、来源广、是再生能源等.故填:无污染.
(4)光电池可以将太阳能直接转化为电能.故填:太阳.点评:
本题考点: 常用燃料的使用与其对环境的影响;有关化学式的计算和推断;物质发生化学变化时的能量变化;质量守恒定律及其应用;化石燃料及其综合利用;氢气的用途和氢能的优缺点.
考点点评: 解答本题的关键是要掌握化石燃料燃烧的情况和节能环保的重要性,只有这样才能对问题做出正确的判断.1年前查看全部
- (2005•青岛)小丽同学在学习了燃烧与燃料的有关知识后,观察到家庭用的燃煤通常加工成蜂窝状,这样会燃烧得更充分.由此她
(2005•青岛)小丽同学在学习了燃烧与燃料的有关知识后,观察到家庭用的燃煤通常加工成蜂窝状,这样会燃烧得更充分.由此她联想到细铁丝在空气中不能燃烧,而在氧气中能剧烈燃烧.于是引发了思考:哪些因素能影响可燃物燃烧的剧烈程度呢?她做出两种猜想并进行了实验探究.请你回答有关问题:
(1)她提出的两种猜想是:①______②______
(2)请选择其中的一种猜想,设计实验加以探究(你所选择的猜想序号______):
(3)为了能使燃料能够得到充分利用,节约能源,请你结合燃料使用的实际,提出一条具体节能的建议:______.实验操作 实验现象 实验结论 ______ ______ ______  leaou1261年前1
leaou1261年前1 -
 zhongjiangsyd 共回答了20个问题
zhongjiangsyd 共回答了20个问题 |采纳率95%解题思路:(1)根据铁丝在氧气中剧烈燃烧和燃煤加工成蜂窝煤使燃烧更充分,可以想到燃烧与氧气的浓度和与氧气的接触面积有关;
(2)如选择“①氧气的浓度”进行探究,可用在空气中的燃烧物再放到纯氧中,并观察其变化,写出现象与结论;如选择“②可燃物与氧气的接触面积”进行探究,可用增加燃烧物与氧气的接触面积与普通情况下对比,并观察其变化,写出现象与结论;
(3)根据(2)小题的试验可知,要使燃料得到充分的燃烧,就要增加氧气的浓度或增大与氧气的接触面积.可据此写出使燃料得到充分利用的方法.(1)细铁丝在空气中不能燃烧,而在氧气中能剧烈燃烧.说明氧气的浓度大小影响燃烧的程度;家庭用的燃煤通常加工成蜂窝状,这样就增加了与空气的接触面积,这样会燃烧得更充分.说明物质与氧气的接触面积大小影响燃烧.故答案为:①氧气的浓度;②可燃物与氧气的接触面积.
(2)若选①氧气的浓度.可进行如下实验操作:
实验操作:在空气中燃烧红热的木炭放在盛有氧气的集气瓶中;
实验现象:发出白光;
实验结论:增大氧气的浓度能促进可燃物的燃烧.
若选择②可燃物与氧气的接触面积.可进行如下实验操作:
实验操作:把在空气中燃烧不太旺盛的木炭截成小段;
实验现象:木炭燃烧更旺;
实验结论:增大可燃物与氧气的接触面积能促进可燃物的燃烧.
(3)在生活中为使燃料燃烧充分,可通过增大与可燃物与氧气的接触面积或增大与氧气的接触面积.如将煤或其他燃料加工成粉末状(或燃料燃烧时不断鼓入空气)点评:
本题考点: 燃烧的条件与灭火原理探究.
考点点评: 本题考查物质燃烧的条件,以及在生活中的应用.激发学生学习化学的兴趣.1年前查看全部
- 下列相关措施有利于保护环境的是( ) A.造纸厂直接将污水排放到附近的河流中 B.将烟囱加高以减少燃煤产生的SO 2
下列相关措施有利于保护环境的是( ) A.造纸厂直接将污水排放到附近的河流中 B.将烟囱加高以减少燃煤产生的SO 2 等气体污染环境 C.将废旧电池投于有害垃圾箱,集中回收处理 D.将废弃塑料袋、一次性饭盒等塑料制品深埋于地下处理  小东西毛毛1年前1
小东西毛毛1年前1 -
 ragi君 共回答了17个问题
ragi君 共回答了17个问题 |采纳率94.1%A、造纸厂应将废水处理后排放到水中就不会有污染了,而不应该直接排放带河流中,故A错误;
B、增加烟筒的高度虽然可以使周围地表面SO2的含量减少,但是二氧化硫的排放总量不变,且污染范围扩大了,故B错误;
C、废电池随意丢弃会造成水体污染和土壤污染,不随意丢弃废电池有利于环境保护,故C正确;
D、塑料、一次性饭盒难以降解,可以深埋于地下处理或尽量使用可降解塑料制品,减少塑料垃圾的污染,即控制了白色污染问题;有利于环境保护.
故选C1年前查看全部
- 以1kg/s的速率烧煤,已知煤的含硫量为3%,计算每年的so2的排放量.计算时通常假设燃煤有5%的硫最终残留在有5%的灰
以1kg/s的速率烧煤,已知煤的含硫量为3%,计算每年的so2的排放量.计算时通常假设燃煤有5%的硫最终残留在有5%的灰分中!
 今雨rain1年前1
今雨rain1年前1 -
 红苹果蓝彤彤 共回答了20个问题
红苹果蓝彤彤 共回答了20个问题 |采纳率90%煤炭的含硫量是3%,每千克煤含硫1000×3%=300(克),
燃烧后,每一个硫原子和空气中的两个氧原子组成一个二氧化硫分子,硫原子量是32、二氧化硫的分子量是64,因此,煤燃烧1克硫,产生的二氧化硫是:1×(64/32)=2(克).
1克硫经燃烧后有5%残留在灰分中,一年365天,每天24小时,每小时60分钟,每分钟60秒.
因此:
2×(1-5%)×365×24×60×60=59918400(克)=59918.4(千克)=59.9184(吨)1年前查看全部
- 燃煤时加石灰石?碳酸钙在高温下才分解成氧化钙啊!燃煤能到达那么高温度?难道是石灰石直接和二氧化硫反应?
 gy20001年前1
gy20001年前1 -
 woshimina 共回答了19个问题
woshimina 共回答了19个问题 |采纳率94.7%800度时碳酸钙就分解了,燃煤可达到1000多度
石灰石在500度以上就可以和SO2反应生成CaSO3放出CO2
物质的热力学稳定性决定了这些1年前查看全部
- 某地修建了一座燃煤的火力发电厂.几年后,原来长在这里的许多绿茸茸的苔藓不见了.这是为什么?
 涓滴浪1年前1
涓滴浪1年前1 -
 吃野牛粪 共回答了25个问题
吃野牛粪 共回答了25个问题 |采纳率80%因为污染太严重了,苔藓对环境要求很高,.1年前查看全部
- 大量燃煤(含杂志硫、氮等) 造成主要的环境问题有 a 酸雨 b 臭氧空洞 c 沙尘暴 d 温室效应
 pxlx1年前1
pxlx1年前1 -
 toshi2007 共回答了16个问题
toshi2007 共回答了16个问题 |采纳率87.5%a 酸雨1年前查看全部
- 某地修建了一座燃煤的火力发电厂,几年后这里许多绿茸茸的苔藓植物都不见了,为什么?
 aa浪子1101年前1
aa浪子1101年前1 -
 minwoo728 共回答了19个问题
minwoo728 共回答了19个问题 |采纳率89.5%解题思路:此题考查的是苔藓植物与人类的关系,据此答题.煤燃烧产生大量的有害气体,如二氧化硫等,由于苔藓植物的叶只有一层细胞,二氧化硫等有毒气体可以从背腹两面侵入叶细胞,威胁到苔藓植物的生存.燃煤火力发电厂在燃煤的过程中会产生大量的二氧化硫等有毒气体,影响苔藓植物的生存,因此在污染严重的火力发电厂附近,苔藓植物一般很少见.
故答案为:苔藓植物的叶只有一层细胞,二氧化硫等有毒气体可以从背腹两面侵入叶细胞,威胁到苔藓植物的生存,燃煤火力发电厂在燃煤的过程中会产生大量的二氧化硫等有毒气体,影响苔藓植物的生存,因此在污染严重的火力发电厂附近,苔藓植物一般很少见.点评:
本题考点: 苔鲜的主要特征及其与人类生活的关系;人类活动对环境的影响.
考点点评: 苔藓植物与人类的关系在考试中经常出现,多以选择题的形式,注意掌握.1年前查看全部
- 炼钢厂有一堆煤,计划每天烧10吨,可以维持三个月(每月按30天计算),后来采用新技术,燃煤量大大节省,
炼钢厂有一堆煤,计划每天烧10吨,可以维持三个月(每月按30天计算),后来采用新技术,燃煤量大大节省,
结果这堆煤用了4个月.每天燃煤节省百分之几? qqq161年前1
qqq161年前1 -
 小敏1986123 共回答了15个问题
小敏1986123 共回答了15个问题 |采纳率73.3%(1/3-1/4)÷1/3
=1/12÷1/3
=1/4
=25%1年前查看全部
- 用氨水脱去燃煤烟气中的硫不需要除去二氧化碳的原因是什么?
 Chevalière1年前1
Chevalière1年前1 -
 小人1 共回答了20个问题
小人1 共回答了20个问题 |采纳率90%亚硫酸比碳酸酸性强,二氧化碳不影响氨水脱去烟气当中的二氧化硫.1年前查看全部
- 燃煤产生什么污染气体这些污染气体对人体有什么危害?
 jzt9jbcl1年前3
jzt9jbcl1年前3 -
 nilu33 共回答了17个问题
nilu33 共回答了17个问题 |采纳率88.2%二氧化硫 在空气中会造成酸雨
一氧化碳 有毒
一些硫的气体化合物 污染空气1年前查看全部
- 我国北方地区冬季用燃煤取暖所造成的大气污染,已越来越引起人们的关注.现在有些家庭已经改用燃油取暖,以降低对大气的污染.小
我国北方地区冬季用燃煤取暖所造成的大气污染,已越来越引起人们的关注.现在有些家庭已经改用燃油取暖,以降低对大气的污染.小明家的住房面积约110m 2 ,若将住房的门窗关闭好,用燃烧柴油来取暖,并使室温升高10℃,已知柴油的热值为4.3×lO 7 J/kg,空气的密度约为1.3kg/m 3 ,空气的比热容为1.0×10 3 J/(kg•℃)所需的柴油约为( ) A.0.0lkg B.0.1kg C.1kg D.10kg  塑料是怎样炼成的1年前1
塑料是怎样炼成的1年前1 -
 y200ee722 共回答了22个问题
y200ee722 共回答了22个问题 |采纳率95.5%由题知,S=110m 2 ,住房高度h一般为3m,ρ 空气 =1.3kg/m 3 ,
则住房房间里的空气质量为:
m 空气 =ρ 空气 Sh=1.3kg/m 3 ×110m 2 ×3m=429kg,
室温升高10℃时空气所吸收的热量:
Q 吸 =c 空气 m 空气 △t=1.0×10 3 J/(kg•℃)×429kg×10℃=4.29×10 6 J
∵Q 放 =Q 吸 ,
∴又Q=mq得:
m=
Q
q =
4.29× 10 6 J
4.3× 10 7 J/kg =0.1kg.
故选B1年前查看全部
- 某地修建了一座燃煤的火力发电厂,几年后这里许多绿茸茸的苔藓植物都不见了,为什么?
 最爱_敏敏1年前1
最爱_敏敏1年前1 -
 iceageiris 共回答了17个问题
iceageiris 共回答了17个问题 |采纳率94.1%解题思路:此题考查的是苔藓植物与人类的关系,据此答题.煤燃烧产生大量的有害气体,如二氧化硫等,由于苔藓植物的叶只有一层细胞,二氧化硫等有毒气体可以从背腹两面侵入叶细胞,威胁到苔藓植物的生存.燃煤火力发电厂在燃煤的过程中会产生大量的二氧化硫等有毒气体,影响苔藓植物的生存,因此在污染严重的火力发电厂附近,苔藓植物一般很少见.
故答案为:苔藓植物的叶只有一层细胞,二氧化硫等有毒气体可以从背腹两面侵入叶细胞,威胁到苔藓植物的生存,燃煤火力发电厂在燃煤的过程中会产生大量的二氧化硫等有毒气体,影响苔藓植物的生存,因此在污染严重的火力发电厂附近,苔藓植物一般很少见.点评:
本题考点: 苔鲜的主要特征及其与人类生活的关系;人类活动对环境的影响.
考点点评: 苔藓植物与人类的关系在考试中经常出现,多以选择题的形式,注意掌握.1年前查看全部
- 某地修建了一座燃煤的火力发电厂,几年后这里许多绿茸茸的苔藓植物都不见了,为什么?
 huanhuan_aa1年前1
huanhuan_aa1年前1 -
 左眼泪 共回答了16个问题
左眼泪 共回答了16个问题 |采纳率75%解题思路:此题考查的是苔藓植物与人类的关系,据此答题.煤燃烧产生大量的有害气体,如二氧化硫等,由于苔藓植物的叶只有一层细胞,二氧化硫等有毒气体可以从背腹两面侵入叶细胞,威胁到苔藓植物的生存.燃煤火力发电厂在燃煤的过程中会产生大量的二氧化硫等有毒气体,影响苔藓植物的生存,因此在污染严重的火力发电厂附近,苔藓植物一般很少见.
故答案为:苔藓植物的叶只有一层细胞,二氧化硫等有毒气体可以从背腹两面侵入叶细胞,威胁到苔藓植物的生存,燃煤火力发电厂在燃煤的过程中会产生大量的二氧化硫等有毒气体,影响苔藓植物的生存,因此在污染严重的火力发电厂附近,苔藓植物一般很少见.点评:
本题考点: 苔鲜的主要特征及其与人类生活的关系;人类活动对环境的影响.
考点点评: 苔藓植物与人类的关系在考试中经常出现,多以选择题的形式,注意掌握.1年前查看全部
- 火力发电厂释放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等气体会造成环境污染.对燃煤废气进行脱硝、脱硫和脱碳等处理,
火力发电厂释放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等气体会造成环境污染.对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的.
(1)脱硝.利用甲烷催化还原NOx:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ•mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2=-1160kJ•mol-1
甲烷直接将NO2还原为N2的热化学方程式为______.
(2)脱碳.将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g);△H3<0
①在一恒温恒容密闭容器中充入1mol CO2和3mol H2,进行上述反应.测得CO2和CH3OH(g)的浓度随时间变化如图1所示.下列说法正确的是______(填字母代号).
A.第10min后,向该容器中再充入1mol CO2和3mol H2,则再次达到平衡时c(CH3OH)=1.5mol•L-1
B.0~10min内,氢气的平均反应速率为0.075mol/(L•min)
C.达到平衡时,氢气的转化率为75%
D.该温度下,反应的平衡常数的值为[3/16]
E.升高温度将使
减小n(CH3OH) n(CO2)
②甲醇燃料电池结构如图2所示.其工作时正极的电极反应式可表示为:______.
(3)脱硫.某种脱硫工艺中将废气经处理后,与一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物作为副产品化肥.硫酸铵和硝酸铵的水溶液的pH<7,其中原因可用一个离子方程式表为:______;在一定物质的量浓度的硝酸铵溶液中滴加适量的NaOH溶液,使溶液的pH=7,则溶液中:c(Na+)+c(H+)______c(NO3-)+c(OH-)(填写“>”“=”或“<”). 冷月心蓝1年前1
冷月心蓝1年前1 -
 25只蜜蜂 共回答了20个问题
25只蜜蜂 共回答了20个问题 |采纳率95%解题思路:(1)利用盖斯定律分析;
(2)①A、再充入1mol CO2和3mol H2,可等效为开始体积变为原来的2倍,加入2mol CO2和6mol H2,平衡后,再将体积压缩为原来的体积,增大压强平衡向体积减小的方向移动,即向正反应移动,反应物的转化率增大;
B、利用v=[△n/△t]计算v(H2)判断;
C、根据转化率的定义计算判断;
D、该温度下该反应的K=
,代入数据计算;[CH3OH][H2O] [CO2][H2]3
E、该反应为放热反应,升高温度平衡向逆反应进行,n(CH3OH)减小,n(CO2)增大.
②正极上氧化剂得电子发生还原反应;
(3)强酸弱碱盐易水解而使其溶液呈酸性,根据电荷守恒判断.(1)已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ•mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2=-1160kJ•mol-1
不管化学反应是一步完成还是分几步完成,其反应热是相同的.两式相加,可得
2CH4(g)+4NO2(g)=2N2(g)+2CO2(g)+4H2O(g)△H=-1734 kJ/mol
即CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867 kJ•mol-1
故答案为:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867 kJ•mol-1;
(2)①由图2可知,开始二氧化碳的浓度为1.0mol/L,开始容器中充入1mol CO2和3mol H2,所以开始氢气的浓度为3.0mol/L,容器体积为[1.0mol/1.0mol/L]=1L.
平衡时,甲醇的浓度为0.75mol/L
CO2(g)+3H2(g)
一定条件
CH3OH(g)+H2O(g)
开始(mol/L):1 3 0 0
变化(mol/L):0.75 2.250.75 0.75
平衡(mol/L):0.25 0.750.75 0.75
A、通过上述计算可知二氧化碳的转化率为[0.75mol/L/1.0mol/L]×100%=75%,再充入1mol CO2和3mol H2,可等效为开始体积变为原来的2倍,加入2mol CO2和6mol H2,平衡后,再将体积压缩为原来的体积,增大压强平衡向体积减小的方向移动,即向正反应移动,反应物的转化率增大,所以再次达到平衡时c(CH3OH)>1.5mol/L,故A错误;
B、10分钟内,氢气的平均反应速率为v(H2)=[2.25mol/L/10min]=0.225mol/(L•min),故C错误;
C.通过上述计算可知氢气的转化率为[2.25mol/L/3mol/L]×100%=75%,故C正确;
D、该温度下该反应的K=
[CH3OH][H2O]
[CO2][H2]3=[0.75×0.75
0.25×(0.75)3=
16/3],故D错误;
E、该反应为放热反应,升高温度平衡向逆反应进行,n(CH3OH)减小,n(CO2)增大,所以n(CH3OH)/n(CO2)值减小,故E正确.
故选:CE;
②正极上氧气得电子和氢离子反应生成水,所以电极反应式为:O2+4e-+4H+=2H2O,故答案为:O2+4e-+4H+=2H2O;
(3)硫酸铵和硝酸铵都是强酸弱碱盐,铵根离子易水解而使其溶液呈酸性,水解离子方程式为:NH4++H2O⇌NH3•H2O+H+,溶液呈中性,则c(H+)=c(OH-),溶液中存在电荷守恒,则c(Na+)+c(H+)+c(NH4+)=c(NO3-)+c(OH-),所以c(Na+)+c(H+)<c(NO3-)+c(OH-),
故答案为:NH4++H2O⇌NH3•H2O+H+;<.点评:
本题考点: 二氧化硫的污染及治理;热化学方程式;化学电源新型电池;化学平衡建立的过程;氮的氧化物的性质及其对环境的影响.
考点点评: 本题考查了盖斯定律、原电池原理、化学平衡、盐类水解等知识点,难点是化学平衡的有关计算,有关化学平衡的计算是考试热点,难度中等.1年前查看全部
- (2013•沈阳一模)位于沈阳市大东区珠林路上的沈阳沈海热电有限公司为全市居民提供着电能.机组利用火力发电,消耗燃煤.而
(2013•沈阳一模)位于沈阳市大东区珠林路上的沈阳沈海热电有限公司为全市居民提供着电能.机组利用火力发电,消耗燃煤.而煤炭同太阳能和水能一样都属于______能源.在家中,用电器在一段时间内消耗的电能通常用电能表来测量.某同学家的电能表上,月初显示为
 ,月末显示为
,月末显示为 .则在这一个月内,该同学家消耗的电能为______kW•h.
.则在这一个月内,该同学家消耗的电能为______kW•h.  nako3501年前1
nako3501年前1 -
 86nga 共回答了18个问题
86nga 共回答了18个问题 |采纳率100%煤炭同太阳能和水能一样都可以从自然界直接获得而不需要加工转换,因此它们都属于一次能源;
由图示可知,该同学家消耗的电能为253.5kW•h-179.3kW•h=74.2kW•h;
故答案为:一次;74.2.1年前查看全部
- 一定条件下发生下列反应可实现燃煤烟气中硫的回收:SO2(g)+2CO(g) 催化剂 .&
一定条件下发生下列反应可实现燃煤烟气中硫的回收:SO2(g)+2CO(g)
2CO2(g)+S(l)△H<0,若反应在恒容的密闭容器中进行,下列有关说法正确的是( )催化剂 .
A.平衡前,随着反应的进行,容器内的压强始终不变
B.平衡时,其他条件不变,分离出硫,正反应速率加快
C.平衡时,其他条件不变,使用合适的催化剂,可提高SO2的转化率
D.其他条件不变,使用不同催化剂,该反应的平衡常数不变 江南好之宝贝1年前1
江南好之宝贝1年前1 -
 理想的小树苗 共回答了14个问题
理想的小树苗 共回答了14个问题 |采纳率100%解题思路:该可逆反应正反应是气体体积减小、放热反应,在反应达到平衡之前,容器内气体的压强在不断减小,分离出液体硫,不影响平衡移动,反应速率不变,使用催化剂只改变化学反应速率但不影响平衡的移动,注意平衡常数只与温度有关,与物质的浓度无关.A.该反应是一个反应前后气体体积减小、放热的可逆反应,在反应达到平衡之前,随着反应的进行,气体的物质的量逐渐减小,则容器的压强在逐渐减小,故A错误;
B.硫是液体,分离出硫,不影响平衡移动,气体反应物和生成物浓度都不变,所以不影响反应速率,故B错误;
C.平衡时,其他条件不变,使用合适的催化剂,不影响平衡移动,不能提高SO2的转化率,故C错误;
D.平衡常数只与温度有关,与使用催化剂无关,故D正确;
故选D.点评:
本题考点: 化学平衡建立的过程.
考点点评: 本题考查了影响化学平衡的因素,难度不大,易错选项是B,注意固体和纯液体改变用量对反应速率无影响,催化剂只影响反应速率不影响平衡的移动.1年前查看全部
- 300MW燃煤电厂计算,锅炉出口二氧化硫浓度计算得1400mg/m3左右.这个数合理么?一般这么大的锅炉二氧化硫浓度范围
300MW燃煤电厂计算,锅炉出口二氧化硫浓度计算得1400mg/m3左右.这个数合理么?一般这么大的锅炉二氧化硫浓度范围多少?
 unicorn12201年前1
unicorn12201年前1 -
 幸福宝贝_hh 共回答了12个问题
幸福宝贝_hh 共回答了12个问题 |采纳率91.7%这个数值很合理,一般在烟气脱硫之前的浓度在一千到一万之间,脱硫效率95%,然后剩余的不到一百,你这个数值很好,属于比较低的.1年前查看全部
- 右图是某燃煤发电厂处理废气的装置示意图.
右图是某燃煤发电厂处理废气的装置示意图.
2SO2+2CaCO3+O2=2CaSO4+2CO2 如果我写长2S+2O2……………………(后面一样)是否正确.图上是这样的燃煤产生的气体(文字)→(一个大的 容器)(图) 木每飞子1年前1
木每飞子1年前1 -
 bzb1006 共回答了17个问题
bzb1006 共回答了17个问题 |采纳率88.2%右图是某燃煤发电厂处理废气的装置示意图.下列说法不正确的是( )
A、根据图示信息可知,进入烟囱的是洁净的气体,并不是纯净物,故选项错误;
B、亚硫酸钙中硫元素的化合价是+4价,硫酸钙中硫元素的化合价是+6价.故选项正确;
C、二氧化硫是形成酸雨的重要物质,经过处理后能减少酸雨的形成.故选项正确;
D、整个过程中,二氧化硫与碳酸钙和氧气反应生成了硫酸钙和二氧化碳,化学反应式可表示为:2SO2+2CaCO3+O2=2CaSO4+2CO2,故选项正确.
故选A.A.进入烟囱的气体为纯净物B.此过程中S元素的化合价发生了改变C.使用此废气处理装置可减少酸雨的形成D.整个过程的反应可表示为:2SO2+2CaCO3+O2═2CaSO4+2CO21年前查看全部
- (2012•沈阳)火力发电厂用燃煤进行发电,由于煤中含有硫元素,燃烧时会产生二氧化硫,所以该发电厂采用石灰石浆吸收废气中
(2012•沈阳)火力发电厂用燃煤进行发电,由于煤中含有硫元素,燃烧时会产生二氧化硫,所以该发电厂采用石灰石浆吸收废气中的二氧化硫以防止污染大气,其发生反应的化学方程式为2CaCO3+2SO2+O2
2CaSO4+2CO2,若处理2000t这种废气(假设废气中的二氧化硫全部被吸收),理论上需要62.6t含碳酸钙80%的石灰石.高温 .
试解答:
(1)若二氧化硫排放到空气中,会造成的环境污染问题是______.
(2)所吸收的废气中二氧化硫的质量分数是多少? 乔峰-阿紫1年前1
乔峰-阿紫1年前1 -
 goodmz 共回答了15个问题
goodmz 共回答了15个问题 |采纳率86.7%解题思路:(1)酸雨产生的原因主要是因为空气中含有二氧化硫、二氧化氮等酸性氧化物引起的.当雨水的pH<5.6时称为酸雨;
(2)根据石灰石浆吸收废气中的二氧化硫的反应方程式找到碳酸钙与二氧化硫的比例关系,根据碳酸钙的质量即可求得所选二氧化硫的质量.(1)雨、雪、雾、霜、露、雹等在降落过程中吸收了空气中的二氧化碳、二氧化硫、氮氧化物等致酸物质,就变成酸性的降水--酸雨.
故填:酸雨;
(2)设废气中二氧化硫的质量为x.则
反应所用CaCO3的质量为:62.6t×80%=50.08t;
2CaCO3+2SO2+O2
高温
.
2CaSO4+2CO2,
200 128
50.08t x
[200/50.08t]=[128/x],
解得,x=32.0512t;
所吸收的废气中二氧化硫的质量分数是:[32.0512/2000t]×100%=1.60256%;
答:所吸收的废气中二氧化硫的质量分数是1.60256%.点评:
本题考点: 含杂质物质的化学反应的有关计算;酸雨的产生、危害及防治.
考点点评: 本题考查了含有杂质物质的化学反应的有关计算.注意,参与反应的反应物的质量应该是纯净物的质量,而非混合物的质量.1年前查看全部
- 右图是某燃煤发电厂处理废气的装置示意图.下列说法正确的是( )
右图是某燃煤发电厂处理废气的装置示意图.下列说法正确的是( )

A.此过程中没有分解反应
B.此过程中S元素的化合价未发生改变
C.二氧化硫是形成酸雨的重要物质
D.整个过程的反应可表示为:2SO2+2CaCO3+O2=2CaSO4+2CO2 yshan1年前1
yshan1年前1 -
 sun212141 共回答了18个问题
sun212141 共回答了18个问题 |采纳率88.9%解题思路:碳酸钙受热生成氧化钙和二氧化碳的反应属于分解反应;根据化合物中元素化合价代数和为零可以求出某种元素的化合价;二氧化硫是形成酸雨的重要物质;根据反应过程可以书写反应的化学方程式.A、碳酸钙受热生成氧化钙和二氧化碳的反应属于分解反应.故选项错误;
B、亚硫酸钙中硫元素的化合价是+4价,硫酸钙中硫元素的化合价是+6价.故选项错误;
C、二氧化硫是形成酸雨的重要物质,经过处理后能减少酸雨的形成.故选项正确;
D、整个过程中,二氧化硫与碳酸钙和氧气反应生成了硫酸钙和二氧化碳.故选项正确.
故选CD.点评:
本题考点: 酸雨的产生、危害及防治;常见元素与常见原子团的化合价;分解反应及其应用.
考点点评: 解答本题要充分理解处理废气的过程,只有这样才能对相关方面的问题做出正确的判断.1年前查看全部
- 3.下列有关防止或减少酸雨的措施中不可行的是 A.对燃煤及燃煤烟气进行脱硫 ...C.人工收集大气雷电产生的氮的氧化物
3.下列有关防止或减少酸雨的措施中不可行的是 A.对燃煤及燃煤烟气进行脱硫 ...C.人工收集大气雷电产生的氮的氧化物 D.推广天然气、甲醇等作为汽车的燃料 A ①②③④ B ①②③ C ①②④ D ①③④
 hezhizhang20001年前1
hezhizhang20001年前1 -
 wh_xb 共回答了24个问题
wh_xb 共回答了24个问题 |采纳率83.3%3、C是错误的.1年前查看全部
- 燃煤烟尘排放量计算项目用煤量600t/a,燃煤含硫量为0.51%.计算二氧化硫的排放量?
 komilll1年前1
komilll1年前1 -
 小蝙蝠 共回答了20个问题
小蝙蝠 共回答了20个问题 |采纳率85%每年600吨煤,含硫量大约600x0.51% = 3.06吨.因为在二氧化硫 SO2中,硫的分子量只占有其一半的量(分子量分别为S = 32;O = 16).所以,二氧化硫的排放量就应该是 3.06吨 x 2 = 6.12 吨.
即,项目每年的二氧化硫排放量,大约是 6.12吨.1年前查看全部
大家在问
- 1Tom always ___ ___ ___ ___ after school.汤姆总是放学后先写作业.
- 2一道修改病句,①当我们骑马越过崇山峻岭驶向阿根廷一侧的时候,在参天大树形成的绿色拱顶下碰上了一个障碍.②那是一颗大树的根
- 3根据语境,填入适当的句子,补全句话
- 4怎么背东西才能又快又准记得牢!
- 5SO2在什么情况下能生成SO3还有反应条件
- 6甲乙丙三辆汽车同时出发,沿一条公路去追赶前面一个骑车人三辆汽车分别用6小时,8小时,10小时追上骑车人,现
- 7迎圣诞,庆元旦的英文怎么写
- 8一个指示牌的形状如下图.求它的面积.
- 9谢谢你们了.就几个计算题,麻烦写在纸上,越快越好 ,可以一题一题的发,一定好评,谢谢
- 10这是哪种昆虫的卵?请知道的朋友跟贴,
- 11什么情况下革兰氏阳性菌进行革兰氏染色后在油镜下看到的是红色
- 12Look at man!He has a sock on one foot but nothing on his ___
- 13sin70度(1-根号3*tan50度)
- 14电路组成中各元件的作用,大家快来帮帮忙
- 15两个完全一样的直角梯形拼成一个长方形,面积是300平方厘米,其中一个梯形的面积是___平方厘米.

