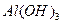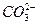石墨的密度大还是小
 中学毕业2022-10-04 11:39:541条回答
中学毕业2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 tom__cat 共回答了17个问题
tom__cat 共回答了17个问题 |采纳率100%- 石墨 英文名称:graphite
分子式:C
分子量:12.01
CAS 登录号:7782-42-5
EINECS 登录号:231-955-3
碳是一种非金属元素,位于元素周期表的第二周期IVA族.拉丁语为Carbonium,意为“煤,木炭”.汉字“碳”字由木炭的“炭”字加石字旁构成,从“炭”字音.石墨是元素碳的一种同素异形体,每个碳原子的周边连结著另外三个碳原子,排列方式呈蜂巢式的多个六边形.由于每个碳原子均会放出一个电子,那些电子能够自由移动,因此石墨属于导电体. 石墨是其中一种最软的矿物. 它的用途包括制造铅笔芯和润滑剂.
碳是一种很常见的元素,它以多种形式广泛存在于大气和地壳之中.碳单质很早就被人认识和利用,碳的一系列化合物——有机物更是生命的根本.碳是生铁、熟铁和钢的成分之一. 碳能在化学上自我结合而形成大量化合物,在生物上和商业上是重要的分子.生物体内大多数分子都含有碳元素.
碳化合物一般从化石燃料中获得,然后再分离并进一步合成出各种生产生活所需的产品,如乙烯、塑料等.
碳的存在形式是多种多样的,有晶态单质碳如金刚石、石墨;有无定形碳如煤;有复杂的有机化合物如动植物等;碳酸盐如大理石等. 单质碳的物理和化学性质取决于它的晶体结构.高硬度的金刚石和柔软滑腻的石墨晶体结构不同,各有各的外观、密度、熔点等.
常温下单质碳的化学性质比较稳定,不溶于水、稀酸、稀碱和有机溶剂;不同高温下与氧反应,生成二氧化碳或一氧化碳;在卤素中只有氟能与单质碳直接反应;在加热下,单质碳较易被酸氧化;在高温下,碳还能与许多金属反应,生成金属碳化物.碳具有还原性,在高温下可以冶炼金属.
石墨是碳质元素结晶矿物,它的结晶格架为六边形层状结构.每一网层间的距离为3.40人,同一网层中碳原子的间距为1.42A.属六方晶系,具完整的层状解理.解理面以分子键为主,对分子吸引力较弱,故其天然可浮性很好.
石墨与金刚石、碳60、碳纳米管等都是碳元素的单质,它们互为同素异形体.
山东省莱西市为我国石墨重要产地之一,石墨探明储量687.11万吨,现保有储量639.93万吨.
石墨质软,黑灰色;有油腻感,可污染纸张.硬度为1~2,沿垂直方向随杂质的增加其硬度可增至3~5.比重为1.9~2.3.比表面积范围集中在1-20m2/g,在隔绝氧气条件下,其熔点在3000℃以上,是最耐温的矿物之一. 它能导电、导热.
自然界中纯净的石墨是没有的,其中往往含有SiO2、Al2O3、FeO、CaO、P2O5、CuO等杂质.这些杂质常以石英、黄铁矿、碳酸盐等矿物形式出现.此外,还有水、沥青、CO2、H2、CH4、N2等气体部分.因此对石墨的分析,除测定固定碳含量外,还必须同时测定挥发分和灰分的含量.
石墨的工艺特性主要决定于它的结晶形态.结晶形态不同的石墨矿物,具有不同的工业价值和用途.工业上,根据结晶形态不同,将天然石墨分为三类.
1.致密结晶状石墨
致密结晶状石墨又叫块状石墨.此类石墨结晶明显晶体肉眼可见.颗粒直径大于0.1毫米,比表面积范围集中在0.1-1m2/g,晶体排列杂乱无章,呈致密块状构造.这种:石墨的特点是品位很高,一般含碳量为60~65%,有时达80~98%,但其可塑性和滑腻性不如鳞片石墨好.
2.鳞片石墨 鳞片石墨
石墨晶体呈鳞片状;这是在高强度的压力下变质而成的,有大鳞片和细鳞片之分.此类石墨矿石的特点是品位不高,一般在2~3%,或100~25%之间.是自然界中可浮性最好的矿石之一,经过多磨多选可得高品位石墨精矿.这类石墨的可浮性、润滑性、可塑性均比其他类型石墨优越;因此它的工业价值最大.
3.隐晶质石墨 隐晶质石墨
隐品质石墨又称非晶质石墨或土状石墨,这种石墨的晶体直径一般小于1微米,比表面积范围集中在1-5m2/g,是微晶石墨的集合体,只有在电子显微镜下才能见到晶形.此类石墨的特点是表面呈土状,缺乏光泽,润滑性也差.品位较高.一般的60~80%.少数高达90%以上.矿石可选性较差.
石墨在工业上运用极广,几乎每个行业都会用到.工业上多用的是人造石墨,也就是特种石墨.按其成型的方式可分为以下几种.
1、等静压石墨.也就是很多人叫的三高石墨,但是并不是三高就是等静压.
2、模压石墨
3、挤压石墨,多为电极材料.
其中按石墨的颗粒度分,也可分为:细节构石墨、中粗石墨(一般的颗粒度在0.8mm左右)、还有就是电极石墨(2-4mm).
石墨由于其特殊结构,而具有如下特殊性质:
1) 耐高温型:石墨的熔点为3850±50℃,沸点为4250℃,即使经超高温电弧灼烧,重量的损失很小,热膨胀系数也很小.石墨强度随温度提高而加强,在2000℃时,石墨强度提高一倍.
2) 导电、导热性:石墨的导电性比一般非金属矿高一百倍.导热性超过钢、铁、铅等金属材料.导热系数随温度升高而降低,甚至在极高的温度下,石墨成绝热体. 石墨能够导电是因为石墨中每个碳原子与其他碳原子只形成3个共价键,每个碳原子仍然保留1个自由电子来传输电荷.
3) 润滑性:石墨的润滑性能取决于石墨鳞片的大小,鳞片越大,摩擦系数越小,润滑性能越好.
4) 化学稳定性:石墨在常温下有良好的化学稳定性,能耐酸、耐碱和耐有机溶剂的腐蚀.
5) 可塑性:石墨的韧性好,可碾成很薄的薄片.
6) 抗热震性:石墨在常温下使用时能经受住温度的剧烈变化而不致破坏,温度突变时,石墨的体积变化不大,不会产生裂纹.
名字来源:源于希腊文“graphein”,意为“用来写”.由德国化学家和矿物学家A. G. Werner 于1789命名;
化学组成:成分纯净者极少,往往含各种杂质;
类别:自然元素-非金属元素-碳族
晶体特征
晶系和空间群:六方晶系,P63/mmm;
晶胞参数:a0=0.246nm,c0=0.670nm;
典型的层状结构,碳原子成层排列,每个碳与相邻的碳之间等距相连,每一层中的碳按六方环状排列,上下相邻层的碳六方环通过平行网面方向相互位移后再叠置形成层状结构,位移的方位和距离不同就导致不同的多型结构.上下两层的碳原子之间距离比同一层内的碳之间的距离大得多(层内C-C间距=0.142nm,层间C-C间距=0.340nm)
形态:单晶体常呈片状或板状,但完整的很少见.集合体通常为鳞片状,块状和土状;
颜色:铁黑色
条痕:光亮黑色
透明度:不透明
光泽:呈半金属光泽
硬度:1-2
解理和断口:平行解理极完全;
比重:2.21-2.26g/cm3
比表面积:5-10m2/g
其他性质:薄片具挠性,有滑感,易污手,具有良好的导电性;
鉴定特征铁黑色,硬度低,一组极完全解理,有滑感和染手;如果将硫酸铜溶液润湿的锌粒放在石墨上,则可析出金属铜的斑点,在与石墨相似的辉钼矿上则无此反应.
成因和产状:石墨是在高温下形成.分布最广是石墨的变质矿床,系由富含有机质或碳质的沉积岩经区域变质作用而成;
主要用途:石墨在工业上用途很广,用于制作冶炼上的高温坩埚、机械工业的润滑剂、制作电极和铅笔芯;广泛用于冶金工业的高级耐火材料与涂料、军事工业火工材料安定剂、轻工业的铅笔芯、电气工业的碳刷、电池工业的电极、化肥工业催化剂等.鳞片石墨经过深加工,又可生产出石墨乳、石墨密封材料与复合材料、石墨制品、石墨减磨添加剂等高新技术产品,成为各个工业部门的重要非金属矿物原料.
石墨新用途:
随着科学技术的不断发展,人们对石墨也开发了许多新用途.
柔性石墨制品.柔性石墨又称膨胀石墨,是年代开发的一种新的石墨制品.
年美国研究成功柔性石墨密封材料,解决了原子能阀门泄漏问题,随后德、日、法也开始研制生产.这种产品除具有天然石墨所具有的特性外,还具有特殊的柔性和弹性.
因此,是一种理想的密封材料.广泛用于石油化工、原子能等工业领域.国际市场需求量逐年增长.
著名产地:纽约Ticonderoga,马达加斯加和Ceylon,我国以黑龙江鸡西市柳毛为最大的产地.
石墨粉里“飞”出金刚石
提起钻石,人们就会联想到光彩夺目、闪烁耀眼的情景,它随着拥有者的活动而光芒四射.但因它的昂贵价格,大多数人只能望而却步.尽管如此,人们对钻石还是很向往的.你知道钻石是什么吗?它的化学成分是碳(C),天然的钻石是由金刚石经过琢磨后才能称之谓“钻石”.天然的钻石是非常稀少的,世界上重量大于1000克拉(1克=5克拉)的钻石只有2粒,400克拉以上的钻石只有多粒,我国迄今为止发现的最大的金刚石重158.786克拉,这就是“常林钻石”.物以稀为贵,正因为可做“钻石“用的天然金刚石很罕见,人们就想“人造“金刚石来代替它,这就自然地想到了金刚石的“孪生“兄弟--石墨了.
金刚石和石墨的化学成分都是碳(C),称“同素异形体”.从这种称呼可以知道它们具有相同的“质”,但“形”或“性”却不同,且有天壤之别,金刚石是目前最硬的物质,而石墨却是最软的物质之一.
石墨和金刚石的硬度差别如此之大,但人们还是希望能用人工合成方法来获取金刚石,因为自然界中石墨(碳)藏量是很丰富的.但是要使石墨中的碳变成金刚石那样排列的碳,不是那么容易的.石墨在5-6万大气压((5-6)×103MPa)及摄氏1000至2000度高温下,再用金属铁、钴、镍等做催化剂,可使石墨转变成金刚石.
目前世界上已有十几个国家(包括我国)均合成出了金刚石.但这种金刚石因为颗粒很细,主要用途是做磨料,用于切削和地质、石油的钻井用的钻头.当前,世界金刚石的消费中,80%的人造金刚石主要是用于工业,它的产量也远远超过天然金刚石的产量.
最初合成的金刚石颗粒呈黑色,0.5mm大小,重约0.1克拉(用于宝石的金刚石一般最小不能小于0.1克拉).现在我国研制的大颗粒金刚石达3mm以上,美国、日本等已制成6.1克拉多的金刚石.我们说金刚石已从石墨中“飞”出,宝石级的人造金刚石也会在不久的将来供应于市场.
石墨何以能取代铜?
20世纪60年代,铜作为电极材料被广泛应用,使用率约占90%,石墨仅有10%左右;21世纪,越来越多的用户开始选择石墨作为电极材料,在欧洲,超过90%以上的电极材料是石墨.铜,这种曾经占统治地位的电极材料,和石墨电极相比它的优势几乎消失殆尽.是什么导致了这个戏剧性的变化?当然是石墨电极的诸多优势.
(1)加工速度更快:通常情况下,石墨的机械加工速度能比铜快2~5倍;而放电加工速度比铜快2~3倍;
材料更不容易变形:在薄筋电极的加工上优势明显;铜的软化点在1000度左右,容易因受热而产生变形;石墨的升华温度为3650度;热膨胀系数仅有铜的1/30.
(2)重量更轻:石墨的密度只有铜的1/5,大型电极进行放电加工时,能有效降低机床(EDM)的负担;更适合于在大型模具上的应用.
(3)放电消耗更小;由于火花油中也含有C原子,在放电加工时,高温导致火花油中的C原子被分解出来,转而在石墨电极的表面形成保护膜,补偿了石墨电极的损耗.
(4)没有毛刺;铜电极在加工完成后,还需手工进行修整以去除毛刺,而石墨加工后没有毛刺,节约了大量成本,同时更容易实现自动化生产;
(5)石墨更容易研磨和抛光;由于石墨的切削阻力只有铜的1/5,更容易进行手工的研磨和抛光;
(6)材料成本更低,价格更稳定;由于近几年铜价上涨,如今各向同性石墨的价格比铜更低,相同体积下,东洋炭素的普遍性石墨产品的价格比铜的价格低30%~60%,并且价格更稳定,短期价格波动非常小.
正是这种无可比拟的优势,石墨逐渐取代铜成为EDM电极的首选材料
石墨的用途:
1、作耐火材料: 石墨及其制品具有耐高温、高强度的性质,在冶金工业中主要用来制造石墨坩埚,在炼钢中常用石墨作钢锭之保护剂,冶金炉的内衬.
2、作导电材料:在电气工业上用作制造电极、电刷、碳棒、碳管、水银正流器的正极,石墨垫圈、电话零件,电视机显像管的涂层等.
3、作耐磨润滑材料:石墨在机械工业中常作为润滑剂.润滑油往往不能在高速、高温、高压的条件下使用,而石墨耐磨材料可以在(一) 200~2000 ℃温度中在很高的滑动速度下,不用润滑油工作.许多输送腐蚀介质的设备,广泛采用石墨材料制成活塞杯,密封圈和轴承,它们运转时勿需加入润滑油.石墨乳也是许多金属加工(拔丝、拉管)时的良好的润滑剂.
4、石墨具有良好的化学稳定性.经过特殊加工的石墨,具有耐腐蚀、导热性好,渗透率低等特点,就大量用于制作热交换器,反应槽、凝缩器、燃烧塔、吸收塔、冷却器、加热器、过滤
器、泵设备.广泛应用于石油化工、湿法冶金、酸碱生产、合成纤维、造纸等工业部门,可节省大量的金属材料.
5、作铸造、翻砂、压模及高温冶金材料:由于石墨的热膨胀系数小,而且能耐急冷急热的变化,可作为玻璃器的铸模,使用石墨后黑色金属得到铸件尺寸精确,表面光洁成品率高,不经加工或稍作加工就可使用,因而节省了大量金属.生产硬质合金等粉末冶金工艺,通常用石墨材料制成压模和烧结用的瓷舟.单晶硅的晶体生长坩埚,区域精炼容器,支架夹具,感应加热器等都是用高纯石墨加工而成的.此外石墨还可作真空冶炼的石墨隔热板和底座,高温电阻炉炉管,棒、板、格棚等元件.
6、用于原子能工业和国防工业:石墨具有良好的中子减速剂用于原子反应堆中,铀一石墨反应堆是目前应用较多的一种原子反应堆.作为动力用的原子能反应堆中的减速材料应当具有高熔点,稳定,耐腐蚀的性能,石墨完全可以满足上述要求.作为原子反应堆用的石墨纯度要求很高,杂质含量不应超过几十个 PPM .特别是其中硼含量应少于 0.5PPM .在国防工业中还用石墨制造固体燃料火箭的喷嘴,导弹的鼻锥,宇宙航行设备的零件,隔热材料和防射线材料.
7、石墨还能防止锅炉结垢,有关单位试验表明,在水中加入一定量的石墨粉(每吨水大约用 4~5 克)能防止锅炉表面结垢.此外石墨涂在金属烟囱、屋顶、桥梁、管道上可以防腐防锈.
8、石墨可作铅笔芯、颜料、抛光剂.石墨经过特殊加工以后,可以制作各种特殊材料用于有关工业部门.
此外,石墨还是轻工业中玻璃和造纸的磨光剂和防锈剂,是制造铅笔、墨汁、黑漆、油墨和人造金刚石、钻石不可缺少的原料.它是一种很好的节能环保材料,美国已用它做为汽车电池.随着现代科学技术和工业的发展,石墨的应用领域还在不断拓宽,已成为高科技领域中新型复合材料的重要原料,在国民经济中具有重要的作用.注:由于不知道您要问什么,只好把百度上的石墨资料全部复制过来. - 1年前
相关推荐
- 石墨中每个碳原子与_____个碳原子以_______键结合,构成的是____.金刚石中每个碳原子与____个碳原子以__
石墨中每个碳原子与_____个碳原子以_______键结合,构成的是____.金刚石中每个碳原子与____个碳原子以_______键结合,构成______空间网状结构.
 fjsmlhhl1年前2
fjsmlhhl1年前2 -
 sunsjt 共回答了19个问题
sunsjt 共回答了19个问题 |采纳率89.5%3 共价键 层状结构 4 共价键 立体1年前查看全部
- 用 石墨做电极 电解硝酸铜 硝酸银混合溶液 现象
 yyyyppoo1年前1
yyyyppoo1年前1 -
 nn胜雪 共回答了13个问题
nn胜雪 共回答了13个问题 |采纳率76.9%在阴极有银析出,阴极变银白色.
在阳极有无色气体(O2)放出.1年前查看全部
- 12g石墨和C60混合固体中含有多少NA个碳原子
 我扔1年前1
我扔1年前1 -
 通信未来 共回答了12个问题
通信未来 共回答了12个问题 |采纳率75%1个阿伏伽德罗常数的量=1NA,即6.02乘以10的23次方.1年前查看全部
- 碳酸钠 氧化钙 石灰水 乙醇 同 石墨 维生素C 矿泉水 属于混合物的 哪个 .单质 .盐
 nulong791年前1
nulong791年前1 -
 501bc 共回答了12个问题
501bc 共回答了12个问题 |采纳率100%属于混合物的:石灰水,矿泉水
单质:石墨
盐:碳酸钠
附:氧化钙:氧化物
乙醇,维生素C:有机物
多谢!1年前查看全部
- 在通常情况下,下列各组材料都是导体的是( ) A.铜、石墨、纯水 B.大地、塑料、油 C.橡皮、铅笔芯、人体 D.铝线
在通常情况下,下列各组材料都是导体的是( ) A.铜、石墨、纯水 B.大地、塑料、油 C.橡皮、铅笔芯、人体 D.铝线、大地、盐水  丽丽不乖1年前1
丽丽不乖1年前1 -
 dreamglass 共回答了18个问题
dreamglass 共回答了18个问题 |采纳率72.2%常见的导体包括:人体、大地、各种金属、石墨、铅笔芯、酸碱盐的溶液等.题中选项中,铜、石墨、大地、铅笔芯、人体、铝线、大地、盐水是导体,其他的都是绝缘体.
故选D.1年前查看全部
- 下列反应的离子方程式正确的是( ) A.用石墨作电极电解CuCl 2 溶液:2Cl - +2H 2 O Cl 2 ↑+
下列反应的离子方程式正确的是( )
A.用石墨作电极电解CuCl 2 溶液:2Cl - +2H 2 O  Cl 2 ↑+H 2 ↑+2OH -
Cl 2 ↑+H 2 ↑+2OH - B.用Na 2 CO 3 溶液作洗涤剂除油污:CO 3 2- +2H 2 O  H 2 CO 3 +2OH -
H 2 CO 3 +2OH - C.硫酸亚铁溶液与稀硫酸、双氧水混合:Fe 2 + +2H 2 O 2 +4H + =Fe 3 + +4H 2 O D.向NaAlO 2 溶液中通入过量的CO 2 :AlO 2 - +CO 2 +2H 2 O=Al(OH) 3 ↓+HCO 3 -  生如草芥1年前1
生如草芥1年前1 -
 飞童小可 共回答了16个问题
飞童小可 共回答了16个问题 |采纳率93.8%D
A项中应是Cu 2 + 和Cl - 放电;B项中CO 3 2- 水解要分步进行;C项中没有配平;D项正确。1年前查看全部
- 石墨中层与层之间的结合力是共价键还是范德华力?
 小鱼游荡1年前2
小鱼游荡1年前2 -
 香草优诺 共回答了21个问题
香草优诺 共回答了21个问题 |采纳率85.7%石墨是混合型晶体
它是片层结构的,层与层之间的结合力是范德华力,而层内碳原子以共价键结合,所以石墨很软(片层脱落只需克服范德华力),但熔沸点很高(变成液态要克服共价键).1年前查看全部
- 纯净的钻石和石墨的组成元素种类是否相同
 没有披肩1年前1
没有披肩1年前1 -
 Gavin2100 共回答了23个问题
Gavin2100 共回答了23个问题 |采纳率100%是相同的,都是碳,只是碳的排列不同1年前查看全部
- 铅笔芯的主要成分是石墨和黏土,这些物质按照不同的比例加以混和、压制,就可以制成铅笔芯.如果铅笔芯质量的一半成分是石墨,且
铅笔芯的主要成分是石墨和黏土,这些物质按照不同的比例加以混和、压制,就可以制成铅笔芯.如果铅笔芯质量的一半成分是石墨,且用铅笔写一个字消耗的质量约为1mg.那么一个铅笔字含有的碳原子数约为( )
A. 2.5×1019个
B. 2.5×1022个
C. 5×1019个
D. 5×1022个 swl8607011年前1
swl8607011年前1 -
 wj370205 共回答了17个问题
wj370205 共回答了17个问题 |采纳率88.2%解题思路:铅笔芯质量的一半成分是石墨,用铅笔写一个字消耗的质量约为1mg,则一个铅笔字含有的碳的质量为0.5mg,根据n=[m/M]计算碳的物质的量,再根据N=nNA计算碳原子数目.铅笔芯质量的一半成分是石墨,用铅笔写一个字消耗的质量约为1mg,则一个铅笔字含有的碳的质量为0.5mg.
所以一个铅笔字含有的碳的物质的量为
5×10−4g
12g/mol=[5/12]×10-4mol,
所以含有的碳原子数目为[5/12]×10-4mol×6.02×1023=2.5×1019,
故选:A.点评:
本题考点: 物质分子中的原子个数计算;阿伏加德罗常数.
考点点评: 考查物质中原子数目及常用化学计量计算,比较基础,注意公式的灵活运用.1年前查看全部
- 下列物质中都是导体的是( )A.铜丝、橡皮、石墨B.大地、食盐水溶液、人体C.塑料、橡胶、玻璃D.陶瓷、干木头、金属
 yerenju0011年前1
yerenju0011年前1 -
 rogerlee 共回答了21个问题
rogerlee 共回答了21个问题 |采纳率95.2%解题思路:根据导体和绝缘体的定义进行判断.
容易导电的物体是导体;不容易导电的物体是绝缘体.A、铜丝、石墨属于导体,橡皮属于绝缘体;
B、大地、食盐水溶液、人体都属于导体;
C、塑料、橡胶、玻璃都属于绝缘体;
D、陶瓷、干木头属于绝缘体,金属属于导体.
故选B.点评:
本题考点: 导体.
考点点评: 常见的导体包括:人体、大地、各种金属、酸碱盐的溶液等.
常见的绝缘体包括:塑料、橡胶、陶瓷、空气、玻璃等.
导体和绝缘体之间没有明显的界线,在条件变化时,是可以相互转化的.
导体和绝缘体不要死记硬背要根据生活中哪些地方用什么来导电,用什么来绝缘来记忆,效果比较好.1年前查看全部
- 选择下列物质填空(填写序号): ①金刚石 ②干冰 ③氩晶体 ④白磷 ⑤氯化钙 ⑥过氧化钠 ⑦石英 ⑧石墨 ⑨氯化铵 ⑩铜
选择下列物质填空(填写序号):
①金刚石 ②干冰 ③氩晶体 ④白磷 ⑤氯化钙 ⑥过氧化钠 ⑦石英 ⑧石墨 ⑨氯化铵 ⑩铜晶体
(1)固态时能导电的有_____________
(2)熔化时不破坏化学键的有_____________
(3)含有配位键的有_____________
(4)含有非极性共价键的有_____________ htsmc0051年前1
htsmc0051年前1 -
 spring89522 共回答了19个问题
spring89522 共回答了19个问题 |采纳率84.2%(1)⑧⑩
(2)②③④
(3)⑨
(4)①④⑥⑧1年前查看全部
- 为什么石墨制成金刚石是化学变化它们都是碳单质啊还有,吸附性为什么是物理性质?
 janzxc1年前5
janzxc1年前5 -
 电子翅膀 共回答了15个问题
电子翅膀 共回答了15个问题 |采纳率73.3%化学变化是指相互接触的分子间发生原子或电子的转换或转移,生成新的分子并伴有能量的变化的过程;化学变化实质是旧键的断裂和新键的生成.石墨和金刚石虽然都是碳单质,但是他们的晶体构型不同:碳是典型的层状晶体,微观结构是分层的,同层之间靠共价键结合,层与层之间靠范德华里吸引,所以表现出光滑,柔软易碎的物理性质.而金刚石是典型的原子晶体,微观结构是碳原子与碳原子之间用共价键结合,一个碳原子周围有六个碳原子.原子与原子之间结合力较强,所以物理性质坚硬,溶沸点高.
从根本上来说,他们的微观结构发生改变,旧键断裂新键生成,产生了新的物质,所以是化学变化.
碳的吸附性是因为碳单质表面有很多小孔,细小的东西趋于孔内,实际上是因为碳的宏观聚集状态而产生的性质,其中没有发生化学变化,所以是物理性质1年前查看全部
- 石墨的密度是多少,怎么计算重量
 snaper1年前1
snaper1年前1 -
 乖乖枫 共回答了15个问题
乖乖枫 共回答了15个问题 |采纳率86.7%先算重量.再用重量乘以单价就是了.如:120*100*100,石墨密度为1.8,重量就等于120*100*100*0.0000018=2.2,接着乘对应的单价就可以了.上海隆继1年前查看全部
- (2分)有:① 1 1 H、 2 1 H、 3 1 H ②H 2 、D 2 、T 2 ③石墨、金刚石④正丁烷和异丁烷四组
(2分)有:① 1 1 H、 2 1 H、 3 1 H ②H 2 、D 2 、T 2 ③石墨、金刚石④正丁烷和异丁烷四组微粒或物质,回答下列问题:(填序号)
(1)互为同素异形体的是_______;(2)互为同分异构体的是__________ ybfq1年前1
ybfq1年前1 -
 decide1 共回答了27个问题
decide1 共回答了27个问题 |采纳率96.3%(2分)(1)③;(2)④
由同一种元素形成的不同单质,互称为同素异形体,所以答案选③。分子式相同而结构不同的化合物互为同分异构体,因此答案选④。1年前查看全部
- 请在“石墨、氮气、二氧化硫、甲烷、熟石灰”中选择合适的物质填空:(填化学式或名称)
请在“石墨、氮气、二氧化硫、甲烷、熟石灰”中选择合适的物质填空:(填化学式或名称)
(1)能形成硫酸型酸雨的空气污染物是 ;
(2)能产生温室效应的气体,且属于有机物的是 ;
(3)具有优良导电性的非金属单质是 ;
(4)常用来改良酸性土壤的碱是 ;
(5)充入食品包装袋中可以防腐,且约占空气体积78%的气体单质是 。 wwwxcxc1年前1
wwwxcxc1年前1 -
 cls-k 共回答了16个问题
cls-k 共回答了16个问题 |采纳率93.8%(1)SO 2 (2)CH 4 (3)C (4)Ca(OH) 2 (5)N 21年前查看全部
- 物质的用途与性质密切相关,下列各项应用主要利用了其化学性质的是( ) A.用石墨做电极 B.用金属钨做灯丝 C.用一
物质的用途与性质密切相关,下列各项应用主要利用了其化学性质的是()
A.用石墨做电极 B.用金属钨做灯丝 C.用一氧化碳作燃料 D.干冰用于人工降雨  cristing1年前1
cristing1年前1 -
 傻强 共回答了19个问题
傻强 共回答了19个问题 |采纳率94.7%C 分析:化学性质是指通过化学变化表现出来的性质,物理性质是指不需要通过化学变化表现出来的性质.A、用石墨作电极是利用石墨的导电性,不需要通过化学变化表现出来,故A错;B、用金属钨作灯丝是利用...1年前查看全部
- 石墨 高温高压 变为金刚石 是化学变化还是物理变化 问什么
石墨 高温高压 变为金刚石 是化学变化还是物理变化 问什么
石墨变金刚石 只改变了分子结构 却生成了另一种物质——金刚石 datougui0071年前7
datougui0071年前7 -
 万般风情不及卿 共回答了18个问题
万般风情不及卿 共回答了18个问题 |采纳率88.9%是化学变化,但是不是因为分子结构发生变化,石墨和金刚石都不存在分子结构,因为他们是原子晶体.石墨变成金刚石是晶体结构发生变化,出现了化学键的断裂和生成,所以是化学变化1年前查看全部
- 石墨是混合物还是纯净物
 ct3dde1年前1
ct3dde1年前1 -
 想不到怎么说 共回答了26个问题
想不到怎么说 共回答了26个问题 |采纳率84.6%石墨 对于化学来说是单质 要是商品来说就是混合物~x0d碳单质的存在形式,除了金刚石和石墨外,还有无定形碳.无定形碳有很多品种,如碳黑、木炭、活性炭、焦碳等等.碳黑可用于制造油墨、油漆、墨汁等.碳黑是以含碳原料...1年前查看全部
- 金刚石和石墨是单质还是混合物
 crystal59231年前2
crystal59231年前2 -
 langstonchen 共回答了21个问题
langstonchen 共回答了21个问题 |采纳率90.5%单质
金刚石和石墨是由碳元素组成的不同单质1年前查看全部
- 我们学习了化学这门学科后,就要从化学的角度去看待我们身边的各种物质.下面是金刚石.石墨的微观结构模型图,请回答问题:
我们学习了化学这门学科后,就要从化学的角度去看待我们身边的各种物质.下面是金刚石.石墨的微观结构模型图,请回答问题: 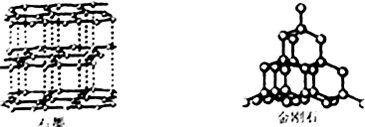
(1)从宏观组成上分析,金刚石、石墨都是由______组成的,属于______(填物质类别).
(2)从微观结构上分析,金刚石、石墨都是由______构成的,但是两者在物理性质上存在很大差异的原因是______
(3)物质性质决定物质的用途,请分别写出它们在生产生活中的重要应用:金刚石______;石墨______. rrrclub1年前1
rrrclub1年前1 -
 首席牛人的tt1 共回答了19个问题
首席牛人的tt1 共回答了19个问题 |采纳率89.5%(1)金刚石、石墨都是由碳元素组成的单质;
(2)金刚石、石墨都是由碳原子构成的,但是两者在物理性质上存在很大差异的原因是碳原子的排列方式不同;
(3)物质性质决定物质的用途,金刚石的硬度大,可以切割玻璃;石墨能导电,可用作电极.
故答案为:(1)碳元素;单质;(2)碳原子;碳原子的排列方式不同;(3)切割玻璃;可用作电极.1年前查看全部
- 下列反应的离子方程式书写正确的是 A.明矾溶液中加入过量的氨水: B.次氯酸钙溶液中通人过量二氧化碳: C.用石墨作电极
下列反应的离子方程式书写正确的是
A.明矾溶液中加入过量的氨水: 
B.次氯酸钙溶液中通人过量二氧化碳: 
C.用石墨作电极电解饱和食盐水: 


D.澄清的石灰水中加人少量的  溶液:
溶液:
 空中雪花1年前1
空中雪花1年前1 -
 hslc311 共回答了24个问题
hslc311 共回答了24个问题 |采纳率91.7%1年前查看全部
- 导电性强弱导电性最差的是( )A铁B铝C石墨D氯化钠晶体
 zzh551年前3
zzh551年前3 -
 grase27 共回答了12个问题
grase27 共回答了12个问题 |采纳率100%D 晶体导电性最差;
因为晶体中不存在离子 所以晶体不能导电1年前查看全部
- 高一化学电解质1.稀硫酸 2. 液氨 3. 氨水 4.铝条 5.熔融氯化钠 6.石墨 7.氢氧化钡溶液8.二氧化硫 9.
高一化学电解质
1.稀硫酸 2. 液氨 3. 氨水 4.铝条 5.熔融氯化钠 6.石墨 7.氢氧化钡溶液
8.二氧化硫 9.水 10.熔融Na2O 11 盐酸 12.乙醇
判断上述物质 ,A能够导电的是
B属于电解质的是
C属于非电解质的是
D属于强电解质的是
CO2 通入石灰水,溶液的导电能力先减弱而后又逐渐加强.试解析其化学变化的原因_______________,______________________________(用化学方程式表示)
金属导电是因为存在___________________,电解质导电是因为存在___________________________.液态HCl不导电是因为__________________________,HCl的水溶液能导电是因为________________,NaCl晶体不导电是因为_______________,熔融的NaCl能导电是因为__________________ winter19821年前2
winter19821年前2 -
 橙色燃烧 共回答了18个问题
橙色燃烧 共回答了18个问题 |采纳率88.9%1.稀硫酸 2.液氨 3.氨水 4.铝条 5.熔融氯化钠 6.石墨 7.氢氧化钡溶液8.二氧化硫 9.水 10.熔融Na2O 11 盐酸 12.乙醇
判断上述物质 ,A能够导电的是1 3 4 5 6 7 10 11
B属于电解质的是5 9 10
C属于非电解质的是2 8 12
D属于强电解质的是5 10
CO2 通入石灰水,先生成碳酸钙,导电能力减弱;过量后生成碳酸氢钙,导电能力又增强了.
金属导电是因为存在可自由移动的电子,电解质导电是因为存在可自由移动的离子.液态HCl不导电是因为共价化合物,熔融态不导电,HCl的水溶液能导电是因为存在自由移动的氢离子和氯离子,NaCl晶体不导电是因为没有课自由移动的离子,熔融的NaCl能导电是因为存在可自由移动的钠离子和氯离子1年前查看全部
- 在“熟石灰、石墨、碳酸钙、聚乙烯、生石灰”中,选用适当的物质填空.
在“熟石灰、石墨、碳酸钙、聚乙烯、生石灰”中,选用适当的物质填空.
(1)用于改良酸性土壤的是______;
(2)用作补钙剂的是______;
(3)常用包装食品的塑料是______;
(4)用作电池中电极的是______;
(5)常用作食品干燥剂的是______. 寞小寞1年前1
寞小寞1年前1 -
 枫是风 共回答了20个问题
枫是风 共回答了20个问题 |采纳率95%解题思路:根据物质的性质分析,熟石灰呈碱性,可以改良酸性土壤,石墨具有良好的导电性,碳酸钙中含有钙元素,聚乙烯无毒,常用来制作塑料袋,生石灰能吸收水,和水反应生成氢氧化钙.(1),因为熟石灰具有碱性,常用于改良酸性土壤,故填:熟石灰;(2)碳酸钙和胃液中的盐酸反应,转变成可溶性的钙离子,用作补钙剂,故填:碳酸钙;(3)聚乙烯对人体无害,常用包装食品的塑料,故填:聚乙烯;(4...
点评:
本题考点: 碳单质的物理性质及用途;酸碱盐的应用;塑料及其应用.
考点点评: 熟悉个物质的性质是解答此类题目的关键,物质的性质决定用途,因此要对物质的性质加强理解,多做知识储备,做到学以致用.1年前查看全部
- 生活离不开化学物质,现有以下五种物质①熟石灰 ②氮气 ③石墨 ④汞 ⑤氧气,请从中选择适当的物质填空(填序号)
生活离不开化学物质,现有以下五种物质①熟石灰 ②氮气 ③石墨 ④汞 ⑤氧气,请从中选择适当的物质填空(填序号)
(1)属于金属的是______;
(2)空气中最多的气体是______;
(3)可用于制铅笔芯的是______;
(4)可用于建筑材料的是______;
(5)可用于医疗急救病人的是______. szwxsm1年前1
szwxsm1年前1 -
 金太阳美发 共回答了27个问题
金太阳美发 共回答了27个问题 |采纳率100%解题思路:物质的性质决定物质的用途,根据常见物质的性质和用途进行分析解答即可.(1)属于金属的是汞,故选 ④;
(2)空气中最多的气体是氮气,故选 ②;
(3)石墨比较软,可用做铅笔芯,故选③;
(4)可用于建筑材料的是熟石灰,故选 ①;
(5)可用于医疗急救病人的是氧气,故选 ⑤.
故答案为:④②③①⑤.点评:
本题考点: 常见的金属和非金属的区分;空气的成分及各成分的体积分数;氧气的用途;常见碱的特性和用途;碳单质的物理性质及用途.
考点点评: 本题难度不大,物质的性质决定物质的用途,掌握常见化学物质的性质和用途是正确解答此类题的关键.1年前查看全部
- 石墨与金刚石都是碳单质,为什么其颜色有这么大差别?难道光的反射与物体原子间的结构有关?
石墨与金刚石都是碳单质,为什么其颜色有这么大差别?难道光的反射与物体原子间的结构有关?
石墨和金属都具有导电性,石墨与金属的性质差不多(柔软,固体,单质)是不是电阻的大小与其原子结构有关?如果以上两问题都成立,光的传播和电的传播都与介质的结构有关系,那么可不可以说光是电的另一种形式?
我认为,光也是一种电子转移,回忆下,光的产生大多数是燃烧,而燃烧意味着原子结合,每一个原子都具有电子,那么在他们结合中,发生碰撞等反应,电子应该会挣脱一些,挣脱的电子,大量聚集形成了光。还记得当光照到手上时是什么感觉吗?热的,我认为那是因为电子进入了身体,与我们体内的原子结合,或撞击,造成原子运动速度加快,当然不是所有的光都会进入物质当中,那决定物体的结构,如白色物体的结构能排斥多量的电子,具体怎样,我也说不清楚, luxun01031年前1
luxun01031年前1 -
 CHUAHYAPWIN 共回答了25个问题
CHUAHYAPWIN 共回答了25个问题 |采纳率88%我觉得如果楼主想弄清楚这个问题,到不如多看看"光电效应"和部分量子力学的知识...
如果还想讨论的话,到不如去物理吧里发贴讨论.
回答你的问题补充:
我觉得只要是能量的转换,都应该与分子原子电子的撞击有关(你们想想所有(除光能)的能量转换是不是吧)
回答:
大部分是这样的,而且光能转为电能也是类似是撞击的结果,这个你可以自己看看”光电效应”那部分的物理知识.
那么光能变为内能应该也是电子的撞击啊,正如不发光的电阻通电发热,是电子撞击造成的一样,所以我觉得光是电子的转移
回答:
光存在波粒二向性,因此是存在光子的.同时光也是一种电磁波,这个在高中物理也有学习.
但是按你所说的光能能否变为内能,就要分情况讨论了.
这涉及到他们两者的晶体结构.
石墨是混合晶体,金刚石是原子晶体,以下为你详细的解释.
石墨是C,电子层结构为2.4,内层的2个电子不参与形成共价键,因此只有最外层的4个电子与形成晶体有关.
其次,石墨是层状的晶体结构(想象成一张一张纸叠在一起),金刚石是立体的晶体结构(想象成钢筋做成的摩天大楼).
所以石墨是一层一层的,每1层1个C都与其他3个C原子形成3个共价键,所以如果以1个C原子为一个点,那么一层就是由N个正六边形拼成的.
而每个C都富裕1个电子,这个电子都贡献出来,类似于金属键.这些电子存在于1层和1层之间,用电磁力把每1层拉的很紧密.
这也就解释了为什么石墨很软可以做铅笔(因为层与层之间容易分离);也解释了为什么金刚石不导电,而石墨能导电(因为每层之间有很多的自由移动的电子);也解释了为什么石墨有乌黑的类似于金属光泽(因为石墨的某些晶体性质和金属很类似,比如那些自由移动的电子)1年前查看全部
- 已知电极材料:铁、铜、银、石墨、锌、铝;电解质溶液:CuCl2溶液、Fe2(SO4)3溶液、盐酸.按要求回答下列问题:
已知电极材料:铁、铜、银、石墨、锌、铝;电解质溶液:CuCl2溶液、Fe2(SO4)3溶液、盐酸.按要求回答下列问题:
(1)电工操作上规定:不能把铜导线和铝导线连接在一起使用.请说明原因______.
(2)若电极材料选铜和石墨,电解质溶液选硫酸铁溶液,外加导线,能否构成原电池______,若能,请写出电极反应式,负极______,正极______.(若不能,后两空不填)
(3)设计一种以铁和硫酸反应为原理的原电池,要求画出装置图:(需标明电极材料及电池的正负.) hajimija1年前0
hajimija1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 高温高压下可以使石墨转化为金刚石是自发的化学反应,这句话为什么不对
 赫狼1年前1
赫狼1年前1 -
 天马行空4 共回答了20个问题
天马行空4 共回答了20个问题 |采纳率90%不是化学反应,只是分子结构的变化,石墨和金刚石的成份都是碳1年前查看全部
- (2014届上海市松江区第一学期期末试题)互为同素异形体的一组物质是 A.氧气和液氧 B.金刚石和石墨 C.一氧化碳和二
(2014届上海市松江区第一学期期末试题)互为同素异形体的一组物质是
A.氧气和液氧 B.金刚石和石墨 C.一氧化碳和二氧化碳 D.水和双氧水  随心的风1年前1
随心的风1年前1 -
 有有成功 共回答了23个问题
有有成功 共回答了23个问题 |采纳率95.7%B
1年前查看全部
- 为什么我做的镁-过氧化氢燃料电池的电压才0.01伏(两极分别是石墨和镁,中间冲入氯化钠和过氧化氢溶液)
 gb6ysc91年前1
gb6ysc91年前1 -
 蓝天下的鱼 共回答了16个问题
蓝天下的鱼 共回答了16个问题 |采纳率87.5%可能是电池的内阻太大,可以多加一些电解质到溶液中.1年前查看全部
- 电解Al2o3时阳极生成的氧气全部与石墨反应转化,若co2和co的体积之比为1:1,当阴极得到27gAl时,若阳极生成的
电解Al2o3时阳极生成的氧气全部与石墨反应转化,若co2和co的体积之比为1:1,当阴极得到27gAl时,若阳极生成的气体用作燃料放出能量多少kj c+o2=co2 △H=-393.5 c+o2=2CO △H=-221.0
 鲁西法的猫1年前2
鲁西法的猫1年前2 -
 场院的碌碡nn心眼 共回答了19个问题
场院的碌碡nn心眼 共回答了19个问题 |采纳率78.9%2CO+O2=2CO2.Delta H=-566.0kJ/mol
27gAl 3mol电子 变为CO的获得三分之一.
故有二分之一molCO,即 566.0/4=141.5(kJ)1年前查看全部
- 铜为阳极,石墨为阴极电解氯化钠关于这个反应,阳极有铜,氢氧根离子和氯离子,我想问这3个哪个的失电子能力强?为什么是铜?难
铜为阳极,石墨为阴极电解氯化钠
关于这个反应,阳极有铜,氢氧根离子和氯离子,我想问这3个哪个的失电子能力强?为什么是铜?难道说是只要是金属就比硫离子那些离子的失电子能力强?要是这样的话,那金呢?意思金的失电子能力也比那些离子强?顺便问一下,加入阳极也为石墨是不是就轮氯离子放电了?还有什么情况下电极会出现水得失电子的情况,我一般做这种写电极方程式的题都是看电极处有什么离子,然后再看他们的放电顺序,但是我发现有些反应居然是水在反应物种,而不是离子,请问什么情况下回出现这种情况?例如惰性电极电解硫酸铜的时候.阳极应该有氢氧根离子和硫酸根离子,应该是氢氧根离子失电子放电啊?怎么它的方程式却是2H20-4e-=O2+4H+?出现了水失电子的情况,这是怎么回事? 卫7121年前3
卫7121年前3 -
 xcwangtao 共回答了13个问题
xcwangtao 共回答了13个问题 |采纳率100%金属活动性顺序表 其中有(H) 仔细看看就行的了
钾 钙 钠 镁 铝 锌 铁 锡 铅 (氢)铜 汞 银 铂 金
另外 非金属的活动性顺序就要自己掌握了
点解反应中写水才是最正确的 因为水是弱点解质 在离子反应方程式中本来就不能拆
只是现在大家都错习惯了 默认写离子正确1年前查看全部
- 金刚石的化学式是什么?为什么同是碳的单质,石墨和金刚石不同?
 Brana1年前3
Brana1年前3 -
 bbqowen 共回答了15个问题
bbqowen 共回答了15个问题 |采纳率86.7%金刚石和石墨的化学式都是C
碳原子的排布方式不同
金刚石是碳原子成正四面体的排布,是原子晶体
而石墨是碳原子的三个外围电子与其他的碳原子的外围电子成共价键,而多余的一个外围电子成为自由电子,石墨是混合晶体
这些知识等你上了高中的选修3《物质结构与性质》之后就会很好的理解了1年前查看全部
- 用石墨作电极,分别电解下列各物质的溶液①CuCl 2 ②CuSO 4 ③NaBr ④NaNO 3 ⑤盐酸 ⑥H 2
用石墨作电极,分别电解下列各物质的溶液①CuCl 2 ②CuSO 4 ③NaBr ④NaNO 3 ⑤盐酸 ⑥H 2 SO 4 ⑦KOH。其中只有水被电解的有 [ ]A.①②⑤
B.③④⑥⑦
C.④⑥⑦
D.③⑤⑥⑦ 雨吧1年前1
雨吧1年前1 -
 我不是黄飞鸿 共回答了18个问题
我不是黄飞鸿 共回答了18个问题 |采纳率100%C1年前查看全部
- 金刚石、石墨、木炭和C60都是由碳元素组成的单质 他们之间有什么不同?
 全天候1年前1
全天候1年前1 -
 以林 共回答了25个问题
以林 共回答了25个问题 |采纳率88%它们都是碳元素组成的不同单质,互称同素异形体.x0d因为它们内部碳原子的连接方式不一样,晶体结构不一样,因此物理性质差别很大,化学性质相似.x0d比如,金刚石中每个碳原子与周围的4个C原子连接成空间网状结构.因此熔点高,沸点高,硬度大.难溶于常见的溶剂.x0d而石墨是层状结构,每一层内每个C原子与周围的3个C形成正六边形结构,层之间靠分子间作用力连接,因此石墨熔点高,层间容易滑动,可做高温润滑剂.x0d而木炭是石墨的微晶加少量杂质形成的.x0dC60 是60个C原子形成一个笼状结构.1年前查看全部
- 下列对相应现象或事实的解释不正确的是 [ ] A.金刚石和石墨的性质差异
下列对相应现象或事实的解释不正确的是 [ ]A.金刚石和石墨的性质差异较大--两者的原子排列方式不同
B.酒香不怕巷子深--分子不断的运动
C.患贫血症--是因为缺钙元素
D.无水硫酸铜能检验酒精中是否含水--无水硫酸铜遇水从白色变为蓝色 酒溅飞花1年前1
酒溅飞花1年前1 -
 jx369963 共回答了19个问题
jx369963 共回答了19个问题 |采纳率94.7%C1年前查看全部
- 金刚石,石墨,足球烯都是由碳原子构成的,但它们的物理性质差别很大,这是因为
金刚石,石墨,足球烯都是由碳原子构成的,但它们的物理性质差别很大,这是因为
A原子内部结构不同 B原子组成的分子不同
C原子的排列顺序不同 D原子的质量不同
为什么选c,A、B不对吗 qiugou1231年前1
qiugou1231年前1 -
 nanjinrennanjin 共回答了26个问题
nanjinrennanjin 共回答了26个问题 |采纳率92.3%首先,这三种物质中除了足球烯以外都不存在分子这一说,这个金刚石是原子晶体,石墨是混合晶体,足球烯是分子晶体,金刚石和石墨中都木有分子,B不对.
此外,他们都是由碳原子直接构成的,所以说原子内部结构也是相同的,A不对.1年前查看全部
- 下列依据热化学方程式得出的结论正确的是( ) A.已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 B
下列依据热化学方程式得出的结论正确的是( ) A.已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 B.已知C(s)+O 2 (g)═CO 2 (g)△H 1 C(s)+
O 2 (g)═CO(g)△H 2 ,则△H 2 >△H 11 2 C.已知2H 2 (g)+O 2 (g)═2H 2 O(g)△H=-483.6kJ/mol,则氢气的燃烧热为241.8kJ/mol D.已知NaOH(aq)+HCl(aq)═NaCl(aq)+H 2 O(l)△H=-57.3kJ/mol,则含20gNaOH的稀溶液与稀盐酸完全中和,中和热为28.65kJ/mol  啥都不懂BJ1年前1
啥都不懂BJ1年前1 -
 幸涛 共回答了23个问题
幸涛 共回答了23个问题 |采纳率82.6%A.已知C(石墨,s)═C(金刚石,s)△H>0,石墨能量小于金刚石,则金刚石比石墨活泼,石墨比金刚石稳定,故A错误;
B.己知2C(s)+2O 2 (g)═2CO 2 (g)△H 1 、2C(s)+O 2 (g)═2CO(g)△H 2 ,一氧化碳转化为二氧化碳是放热过程;焓变包含负号,则△H 1 <△H 2 ,故B正确;
C.氢气的燃烧热是值1mol氢气完全燃烧生成液态水放出的热量,单位是kJ/mol,气态水不是稳定氧化物,2H 2 (g)+O 2 (g)═2H 2 O(g)△H=-483.6kJ•mol -1 ,则燃烧热>
483.6KJ•mo l -1
2 =241.8kJ•mol -1 ,故C错误;
D.已知NaOH(aq)+HCl(aq)═NaCl(aq)+H 2 O(l)△H=-57.4 kJ•mol -1 ,中和热指1molNaOH和molHCl溶液发生中和反应生成1mol水时所放出的热量为57.4 kJ,则0.5molNaOH与强酸,中和热不变,中和热为△H=-57.4 kJ•mol -1 ,故D错误;
故选:B.1年前查看全部
- 下列关于石墨的性质和用途的说法不正确的是( ) A.熔点高,有滑腻感,可用于制润滑剂 B.质软,在纸上划过留痕迹,
下列关于石墨的性质和用途的说法不正确的是( )
A.熔点高,有滑腻感,可用于制润滑剂 B.质软,在纸上划过留痕迹,可用于制铅笔芯 C.有良好的导电性,可用于制干电池的电极 D.耐高温,可用于制作刻划玻璃的工具  neodawn1年前1
neodawn1年前1 -
 蓝筹被套 共回答了13个问题
蓝筹被套 共回答了13个问题 |采纳率84.6%D
物质的用途与性质是紧密联系的。由于石墨有滑腻感,可减小物质间的摩擦力,可作润滑剂,又由于耐高温可作耐高温的润滑剂。用作电池的电极,必须要求要有良好的导电性。玻璃较硬,刻划玻璃的工具必须是硬度很大的物质。1年前查看全部
- 为什么石墨和金刚石的差别那么大?
为什么石墨和金刚石的差别那么大?
与什么有关? shuiyaooo1年前3
shuiyaooo1年前3 -
 qianshen2006 共回答了23个问题
qianshen2006 共回答了23个问题 |采纳率100%石墨是层状结构,碳原子是sp2杂化,形成正六边形,每个层状结构就是这个六边形构成,层与层之间是范德法力,作用比较弱,然后碳原子还有一个电子空余,形成一个很大的π键,因此导电性、导热性很好.金刚石是共价晶体,碳原子...1年前查看全部
- 石墨在纸上划过后会留下痕迹,
 shun05_15291年前4
shun05_15291年前4 -
 威尔斯wells 共回答了17个问题
威尔斯wells 共回答了17个问题 |采纳率94.1%当然是物理变化,你再理解下化学反应的定义,
没有新分子产生1年前查看全部
- 相等质量的金刚石,石墨,C60的物质的量相同吗?
 ppul1n1年前1
ppul1n1年前1 -
 一是理想志向 共回答了23个问题
一是理想志向 共回答了23个问题 |采纳率95.7%相等质量金刚石和石墨物质的量相同,但是与C60不同,C60物质的量是以C60分子数计,不按C原子数计.1年前查看全部
- 比较金刚石和石墨的结果,下列说法正确的是() A.它们是同一种物质,只是内部微粒的排列不同 B.它们的物理性质有很大的差
比较金刚石和石墨的结果,下列说法正确的是() A.它们是同一种物质,只是内部微粒的排列不同 B.它们的物理性质有很大的差异 C.由于它们内部微粒排列规则不同,所以金刚为石晶体,石墨非晶体 D.金刚石是单晶体,石墨是多晶体 请回答者析下.
 WangXu99901年前2
WangXu99901年前2 -
 dghpkj 共回答了19个问题
dghpkj 共回答了19个问题 |采纳率89.5%a同一种元素形成的多种单质互为同素异形体.例如金刚石和石墨是碳的同素异形体.许多元素都能形成同素异形体,形成方式有:(1)分子里原子个数不同,如氧气和臭氧;(2)晶体里原子的排列方式不同,如金刚石和石墨;(3...1年前查看全部
- 下列物质的用途中,利用其化学性质的是A钨用于制作白炽灯丝B铁用于制作炊具C一氧化碳作燃料D石墨作电极
 掸烟先生1年前1
掸烟先生1年前1 -
 太阳mami 共回答了12个问题
太阳mami 共回答了12个问题 |采纳率83.3%c一氧化碳燃烧放热1年前查看全部
- 已知标准状态下石墨的燃烧焓为-393.7kJ.mol-1
已知标准状态下石墨的燃烧焓为-393.7kJ.mol-1
石墨转变为金刚石反映的焓变为+1.9kJ.mol-1
则金刚石的燃烧焓(kJ.mol-1)应为( )
A.+395.6
B.391.8
C.-395.6
D.-391.8
B.+391.8
漏了个+号,抱歉 大冬枣1年前2
大冬枣1年前2 -
 z3310762 共回答了25个问题
z3310762 共回答了25个问题 |采纳率88%燃烧当然是放热啦,所以只能选择C或D,又因为石墨的燃烧热为-393.7kj/mol,所以金刚石的燃烧热为393.7+1.9=395.6kj/mol;就看成是石墨先变成金刚石,先吸收1.9KJ,再由金刚石燃烧生成二氧化碳和水,放出395.6kj的能量!答案选C,是对的,希望可以帮上你的忙!1年前查看全部
- 高一化学两道选择题 只要答案下列物质属电解质的是 A胆矾B二氧化碳C新制的氯水D石墨 在铜-锌原电池中,锌片为A正极B负
高一化学两道选择题 只要答案
下列物质属电解质的是 A胆矾B二氧化碳C新制的氯水D石墨 在铜-锌原电池中,锌片为A正极B负极C阴极D阳极 yhq102251年前4
yhq102251年前4 -
 5201979100 共回答了15个问题
5201979100 共回答了15个问题 |采纳率93.3%下列物质属电解质的是 A胆矾B二氧化碳C新制的氯水D石墨(答案是A)
在铜-锌原电池中,锌片为A正极B负极C阴极D阳极(答案是B)补充:请问电极有阴阳极之分吗?哪个ZHU选C!1年前查看全部
- 金刚石1000度可以缓慢变会石墨 那常温下会不会也在超级缓慢进行这种反应?
 蔡寒雨1年前5
蔡寒雨1年前5 -
 inn001 共回答了17个问题
inn001 共回答了17个问题 |采纳率94.1%一百年有一个分子转变
那种速度可以理解为不进行1年前查看全部
- 石墨转变成金刚石的根本原因
 他吗的怎么这样1年前1
他吗的怎么这样1年前1 -
 wkb5445 共回答了20个问题
wkb5445 共回答了20个问题 |采纳率90%石墨与金刚石的成份都是碳,只是结构不同,金刚石的结构能量高,只有以适当的方式给予石墨能量,转变碳的结构,就可以转变为金刚石了1年前查看全部
- 为什么石墨中碳碳键键长比金刚石中的要短?
 anbooo1年前4
anbooo1年前4 -
 ss小熊 共回答了16个问题
ss小熊 共回答了16个问题 |采纳率93.8%石墨中的碳原子是sp2杂化,金刚石中的碳原子是sp3杂化原理基本如同楼上所说,但不必这么麻烦.石墨中碳碳之间由一根“西伽马”键和半根“派”键(其实是离域大派键)键合(引号中为发音,打不出希腊字母.),而金刚石中碳...1年前查看全部
大家在问
- 1求通项公式:1+1/2,1-3^2/4,1+5^2/6,1-7^2/8,…
- 2f(x)=loga&(a-a^x),(a大于1),f(x)的定义域和值域
- 3“首先,我们培养习惯;然后,习惯塑造我们。”这句话强调了 [ ] A.我
- 4意大利科学家最近合成了一种新型分子,它由4个氧原子构成.专家认为它液化后能量、密度都比普通氧分子高得多.关于该分子的叙述
- 5以生命科学、新能源、新材料、空间、海洋、环境和管理七大科技产业为龙头的新经济——网络经济已见端倪,这无疑是各国经济发展的
- 6已知,如图,在三角形abc中,ab=ac,点d,e分别在ab,ac上,且角abd=角ace,bd与ce相交于点o.求证(
- 7180字的高质量作文可以写什么?求学霸帮忙。悬赏五,不用写,只用帮我定个题。谢谢啦~
- 8如果甲数等于乙数的2.5倍,那么甲数和乙数______正比例关系.
- 9作文题目:人间温情处处在。开头和结尾怎么写(要原创)
- 10加工一批零件,甲独做8天完成,乙独做10天完成.甲乙合作,加工完这批零件的10分之9,需要几天?
- 11解方程组:{二分之x+y+二分之x-y=6,4(x+y)-5(x-y)=2()
- 12描写自然风光,气候特点,人物品质的词语(全部四个).
- 132009³+2009²-2010 分2009³-2*2009²-2007 简便运
- 14有一物体在10min内振内了1.8×106次,则该物体振动的频率为______Hz.
- 15关于雨的诗,词,句的精彩描述诗.词.例:卧听潇潇雨打蓬.什么什么而今听雨憎庐下,髻已星星也