铁在纯氧燃烧把铁丝作成旋转状的目的是什么?能使铁充分反应从而提高利用率吗?是提高利用率还是速率?
 胡萝卜心2022-10-04 11:39:542条回答
胡萝卜心2022-10-04 11:39:542条回答
已提交,审核后显示!提交回复
共2条回复
 lllppp3 共回答了18个问题
lllppp3 共回答了18个问题 |采纳率94.4%- 为了增大铁的受热面积,更好的与氧气有效高温接触,加快反应速率.聚集热量,防止热量散失
- 1年前
 西ff 共回答了2个问题
西ff 共回答了2个问题 |采纳率- 提高与氧气的接触面,从而使充分反应
- 1年前
相关推荐
- 在纯氧中燃烧一定量的铁粉,铁粉完全燃烧后生成固体质量增加,经测定固体增加的质量与2.4克镁完全燃烧后增加的质量相同,则铁
在纯氧中燃烧一定量的铁粉,铁粉完全燃烧后生成固体质量增加,经测定固体增加的质量与2.4克镁完全燃烧后增加的质量相同,则铁粉的质量是?
A、5.8g B、8.4g C、4.2g D、4g
我要计算过程,越清楚越好 他日尘去光生1年前2
他日尘去光生1年前2 -
 sffitness 共回答了15个问题
sffitness 共回答了15个问题 |采纳率86.7%2Mg+O2=2Mgo
48 80
2.4g 4g
∴增加的质量为1.6g
3Fe+2O2=Fe3O4
168 232
xg (x+1.6)g
x/168=(x+1.6)/232
x=4.2g
∴C1年前查看全部
- 演示铁在纯氧中燃烧实验时.将铁丝绕成螺旋状 ,为什么?
演示铁在纯氧中燃烧实验时.将铁丝绕成螺旋状 ,为什么?
A 提高利用率
B 增大反应的接触面积
C 提高反应温度
D 使瓶底氧气充分利用 tddnr1年前1
tddnr1年前1 -
 demiduan 共回答了18个问题
demiduan 共回答了18个问题 |采纳率94.4%B 增大反应的接触面积
B 增大反应的接触面积
B 增大反应的接触面积
B 增大反应的接触面积
B 增大反应的接触面积
B 增大反应的接触面积
B 增大反应的接触面积
B 增大反应的接触面积
B 增大反应的接触面积
B 增大反应的接触面积
B 增大反应的接触面积
B 增大反应的接触面积
B 增大反应的接触面积
B 增大反应的接触面积
B 增大反应的接触面积
B 增大反应的接触面积
B 增大反应的接触面积1年前查看全部
- 用CO还原赤铁矿可得到一种具有银白色金属光泽的单质A,A在纯氧中燃烧可得到一种黑色固体B,将A投入到稀盐酸溶液中,可产生
用CO还原赤铁矿可得到一种具有银白色金属光泽的单质A,A在纯氧中燃烧可得到一种黑色固体B,将A投入到稀盐酸溶液中,可产生一种可燃性气体C,将A投入硫酸铜溶液中,生成一种红色固体D.
(1)写出A、B、C、D的名称:
A______,B______,C______,D______.
(2)写出各步反应的化学方程式:
①______,②______,______③______,④______. leilil1年前3
leilil1年前3 -
 亲爱的萱 共回答了24个问题
亲爱的萱 共回答了24个问题 |采纳率95.8%解题思路:一氧化碳还原氧化铁生成二氧化碳和金属铁,铁在氧气中燃烧生成四氧化三铁,铁和盐酸反应生成氯化亚铁和氢气,金属铁可以和硫酸铜发生置换反应.(1)一氧化碳还原氧化铁生成二氧化碳和金属铁,故A是金属铁,铁在氧气中燃烧生成四氧化三铁,即B是四氧化三铁,铁和盐酸反应生成氯化亚铁和氢气,所以C是氢气,金属铁可以和硫酸铜发生置换反应,生成硫酸亚铁和金属铜,故D是金属铜.
故答案为:铁;四氧化三铁;氢气;铜.
(2)①一氧化碳还原氧化铁生成二氧化碳和金属铁,即2Fe2O3+3CO
高温
.
2Fe+3CO2,故答案为:2Fe2O3+3CO
高温
.
2Fe+3CO2;
②铁在氧气中燃烧生成四氧化三铁,即3Fe+2O2
点燃
.
Fe3O4,故答案为:3Fe+2O2
点燃
.
Fe3O4;
③铁和盐酸反应生成氯化亚铁和氢气,即Fe+2HCl=FeCl2+H2↑,故答案为:Fe+2HCl=FeCl2+H2↑;
④金属铁可以和硫酸铜发生置换反应,生成硫酸亚铁和金属铜,即Fe+CuSO4=FeSO4+Cu,故答案为:Fe+CuSO4=FeSO4+Cu.点评:
本题考点: 铁的化学性质;铁的氧化物和氢氧化物.
考点点评: 本题考查学生金属铁以及化合物的性质,注意知识的积累是解题的关键,难度不大.1年前查看全部
- 为了验证细铁丝在纯氧中燃烧产生“火星四溅”现象的原因,你设计的实验方案是?
 dogandwei1年前2
dogandwei1年前2 -
 蓝色ll鱼cupl 共回答了16个问题
蓝色ll鱼cupl 共回答了16个问题 |采纳率93.8%把细铁丝弯成螺旋状,下端绕上火柴,火柴即将烧尽前迅速把细铁丝伸入装有纯氧的集气瓶中(瓶底要放少量水或细沙)1年前查看全部
- 某钢样1.1 g在纯氧中完全燃烧,得到0.013 g二氧化碳,求此钢样中碳的质量分数.
某钢样1.1 g在纯氧中完全燃烧,得到0.013 g二氧化碳,求此钢样中碳的质量分数.
 jones1年前1
jones1年前1 -
 ai20031023 共回答了25个问题
ai20031023 共回答了25个问题 |采纳率92%解题思路:钢样在氧气中完全燃烧,其中的碳全部燃烧生成二氧化碳,可根据二氧化碳的质量计算出碳元素质量即钢样中所含碳的质量.0.013g CO2中C元素质量=0.013 g×[12/44×100%≈0.0035g
此钢样中碳的质量分数=
0.0035g
1.1g]×100%≈0.3%
答:此钢样中碳的质量分数约为0.3%.点评:
本题考点: 含杂质物质的化学反应的有关计算.
考点点评: 也可根据碳燃烧生成二氧化碳的化学方程式计算钢样中碳的质量.1年前查看全部
- 1.1g某钢样在纯氧中完全燃烧得到0.013g二氧化碳.求此钢样中碳的质量分数
 秋易浓1年前1
秋易浓1年前1 -
 萌梓 共回答了11个问题
萌梓 共回答了11个问题 |采纳率90.9%碳的质量=0.013*12/44=0.0035g
钢样中碳的质量分数=0.0035/1.1=0.32%1年前查看全部
- 某钢样1.1 g在纯氧中完全燃烧,得到0.013 g二氧化碳,求此钢样中碳的质量分数.
某钢样1.1 g在纯氧中完全燃烧,得到0.013 g二氧化碳,求此钢样中碳的质量分数.
 lee3322607091年前1
lee3322607091年前1 -
 马亮蛋 共回答了26个问题
马亮蛋 共回答了26个问题 |采纳率92.3%解题思路:钢样在氧气中完全燃烧,其中的碳全部燃烧生成二氧化碳,可根据二氧化碳的质量计算出碳元素质量即钢样中所含碳的质量.0.013g CO2中C元素质量=0.013 g×[12/44×100%≈0.0035g
此钢样中碳的质量分数=
0.0035g
1.1g]×100%≈0.3%
答:此钢样中碳的质量分数约为0.3%.点评:
本题考点: 含杂质物质的化学反应的有关计算.
考点点评: 也可根据碳燃烧生成二氧化碳的化学方程式计算钢样中碳的质量.1年前查看全部
- "硫在空气中燃烧的产物是二氧化硫,在纯氧中燃烧的产物是三氧化硫"
"硫在空气中燃烧的产物是二氧化硫,在纯氧中燃烧的产物是三氧化硫"
这句话为什么不对? z621571年前1
z621571年前1 -
 zhuxucn 共回答了17个问题
zhuxucn 共回答了17个问题 |采纳率100%因为在纯氧中由于氧气浓度高,会使生成的二氧化硫被氧化生成三氧化硫,这样就使生成的二氧化硫的量减少了.而空气中的氧含量较低,只能使少量的二氧化硫被氧化成为三氧化硫.我是这样理解的,三氧化硫不是燃烧产物,是又被氧化了的氧化产物1年前查看全部
- 22.使8.9g 乙醛、乙酸和甲酸甲酯的混合液体在纯氧中完全燃烧,经测定生成标准状况下CO2的体积为6.72L,此过程中
22.使8.9g 乙醛、乙酸和甲酸甲酯的混合液体在纯氧中完全燃烧,经测定生成标准状况下CO2的体积为6.72L,此过程中共消耗氧气的质量为
 believe01年前1
believe01年前1 -
 方辉 共回答了15个问题
方辉 共回答了15个问题 |采纳率93.3%本题比较复杂
乙醛分子式:C2H4O
乙酸分子式:C2H4O2
甲酸甲酯分子式:C2H4O2
很明显 乙酸 与 甲酸甲酯 的 分子式 相同
所以 燃烧的化学方程式 也与 乙酸相同
故可以把混合物乙酸 与 甲酸甲酯看做一种 物质 即 C2H4O2
设乙醛的 即C2H4O 物质的量为X,C2H4O2的物质的量为 Y
所以
44X + 60Y = 8.9 (1) 根据二者质量之和为8.9 克
因为生成标准状CO2体积6.72升
即CO2物质的量为:6.72/22.4=0.3mol
根据碳原子守恒
故原混合物有 0.3 / 2 = 0.15 mol
所以
X + Y = 0.15 (2)
结合 (1)(2)
得
X = 0.00625 mol
Y = 0.14375 mol
设C2H4O 消耗 O2 的物质的量为 M mol,C2H4O2消耗的O2 物质的量为 N mol
则
2C2H4O + 5 O2 =点燃= 4CO2 + 4H2O
2--------------5
0.00625------M
则
2 / 0.00625 = 5 / M
得
M=0.015625 mol
C2H4O2 + 2O2 =点燃= 2CO2 + 2H2O
1--------------2
0.14375-----N
则
1 / 0.14375 = 2 / N
得
N = 0.2875 mol
所以
消耗O2 物质的量为:0.015625 + 0.2875 = 0.303125 mol
氧气质量 m=0.303125 * 32 = 9.7 g
不明白HI1年前查看全部
- 某仅由碳、氢、氧三种元素组成的有机化合物,经测定其相对分子质量为90.去该有机化合物样品1.8g,在纯氧中完全燃烧,将产
某仅由碳、氢、氧三种元素组成的有机化合物,经测定其相对分子质量为90.去该有机化合物样品1.8g,在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重1.08g和2.64g.试求该有机化合物的分子式.
为什么后面增重1.08和2.64是水和co2的质量,通过浓硫酸和碱石灰会发生什么反应 feihu84101年前3
feihu84101年前3 -
 yllly 共回答了24个问题
yllly 共回答了24个问题 |采纳率91.7%燃烧生成水和二氧化碳,浓硫酸具有吸水性,吸收生成的水,没发生化学反应;碱石灰吸收二氧化碳:2NaOH + CO2 ==== Na2CO3 + H2O
氢的质量:1.08X2/18=0.12g
碳的质量:2.64X12/44=0.72g
氧的质量:1.8-0.12-0.72=0.96g
碳、氢、氧的个数比=(0.72/12):(0.12/1):(0.96/16)=1:2:1
分子式:(CH2O)n
n=3
C3H6O31年前查看全部
- 镁在 纯氧 和 二氧化碳气体空间里 那个气体会让镁燃烧最猛烈 是氧气中还是二氧化碳中
 深nn海1年前1
深nn海1年前1 -
 晨梦楚醒 共回答了12个问题
晨梦楚醒 共回答了12个问题 |采纳率100%大哥,这个小学生也该知道吧!氧气是助燃剂!二氧化碳是灭火用的!你应该知道答案了吧!1年前查看全部
- 铁丝在纯氧中燃烧 螺旋状铁丝提高局部温度 还是 增大反应面积?增大反应面积怎么理解?
 leesiro1年前2
leesiro1年前2 -
 tanxiangjun 共回答了13个问题
tanxiangjun 共回答了13个问题 |采纳率84.6%铁丝弯成螺旋状,增长了在氧气燃烧的铁丝的长度,同样可以说是增大了反应面积.1年前查看全部
- 乙炔在纯氧中燃烧的化学文字表达式
 shenlb20001年前1
shenlb20001年前1 -
 深圳酷儿 共回答了15个问题
深圳酷儿 共回答了15个问题 |采纳率86.7%乙炔+氧气----二氧化碳+水1年前查看全部
- 相同温度下,把水面上的空气换成同压的纯氧,100克水中溶解氧增多
相同温度下,把水面上的空气换成同压的纯氧,100克水中溶解氧增多
请说得详细点 谢谢 柳庄1年前1
柳庄1年前1 -
 独守奈何桥 共回答了21个问题
独守奈何桥 共回答了21个问题 |采纳率100%亨利定律:气体在理想液体中的溶解度与其分压成正比
纯氧压力1atm,空气中氧气分压0.2atm
so.1年前查看全部
- 相同质量的硫在纯氧中和空气中充分燃烧放热谁多
 糊糊抱个熊熊1年前3
糊糊抱个熊熊1年前3 -
 cyj622 共回答了14个问题
cyj622 共回答了14个问题 |采纳率100%忘记了
应该和纯氧中燃烧S形成三氧化硫有关,倒是忘记二氧化硫和氧气反应形成三氧化硫是吸热还是放热了(纯氧中燃烧S形成三氧化硫可以看作,再形成二氧化硫,在形成三氧化硫)1年前查看全部
- s在纯氧中燃烧生成so2吗?为什么呢?
s在纯氧中燃烧生成so2吗?为什么呢?
S在纯氧中燃烧为什么不生成SO3呢? 持续沸点1年前1
持续沸点1年前1 -
 升级买配件 共回答了16个问题
升级买配件 共回答了16个问题 |采纳率81.3%温度太高,so3又变为so2了,因为so2+o2的反应是放热反应.由于化学平衡,反应向逆反应移动,so3又恢复为so21年前查看全部
- 氨气在纯氧中点燃反应化学方程式?
 MorningFool1年前1
MorningFool1年前1 -
 騎李湘 共回答了15个问题
騎李湘 共回答了15个问题 |采纳率100%4 NH3 + 3 O2 ==点燃== 2 N2 + 6 H2O
一般不会生成氮氧化物,因为NO2、NO的形成需要高温,
点燃温度不够1年前查看全部
- 铁在纯氧中燃烧的现象是什么?之后又会生成四氧化三铁还是三氧化二铁?我要做作业,请快点回答,谢谢
 molly18lau1年前5
molly18lau1年前5 -
 唐娟 共回答了22个问题
唐娟 共回答了22个问题 |采纳率90.9%剧烈燃烧,火星四射,大量放热,生成黑色固体
之后生成四氧化三铁,3Fe+2O2=Fe3O41年前查看全部
- 取4.8克化合物M在纯氧中燃烧,生成二氧化碳13.2克,水10.8克,则化合物M的元素组成应为?
取4.8克化合物M在纯氧中燃烧,生成二氧化碳13.2克,水10.8克,则化合物M的元素组成应为?
A 一定含有C、H 可能含有O B.一定含有C.H.O
C 一定含有C.H 一定不含O D 缺少条件 无法判断 bluepatty1年前1
bluepatty1年前1 -
 月亮2007 共回答了15个问题
月亮2007 共回答了15个问题 |采纳率93.3%13.2g二氧化碳含碳 13.2g*12/44=3.6g
10.8g水 含氢 10.8g*2/18=1.2g
4.8g=3.6g+1.2g
所以 选 C 一定含有碳.氢元素,一定不含氧元素1年前查看全部
- 空气中的氧分子与纯氧中的氧分子化学性质相同么‘
 温柔的野马1年前3
温柔的野马1年前3 -
 香孩儿 共回答了25个问题
香孩儿 共回答了25个问题 |采纳率92%相同.因为通常来讲,分子是保持物质化学性质的最小微粒,只要分子相同,化学性质一定相同.
不过有的反应现象不同,是因为O2浓度不同.比如Fe在空气中加热只能达到红炽状态,而在纯氧中则能剧烈燃烧.1年前查看全部
- 在纯氧中燃烧一定量的铁粉,铁粉完全燃烧后生成固体质量增加,经测定固体增加的质量与2.4g的镁完全燃烧后增加的质量相同,则
在纯氧中燃烧一定量的铁粉,铁粉完全燃烧后生成固体质量增加,经测定固体增加的质量与2.4g的镁完全燃烧后增加的质量相同,则铁粉的质量是多少?
 bocheng0021年前1
bocheng0021年前1 -
 lilifeng98 共回答了24个问题
lilifeng98 共回答了24个问题 |采纳率75%根据反应方程式6Fe+4O2=2Fe3O4,2Mg+O2=2MgO可以看出,两个反应后固体增加的质量都为参加氧气的质量,经测定固体增加的质量与2.4g的镁完全燃烧后增加的质量相同,那么2.4克Mg消耗的氧气和铁粉完全燃烧消耗的氧气的量是一样的.然后由氧气的量可以算出铁的量!
清楚吗?你就自己去算吧,我也可以偷懒一下~1年前查看全部
- 为什么远古生物可以长这么大RT,有解释说是因为空气含氧量高,可我觉得就是在纯氧条件下,恐龙也不能长那么大.现在路地上最大
为什么远古生物可以长这么大
RT,有解释说是因为空气含氧量高,可我觉得就是在纯氧条件下,恐龙也不能长那么大.现在路地上最大的动物就是大象了,大象不能跳跃因为身体质量太大.我看恐龙的骨骼结构并不能支持那么大的身体蹦蹦跳跳的.除了氧气含量高,还有什么原因?古时地球引力小可不可能?
 dljiang1年前1
dljiang1年前1 -
 淡淡璎珞 共回答了19个问题
淡淡璎珞 共回答了19个问题 |采纳率84.2%原生态环境应该有利于动植物的生长,古时大型食肉恐龙,除了天灾几乎没有天敌,又有那么多的猎物.1年前查看全部
- 一克某样钢材在纯氧之中完全燃烧得到零点013克的二氧化碳求此钢材中碳的质量分数
 Mutian0501年前1
Mutian0501年前1 -
 newind33 共回答了17个问题
newind33 共回答了17个问题 |采纳率88.2%设该钢材中含碳元素的质量为X
C + O2 =点燃= CO2
12 44
X 0.013g
X=0.0035g
此钢材中碳的质量分数=0.0035g/1g*100%=0.35%
希望我的回答能对你的学习有帮助!1年前查看全部
- 铁在纯氧中燃烧生成的最高价氧化物是什么
 boden1231年前7
boden1231年前7 -
 这一生无悔 共回答了15个问题
这一生无悔 共回答了15个问题 |采纳率86.7%Fe 在氧气中燃烧 只能生成Fe3O4 无法生成Fe2O3
其中Fe3O4中有2个Fe是+3价 一个是+2价
可以看做Fe2O3-FeO1年前查看全部
- 实验室收集氧气,如需纯氧应用什么方法?
 绝情非无情1年前1
绝情非无情1年前1 -
 陈金华 共回答了22个问题
陈金华 共回答了22个问题 |采纳率95.5%排水集气法1年前查看全部
- 某仅由碳、氢、氧三种元素组成的有机化合物,经测定其相对分子质量为90.取有机物样品1.8g,在纯氧中完全燃烧,将产物先后
某仅由碳、氢、氧三种元素组成的有机化合物,经测定其相对分子质量为90.取有机物样品1.8g,在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重1.08g和2.64g.
(1)试求该有机物的分子式.
(2)若该有机物呈现酸性,且该有机物的核磁共振氢谱图中出现4个吸收峰,面积比为3:1:1:1,写出其结构简式. 戎装书生1年前0
戎装书生1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- A是只含碳、氢元素的有机物,相对分子质量为72;某学生设计了如图实验装置,使该Q试样在纯氧中燃烧,观察实验现象,分析有关
A是只含碳、氢元素的有机物,相对分子质量为72;某学生设计了如图实验装置,使该Q试样在纯氧中燃烧,观察实验现象,分析有关数据,推算元素含量.
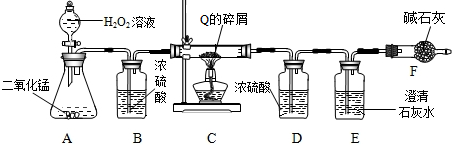
(1)仪器B的作用是______.
(2)A中产生32g氧气的体积相当于______升空气的含氧量(氧气密度按1.43g/L计算).
(3)若仪器C的玻璃管中放入的试样质量为43.2g,试样充分燃烧后,若仪器D增重64.8g,仪器E增重132.0g,则试样中含氢元素的质量为______g,试样中含碳元素的质量为______g,则Q的化学式为______.装置D与装置E如果颠倒的后果是使Q中______的质量分数变小.
(4)若装置中没有连接仪器B,将使该试样中氢元素的质量测算结果______(填“偏小”、“偏大”、“无影响”中之一).若装置中没有连接仪器F,将使该试样中______. lyg_wjs1年前1
lyg_wjs1年前1 -
 微笑的老狼 共回答了21个问题
微笑的老狼 共回答了21个问题 |采纳率95.2%解题思路:(1)根据浓硫酸的吸水性考虑;(2)用氧气的质量除以氧气的密度,算出氧气的体积,再根据氧气在空气中的体积分数算出空气的体积;(3)仪器D增重64.8g是有机物燃烧生成的水的质量,根据水的质量算出氢元素的质量;仪器E增重132.0g是有机物燃烧生成的二氧化碳的质量,根据二氧化碳的质量算出碳元素的质量,再根据碳元素与氢元素的原子个数比,结合相对分子质量,求出有机物的化学式,根据装置D与装置E如果颠倒的后果考虑谁的质量分数偏小;(4)根据装置B的作用考虑该试样中氢元素的质量偏大还是偏小;根据仪器F的作用考虑实验结果.(1)因为浓硫酸具有吸水性,所以仪器B的作用是除去氧气中的水蒸气,防止影响对有机物中氢元素的测定;(2)氧气的体积为:32g1.43g/L=22.38L,由于氧气约占空气体积的15,所以空气体积为:22.38L×5=111.9L;(3)...
点评:
本题考点: 物质的鉴别、推断.
考点点评: 解答本题关键是要知道氧气在空气中约占体积的[1/5];知道浓硫酸具有吸水性,根据浓硫酸质量的增加量,是水的质量,进而算出氢元素的质量;澄清石灰水能吸收二氧化碳,根据石灰水的质量的增加量就是二氧化碳的质量,进而计算出碳元素的质量,再计算出原子个数比,写出化学式.1年前查看全部
- 火燃烧是所产生的能量来自哪里?举个例子,在纯氧中,白磷燃烧,那么所得物质的质量与瓶中氧气和白磷的质量之和相等,那么火产生
火燃烧是所产生的能量来自哪里?
举个例子,在纯氧中,白磷燃烧,那么所得物质的质量与瓶中氧气和白磷的质量之和相等,那么火产生的那些热能和光能是来自于哪里的?如果它是来自白磷的,那么白磷的质量为什么不会减少.还有,核聚变算物理反应还是什么? zhaomqd1年前5
zhaomqd1年前5 -
 集市 共回答了18个问题
集市 共回答了18个问题 |采纳率94.4%化学反应的实质是化学键的重组,即旧键断裂,新键形成.旧键断裂时需吸收能量,新键形成是要放出能量,最终表现在放热或吸热要看那个过程占强势.1年前查看全部
- 下列说法符合事实的是( )A.纯碱不是碱B.碘化钾的水溶液遇淀粉显蓝色C.硫在空气中燃烧生成SO2,在纯氧中燃烧生成S
下列说法符合事实的是( )
A.纯碱不是碱
B.碘化钾的水溶液遇淀粉显蓝色
C.硫在空气中燃烧生成SO2,在纯氧中燃烧生成SO3
D.二氧化硅是一种酸性氧化物,不能与任何酸反应 wulinghello1年前1
wulinghello1年前1 -
 宴之逃者 共回答了18个问题
宴之逃者 共回答了18个问题 |采纳率83.3%解题思路:A.纯碱为碳酸钠;
B.淀粉遇碘变蓝色;
C.硫和氧气反应只生成SO2;
D.二氧化硅可与氢氟酸反应.A.纯碱为碳酸钠,为钠盐,因水解呈碱性,俗称纯碱,故A正确;
B.淀粉遇碘变蓝色,碘化钾不具有此性质,故B错误;
C.硫和氧气反应只生成SO2,不能生成SO3,故C错误;
D.二氧化硅可与氢氟酸反应,故D错误.
故选A.点评:
本题考点: 钠的重要化合物;硅和二氧化硅;含硫物质的性质及综合应用.
考点点评: 本题综合考查元素化合物知识,侧重于基础知识的综合考查和应用,为高频考点,有利于培养学生的良好的科学素养,提高学生学习的积极性,难度不大.1年前查看全部
- 取100g煤粉样品在纯氧中完全燃烧,经检验产生的气体中含二氧化碳275g,记算此煤是什么煤(假设无杂质)
取100g煤粉样品在纯氧中完全燃烧,经检验产生的气体中含二氧化碳275g,记算此煤是什么煤(假设无杂质)
算出含碳量 zxycf_1231年前2
zxycf_1231年前2 -
 心zz10000 共回答了19个问题
心zz10000 共回答了19个问题 |采纳率94.7%m(CO2) = 275g
m(C) = 275*12/44 = 75g
含碳量为75%,应该属于烟煤.1年前查看全部
- \某课外活动小组探究CH4和纯氧的反应,取CH4和纯氧组成的混合气体a mol通入装有9.3
某课外活动小组探究CH4和纯氧的反应,取CH4和纯氧组成的混合气体a mol通入装有9.3
某课外活动小组探究CH4和纯氧的反应,取CH4和纯氧组成的混合气体a mol通入装有9.36g Na2O2固体的密闭容器中,用电火花不断引燃,使之高温下充分反应,恢复至常温时,容器内压强几乎为零.剩余固体成分与a的取值及CH4与O2的体积比值n之间有很多种情况,试帮助该小组同学填写如下几种情况.
a取值n=VCH4/VO2剩余固体
Na2CO3,NaOH,Na2O2
Na2CO3,NaOH
Na2CO3,NaOH
Na2CO3 uptosupperman1年前1
uptosupperman1年前1 -
 amw1130906 共回答了15个问题
amw1130906 共回答了15个问题 |采纳率86.7%过程蛮多的,不好写,主要是利用质量守恒定律.其中C H O Na的物质的量守恒.
1.剩余固体为碳酸钠、氢氧化钠、过氧化钠隐含条件不存在水 01年前查看全部
- 氨气在空气中不能燃烧,但在纯氧中能剧烈燃烧?这是为什么?
 kmbbk1年前1
kmbbk1年前1 -
 灵魂dd 共回答了21个问题
灵魂dd 共回答了21个问题 |采纳率90.5%因为空气中氧气含量太低,有太多的堕性气体.1年前查看全部
- 氨气在纯氧中燃烧的方程式
 wwlftech1年前1
wwlftech1年前1 -
 虾丸 共回答了26个问题
虾丸 共回答了26个问题 |采纳率76.9%4NH3 + O2 = 2N2 + 6H2O1年前查看全部
- 为什么同样会生成Al2O3,Al在空气中不能燃烧,而在纯氧中就可以,或者说,为什么在纯氧中氧化铝不会阻止反应的继续发生?
 lyf228129021年前3
lyf228129021年前3 -
 lich_nova 共回答了23个问题
lich_nova 共回答了23个问题 |采纳率78.3%燃烧代表AL和氧气反应剧烈了,纯氧中氧浓度比空气中氧浓度高很多,浓度对反应速率有影响,浓度大,反应速率快,所以就燃烧了,空气中虽然没燃烧,但是也是在和氧气反应,虽然表面现象不同,其实本质是一样的,只不过是反应剧烈程度有差异1年前查看全部
- 为了验证细铁丝在纯氧中燃烧产生“火星四射”的现象的原因,应该怎样设计实验方案?
 huang_lin1年前1
huang_lin1年前1 -
 李软软 共回答了20个问题
李软软 共回答了20个问题 |采纳率80%取两段含碳量不同的铁丝 分别放入氧气瓶中1年前查看全部
- 某化合物在纯氧中燃烧成二氧化碳,二氧化硫
 zwl180202061年前1
zwl180202061年前1 -
 leandra 共回答了20个问题
leandra 共回答了20个问题 |采纳率100%CS2+3O2=燃烧=CO2+2SO21年前查看全部
- 某钢样1.1 g在纯氧中完全燃烧,得到0.013 g二氧化碳,求此钢样中碳的质量分数.
某钢样1.1 g在纯氧中完全燃烧,得到0.013 g二氧化碳,求此钢样中碳的质量分数.
 zizhe111年前1
zizhe111年前1 -
 peter5896 共回答了19个问题
peter5896 共回答了19个问题 |采纳率94.7%解题思路:钢样在氧气中完全燃烧,其中的碳全部燃烧生成二氧化碳,可根据二氧化碳的质量计算出碳元素质量即钢样中所含碳的质量.0.013g CO2中C元素质量=0.013 g×[12/44×100%≈0.0035g
此钢样中碳的质量分数=
0.0035g
1.1g]×100%≈0.3%
答:此钢样中碳的质量分数约为0.3%.点评:
本题考点: 含杂质物质的化学反应的有关计算.
考点点评: 也可根据碳燃烧生成二氧化碳的化学方程式计算钢样中碳的质量.1年前查看全部
- 在铁丝在纯氧中燃烧的实验中,为延长铁丝燃烧的时间,向盛有氧气的及其瓶中伸入铁丝的方法是什么?为什么?具体解释一下“从上到
在铁丝在纯氧中燃烧的实验中
,为延长铁丝燃烧的时间,向盛有氧气的及其瓶中伸入铁丝的方法是什么?为什么?
具体解释一下“从上到下,缓慢伸入”的含义.将铁丝弯成螺旋状,增大铁丝与氧气的接触面积 这我知道.
3楼的说 “又充分利用瓶内的氧气”
感激不尽! scully三三1年前1
scully三三1年前1 -
 童年江南 共回答了20个问题
童年江南 共回答了20个问题 |采纳率95%如果你一下就伸入进底部的话 、那么瓶口附近的空气就会被挤压出去
、 所以只能重上到下、 至于缓慢、 是为了让它的空气完全消耗1年前查看全部
- 为什么炭在纯氧中比在空气中燃烧得激烈?
 浪子爱洁1年前6
浪子爱洁1年前6 -
 醉舞ㄨ残月 共回答了21个问题
醉舞ㄨ残月 共回答了21个问题 |采纳率90.5%反应要接触面的
在纯氧中炭和氧接触机会大
在空气中炭和氧接触机会不如在纯氧中大1年前查看全部
- 为什么做探究某些化学物质与氧气产生反应的实验时,一般不取纯氧,而是直接使用空气?
 520zgc1年前3
520zgc1年前3 -
 冰嘉诺ice 共回答了23个问题
冰嘉诺ice 共回答了23个问题 |采纳率82.6%1)有些物质与氧气反应很剧烈,会造成意外伤害
2)节省资源1年前查看全部
- (3分)通过学习化学,我们知道氧气能使带火星的木条复燃,那么能使带火星的木条复燃的是否一定是纯氧呢?为了弄清这个问题,才
(3分)通过学习化学,我们知道氧气能使带火星的木条复燃,那么能使带火星的木条复燃的是否一定是纯氧呢?为了弄清这个问题,才仕实验学校化学小组进行了如下探究:
①取5个大小相同的集气瓶,分别编为1、2、3、4、5号,并分别使瓶内留有占集气瓶容积10%、20%、30%、40%、50%的水(余下为空气),用玻璃片盖住并倒扣在装有水的水槽中。
②分别用排水法向上述5个瓶子中通入氧气,小心地把5个瓶内的水排完后,用玻璃片盖住瓶口,取出正放好。
③将带火星的木条伸入5个瓶中,观察到的现象如下:
请你参与探究,回答下列问题:编号 1 2 3 4 5 现象 微亮 亮 很亮 复燃 复燃
(1)从观察到的现象可知,使带火星的木条复燃所需氧气的最小体积分数介于 号瓶与 号瓶之间。
(2)用排水法收集满氧气后,4号瓶中氧气的体积分数约为 ;
(提示:空气中氧气的体积分数约为21%)
(3)若要得到更准确的体积分数范围,只要调整①步骤中集气瓶内水的体积,并重复上述实验即可,你认为调整后瓶内水占集气瓶容积的体积分数为 。 agkof1年前1
agkof1年前1 -
 zhfufo 共回答了18个问题
zhfufo 共回答了18个问题 |采纳率94.4%(1)3 4 (2)52.6% (3)30%~40%
(1)探究能使带火星木条复燃所需氧气的最低体积分数:用等距法(如用五瓶不同组分的气体)、中值法(用空气和氧气按1:1混和,依次实验);找到木条复燃和不复燃的分界点,在于3号瓶和4号瓶间;
(2)4号瓶中氧气的体积分数约为:40%+60%х21%=52.6%;
(3)更准确的体积分数范围应介于3号瓶和4号瓶体积分数之间。1年前查看全部
- 下列叙述中,不正确的是( )A.花香四溢说明分子不停地做无规则运动B.铁在纯氧中剧烈燃烧,生成氧化铁C.大量的二氧化硫
下列叙述中,不正确的是( )
A.花香四溢说明分子不停地做无规则运动
B.铁在纯氧中剧烈燃烧,生成氧化铁
C.大量的二氧化硫气体排放到空气中易形成酸雨
D.一切化学反应都遵循质量守恒定律 2qg9n8w31年前1
2qg9n8w31年前1 -
 qrmkdm 共回答了24个问题
qrmkdm 共回答了24个问题 |采纳率83.3%解题思路:A、花香四溢说明分子不停地做无规则运动;
B、铁在纯氧中剧烈燃烧,生成四氧化三铁;
C、大量的二氧化硫气体排放到空气中易形成酸雨,因为二氧化硫与水反应生成亚硫酸,继而生成硫酸;
D、一切化学反应都遵循质量守恒定律.A、花香四溢说明分子不停地做无规则运动,说法正确,故A正确;
B、铁在纯氧中剧烈燃烧,生成四氧化三铁而非氧化铁,故B错误;
C、大量的二氧化硫气体排放到空气中易形成酸雨,因为生成硫酸,故C说法正确;
D、一切化学反应都遵循质量守恒定律,说法正确,故D正确.
故选B.点评:
本题考点: 物质的微粒性;空气的污染及其危害;金属的化学性质;酸雨的产生、危害及防治;质量守恒定律及其应用.
考点点评: 了解利用原子和分子的性质分析和解决问题的方法;掌握分子的性质:1.分子是独立存在而保持物质化学性质的最小粒子;2.分子有一定的大小和质量;分子间有一定的间隔;分子在不停的运动;分子间有一定的作用力.1年前查看全部
- 一个树一年能制造多少纯氧
 隋炀帝1101年前2
隋炀帝1101年前2 -
 大楼的窗外 共回答了21个问题
大楼的窗外 共回答了21个问题 |采纳率81%很多,够一个人呼吸的1年前查看全部
- 下列说法不正确的是( )①Al2O3用作耐火材料、Al(OH)3用作阻燃剂②硫粉在过量的纯氧中燃烧可以生成SO3③少量
下列说法不正确的是( )
①Al2O3用作耐火材料、Al(OH)3用作阻燃剂
②硫粉在过量的纯氧中燃烧可以生成SO3
③少量SO2通过浓的CaCl2溶液能生成白色沉淀
④工业上生产水泥和玻璃均用到的原料是石灰石
⑤在工业生产中用银和浓硝酸反应制取硝酸银
⑥工业上常用硅制造光导纤维
⑦镁的冶炼MgCl2(熔融)
Mg+Cl2↑电解 .
⑧用热的纯碱溶液清洗油污CO32-+2H2O⇌H2CO3+2OH
⑨用氢氟酸刻蚀玻璃:4HF+SiO2═SiF4↑+2H2O
⑩自然界中不存在游离态的硅,硅主要以二氧化硅和硅酸盐的形式存在.
A.②③⑤⑥⑧
B.①③⑥⑨
C.④⑤⑨⑩
D.②③⑥⑦ billfoxf21年前1
billfoxf21年前1 -
 tygg3 共回答了21个问题
tygg3 共回答了21个问题 |采纳率85.7%解题思路:①Al2O3熔点高、Al(OH)3加热易分解;
②硫粉在过量的纯氧中燃烧可以生成SO2;
③SO2通与CaCl2溶液不反应;
④水泥和玻璃均含有硅酸钙;
⑤工业生产中制取硝酸银应尽量避免环境污染,且节约原料;
⑥制造光导纤维的主要原料为二氧化硅;
⑦工业用电解熔融的氯化镁的方法冶炼镁;
⑧用热的纯碱溶液呈碱性,可用于除去油污;
⑨氢氟酸与二氧化硅反应;
⑩硅为亲氧元素.①Al2O3熔点高、Al(OH)3加热易分解,可用于阻燃剂,故正确;
②硫粉在过量的纯氧中燃烧可以生成SO2,不能生成三氧化硫,应在催化作用下生成,故错误;
③亚硫酸酸性比盐酸弱,SO2通与CaCl2溶液不反应,故错误;
④水泥和玻璃均含有硅酸钙,可用石灰石为原料,故正确;
⑤工业生产中制取硝酸银应尽量避免环境污染,且节约原料,可用氧化银和硝酸反应,故错误;
⑥制造光导纤维的主要原料为二氧化硅,故错误;
⑦工业用电解熔融的氯化镁的方法冶炼镁,故正确;
⑧用热的纯碱溶液呈碱性,可用于除去油污,但水解以一步为主,应为CO32-+H2O⇌HCO3-+OH-,故错误;
⑨氢氟酸与二氧化硅反应,可用于雕刻玻璃,故正确;
⑩硅为亲氧元素,在自然界中主要以二氧化硅和硅酸盐的形式存在,故正确.
故选A.点评:
本题考点: 硅和二氧化硅;含硫物质的性质及综合应用;镁、铝的重要化合物.
考点点评: 本题综合考查硅及其化合物的考查,为高考高频考点,侧重于元素化合物知识的综合理解和运用的考查,注意相关基础知识的积累,难度不大.1年前查看全部
- 0.94g某有机物在纯氧中完全燃烧,可生成二氧化碳2.64g,水0.54g,同时消耗氧气2.24g.又知此有机物蒸气0.
0.94g某有机物在纯氧中完全燃烧,可生成二氧化碳2.64g,水0.54g,同时消耗氧气2.24g.又知此有机物蒸气0.224L(已折算成标准状况下)的质量为0.94g.
(1)求此有机物的分子式.
(2)若此有机物跟FeCl3溶液作用显紫色,写出此有机物的结构简式. guo20011991年前0
guo20011991年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 某烃5.6g,在纯氧中燃烧,产物通过浓H2SO4后,增重7.2g,通过NaOH溶液增重17.6g,若该有机物蒸汽对H2相
某烃5.6g,在纯氧中燃烧,产物通过浓H2SO4后,增重7.2g,通过NaOH溶液增重17.6g,若该有机物蒸汽对H2相对密度28,求烃分子式.
 闲云悠水1年前1
闲云悠水1年前1 -
 太郎的袜子 共回答了16个问题
太郎的袜子 共回答了16个问题 |采纳率93.8%因为改有机物对H2的相对密度是28,即摩尔质量为H2的28倍,所以M=2X28=56,质量为5.6g,物质的量n=m/M=5.6/56=0.1mol,烃类燃烧后的产物有2种,即H2O和CO2,浓H2SO4增重7.2g,即水的质量为7.2g,由此可算出水的物质的量为0.4mol,NaOH溶液增重17.6g,即CO2的质量为17.6g,由此可知CO2的物质的量为0.4mol,根据元素守恒,0.1mol的该烃中有0.4mol的C和0.8mol的H,所以该烃的分子式应为C4H8 谢谢1年前查看全部
- 铁丝在纯氧中燃烧火星四射的原因,实验工具有细纯铁丝、细含碳铁丝、镁条、几瓶纯氧、酒精灯、火柴、镊子
铁丝在纯氧中燃烧火星四射的原因,实验工具有细纯铁丝、细含碳铁丝、镁条、几瓶纯氧、酒精灯、火柴、镊子
要有假设及验证方法,简洁的 shin71年前1
shin71年前1 -
 亚琛 共回答了18个问题
亚琛 共回答了18个问题 |采纳率72.2%①(3分)是否所有金属在纯氧中燃烧都没有火焰 (1分) 取镁条,细铜丝(1分)用同样方法点燃伸入装纯氧的集气瓶,观察是否有火焰(1分)
②(4分)若为铁丝中含碳引起的(1分),应取细纯铁铁丝,细含碳铁丝分别在纯氧中点燃观察(1分);若所有金属丝在纯氧中燃烧都会火星四射(1分),则应同时取上述几种金属丝用砂子将表面打磨后分别在纯氧中燃烧观察现象(1分)1年前查看全部
- 汽油、柴油、煤气、煤的燃烧温度请问汽油、柴油、煤气和煤在空气中和在纯氧的环境中的燃烧温度各是多少?
 梦赢6181年前1
梦赢6181年前1 -
 shuwing 共回答了21个问题
shuwing 共回答了21个问题 |采纳率81%汽油:燃点427℃ 汽油燃烧最高温度1200℃ 柴油:燃点220℃ 柴油燃烧最高温度1800℃ 煤气:外火1000℃ 内火800℃煤:无烟煤+鼓风机吹风的情况下燃烧1700℃ ——1900℃1年前查看全部
- 1.用还原赤铁矿可得到一种具有银白色金属光泽的单质A,A在纯氧中燃烧得到一种黑色固体B,将B投入到稀硫酸中,可得到溶质为
1.用还原赤铁矿可得到一种具有银白色金属光泽的单质A,A在纯氧中燃烧得到一种黑色固体B,将B投入到稀硫酸中,可得到溶质为C和D的混合溶液,则A、B、C、D的化学式分别是:
2. 将一定质量的镁铝合金投入100mL一定物质的量浓度HCl中,合金全部溶解,向所得溶液中滴加5mol/L的NaOH溶液到过量,生成沉淀的质量与加入的NaoH溶液的体
积关系如图:
求A点为多少?具体的方程式和式子)

图上有个地方错了。A点的地方,沉淀是19.4... 5513600011年前1
5513600011年前1 -
 alexissui 共回答了19个问题
alexissui 共回答了19个问题 |采纳率94.7%赤铁矿被还原生成铁单质,A是Fe.Fe在纯氧中燃烧生成四氧化三铁B为Fe3O4.Fe3O4可视为FeO·Fe2O3所以C和D分别为FeSO4和Fe2(SO4)3.就是这个分析,真的没有计算方法.
2.当加入体积为20ml的时候把盐酸完全的中和了,在A点的时候生成Mg(OH)2和Al(OH)3,在180的时候Al(OH)3反应生成AlO2^-
Al(OH)3 + OH- = AlO2^- + 2H2O.得到Al(OH)3的质量为15.5 - 11.6 = 3.9g 氢氧化铝的物质的量为3.9/78 = 0.05mol,消耗氢氧根为0.05mol
11.6为氢氧化镁的质量Mg(OH)2,物质的量为11.6/58 = 0.2mol,则消耗氢氧根的量为0.4mol
共消耗氢氧化钠0.45mol.体积为0.45/5 x 1000 = 90ml
加上一开始中和盐酸的20ml,则在A点的体积为90+20 = 110ml
不够详细,很多都是文字,请见谅.
有问题欢迎追问.
希望我的回答能够对你有所帮助1年前查看全部
大家在问
- 1一堆水果有梨、桃、苹果,它们的重量之比为4:5:8,桃比苹果少36千克,这堆水果重多少千克?
- 2淘气的云雀津津乐道的,是飞行中看到的好风景.仿写句子
- 3证明:若a,b,c属R,则a+1/b,b+1/c,c+1/a中至少有一个不小于2
- 4词语释义。 1. take care of [ ] A. a lot o
- 5如果一个正方形的一对对边各增加2厘米成为长方形,面积就增加16平方厘米,原来的正方形面积是______.
- 6雨滴从屋顶上自由下落,经0.2s的时间通过竖直方向上1.8m高的窗户,空气阻力不计,求窗户上沿距屋顶的高度.(g取10m
- 7什么是榆钱?什么是榆钱树?5该比张图来,THANKS
- 8( ),虽相隔万水千山.诗句
- 9myfavouritesport作文70词
- 10如果每千克盈利15元,每天可出售500KG,经调查,每涨一元,销量减少20kg.为获得最大利润,应该涨几元?
- 11ATP和磷酸肌酸肌肉中,什么时候ATP转化为磷酸肌酸?什么时候磷酸肌酸转化为ATP?
- 12一篇阅读短文,
- 13问一道圆的方程的题目已知过2定圆的一个交点O 的动直线 与2圆分别交于 A B 求线段AB中点P的轨迹方程以O点为圆心
- 14i didnt know what did u say翻译成中文是什么?
- 15语法填空(共10小题,每小题1.5分,共15分)
