在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计如图实验以确认上述混合气体中有C2H4和
 yangjh0252022-10-04 11:39:541条回答
yangjh0252022-10-04 11:39:541条回答 在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计如图实验以确认上述混合气体中有C2H4和SO2.
在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计如图实验以确认上述混合气体中有C2H4和SO2.(1)写出实验室制备乙烯的化学方程式:
| 浓硫酸 |
| 170℃ |
| 浓硫酸 |
| 170℃ |
(2)I、II、III、IV装置可盛放的试剂是I______;II______;III______;IV______(将下列有关试剂的序号填入空格内);
A.品红溶液B.NaOH溶液 C.浓H2SO4D.酸性KMnO4溶液
(3)能说明SO2气体存在的现象是______;
(4)使用装置II的目的是______;
(5)使用装置III的目的是______;
(6)确定含有乙烯的现象是______.

已提交,审核后显示!提交回复
共1条回复
 porsche25 共回答了17个问题
porsche25 共回答了17个问题 |采纳率94.1%- 解题思路:(1)实验室制备乙烯所用的原料为乙醇,浓硫酸作催化剂、脱水剂,反应条件是加热到170℃,溶液加热为防暴沸,加入沸瓷片;
(2)多种产物需检验时,应考虑先后顺序;
(3)二氧化硫能漂白品红;
(4)氢氧化钠能吸收二氧化硫;
(5)品红溶液不褪色确认SO2已除干净;
(6)Ⅲ中无二氧化硫,Ⅳ中与高锰酸钾溶液作用的为乙烯.(1)利用乙醇在浓硫酸的催化作用下发生分子内脱水制取乙烯,乙醇发生了消去反应,故答案为:CH3CH2OH
浓硫酸
170℃ CH2=CH2↑+H2O;催化剂、脱水剂;防止暴沸;
(2)检验二氧化硫用品红溶液,检验乙烯用高锰酸钾酸性溶液,乙烯和二氧化硫都能使高锰酸钾酸性溶液褪色,所以先检验二氧化硫,然后检验乙烯,同在检验乙烯之前用NaOH溶液除尽SO2,再通过品红溶液不褪色确认SO2已除干净,最后用高锰酸钾酸性溶液褪色检验乙烯,因装置I用来检验SO2,试管中品红溶液褪色,说明含有SO2,装置II试管装有NaOH溶液除去SO2,装置III试管通过品红溶液不褪色确认SO2已除干净,装置IV 通过高锰酸钾酸性溶液褪色检验乙烯,
故答案为:A;B;A;D;
(3)装置I用来检验SO2,试管中品红溶液褪色,说明含有SO2,故答案为:Ⅰ中品红溶液褪色;
(4)装置Ⅱ试管装有NaOH溶液除去SO2,故答案为:吸收SO2;
(5)装置Ⅲ试管通过品红溶液不褪色确认SO2已除干净,故答案为:检验SO2是否已经被完全吸收;
(6)装置Ⅳ通过高锰酸钾酸性溶液褪色检验乙烯,故答案为:Ⅲ中的品红不褪色,Ⅳ中的高锰酸钾溶液褪色.点评:
本题考点: 乙烯的实验室制法.
考点点评: 本题考查了乙烯的实验室制法以及产物的检验,注意当有多种产物需检验时,应考虑先后顺序,高锰酸钾既能氧化二氧化硫,又能氧化乙烯,是解答本题的关键. - 1年前
相关推荐
- 下列装置常用于实验室制取气体。根据给出的装置回答下列问题:
下列装置常用于实验室制取气体。根据给出的装置回答下列问题:

(1)指出编号仪器名称:① ;② 。
(2)实验室利用D装置制取氧气,反应原理用化学方程式表示为 。利用F装置收集氧气的最佳时刻是 。
(3)制取并收集二氧化碳应选择的装置是 ,使用该套装置制取气体的突出优点是 ,该反应原理用化学方程式表示为 。
(4)实验室选用右图装置收集二氧化碳,气体应该从 (填“a”或“b”)进入。若G装置内装满水时,还可以用于测定不溶于水且不与水反应的气体体积,此时还需要 (填仪器名称),该气体应从 (填“a”或“b”)进入
 tayo1年前1
tayo1年前1 -
 缺憾是有的 共回答了23个问题
缺憾是有的 共回答了23个问题 |采纳率95.7%(1)①长颈漏斗 ②试管
(2)2KMnO 4 △ K 2 MnO 4 + MnO 2 + O 2 ↑ 当气泡连续不断均匀产生时开始收集
(3)BE能控制反应的速率 CaCO 3 +2HCl==CaCl 2 +H 2 O+CO 2 ↑ (4)a量筒 b
1年前查看全部
- 实验室配制90g溶质质量分数为10%的稀硫酸,需要60%的硫酸(密度1.5g/cm3)多少毫升?需水多少
实验室配制90g溶质质量分数为10%的稀硫酸,需要60%的硫酸(密度1.5g/cm3)多少毫升?需水多少
要过程、、那个密度有什么用啊@@ 8303191年前1
8303191年前1 -
 婷儿BLOG 共回答了8个问题
婷儿BLOG 共回答了8个问题 |采纳率75%需要60%浓硫酸的质量90×10/60=15克
15克浓硫酸的体积15/1.5=10毫升
需要水75克.1年前查看全部
- 实验室用下图装置制取少量溴苯,试填写下列空白。
实验室用下图装置制取少量溴苯,试填写下列空白。

(1).写出仪器A的名称 ;B的名称 ;
(2).请你写出实验室制取溴苯的化学方程式 ___ ;
(3).长导管的下口为什么不插入锥形瓶的液面下
(4).反应完毕后,向烧瓶A中滴加NaOH 溶液的作用是:
(5).冷凝水的进水口是(填m或n) ,,图中干燥管C的作用是 爱情的契约1年前1
爱情的契约1年前1 -
 wwwindy 共回答了8个问题
wwwindy 共回答了8个问题 |采纳率87.5%1年前查看全部
- 实验室如何分离苯钾酸和苯钾醛
 simon周1年前1
simon周1年前1 -
 天天水吧 共回答了19个问题
天天水吧 共回答了19个问题 |采纳率84.2%稀碱液处理,弱碱性条件下萃取分离.萃取后水相酸化,此时可再行萃取,以与盐类分离.1年前查看全部
- 下列说法正确的是( )A.用点燃的方法鉴别甲烷和乙烯B.等物质的量的乙醇和乙酸完全燃烧时所需氧气的质量相等C.实验室常
 下列说法正确的是( )
下列说法正确的是( )
A.用点燃的方法鉴别甲烷和乙烯
B.等物质的量的乙醇和乙酸完全燃烧时所需氧气的质量相等
C.实验室常用如图所示的装置制取少量的乙酸乙酯
D.糖类、蛋白质、油脂属于天然高分子化合物 caodefeng1年前1
caodefeng1年前1 -
 polopolo2223 共回答了21个问题
polopolo2223 共回答了21个问题 |采纳率95.2%A.乙烯中含碳量高,燃烧有黑烟,甲烷燃烧有淡蓝色的火焰,现象不同,能鉴别,故A正确;
B.1mol乙醇消耗3mol氧气,1mol乙酸消耗2mol氧气,消耗的氧气的质量不等,故B错误;
C.装置制取少量的乙酸乙酯,导管不能深入碳酸钠溶液中,易倒吸,故C错误;
D.糖类中的多糖为高分子化合物,油脂、单糖、二糖均不属于高分子化合物,故D错误;
故选A.1年前查看全部
- (5分)下图所示为实验室常用的实验装置:
(5分)下图所示为实验室常用的实验装置:

据此回答下列问题:
(1)实验室制取和收集CO 2 时应选用 两种装置相连接,检验集气瓶中CO 2 是否收集满的方法是 。
(2)F装置可用来测量生成的CO 2 气体的体积,其中在水面上放一层植物油的目的是 。用100mL量筒接收排出的水时,液面如右图所示,该液体的体积是 mL。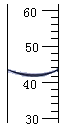
(3)实验室用KMnO 4 制取O 2 时,可选用的发生装置是 。 ago9p1年前1
ago9p1年前1 -
 失落上海 共回答了18个问题
失落上海 共回答了18个问题 |采纳率88.9%(1)BD,用燃着的木条,放在集气瓶口,熄灭,则满
(2)隔开水和二氧化碳,防止二氧化碳溶于水, 42.0 (3)A
1年前查看全部
- 小明和同学在打扫实验室时,发现实验桌上有一个灯泡,灯泡上标明额定电压为4V,额定功率看不清楚.小明很想知道它的额定功率,
小明和同学在打扫实验室时,发现实验桌上有一个灯泡,灯泡上标明额定电压为4V,额定功率看不清楚.小明很想知道它的额定功率,刚好桌上还有电阻箱、电流表、开关、12V的稳压电源各一个,小明用它们连成了如图所示的电路,其中R为电阻箱,小明测出了电流表示数随电阻箱阻值变化的几组值,并将其记录在如下的表格中.
(1)当电流为0.50A时,电阻箱两端的电压是______V,灯泡的电阻为______Ω.电流/A O.90 0.80 0.50 O.36 0.28 0.22 电阻/Q 8 10 20 30 40 50
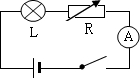
(2)根据表中数据,请求出小灯泡的额定功率.
(3)小明的同学发现小明记录的数据中有一个电流值有错误,这个错误数据是______A.
(4)小明的同学认为利用图示器材还能进行下列实验,其中无法完成的是______.
A.测量小灯泡正常工作时的电阻B.探究小灯泡的亮度与灯泡功率的关系
C.探究导体中的电流与电压的关系D.探究串联电路中电流的特点. rxc04441年前1
rxc04441年前1 -
 xinli65053 共回答了14个问题
xinli65053 共回答了14个问题 |采纳率78.6%解题思路:(1)由实验数据知,当电流为0.50A时,电阻箱接入电路的电阻,利用U=IR得到电阻箱两端电压;已知电源电压和电阻箱两端电压,可以得到灯泡两端电压;已知灯泡两端电压和通过的电流,利用R=[U/I]得到灯丝电阻;
(2)灯泡正常发光时,两端电压为额定电压,已知电源电压和灯泡两端电压,可以得到电阻箱两端电压;利用电阻箱两端电压确定表格中电流和电阻的对应关系;已知电路电流和灯泡额定电压,利用P=UI得出额定功率.
(3)确定错误的电流值,应该利用公式I=[U/R],从电压或电阻两方面分析,已知电源电压不变,所以电流错误从电阻角度考虑.
(4)明确每一个实验的原理和基本实验过程,就能确定正确的选项.(1)由实验数据知,当电路电流为I=0.5A时,电阻箱接入电路的电阻为R=20Ω,电阻箱两端电压为UR=IR=0.5A×20Ω=10V;
灯泡两端电压为UL=U-UR=12V-10V=2V
所以灯泡的电阻为RL=
UL
I =[2V/0.5A]=4Ω
(2)灯泡正常发光时,电阻箱两端电压为U′R=U-U额=12V-4V=8V;
因为U=IR,也就是8V=IR,查表知,此时通过电阻箱的电流为0.8A
所以灯泡的额定功率为P额=U额I额=0.8A×4V=3.2W;
(3)由上面的计算知,在电流为0.5A时,灯泡电阻为4Ω,由于灯丝电阻随温度的升高而增大,随电路电流的减小而减小,在最后一组数据中,灯泡电阻应该小于4Ω,而电路电流I=0.22A时,灯泡电阻大于4Ω,所以是此电流值错误.
(4)A 既然能完成上面的第一小题,所以此实验可完成;
B 灯泡亮度决定于实际功率,改变电阻箱接入电路的电阻,灯泡两端电压发生改变,亮度相应改变,所以此实验可完成;
C 探究电流与电压的关系,需要保持电阻一定,而灯泡电阻随电流大小发生改变,所以此实验无法完成;
D 在现有器材中,只要改变电流表的位置,就能探究串联电路电流的特点,所以此实验可完成.
故选C.
故答案为:(1)10;4;(2)3.2;(3)0.22;(4)C.点评:
本题考点: 探究用电器的电功率实验;电功率的计算.
考点点评: 灯泡电阻随温度的升高而变大,能够考虑到电阻与温度的关系,是第三小题突破的关键.1年前查看全部
- 下面是实验室里几种常见的仪器,请你指出其中几种仪器的用途.
下面是实验室里几种常见的仪器,请你指出其中几种仪器的用途.
天平和砝码:
电流表:
停表:
酒精灯: eretgd1年前1
eretgd1年前1 -
 薏苡人 共回答了26个问题
薏苡人 共回答了26个问题 |采纳率96.2%天平和砝码:称量
电流表:测电流
停表:计算单摆周期
酒精灯:加热1年前查看全部
- (2009•崇明县二模)实验室用氯化钠配制lOOg溶质质量分数为20%的氯化钠溶液,现有下列操作:①溶解;②称取氯化钠;
(2009•崇明县二模)实验室用氯化钠配制lOOg溶质质量分数为20%的氯化钠溶液,现有下列操作:①溶解;②称取氯化钠;③计算;④量取水;⑤装瓶贴标签.正确的操作顺序是( )
A.①②③④⑤
B.③②④①⑤
C.①③⑤②④
D.③②④⑤① intria1年前1
intria1年前1 -
 startle 共回答了19个问题
startle 共回答了19个问题 |采纳率89.5%解题思路:根据配制溶质质量分数一定的溶液的基本步骤考虑;配制溶质质量分数一定的溶液的基本步骤:计算、称量、量取、溶解、装瓶存放.
故选B.点评:
本题考点: 一定溶质质量分数的溶液的配制.
考点点评: 通过回答本题知道了配制溶质质量分数一定的溶液的基本步骤,要熟记它们并能灵活运用.1年前查看全部
- 如图所示的装置是实验室常用来制取和收集气体的装置.
如图所示的装置是实验室常用来制取和收集气体的装置.
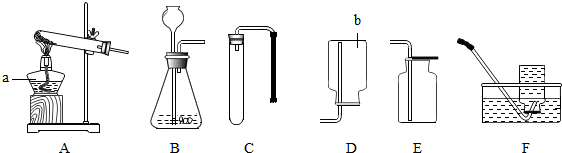
(1)写出仪器a和b的名称:a______,b______;如果选择实验装置A和F组合,用氯酸钾和二氧化锰来制取氧气,反应的方程式为2KClO3
2KCl+3O2↑MnO2 .△ 2KClO3,加热时试管口为什么应略向下倾斜______.
2KCl+3O2↑MnO2 .△
(2)某同学打算用大理石和稀盐酸制取二氧化碳,他选择了装置B和E连接,当稀盐酸和大理石都加入装置B一段时间后,他用燃着的火柴在E的瓶口试验,火柴仍然燃烧,你认为原因可能是______.
(3)过氧化钠(Na2O2)是一种淡黄色固体,能与水反应生成氢氧化钠和氧气.用该反应来制取一瓶氧气,应选择的实验装置是______(填字母编号).反应方程式为______. DLSS0011年前1
DLSS0011年前1 -
 北极的星星草 共回答了28个问题
北极的星星草 共回答了28个问题 |采纳率92.9%解题思路:(1)据常用仪器回答;并据氯酸钾分解的反应原理书写方程式,加热时试管口下倾是为了防止冷凝水倒流引起试管炸裂;
(2)根据装置特点分析原因;
(3)据反应物状态和反应条件选择发生装置,据气体的密度和性质选择收集装置,据反应原理书写方程式.(1)标号仪器分别是酒精灯和集气瓶;用氯酸钾和二氧化锰来制取氧气,反应的方程式为2KClO3
MnO2
.
△2KCl+3O2↑;加热时试管口下倾是为了防止冷凝水倒流引起试管炸裂;
(2)观察装置可知:B装置中的长颈漏斗下端未伸入液面以下,会导致生成的二氧化碳从长颈漏斗逸出;
(3)过氧化钠(Na2O2)是一种淡黄色固体,能与水反应生成氢氧化钠和氧气,该反应不需加热,属于固液常温型,故选发生装置C,氧气密度比空气大且不易溶于水,可用向上排空气法或排水法收集,根据反应原理,方程式是:2Na2O2+2H2O=4NaOH+O2↑;
故答案为:
(1)酒精灯;集气瓶;2KClO3
MnO2
.
△2KCl+3O2↑;防止冷凝水倒流使试管破裂;
(2)CO2已经从长颈漏斗上口逸出到空气中;
(3)C和E(或C和F);2Na2O2+2H2O=4NaOH+O2↑.点评:
本题考点: 常用气体的发生装置和收集装置与选取方法;实验室制取氧气的反应原理;二氧化碳的实验室制法;书写化学方程式、文字表达式、电离方程式.
考点点评: 据反应物状态和反应条件选择发生装置,据气体的密度和性质选择收集装置,据反应原理书写方程式,并能据装置特点分析相关问题.1年前查看全部
- 、从实验室用氯酸钾于二氧化锰制取氧气后的残渣中(假定反应充分)回收氯化钾和二氧化锰.
 zjx21cn1年前4
zjx21cn1年前4 -
 小鱼蛮儿 共回答了16个问题
小鱼蛮儿 共回答了16个问题 |采纳率93.8%加水后,用过滤纸过滤氯化钾和二氧化锰,把过滤纸上的水分蒸发掉,就可以得到干燥的氯化钾和二氧化锰.1年前查看全部
- 脱落酸的全合成路线哪里有?但是我要的是实验室可以实现的有机合成的全合成路线……
 孤心蓝冰1年前1
孤心蓝冰1年前1 -
 Ж一箭穿心Ж 共回答了19个问题
Ж一箭穿心Ж 共回答了19个问题 |采纳率94.7%脱落酸(ABA)生物合成一般有两条途径:C15直接途径和C40间接途径,前者经C15法呢焦磷酸(FPP)直接形成ABA;后者经由类胡萝卜素的氧化裂解间接形成ABA,是高等植物ABA生物合成的主要途径.9-顺式环氧类胡萝卜素氧化裂解为黄质醛是植物ABA生物合成的关键步骤,然后黄质醛被氧化形成一种酮,该过程需NAD为辅因子,酮再转变形成ABA-醛,ABA-醛氧化最终形成ABA.在该途径中,玉米黄质环氧化酶(ZEP)、9-顺式环氧类胡萝卜素双加氧酶(NCED)和醛氧化酶(AO)可能起重要作用.
将吲哚、γ-丁内酯、氢氧化钾加入到四氢萘中,搅拌下加热溶解,回流脱水,升温至200℃,脱水至理论量的四分之三,开始脱溶,在1~1.5h内脱水至理论量,温度上升至300℃,并保持0.5h.稍冷后加入二甲苯和热水溶解,趁热分液.水层冷却后用盐酸中和,得粗品,再用苯重结晶,得成品1年前查看全部
- (2012•泰安)某兴趣小组的同学从实验室收集到一桶含有FeSO4、CuSO4的废液,他们想从中回收金属铜和硫酸亚铁晶体
(2012•泰安)某兴趣小组的同学从实验室收集到一桶含有FeSO4、CuSO4的废液,他们想从中回收金属铜和硫酸亚铁晶体,设计了如下实验方案.结合实验方案回答下列问题:

(1)步骤①中,金属X是______,该反应的化学方程式为______;
(2)步骤②中,加入过量稀硫酸的目的是______;
(3)从滤液中获得硫酸亚铁晶体采用的方法是______. 踩了谁的尾巴1年前1
踩了谁的尾巴1年前1 -
 流浪的ll 共回答了14个问题
流浪的ll 共回答了14个问题 |采纳率92.9%解题思路:(1)由于目的是获得铜单质和硫酸亚铁,所以需要将铜离子转化为铜单质,而溶液中需要的是硫酸亚铁而不能引入新的杂质,所以加入的能够将铜离子转化为铜单质的只能是单质铁;
(2)由于加入的铁是过量的,加入过量稀硫酸的目的是除去铜中的铁;
(3)蒸发从溶液中获得晶体常采用的方法.(1)由题意可知,由于需要将铜离子转化为铜单质,而溶液还必须为硫酸亚铁,即不能引入新的杂质,所以可以加入铁将铜离子转化为铜单质.该反应的化学方程式为:Fe+CuSO4 ═FeSO4 +Cu;
(2)步骤②中,加入过量稀硫酸的目的是:使铁完全反应,除去铜中的铁;
(3)从滤液中获得硫酸亚铁晶体采用的方法是蒸发.
故答为:(1)铁,Fe+CuSO4 ═FeSO4 +Cu;(2)使铁完全反应,除去铜中的铁;(3)蒸发.点评:
本题考点: 金属活动性顺序及其应用.
考点点评: 解答本题时要注意混合物的分离要考虑为彻底分开而加入过量试剂,所以后一环节需要将之除去.1年前查看全部
- 高中化学除杂有关CO2实验室中除去生成气体中的CO2我只知道有氢氧化钠、碱石灰、石灰水还有什么液体和固体可以除主要是固体
高中化学除杂有关CO2
实验室中除去生成气体中的CO2
我只知道有氢氧化钠、碱石灰、石灰水
还有什么液体和固体可以除
主要是固体、、高中阶段哦,稍微超一点只要能理解也行
为啥要问固体除杂、、给个例子吧
将一种烃燃烧,生成的有水二氧化碳
现在要检测它俩的质量,将生成气体先通入广口瓶(长进短出),然后过U形管
因为要测质量所以要先除水、、后除二氧化碳
广口瓶放浓硫酸无疑问,U形管内放什么去除二氧化碳? orthodox1年前2
orthodox1年前2 -
 derrick8511 共回答了21个问题
derrick8511 共回答了21个问题 |采纳率76.2%首先你要明白co2是酸性氧化物
而酸性氧化物之间是有一定的通性的通性1.与水反应生成相应的酸(除了二氧化硅SiO2,它不与水反应)2.与碱反应生成盐和水3.与碱性氧化物反应故Co2能与任何碱性氧化物反应1年前查看全部
- 下列方法不可用于实验室制备卤化氢气体的是
下列方法不可用于实验室制备卤化氢气体的是
A.NaCl饱和溶液与稀硫酸共热制备HCl
B.NaF固体与浓硫酸共热制备HF
C.KI固体与浓硫酸共热制备HI
D.NaBr固体与稀硫酸共热制备HBr
详细解析!谢~~~~!
说一下为什么,怎么办,会有哪些后果,好的给分! yx_shan1年前1
yx_shan1年前1 -
 漫步憧憬 共回答了13个问题
漫步憧憬 共回答了13个问题 |采纳率92.3%B 是正确答案2NAF+H2SO4=2HF+_NA2SO41年前查看全部
- 怎么才花费最少?某实验室需购某种化工原料150千克,现在市场上原料按袋出售,有两种包装,一种是每袋45千克,价格为280
怎么才花费最少?
某实验室需购某种化工原料150千克,现在市场上原料按袋出售,有两种包装,一种是每袋45千克,价格为280元;另一种是每袋36千克,价格为240元,在满足需要的条件下,最少要花费多少元?(答案是1000元)
怎么求出来的? shulun04281年前1
shulun04281年前1 -
 关东项羽 共回答了23个问题
关东项羽 共回答了23个问题 |采纳率82.6%第一种x袋,第二种y袋
则需满足45x+36y>=150
求花费S=280x+240y最小值
这里利用的方法是 线性规划分析
通过作图,平移,就可以得出合适的整数点.课本上有这个内容吧
这里只有x=1,y=3满足条件.1年前查看全部
- 实验室里有两卷钢丝,甲卷钢丝标签注明直径是0.9毫米;乙卷钢丝比这卷更细,但没有标签.如果没
实验室里有两卷钢丝,甲卷钢丝标签注明直径是0.9毫米;乙卷钢丝比这卷更细,但没有标签.如果没
实验室里有两卷钢丝,甲卷钢丝标签注明直径是0.9毫米;乙卷钢丝比这卷更细,但没有标签.如果没有刻度尺,请你利用简易的物品,设计一下方案测出乙卷钢丝的直径. limengxuan1年前3
limengxuan1年前3 -
 江作青罗带 共回答了14个问题
江作青罗带 共回答了14个问题 |采纳率92.9%1、截取两种钢丝相同的长度(最好长些可减小误差):质量甲、质量乙.
2、因为质量 = 密度 * 体积,体积 = 横截面 * 长度,
所以:质量 = 密度 * 横截面 * 长度
3、又因为:甲乙密度,长度都相等,所以横截面比等于质量比:
横截面甲 :横截面乙 = 质量甲 :质量乙
4、又因为横截面比等于直径比的平方:
横截面甲 :横截面乙 = 直径甲2:直径乙2
5、 所以开方后即可得甲乙的直径比,又知道了甲的直径,当然就可以
算出乙的直径大小了.1年前查看全部
- 实验室用温度计最小刻度是多少啊就是那个……最小刻度就是了啊
 我享我瘦1年前1
我享我瘦1年前1 -
 mia_rua 共回答了16个问题
mia_rua 共回答了16个问题 |采纳率100%21年前查看全部
- 氢气的 实验室制法 还有工业制法.
氢气的 实验室制法 还有工业制法.
用化学方程式表达. 9qhbud1年前1
9qhbud1年前1 -
 kele555 共回答了12个问题
kele555 共回答了12个问题 |采纳率91.7%实验室制法:
用锌与稀盐酸反应
Zn+H2SO4=ZnSO4+H2↑
工业制法:
利用电解饱和食盐水产生氢气
2NaCl+2H2O=电解=2NaOH+Cl2↑+H2↑1年前查看全部
- 药品实验室配制一种试剂,药与水的比是3:5,药比水的质量少100克,药有多少克?(用三种方法解答)
 492948991年前1
492948991年前1 -
 hotsunsea12 共回答了15个问题
hotsunsea12 共回答了15个问题 |采纳率93.3%5*X-3*X=100
X=50G
药是 3*50=150g
水是 5*50=250g1年前查看全部
- 实验室制氨气的化学方程式为______.
 u159zaq1年前1
u159zaq1年前1 -
 258936 共回答了16个问题
258936 共回答了16个问题 |采纳率100%解题思路:实验室制取氨气根据盐和碱的复分解反应的原理,常用氯化铵固体与熟石灰固体混合加热,生成氯化钙,水和氨气,依此确定方程式.实验室制取氨气,通常采用氯化铵和氢氧化钙发生复分解反应,生成氯化钙、氨气和水制得氨气,化学反应方程式为Ca(OH)2+2NH4Cl
△
.
CaCl2+2H2O+2NH3↑,
故答案为:Ca(OH)2+2NH4Cl
△
.
CaCl2+2H2O+2NH3↑.点评:
本题考点: 氨的实验室制法.
考点点评: 本题考查了氨气的制备原理,解答时需理解盐和碱的复分解反应的原理,题目难度不大.1年前查看全部
- 急,高中重要的化学方程式,实验室制各种气体,及注意事项
急,高中重要的化学方程式,实验室制各种气体,及注意事项
高考 tc9mvpr1年前1
tc9mvpr1年前1 -
 karleuleralbert 共回答了23个问题
karleuleralbert 共回答了23个问题 |采纳率69.6%实验指导书有!还有得买一本数理化公式大全!当工具书用,别拿来背额- -!1年前查看全部
- 生石灰放入水中的化学方程式( ) 实验室制取氢气的方法(
生石灰放入水中的化学方程式( ) 实验室制取氢气的方法(
生石灰放入水中的化学方程式( ) 实验室制取氢气的方法( ) spirit_ll1年前1
spirit_ll1年前1 -
 真的喝高了 共回答了19个问题
真的喝高了 共回答了19个问题 |采纳率84.2%CaO + H2O = Ca(OH)2
2HCl +Zn = H2(向上箭头)+ZnCl21年前查看全部
- 实验室需要标况下11.2L的CO2,现用CaCO3与250ml足量稀盐酸反应怎么以物质的量来求
 怕输才不怪1年前3
怕输才不怪1年前3 -
 紧张的可怜人 共回答了20个问题
紧张的可怜人 共回答了20个问题 |采纳率90%CaCO3 + 2HCl = CaCl2 + H2O + CO2
2mol 1mol
M×250/1000 11.2/22.4
计算M就是要用的HCl的摩尔浓度.1年前查看全部
- 实验室制氧气时,选择下列哪组药瓶产生氧气的速度快而且质量多?
实验室制氧气时,选择下列哪组药瓶产生氧气的速度快而且质量多?
A.10克KClO3和5克Mno2 B.10克KClO3和5克KMnO4
C.10克MnO2和5克KClO3 D.10克KMnO4和5克KClO3 忆哥1年前1
忆哥1年前1 -
 iiii 共回答了15个问题
iiii 共回答了15个问题 |采纳率93.3%答案选 B.1年前查看全部
- 实验室制取二氧化碳不能使用稀硫酸的原因是
 小胖雪爱大头飞1年前1
小胖雪爱大头飞1年前1 -
 rilson 共回答了19个问题
rilson 共回答了19个问题 |采纳率78.9%硫酸钙是微溶于水的,多了之后会阻碍反应进行1年前查看全部
- 某校进行化学实验需要1000g质量分数为19.6%的稀硫酸,但是实验室中只有质量分数为98%的浓硫酸,则需要进行的操作如
某校进行化学实验需要1000g质量分数为19.6%的稀硫酸,但是实验室中只有质量分数为98%的浓硫酸,则需要进行的操作如下
需要浓硫酸的质量为 需要加入水的质量为 藏珍斋1年前1
藏珍斋1年前1 -
 dingshaoning 共回答了21个问题
dingshaoning 共回答了21个问题 |采纳率95.2%浓硫酸稀释一定要将浓硫酸慢慢倒入水中,并且不停的搅拌.
需要浓硫酸的量=1000*19.6%/98%=
1000克减去浓硫酸的量,就是需要加水的量.1年前查看全部
- 电泳时loading buffer和样品DNA比例多少?实验室常用6x的,为毛有人用1:5,有人1:1呢?3Q~
 眼小聚光1年前1
眼小聚光1年前1 -
 热带袋鼠 共回答了14个问题
热带袋鼠 共回答了14个问题 |采纳率78.6%这玩意,说白了就是溴酚蓝做一个参照,你不加都一样的能够跑出条带来,我从来都是1:10加的,没问题.所谓6X就是稀释6倍使用,你如果严格的话按1:5加.1年前查看全部
- 实验室用浓度为0.500mol/L的标准氢氧化钠溶液来测定未知浓度的盐酸,完善下列实验过程:
实验室用浓度为0.500mol/L的标准氢氧化钠溶液来测定未知浓度的盐酸,完善下列实验过程:
(1)滴定管使用前,先要检查滴定管的活塞______,活塞旋转是否灵活.
(2)把标准氢氧化钠溶液注入用标准氢氧化钠溶液润洗过的蓝色手柄滴定管中,使液面位于______位置,记录读数.
(3)在锥形瓶中放入20.00mL的待测溶液,再滴加2滴酚酞,摇匀.用标准氢氧化钠溶液滴定,边滴边摇动锥形瓶,眼睛注视______的变化.直到滴入最后一滴氢氧化钠溶液,指示剂的颜色由______色变为______色,并在半分钟内溶液颜色不发生变化,停止滴定,记录读数.
(4)重复(2)和(3)操作,并记录数据.再次滴定消耗氢氧化钠溶液的数据如下表:
次数 滴定前(mL) 滴定后(mL) 1 0.40 21.10 2 0.10  第2次滴定后滴定管的读数如图所示,将这一读数填入上表中.根据表中的数据计算出盐酸的浓度为______mol/L.
第2次滴定后滴定管的读数如图所示,将这一读数填入上表中.根据表中的数据计算出盐酸的浓度为______mol/L.
已知盐酸的准确浓度为0.490mol/L,则实验误差为______%.
(5)会造成实验结果偏高的操作是______(填写编号).
a.锥形瓶用蒸馏水洗净后,立即装入待测溶液
b.振荡时溶液溅出锥形瓶外
c.滴定时蓝色手柄滴定管中的液体滴在锥形瓶外. zhengwenhua1年前1
zhengwenhua1年前1 -
 jally521 共回答了13个问题
jally521 共回答了13个问题 |采纳率84.6%解题思路:(1)滴定管使用前,先要检查活塞是否漏水;
(2)装液后要调0,使液面处于0刻度或0刻度以下某一刻度记录读数;
(3)酸碱中和滴定时,眼睛要注视锥形瓶内溶液的颜色变化;溶液颜色变化且半分钟内不变色,可说明达到滴定终点;
(4)滴定管的刻度由上而下刻度增大,精度为0.01mL,据此结合图象读数;求出1、2组平均消耗V(NaOH),根据盐酸和NaOH反应求出C(盐酸);根据实验误差=
×100%;△c c(标准)
(5)根据c(待测)=
分析不当操作对V(标准)的影响,以此判断浓度的误差;c(标准)×V(标准) V(待测) (1)滴定管使用前,先要检查活塞是否漏水;
故答案为:是否漏液;
(2)装液后要调0,使液面处于0刻度或0刻度以下某一刻度记录读数;
故答案为:0刻度或0刻度以下;
(3)酸碱中和滴定时,眼睛要注视锥形瓶内溶液的颜色变化,滴定终点时溶液颜色由无色突变为粉红色,且半分钟内不褪色;
故答案为:锥形瓶中溶液颜色;无色;粉红;
(4)第2次滴定后滴定管的读数20.10mL,两次滴定消耗氢氧化钠溶液的体积分别为:19.70mL,20.00mL,
求出1、2组平均消耗V(NaOH)=19.85mL,
HCl+NaOH═NaCl+H2O
20.00mL×C( HCl)19.85mL×0.500mol/L
则C(HCl)=[19.85mL×0.500mol/L/20.00mL]=0.496mol/L,
已知盐酸的准确浓度为0.490mol/L,则实验误差为[0.496mol/L−0.490mol/L/0.490mol/L]×100%=1.2%;
故答案为:0.496mol/L;1.2%;
(5)a.锥形瓶用蒸馏水洗净后,立即装入待测溶液,待测液的物质的量不变,对V(标准)无影响,根据
c(待测)=
c(标准)×V(标准)
V(待测)可知,c(待测)无影响,故a错误;
b.振荡时溶液溅出锥形瓶外,待测液的物质的量偏小,导致V(标准)偏小,根据c(待测)=
c(标准)×V(标准)
V(待测)可知,c(待测)偏小,故b错误;
c.滴定时蓝色手柄滴定管中的液体滴在锥形瓶外,导致V(标准)偏大,根据c(待测)=
c(标准)×V(标准)
V(待测)可知,c(待测)偏大,故c正确;
故选:c;点评:
本题考点: 配制一定物质的量浓度的溶液.
考点点评: 本题主要考查了中和滴定操作、误差分析以及计算,难度不大,理解中和滴定的原理是解题关键.1年前查看全部
- 实验室怎样制取CO方程式
 范冰冰的苹果1年前2
范冰冰的苹果1年前2 -
 wgy528 共回答了12个问题
wgy528 共回答了12个问题 |采纳率83.3%实验室一般使用浓硫酸在加热条件下催化草酸分解并用氢氧化钠除掉二氧化碳制得一氧化碳,具体反应如下:
1.COOH・COOH===Δ===CO2↑+CO↑+H2O(H2SO4催化)
2.2NaOH+CO2======Na2CO3+H2O1年前查看全部
- 实验室需要22g二氧化碳,现用含碳酸钙90.00%的石灰石与足量的稀盐酸反应
实验室需要22g二氧化碳,现用含碳酸钙90.00%的石灰石与足量的稀盐酸反应
实验室需要22g(标准状况)二氧化碳,现用含碳酸钙90.0%的石灰石与足量的稀盐酸反应(该石灰石中的杂质不与稀盐酸反应).问
(1)至少需要含碳酸钙90.0%的石灰石多少克?
(2)生成的氯化钙的物质的量是多少? 封361年前1
封361年前1 -
 漱芳斋呀 共回答了21个问题
漱芳斋呀 共回答了21个问题 |采纳率90.5%22gCO2是0.5mol,对应0.5mol的C原子完全来源于CaCO3,每个碳酸钙分子含有1个C
所以需要0.5mol碳酸钙,即50g,需要石灰石50/90%=55.6g
同理,消耗了0.5mol碳酸钙,里面的钙为0.5mol,且全部转化为CaCl2,所以氯化钙的物质的量为0.5mol1年前查看全部
- 实验室制乙酸乙酯,可不可采用乙酸过量,为什么?
 homechangshu1年前1
homechangshu1年前1 -
 lom110 共回答了22个问题
lom110 共回答了22个问题 |采纳率86.4%不可以,浓硫酸在受热时被乙醇还原,生成二氧化硫气体,
乙醇过量,浓硫酸损耗大起不到催化、脱水的作用.1年前查看全部
- 实验室利用大理石与100克稀盐酸刚好反应制取二氧化碳,如果制取二氧化碳4.4克,求:(见下面的补充)
实验室利用大理石与100克稀盐酸刚好反应制取二氧化碳,如果制取二氧化碳4.4克,求:(见下面的补充)
(1)需用含碳酸钙质量分数为96%的大理石多少克?(2)稀盐酸的质量分数是多少? gaozai11年前1
gaozai11年前1 -
 yamaziyi 共回答了24个问题
yamaziyi 共回答了24个问题 |采纳率79.2%CaCO3+2HCl=CaCl2+H2O+CO2(气体箭号)
100 73 44
0.96x y 4.4g
100 44
一一一= 一一
0.96x 4.4g
x=10.4g
73 44
一一一=一一一
y 4.4g
y=7.3g
(HCl)%=7.3g/100g=7.3%1年前查看全部
- 实验室中需要标准状况下11.2升的二氧化碳,现在含碳酸钙99%的石灰石与250毫升足量的稀盐酸反应,该石灰石中的杂质不与
实验室中需要标准状况下11.2升的二氧化碳,现在含碳酸钙99%的石灰石与250毫升足量的稀盐酸反应,该石灰石中的杂质不与盐酸反应,问至少需要含碳酸钙90%的石灰石多少克?
 170355411年前4
170355411年前4 -
 装靓宝宝 共回答了18个问题
装靓宝宝 共回答了18个问题 |采纳率94.4%11.2 L 0.5 mol
CaCO3 + 2 H+ = Ca2+ + H2O + CO2(气体)
0.5 mol 0.5 mol
0.5 mol / 90% * 100 g/mol = 55.6 g
答案:55.6g1年前查看全部
- 实验室区分硫酸钠及亚硫酸钠溶液应采用
实验室区分硫酸钠及亚硫酸钠溶液应采用
实验室区分Na2SO4及Na2SO3溶液应采用
A 硝酸钡溶液
B 加热煮沸
C 加入盐酸或硫酸
D 加入苛性钠溶液 mousecui1年前2
mousecui1年前2 -
 音乐机 共回答了23个问题
音乐机 共回答了23个问题 |采纳率87%应选C,因为亚硫酸钠溶液会与酸反应生成SO2气体,会产生大量气泡1年前查看全部
- 实验室配制溶液的问题.未冷却至室温就将溶液转移到容量瓶并定容.会有什么结果,为什么?
 西部传奇1年前1
西部传奇1年前1 -
 池洼胜治 共回答了9个问题
池洼胜治 共回答了9个问题 |采纳率88.9%导致溶液体积小于预期体积.原因是,高温情况下存在体积膨胀现象1年前查看全部
- 氨是重要的化工原料,实验室制取氨气的化学方程式为?这套卷子是?
 zzq5841年前1
zzq5841年前1 -
 fba365 共回答了15个问题
fba365 共回答了15个问题 |采纳率73.3%氯气 制取原理——强氧化剂氧化含氧化合物 制取方程式——MnO2 4HCl(浓)MnCl2 Cl2↑ 2H2O 装置——分液漏斗,圆底烧瓶,加热 检验——能使湿润的蓝色石蕊试纸先变红后褪色; 除杂质——先通入饱和食盐水(除HCl),再通入浓H2SO4(除水蒸气) 收集——排饱和食盐水法或向上排气法 尾气回收——Cl2 2NaOH=== NaCl NaClO H2O1年前查看全部
- 科学,两个字“急,”1、氧气在通常情况下是一种()颜色、()气味的气体.实验室可以采用()法和()法收集氧气,这是根据氧
科学,两个字“急,”
1、氧气在通常情况下是一种()颜色、()气味的气体.实验室可以采用()法和()法收集氧气,这是根据氧气()和()的性质而决定的.
2、有4瓶无色气体,它们分别是氧气、空气、氮气和二氧化碳气体.用燃着的木条去鉴别它们时,木条燃烧现象没有显著变化的是(),能使木条燃烧更加剧烈的是(),能使燃着的木条熄灭的气体是()和(),要想确定这两瓶气体究竟是哪一种物质,还应该进行的简便操作是( ),判断的依据是( ) 希望沉默的P1年前2
希望沉默的P1年前2 -
 yc52 共回答了16个问题
yc52 共回答了16个问题 |采纳率93.8%无,无,排水法,向上排空气法,不易溶于水,密度大于空气
空气,氧气,二氧化碳,氮气,加入澄清石灰水,石灰水变混浊1年前查看全部
- 适合实验室用的1200度马弗炉有哪些规格?
 刚好1年前2
刚好1年前2 -
 瓜瓜猪猪 共回答了22个问题
瓜瓜猪猪 共回答了22个问题 |采纳率86.4%常用的是SXF-5-12可编程高温炉,SXC-4-13C一体化程控高温炉1年前查看全部
- 实验室制取二氧化碳一般有五步实验操作:请排列顺序
实验室制取二氧化碳一般有五步实验操作:请排列顺序
检查装置的气密性
按要求组装好仪器
向长颈漏斗中注入吸盐酸
向锥形瓶中加入大理石块
检查气体是否集满
收集二氧化碳 歪木瓜1年前1
歪木瓜1年前1 -
 穿越麦田 共回答了17个问题
穿越麦田 共回答了17个问题 |采纳率88.2%按要求组装好仪器
检查装置的气密性
向锥形瓶中加入大理石块
向长颈漏斗中注入吸盐酸
收集二氧化碳
检查气体是否集满1年前查看全部
- 某同学在做电池的串联实验室,他先测出每接干电池的电压为1.5V,然后他将三节电池串联起来,但是他将最右边的电池接反了!问
某同学在做电池的串联实验室,他先测出每接干电池的电压为1.5V,然后他将三节电池串联起来,但是他将最右边的电池接反了!问这时候用电压表测该电池组的电压,回是多少V?
 鎏法世家1年前1
鎏法世家1年前1 -
 valencia 共回答了19个问题
valencia 共回答了19个问题 |采纳率100%因为一个装反了,就会相互抵消同样的电压大小,所以应该是是3v-1.5v=1.5v.
谢谢1年前查看全部
- 氯气的实验室制法:参与反应的4molHCL中 多少molHCL被氧化,多少molHCL体现酸性?
 guomian19831年前2
guomian19831年前2 -
 aibuzaila2 共回答了21个问题
aibuzaila2 共回答了21个问题 |采纳率90.5%有2mol体现氧化性,2mol体现酸性.主要看Cl原子的化合价,有2mol化合价有-1升高到0,故有2mol被氧化,2mol化合价没变,是做酸.1年前查看全部
- 实验室用6.96g二氧化锰和50g36.5%的盐酸共热,问:
实验室用6.96g二氧化锰和50g36.5%的盐酸共热,问:
1.在标准状况下可产生氯气多少升?
2.如不考虑HCL挥发,将反应后溶液加水稀释到250毫升,取25毫升和足量硝酸银溶液反应,可得沉淀多少克?
第一小题做出来了.主要是第2小题不会.. 微色芽芽1年前2
微色芽芽1年前2 -
 洋洋泡泡 共回答了24个问题
洋洋泡泡 共回答了24个问题 |采纳率91.7%1.二氧化锰的物质的量为:6.96g÷87g/mol=0.08mol
HCl的物质的量为:50g×36.5%÷36.5g/mol=0.5mol
MnO2量不足,所以用MnO2来算.
Cl2的体积为:0.08mol×22.4L/mol=1.792L
2.Cl^-的物质的量为:0.5mol-0.08mol×2=0.34mol 沉淀的质量为:0.34mol×143.5g/mol×10%=4.879g1年前查看全部
- 一道选择(选错的)A地球上物体自转的向心加速度不一定都指向地心,赤道上的向心加速度比两级大B卡文地许第依次在实验室测出万
一道选择(选错的)
A地球上物体自转的向心加速度不一定都指向地心,赤道上的向心加速度比两级大
B卡文地许第依次在实验室测出万有引力常量
C可在运行的太空藏用弹簧称测物体所受到的重力 mzylee1年前1
mzylee1年前1 -
 fm1068 共回答了24个问题
fm1068 共回答了24个问题 |采纳率83.3%选c
A 地球并不完全均匀 是一个两极略扁 赤道略鼓的类球体 因此向心加速度不一定都指向地心 且赤道上的向心加速度比两级大
B 这个是事实 卡文迪许也因此被称作第一个能测量地球质量的人
c 太空舱中所有物体的万有引力提供向心力 视重为0 不能用弹簧称测量 但可以拉伸弹簧称1年前查看全部
- 小学检讨原因:是因为科学老师让我们科学课去实验室,我去晚了》300~500字
 SUNSHINE111年前1
SUNSHINE111年前1 -
 lene-123 共回答了19个问题
lene-123 共回答了19个问题 |采纳率89.5%今天科学老师让我们都实验室上课,可是我没有抓紧时间,迟到了,影响了老师和其他同学的上课.这是一个错误,经过老师的批评教育,我认识到自己的错误,现在深刻检查自己的错误,希望得到老师的谅解.今后我一定遵守纪律,做到准时上课,再也不犯错误了. JIAFAI1年前查看全部
- 用同一种方砖铺地,铺一间长12米宽8米的实验室地用了600块方砖,那么铺一间长10米宽8米的教室地面,需要多
用同一种方砖铺地,铺一间长12米宽8米的实验室地用了600块方砖,那么铺一间长10米宽8米的教室地面,需要多
少块? szwpr1年前2
szwpr1年前2 -
 这个qq太寒碜 共回答了21个问题
这个qq太寒碜 共回答了21个问题 |采纳率100%12*8=96平方米
96平方米=9600分米
9600/600=16平方分米
10*8=80平方米
80平方米=8000平方分米
8000/16=500块1年前查看全部
- 实验室制取硝基苯,应选用浓硫酸,浓硝酸在55℃到60℃条件下生成.回答1.2小问
 爱娇-无尘1年前1
爱娇-无尘1年前1 -
 懂得了11 共回答了24个问题
懂得了11 共回答了24个问题 |采纳率95.8%选b 优点温度易控制1年前查看全部
- 自由落体的一个历史问题伽利略在高塔上做实验前,是否有自己已经有在塔上做过这个实验,还是只是停留在实验室阶段而大胆的猜想?
 justice_3191年前4
justice_3191年前4 -
 melyan 共回答了15个问题
melyan 共回答了15个问题 |采纳率100%都说伽利略在比萨斜塔做过一大一小重量不等两个铁球同时下落的著名实验,霍金的《时间简史》中却对这一说法提出置疑,并说伽利略并没有作过这一实验,只是作过一类似的实验既一大一小质量不等两个铁球从光滑斜面自由下滑的实验.1年前查看全部
- 实验室有100克60%的浓硫酸,求
实验室有100克60%的浓硫酸,求
实验室有100克百分之60的浓硫酸,求 1.该浓硫酸中含溶质多少克?2.把该浓硫酸稀释为百分之20,需加多少克水?
3.稀释后的浓硫酸的体积为多少?(已知百分之20的硫酸密度为:1.14克
每立方厘米)【不要抄袭】 E大有可为1年前2
E大有可为1年前2 -
 苦涩含羞 共回答了27个问题
苦涩含羞 共回答了27个问题 |采纳率81.5%1.溶质是100*60%=60g
2.设,把该浓硫酸稀释为百分之20,需加x克水
60=(100+x)*20%
x=200g
3.稀释后的浓硫酸的体积为(100+200)/1.14=263.16立方厘米1年前查看全部
大家在问
- 1这是我欠你的 英语怎么说?
- 2H400*200*10*8工字钢理论重量是多少
- 310mL浓度为0.1mol/L的NaH2PO4 和10mL浓度为0.2mol/L的Na2HPO4溶液混合,溶液pH为多少
- 4什么是仄起平收?
- 5小明从家到学校,出发时看看手表,发现如果每分钟步行80米,他将迟到5分钟,如果先步行10分钟后,再改成骑车每分钟行200
- 6我的未来只为钱英语翻译
- 7团组织生活 以“我的2012”为主题 怎样策划?
- 8动物园的海豚表演馆里,海豚正在做顶球表演,海豚的这种行为属于( ) A.先天性行为 B.学习行为 C.经验行为 D.适
- 9已知双曲线x^2/9-y^2/16=1的左、右焦点分别是F1、F2,若双曲线上存在一点P,使得|PF1|乘|PF2|=3
- 10英语演讲稿-一份特殊的礼物要求150个单词.急,
- 11核舟记中写出右边舟子的神情和动作的句子?
- 12点P在x轴的下侧,y轴的左侧,距离每个坐标轴都是3个单位长度,则点P的坐标为( )
- 13三角形abc中,AB=AC,圆O经过ABC三点且半径为4,点O到BC的距离为1,求AB长
- 14如图,A、B、C、D四点都在⊙O上,AD是⊙O的直径,且AD=6cm,若∠ABC=∠CAD,求弦AC的长.
- 15用一个字,表示下面的时间1.很长的时间( )2.很短的时间( )3.三个月的时间( )4.早上的时间( )5.黄昏的时间

