加水稀释CH3COOH,氢离子的物质的量怎么变
 一家比兴2022-10-04 11:39:543条回答
一家比兴2022-10-04 11:39:543条回答
已提交,审核后显示!提交回复
共3条回复
 幽忧悠莜 共回答了17个问题
幽忧悠莜 共回答了17个问题 |采纳率82.4%- 物质的量增加,浓度减少
- 1年前
 0iof 共回答了1147个问题
0iof 共回答了1147个问题 |采纳率- 氢离子物质的量不断增大,氢离子浓度先变大后减小。
- 1年前
 qinngqingjieoral 共回答了22个问题
qinngqingjieoral 共回答了22个问题 |采纳率86.4%- 物质的量浓度变小
- 1年前
相关推荐
- 1.体积相同,浓度均为0.2MOL/L的盐酸和醋酸溶液.分别加水稀释10倍,溶液的PH分别变成M 和N M与N关系
1.体积相同,浓度均为0.2MOL/L的盐酸和醋酸溶液.分别加水稀释10倍,溶液的PH分别变成M 和N M与N关系
2.体积相同 浓度均为0.2MOL/L的盐酸和醋酸溶液.分别加水稀释M倍 和N倍 溶液PH都变成3.M与N 关系 求详解 我比较笨
第一个是N>M 第二个是M>N ylindi1年前3
ylindi1年前3 -
 ts_hwt112 共回答了19个问题
ts_hwt112 共回答了19个问题 |采纳率84.2%M1年前查看全部
- 要用含氨0.15%的氨水对油菜进行施肥.现有含氨16%的氨水6kg,配制时需加水多少kg?
 黑帽猫1年前1
黑帽猫1年前1 -
 aw5555 共回答了24个问题
aw5555 共回答了24个问题 |采纳率83.3%6*16%/0.15%-6=6341年前查看全部
- pH=2的A、B两种酸溶液各1mL,分别加水稀释到1L(其pH与溶液体积V的关系如图所示),下列说法正确的是( )
 pH=2的A、B两种酸溶液各1mL,分别加水稀释到1L(其pH与溶液体积V的关系如图所示),下列说法正确的是( )
pH=2的A、B两种酸溶液各1mL,分别加水稀释到1L(其pH与溶液体积V的关系如图所示),下列说法正确的是( )
①a=5时,A是强酸,B是弱酸;
②若A、B都是弱酸,则5>a>2;
③稀释后,A酸溶液的酸性比B酸溶液强;
④A、B两种酸溶液的物质的量浓度一定相等.
A.①②
B.③④
C.①③
D.②④ ssamc1年前1
ssamc1年前1 -
 sadfhbsadfkj 共回答了15个问题
sadfhbsadfkj 共回答了15个问题 |采纳率100%解题思路:由图可知,稀释相同的倍数,A的变化大,则A的酸性比B的酸性强,溶液中氢离子浓度越大,酸性越强,对于一元强酸来说c(酸)=c(H+),但对于一元弱酸,c(酸)>c(H+),以此来解答.①由图可知,若a=5,A完全电离,则A是强酸,B的pH变化小,则B为弱酸,故①正确;
②若A和B都是弱酸,加水稀释时促进弱酸电离,所以溶液中pH为5>a>2,故②正确;
③由图可知,B的pH小,c(H+)大,则B酸的酸性强,故③错误;
④因A、B酸的强弱不同,一元强酸来说c(酸)=c(H+),对于一元弱酸,c(酸)>c(H+),则A、B两种酸溶液的物质的量浓度不一定相等,故④错误.
故选:A.点评:
本题考点: 弱电解质在水溶液中的电离平衡.
考点点评: 本题考查酸的稀释及图象,侧重于学生的分析能力的考查,明确强酸在稀释时pH变化程度大及酸的浓度与氢离子的浓度的关系是解答本题的关键,难度不大.1年前查看全部
- 有200克含盐率是10%的盐水,现在需要把它改制成含盐率是5%的盐水,需要加水多少克?
有200克含盐率是10%的盐水,现在需要把它改制成含盐率是5%的盐水,需要加水多少克?
如题! 婷杰1年前1
婷杰1年前1 -
 墨墨N 共回答了4个问题
墨墨N 共回答了4个问题 |采纳率100%10%5%=2
2*200=400g
400-200=200g
答:.
①
200*10%=20克
20/5%=400克
需要加水:400-200=200克
②
10%/5%=2
2*200+400
400-200=200
答:需要加水200克
③
盐:200*10%=20
然后总水量:20/(5%)=400
所以加的水量:400-200=200
④1年前查看全部
- (2010•黔东南州)如图所示,一束光线斜射入容器中,在P处形成一光斑,在向容器里逐渐加水,直到加满的过程中,光斑将(
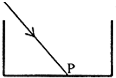 (2010•黔东南州)如图所示,一束光线斜射入容器中,在P处形成一光斑,在向容器里逐渐加水,直到加满的过程中,光斑将( )
(2010•黔东南州)如图所示,一束光线斜射入容器中,在P处形成一光斑,在向容器里逐渐加水,直到加满的过程中,光斑将( )
A.仍在原来位置
B.向右移动后静止
C.向左移动后静止
D.先向左移动再向右移动 牵着生活走1年前1
牵着生活走1年前1 -
 眼热了 共回答了16个问题
眼热了 共回答了16个问题 |采纳率81.3%1年前查看全部
- 将KClO 3 和MnO 2 的混合物15.5克,加热完全反应后,剩余固体加水溶解,过滤,洗涤不溶物,洗涤液与滤液合并,
将KClO 3 和MnO 2 的混合物15.5克,加热完全反应后,剩余固体加水溶解,过滤,洗涤不溶物,洗涤液与滤液合并,得100克溶质质量分数为7.45%的溶液,求
(1)产生O 2 的质量;
(2)原混合物中MnO 2 的质量. 余山雨夜1年前1
余山雨夜1年前1 -
 流浪乡下 共回答了20个问题
流浪乡下 共回答了20个问题 |采纳率90%设生成氧气的质量为x.
2KClO 3
Mn O 2
.
△ 2KCl+3O 2 ↑
149 96
100g×7.45% x
(1)
149
96 =
100g×7.45%
x ,x=4.8g
(2)MnO 2 的质量为:15.5g-(100g×7.45%+4.8g)=3.25g
答:(1)产生4.8g氧气;(2)二氧化锰的质量为3.25g.1年前查看全部
- 波尔多液是一种农业上常用的杀菌剂,它是由硫酸铜、石灰加水配制而成,但不能用铁制容器来配制波尔多液,原因是(用化学方程式表
波尔多液是一种农业上常用的杀菌剂,它是由硫酸铜、石灰加水配制而成,但不能用铁制容器来配制波尔多液,原因是(用化学方程式表示):______,该反应的基本反应类型是:______.
 linglingpyro1年前3
linglingpyro1年前3 -
 微风浊月 共回答了14个问题
微风浊月 共回答了14个问题 |采纳率100%解题思路:首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写;再根据反应特征确定反应类型.铁的金属活动性比铜强,能与硫酸铜溶液反应生成硫酸亚铁溶液和铜,故不能用铁制容器来配制波尔多液,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu;该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应.
故答案为:Fe+CuSO4═FeSO4+Cu;置换反应.点评:
本题考点: 书写化学方程式、文字表达式、电离方程式;反应类型的判定.
考点点评: 本题难度不大,考查学生根据反应原理书写化学方程式、判定反应类型的能力,掌握化学方程式的书写方法、四种基本反应类型的特征即可正确解答本题.1年前查看全部
- 一种农药,纯药液与水重量比是1:800,20克纯药液要加水多少克?如果加水560千克,需要多少千克纯药液?
 千年魔道1年前3
千年魔道1年前3 -
 yaoyao_04 共回答了18个问题
yaoyao_04 共回答了18个问题 |采纳率88.9%解题思路:药液和水重量的比是1:800,是一定的,知道药液的重量,求要加水多少克,知道水的重量,求需要多少千克纯药液,据此分别设出未知数,组成比例,解比例即可.(1)设需要加水x克.
1:800=20:x,
x=800×20,
x=16000,
(2)设需要用y千克药液.
1:800=y:560,
800y=560,
800y÷800=560÷800,
y=0.7.
答:20克药液要加水16000克.如果用560千克水,需要用0.7千克药液.点评:
本题考点: 比的应用.
考点点评: 解决本题要分析题干,设出未知数,组成比例解答.1年前查看全部
- 今有酒精溶液若干克,若加水10克,则酒精浓度变为25%,若在加酒精40克,浓度又变为35%.原来酒精浓度是多少
今有酒精溶液若干克,若加水10克,则酒精浓度变为25%,若在加酒精40克,浓度又变为35%.原来酒精浓度是多少
算数、方程都可以,方程的话只可以有一个未知数.方程要有两个未知数的话,六年级要看得懂.要有每一步的解释,方程要一步步下来不要只有一个开始一个结束.
要求比较多啊, kqnybas1年前3
kqnybas1年前3 -
 妖蕊 共回答了19个问题
妖蕊 共回答了19个问题 |采纳率84.2%利用一元二次方程组来求解.
设原酒精溶液z克,含酒精x克.
则原来酒精浓度为:x/z *100%
由题意,可列出以下方程:
(1)x/(z+10)=25%
(2)(x+40)/(z+40)=35%
由(1)得:z=4x-10
代入(2)中求解得:x=73.75
则z=4x-10=285
所以,原来酒精浓度为:
x/z *100%=73.75/285 *100%=25.88%1年前查看全部
- 为了配制实验用的680克5%的过氧化氢溶液,需要20%的双氧水多少克?加水多少ml?
 lanmda1年前1
lanmda1年前1 -
 xc0629 共回答了18个问题
xc0629 共回答了18个问题 |采纳率88.9%m=680*5%/20%=170g
V=680-170=510mL1年前查看全部
- .33.2g KClO3和MnO2的混合物,加热一段时间后,质量变为28.4g.冷却后加水搅拌,溶解完全后过滤,在滤液中
.33.2g KClO3和MnO2的混合物,加热一段时间后,质量变为28.4g.冷却后加水搅拌,溶解完全后过滤,在滤液中加硝酸银.滤纸上的不溶物与足量的浓盐酸反应,可生成0.1molCl2,求:
(1)KClO3的分解百分率.
(2)可生成AgCl沉淀的质量. zhutianren1年前1
zhutianren1年前1 -
 gujienanhai88 共回答了14个问题
gujienanhai88 共回答了14个问题 |采纳率78.6%(2) 氯酸钾分2KClO3=(Δ/MnO2)=2KCl+3O2↑
Δm=m(O2)=33.2-28.4=4.8g 则n(O2)=0.15mol 推得n(KCl)=0.15×2/3=0.1mol
加水后,滤液中溶解有生成的KCl,则生成AgCl沉淀物质的量与KCl相同.
n(AgCl)=0.1mol m(AgCl)=14.35g
(1) 2步骤中先加水滤出的沉淀是MnO2,方程式:MnO2+4HCl(浓)=(加热)=MnCl2+Cl2↑+2H2O
生成n(Cl2)=0.1mol,则n(MnO2)=0.1mol 推得m(MnO2)=8.7g
原混合物质量为33.2g,分解后剩余28.4g,
则总m(KClO3)=33.2-8.7g=24.5g,
分解的m(KClO3)=0.1×122.5=12.25g
则分解率(用质量算)=12.25/24.5=50%1年前查看全部
- 有酒精含量为36%的酒精溶液若干,加了一定数量的水后稀释成酒精含量为30%的溶液.如果再稀释到24%,那么还需要加水的数
有酒精含量为36%的酒精溶液若干,加了一定数量的水后稀释成酒精含量为30%的溶液.如果再稀释到24%,那么还需要加水的数量是上次加的水的几倍?
 用烈火点只烟1年前1
用烈火点只烟1年前1 -
 楼下的是tttt 共回答了15个问题
楼下的是tttt 共回答了15个问题 |采纳率86.7%解题思路:假设36%的酒精溶液100克,那么含酒精100×36%=36克,是不变的;30%的浓度的酒精溶液是 36÷30%=120克,比100克多了20克水;24%的浓度的盐水是 36÷24%=150克,比100克多了50克水;第一次加了20克,第2次又加了50-20=30克,进而得出结论.假设36%的酒精溶液100克,那么含酒精100×36%=36(克);
36÷30%-100=20(克);
(36÷24%-100-20)÷20,
=30÷20,
=1.5倍;
答:还需要加水的数量是上次加的水的1.5倍.点评:
本题考点: 浓度问题.
考点点评: 解答此题的关键是抓住不变量,然后根据“对应量÷对应分率=单位“1”的量,进行解答即可.1年前查看全部
- 一定温度下,冰醋酸加水稀释过程中溶液的导电能力变化曲线如图所示,请回答:
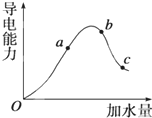 一定温度下,冰醋酸加水稀释过程中溶液的导电能力变化曲线如图所示,请回答:
一定温度下,冰醋酸加水稀释过程中溶液的导电能力变化曲线如图所示,请回答:
(1)O点为什么不导电______.
(2)a、b、c三点的pH由小到大的顺序是______.
(3)H+的物质的量最大的是______(填“a”、“b”或“c”).
(4)若使c点溶液中的c(CH3COO-)增大,可以采取下列措施中的______(填序号).
A.加热B.加很稀的NaOH溶液 C.加NaOH固体 D.加水E.加固体CH3COONa F.加入锌粒. 过去就让它过去1年前1
过去就让它过去1年前1 -
 大鱼头 共回答了22个问题
大鱼头 共回答了22个问题 |采纳率77.3%解题思路:(1)溶液的导电性与离子浓度有关,离子浓度越大,导电性越强;
(2)导电能力越强,离子浓度越大,氢离子浓度越大,pH越小;
(3)溶液越稀,越促进醋酸电离,则溶液中氢离子的物质的量越大;
(4)要使醋酸根离子浓度增大,可以采用加热、加入含有醋酸根离子的物质、加入和氢离子反应的物质.(1)溶液的导电性与离子浓度有关,离子浓度越大,导电性越强,冰醋酸中没有自由移动的离子,所以冰醋酸不导电,故答案为:无自由移动的离子;
(2)导电能力越强,离子浓度越大,氢离子浓度越大,pH越小,则a、b、c三点溶液的pH为b<a<c,故答案为:b<a<c;
(3)溶液越稀,越促进醋酸电离,则溶液中氢离子的物质的量越大,所以氢离子物质的量最大的是c,故选C;
(4)要使醋酸根离子浓度增大,可以采用加热、加入含有醋酸根离子的物质、加入和氢离子反应的物质,
A.加热促进醋酸电离,则溶液中醋酸根离子浓度增大,故正确;
B.加很稀的NaOH溶液,促进醋酸电离,但溶液的体积增大,导致醋酸根离子浓度减小,故错误;
C.加NaOH固体,氢氧化钠和氢离子反应促进醋酸电离,所以醋酸根离子浓度增大,故正确;
D.加水稀释能促进醋酸电离,但醋酸根离子浓度减小,故错误;
E.加固体CH3COONa,能抑制醋酸电离,但醋酸钠电离出的醋酸根离子大于抑制醋酸电离出的醋酸根离子,所以醋酸根离子浓度增大,故正确;
F.加入锌粒,和氢离子反应,促进醋酸电离,所以醋酸根离子浓度增大,故正确;
故选ACEF.点评:
本题考点: 弱电解质在水溶液中的电离平衡.
考点点评: 本题考查电解质的电离,题目难度中等,易错选项是D,加水稀释醋酸,能促进醋酸电离,但溶液中醋酸根离子增大的量远远小于水体积增大的量,所以醋酸根离子浓度减小,为易错点.1年前查看全部
- 碱性的液体加水稀释可以降低PH值吗?
碱性的液体加水稀释可以降低PH值吗?
现在的液体是PH9 , 加水以后可以降低PH值吗?
我问你问题, 你还让我先搞清楚什么PH值的概念, 你会就说,不会别来墨迹, 我要是了解 还来这里询问啊 ?
所答非所问@
你看看FYC1188的回答, 多好。感谢fyc1188 sam12345671年前1
sam12345671年前1 -
 aeiou66 共回答了22个问题
aeiou66 共回答了22个问题 |采纳率86.4%可以的.
碱溶液我就以氢氧化钠溶液为例吧,原来的溶液中有钠离子,氢氧根离子(包括氢氧化钠电离的与水电离的)以及氢离子(水电离的),加水稀释后,由于氢氧根离子增加不如溶液体积增加得多,所以氢氧根离子浓度下降,此时水电离平衡的方程式向生成氢氧根离子与氢离子的方向移动,但根据勒夏特列原理,移动只能减弱而不能抵消变化,所以尽管水电离平衡的方程式向生成氢氧根离子与氢离子的方向移动,但是溶液中氢氧根离子浓度依然比之前的低.对氢离子而言,情况是不同的,因为原来的溶液中氢离子浓度比加入的水的氢离子浓度低,(因为原来的溶液中有来自氢氧化钠电离的大量的氢氧根离子,致使水电离平衡向生成水的方向移动,氢离子浓度比纯水中氢离子浓度要低),加入水后,溶液中氢离子浓度上升(此过程包含了水电离建立新平衡过程),溶液PH取决于溶液中氢离子浓度,氢离子浓度上升,酸性增强(这里是碱性减弱),PH下降.1年前查看全部
- 将60kg20%的浓氨水稀释成农业施肥用的0.3%稀氨水,应加水多少千克?
将60kg20%的浓氨水稀释成农业施肥用的0.3%稀氨水,应加水多少千克?
要详细过程
要用设x求!
我很菜,高手详细点教啊!
 yygywc1年前1
yygywc1年前1 -
 卡卡也爱打炮 共回答了20个问题
卡卡也爱打炮 共回答了20个问题 |采纳率90%设加水X千克
60*20%/(60+X)*100%=0.3%
解X=3940千克1年前查看全部
- 1种70%的农药,如稀释到1.75%治虫最有效,用多少千克浓度为35%的加水多少千克才能配成1.75%的农药800千克
 1819236961年前1
1819236961年前1 -
 夏日玉米 共回答了15个问题
夏日玉米 共回答了15个问题 |采纳率93.3%(1.75-0):(35-1.75)=1:19
需要35%农药:800÷(1+19)×1=40千克
加水:800-40=760千克1年前查看全部
- AL和什么单质反应生成的化合物加水会生成氨气和沉淀
 宝宝蛇1年前3
宝宝蛇1年前3 -
 温闲 共回答了13个问题
温闲 共回答了13个问题 |采纳率84.6%Al 和 N2 反应生成的化合物加水会生成氨气和沉淀.
Al 和 N2生成的化合物是AlN
方程式:AlN + 3H2O == Al(OH)3↓+ NH3↑
双水解反应.1年前查看全部
- 向饱和BaSO4溶液中加水溶液度为什么不变?加水不是朝着溶解方向移动吗?
向饱和BaSO4溶液中加水溶液度为什么不变?加水不是朝着溶解方向移动吗?
是溶解度为什么不变 题目上打错了 TheEnd_xx1年前1
TheEnd_xx1年前1 -
 客家流云 共回答了18个问题
客家流云 共回答了18个问题 |采纳率83.3%不可能不变的 除非交代你了溶液中有BaSO4沉淀,加水的确是朝着溶解方向移动,但水多了,沉淀溶解的也多了,加多少水就多溶解多少BaSO4,此温度下Ksp是一定的,所以溶液浓度不变
溶解度就更好说了,溶解度指的是100g水溶解溶质的质量,只和温度有关1年前查看全部
- 将KClO 3 和MnO 2 的混合物15.5克,加热完全反应后,剩余固体加水溶解,过滤,洗涤不溶物,洗涤液与滤液合并,
将KClO 3 和MnO 2 的混合物15.5克,加热完全反应后,剩余固体加水溶解,过滤,洗涤不溶物,洗涤液与滤液合并,得100克溶质质量分数为7.45%的溶液,
求:
(1)产生O 2 的质量;
(2)原混合物中MnO 2 的质量。 swq5021年前0
swq5021年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 0.1mol/L的CH3COOH加水稀释,溶液中氢氧根粒子浓度变大.
0.1mol/L的CH3COOH加水稀释,溶液中氢氧根粒子浓度变大.
我知道正确的思路是 稀释促进水解 氢离子量变多 但浓度却因加水而变低,所以……
但我始终还有个想法 没绕过湾 觉得因为加水所以氢氧根粒子也应浓度降低 ,能不能帮我消除下误区 潇湘醉影1年前2
潇湘醉影1年前2 -
 f6bsn 共回答了19个问题
f6bsn 共回答了19个问题 |采纳率94.7%加水稀释,虽然电离总量增加,但氢离子浓度减小,氢氧根粒子浓度变大
氢氧根粒子来源于水的电离,水的电离虽氢离子浓度减小而增大,要保持平衡常数不变,浓度也要变大,因为平衡常数是以浓度计算的1年前查看全部
- 说明原因在铁粉和氧化铜粉的混合物中,加水一定质量的稀硫酸,充分反应后过滤,在滤渣中加入稀盐酸有气泡产生,下列说法正确的是
说明原因
在铁粉和氧化铜粉的混合物中,加水一定质量的稀硫酸,充分反应后过滤,在滤渣中加入稀盐酸有气泡产生,下列说法正确的是 ( ) A 滤渣中一定有Fe,可能含有Cu B 滤渣中一定含有Fe和Cu yzw19831年前1
yzw19831年前1 -
 未来的爱好 共回答了20个问题
未来的爱好 共回答了20个问题 |采纳率95%B 滤渣中一定含有Fe和Cu
氧化铜先与稀硫酸反应 CuO+H2SO4==CuSO4+H2O
铁再置换铜 Fe+CuSO4==FeSO4+Cu
最后铁再置换氢 Fe + H2SO4 === FeSO4 + H2↑
在滤渣中加入稀盐酸有气泡产生,说明滤渣中有铁,铜与盐酸不反应
所以 滤渣中一定含有Fe和Cu1年前查看全部
- 苯加甲醇是生成甲苯加水,还是苯酚加甲烷?反应条件是什么?
 lwx200520061年前1
lwx200520061年前1 -
 犹豫当中 共回答了24个问题
犹豫当中 共回答了24个问题 |采纳率91.7%在AlCl3催化下,苯也可以和醇反应,苯环上的氢原子被烷基取代生成烷基苯1年前查看全部
- 现有40千克浓度为15%的盐水,现在要使盐水的浓度达到10%,需要加水多少千克?
现有40千克浓度为15%的盐水,现在要使盐水的浓度达到10%,需要加水多少千克?
不要方程,要算式 yaozongfa1年前1
yaozongfa1年前1 -
 vivi_洁 共回答了14个问题
vivi_洁 共回答了14个问题 |采纳率92.9%40×15%÷10%-40=20(千克)1年前查看全部
- 常温下把4种不同体积不同浓度的醋酸溶液分别加入4个盛有10mL2mol/L氢氧化钠溶液中并加水稀释到100ml
常温下把4种不同体积不同浓度的醋酸溶液分别加入4个盛有10mL2mol/L氢氧化钠溶液中并加水稀释到100ml
其中反应速率最大的是 A.20mL,3 mol·L-1 B.25mL,2 mol·L-1
C.10mL,3 mol·L-1 D.18mL,4 mol·L-1 winging1231年前1
winging1231年前1 -
 洪都拉斯小猪 共回答了15个问题
洪都拉斯小猪 共回答了15个问题 |采纳率86.7%常温下把4种不同体积不同浓度的醋酸溶液分别加入4个盛有10mL2mol/L氢氧化钠溶液中并加水稀释到100ml
D.18mL,4 mol·L-1中所含醋酸最多 所以加水稀释到100ml浓度最大,速率最快1年前查看全部
- 将0.l mol• 醋酸溶液加水稀释,下列说法正确的是 A.溶液中c(H+)和c( )都减小 B.溶液中c(
将0.l mol• 醋酸溶液加水稀释,下列说法正确的是 A.溶液中c(H+)和c( )都减小 B.溶液中c(H+)
将0.l mol• 醋酸溶液加水稀释,下列说法正确的是
A.溶液中c(H+)和c( )都减小 B.溶液中c(H+)增大
C.醋酸电离平衡向左移动 D.溶液的pH增大
求D的详细解答 香皂泡泡1年前2
香皂泡泡1年前2 -
 天蝎座1106 共回答了14个问题
天蝎座1106 共回答了14个问题 |采纳率85.7%加入水,CH3COOH溶液电离程度增大
因为加水稀释体积扩大,微粒总浓度减小,平衡为抑制减小,要向生成更多微粒方向移动,也就是正向移动,从而促进电离.越稀越电离.
但因为体积扩大占优势,所以氢离子浓度还减小,氢氧根浓度增加.(因为离子积常数不变)
所以选D
其实换个想法,联系实际,醋是越稀释,越不酸(pH增大).
4465864452011-11-27 16:49
氢离子不是变多了嘛?为什么氢离子浓度还减小?不懂啊.T T回复
张家琛wd2011-11-27 16:54
回复 446586445:氢离子数量/变多没错,但是体积也是变大.体积变大比氢离子变多要快,氢离子浓度=氢离子数量/体积,综合一下,氢离子浓度反而变小了.回复
如果有疑问最好追问,如果评论有时候会注意不到的.1年前查看全部
- 把浓度为95%的酒精150千克稀释为75%的酒精,需加水______千克.
 暗地的鱼1年前1
暗地的鱼1年前1 -
 skjcmz 共回答了27个问题
skjcmz 共回答了27个问题 |采纳率100%解题思路:根据题意,把浓度为95%的酒精150千克稀释为75%的酒精,酒精的质量不变,根据一个数乘百分数的意义,用乘法求出酒精的质量,再根据已知一个数的百分之几是多少,求这个数,用除法求出稀释后的酒精溶液的质量,减去150千克就是需要加水的数量.由此列式解答.150×95%÷75%-150
=142.5÷0.75-150
=190-150
=40(千克);
答:需加水40千克.
故答案为:40.点评:
本题考点: 百分数的实际应用.
考点点评: 此题属于百分数乘法、除法应用题的综合应用,根据一个数乘百分数的意义和已知一个数的百分之几是多少,求这个数,列式解答即可.1年前查看全部
- 用含氨25分之3的氨水进行有才追肥.现有含氨20分之4的氨水30千克,配制时需加水多
 zzg20081年前1
zzg20081年前1 -
 hellen78118 共回答了16个问题
hellen78118 共回答了16个问题 |采纳率93.8%(4/20)×30=(3/25)×(30 +x)
解得X=20Kg
所以,需加20Kg水.1年前查看全部
- 测定空气中氧气含量的实验中分析产生该实验现象的原因 实验的注意事项 加水的作用
测定空气中氧气含量的实验中分析产生该实验现象的原因 实验的注意事项 加水的作用
实验的注意事项?加水的作用?如果进入的水多于1/5,可能的原因有? 假老练1年前1
假老练1年前1 -
 3wdiancom 共回答了19个问题
3wdiancom 共回答了19个问题 |采纳率89.5%用红磷
检验气密性
吸收五氧化二磷
红磷燃烧后没有立即盖紧塞子
没等冷却就打开止水夹1年前查看全部
- 有一公斤95%的酒精,要配制成75%的酒精需加水多少克,按重量算
 骑单车送煤气1年前3
骑单车送煤气1年前3 -
 bobotata 共回答了20个问题
bobotata 共回答了20个问题 |采纳率90%W=1*95%/75%=1.27kg
加水0.27kg1年前查看全部
- 将30mL 0.5mol/L NaOH 溶液加水稀释到500mL,稀释后溶液中NaOH的物
将30mL 0.5mol/L NaOH 溶液加水稀释到500mL,稀释后溶液中NaOH的物质的量浓度为( )
A. 0.3 mol/L
B. 0.03 mol/L
C. 0.05 mol/L
D. 0.04 mol/L 形制开古迹1年前2
形制开古迹1年前2 -
 雨中蝶儿纷飞 共回答了17个问题
雨中蝶儿纷飞 共回答了17个问题 |采纳率88.2%解题思路:根据稀释定律可知,溶液稀释前后溶质的物质的量不变,据此计算.令稀释后溶液中NaOH的物质量浓度为c,则:
30×10-3L×0.5mol/L=500×10-3L×c
解得c=0.03mol/L.
故选:B.点评:
本题考点: 物质的量浓度的相关计算.
考点点评: 本题考查物质的量浓度有关计算,难度较小,关键清楚稀释定律,溶液稀释前后溶质的物质的量不变.1年前查看全部
- A,B两种盐加水溶解,生成K2SO4和CuCO3,则A,B为?
A,B两种盐加水溶解,生成K2SO4和CuCO3,则A,B为?
RT,是K2SO4和CuCO3,还是K2CO3和CuSO4,还是均可? 老板下碗面1年前2
老板下碗面1年前2 -
 swwgg 共回答了14个问题
swwgg 共回答了14个问题 |采纳率92.9%是K2CO3和CuSO4
因为CuCO3不溶于水,所以不可能是K2SO4和CuCO3
K2CO3和CuSO4加水溶解后反应生成K2SO4和CuCO3
K2CO3+CuSO4==CuCO3↓+K2SO41年前查看全部
- 把100毫升98%的浓硫酸稀释成10%的稀硫酸,需要加水多少毫升?
把100毫升98%的浓硫酸稀释成10%的稀硫酸,需要加水多少毫升?
98%的浓硫酸的密度为1.84克每立方厘米
10%的稀硫酸的密度为1.07克每立方厘米 farmerdavid1年前1
farmerdavid1年前1 -
 liyouting1 共回答了19个问题
liyouting1 共回答了19个问题 |采纳率73.7%100*1.84*98%=w*10%
m=w-100*1.841年前查看全部
- 化学题(看补充)(1)体积相同,ph=2的盐酸和CH3COOH溶液,分别加水稀释m倍,n倍,溶液的ph变成4,m与n关系
化学题(看补充)
(1)体积相同,ph=2的盐酸和CH3COOH溶液,分别加水稀释m倍,n倍,溶液的ph变成4,m与n关系为?
(2)ph=12氨水与naoh加水稀释m倍,n倍 溶液ph变为9,m与n关系为 meihuayiju1年前1
meihuayiju1年前1 -
 白玉为堂金做马 共回答了20个问题
白玉为堂金做马 共回答了20个问题 |采纳率100%(1)M小于N.因为CH3COOH是弱电解质.
(2)M大于N.因为氨水是弱电解质.
弱电解质不完全电离,但越稀释越电离.1年前查看全部
- 医院实验室配制一种药水,药粉与水的比是3:200,0.3千克这种药粉需要加水多少千克?
医院实验室配制一种药水,药粉与水的比是3:200,0.3千克这种药粉需要加水多少千克?
要详细的解题思路 sunqianya1年前1
sunqianya1年前1 -
 晨起沙砾 共回答了16个问题
晨起沙砾 共回答了16个问题 |采纳率75%设需要加水x千克.
3:200=0.3:x
x =20
答:0.3千克这种药粉需要加水20千克.1年前查看全部
- 配制0.184mol/L的硫酸时,向1000ml容量瓶中注入10ml18.4mol/LH2SO4,不断振荡,加水至刻度.
配制0.184mol/L的硫酸时,向1000ml容量瓶中注入10ml18.4mol/LH2SO4,不断振荡,加水至刻度.为什么不对?
 业务流程1年前2
业务流程1年前2 -
 tvrynifqp 共回答了12个问题
tvrynifqp 共回答了12个问题 |采纳率75%因为容量瓶是有温度限制的,而浓硫酸稀释时会大量放热,使得容量瓶受热膨胀,导致刻度不准确,因此不能直接在容量瓶里稀释定容,而应该先用蒸馏水在烧杯中稀释浓硫酸后再加入容量瓶定容.1年前查看全部
- ( Na2CO3溶液加水稀释后,恢复至原温度,pH和Kw均减小 为啥错?
 11fg1年前3
11fg1年前3 -
 wlawyer7610 共回答了15个问题
wlawyer7610 共回答了15个问题 |采纳率86.7%Kw只与温度有关,是关于温度的函数,温度不变,Kw不变.加水稀释,用极限思想最好理无限稀释Na2CO3溶液后,溶液由碱性无限接近中性,故PH减小.1年前查看全部
- 取样,加水溶解,溶液蓝色的是CuSO4.在溶液中,滴加无色酚酞试液,变红色的是NaOH.
取样,加水溶解,溶液蓝色的是CuSO4.在溶液中,滴加无色酚酞试液,变红色的是NaOH.
在溶液中再滴加AgNO3溶液,产生白色沉淀的是NaCl.
无现象的是KNO3
写出这个过程中所发生反应的化学方程式 comicon1年前1
comicon1年前1 -
 魑魅魍魉1999 共回答了21个问题
魑魅魍魉1999 共回答了21个问题 |采纳率85.7%AgNO3 HCl=AgCl(沉淀,标下箭头) HNO31年前查看全部
- 工人师傅用98%的浓硫酸,稀释成500g19.6%的稀硫酸除铁锈问需要98%的浓硫酸多少毫升,加水多少毫升
 hank00720071年前1
hank00720071年前1 -
 fei8531953 共回答了14个问题
fei8531953 共回答了14个问题 |采纳率78.6%500*19.6%=98g
98/98%=100g 98%的硫酸98%硫酸的密度是1.84
100g/1.84=54.3ml 98%的硫酸
需要加水500-54.3=445.7ML水1年前查看全部
- 有浓度为30%的糖水40千克,要得到浓度为10%的糖水,需要加水多少千克
 tae812bip0b3b1年前1
tae812bip0b3b1年前1 -
 112334 共回答了28个问题
112334 共回答了28个问题 |采纳率85.7%设需要加水x千克,由题意知
30%×40=(40+x)·10%
x=801年前查看全部
- 氢硫酸加水稀释的化学式
 樱桃小小酥1年前2
樱桃小小酥1年前2 -
 1894年在tt英女 共回答了10个问题
1894年在tt英女 共回答了10个问题 |采纳率80%H2S+3H2O=H2SO3+3H21年前查看全部
- 求 胆矾加水 的反应化学式水(H2O) 加上 胆矾(CuSo4.5H2O)
 3745031年前6
3745031年前6 -
 adan_huhu 共回答了12个问题
adan_huhu 共回答了12个问题 |采纳率75%胆矾加水是溶解,是物理变化
如果你想问,硫酸铜与水的反应,则为 CuSO4+5H2O=CuSO4.5H2O1年前查看全部
- 解释以下现象:未洗涤烧杯和玻璃棒2次~3次.(mB偏小,cB偏低)在定容时加水超过刻度线,再用胶头滴管吸出多余部分。(V
解释以下现象:
未洗涤烧杯和玻璃棒2次~3次.(mB偏小,cB偏低)在定容时加水超过刻度线,再用胶头滴管吸出
多余部分。(V偏大,cB偏低) mfxs0071年前3
mfxs0071年前3 -
 lili8502 共回答了16个问题
lili8502 共回答了16个问题 |采纳率87.5%未洗涤烧杯、玻棒的上面残留有溶质,所以溶质质量偏小,浓度偏低.
定容时超过刻度线的那部分溶液中也含有溶质,吸出后溶质浓度偏低,V偏大.1年前查看全部
- 农药“乐果”乳剂加水可治棉花虫害,已知药液和水的重量比是1:1000.
农药“乐果”乳剂加水可治棉花虫害,已知药液和水的重量比是1:1000.
1.·4克药液要加水多少千克?
2·如果要配置5005千克药水和水各多少千克? 逝去Les1年前2
逝去Les1年前2 -
 过山车W 共回答了12个问题
过山车W 共回答了12个问题 |采纳率100%1.
4克药液要加 4千克水(就是4公斤)
2.5005/(1+1000)=5
药5千克,水5000千克1年前查看全部
- 农药“20%乐果”乳液加水可活棉花红蜘蛛害虫,要喝水的重量比是1:1000 .100克药液要加水多少千克
农药“20%乐果”乳液加水可活棉花红蜘蛛害虫,要喝水的重量比是1:1000 .100克药液要加水多少千克
(2)如果用3000千克水,要用多少药液?
(3)如果要配制5005千克药水需要药液和水各多少千克? dd郑1年前1
dd郑1年前1 -
 内心就是kk 共回答了12个问题
内心就是kk 共回答了12个问题 |采纳率100%1.加水100*1000/1000=100千克
2.3000/1000=3千克药液
3.需要药液5005*1/(1000+1)=5千克
需要水5005-5=5000千克1年前查看全部
- 农药“20%乐果”乳液加水可防治果树害虫,药液和水的重量比是1:800.如果用水250千克,要加多少克药液?
 wensong551年前1
wensong551年前1 -
 xuehaowu 共回答了18个问题
xuehaowu 共回答了18个问题 |采纳率88.9%药液质量为250/800=0.3125kg=312.5g1年前查看全部
- 有盐水750千克,含盐20%,加了一些水后含盐8%,加水多少千克?
 _左岸_1年前1
_左岸_1年前1 -
 h0elp 共回答了22个问题
h0elp 共回答了22个问题 |采纳率90.9%解题思路:根据加水前后,盐水的含盐量不变,求出750千克浓度为20%的盐水含盐量750×20%=150千克,设加入x千克水,数量间的相等关系为(750+x)×8%=750×20%,据此解答即可.解;设加入x千克水,
(750+x)×8%=750×20%
60+0.08x=150,
60+0.08x-60=150-60,
0.08x=90,
0.08x÷0.08=90÷0.08,
x=1125.
答:应加入1125千克水.点评:
本题考点: 浓度问题.
考点点评: 此题考查百分率的应用题,解决此题的关键是,加水前后盐的数量不变.1年前查看全部
- 向氯化氨溶液中加水,水的电离是促进还是抑制?为什么?
向氯化氨溶液中加水,水的电离是促进还是抑制?为什么?
其他方法有什么 kofer20031年前1
kofer20031年前1 -
 xmkj521 共回答了16个问题
xmkj521 共回答了16个问题 |采纳率100%最简单的方法是极限法去考虑,无限稀释时,就相当于纯水的电离.
而氯化铵溶液水解显酸性,促进了水的电离,也就大于纯水.
所以水的电离被抑制~
也可以用别的方法想,但都没有这个简单~
纯手打~希望能帮到您~有不懂的欢迎追问~望采纳^_^1年前查看全部
- 向10.6克可能含有碳酸钠、硝酸钠、硝酸钡的样品加水,全部溶解
向10.6克可能含有碳酸钠、硝酸钠、硝酸钡的样品加水,全部溶解
再将溶液加入过量氯化钙溶液有10克沉淀 判断样品组成 qq的人是不是我1年前2
qq的人是不是我1年前2 -
 Ж阿哟 共回答了15个问题
Ж阿哟 共回答了15个问题 |采纳率93.3%10克沉淀必定全为碳酸钙,故其物质的量为0.1mol,
由碳酸根守恒,知
碳酸钠的物质的量为0.1mol,
所以碳酸钠的质量为106*0.1=10.6g
故样品全为碳酸钠.
打这么多字不容易,1年前查看全部
- 有含盐30%的盐水100克,要使它含盐25%,应加水多少克
 qinshuyun20061年前4
qinshuyun20061年前4 -
 一滴水的阳光 共回答了20个问题
一滴水的阳光 共回答了20个问题 |采纳率90%盐一共100×30%=30克
所以现在盐水是30÷25%=120克
所以加水120-100=20克1年前查看全部
大家在问
- 1一辆汽车从甲城开往乙城,6小时到达.返回时加快了速度,每小时比原来多行8千米,结果只用了5小时.求甲城到乙城的路程有多少
- 2刘姥姥二进大观园 刘姥姥的人物形象和个性特点是什么?
- 3某化学兴趣小组根据下图所示装置进行实验室制取气体的探究
- 4"正确透彻的见解"可以改成什么成语?
- 5选出下列加点字的注音有误的一项( )。(3分) A. 行 伍(háng) 跬 步(kuǐ)
- 6英语翻译低垂的柳枝丢失了找寻你的地址,放飞的蝴蝶带走了对你的思念,掉落的残叶写满了想对你的好,冰冷的枯枝见证了没有你后的
- 7交错级数收敛性和-1指数的关系(-1)^(n+1)和(-1)^n有区别吗?例如(-1)^n ln(1+1/n)和(-1)
- 8三个小朋友在玩跳皮筋,你认为用“石头、剪刀、布 ”决定谁先跳公平吗?
- 9九宫格横竖斜三个数相加都等于10
- 10旋转对称2、钟表的分针从5分钟走到25分钟,分针旋转了 度.3、关于中心对称的两个图形,对应线段的关系是 .对应角 .4
- 11他今晚请我们吃饭英文该怎么说?我用过:He treat us a diner tonight.老外还是不太懂,于是我换成
- 12麻烦老师解答:甲用50牛水平力推动一
- 13英语阅读题lily is american she is twelve she is a middle school s
- 14硝酸银和铜反应方程式
- 15英语关于部分否定与全部否定的语法区别