(2011•沙洋县模拟)连二亚硫酸钠(Na2S2O4),是重要化工原料,该物质在潮湿空气中极不稳定,易分解并引起燃烧,反
 huamei112022-10-04 11:39:541条回答
huamei112022-10-04 11:39:541条回答A.该反应属于分解反应
B.X的化学式为SO2
C.Na2S2O3中S的化合价为+3价
D.Na2S2O4通常要在干燥阴凉处密闭贮存

已提交,审核后显示!提交回复
共1条回复
 lkdsjfoi 共回答了18个问题
lkdsjfoi 共回答了18个问题 |采纳率100%- 解题思路:A、根据分解反应的概念和特征分析;
B、根据质量守恒定律的微观解释:化学反应前后原子的种类和数目不变.可知在化学反应方程式中,反应物和生成物中所含的原子的种类和数目相同.由此可推断化学反应方程式中反应物或生成物的化学式;
C、根据化合物中正负化合价的代数和为零分析;
D、根据Na2S2O4的性质分析判断.A、分解反应,是化学反应的常见类型之一,是化合反应的逆反应.它是指一种化合物在特定条件下(如加热、通直流电、催化剂等)分解成二种或二种以上较简单的单质或化合物的反应,故A说法正确;
B、根据质量守恒定律和化学方程式可得,X的化学式含有Na的个数为:2×2-(2+2)=0,含有S的个数为:2×2-(2+1)=1,含有O的个数为:2×4-(3+3)=2;故可判断X的化学式为:SO2,故B说法正确;
C、因为Na是+1价,O是-2价,则Na2S2O3中S的化合价为+2价,故C说法不正确;
D、由已知条件可知,该物质在潮湿空气中极不稳定,易分解并引起燃烧.故通常要在干燥阴凉处密闭贮存,故D说法正确.
故选:C.点评:
本题考点: 有关化学式的计算和推断;有关元素化合价的计算;分解反应及其应用;质量守恒定律及其应用.
考点点评: 本题主要考查学生对分解反应的概念的掌握,根据质量守恒定律推断化学式的能力,以及根据化合价的规律和原则推断元素的化合价的能力. - 1年前
相关推荐
- (2010•沙洋县模拟)下列各组物质的区分方法中,不可行的是( )
(2010•沙洋县模拟)下列各组物质的区分方法中,不可行的是( )
A.硬水、软水--加肥皂水,振荡,观察泡沫的多少
B.氮气、二氧化碳--用燃着的木条检验,观察燃烧的现象
C.铁粉、氧化铜粉末--加稀盐酸,观察有无气泡产生
D.氯化钾、氯化铵--加熟石灰研磨,闻气味 云麓子随1年前1
云麓子随1年前1 -
 诸葛亮亲自打蚊子 共回答了12个问题
诸葛亮亲自打蚊子 共回答了12个问题 |采纳率83.3%解题思路:A、根据硬水与软水的鉴别方法来考虑;
B、根据氮气和二氧化碳的性质的相似之处与不同之处考虑;
C、根据铁粉、氧化铜与盐酸反应现象的不同来鉴别;
D、根据铵态氮肥的特点考虑鉴别方法.A、硬水与软水的鉴别方法是加肥皂水,振荡,观察泡沫的多少,泡沫多的是软水,泡沫少的是硬水,故A正确;
B、氮气和二氧化碳都不支持燃烧,都能使燃着的木条熄灭,不能用燃着的木条检验,故B错误;
C、铁粉能与盐酸反应生成氢气、氧化铜粉末与盐酸反应生成氯化铜和水,所以--加稀盐酸,观察有无气泡产生,可监别开两种物质,故C正确;
D、铵态氮肥与熟石灰反应能生成有刺激性气味的氨气,所以加熟石灰研磨,闻气味可鉴别开氯化钾和氯化铵.故D正确.
故选B.点评:
本题考点: 硬水与软水;常见气体的检验与除杂方法;金属的化学性质;铵态氮肥的检验.
考点点评: 通过回答本题知道了鉴别硬水和软水的方法是用肥皂水,鉴别两种试剂的基本思路是加入一种物质使其呈现的现象不同.1年前查看全部
- (2010•沙洋县模拟)取一定质量的某纯净的碳酸钠样品放入烧杯中,加入95.8g水充分溶解,再向其中加入稀硫酸,反应放出
 (2010•沙洋县模拟)取一定质量的某纯净的碳酸钠样品放入烧杯中,加入95.8g水充分溶解,再向其中加入稀硫酸,反应放出气体的总质量与所加入稀硫酸的质量关系曲线如下图所示,请根据题意解答问题:
(2010•沙洋县模拟)取一定质量的某纯净的碳酸钠样品放入烧杯中,加入95.8g水充分溶解,再向其中加入稀硫酸,反应放出气体的总质量与所加入稀硫酸的质量关系曲线如下图所示,请根据题意解答问题:
(1)当加入98g稀硫酸时,放出气体的质量为______g.
(2)计算所加入的稀硫酸的溶质质量分数为______,若配制100g这种稀硫酸需20%的硫酸溶液______g.
(3)试通过计算求出加入98g稀硫酸(即A点)时烧杯中溶液溶质的质量分数.(写出计算过程) _心似琉璃_1年前1
_心似琉璃_1年前1 -
 xupingan2000 共回答了18个问题
xupingan2000 共回答了18个问题 |采纳率94.4%解题思路:(1)根据图示数据,找出与纵坐标98对应的横坐标的数值;
(2)利用碳酸钠与硫酸反应的化学方程式和生成二氧化碳的质量,列出比例式,就可计算出完全反应时参与反应的H2SO4质量;然后根据溶质质量分数公式即可求出所加入的稀硫酸的溶质质量分数;根据“100g×所加入的稀硫酸的溶质质量分数÷20%”健康计算出配制100g这种稀硫酸需20%的硫酸溶液的质量;
(3)完全反应后(即A点),溶液中的溶质为Na2SO4.利用碳酸钠与硫酸反应的化学方程式可计算出反应生成Na2SO4的质量和Na2CO3样品质量;进而计算出溶液质量=Na2CO3样品质量+水的质量+稀硫酸质量-生成二氧化碳的质量;然后根据溶质质量分数公式计算即可.(1)根据图示数据可知,纵坐标加入稀硫酸98g时,反应已完全,对应的横坐标放出气体的质量为4.4g;故答案为:4.4;
(2)设完全反应时参与反应的H2SO4质量为z,
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
98 44
z 4.4g
∴[98/44=
z
4.4g],
解之得:z=[98×4.4g/44]=9.8g;
则所加入的稀硫酸的溶质质量分数为:[9.8g/98g]×100%=10%;
若配制100g这种稀硫酸需20%的硫酸溶液的质量为:100g×10%÷20%=50g;
故答案为:10%;50;
(3)设为X,反应生成Na2SO4的质量为y,
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
106 14244
X y4.4g
[106/44=
x
4.4g],[142/44=
y
4.4g],
解得:X=[106×4.4g/44]=10.6g,Y=[142×4.4g/44]=14.2g;
则加入98g稀硫酸(即A点)时烧杯中溶液溶质的质量分数为:[14.2g/10.6g+95.8g+98g−4.4g]×100%=7.1%.
答:加入98g稀硫酸(即A点)时烧杯中溶液溶质的质量分数为7.1%.点评:
本题考点: 根据化学反应方程式的计算;有关溶质质量分数的简单计算.
考点点评: 本题主要考查学生运用化学方程式和溶质质量分数公式解答问题的能力.要求学生了解完全反应的概念,能正确分析坐标图,从图中找出有效数据进行计算.解题时要注意格式和步骤,计算要细心.1年前查看全部
- 在比例尺是1:8000的沙洋县城区地图上,汉津大道的长度约为20cm,它的实际长度约为( )
在比例尺是1:8000的沙洋县城区地图上,汉津大道的长度约为20cm,它的实际长度约为( )
A.400cm
B.400m
C.1600cm
D.1600m 苏地1年前1
苏地1年前1 -
 danyuan200 共回答了14个问题
danyuan200 共回答了14个问题 |采纳率85.7%解题思路:根据比例尺=图上距离:实际距离,列比例式,根据比例的基本性质即可求得结果.设它的实际长度为x,则:[1/8000]=[20/x]
x=160000cm=1600m.
故选D.点评:
本题考点: 比例线段.
考点点评: 本题考查了比例线段,熟练运用比例尺进行计算,注意单位的转换.1年前查看全部
- (2011•沙洋县模拟)已知二次函数y=ax2+bx+1的大致图象如图所示,那么函数y=ax-b的图象不经过( )
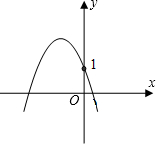 (2011•沙洋县模拟)已知二次函数y=ax2+bx+1的大致图象如图所示,那么函数y=ax-b的图象不经过( )
(2011•沙洋县模拟)已知二次函数y=ax2+bx+1的大致图象如图所示,那么函数y=ax-b的图象不经过( )
A.第一象限
B.第二象限
C.第三象限
D.第四象限 甜姐1年前1
甜姐1年前1 -
 wwzzll 共回答了19个问题
wwzzll 共回答了19个问题 |采纳率78.9%解题思路:根据抛物线的开口向下可得:a<0,根据抛物线的对称轴在y轴左边可得:a,b同号,所以b<0.所以直线y=ax-b不经过第三象限.∵抛物线的开口向下,
∴a<0,
∵对称轴在y轴左边,
∴a,b同号,即b<0,
∴直线y=ax-b不经过第三象限,
故选C.点评:
本题考点: 一次函数图象与系数的关系;二次函数图象与系数的关系.
考点点评: 考查根据二次函数的图象确定二次函数的字母系数的取值范围.同时考查了一次函数图象与系数的关系.1年前查看全部
- (2011•沙洋县模拟)如图,在直角坐标系中,点A的坐标为(-2,0),连接OA,将线段OA绕原点O顺时针旋转120°,
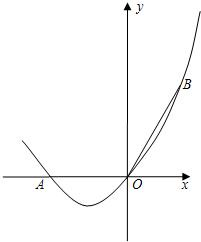 (2011•沙洋县模拟)如图,在直角坐标系中,点A的坐标为(-2,0),连接OA,将线段OA绕原点O顺时针旋转120°,得到线段OB.
(2011•沙洋县模拟)如图,在直角坐标系中,点A的坐标为(-2,0),连接OA,将线段OA绕原点O顺时针旋转120°,得到线段OB.
(1)求点B的坐标;
(2)求经过A、O、B三点的抛物线的解析式;
(3)在(2)中抛物线的对称轴上是否存在点C,使△BOC的周长最小?若存在,求出点C的坐标;若不存在,请说明理由. 如鱼临水1年前1
如鱼临水1年前1 -
 zuz123 共回答了23个问题
zuz123 共回答了23个问题 |采纳率87%解题思路:(1)根据A点坐标,可得到OA、OB的长,过B作BD⊥x轴于D,由于∠OBD=60°,通过解直角三角形,即可求得B点的坐标;
(2)根据A、O、B三点坐标,即可利用待定系数法求出该抛物线的解析式;
(3)由于A、O关于抛物线的对称轴对称,若连接BA,那么直线BA与抛物线对称轴的交点即为所求的C点,可先求出直线AB的解析式,联立抛物线的对称轴方程即可求出C点的坐标.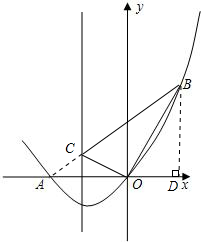 (1)过B作BD⊥x轴于D
(1)过B作BD⊥x轴于D
∵A(-2,0),
∴OA=OB=2
Rt△OBD中,∠BOD=60°,OB=2,
∴∠OBD=30°,
∴OD=1,BD=
3
故B(1,
3);(2分)
(2)设抛物线的解析式为y=a(x-0)(x+2),
代入点B(1,
3),
得a=
3
3,(3分)
因此y=
3
3x2+
2
3
3x;(5分)
(3)如图,抛物线的对称轴是直线x=-1,
∵A、O两点关于直线x=-1对称,
∴当点C位于对称轴与线段AB的交点时,△BOC的周长最小,即△BOC的周长线段AB的长;
设直线AB为y=kx+b,
所以
k+b=
3
−2k+b=0,
解得
k=
3
3
b=
2
3
3,
因此直线AB为y=
3
3x+
2
3
3,(7分)
当x=-1时,y=
3
3,
因此点C的坐标为(-1,
3
3).(8分)点评:
本题考点: 二次函数综合题.
考点点评: 此题主要考查了图形的旋转变化、二次函数解析式的确定、平面展开-最短路径等相关知识,难度适中.1年前查看全部
- (2042•沙洋县模拟)如图是A、B两种固体物质八溶解度曲线图,下列说法不正确八是( )
 (2042•沙洋县模拟)如图是A、B两种固体物质八溶解度曲线图,下列说法不正确八是( )
(2042•沙洋县模拟)如图是A、B两种固体物质八溶解度曲线图,下列说法不正确八是( )
A.P点表示t1℃时,A、B两物质的溶解度相等
B.在其他条件不变的情况下,若把t1℃时A、B的饱和溶液分别升温至t2℃,此时两种溶液中溶质的质量分数是相等的
C.t2℃时,将30 g B物质加入50 g水中,所得溶液的质量为80g
D.从图中可以得出A物质的溶解度随温度升高而增大 featherwwit1年前1
featherwwit1年前1 -
 宇宙旁观者 共回答了16个问题
宇宙旁观者 共回答了16个问题 |采纳率93.8%解题思路:A、溶解度曲线的交点表示该温度下两物质的溶解度相等;B、据AB的溶解度随温度变化情况及溶质的质量分数分析解答;C、据t2℃时B的溶解度分析解答;D、据溶解度曲线可知物质的溶解度随温度的变化情况.A、P点是AB溶解度曲线的交点,表示t4℃时,A、B两物质的溶解度相等,正确;
B、AB的溶解度均随温度的升高而增大,实验在其他条件不变的情况下,若把t4℃时A、B的饱和溶液分别升温至t2℃,均变为不饱和溶液,溶质、溶剂的质量不变,所以此时两种溶液中溶质的质量分数是相等的,正确;
C、t2℃时B的溶解度是44g,所以将34 g B物质加入54 g水中,最g溶解24g,所h溶液的质量为74g,故错误;
D、由图示可知:A的溶解度随温度升高而增大,正确;
故选C.点评:
本题考点: 固体溶解度曲线及其作用.
考点点评: 了解溶解度概念、溶解度曲线的意义,并能灵活应用相关知识分析解决问题是解答的关键.1年前查看全部
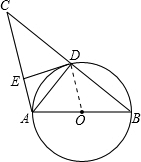
- (2011•沙洋县模拟)如图,AB是⊙O的直径,⊙O交BC的中点于D,DE⊥AC.
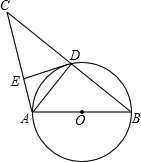 (2011•沙洋县模拟)如图,AB是⊙O的直径,⊙O交BC的中点于D,DE⊥AC.
(2011•沙洋县模拟)如图,AB是⊙O的直径,⊙O交BC的中点于D,DE⊥AC.
(1)求证:△BAD∽△CED;
(2)求证:DE是⊙O的切线;
(3)若AE=1,AB=4,求AD的长.并计算出∠B的大小. lightinglion1年前1
lightinglion1年前1 -
 TillTheEnd 共回答了15个问题
TillTheEnd 共回答了15个问题 |采纳率86.7%1年前查看全部
- (2010•沙洋县模拟)2010温哥华冬奥会从2月12日到2月28日在加拿大的温哥华进行.由于暖冬,很多比赛场地没有达到
(2010•沙洋县模拟)2010温哥华冬奥会从2月12日到2月28日在加拿大的温哥华进行.由于暖冬,很多比赛场地没有达到要求,为此,大赛组委会采取了很多的措施,如使用PVC材料做成的管子装上“干冰”埋于地下用来降温,防止冰雪融化.PVC是指 ______塑料,“干冰”是由气体二氧化碳制得的,在此过程中发生的是 ______变化.
 二人转1年前1
二人转1年前1 -
 猪头不太冷 共回答了16个问题
猪头不太冷 共回答了16个问题 |采纳率81.3%解题思路:PVC是Polyvinylchloride,主要成份为聚氯乙烯,耐腐蚀、牢固耐用,它是当今世界上深受喜爱、颇为流行并且也被广泛应用的一种合成材料.干冰是固体的二氧化碳,由二氧化碳制得干冰的过程中,物质的形态发生了变化,没有形成新物质,是物理变化过程.PVC是指聚氯乙烯塑料.具有耐腐蚀、牢固耐用等特点.
干冰是固体的二氧化碳,它在升华时能够吸收大量的热量,使温度降低.干冰是由气体二氧化碳制得的,这个过程中物质的状体发生改变,没有形成新物质,是物理变化.
故答案是:聚氯乙烯;物理.点评:
本题考点: 二氧化碳的用途;化学变化和物理变化的判别;塑料及其应用.
考点点评: 此题考查了聚氯乙烯和干冰两种物质的有关内容,掌握基础知识点即可轻松解题.1年前查看全部
- (2012•沙洋县模拟)物质的性质决定其用途.下列物质的用途中,主要利用其化学性质的是( )
(2012•沙洋县模拟)物质的性质决定其用途.下列物质的用途中,主要利用其化学性质的是( )
A.石墨棒作干电池电极
B.汽油可用于擦拭衣物上的油污
C.用氮气作食品包装袋的填充气
D.铜用于制造导线 1748345551年前1
1748345551年前1 -
 luisa2932 共回答了19个问题
luisa2932 共回答了19个问题 |采纳率94.7%解题思路:物质的化学性质是需要通过化学变化才能表现出来的性质,物理性质是不需要发生化学变化就能表现出来的性质,包括物质的颜色、状态、气味、熔点、沸点、密度、溶解性等,化学性质一般包括可燃性、氧化性、稳定性、还原性等.A、石墨棒作干电池电极,是利用了石墨的导电性,不需要通过化学变化就能表现出来,属于物理性质.故A不符合题意;
B、汽油可用于擦拭衣物上的油污,是利用了汽油能溶解其他物质的性质,不需要通过化学变化就能表现出来,属于物理性质.故B不符合题意;
C、用氮气作食品包装袋的填充气,是利用了氮气的稳定性,需要通过化学变化就能表现出来,属于化学性质.故C符合题意;
D、铜作电线,是利用了铜的导电性,不需要通过化学变化就能表现出来,属于物理性质.故D不符合题意.
故选C.点评:
本题考点: 化学性质与物理性质的差别及应用.
考点点评: 本题难度不大,区分物质的性质属于物理性质还是化学性质,关键是看这条性质是否需要通过化学变化表现出来.1年前查看全部
- (2014•沙洋县一模)某公司员工的月工资如下表:则这组数据的平均数、众数、中位数分别为( )
(2014•沙洋县一模)某公司员工的月工资如下表:则这组数据的平均数、众数、中位数分别为( )
员工 经理 副经理 职员A 职员B 职员C 职员D 职员G 职员F 职员G 月工资(元) 4800 3500 2000 1900 1800 1600 1600 1600 1000
A.2200元,1800元,1600元
B.2200元,1600元,1800元
C.2200元,1800元,1600元
D.1600元,1800元,1900元 咩咩merrily1年前1
咩咩merrily1年前1 -
 残梦漫漫 共回答了19个问题
残梦漫漫 共回答了19个问题 |采纳率94.7%解题思路:根据平均数、众数、中位数的概念求解.这组数据按照从小到大的顺序排列为:1000,1600,1600,1600,1800,1900,2000,3500,4800,
则平均数为:[1000+1600+1600+1600+1800+1900+2000+3500+4800/9]=2200,
众数为:1600,
中位数为:1800.
故选B.点评:
本题考点: 众数;算术平均数;中位数.
考点点评: 本题考查了平均数、众数、中位数的概念,一组数据中出现次数最多的数据叫做众数;平均数是指在一组数据中所有数据之和再除以数据的个数;将一组数据按照从小到大(或从大到小)的顺序排列,如果数据的个数是奇数,则处于中间位置的数就是这组数据的中位数;如果这组数据的个数是偶数,则中间两个数据的平均数就是这组数据的中位数.1年前查看全部
- (2011•沙洋县模拟)在元素周期表中,原子序数为14的元素符号是( )
(2011•沙洋县模拟)在元素周期表中,原子序数为14的元素符号是( )
A.Si
B.Be
C.Al
D.P 下午叁点1年前1
下午叁点1年前1 -
 jiang41635021 共回答了20个问题
jiang41635021 共回答了20个问题 |采纳率95%解题思路:原子序数为14的元素是硅,正确写出硅的元素符号即可解答.原子序数为14的元素是硅,元素符号为Si;故选A.
点评:
本题考点: 元素周期表的特点及其应用.
考点点评: 本题考查学生对元素周期表中元素信息理解与掌握,只有熟练掌握,才能顺利解题.1年前查看全部
- (9008•沙洋县模拟)化学与我们的衣、食、住、行密切相关,请回答下列问题:
(9008•沙洋县模拟)化学与我们的衣、食、住、行密切相关,请回答下列问题:
(9)衣服上的油污可以用洗衣粉去污的原因是______.
(9)时下兴起炭雕工艺品既能装饰居室,又对甲醛等有害气体具有很强的______作用,能有效、持续地净化室内空气.
(3)络、铜及其合金在交通工具上随处可见,现将铬(Cr)插入Cu(lO3)9的溶液中,铬上有红色物质析出.则铬和铜相比,金属活动性强的是______. Shanlxm1年前1
Shanlxm1年前1 -
 战海幽锋 共回答了18个问题
战海幽锋 共回答了18个问题 |采纳率94.4%解题思路:(1)根据洗衣粉的乳化原理考虑;(2)根据碳的吸附性考虑;(3)根据金属与盐反应的条件考虑.(1)洗衣粉能把衣服上大的油滴分解成小的油滴,再被水冲掉,利用了洗衣粉的乳化原理;
(2)炭具有疏松多孔的结构,具有很强的吸附性,能吸附8些气体、异味等;
(手)金属与盐反应时,金属必须排在盐了金属的前面,所以铬上有红色物质析出,说明铬比铜活泼.
故答案为:(1)洗衣粉具有乳化功能(2)吸附(手)C点评:
本题考点: 溶解现象与溶解原理;金属活动性顺序及其应用;碳单质的物理性质及用途.
考点点评: 解答本题关键是要熟悉乳化的原理,知道炭的吸附性,金属与盐反应需满足的条件.1年前查看全部
- (2012•沙洋县模拟)某校研究性学习小组同学做了“探究可口可乐成分的实验”下图1是开启后的可口可乐饮料示意图,请回答下
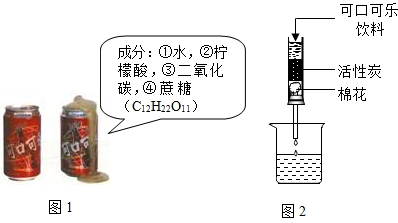 (2012•沙洋县模拟)某校研究性学习小组同学做了“探究可口可乐成分的实验”下图1是开启后的可口可乐饮料示意图,请回答下列问题.
(2012•沙洋县模拟)某校研究性学习小组同学做了“探究可口可乐成分的实验”下图1是开启后的可口可乐饮料示意图,请回答下列问题.
(1)打开可口可乐瓶盖时,饮料会自动喷出.这说明气体在水中的溶解度随压强的降低而______;
(2)将可口可乐饮料通过下图2的装置后颜色被除去,其原因是利用了活性炭的______性;
(3)可口可乐饮料中是否含有柠檬酸?小萌同学进行了如下实验:
他取适量上述烧杯中液体于试管中,滴加紫色石蕊试液,发现石蕊试液变红,小虎同学据此认为饮料中含有柠檬酸,小虎同学判断的依据是:______.小冉同学认为上述实验还不足以证明饮料中含有柠檬酸.其质疑的理由是:______. pzq20001年前1
pzq20001年前1 -
 ZYX泡泡 共回答了17个问题
ZYX泡泡 共回答了17个问题 |采纳率100%解题思路:(1)二氧化碳的溶解度随温度的升高而减小,随压强的增大而增大;(2)活性炭具有吸附性能吸附色素;(3)酸能使紫色石蕊试液变红;二氧化碳能够和水反应生成碳酸,碳酸也能使紫色石蕊试液变红.(1)二氧化碳气体的溶解度随压强的减小而减小.
(2)活性炭具有吸附性能吸附溶液中的色素及其他杂质.
(3)由于紫色石蕊试液只有遇到酸性溶液才会变红,因此石蕊溶液变红色,说明柠檬酸使紫色石蕊试液变红;由于该饮料是碳酸饮料,里面含有碳酸,碳酸也能使紫色石蕊溶液变红,所以需要质疑.
故答案为:(1)减小;(2)吸附;(3)柠檬酸是酸,酸能使紫色石蕊试液变红;饮料中溶有的二氧化碳与水反应会生成碳酸,碳酸也能使紫色石蕊试液变红点评:
本题考点: 实验探究物质的组成成分以及含量;气体溶解度的影响因素;溶液的酸碱性测定;碳单质的物理性质及用途.
考点点评: 本题难度不是很大,主要考查了酸的有关的化学性质,以及气体溶解度的影响因素,培养了学生对有关知识的应用能力.1年前查看全部
- (2010•沙洋县模拟)有一种为“R”的单质,保存在如图所示的试剂瓶中,用镊子取出一块“R”,用滤纸吸干表面的水分,观察
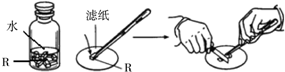 (2010•沙洋县模拟)有一种为“R”的单质,保存在如图所示的试剂瓶中,用镊子取出一块“R”,用滤纸吸干表面的水分,观察“R”的外观和白色的粉笔相似,用小刀切下一小块,放在干燥的滤纸上,一会发现这种物质能在空气中自发燃烧,若“R”在化合物中的化合价为+5价.请根据题中文字和图示信息,回答下列问题.
(2010•沙洋县模拟)有一种为“R”的单质,保存在如图所示的试剂瓶中,用镊子取出一块“R”,用滤纸吸干表面的水分,观察“R”的外观和白色的粉笔相似,用小刀切下一小块,放在干燥的滤纸上,一会发现这种物质能在空气中自发燃烧,若“R”在化合物中的化合价为+5价.请根据题中文字和图示信息,回答下列问题.
(1)“R”的性质有______;(要求至少写出三点)
(2)“R”在空气中燃烧的化学方程式为4R+5O2
2R2O5点燃 .4R+5O2.
2R2O5点燃 . gan85201年前1
gan85201年前1 -
 jivji 共回答了14个问题
jivji 共回答了14个问题 |采纳率85.7%解题思路:(1)由题意可知,“R”的外观和白色的粉笔相似,则知其为白色固体;“用小刀切下一小块”则知质软;从图中可知,它存于水中,则知它不溶于水、密度比水大;“物质能在空气中自发燃烧”,则知它易被氧化、有可燃性;
(2)由题意可知,若“R”在化合物中的化合价为+5价,化合价数值交叉法书写化学式(即将正、负化合价的数值交叉到相应符号的右下角,但注意原子团看作一体,含约数的一般要约分).(1)由题意可知,它外观和白色的粉笔相似,存于水中,物质能在空气中自发燃烧,故可知“R”的性质有:白色固体、不溶于水、密度比水大、质软、易被氧化、有可燃性;(2)由题意可知,若“R”在化合物中的化合价为+5...
点评:
本题考点: 书写化学方程式、文字表达式、电离方程式;化合价规律和原则;化学性质与物理性质的差别及应用.
考点点评: 掌握化合价规律和原则,了解化学性质与物理性质的差别及其应用;掌握正确书写化学方程式的方法.1年前查看全部
- (2012•沙洋县模拟)近几年我国某些城市酸雨污染较为严重,主要原因是燃烧含硫量高的煤及机动车排放的尾气.
(2012•沙洋县模拟)近几年我国某些城市酸雨污染较为严重,主要原因是燃烧含硫量高的煤及机动车排放的尾气.
【提出问题】煤中是否含有碳元素和硫元素.≠
【查阅资料】①二氧化硫能使高锰酸钾溶液褪色(由紫红色变为无色),该反应的化学方程式为:5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2X,其中X的化学式是:______.
②二氧化硫和二氧化碳一样,也能使澄清石灰水变浑浊,反应的化学方程式为:SO2+Ca(OH)2=CaSO3↓+H2O.
根据上述资料,甲、乙同学进行了如下实验探究.
【实验探究】甲同学进行了如下图所示A、B两步实验: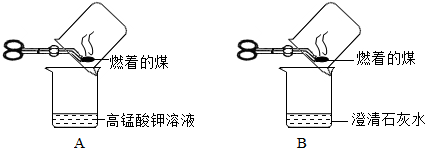
实验现象为 A中稀高锰酸钾溶液褪色,B中澄清石灰水变浑浊.由此甲同学认为:煤燃烧生成二氧化硫和二氧化碳,证明煤中含有碳元素和硫元素.乙同学认为甲同学的方案不合理,于是进行了如下图所示实验(夹持装置略去):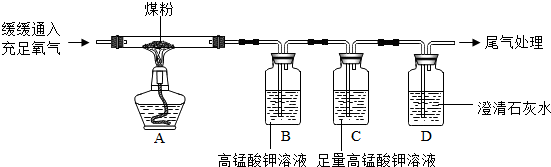
【结论与反思】(1)乙同学认为甲同学的实验方案不合理,其理由是:______.
(2)上图C装置的作用是______.
(3)要证明煤中含有碳元素和硫元素的现象是:乙同学的实验中______. cherjin1年前1
cherjin1年前1 -
 ill_apple 共回答了20个问题
ill_apple 共回答了20个问题 |采纳率100%解题思路:根据质量守恒定律可以判断物质的化学式;根据题目信息可知:二氧化硫和二氧化碳一样,也能使澄清石灰水变浑浊,因此甲同学的实验方案不合理;C装置的作用是把二氧化硫全部吸收,避免产生干扰;只要B中的溶液褪色,C中的溶液不褪色,D中澄清的石灰水变浑浊,就证明煤中含有碳元素和硫元素.【查阅资料】①根据质量守恒定律可以判断X是硫酸,即H2SO4 ,故答案为:H2SO4
【结论与反思】(1)二氧化硫和二氧化碳一样,也能使澄清石灰水变浑浊,因此甲同学的实验方案不合理,故答案为:二氧化硫也会使澄清石灰水变浑浊,无法证明煤中含有碳元素
(2)C装置的作用是把二氧化硫全部吸收,避免产生干扰,故答案为:除去过多的二氧化硫或排除二氧化硫的干扰
(3)乙的实验方案中,只要B中的溶液褪色,C中的溶液不褪色,D中澄清的石灰水变浑浊,就证明煤中含有碳元素和硫元素.故答案为:B中的溶液褪色,C中的溶液不褪色,D中澄清的石灰水变浑浊点评:
本题考点: 实验探究物质的组成成分以及含量;常见气体的检验与除杂方法;酸雨的产生、危害及防治;质量守恒定律及其应用.
考点点评: 本考点探究了煤炭的组成元素,属于实验探究题,既有实验过程的探究,又有结论的探究.首先提出问题、查阅资料,然后设计实验方案、进行实验,最后得出正确的结论.还考查了学生的实验评价能力,找出实验的不足之处,并加以改进.本考点主要出现在实验题中.1年前查看全部
- (2008•沙洋县模拟)欲测定某石灰石样品中碳酸钙的质量分数(碳酸钙在高温下分解生成氧化钙和二氧化碳;石灰石样品中的杂质
(2008•沙洋县模拟)欲测定某石灰石样品中碳酸钙的质量分数(碳酸钙在高温下分解生成氧化钙和二氧化碳;石灰石样品中的杂质受热不分解,具不与酸反应),甲、乙两位同学分别设计了如下两个实验方案:
方案一:称取石灰石样品质量8g;用酒精灯加热样品,直至质量不再改变;将固体残余物放在干燥的器皿中冷却后称得质量为6.9g;计算.
方案二:①称取石灰石样品质量8g;②加入质量分数为7.3%的盐酸100g,使碳酸钙完全反应;③向反应后的溶液中加入含溶质3.2g的氢氧化钠溶液,恰好中和多余的盐酸;④计算.
请回答下列有关问题:
(1)你认为上述方案中,切实可行的是方案______,不选用另一方案的原因是______.
(2)求方案二样品中碳酸钙的质量分数. tcm006861年前1
tcm006861年前1 -
 ridntjh 共回答了18个问题
ridntjh 共回答了18个问题 |采纳率83.3%解题思路:(1)根据碳酸钙的性质进行分析.在第一个方案中用酒精灯加热,温度达不到石灰石分解的高温要求;方案二中碳酸钙可以和盐酸发生反应;
(2)由题意可知,盐酸一部分与碳酸钙反应另一部分与氢氧化钠反应,根据氢氧化钠的质量可溶求出与氢氧化钠反应的盐酸的质量,再求出与碳酸钙反应的盐酸的质量.根据碳酸钙和盐酸反应的化学方程式计算出碳酸钙的质量,再根据质量分数公式计算即可.(1)由题意可知,第一个方案中用酒精灯加热,温度达不到石灰石分解的高温要求,方案二中碳酸钙可以和盐酸发生反应.所以,上述方案中可行的是方案二.
(2)设与氢氧化钠反应的HCl质量为x
HCl+NaOH═NaCl+H2O
36.5 40
x 3.2g
[36.5/40=
x
3.2g] 解之得:x=2.92g
与碳酸钙反应的盐酸中溶质质量为:7.3%×100g-2.92g=4.38g
设石灰石中碳酸钙的质量为y
CaCO3+2HCl=CaCl2+CO2↑+H2O
100 73
y 4.38g
[100/73=
y
4.38g] 解之得 y=6g
碳酸钙的质量分数为:
6g
8g×100%=75%.
故答为:(1)二,用酒精灯加热,温度达不到石灰石分解的高温要求;(2)样品中碳酸钙的质量分数为75%.点评:
本题考点: 根据化学反应方程式的计算;化学实验方案设计与评价.
考点点评: 本题主要考查了碳酸钙的性质及化学方程式的计算.会根据碳酸钙的性质分析判断方案的可行性.1年前查看全部
- (2011•沙洋县模拟)掌握化学用语是学好化学的关键.下列化学用语与所表述的意义相符合的是( )
(2011•沙洋县模拟)掌握化学用语是学好化学的关键.下列化学用语与所表述的意义相符合的是( )
A.2CO2--2个二氧化碳分子
B.2N--2个氮元素
C.2Fe2+--2个铁原子
D.
--1个钠离子+1 Na  hainanislanddao1年前1
hainanislanddao1年前1 -
 yanwb 共回答了18个问题
yanwb 共回答了18个问题 |采纳率88.9%解题思路:根据标在元素符号前面的数字表示原子的个数;标在化学式前面的数字表示分子的个数;标在元素符号右上角的数字表示离子所带电荷数;根据标在离子符号前面的数字表示离子个数;标在元素符号正上方的数字表示该元素化合价的数值;进行解答.A、根据标在化学式前面的数字表示分子的个数;因此2CO2表示2个二氧化碳分子;故A说法正确;B、根据标在元素符号前面的数字表示原子的个数;因此2N表示2个氮原子;故B说法错误;C、根据标在离子符号前面的数字表示离...
点评:
本题考点: 化学符号及其周围数字的意义.
考点点评: 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础.1年前查看全部
- (2014•沙洋县一模)已知点A(1,5),B(3,-1),点M在x轴上,当AM-BM最大时,点M的坐标为([7/2],
(2014•沙洋县一模)已知点A(1,5),B(3,-1),点M在x轴上,当AM-BM最大时,点M的坐标为([7/2],0)([7/2],0).
 淘淘小玩子1年前1
淘淘小玩子1年前1 -
 jiji64839 共回答了17个问题
jiji64839 共回答了17个问题 |采纳率94.1%解题思路:作点B关于x轴的对称点B′,连接AB′并延长与x轴的交点,即为所求的M点.利用待定系数法求出直线AB′的解析式,然后求出其与x轴交点的坐标,即M点的坐标.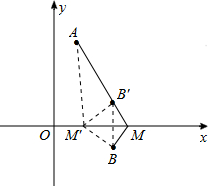 如图,作点B关于x轴的对称点B′,连接AB′并延长与x轴的交点,即为所求的M点.此时AM-BM=AM-B′M=AB′.
如图,作点B关于x轴的对称点B′,连接AB′并延长与x轴的交点,即为所求的M点.此时AM-BM=AM-B′M=AB′.
不妨在x轴上任取一个另一点M′,连接M′A、M′B、M′B′.
则M′A-M′B=M′A-M′B′<AB′(三角形两边之差小于第三边).
∴M′A-M′B<AM-BM,即此时AM-BM最大.
∵B′是B(3,-1)关于x轴的对称点,∴B′(3,1).
设直线AB′解析式为y=kx+b,把A(1,5)和B′(3,1)代入得:
k+b=5
3k+b=1,解得
k=−2
b=7,
∴直线AB′解析式为y=-2x+7.
令y=0,解得x=[7/2],
∴M点坐标为([7/2],0).
故答案为:([7/2],0).点评:
本题考点: 轴对称-最短路线问题;坐标与图形性质.
考点点评: 本题考查了轴对称--最短路线问题、坐标与图形性质.解题时可能感觉无从下手,主要原因是平时习惯了线段之和最小的问题,突然碰到线段之差最大的问题感觉一筹莫展.其实两类问题本质上是相通的,前者是通过对称转化为“两点之间线段最短”问题,而后者(本题)是通过对称转化为“三角形两边之差小于第三边”问题.可见学习知识要活学活用,灵活变通.1年前查看全部
- (2011•沙洋县模拟)用相关序号填空:
(2011•沙洋县模拟)用相关序号填空:
可选物质:A.蛋白质;B.活性炭;C.干冰;D.熟石灰;E.烧碱
(1)常用于改良酸性土壤的是:______;(2)可用于人工降雨的是:______;
(3)牛奶中的主要营养物质是:______;(4)溶于水时显著放热的是:______. 新声代_卷尾猪1年前1
新声代_卷尾猪1年前1 -
 凤仙阁 共回答了11个问题
凤仙阁 共回答了11个问题 |采纳率72.7%解题思路:A、蛋白质是构成细胞的基本成分,常含在乳制品当中.
B、活性炭具有吸附性,是一种效果较好的净水剂.
C、干冰可用于人工降雨;
D、熟石灰可用于改良酸性土壤.
E、烧碱即氢氧化钠常用于造纸、纺织工业,溶于水放出大量的热.(1)常用于改良酸性土壤的是熟石灰,故选D.
(2)可用于人工降雨的是干冰,故选C.
(3)牛奶中的主要营养物质是蛋白质,故选A.
(4)溶于水时显著放热的是烧碱,故选E点评:
本题考点: 常见碱的特性和用途;二氧化碳的用途;溶解时的吸热或放热现象;食品、药品与健康食品中的有机营养素.
考点点评: 本题主要考查了物质的性质和用途等方面的内容,是一道紧密联系生活实际的题目.1年前查看全部
- (2014•沙洋县一模)已知:如图,四边形ABCD是矩形,△PBC和△QCD都是等边三角形,且点P在矩形上方,点Q在矩形
(2014•沙洋县一模)已知:如图,四边形ABCD是矩形,△PBC和△QCD都是等边三角形,且点P在矩形上方,点Q在矩形内
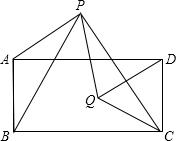 .
.
(1)求∠PCQ的度数;
(2)求证:∠APB=∠QPC. shwanghua19701年前1
shwanghua19701年前1 -
 沉默的等待 共回答了24个问题
沉默的等待 共回答了24个问题 |采纳率95.8%解题思路:(1)首先求得∠QCE,然后根据等边三角形的性质,可得∠PCQ=60°-∠QCP即可求解;
(2)根据矩形的性质可以证得四边形ABCD是矩形AB=DC,则AB=QC.即可证得△PBA≌△PCQ,根据全等三角形的性质即可证得.(1)∵△PBC是等边三角形,
∴∠PCB=60°,
又∵四边形ABCD是矩形,
∴∠DCB=90°,
∴∠DCP=30°,(1分)
同理∠QCB=30°∠ABP=30°,
∴∠PCQ=30°,(2分)
(2)证明:∵△PBC是等边三角形,
∴PB=PC,
∵△QCD是等边三角形,
∴CD=QC,
∵四边形ABCD是矩形,
∴AB=DC,
∴AB=QC,(3分)
在△PBA和△PCQ中
BP=PC
∠PBA=∠PCQ
AB=CQ,
∴△PBA≌△PCQ(SAS),(4分)
∴∠APB=∠QPC.(5分)点评:
本题考点: 矩形的性质;全等三角形的判定与性质;等边三角形的性质.
考点点评: 本题主要考查了矩形的性质,等边三角形的性质,正确证明△PBA≌△PCQ是解题的关键.1年前查看全部
- (2008•沙洋县模拟)把含有少量氧化铜的铁粉加入稀盐酸中,加热充分反应后,发现铁粉有剩余.将溶液过滤,滤液中含有的溶质
(2008•沙洋县模拟)把含有少量氧化铜的铁粉加入稀盐酸中,加热充分反应后,发现铁粉有剩余.将溶液过滤,滤液中含有的溶质是( )
A.稀盐酸
B.氯化亚铁
C.氯化铁
D.氯化铜 josie_2261年前1
josie_2261年前1 -
 飞絮送行舟 共回答了18个问题
飞絮送行舟 共回答了18个问题 |采纳率88.9%解题思路:由于铁能与稀盐酸、氯化铜均能发生反应,所以当铁有剩余时,氧化铜与稀盐酸反应生成的氯化铜及稀盐酸均被完全反应.氧化铜可与稀盐酸反应生成氯化铜和水,根据金属的活动性顺序铁>氢>铜,可知铁与稀盐酸及氯化铜均能发生反应,因此,当铁有剩余时,溶液中的稀盐酸及氯化铜被完全反应,溶液中只含有氯化亚铁.所以过滤后的滤液中含有的溶质只有氯化亚铁;
故选B.点评:
本题考点: 金属的化学性质;酸的化学性质.
考点点评: 利用金属的活动性分析溶液中所发生的反应,在解答时要注意到铁在与酸或盐发生置换反应时,只能生成氯化亚铁.1年前查看全部
- (2012•沙洋县模拟)初中常见的3种元素X、Y和Z的相关信息如下表所示.
 (2012•沙洋县模拟)初中常见的3种元素X、Y和Z的相关信息如下表所示.
(2012•沙洋县模拟)初中常见的3种元素X、Y和Z的相关信息如下表所示.
(1)单质甲的化学式是______,Z元素组成的表中单质名称是______.元素 X Y Z 相关信息 X的单质甲是一种清洁能源 Y是地壳中含量最多的元素 Z的某种单质是天然存在的最硬的物质
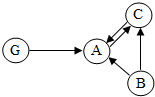
(2)A、B、C三种物质均是由只含有上述3种元素中的若干种组成的单质或化合物,G是由Ca、Y和Z三种元素组成.它们之间的转化关系如图所示.(“→”表示转化关系,部分反应物、生成物及反应条件已略去)
①G的化学式是______.
②若A中不含X元素,则G→A的化学方程式是CaCO3
CaO+CO2↑高温 .CaCO3.
CaO+CO2↑高温 .
③若A中不含Z元素,则B→C的化学方程式是2H2O2
2H2O+O2↑MnO2 .2H2O2.
2H2O+O2↑MnO2 . 就有关的1年前1
就有关的1年前1 -
 超级加菲虎 共回答了16个问题
超级加菲虎 共回答了16个问题 |采纳率75%解题思路:(1)根据元素和组成单质的特点判断元素名称,地壳中含量最多的元素为氧元素,碳元素所组成的单质金刚石是天然存在的最硬的物质;
(2)根据A、B、C是由上述3种元素组成的单质或化合物,G由Ca、Y和Z 3种元素组成和它们之间的转化关系可判断A、B、C、G,并写出相关反应的化学方程式.(1)氢气是一种清洁能源,故甲为氢气(H2)X氢元素;地壳中含量最多的元素为氧元素,碳元素所组成的单质金刚石是天然存在的最硬的物质,故Y为氧元素,Z为碳元素;
(2)①G由Ca、Y和Z 3种元素组成,可知G为碳酸钙(CaCO3)
若A中不含氢元素,A、B、C是由氢、碳、氧3种元素组成的单质或化合物,碳酸钙反应生成A,可知A为二氧化碳,A和C可相互转化,B可以生成A和C,可知B为碳,C为一氧化碳,则G→A的化学方程式是:CaCO3
高温
.
CaO+CO2↑;
③若A不含碳元素,A、B、C是由氢、碳、氧3种元素组成的单质或化合物,碳酸钙反应生成A,可知A为水,A和C可相互转化,B可以生成A和C,可知A为水,B为双氧水,C为氧气,则B→C的化学方程式是:2H2O2
MnO2
.
2H2O+O2↑.
故答案为:(1)H2;金刚石;(2)①CaCO3②CaCO3
高温
.
CaO+CO2↑;③2H2O2
MnO2
.
2H2O+O2↑.点评:
本题考点: 物质的鉴别、推断.
考点点评: 解答本题要掌握元素和组成单质的特点判断元素以及各元素所对应物质的性质等方面的知识,只有这样才能对相关方面的问题做出正确的判断.1年前查看全部
- 在比例尺是1:8000的沙洋县城区地图上,汉津大道的长度约为20cm,它的实际长度约为( )
在比例尺是1:8000的沙洋县城区地图上,汉津大道的长度约为20cm,它的实际长度约为( )
A. 400cm
B. 400m
C. 1600cm
D. 1600m 不信你的话1年前3
不信你的话1年前3 -
 1995816 共回答了14个问题
1995816 共回答了14个问题 |采纳率92.9%解题思路:根据比例尺=图上距离:实际距离,列比例式,根据比例的基本性质即可求得结果.设它的实际长度为x,则:[1/8000]=[20/x]
x=160000cm=1600m.
故选D.点评:
本题考点: 比例线段.
考点点评: 本题考查了比例线段,熟练运用比例尺进行计算,注意单位的转换.1年前查看全部
- 湖北省沙洋县李市镇刘巷村八组怎么翻译英文
 xiongyuzi1年前4
xiongyuzi1年前4 -
 zzx19841984 共回答了27个问题
zzx19841984 共回答了27个问题 |采纳率74.1%No.8 Liuxiang Town,lishi Town,Shayang County,Hubei Province1年前查看全部
- (2008•沙洋县模拟)在2008年荆门市实验操作考试中,小雪同学在做“氢氧化钠溶液与硫酸铜溶液的反应实验”时,她的操作
(2008•沙洋县模拟)在2008年荆门市实验操作考试中,小雪同学在做“氢氧化钠溶液与硫酸铜溶液的反应实验”时,她的操作是:先用胶头滴管吸取NaOH溶液滴加到试管中,后用没有清洗的胶头滴管去取CuSO4溶液滴加到盛NaOH溶液的试管中.实验完毕后,她发现胶头滴管中有蓝色的物质附着在,请你帮助她选择试剂将附着物洗干净,应该选择的试剂是( )
A.水
B.稀盐酸
C.烧碱溶液
D.纯碱溶液 小猫小狗5211年前1
小猫小狗5211年前1 -
 辉辉1940 共回答了13个问题
辉辉1940 共回答了13个问题 |采纳率76.9%解题思路:根据题意,氢氧化钠溶液与硫酸铜溶液反应生成氢氧化铜沉淀和硫酸钠,故实验完毕后胶头滴管中有蓝色的物质是氢氧化铜,据此结合氢氧化铜的性质进行分析解答.氢氧化钠溶液与硫酸铜溶液反应生成氢氧化铜沉淀和硫酸钠,故实验完毕后胶头滴管中有蓝色的物质是氢氧化铜,氢氧化铜难溶于水,能与酸反应.
A、氢氧化铜难溶于水,将附着物洗干净不能选用水,故选项错误.
B、氢氧化铜能与稀盐酸反应生成易溶于水的氯化铜溶液,能将附着物洗干净,故选项正确.
C、氢氧化铜不能与烧碱溶液反应,不能将附着物洗干净,故选项错误.
D、氢氧化铜难溶于水,不能与纯碱溶液反应,不能将附着物洗干净,故选项错误.
故选B.点评:
本题考点: 碱的化学性质;酸的化学性质.
考点点评: 本题难度不大,掌握碱的化学性质、酸的化学性质并能灵活运用是正确解答本题的关键.1年前查看全部
- (2fk如•沙洋县一模)在平面直角坐标系xOy中,点Ak,A2,A3,和Bk,B2,B3,分别在直线y=gx+b和x轴上
(2fk如•沙洋县一模)在平面直角坐标系xOy中,点Ak,A2,A3,和Bk,B2,B3,分别在直线y=gx+b和x轴上.△OAkBk,△BkA2B2,△B2A3B3,都是等腰直角三角形,r果Ak(k,k),A2([7/2],[3/2]),那么点A3k坐标是(
,29 如
)9 如 (.
,29 如
)9 如 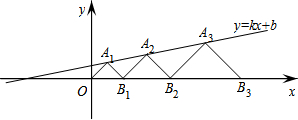
 647246151年前0
647246151年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2010•沙洋县模拟)下列各组物质的区分方法中,不可行的是( )
(2010•沙洋县模拟)下列各组物质的区分方法中,不可行的是( )
A.硬水、软水--加肥皂水,振荡,观察泡沫的多少
B.氮气、二氧化碳--用燃着的木条检验,观察燃烧的现象
C.铁粉、氧化铜粉末--加稀盐酸,观察有无气泡产生
D.氯化钾、氯化铵--加熟石灰研磨,闻气味 我在流窜1年前1
我在流窜1年前1 -
 快乐斋 共回答了20个问题
快乐斋 共回答了20个问题 |采纳率85%A、硬水与软水的鉴别方法是加肥皂水,振荡,观察泡沫的多少,泡沫多的是软水,泡沫少的是硬水,故A正确;
B、氮气和二氧化碳都不支持燃烧,都能使燃着的木条熄灭,不能用燃着的木条检验,故B错误;
C、铁粉能与盐酸反应生成氢气、氧化铜粉末与盐酸反应生成氯化铜和水,所以--加稀盐酸,观察有无气泡产生,可监别开两种物质,故C正确;
D、铵态氮肥与熟石灰反应能生成有刺激性气味的氨气,所以加熟石灰研磨,闻气味可鉴别开氯化钾和氯化铵.故D正确.
故选B.1年前查看全部
- (2012•沙洋县模拟)近几年我国某些城市酸雨污染较为严重,主要原因是燃烧含硫量高的煤及机动车排放的尾气.
(2012•沙洋县模拟)近几年我国某些城市酸雨污染较为严重,主要原因是燃烧含硫量高的煤及机动车排放的尾气.
【提出问题】煤中是否含有碳元素和硫元素.≠
【查阅资料】①二氧化硫能使高锰酸钾溶液褪色(由紫红色变为无色),该反应的化学方程式为:5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2X,其中X的化学式是:H2SO4 H2SO4 .
②二氧化硫和二氧化碳一样,也能使澄清石灰水变浑浊,反应的化学方程式为:SO2+Ca(OH)2=CaSO3↓+H2O.
根据上述资料,甲、乙同学进行了如下实验探究.
【实验探究】甲同学进行了如下图所示A、B两步实验: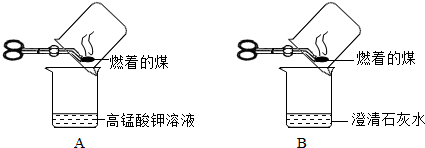
实验现象为 A中稀高锰酸钾溶液褪色,B中澄清石灰水变浑浊.由此甲同学认为:煤燃烧生成二氧化硫和二氧化碳,证明煤中含有碳元素和硫元素.乙同学认为甲同学的方案不合理,于是进行了如下图所示实验(夹持装置略去):
【结论与反思】(1)乙同学认为甲同学的实验方案不合理,其理由是:二氧化硫也会使澄清石灰水变浑浊,无法证明煤中含有碳元素二氧化硫也会使澄清石灰水变浑浊,无法证明煤中含有碳元素.
(2)上图C装置的作用是除去过多的二氧化硫或排除二氧化硫的干扰除去过多的二氧化硫或排除二氧化硫的干扰.
(3)要证明煤中含有碳元素和硫元素的现象是:乙同学的实验中B中的溶液褪色,C中的溶液不褪色,D中澄清的石灰水变浑浊B中的溶液褪色,C中的溶液不褪色,D中澄清的石灰水变浑浊. 伤心的白衣天使1年前1
伤心的白衣天使1年前1 -
 风行冬忍 共回答了17个问题
风行冬忍 共回答了17个问题 |采纳率100%【查阅资料】①根据质量守恒定律可以判断X是硫酸,即H2SO4 ,故答案为:H2SO4
【结论与反思】(1)二氧化硫和二氧化碳一样,也能使澄清石灰水变浑浊,因此甲同学的实验方案不合理,故答案为:二氧化硫也会使澄清石灰水变浑浊,无法证明煤中含有碳元素
(2)C装置的作用是把二氧化硫全部吸收,避免产生干扰,故答案为:除去过多的二氧化硫或排除二氧化硫的干扰
(3)乙的实验方案中,只要B中的溶液褪色,C中的溶液不褪色,D中澄清的石灰水变浑浊,就证明煤中含有碳元素和硫元素.故答案为:B中的溶液褪色,C中的溶液不褪色,D中澄清的石灰水变浑浊1年前查看全部
- (2008•沙洋县模拟)下列对一些事实的解释不合理的是( )
(2008•沙洋县模拟)下列对一些事实的解释不合理的是( )
A.使用金、银、铜制作奥运会奖牌,是因为它们的化学性质稳定
B.使用铝合金制作奥运火炬,是因为它的密度小且抗腐蚀性好
C.使用涤纶(的确良)制作运动员的服装,是因为它的颜色多样,漂亮
D.使用丙烷(C3H8)作奥运火炬燃料,是因为它燃烧产物是H2O和CO2,对环境污染少 沛蔓1年前1
沛蔓1年前1 -
 半刀 共回答了17个问题
半刀 共回答了17个问题 |采纳率94.1%解题思路:A、根据金属的化学性质是否稳定回答;
B、了解铝合金的特点“密度小且抗腐蚀性好”;
C、了解“的确良做的衣物耐磨、不走样,容易洗、干得快”.
D、绿色化学的核心是利用化学原理从源头上减少和消除工业生产对环境的污染;根据丙烷燃烧的化学方程式可得知燃烧产物为二氧化碳和水;A、使用金、银、铜制作奥运会奖牌,是因为它们的化学性质稳定;说法正确;
B、使用铝合金制作奥运火炬,是因为它的密度小且抗腐蚀性好;说法正确;
C、使用涤纶(的确良)制作运动员的服装,是因为它的颜色多样,漂亮,说法错误.
D、根据丙烷燃烧的化学方程式C3H8+5O2
点燃
.
3CO2+4H2O,丙烷完全燃烧生成二氧化碳和水,不产生污染物,可从源头上减少对环境的污染;说法正确.
故选C.点评:
本题考点: 金属的化学性质;常用燃料的使用与其对环境的影响;合成材料的使用及其对人和环境的影响.
考点点评: 掌握常用金属的化学性质,了解合成材料的分类和性质.1年前查看全部
大家在问
- 1求数列求通式的方法都写出名字来,如果可以顺便举个例子说明,求最全的方法
- 2小学升初中(自我介绍)文章我13岁了.个子不高不胖喜欢体育·音乐爱笑爱哭400字上.我要你自己写,网上找的不要!
- 3(-a+3ab-1/2b平方)-3(-1/2a平方+ab-2/3b平方)化简
- 4(2010•三明)根吸收水分和无机盐的主要部位是根尖的( )
- 5如图在匀强电场中有A、B两点,他们之间的间距为2cm,两点的连线与场强方向成60度角.将一个电量为-2*10^-5C的电
- 63x+12=66和2.2X-X=0.3
- 7video,there,a,and,arcade,between,the,is,supermaket,the post
- 8懂得分享的作文
- 9岁寒三友分别是哪三个?
- 10小兰期中考试语文 数学 科学三科平均成绩93分 除数学外 的平均成绩是901分 他数学考了多少分 列算是
- 11一物体做匀加速直线运动,初速度为0.5米每秒,第7秒内的位移比第5秒内的位移多4m,求(1)物体的加速度
- 12求一个以下雨为主题的作文名字~是以下雨为主题的作文的名字,只要名字,不要内容~
- 13如图,已知AB是圆o的弦,AB的垂直平分线交圆o于点C,D,交A,B于点E,AB=6,DE:CE=1:3,求圆o的直径
- 14一个数的40%比它的一半少3,这个数是多少?
- 15四、和妈妈谈谈心,进一步了解妈妈的生活与工作,把情况记录下来.